
















Il llll llll I | .] II II I llll III
c
. . iảổ'y TẾ — PRODUCT: ONGLYZA s mg 4Ữ/24 =,q _
ỵL “Cục QUẦN LÝ DƯỌC CARITON
”T ——
DA BHÊ DUYÊT *
' LÌẳh/Ắl-Ểỳjeơ Wet mtains 5.58 mg saxaợlpiin hydrochloride (anhydrous) equivalent to 5 mg saxagiptin. `
sùv2bWt op out of reach ol chlldren.
See acoompanylm pmjaue inseđ lor in…ons and dosing information.
_12 … _ _ __ —
@ 2013 BristoI—Myers Squibb and AstraZeneca
wuma
Onglyza isallademakdBtistd-MyetsSqibủnpam.
…
ổ ả 5- Mõi viên nén ban phim chửa 5,58 mg saxagliptin hydrochloride (dạng khan) twng ứng vứi 5 mg saxagliptin.
Ễ ẵ Ễ Viên nén ban phim. Hộp Zvix i4viên.
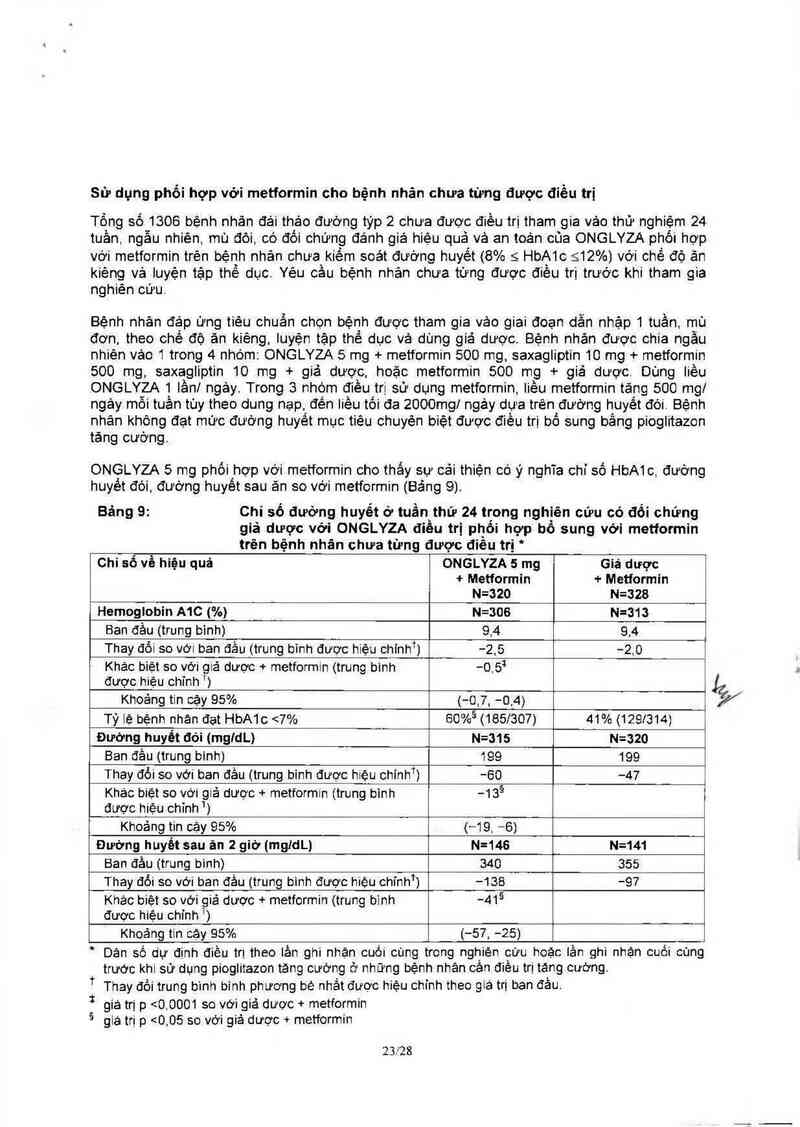
Ễ Ễ ›< Chidfmh. cách dùng, . 5% ở cảc bệnh nhân được điều trị phối
hợp ONGLYZA 5 mg + metformin (vả xảy ra thường xuyên hơn so
với bệnh nhán chỉ sử dụng metformin)
sô bệnh nhân (%)
ONGLYZA 5 mg + Metformin' Metformin'
N=320 N=328
Nhức đầu 24 (7,5) 17 (5,2)
Viêm mũi-hầu 22 (6,9) 13 (4,0)
' Metformin được khởi đảu bảng liêu 500 mg mỗi ngáy vả fflẻu chỉnh đén liều tỏi đa 2000 mg mỏi ngáy.
Hạ glucose trong máu
Tác dụng không mong muốn gảy ha glucose ma'u được thu thập qua tất cả cảc báo cáo về hạ
glucose mảu. Một số bệnh nhân không được yêu cầu đo chỉ số glucose ma'u cùng lúc hoặc chỉ
số đo được vẫn trong giới hạn binh thường. Vì vậy, không thể xảo định rõ các báo cáo náy có
phản ánh đúng về hạ glucose trong mảu hay không.
Trong thử nghiệm phỏi hợp bổ sung với glyburid, tỷ lệ chung các trướng hợp hạ glucose trong
máu xảy ra cao hơn ở bệnh nhân sử dụng ONGLYZA 2.5 mg vá ONGLYZA 5 mg (13,3% vả
14,6%) so với giả dược (10,1%). Trong nghiên cứu nèy, tần suất các trướng hợp hạ glucose
trong máu được chấn đoán xác định qua các triệu chứng hạ glucose kèm theo xét nghiệm
glucose bằng mảu ở đầu ngón tay 5 50 mgldL, lả 2,4% đối với ONGLYZA 2.5 mg vả 0,8% đỏi
với ONGLYZA 5 mg so với 0,7% đói với giả dược [Xem mục Lưu ý vá Thận trọng đặc biệt khi
sử dụng]. Tằn suất xảy ra hạ giucose trong máu khi sử dụng chế đó đơn trị lả 4,0% đối với
bệnh nhản sử dụng ONGLYZA 25 mg, 5,6% đối với ONGLYZA s mg so với 4,1% đối với giá
dược; trong trị liệu phối hợp bổ sung với metformin lả 7,8% đối với ONGLYZA 2,5 mg, 5,8% đôi
vởi ONGLYZA 5 mg so với 5% đối với giả dược; trong trị liệu phối hợp bổ sung với
thiazolidindion lả 4,1% đói với ONGLYZA 2,5 mg, 2,7% đối với ONGLYZA s mg so với 3,8% đổi
với giả dược; trong trị liệu cho đối tượng chưa từng được điêu trị lả 3,4% ở bệnh nhân sử dụng
ONGLYZA 5 mg + metformin vả 4,0% ở bệnh nhân chỉ sử dụng metformin.
Trong nghiên cứu có kiểm soát, so sánh liệu pháp đièu trị phối hợp ONGLYZA 5mg với điêu trị
phối hợp glipizid trên bệnh nhân chưa kiêm soát đướng huyêt tốt với metformin đơn trị, tỷ lệ ha
glucose mảu được ghi nhặn ở nhóm sử dụng ONGLYZA 5mg lả 3% (19 biên có trong 13 bệnh
nhân) vả ở nhóm sử dụng glipizid lá 36,3% (750 biên có trong 156 bệnh nhản). Hạ glucose mảu
được chần đoán xảc định qua các triệu chứng hạ glucose kèm theo xét nghiệm glucose ở đầu
ngón tay sso mg/dL không quan sát thắy ớ nhóm bệnh nhân điều trị ONGLYZA vả xảy ra ớ as
bẻnh nhân (8,1%) (p<0,0001) điều trị glipizid.
6/28
Trong 12 tuần điêu trị cho bệnh nhân suy thặn trung bình, suy thặn nặng hofiặc hệnhothìạn _giai
đoạn cuối (ESRD), tỷ lệ chung các trường hợp hạ glucose mau được ghi nhạãn la 20% ơ_Pẹnh
nhản điều trị ONGLYZA 2,5mg vả 22% ở bệnh nhân điêu trị gia dược. 4_bẹnh nhan qu tn
ONGLYZA (4,7%) vả 3 bệnh nhân điều trị giá dược (3,5%) đă được ghi nhạn Ia có. it nhat mot
iần hạ glucose mảu được chấn doán xác định qua cảc triệu chưng hạ glucose kem theo xet
nghiệm glucose ở đảu ngón tay 550 mgldL.
Trong thử nghiệm phối hợp bổ sung với insuiin, tỷ lệ chung các trướng hợp hạ glucose trong
mảu được ghi nhặn lả 18,4% đối với ONGLYZA 5 mg vả 19,9% đổi với gia dược. Tuy nhtẻn,
tần suất các trướng hợp hạ glucose trong máu có triệu chứng được chẩn đoặn xảo định (co
kèm theo xét nghiệm glucose bằng máu ở đầu ngón tay 5 50 mgldL) cao hơn ơ bệnh nhân sư
dụng ONGLYZA 5 mg (5,3%) so với giả dược (3,3%) [Xem mục Lưu ý vá Thận trọng đạc biệt
khi sử dụng].
Phản ứng quá mẫn
Trong phân tỉch gộp của 5 thử nghiệm kéo dái 24 tuần, các biên có liên quan đén quả mẫn như
nối mề đay, phủ ở mặt được ghi nhận xảy ra vởi tỷ lệ lả 1,5% ở bệnh nhản sử dụng ONGLYZA
2,5 mg, 1,5% ở bệnh nhân sử dụng ONGLYZA 5 mg và 0,4% ở bệnh nhân sử dụng giá dược.
Không có bảt kỳ trường hợp sử dụng ONGLYZA nảo phải nhập viện hOặc xảy ra với mức độ
gảy nguy hiểm đến tinh mạng. Có 1 bệnh nhản dược điều trị với saxagliptin ngưng sử dụng
thuốc do nổi mè day toản thản vả phủ ở mặt.
Nhiễm khuẩn
Dữ liệu nghiên cừu lâm sảng có đôi chứng, không mù của saxagliptin cho đên nay đã ghi nhận
có 6 báo các nhiễm bệnh Iao (chiêm 0,12%) trong số 4959 bệnh nhân điều trị với saxagliptin
(chiềm 1,1 trên 1000 bệnh nhân-nảm) so với không có bảo cảo nhiễm bệnh Iao nảo trong số
2868 bệnh nhân điêu trị với nhóm chứng. Hai trong số sáu trường hợp được xảo định bằng xét
nghiệm. Cảo trướng hợp còn lại có thông tin hạn chế hoặc chẩn đoán sơ bộ nhiễm Iao. Không
có trướng hợp nảo trong sáu trướng hợp bệnh xảy ra ở Mỹ hay Tây Àu. Một trướng hợp bệnh
xảy ra ở Canada trên bệnh nhân gốc Indonesia vả gần đây có đến du lịch Indonesia. Thời gian
điều trị với sax_agliptin cho đến khi có báo cáo nhiễm bệnh lao biến thiên từ 144 đến 929 ngảy.
Chỉ số bạch câu lympho sau khi điều tri phủ hợp với dảy chỉ số tham khảo ở 4 ca bệnh. Một
bệnh nhản có giảm bạch cằu lympho trước khi bắt đầu điều trị vởi saxagliptin vẫn trong tình
trạng ồn định suốt quá trinh điều trị bằng saxagliptin. Bệnh nhán cuối cùng có số lượng bach
cầu lympho được phân lặp thấp dưới mức binh thường khoảng 4 tháng trưởc khi bảo cáo
nhiẽm bệnh Iao. Không có báo các tự phát về mối liên quan giữa nhiễm bệnh iao vá việc sử
dụng saxagliptin. Nguyên nhân nhiễm lao chưa được xác định vả cho đén nay có rất ít trường
hợp bệnh để xảo định liệu có mối liện quan giữa sữ dụng saxagliptin vả nhiễm bệnh Iao. Trong
dữ liệu nghiên cứu lâm sảng có đói chứng, không mù cho đên nay đã ghi nhận có một trướng
hợp nhiễm khuấn cơ hội ở bệnh nhản điều trị bằng saxagliptin, tiến triển dẻn tử vong do nhiễm
khuẩn huyết nghi do nhiễm Salmonella từ thức ăn sau gần 600 ngảy điều trị với saxagliptin.
Không có báo cảo tự phát về nhiễm khuần cơ hội có liên quan đến sử dụng thuốc saxagliptin.
Dấu hiệu sinh tồn
Không có sự thay đối có ý nghĩa lâm sảng về các dấu hiệu sinh tồn được ghi nhặn trên các
bệnh nhân được cũều trị với ONGLYZA.
7/28
Cảo xét nghiệm lâm sảng
Số Iưọng bạch cầu lympho tuyệt đối
Giảm số lượng bạch câu lympho tuyệt đối được ghi nhận khi điều trị với ONGLYZA vả tác dụng
nảy lệ thuộc vảo liêu lượng sử dụng. Trong phân tích gộp của 5 thử nghiệm lâm sảng có đối
chứng kéo dải 24 tuần, với số lượng bạch cầu lympho ban đầu khoảng 2200 tế bảo/microL, sự
giảm bạch cầu lympho trụng binh so vởi ban đầu lả khoảng 100 té bảo/microL đối với
ONGLYZA 5 mg vả 120 tẻ bảolmicroL đối với ONGLYZA 10 mg so với giả dược. Tảo dụng
tương tự đã được ghi nhận khi sử dụng ONGLYZA 5 mg phối hợp với metformin so Với chỉ sử
dụng metformin đơn lẻ. Không có sư khảo biệt giữa ONGLYZA 2.5 mg so với giả dược. Tỷ lệ
bệnh nhân có số lượng bạch cảu lympho giảm dưới s7so té báo/microL lả 0,5% đối với
saxagliptin 25 mg, 1,5% đối Với saxagliptin 5 mg, 1,4% đối với saxagliptin 10 mg, vả 0,4% đôi
với giả dược. Trong phân lớn bệnh nhân, không có hiện tượng tái phảt giảm bạch cầu lympho
khi sử dụng lặp lại ONGLYZA, mặc dù có một vải bệnh nhân có sự giảm bạch cầu trở lại vả
phải ngưng thuốc. Sự giảm số lượng bach cầu lympho khỏng liẻn quan đên cảc tảo dụng không
mong muốn trẻn lâm sảng.
Ý nghĩa lâm sảng của sự giảm số lượng bạch cầu lympho liên quan đén giả dược chưa được
xảo định. Khi có chỉ định lâm sảng, ví dụ như nhiễm trùng bất thướng hoặc kéo dải thì cần phải
xét nghiệm số lượng bạch cầu lympho. Tác động của ONGLYZA trện số lượng bạch cáu
lympho ở bệnh nhân bât thướng vè bạch cầu lympho (ví dụ như nhiễm HIV) chưa xác định
được.
Tiểu cẩu
Với 6 thử nghiệm lâm sảng có đối chứng, mù đôi về hiệu quả vả tinh an toản cùa ONGLYZA
cho thảy, ONGLYZA không gây bất kỳ tác động lâm sảng có ý nghĩa nảo trện số lượng tiều
cầu.
Kinh nghiệm khi thuốc lưu hảnh trên thị trường
Có thẻm các tác dụng không mong muốn được xảo định sau khi ONGLYZA lưu hảnh trên thị
tnrớng. Do các phản ứng ghi nhặn tự phát từ một quần thể khỏng xác định sô lượng nên không
thể ước tính đúng tần suất hoặc xác lặp mối quan hệ nhân quả với việc sử dụng thuốc.
c Các phản ứng quá mẫn như phản ứng phản vệ, phù mạch hoặc cảc tinh trạng da tróc vảy.
[Xem mục Chống chỉ định vả mục Lưu ý về thận trọng đặc biệt khi sử dụng}
o \hẽm tụy cấp. [Xem mục Chỉ định trị liệu vả mục Lưu ý và thận trọng đặc biệt khi sử dụng].
TƯỜNG TÁC THUỐC
Cảc thuốc ức chế mạnh enzym CYP3A4l5
Ketoconazot lảm tảng có ý nghĩa nồng độ vả thời gian tiếp xúc với saxagliptin. Sự gia tảng nồng
độ của saxagliptin trong huyết tương củng xảy ra khi sử dụng đồng thời cảc thuốc ức chế mạnh
CYP3A4l5 (ví dụ như atazanavir, clarithromycin, indinavir, itraconazol, nefazodon, nelfinavir,
ritonavir, saquinavir vả telithromycin). Liều của ONGLYZA nên hạn chế ở mừc 2,5 mg khi sử
dụng đồng thời với cảc thuốc ức chế mạnh CYP3A4IS [Xem mục Líêu Iuợng và cách sử dụng
vả Dược lý lâm sâng].
8728
2
sử DỤNG TRÊN cÁc ĐỐI TƯỢNG ĐẶC BIẸT
Phụ nữ có thai
Phụ nữ có thai - nhóm B
Chưa có đủ cảc nghiên cứu có đối chứng về việc sử dụng saxagliptin trẻn phụznữ đang mang
thai. Do cảc nghiên cứu về sinh sản trện động vặt khỏng thể Iuôn Iuôn dùng đe tiên đoán đảp
ứng xảy ra trên ngưới, vì thế không nên sử dụng ỌNGLYZA vả cảc thuốc trị đải thảo đường
khảo trong khi đang mang thai trừ khi thặt sự cằn thiêt.
Saxagiiptin khòng gây quải thai ở bât kỳ liều lượng khảo s_ảt nảo trện. chuột cống vả thỏ đang
mang thai. Trên chuột cống, saxagliptin liều 240 mglkg (xâp xi 1503 lân nòng độ saxagliptin ở
người vả 66 lần nòng độ chắt chuyen hóa có hoạt tinh ở ngưới khi sử dụng liều tối đa 5 mg)
Iảm giảm quá trinh côt hòa (lảm chặm phảt triển) xương ohặu bảo thai. Độc tính xảy ra trẻn
chuột mẹ vả giảm trọng lượng bảo thai ghi nhận được ở liêu cao gáp 7986 lần (saxagliptin) vả
cao gắp 328 lần (chắt chuẵển hóa có hoạt tính) khi sử dụng liêu tôi đa cho người. Trên thỏ, chỉ
ghi nhận được oảc thay đ i nhỏ của bộ xương ở Iièu gây độc tinh trẻn thỏ me 200 mglkg (xấp
xỉ gấp 1432 lần nòng độ saxagliptin vả cao gâp 992 lần nồng độ chất chuyển hóa có hoạt tinh
khi sử dụng theo liều khuyên cảo tối đa ở ngưới).
Sử dụng phối hợp saxagliptin vả metformin cho chuột công vả thỏ đang mang thai trong suốt
giai đoạn thánh lập cơ quan, không phảt hiện gây chêt phôi thai hay quái thai khi khảo sảt ở liều
mả nồng độ toản thân đạt được (AUC) ở chuột cóng lên đên 100 vả gắp 10 lần liều tối đa
khuyến cảo ở ngưới (MRHD; saxagliptin 5 m vả metformin 2000 mg); nồng độ toản thản đạt
được ở thỏ Iện đến 249 vả gảp 1,1 lần liều tẵi đa khuyến cảo ở người. Trèn ohuột cống, sư
tiến triến của độc tinh thứ yếu được giới hạn ở mức tỷ lệ tảng của đường oong; độc tính thai kỳ
được giới hạn ở mức tỷ lệ giám trong lượng từ 11% đẻn 17% trong tiến trinh nghiên cứu vả liên
quan đén sự ia’m thực phấm trong thai kỳ. Trẻn thỏ, có xuất hiện tinh trạng dung nạp kém
dạng thuốc phỄi hợp ớ một phân nhóm cảc thỏ mẹ (12 con trong số so con), két quả lả dẫn đến
tử vong, hấp hối hoặc sầy thai. Tuy nhiên, trong số cảc thỏ mẹ sống sót của lứa đẻ đảnh giả,
độc tính thai kỳ được giới hạn ở mức biện độ giảm oùa trọng lượng Cơ thể từ ngảy 21 đẻn
ngảy 29 của thai kỳ. Vả độc tính tiến triển ở các lứa đẻ nảy được giới hạn ở mức giảm trọng
lượng thai nhi 7% vả một tỷ lệ thảp chậm cốt hóa ở mòng của thai nhi.
Khi sử dụng saxagliptin trên chuột cống cải từ ngảy thứ 6 trong thời gian mang thai cho đên
ngảy 20 trong thới kỳ cho bú, trọng lượng cúa chuột oon (đực vả cái) chỉ giảm ở liệu gảy độc
tỉnh cho chuột mẹ (nồng độ saxagliptin cao gắp 21629 và nồng độ chắt chuyển hóa có hoạt tinh
cao gáp 53 lần so với liều tôi đa sử dụng ở người). Không có độc tỉnh trên chức nảng vả hảnh
vi xảy ra trên chuột con sử dụng saxagliptin ở bắt kỷ liều nảo.
Saxagliptin qua được nhau thai vả vảo bảo thai theo liều sử dụng trện chuột mẹ đang mang
thai.
Phụ nữ đang cho con bú
Saxagiiptin được bải tiết trong sữa ở chuột đang oho con bú với tỷ lệ khoảng 1:1 so với nồng độ
trong huyêt tương. Chưa xảo định được saxagliptin có bải tiết trong sửa mẹ ở người hay
không. Do rẩt nhiều thuốc bải tiết trong sữa mẹ, oần thặn trọng khi sử dụng ONGLYZA ở phụ
nữ đang cho con bú.
9/28
Sử dụng ở trẻ em
Chưa xảo định được tinh an toản vả hiệu quả của ONGLYZA ở trẻ em.
Sử dụng ở người cao tuồi
Trong 6 thử nghiệm lâm sảng ngẫu nhiên, mù đôi, có đối chứng nhằm đảnh giá hiệu quả vả tính
an toản của ONGLYZA trèn 4148 bệnh nhân, có 634 (15,3%) bệnh nhân từ 65 tuối trớ lện vả có
59 (1,4%) bệnh nhân từ 75 tuối trở lẻn. Không có sự khảo biệt tồng thể về tinh an toản hay hiệu
quả của ONGLYZA giữa bệnh nhản 265 tuổi vả bệnh nhân trẻ tuổi. Tuy kinh nghiệm lâm sảng
chưa xảo đinh được sự khảo biệt về đáp ứng giữa bệnh nhân lớn tuồi vả bệnh nhân trẻ tuồi,
chưa thể loai trừ khả nảng nhạy cảm với thuốc hơn ở một số bệnh nhân cao tuổi.
Saxagliptin vả chất chuyến hóa có hoạt tính của nó được đảo thải một phần qua thặn. Do cảc
bệnh nhân cao tuổi thướng có khá nảng suy giảm ohức nảng thận, cản thận trọng khi chọn liều
sử dụng cho người cao tuôi dựa trẻn chức nảng thặn [Xem mục Liều lượng vả cách sử dụng vả
Duợc lý lâm sảng].
Sử dụng ở người lái xe vả vận hảnh mảy móc
Chưa có nghiên cứu về tảo động của thuốc lẻ_n khả nảng lải xe vả vận hảnh mảy móc. Tuy
nhiên khi lái xe hoặc vặn hảnh máy, cần lưu ý rảng chóng mặt đã được ghi nhặn khi điều trị với
saxagliptin.
QUÁ LIÊU ảỄ/
7
Trong 1 thử nghiệm lảm sảng có đôi chứng, ONGLYZA được sử dụng 1 Iần/ngảy đướng uống
trẻn đối tượng khỏe mạnh với liều tối đa Ièn đén 400 mglngảy trong 2 tuần (gẩP 80 lân liêu tối
đa khuyên cảo ở ngưới), không có _tảc dụng không mong muốn Iiên quan đén lieu sử dung trẻn
lảm sảng vả vả không có sự thay đội có ý nghĩa lâm sảng về khoảng QTc hay nhịp tim.
Trong trường hợp quá liều, cần ảp dụng cảc biện phảp điều trị hỗ trợ thích hợp dựa trẻn tinh
trang Iảm sảng của bệnh nhân. Saxagliptin vả ohất ohuyển hóa có hoạt tinh cùa nó có thể được
loại trừ qua tham phân mảu (23% liều trong 4 giớ).
oược LÝ LÀM SÀNG
cơ CHẾ TÁC ĐỌNG
Nồng độ của cảc hormon incretin như GLP-1 (glucagon-Iike peptide-1) vả GIP (glucose-
dependent insulinotropic polypeptide) được tảng phóng thích từ ruột non vảo mảu khi có đảp
ứng với thức ản. Những hormon nảy gây phóng thioh insulin từ tế bảo beta của tuyến tụy theo
phương cảch tùy thuộc váo nồng độ glucose, nhưng sẽ bị bất hoạt bởi enzym DPP4 trong
vòng vải phút. GLP-1 cũng lảm giảm lượng glucagon tiết ra từ tế bảo alphả của tuyến tuy, iảm
giảm sự tổng hợp glucose ở gan. Ở bệnh nhản bị đái thảo đường týp 2, nông độ GLP-j giảm
nhưng đáp ứng cùa insulin với GLP-1 vẫn không thay đòi. Saxagiiptin lá thuốc ức chê oạnh
tranh DPP4 gảy giảm sự bắt hoạt của hormon incretin, vì thế lảm tảng nòng độ cùa các hormon
nảy trong máu vả lảm giảm nồng độ glucose lúc đỏi vả sau bữa án theo cảch lệ thuộc vảo
lượng glucose ở bệnh nhân đái thảo đường týp 2.
10728
DƯỢC LỰC HỌC
Ở các bệnh nhản đải thảo đường týp 2, sử dụng ONGLYZA sẽ ức ohế hoat tinh enzym DPP-4
trong 24 giờ Sau khi sử dụng nghiệm phảp glucose qua đường uống hoặc sau bữa ản, sư ức
chế DPP-4 sẽ lảm tảng 2- 3 lần nồng độ hormon GLP- 1 vả GIP có hoạt tính trong mảu, lảm
giảm nồng độ glucagon vả tảng sự phóng thích insulin lệ thuộc glucose từ tế bảo beta cúa
tuyến tụy Sự tảng nồng độ insulin vả giảm nồng độ giucagon có liên quan đến việc lảm giảm
nỏng độ glucose lúc đói vả giảm glucose sau khi uống glucose hay sau bữa ăn
Sinh iỷ điện tim
Trong 1 thử nghiệm Iảm sảng có đối chứng, ngẫu nhiên, mù đôi, chéo 4, sử dụng thuốc đối
chứng lả moxifloxacin trên 40 đối tượng khỏe mạnh, ONGLYZA không gây thay đỗi có ý nghĩa
lảrn sảng trên sự kéo dải khoảng QTc hay nhịp tim ở liều iên đến 40 mglngảy (gấp 8 lần liều tối
đa khuyến cảo sử dụng)
DƯỢC ĐỘNG HỌC
Dược động hoc của saxagliptin vả chắt chuyền hòa oó hoạt tinh, 5- -hydroxy saxagliptin lả tương
tự nhau giữa đối tượng tinh nguyện khỏe manh vả bệnh nhân đải thảo đướng týp 2 C,… vả
AUC của saxagliptin vá chất chuyến hóa có hoạt tỉnh tảng tỉ lệ theo liều lượng saxagliptin sử
dụng trong khoảng liều từ 2 5 mg đến 400 mg. Sau khi uông 5 mg liều đơn saxagliptin ở ngưới
tinh nguyện khỏe mạnh, trị số AUC trung binh trong huyềt tương cùa saxagliptin vả chẩt chuyển
hóa có hoạt tính của nó lần lượt la 78 ng gịớ/ml vả 214 ng giớlml Trị sộ Cmax trong huyêt tương
tương ứng lả 24 nglml vả 47 nglml Hệ sỏ biến thiên nội cả thể trung bình (%CV) vè Cmax vả
AUC của saxagliptin vả chắt chuyền hóa có hoat tinh oủa nó lả dưới 25%
Không có sư tich lũy saxagliptin vả chắt chuyến hòa có hoạt tinh cùa nó được ghi nhặn khi sư
dụng lặp lại ca'c liều 1 Iầnlngảy ở bầt kỳ liêu lượng nảo Không có sư lệ thuộc vảo lièu lượng về
thới gian được ghi nhận trẻn sự thanh thải saxagliptin vả chắt chuyến hóa có hoạt tỉnh của nó
trong 14 ngảy sử dụng liêu saxagliptin 1 Iầnlngảy trong khoảng liều từ 2 ,5- 400 mg J
. z. .
Hảp thu %
Thới gian trung bình để đạt nồng độ tối đa trong huyết tương (Tmaf) sau khi sử đụng liều 5 mg 1
lầnlngảy lả 2 giờ đối với saxagliptin vả 4 giờ đối với chắt chuyền hóa có hoạt tinh Sử dụng
cùng lúc với thức ản nhiêu chất béo lảm tảng Tmax của saxagliptin khoảng 20 phút so vởi lúc
đói AUC của sạxagliptin tảng khoảng 27% khi sử dụng cùng với thức ăn so với lúc đói.
ONGLYZA có thế được sử dụng trong hoặc ngoải bữa ản
Phán bố
Nghiên cứu in vítro cho thắy khả năng gắn kết của saxagliptin vả chất chuyến hóa có hoạt tính
của nó với protein huyềt thanh ngưới không đảng kề Vi thế, những thay đối về hảm lượng
protein mảu trong các tình trạng bệnh khảo nhau (ví dụ như suy thận hay suy gan) sẻ không
ảnh hướng đến sự phân bố của saxagliptin
Chuyển hóa
Chuyền hòa cũa saxagliptin chủ yếu xảy ra qua hệ cytochrom P450 3A4/5 (CYP3A4IS) Chắt
chuyền hóa có hoạt tính của saxagliptin củng có ta'c dụng ức chế DPP-4 vả có hoạt tính bắng %
so với saxagliptin Vì thế những thuộc ức chế vả cảm ứng mạnh CYP3A4IS sẽ Iảm thay đỏi
dược động học cùa saxagliptin vả chất chuyển hóa có hoat tính của nó [Xem mục Tương tác
thuốc]
I | .i28
Thải trừ
Saxagiiptin được đảo thải qua cả 2 đường thặn vá gan. Sau khi uống một iiều đơn
14C-saxạgliptin 50 mg thỉ saxagliptin nguyện vẹn, dạng chuyển hóa có hoạt tính vả tống các
hợp chải có hoạt tinh phóng xạ được bải tiêt qua nước tiểu với tỷ lệ lần lượt 24%. 36%, và 75%
liệu sử dụng. Độ thanh thái trung binh qua thản oùa saxagliptin (~230 mllphút) cao hơn so với
tòc độ lọc trung binh qua cầu thận (~120 mllphút), cho thắy có những cơ chế bải tiết chủ động
ở thận. Khoáng_22% chảt có hoạt tinh phóng xạ hiện diện trong phản, chứng tỏ có 1 phần
sạxagliptịn bải tièt qua mặt vảlhay một phân không được hấp thu qua đướng tiêu hóa. Sau khi
uông 1 liêu đơn ONQLYZA 5 mg trên đôi tượng khỏe mạnh, thời gian bán thải trung binh (TW)
của saxagliptin vá chải chuyên hóa có hoạt tính cùa nó trong huyềt tương tương ứng lần lượt iá
2,5 giờ vả 3,1 gìờ.
Nhóm đối tượng đặc biệt
Suy thận
Một nghiên cứu mở, sử dụng iiều đơn saxagliptin đã được tiến hảnh đề đảnh giả dược động
học oủa saxagliptin sau khi uống liều 10 mg, trên cảc đối tượng có suy giảm chức năng thặn
mạn tinh ở những mức độ khảo nhau (n=8 bệnh nhân cho mỗi nhóm) so với đồi tượng có chức
năng thặn binh thường. Nghiên cứu bao gồm những bệnh nhân suy thặn được phân loại theo
có thanh thải creatinin ở mức độ nhẹ (>50 đến s80 mL/phút), trung binh (30 đên s50 mL/phút),
và nặng (<30 mL/phút), cũng như cảc bệnh nhán suy thận giai đoạn cuối đang thẳm phản mảu.
Độ thanh thải creatinin được ước lượng từ cộng thức Cockoroft-Gault:
Nam: CrCl (m Llphút) = [140 - tuổi (năm)] x thể trọng (kg) Àỹ
[72 >< nộng độ creatinin huyêt thanh (mgidL)l
Nữ: CrCl (lephút) = 0,85 x giá trị tĩnh theo công thức cùa Nam
Mức đó suy thận không ảnh hưởng đền Cmax cúa saxagliptin hay chắt ohuyển hòa có hoạt tính
của nó. Ở các đôi tượng suy thận nhẹ. trị số AUC của saxagliptin vả chầt chuyền hóa có hoạt
tỉnh cao hơn AUC cũa đối tượng có chức nảng thận bình thường tương ứng lả 20°/o vả 70%.
Do mức độ tảng nảy không lièn quan đên ý nghĩa lâm sảng nên không cần điều chinh _lièu ở
bệnh nhân suy thận nhẹ. Ở cảc đối tượng suy thặn ở mức độ trung binh hoặc nặng, trị sô AUC
của saxagliptin vả chảt chuyền hóa có hoạt tinh tăng cao hơn tương ứng lả 2,1 vả 4,5 lần so
với trị số AUC ở đối tượng có chừc năng thận bình thường. Để có được nòng độ saxagliptin
trong huyết tương tương tự như ở đối tượng có chức năng thặn binh thướng, Iiẻu 2,5 mg 1
iần/ngảy được khuyên cảo sử dụng ở cảc bệnh n_hân suy thận ở mức trung binh vả suy thận
nặng, oũng như bệnh nhân suy thận giai đoạn cuội cân thầm phân mảu. Saxagiiptin được loại
trừ qua tham phân mảu.
Suy gan
Ở ca'c đối tượng suy giảm chức nảng gan (Child-Pugh Class A, B vá C), sau khi sử dụng liềp
đơn saxagliptin 10 mg, Cmax vá AUC trung binh của saxagliptin cao hơn Cmax vả ARUC ở đoi
tượng khỏe mạnh tương ưng lả 8% vả 77%. Giá trị C,… tương ứng của chắt chuyen hộa có
hoạt tinh ở đối tượng suy gan cao hơn 59% vả giả trị AUC cùa chất chuyen hóa có hoạt tính
thắp hơn 33% so với đối tượng khỏe mạnh binh thướng tương ứng. Sư khảo biệt nảy không có
ý nghĩa về mặt lâm sảng. Khỏng cần fflèu chỉnh liêu tượng ở cảc bệnh nhản suy gan.
12128
Chỉ số khối cơ thể
Không oản điều chĩnh liều lượn dựa trèn chỉ số BMI vì chỉ số nảy khỏpg phải lệ đồng hiến cố
có ý nghĩa đên độ thanh thải bieu kiên của saxagliptin hoặc chảt chuyen hóa co hoạt tinh oua
nó, trện dân số được phân tich về mặt dược động học.
Giới tinh
Không cần điều chỉnh Iièu lượng theo giởi tính. Khỏng có sư khác biệt về dược động học của
saxagliptin giữa nam giới vả nữ giới. Nữ giới oò nồng độ chât chuyển hòa có hoạt tính trong
huyêt tương cao hơn khoảng 25% so với nam giới nhưng sự khác biệt nảy ít có ý nghĩa trên
Iảm sảng. Giới tính không phải lả đồng biến sô có ý nghĩa trên độ thanh thải biểu kiến cúa
saxagliptin vả chắt chuyển hóa có hoạt tính oùa nó trên dản số được phân tich về mặt dược
động học.
Bệnh nhân cao tuổi
Không cản điều chỉnh liều lượng theo độ tuỗi. Bệnh nhân cao tuối (65-80 tuồi) có trung binh
nhản Cmax vả AUC của saxagliptin cao hơn tương ứnẵ khoảng 23% vả 59% so với Cmax vả AUC
cúa bệnh nhân trẻ tuỗi (18-40 tuỗi). Sự khảo nhau v dược động học của chất chuyển hóa có
hoạt tinh giữa bệnh nhân cao tuồi vả bệnh nhân trẻ tuổi thường phản ảnh sư khảo nhau về
dược động học oũa saxagliptin. Sự khảo nhau về dược động học oùa saxagliptin vả chất
chuyển hóa có hoạt tinh oùa nó giữa bệnh nhân cao tuồi vả bệnh nhân trẻ tuổi có thể do nhiều
yêu tố_ảnh hưởng, bao gồm suy giảm chức nảng thận vả khá nảng chuyển hóa táng theo tuồi.
Độ tuôi không phải lả đông biến số có ý nghĩa trên độ thanh thải biểu kiên của saxagliptin vả
chảt chuyền hóa có hoạt tinh của nó trện dân số được phân tich về mặt dược động học.
Trẻ em Ắỳ
Chưa có nghiên cứu về dược động học của saxagliptin trên trẻ em. Ý/
Chủng tộc vả sắc tộc
Không cần điều chỉnh liều lượng theo ohùng tộc. Phản tich dược động học vả so sánh dược
động học cùa saxagliptin vả chât chuyến hóa oó hoạt tinh của nó trẻn 309 đối tượng da trắng
vơi 105 đôi tượng không thuộc chủng tộc da trảng (gồm 6 chủng tộc khảo nhau) đã khỏng cho
thay sự khác biệt có ý nghĩa về dược động học của saxagliptin vả chât chuyển hóa có hoạt tính
giữa 2 nhỏm nảy.
Tương tảo thuốc
Đánh giá tương tảo thuốc in vitro
Saxagiiptin chủ yếu được chuyển hóa bởi CYP3A4IS.
Trong các nghiên cứu in vitro, saxagliptin vả chất chuyển hóa có hoạt tinh của nó không ức chế
CYP1A2, 2A6, 286, 2C9, 2C19, 206, 2E1, hay 3A4, cũng không gảy cảm ứng CYP1A2, 286.
269, hay 3A4. Vi thê saxagliptin không lảm thay đổi sự thanh thải qua chuyền hóa của cảc
thuốc được chuyền hóa qua các enzym trên khi sử dụng cùng lúc. Saxagiiptin lả 1 chảt nèn của
P-glycoprotein (P-gp) nhưng không gây ức chẻ cũng như cảm ứng P-gp.
13/28
Đánh giá tương tảo thuốc in vívo
Bảng 3: Tảc động của thuốc dùng chung Iẽn nống độ vả thời gian tiếp xúc của saxagliptin
vả chẩt chuyển hóa có hoạt tinh 5- -hydroxy saxagliptin
Thuốc dùng Liêu cũa thuốc Liêu của _ Tỉ số trung binh nhán
chung dùng chung“ saxagliptin“ (ti sỏ cộ thuôo dùng chunglkhóng có thuốc
dùng chung)
Khỏng ảnh hướng = 1,00
AUC" c,…
Khóng cẩn chỉnh liều đối với các thuốc:
Metformin 1000 mg 100 mg saxagliptin 0,98 0,79
5—hydroxy saxagliptin 0,99 0,88
Glyburid 5 mg 10 mg saxagliptin 0,98 1,08 "
5-hydroxy saxagliptin ND ND
Piogiitazon² _ 45 mg 10 mg saxagliptin 1,11 1,11
1 lản/ngảy x 10 ngảy 1 lânlngảy 5-hyđroxy saxagliptin ND ND
x 5 ngảy
Digoxin 0,25 mg mỗi 6 giờ 10 mg saxagliptin 1,05 0,99
ngảy đả_u tiên, 1 lảnlngảy 5—hydroxy saxagliptin 1,06 1,02
sau độ môi 12 giờ x 7 ngảy
ngặy thứ 2, sau đó là
1 lân/ngảy x 5 ngáy /
Sirnvastatin _ 40 mg 10 mg saxagliptin 1,12 1,21
1 lânlngảy x 8 ngảy 1 iảnlngảy 5-hydroxy saxagliptin 1,02 1,08
x 4 ngảy
Diltiazem 360 mg kéo dải 10 mg saxagliptin 2,09 1,63
1 lần/ngảy x 9 ngảy 5—hydroxy saxagliptin 0,66 0,57
Riiampins 600 mg 5 mg saxagliptin o,24 o,47
1 lầnlngảy x 6 ngáy 5-hydroxy saxagliptin 1,03 1,39 L
Omeprazol 40 mg 10 mg saxagliptin 1,13 0,98
1 lần/ngảy x 5 ngảy 5-hydroxy saxagliptin ND ND
Nhộrn nhòm hydroxyd: 2400 10 mg saxagliptin 0,97 0,74
hydroxyd + mg 5—hydroxy saxagliptin ND ND
magnesi magnesi hydroxyd:
hydroxyd + 2400 mg
simethicon simethicon: 240 mg
Famotidin 40 mg 10 mg saxagliptin 1,03 1,14
5-hydroxy saxagliptin ND ND
Giới hạn liều Ongiyza đến 2,5 mg 1 lầnlngảy khi dùng chung với chất ức chế mạnh cvpaA4isz
Ketoconazol i 200 mg 100 mg saxagliptin 2,45 1,62
2 lầningảy x 9 ngảy 5—hydroxy saxagliptin 0,12 0,05
Ketoconazol 200 mg zo mg saxagliptin 3,67 2,44
2 iầnlngảy x 7 ngáy 5—hydroxy saxagliptin ND ND
l4/28
' Đơn liều trừ khi oò lưu ý khảo
*AUC= AUC(INF) đôi với thuổc dùng đợn liêu vả AUC= AUC(TAU) đồi với thuôo ơùng đa iièu
* Kẻt quả khộng bao gồm một đôi tượng
5 Hoạt tinh ức ohê dipeptiđyi peptidase-4 (DPP4) huyềt tương trong khoảng liều 24 giờ khộng bị ảnh
hưởng bởi rifampin
ND=ohưa xảo định; QD=1Iần/ngảy, q6h=mõi 6 giớ,q12h=mỗi 12 giớ; BID= 2-lân/ngảy, LA=tảc dụng kệo dải
Bảng 4: Tảo động của saxagliptin đến nồng độ và thời gian tiếp xúc của thuốc dùng chung
Thuốc dùng Liều của thuốc Liều của Tỉ số trung bình nhân
chung dũng chung' saxagliptin' (ti số oó thuốc dũng chunglkhông cộ thuổc
dùng chung)
Không ảnh hướng = 1,00
Auci C…ax
Không cẩn chỉnh liều đối với những thuốc sau:
Metformin 1000 mg 100 mg metformin 1,20 1,09
Glyburid 5 mg 10 mg glyburid 1,06 1,16
Piogiitazon* _ 45 mg … mg pioglitazon 1,08 1,14
1 lân/ngảy x 10 ngảy 1 Iân/ngảy hydroxy-pioglitazon ND ND
x 5 ngảy
Digoxin 0 ,25 mg mỗi 6 giờ ngáy 10 mg ' digoxin 1,06 1,09
đảu tiện, sau đó mội 12 1 lảnfngảy
giờ ngảy thứ 2, sau đó x 7 ngảy
1 lầnlngảy x 5 ngảy
Simvastatin 40 mg 10 mg simvastatin 1.04 0,88
1 Iằnlngèy x 8 ngảy 1 iầnlngảy acid simvastatin 1,16 1,00
x 4 ngảy
Diltiazem 360 mg keo dải 10 mg diltiazem 1,10 1,16
1 lầnlngảy x 9 ngảy
Ketoconazol _ 200 mg 100 mg ketoconazol 0,87 0,84
2 lảnlngảy x 9 ngáy
Ethinyl ethinyl estradiol 0,035 Ế mg _ ethinyl estradiol 1,07 0,98
estradiol vả mg vả norgestimat 0,250 1 Ian/ngạy noreigestromin 1,10 1,09
Norgestimat mg x 21 ngảy X 21 ngay norgestrei 1,13 1,17
' Đơn liêu trừ khi có lưu y' khảo
AỤC'= AUC(INF) đổi với thuôo dùng đơn lièu vả AUC= AUC(TAU) đối Với thuốc dùng đa Iièu
Kết quả bao gôm tất oả oảc đói tượng bệnh nhảm
ND=chưa xác định; QD=1lầnỉngáy, q6h= mỗi 6 giớ; q12h= mỗi 12 giớ; BlD=2lầnlngảy; LA=tảc dụng kéo
dái
NGHIÊN cửu LÃM SÀNG
ONGLYZA đã được nghiên cứu trong đơn trị liệu vả điều trị phối hợp với metformin, glyburid, vả
thiazolidinedion (pioglitazon vả rosiglitazoe).
Tồng số 4148 bệnh nhản đải tháo đướng tỷp 2 được chia ngẫu nhiên vảo 6 thử nghiệm lảm
sảng mũ đôi, có đối chừng, đảnh giả an toản vả hiệu quả kiểm soát đướng huyết của
ONGLYZA. Có 3021 bệnh nhản trong oảc thử nghiệm nảy được điều trị với ONGLYZA. Trong
ca'o thử nghiệm nảy, độ tuồi trung binh lả 54 tuồi vả 71% bệnh nhân lả người da trắng, 16% lả
l5728
ngưới Châu Á, 4% ngưới da đen vá 9% thuộc các chủng tộc khác Có thêm 423 bệnh nhân bao
gốm 315 bệnh nhân sử dụng ONGLYZA, tham gia vảo một nghiên cữu dò liều, có đối ohứng
với giả dược, trong 6 đên 12 tuần
Trong 6 thử nghiệm lảm sảng mù đội nảy ONGLYZA được đảnh giả ở mưc liều 2, 5 mg vả 5
mg 1 lần! ngảy. 3 trong sô các thử nghiệm nảy củng đảnh giá saxagliptin ở iiều 10 mg! ngảy
Liêu saxagliptin 10 mg] ngảy khộng cho thấy hiệu quả tốt hợn liều 5 mgl ngảy Điều trị với
ONGLYZA ở tắt oả cảo mức liều cho thây sự cải thiện có ý nghĩa thống kê vả oó liên quan về
mặt Iảm sảng cảo chí số Hemoglobin A1o (HbA1c), đường huyết đói (FPG) vá đường huyết sau
ăn 2 giờ (PPG) sau khi thực hiện nghiệm pháp dung nạp glucose đường uống chuẩn (OGTT)
so với nhóm đối ohứng. Giảm HbA1c được ghi nhặn ở tất cả cảc phân nhóm bệnh nhản bao
gồm giới tính, tuốt. ohủng tộc vả chí số khối cơthế (BMI) ban đầu
So với giả dược, ONGLYZA không liên quan đẻn sư thay đỗi có ý nghĩa của cản nặng cơ thể
hoặc lipid mảu lúc đói so với mức ban đầu.
ONGLYZA còn được đảnh giá thêm trong 2 thử nghiệm trện bệnh nhân đải thảo đướng týp 2:
một thử nghiệm có đối chứng so sánh phối hợp ONGLYZA với glipizid ở 858 bệnh nhân chưa
kiếm soát đầy đủ với metformin đơn trị Iìệu vả một thử nghiệm so sánh ONGLYZA với giả dược
trẻn 170 bệnh nhân đải thảo đường týp 2 bị suy thận trung bỉnh hoặc suy thận nặng hoặc suy
thận giai đoạn cuối (ESRD).
Đớh trị liệu <Ề/
Tồng số 766 bệnh nhản đái tháo đướng tỷp 2 chưa Kiếm soát đầy đủ bằng ohế độ ăn kiệng vả
Iuyện tập thể dục (7% s HbA1c s10%) tham gia vảo 2 thử nghiệm 24 tuần, mù đôi, có đối
chứng với giả dược đế đảnh giá hiệu quả vả an toản cúa ONGLYZA đơn trị liệu.
Trong thử nghiệm thử nhắt, 401 bệnh nhân đã thực hiện chế độ ản kiệng, Iuyện tâp vả sử dụng
giá dược ở giai đoạn dẫn nhập trong 2 tuần được sử dung ngẫu nhiên ONGLYZA 2 ,5 mg, 5
mg hoặc 10 mg hoặc giả dược. Bệnh nhân không đạt mức đường huyết mục tiêu ohuyên biệt
trong suốt nghiện oứu được điều trị tăng cường bằng metformin, phối hợp với giả dược hoặc
ONGLYZA. Hiệu quả được đánh giá ở lần đo cuối cùng trước khi tiến hảnh điều trị tảng cướng
cho bệnh nhân cằn điều trị. Không được điều chinh lièu ONGLYZA.
Điều trị với ONGLYZA 2, 5 mgl ngảy vả 5 mg/ ngảy cho thắy sự cải thiện có ý nghĩa ohi số
HbA1c, đướng huyết đói (FPG) vả đướng huyết sau ăn (PPG) so với giả dược (Bảng 5) Tỷ lệ
bệnh nhân ngưng điêu trị do không kiếm soát đướng huyết hoặc phải điêu trị tảng cướng vi đảp
ứng tiêu chỉ đướng huyết được định sẵn lả 16% ở nhóm điều trị với ONGLYZA 2, 5 mg, 20%ở
nhóm điều trị với ONGLYZA 5 mg vả 26% ở nhóm dùng giả dược.
Bảng 5: Chỉ số đướng huyết ở tuần thứ 24 trong thử nghiệm có đối chứng
giả dược với ONGLYZA đơn trị liệu trên bệnh nhân đái thảo
đướng tỷp 2 *
cm số về hiệu quả ONGLYZA 2,5 mg ONGLYZA s mg Giả dược
N=102 N=106 N=95
Hemoglobin A1C (%) N=100 N=103 N=92
Ban đầu (trung binh) 7,9 8,0 7,9
Thay đổi so với ban đầu (trung binh -0_4 -0,5 +0,2
được hìệu chỉnh'f)
I 6728
Bảng 5: Chỉ số đướng huyết ở tuần thứ 24 trong thử nghiệm có đối chứng
giả dược với ONGLYZA đơn trị liệu trên bệnh nhân đái tháo
đướng tỷp 2 *
cm số về hiệu quả ONGLYZA 2,5 mg ONGLYZA 5 mg Giá dược
N=102 N=106 N=95
Khác biệt so với giả dược (trung binh -0,6t —0,62
được hiệu chinh )
Khoảng tin cậy 95% (-0,9, -0,3) (-0,9, -0,4)
Tỷ lệ bệnh nhản đai HbA1c <7% 35% (351100) 38%5 (39/103) 24% (22/92)
Đường huyết đói (mgldL) N=101 N=105 N=92
Ban đảu (trung bình) 178 171 172
Thay đổi so với ban đầu (trung binh —15 -9 +6
được hiệu chỉnh )
Khác biệt so với giả dược (trung binh —215 —155
được hiệu chỉnh )
Khoảng tin cậy 95% (-31, —10) (—25, —4)
Đường huyết sau ăn 2 giờ (mgldL) N=78 N=84 N=71
Ban đầu (trung binh) 279 278 283
Thay đỏi so với ban đầu (trung binh -45 —43 -6
được hiệu chĩnh )
Khảo biệt so với giả dược (trung binh -39'IT -37ã
được hiệu ohinh T)
Khoảng tin cặy 95% (— 61 —16) (- 59 —15)
ì
Dản số dự định điều trị theo lần ghi nhện cuối cũng trong nghiện oứu hoặc lần ghi nhận cuối cũng
trước khi sử dụng metformin táng cướng ở những bệnh nhân cán điêu trị tăng cướng
† Thay đôi trung binh bình phương bé nhất được hiệu chinh theo giá trị ban đầu
1 giá trị p <0,0001 so vđi giả dược
Ế giá trị p <0,05 so với giả dược
" Không kiêm định ý nghĩa thộng kẽ đôi Với đường huyết sau ăn 2 giờ ở liêu ONGLYZA 2, 5 mg.
%
Thử nghiệm đơn trị liệu thứ 2 được tiến hảnh trong 24 tuần nhằm đảnh giá khoảng liều dùng
cùa ONGLYZA. Những bệnh nhân đải thảo đường ohưa được điều trị vá chưa kiểm soát
glucose máu đầy đủ (7%< - x
g oc - ~~-…2\ O`|'
z\___,___.\_ lị
Ổ '0ta _ """"""""" A~ ............ A ~~~~~~~~~ A """""""""" A
U
% 1 o -
5 I T Ì [ [ | 7 T |
Ban 4 6 8 12 16 20 24 24
dầu Tuấn LOCI
—— o ONGLYZA 2.5 mg + Metformin
vvvvvvvvv A ONGLYZA 5 mg + Metlormln
______ o Glả dược o Metformln
" Bao gòm bệnh nhản oó ohi số ban đảu va chí số ở tuần thứ 24.
Tuần 24 (LOCF- số liệu tính đến lần ghi nhặn cuối oùng) bao gồm dản số dự định điêu trị theo lần ghi
nhặn ouối cùng trong nghiện cứu trước khi sử dụng pioglitazon táng oướng ở những bệnh nhản cản
điêu trị tảng cường. Thay đổi trung binh so với ban đầu được hiệu chỉnh theo giá trị ban đảu.
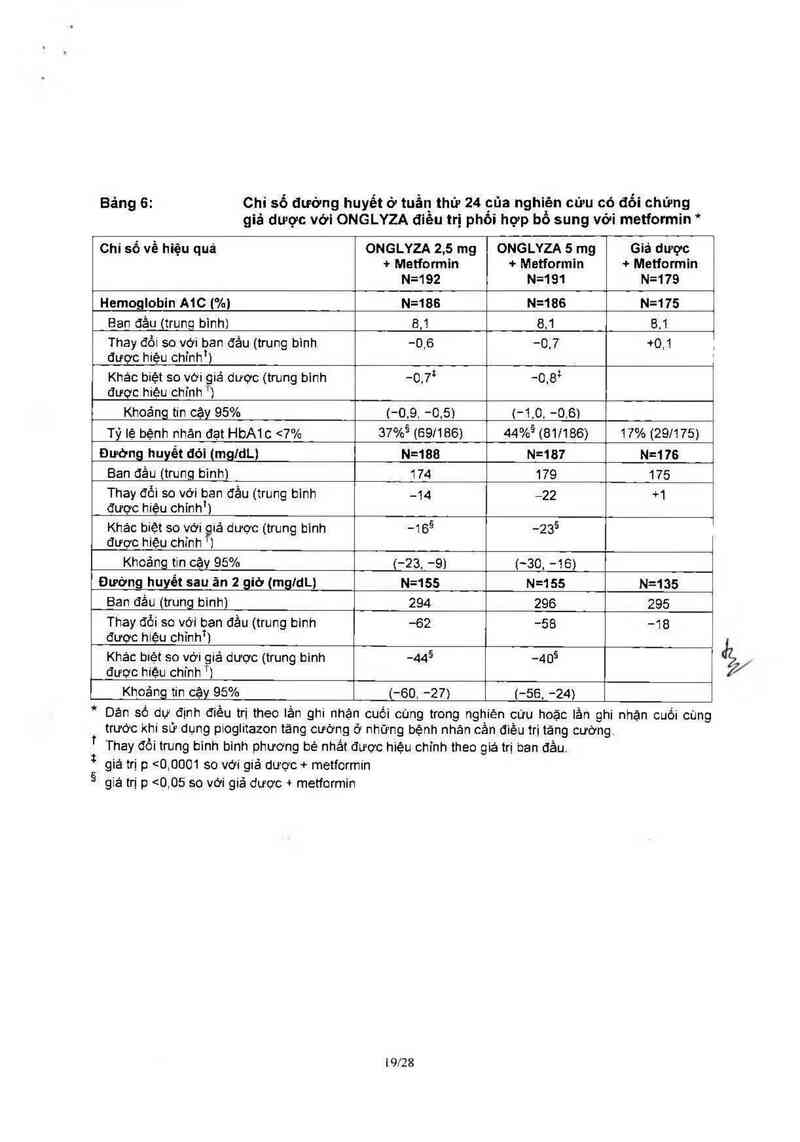
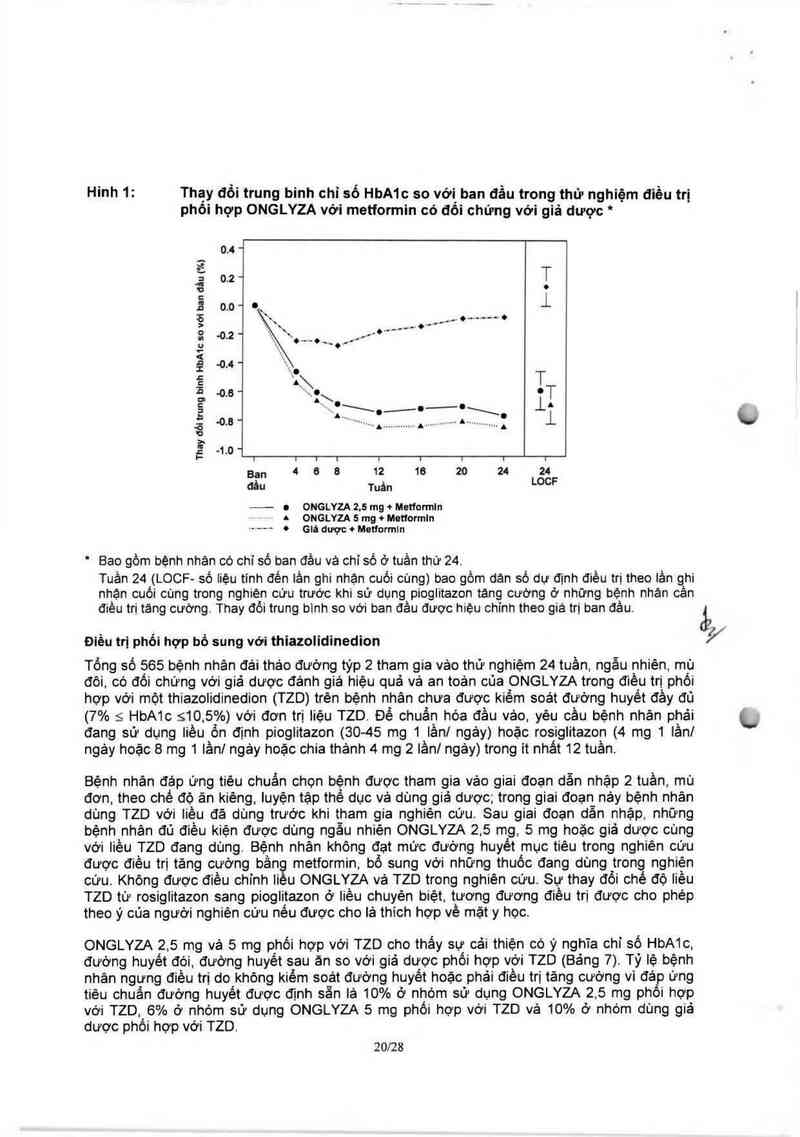
Điều trị phối hợp bổ sung với thiazolidinedion
Tồng số 565 bệnh nhân đải thảo đướng týp 2 tham gia vảo thử nghiệm 24 tuần, ngẩu nhiên, mù
đôi, có đối chứng với giả dược đánh giá hiệu quả vả an toản cùa ỌNGLYZA trong điêu trị phối
hợp với một thiazolidinedion (TZD) trén bệnh nhân chưa được kiêm soát đướng huyêt đầy đủ
(7% s HbA1c s10,5%) với đơn trị liệu TZD. Để chuẩn hóa đầu vảo, yêu oầu bệnh nhân phải
đang sử dụng liều ổn định pioglitazon (30-45 mg 1 tầnl ngảy) hoặc rosiglitazon (4 mg 1 lần]
ngảy hoặc 8 mg 1 lần] ngảy hoặc chia thảnh 4 mg 2 lần] ngảy) trong it nhất 12 tuần.
Bệnh nhân đáp ứng tiêu chuẩn chọn bệnh được tham gia vảo giai đoạn dẫn nhặp 2 tuần, mũ
đơn, theo chế độ ản kiệng, Iuyện tập thể dục vả dùng giả dược; trong giai đoạn nảy bệnh nhân
dùng TZD với liều đã dùng trước khi tham gia nghiên cứu. Sau giai đoạn dẳn nhặp, những
bệnh nhân đủ điếu kiện được dùng ngẫu nhiện ONGLYZA 2,5 mg, 5 mg hoặc giả dược cùng
với liều TZD đang dùng. Bệnh nhân không đạt mức đường huyêt mục tiêu trong nghiên cứu
được điều trị tảng cường bằn metformin, bổ sung với những thuốc đang dùng trong nghiện
cứu. Không được điều chính iiỄu ONGLYZA vả TZD trong nghiên cưu. Sự thay đồi chế độ liêu
TZD từ rosiglitazon sang pioglitazon ở liều ohuyên biệt, tương đương điều trị được cho phép
theo ý của ngưới nghiên cứu néu được cho lá thich hợp về mặt y học.
ONGLYZA 25 mg vả 5 mg phối hợp với TZD cho thấy sự oải thiện có ý nghĩa chi số HbA1c,
đường huyết đói, đường huyết sau ản so với giả dược phối hợp với TZD (Bảng 7). Tỷ lệ bệnh
nhân ngưng điều trị do khộng kiểm soát đường huyết hoặc phải điều trị tảng oướng vì đảP ứng
tiêu chuẩn đường huyết được định sẳn lả 10% ở nhóm sử dụng ONGLYZA 2,5 mg phoi hợp
vời TZD, 6% ở nhóm Sứ dung ONGLYZA 5 mg phối hợp vời TZD và 10% ở nhóm dùng giả
dược phối hợp với TZD.
2008
L
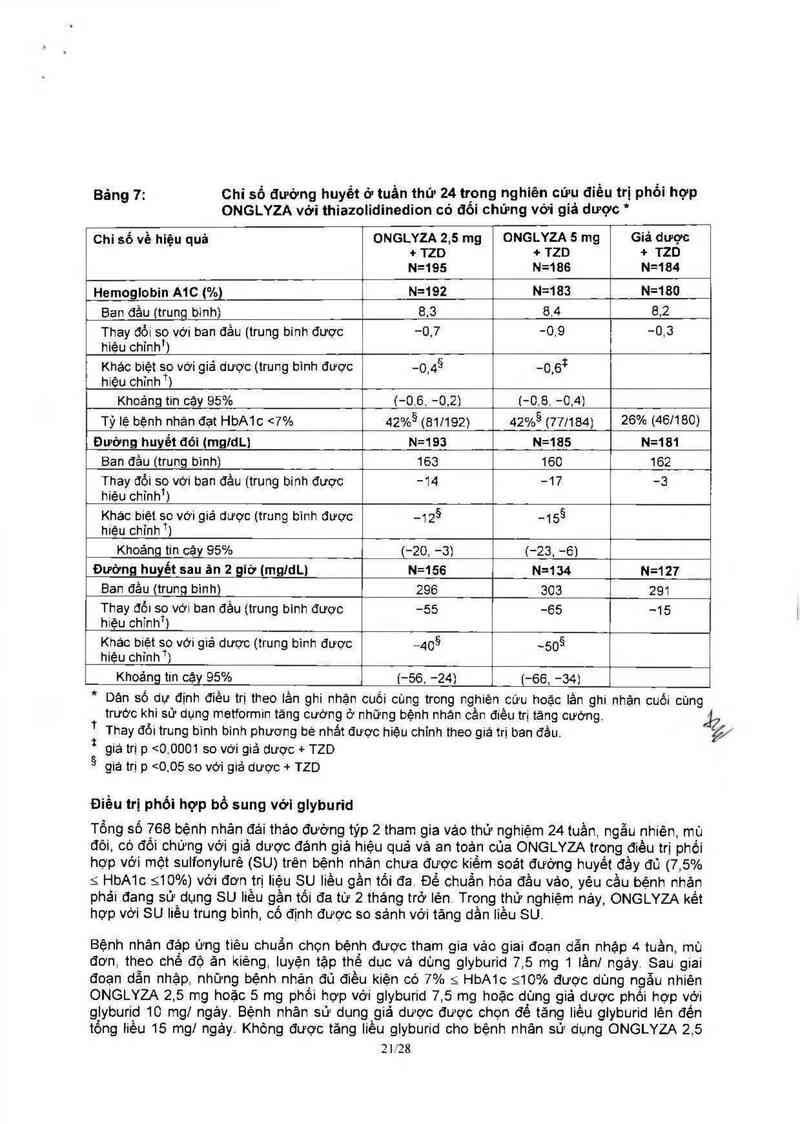
Bảng 7: Chỉ số đướng huyết ở tuần thứ 24 trong nghiên cứu điều trị phối hợp
ONGLYZA với thiazolidinedion có đối chửng với giả dược
Chi số về hiêu quả ONGLYZA 2,5 mg ONGLYZA s mg Giả dược
' + TZD + TZD + TZD
N=195 N=186 N=184
Hemoglobin A1C (%) N=192 N=183 N=180
Ban đầu (trung binh) 8.3 8,4 8,2
Thay đỏi so với ban đảu (trung binh được —0,7 -0,9 -0,3
hiệu ohinh )
Khác biệt so Với giá dược (trung bình được -o,4ẵ _0_61
hiệu chinh )
Khoảng tin cậy 95% (~0,6, —0.2) (-0,8, —0,4)
Tỷ 16 bệnh nhản đạt HbA1c <7% 42%ẵ (817192) 42%ã (77/184) 26% (46/180)
Đường huyết đói (mgidL) N=193 N=185 N=181
Ban đầu (trung binh) 163 160 162
Thay đổi so với ban đảu (trung binh được —14 —17 -3
hiệu chỉnh )
Khác biệt so Với giá dược (trung bình được -125 -15Ề
hiệu ohinh T)
Khoảng tin cặy 95% (-20, -3) (-23. -6)
Đường huyết sau ản Zjiớ (mgldL) N=156 N=134 N=127
Ban đầu (trung binh) 296 303 291
Thay đối so với ban đầu (trung binh được —55 -65 -15
hiệu chinh )
Khác biệt so với giá được (trung bình được —4oẵ `goẵ
hiệu chinh †)
Khoáng tin cậy 95% ( 56, -24) (- 66, -34)
" Dăn số dự định điều trị theo lản ghi nhặn cuối cùng trong nghiên cứu hoặc lần ghi nhận ouối củng
trước khi sử đụng metformin tăng cướng ở những bệnh nhán cản điêu trị tăng cường
Thay đói trung binh binh phương be nhảt được hiệu ohinh theo giá trị ban đầu
* giá trị p <0, 0001 so với giả được + TZD
ã giá trị p <0,05 so với giả dược + TZD
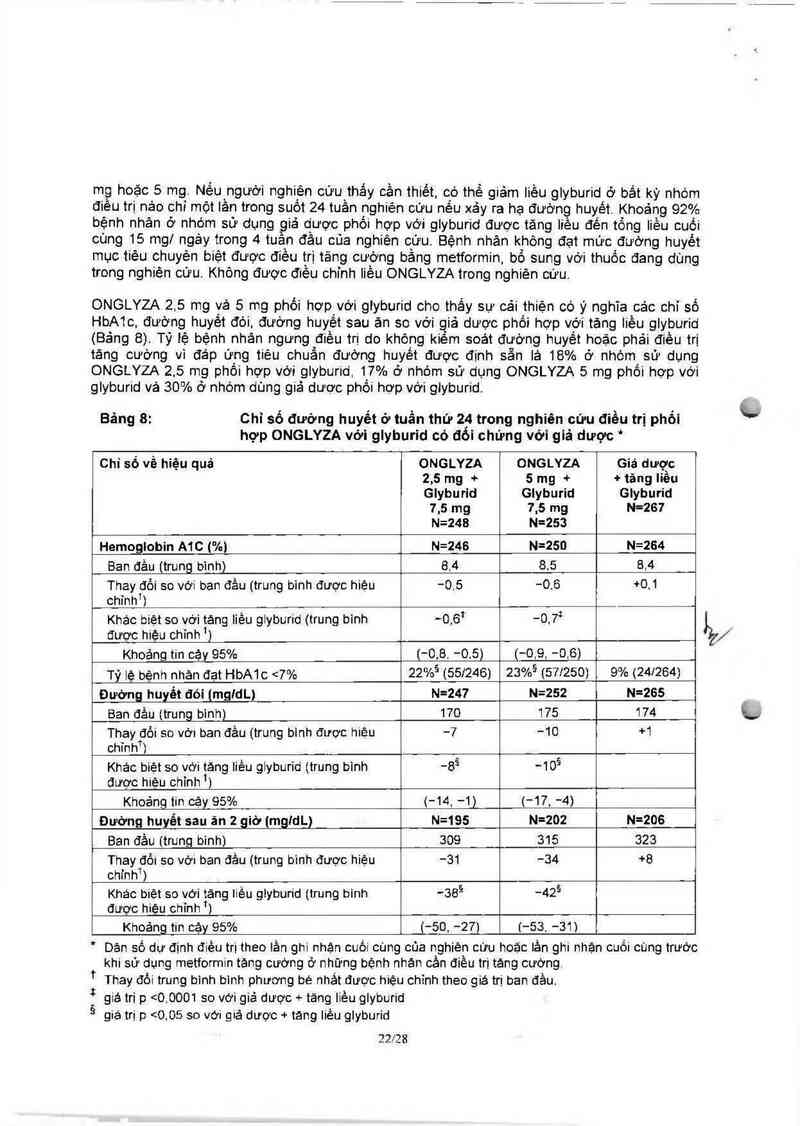
Điều trị phối hợp bổ sung với glyburid
Tồng số 768 bệnh nhân đải thảo đướng tỷp 2 tham gia vảo thử nghiệm 24 tuần, ngẫu nhiên, mù
đôi, có đối chứng với giả dược đánh giá hiệu quả vả an toản oùa ONGLYZA trong điều trị phối
hợp với một sulfonyiurê (SU) trẻn bệnh nhân chưa được kiểm soát đướng huyềt đầy đủ (7,5%
5 HbA1c s10%) với đơn trị liệu SU lièu gần tối đa Để chuẩn hóa đầu vảo, yêu cầu bệnh nhản
phai đang sử _dụng SU liệu gần tối đa từ 2 thảng trớ Iện Trọng thử nghiệm nảy, ONGLYZA kết
hợp với SU liêu trung bình, có định được so sánh với tảng dần liều SU
Bệnh nhân đảo ứng tiêu ohuần chọn bệnh được tham gia vảo giai đoạn dẫn nhập 4 tuần, mũ
đơn, theo ohế độ ản kiêng, iuyện tập thể dục vả dùng glyburid 7, 5 mg 1 lầnl ngảy Sau giai
đoạn dẫn nhập, những bệnh nhản đủ điều kiện có 7% s HbA1c <10% được dùng ngẫu nhiên
ONGLYZA 2, 5 mg hoặc 5 mg phối hợp với glyburid 7, 5 mg hoặc dùng giả dược phối hợp với
giyburi_d 10 mg] ngảy. Bệnh nhân sử dung giả dược được chọn để tảng Iièu giyburid lẻn đên
tồng iiều 15 mg! ngảy Không được tảng liều glyburid cho bệnh nhân sử dụng ONGLYZA 2, 5
2ls'28
%
mg hoặc 5 mg Nếu ngưới nghiện cứu thắy oần thiết, có thể giảm liều glyburid ở bầt kỳ nhóm
điều trị nảo chỉ một lần trong suốt 24 tuần nghiện cứu nều xảy ra hạ đướng huyêt i_ 8 tuần trước khi vảo sảng iọc Bệnh nhán tham gia
vảo nghiên cứu sử dụng insulin tác dụng trung binh hoặc kéo dải (insulin nền) hoặc insulin hỗn
hợp pha sẳn. Bệnh nhân dùng insulin tác dụng nhanh không được chọn trừ khi insulin tác dụng
nhanh iả một thảnh phần của insulin hỗn hợp pha sẵn
Bệnh nhản đảp ứng tiêu chuẩn ohon bệnh tham gia vảo giai đoạn dẫn nhập với giả dược 4
tuần, mù đơn, theo chế độ ản kiệng, luyện tập thể dục vả vân sử dụng insuiin (vá metformin
nếu thích hợp) với liẻu đang dùng trước khi tham gia thử nghiệm. Sau giai đoạn dẫn nhập,
bệnh nhân đủ điều kiện được phận ngẫu nhiên sử dụng phối hợp với ONGLYZA 5 mg hoặc với
giả dược Liều dũng cũa thuốc điều trị đải thảo đường được giữ Ổn định, nhưng bệnh nhản cần
được điều trị tảng cướng vả cho phép điều ohinh liều insulin nếu bệnh nhân không đạt mưc
đướng huyêt mục tiêu hoặc nêu ngưới nghiện oữu biết được bệnh nhân đã tự tãng liều insuiin
> 20%. Dữ liệu sau khi điều trị tăng cướng khộng được sư dụng cho các phân tích chính vê
hiệu quả
Sau 24 tuần, so với phối hợp giả dược, điều trị phối hợp với ONGLYZA 5 mg cho thấy sự cải
thiện có ý nghĩa chỉ sỏ HbAic vả đướng huyết sau ản so với ban đầu (Bảng 11). Khi so với giả
25/28
.,
dược, thay đổi trung binh HbA1c ở bệnh nhân dùng ONGLYZA 5 mg phối hợp với insulin vả
ONGLYZA 5 mg phối hợp với insuiin vả metformin iả tương đương nhau (tương ứng -0, 4% vả
-0 ,.4%) Tỷ lệ bệnh nhản ngưng điều trị do không kiềm soát đướng huyết hoặc được điều trị
tãng cướng lả 23% ở nhóm dùng ONGLYZA vả 32% ở nhóm dùng giá dược
Liều insulin trung binh hằng i_1gảy lả 53 đơn vị ở bệnh nhãn điều trị với ONGLYZA 5 mg vả 55
đơn vị ở bệnh nhân dùng giả dược. Thay đỗi trung binh so với ban đầu cũa liều insulin hằng
ngảy lẻ 2 đơn vị ở nhóm dùng ONGLYZA 5 mg vả 5 đơn vị ở nhỏm dũng giả dược
Bảng 11: Chỉ số đường huyết ở tuần thứ 24 trong thử nghiệm điều trị phổi
hợp ONGLYZA vởi insulin có đối ohứng với giả dược.*
cm số về hiệu quả ONGLYZA 5 mg Giả được
+ Insulin + Insulin
(+I— Metformin) (+I- Metformin)
N=304 N=151
Hemoglobin A1C (%) N=300 N=149
Ban đầu (trung bình) 8,7 8,7
Thay đối so với ban đầu (trung bình được hiệu -0,7 -0,3
chỉnh )
Khảo biệt so với giả dược (trung binh được hiệu -olqị
chỉnh T)
Khoảng tin cậy 95% (-0,6, -0,2)
Tỷ lệ bệnh nhản đạt HbA1c <7% 17% (52l300) 7% (101149) Ị
Đường huyết đói (mgidL) N=300 N=149
Ban đầu (trung bình) 173 173
Thay đối so với ban đầu (trung binh được hiệu —10 —6
chỉnhT)
Khảo biệt so với giả dược (trung binh được hiệu -4
chỉnh ')
Khoảng tin cặy 95% (—13, 5)
Đường huyết sau ãn 2 giờ (mgldL) N=262 N=129
Ban đảu (trung bình) 251 255
Thay đồi so với ban đầu (trung binh được hiệu -27 -4
chinh )
Khác biệt so với giả dược (trung binh được hiệu —235
chỉnh t)
Khoảng tin cậy 95% (-37, -9)
* Dản số dự định điêu trị theo lần ghi nhận cuối cùng trong nghiên cữu hoac iần ghi nhận cuối cùng
trước khi sử dụng insulin tăng cướng ở những bệnh nhan cản điêu trị tăng cướng.
† Thay đồi trung binh binh phương be nhắt được hiệu chinh theo giá trị ban đầu vả metformin sữ đụng
Iùc ban đầu.
² giá trị p <0,0001 so với giả được + insulin
ẵ giá trị p <0,05 so với giả dược + insulin
Suy thận
Tổng số 170 bệnh nhản tham _gia vảo thử nghiệm 12 tuân, ngẫu nhiên, mù đỏi, có đối chứng
với giả được đảnh giá hiệu quả vả an toản của ONGLYZA 2, 5 mg 1 lầnl ngây so với giả dược
267'2 8
7
l '.
, \
trện bệnh nhân đải thảo đường týp 2 bị suy thặn trung binh (n=90), suy thặn nặng_ (n=41) hoạỊc
suy thân giai đoạn cuối (ESRD) (n=39). Trong thử nghiệm nảy, 98% bẹnh nhản sư dụng thuoc
điều trị đải thảo đướng nèn (75% sử dung insulin vả 31% sử dụng thuốc điều trị đải thảo đướng
đướng uống, đa số lả sultonylurê)
Sau 12 tuần điều trị, ONGLYZA 2,5 mg cho thảy sự cải thiện có ý.nghĩa chỉ sỏ HbA1c so Với giá
dược (Bảng 12). Ở phản nhóm bệnh nhân suy_thận giai đoạn c__uôi, ONGLYZA vả gia d_ược cho
thảy HbA1c giảm có sư khảo biệt so với chỉ sô ban đầụ cho đen tuần 12. Ghi nhạn nay khong
được két Iuận vi thử nghiệm không đủ mạnh để cho thây hiệu quả trong từng phan nhom bẹnh
nhân suy thận riêng biệt.
Sau 12 tuần điều trị, thay đối trung binh đướng huyết đói iả -12 mgldL đôi với ONGLYZA
2,5 mg vả —13 mgldL đối với giả dược. So với giả dược, thay đồi trung binh đướng huyết đói
đối với ONGLYZA lẻ —12 mg/dL ở nhóm bệnh nhán suy thặn trung binh, -4 mgldL ở nhóm
bệnh nhân suy thận nặng, +44 mgldL ở nhóm bệnh nhân suythận giai đoạn cuối. Ghi nhân nảy
không được két luân vỉ thử nghiệm không đủ mạnh để cho thây hiệu quả trong từng phân nhóm
bệnh nhân suy thận riêng biệt.
Báng 12: HbA1c ở tuần 12 trong thử nghiệm oùa ONGLYZA có kiểm chứng
giả dược ở bệnh nhản suy thận *
cm số về hiệu qua' ONGLYZA 25 mg Giá được
N=85 N=85
Hemgqlobin A1C (%) N=81 N=83
Ban đầu (trungẸnh) 8,4 8,1
Thay đôi so với ban đảu (trung bình được hiệu -0,9 -0,4
chinh’)
Khảo biệt so với giả dược (trung binh được hiệu -0,4²
chỉnh †) , ả}
Khoảng tin cậy 95% (-0,7, -0.1) ]
' Dân số dự định điêu trị theo lản ghi nhận cuối cùng cũa nghiện oứu
T Thay đổi trung binh binh phương bé nhât được hiệu ohinh theo giá trị ban đảu.
² giả trị p
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng