













ZVZ "':
/
/ ,
f
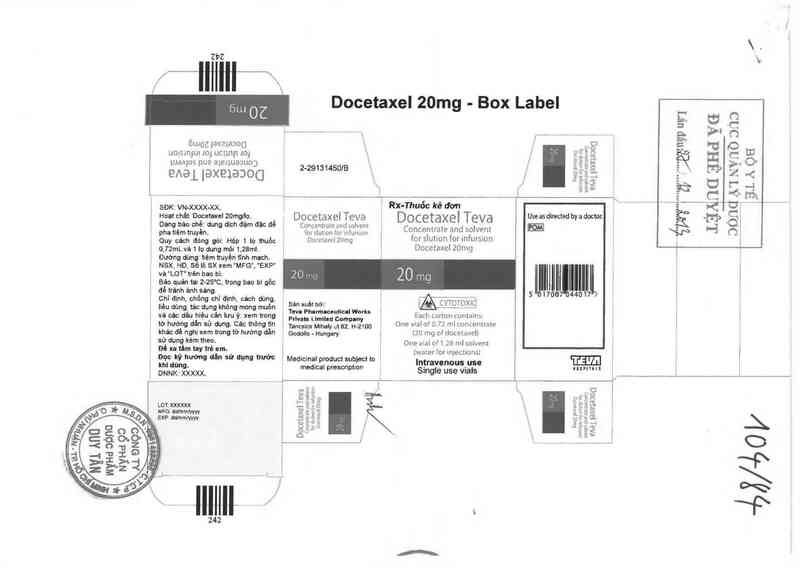
J Docetaxel 20mg - Box Label
ẸT cs fỡ
_ = › _ d
1——…— _ ~ ả …
õLUOZ 1axmaaoq , _.r’ g; q 0
uogsm1ug …; ucums .10J f Ễ Po C
ỊUBA|OS pue awnuaauog J’ . ẫ²ặ ’Q< '?~' ’
2-29131450/B | :
EABlJĐXElĐDOG / Ễ s“
/ ả ' —-1
Íả1 , - Ề …,
Ị sex:vu-xxxx-xx. 1 1 Rx-Thuốc kê dơn _ __ _ C A
Hoạt chảt: Doècetaxel20mg/Io. é Docetaxel Teva Docetaxel Teva Useasdiređed byadoctor. 1 m) Q
Dạng báo … :dung dich đặm đặch c l ; a … lv , v… . '
pha tiêm truyền. ẹonrcẵZtĩẩnefoẹlníẵrsxennn 1 Concentrạte and_ SOỈVEHI \ Ở ”4 Ô ,
Quy cách đỏng gói; Hộp 1 lọ thuôc , Do…axcllơmg , forsluhon for mfumon , 1 1
0,72mL vả 1 lọ dung môi 1,28m1. Docetaxel ZOmg 1 ỉ
Đường dùng: tiêm truyền tĩnh mạch.
NSX. HD, SỐ ló SX xem uMer“. 'EXP'
Vả "LOT' trên bao bì.
Bảo quản tạ12-25°C. trong bao bl gốc
1 Chỉ đgnh, ch ng ch dinh. cách dùng, , " _ 1
lièu dùng. tác dung không mong muôn , Ệán XỂỀLDỜ" . …… k 1 t—T-OẸ
vá cảc dán hiệu cân lưu ỷ: xem trong th U'ẸỆJ'ỄỈẮPỦJ ' Each carton contains: 1
tờ hưởng dãn sủ dụng. Các thdng tin Tancsìm WhaN ulaz. H-2100 One vval of 0.72 rv1 concentrate
khác đề nghị xem trong tờ hưởng dẳn _ 6on110 . Hungary . (20 mg of docetaxel)
SỬ dụng kèm theo. ' One v1al of 1_28 ml solvent
ĐỒ xa tâm tẾY “è em. _ _ (water for 1nJecaions)
Đọc lfỸ hương dấn SV dụng '… Medicinal product subject to Intravenous use TỂVIỈ 1 {
khi dung- medlcal prescription Sin ' — ' nnan 1
DNNK: xxxxx. 9 e use wa s 1
__… _… _ J _ _ \
LOT: XXX xxx
M FG: ddlmmlyyyy
EXP dd/mmMyy
enal |axelaaoq
Dọcetaxel Teva
OS
wỵuaoònu
NVHd
Docetaxel 20mg
Docetaxel Teva
Concentrate for solution for infusion I.V.
Docetaxel 20 mg
Manufacturer: Teva Pharmaceutỉcal Works
Private Limited Company - Hungary
20 ang
- Drug Via! label
ỉ“
è
ỉ
0.72 ml (Fill: 0.88 m|)
242
OT: XXXXX
EXP: dd/m m/yyyy
L
Docetaxel 20mg - Solvent Label
Water for injections
SOIvent for 1.28 ml (Fill: 1.71 ml)
Docetaxe| TeVa Manufacturer:Teva
Pharmaceutical Works
| V Private Limited Company
' ' Hungary
Ll Ẹ= I||
HOSPITALS
OT: XXXXX
EXP; dd/mm/yyyy
%
243
Đọc kỹ hưởng dẫn sử dung trước khi dùng. Nếu cẩn thêm thông tin xin hỏi ý kiển bác sỹ.
Để thuốc ngoải tầm tay trẻ em. Thuốc nãy chỉ dùng theo đơn của bác sỹ
DOCETAXEL TEVA
Dung dịch đậm đặc đễplm tiêm truyền
Thânh phần:
Lo thuốc:
-Hoạt chất:
Docetaxel T eva 20 mg: Docetaxel 20 mg/lọ
Docetaxel Teva 80 mg: Docetaxel 80 mg/lọ
-Tá dược: Ethanol, polysorbat 80
Lo dung môi: nước pha tiêm
Các đặc tính dược lực học:
Nhóm điều trị: taxan ấ'WL/
Mã ATC: LOICD 02
Docetaxel lá thuốc chống ung thư có tảo dụng thủc đấy po1yme hóa tubulỉn thảnh các vi ống
ổn định và ức chế sự phân rã các vi ống nảy, lảm giảm rõ rệt tubulỉn tự do. Docetaxel không
lảm thay đổi số lượng tiền sợi cùa những vì ông đã liên kết.
Nghiên cứu in vitro cho thấy docetaxel lảm phá vỡ mạng lưới vi ống trong tế bảo, lả yếu tố
cân thiết cho kỳ trung Igian và quá trình giảm phân cùa tế bảo.
Docetaxel gây độc với tế bảo in vitro trên nhiều dòng tế bảo khối u chuột và người cũng như
trên các tế bảo khối u người mới sinh thiết trong các thử nghiệm clonogenic. Docetaxel đạt
nồng độ cao trong tế bảo vả thời gian lưu trong tế bảo kéo dải. Ngoài ra, docetaxel có hoạt
hính trên một sô (nhưng không phải tất cả) cảc dòng tế bảo biếu hiện quá mức p- glycoprotein
được mã hóa bời các gen đa khảng thuốc. ln vívo, docetaxel có phổ tảc dụng rộng trên các
khối u ghép ơ chuột và người.
Các đặc tính dược động học:
Dược động học của docetaxel đã được đánh gỉả trên bệnh nhân ung thư sau khi sử dụng liếu
20— 115 mg/m2 trong cảc nghiên cứu pha 1. Dữ liệu động học của docetaxei không phụ thuộc
liếu và phù hợp với mô hình động học 3 ngăn với thời gian bán thải tương ứng vởi các pha 01,
B và y lần lượt là 4 phút, 36 phứt và 11,1 giờ. Sự xuât hiện cứa pha muộn một phần là do
docetaxel được vận chưyển tương đối chậm ra khỏi ngăn ngoại vi Sau khi sử dụng docetaxel
liều 100 mg/m2 truyên tĩnh mạch 1 giờ, nồng độ đinh trung bình của thuốc trong huyết tương
lả 3, 7 ụg/ml và trị sô AUC tương ứng là 4, 6 giờ°pg/mL Độ thanh thải toản thân trung bình và
thể tích phân bố ở trạng thái on đỉnh cùa docetaxel lần lượt là 21 ngiòt/m2 và 1 13 L. Sự khác
biệt về độ thanh thải toản thân giữa cảc cả thể là khoảng 50%. Hơn 95% lượng docetaxel liên
kểt với protein huyết tương.
Một nghiên cứu sử dụng C— docetaxel đã được tiến hảnh trên 3 bệnh nhân ung thư. Docetaxel
được thải trừ qua cả nước tiếu và phân sau khi bị oxy hóa nhóm tert- -butyl ester qua trung gian
cytochrom P450. Sau 7 ngảy, lượng thuốc được tìm thấy trong nước tiêu vả phân chiếm lần
lượt 6% và 75% liều thuốc gắn 140 Khoảng 80% liều có găn nguyên tứ đ’ âu được tìm
thấy trong phân trong 48 giờ đầu tiên, bao gôm một chất chuyển hóa c 'sOỂỂẺ ơÊâkchuyến
hóa phụ đếu không có hoạt tính cùng với một 1ượng rắt nhỏ docetaxel ng@hụyẹnỂ
Phân tích dược động học quần thể đã được tiến hảnh trên 577 bệnh `ăn. Ẹểơ:ùhâng sọ*được
động học của docetaxel được ước lượng theo mô hình rất gần vởi ỄĨ D'quưgng ỄừJcảc
nghiên cứu pha I. Dược động học của docetaxel không bị ảnh hưởng _tụỂjwảz giúi tểlả cùa
bệnh nhân. Trong một nhóm nhỏ bệnh nhân (n= 23), dữ liệu sinh hóa iì\thay chức nặng gan
1
bị giảm mức độ vừa ALT, AST > 1,5 lần ULN kèm theo phosphatase kiềm > 2,5 lần ULN),
độ thanh thải toản phan giảm trung bình 27% (xem mục Liều lượng và cảch dùng). Độ thanh
thải docetaxel không bị thay đổi ở những bệnh nhân bị giữ nước mức độ nhẹ đến vừa và chưa
có dữ liệu về độ thanh thải docetaxel ở bệnh nhân bị gỉữ nước nặng.
Khi sử dụng đồng thời, docetaxel không ảnh hưởng đến độ thanh thải doxorubicin và nồng độ
doxorubicinol (dạng chuyến hỏa của doxorubicin) trong huyết tương. Dược động học của
docetaxel, doxorubicin vả cyclophosphamid không bị ảnh hưởng khi dùng đồng thời.
Nghiên cứu pha I đảnh giá ảnh hưởng cùa capecitabin đến dược động học cứa docetaxel cho
thây capecitabin không ảnh hưởng đến dược động học của docetaxel (thế hiện qua Cmax vả
AUC) cũng như docetaxel không ảnh hướng đến dược động học của chất chuyến hóa 5’-
DFUR của capecitabin
Độ thanh thải của docetaxel khi sử dụng phối hợp cùng với cisplatỉn tương tự như khi dùng
đơn trị liệu. Dữ lỉệu dược động học cùa cisplatin khi dùng ngay sau docetaxel tương tự như
khi sử dụng cisplatin đơn độc.
Sử dụng phối hợp docetaxel, cisplatin và 5- fluorouracil trên 12 bệnh nhân mang khối u rắn
không ảnh hưởng đến dược động học cùa mỗi thuốc.
Ành hưởng cùa prednỉson đến dược động học của docetaxel đã được nghiên cứu trên 42 bệnh
nhân. Không ghi nhận thấy ảnh hưởng nảo của prednỉson đến dược động học của docetaxel.
Chỉ định điều trị: W
Ung thư vú:
Docetaxel Teva được chỉ định phối hợp với doxorubicin vả cyclophosphamỉd đề đỉều trị hỗ
trợ cho những bệnh nhân ung thư vú có hạch dương tính có thế phẫu thuật.
Docetaxel Teva phối hợp với doxorubicin được chỉ định điều trị cho những bệnh nhân ung
thư vú tiến trỉến khu trú hoặc ung thư vú di căn chưa được điều trị bằng cảc thưốc chống ung
thư trước đó.
Doxetaxel đơn trị liệu được chỉ định điều trị cho những bệnh nhân ung thư vú tiến triến khu
trú hoặc ung thư vú di căn sau khi đỉều trị thất bại bằng một thuốc chống ung thư thuộc nhóm
dẫn chất anthracyciin hoặc một thuốc alkyl hóa.
Docetaxel Teva phối hợp với trastuzumab được chỉ định điều trị cho những bệnh nhân ung
thư vú dí cãn mả khối u biếu hìện quá mức HER2 và bệnh nhân chưa được sử dụng hóa trị
liệu điều trị ung thư di căn trưởc đó.
Docetaxel Teva phối hợp với capecỉtabin được chỉ định điều trị cho những bệnh nhân ung thư
vú tiến triến khu trú hoặc di căn sau điều trị thất bại bằng một thuốc chống ung thư thuộc
nhóm dẫn chất antharacyclin.
Ung thư Dhổi không ohải tế bảo nhỏ:
Docetaxel Teva được chỉ định điều trị cho những bệnh nhãn mắc ung thư phổi không phải tế
bảo nhỏ tiến triến khu trú hoặc di căn sau khi đã thất bại với liệu pháp hóa trị trước đó.
Docetaxel Teva phối hợp với cisplatỉn được chỉ định điều trị cho những bệnh nhân mắc ung
thư phổi không phải tế bảo nhỏ tỉến triển khu trú không thể cắt bỏ hoặc di căn, trước đó chưa
sử dụng thuốc chống ung thư nảo khác.
Ung thư tiến liết tuvến:
Docetaxel Teva phối hợp với prednỉsolon hoặc prednỉsolon được chỉ định đìều trị cho những
bệnh nhân ung thư tiến liệt tuyển di căn khảng hormon.
Ung thư biếu mô tuvến da dảv:
Docetaxel Teva phối hợp với cỉsplatin và 5- fiuorouracil được chỉ
bệnh nhân ung thư biếu mô tuyên dạ dảy di căn, kể cả ung thư biền
quản, trước dó bệnh nhân chưa sử dụng thuốc chống ung thư nảo khá
Ung thư đầu vả cổ:
Docetaxel Teva phối h với cisplatin vả S— fluorouracil được chỉ định điều trị cho những
bệnh nhân mắc ung thư te bảo vảy tiến triến khu trú ở đầu và cổ.
Liều lượng và cách dùng:
Đường dùng: tiêm truyền tĩnh mạch
Docetaxel chi được dùng tại những cơ sở chuyên khoa được phép dùng hóa trị liệu gây độc tế
bảo và phải được sử dụng dưới sự giám sảt của bảo sĩ đã có kinh nghiệm dùng thuốc chống
th .
Ềrilẵu để nzhỉ: JẬWLI/
Đối với ung thư vú, ung thư phối không phải tế bảo nhỏ, ung thư đầu và cố, có thế sử dụng
corticosteroid theo đường uống, chẳng hạn như dexamethason 16 mg mỗi ngảy (chia 2 lần,
mỗi lần 8 mg) trong 3 ngảy, bãt đầu ] ngảy trước khi sử dụng docetaxel, trừ khi có chống chỉ
định (xem mục Những cảnh báo đặc biệt và thận trọng khi sử dụng). Có thế sử dụng G- CSF
dự phòng để giảm bớt nguy cơ gây độc trên huyết học.
Đối với ung thư tiến liệt tuyến, khi sử dụng đồng thời prednỉson hoặc prednỉsolon, nên dùng
dexamethason liều 8 mg theo đường uông tại cảc thời điểm 12 giờ, 3 giờ vả 1 giờ trước khi
truyền docetaxel (xem mục Những cảnh bảo đặc biệt vả thận trọng khi sử dụng).
Docetaxel được dùng theo đường truyền tĩnh mạch trong vòng 1 giờ sau môi 3 tuần.
Ung thư vú.
Trong trường hợp ung thư vú có hạch dương tính có thế phẫu thuật, liều docetaxel đề nghị là
75 mg/m2 sử dụng 1 giờ sau khi dùng doxorubicin 50 mg/m2 vả cyclophosphamid 500 mg/m2
sau môi 3 tuần trong 6 đợt điều trị (xem thêm mục Hiệu chỉnh liểu trong quá trình đỉều trị).
Đế điếu trị cho những bệnh nhân măc ung thư vú tiến triển khu trú hoặc di căn, 1iếu docetaxel
đề nghị là 100 mglm đơn trị liệu. Chzế độ trị liệu ban đầu là sử dụng phối hợp docetaxel 75
mg]…2 cùng với doxorubicin 50 mg/mz.
Khi sử dụng phối hợp với trastuzumab, liếu đocetaxel đề nghị là 100 mg/m2 sau mỗi 3 tuần,
còn trastuzumab sử dụng hảng tuần. lTrong một nghiên cứu, liếu docetaxel khởi đầu truyền
tĩnh mạch được sử dụng vảo ngảy tiếp sau ngảy sử dụng trastuzumab liều đầu tiên. Cảc liếu
docetaxel tiếp theo được chỉ định ngay sau khi kết thúc truyền trastuzumab, nếu liếu
trastuzumab trước đó được dung nạp tốt. Thông tin về liếu lượng và cảch dùng cùa
trastuzumab có thể xem trong tóm tắtđặc tính sản phẩm trastuzumab.
Khi sử dụng phối hợp với capecitabin, liều docetaxel đề nghị lả 75 mg/m2 sau mỗi 3 tuần
cùng với capecitabin liều 1250 mg/m2 ngảy 2 Tần (trong vòng 30 phứt sau khi ăn) trong 2
tuần, sau đó nghỉ dùng capecitabin trong 1 tuần. Thông tin vê liều capecitabin tính theo diện
tích bề mặt cơ thể có thể xem trong tóm tắt đặc tính sản phẩm capecitabin.
Ung thư phồi không phái tế bảo nhỏ:
Trong hóa trị liệu cho bệnh nhân chưa từng được điếu trị ung thư phổi không phải tế bảo nhỏ
trước 2đó, liếu docetaxel đề nghị là 75 mg/mz, ngay sau đó truyền tĩnh mạch cisplatin 75
mg/m2 trong 30- 60 phút. Trong trường hợp điều trị cho bệnh nhân sau khi thất bại với việc
điều trị bằng một dẫn chất platin, liều docetaxel đề nghị là 75 mg/m2 sử dụng đơn độc.
Ung thu tiền liêt tuỵến.
Liều docetaxel đề nghị là 75 mg/m2. Prednison hoặc prednỉsolon 1iều 5 mg ngảy 2 Tần được sử
dụng liên tục theo đường uống (xem mục Cảo đặc tính dược lực học).
Ung thư biếu mô guvến da dảv:
liên tục 24 giờ trong 5 ngảy, bắt đầu vảo thời điếm kết thức truyền tĩnh\:ực
điều trị được lặp lại sau môi 3 tuần. Bệnh nhân phải sử dụng thuốc ch
nước đầy đủ trước khi dùng cisplatin. Cần sử dụng G— CSF dự phòng để giảm nhẹ nguy cơ gây
độc trên huyết học (xem thêm mục Hiệu chỉnh liều trong quá trình điếu trị)
Ung thư đầu và cố:
Bệnh nhân phải sử dụng thuốc chống nôn và bổ sung nước đầy đủ trước và sau khi dùng
cisplatin Có thế sử dụng G- CSF dự phòng để giảm nhẹ nguy cơ gây độc trên huyết học. Tất
cả bệnh nhân sử dụng docetaxel trong các nghỉên cứu TAX 323 và TAX 324 đều được sử
dụng kháng sỉnh dự phòng.
' Hóa trị liệu trước, sau đó tiến hảnh xạ trị (TAX 323)
Đề điếu trị ung thư tế bảo vảy tiến triến khu trú không thế phẫu thuật ở đầu và cổ, liếu
docetaxel đề nghị là 75 mg/m sử dụng theo đường truyền tĩnh mạch trong 1 giờ, sau đó
truyền tĩnh mạch cispzlation 75 mg/m2 trong 1 giờ vảo ngảy thứ 1, tiếp theo sử dụng 5-
fiuorouracil 750 mg/m2 truyền tĩnh mạch liên tục hảng ngảy trong 5 ngảy. Chế độ trị liệu nây
được lặp lại sau mỗi 3 tuần vả qua 4 đọt điếu trị. Sau khi dùng hóa trị, bệnh nhân cần dùng xạ
trị.
~ Hóa trị liệu trước, sau đó tiến hảnh hóa xạ trị (TAX 324)
Để điều trị ung thư tế bảo vảy tiến triến khu trú (khộng thể cắt bò, khả năng điếu trị bằng phẫu
thuật thẩp do phải giữ lại cơ quan) ở đằu và cô, liếu docetaxel đề nghị là 75 mg/m2 sử dụng
theo đường truyền tĩnh mạch trong 1 giờ, sau đó truyền tĩnh mạch cisplatỉon 100 2²mg/m trong
30 phủt đến 3 giờ vảo ngảy thứ 1, tiếp theo sử dụng 5- fiuorouracil 1000 mglm 2lngậy truyền
tĩnh mạch lỉên tục từ ngảy 1 đến ngảy 4. Chế độ trị lỉệu nảy được lặp lại sau mỗi 3 tuần và qua
3 đợt điếu trị. Sau khi dùng hóa trị, bệnh nhân cần dùng hóa xạ trị.
Đế hiệu chỉnh liều cisplatin và 5— fiuorouracil, tham khảo thông tin trong tóm tắt đặc tính của
cảc thuốc nảy. x
Hiên chinh liếu trong guá trình đíếu tri: MI
N guỵên tắc chung:
Chỉ được sử dụng docetaxe] khi số lượng bạch cầu trung tính > 1.500 tế bảo/mm3.
Ở bệnh nhân đã từng trải qua sốt do giảm bạch cầu trung tính có số lượng bạch cầu trung tính
< 500 tế bảo/mm3 trong hơn 1 tuần gặp phải cảc phản ứng nghiếm trọng vả ngảy cảng nặng
thêm trên da hoặc bệnh thần kinh ngoại vi nặng trong quá trình điếu trị bằng docetaxel, cân
giảm 2liếu docetaxel từ 100 mg/m2 xuông 75 mg/m2 vả/hoặc từ 75 mg/rn2 xuống còn 60
mg/mz. Nếu bệnh nhân tiếp tục gặp cảc phản ứng bất lợi nảy khi dùng liếu 60 mg/m2, cần
ngừng sử dụng docetaxel.
Điều tri ung thư vú:
Trong một nghiến cứu trên bệnh nhân sử dụng docetaxel đế điếu trị ung thư vú vả đã từng bị
biến chứng do giảm bạch cầu trung tinh (như giảm bạch cầu trung tinh kéo dải, sốt do giảm
bạch cầu trung tính hoặc nhiễm khuấn), tất cả các bệnh nhân đến được khuyến cảo sử dụng G-
CSF để dự phòng (vảo ngảy thứ 4 đến 11) Những bệnh nhân tiếp tục gặp cảc phản ứng bât lợi
nảy cần duy trì sử dụng G- CSF và giảm liếu docetaxel xuống còn 60 mg/mz.
Tuy nhiên, trong thực hảnh lâm sảng, tình trạng giảm bạch cầu trung tính có thể xuất hiện
sớm hơn. Do đó, việc sử dụng G— CSF là cần thiêt đế giảm nguy cơ giảm bạch cầu trung tính.
Bệnh nhân bị vỉêm miệng độ 3 hoặc 4 cần sử dụng liếu docetaxel giảm còn 60 mg/mz.
Phối hơn với cisglatin:
Ở bệnh nhân sử dụng docetaxel liếu khời đầu 75 mg/m2 phối hợp với cisplatin vả _
tiếu cầu tối thiếu trong đợt điều trị trước < 25. 000 tiêu cầu/mm3 hoặc ở bệ ,… a
giảm bạch cầu trung tính, bệnh nhân nhiễm độc huyết học nặng, cần giả
/<_1 _ _
những đợt điếu trị tiếp sau còn 65 mg/mz. Thông tin vế hiệu chỉnh liều c ':1 :. :
khảo trong tóm tắt đặc tính sản phấm cisplatin. '
Phổi hơn với cạnecitabin: ` . , '%
~ Thông tin về hiệu chỉnh liêu capecitabin có thế xem trong tóm tăt đ\ ' «.
capecitabỉn
' Với nhmg bệnh nhân tiến triến độc tính độ 2 lằn đầu tiên, kéo dải đến thời điểm sử dụng
docetaxellcapecitabin lẩn kế tiếp, cần tạm ngừng dùng thuốc cho đến khi độc tính trở về mức
0-1, sau đó mới dùng thuốc trờ lại với liếu như ban đầu
' Với bệnh nhân tiển triến độc tính dộ 2 lần thứ hai, hoặc lần đầu tiên xuất hiện độc tính độ 3
tại bất kỳ thời điếm nảo của đợt điếu trị, cần tạm ngừng thuốc cho đến khi độc tính trở về mức
0-1 rồi mới dùng thuốc trở lại với liếu docetaxei là 55 mgím².
~ Nếu bệnh nhân gặp độc tinh bất kỳ lần nảo tiếp sau, hoặc bắt kỳ thời điếm nảo xuất hiện độc
tính độ 4, cần ngừng sử dụng docetaxel.
Thông tin về hiệu chỉnh liếu trastuzumab có thể tham khảo trong tóm tắt đặc tính sản phẩm
trastuzumab.
Phối hơn vởỉ cisplatin và 5- fluorouracz'l.
Nếu tình trạng sốt do giảm bạch cầu trung tính, giảm bạch cầu trung tính kéo dải hoặc nhiễm
khuẩn do giảm bạch câu trung kính vẫn xuất hizện ngay cả khi đã sử dụng G— CSF, cần giảm
liếu docetaxel từ 75 mg/m2 xuông còn 60 mg/mz. Trường hợp các tình trạng bíến chứng giảm
bạch cầu trung tính vẫn xuất hiện sau đó, cân tỉếp tục giảm liều docetaxel từ 60 mgl'm2 xuông
còn 45 mg/mz. Bệnh nhân không nến sứ đụng docetaxel ở những đợt điếu trị tiếp theo cho đến
khi số lượng bạch cầu trung tính trở về mức > 1 500 tế bảo/mm3 và số lượng tiếu cầu >
100.000 tiếu cầu/mma. Ngừng dùng thuốc nếu tinh trạng nhiễm độc vẫn còn tiếp tục kéo dải
(xem mục Những cảnh báo đặc biệt vả thận trọng khi sử dụng).
Khuyển cảo hiệu chinh liếu cho bệnh nhân điếu trị bằng docetaxel phối hợp vởi cisplatin và 5-
fiuorouraci] (S-FU) như sau: _41 ; __
Độc tính Hiệu chỉnh 1iến W
r ả _ - 9 0 . À _
Tiếu chảy độ 3 Đợt thư nhat. giam 20 /o lieu 5 FU
Đợt thứ hai: giảm 20% liều docetaxel.
Đợt thứ nhất: giảm 20% liếu docetaxel vả 5-FU
T1eu chay đọ 4 Đọt thứ hai: ngừng điều trị
Đợt thứ nhất: giảm 20% liếu S-FU
Viêm miệng/viêm niêm mạc độ 3 .
sau đo `
Đợt thứ 3: giảm 20% 1iêu docetaxel
Viêm miệng/viêm niêm mạc độ 4 sau đó
Đợt thứ hai; giảm 20% liên docctaxel
Thông tin về hiệu chỉnh liếu ciSplatin vả 5-fiuorouracil có thể tham khảo trong tóm tắt đặc
tính sản phẩm của các thuốc nảy
Trong nghiến cứu SCCHN, những bệnh nhân gặp các biến chứng giảm bạch cầu trung tính
(như giảm bạch cầu trung tinh kéo đải, sốt do gỉảm bạch cầu trung tính hoặc nhiễm khuẩn),
G- CSF được khuyến cáo sử dụng để dự phòng trong tất cả cảc đợt điếu trị sau đó (vảo ngảy
thứ 6-15).
Các nhóm bếnh nhân đăc biêt:
Bênh nhân suỵ gan:
Dựa trên dữ liệu dược động học khi sử dụng docetaxel 100 mg/m2 liếm duy nhắt, với nhũng
bện nhân có mức tãng transaminase (ALT vảfhoặc AST) cao hơn 1,5 lần iơr=hạn trên bình
thường (ULN) vả phosphatase kiếm cao hơn 2,5 lần ULN, liếu docetaxgỂị gĨ’ẵTỦỀm m2
(xem mục Những cảnh báo đặc biệt và thận trọng khi sử dụng và (ểac/đầoNfflỉ`đượ o-ẹđộng
học) Với những bệnh nhân có nồng độ bilirubin huyết thanh > UL ' Ễ" hđặề fflẨleả~Ắ ỀT >
3,5 lần ULN cùng vởí phosphatase kiếm > 6 lần ULN, không khuyếị \ịẵế ậiãìfi Hếỗ,Mvặifhông
được sử dụng docetaxel trừ khi có chỉ định nghiêm ngặt. \“ặ DUY TAN 1 ~=` ;,
Trong nghiên cứu lâm sáng sử dụng phối hợp với cisplatin vả 5- í]uoreumcrl đế găẹu trị cho
những bệnh nhân ung thư biếu mô tuyến dạ dảy, những bệnh nhân có AL "
Đợt thứ hai: ngừng sử dụng 5-FU ở tắt cả cảc đợt điếu trị
Đợt thứ nhất: ngừng sử dụng 5-FU ở tất cả các đợt điếu trị
lần ULN kèm theo phosphatase kỉếm > 2,5 lần ULN vả bilirubin > ULN đến bị loại khỏi
nghiên cứư. Vởí những bệnh nhân nảy, không khuyến cảo giảm liều, và không được sử dụng
docetaxel trư khí có chỉ định nghiếm ngặt. Chưa có dư liệu vê việc hiệu chỉnh liếu ở bệnh
nhân suy gan được điếu trị bằng docetaxel trong các chỉ định khác
Trẻ em vò thanh m'ên:
Dữ liệu về víệc sử dụng docetaxel trên bệnh nhân nhi chưa đầy đù.
Bẽnh nhân cao tuôi
Dựa trên kết quả phân tích dược động học quần thế, chưa có hướng dẫn riêng về víệc sử dụng
đocetaxel cho bệnh nhân cao tuõi. Khi phối hợp với capecitabin đế điếu trị cho nhũng bệnh
nhân từ 60 tuổi trở lến, cần giảm Iiếu capecitabin còn 75% (xem tóm tắt đậc tính sản phấm
cùa capecitabin).
Chống chỉ định:
Quả mẫn với docetaxel hoặc bất kỳ thảnh phẩn nảo của thuốc.
Không được sử dụng docetaxel cho những bệnh nhân có số lượng bạch cầu trung tính < 1.500
tế bảo/mm3.
Không được dùng docetaxel cho những bệnh nhân suy gan nặng do chưa có đủ dữ liệu về vìệc
sử dụng thuốc cho đối tượng bệnh nhân nảy (xem mục Liều lượng và cảch dùng vả Những
cảnh bảo đặc biệt vả thận trọng khi sử dụng)
Chống chỉ định đối với cảc thuốc khảo sử dụng phối hợp với docetaxel cũng đượơáp dụng.
Nhĩmg cãnh báo đặc biệt và thận trọng khi sử dụng: MV
Ở bệnh nhân ung thư vú và ung thư phối không phải tế bảo nhỏ, sư dụng corticoid theo đường
uống, chăng hạn đùng dexamethason 16 mg mỗi ngảy (8 mg mỗi lần, ngảy 2 lần) trong 3 ngảy
bắt đầu từ thời điểm ] ngảy trước khi sử dụng docetaxel, trừ khi có chống chỉ định, có thế lảm
giảm tần suất vả mức độ nghiêm trọng cùa tình trạng giữ nước cũng như mức độ nghiêm
trỌng cùa cảc phản ứng quá mân. Trong trường hợp điếu trị ung thư tiến lỉệt tuyển, nến sử
dụng đexamethamn 8 mg tại cảc thời đỉếm 12 giờ, 3 giờ vả 1 giờ trước khi truyền tĩnh mạch
docetaxel (xem mục Liều lượng vả cảch dùng).
Huvết hoc
Giảm bạch cầu trung tính là tảc dụng bắt lợi thường gặp nhất khi sử dụng docetaxel. Số lượng
bạch cầu trung tinh thường giảm thấp nhẳt sau 7 ngảy điếu trị nhưng khoảng thời gian nảy có
thế ngắn hon 0 những bệnh nhân đã được điếu trị bằng thuốc chống ưng thư liếu cao trưởc đó.
Cần thường xuyên theo dõi số lượng tế bảo máu toản phần ở tất cả cảc bệnh nhân sử dụng
docetaxel Bệnh nhân chỉ nên sử dụng docetaxel trở lại khi sô lượng bạch cầu trung tính trở vê
mức > 1.500 tế bảo/mm3 (xem mục Liều lượng và cách dùng).
Trong trường họp bệnh nhân bị giảm bạch câu trung tính nặng (< 500 tế bảolmm sau 7 ngảy
điếu trị hoặc dải hơn) trong quá trình điều trị bằng docetaxel, cân giảm liếu docetaxel trong
những đợt điếu trị tiếp sau hoặc phải ảp dụng cảc biện phảp điều trị triệu chứng thích hợp
(xem mục Liều lượng và cách dùng).
Ở bệnh nhân được điếu trị bằng docetaxei phối hợp với cisplatin vả 5- fluorouracil, sốt và
nhiễm khuấn do giảm bạch câu trung tính có thể xảy ra với tần sưất thế hơn khi bệnh nhân
được dự phòng bằng G- CSF. Bệnh nhân đìếu trị bằng docetaxel ph “___ ²__ ịpplatin vả 5—
fiuorouracil nên sử đụng G- CSF dự phòng để giảm bởt nguy cơ bịắ ỳhưngăìeỵgiamxbach cầu
trưng tinh (sốt do giảm bạch cầu trung tính, giảm bạch câu tru |ụỄ""tiriìiỂ 2_kéqfflỉ hớặc nhiễm
khuẩn do giảm bạch câu trung tính) Cần theo dõi chặt chế những' bểnhgtịaệuiựiứqcl điều trị
bầng docetaxel phối hợp với cisplatin vả 5- fiuorouracil (xem mụ ịẳu hxỡng—Ầaịcágfị ửng vả
Tác dụng không mong muốn). `
Các ohản ứng ơuá mẫn:
Cần theo dõi chặt chẽ cảc phản' ưng quả mẫn, đặc biệt là trong cảc lần dùng thuốc đầu tiên vả
thứ hai Các phản ứng quả mân có thể xuất hiện trong vòng vải phút sau khi bắt đằu truyền
tĩnh mạch docetaxel, do đó, cần chuẩn bị sẵn sảng các phương tiện cân thiết để cắp cứu trong
trườn hợp bệnh nhân bị tụt huyết áp hoặc cơ thăt phế quản. Nếu các phản ứng quả mẫn nhẹ
như boc hỏa hoặc phản ứng cục bộ trên da xuất hiện, không cần phải ngững thuốc. Tuy nhiên,
nếu bệnh nhân gặp các phản ứng nghiêm trọng như tụt huyết áp nặng, co thắt phế quản và
phát ban toản thân, cần ngừng sử dụng docetaxel ngay lập tức và ảp dụng các biện pháp xử trí
thich hợp. Bệnh nhân đã gặp cảc phản ứng quả mẫn nghiêm trọng do sử dụng docetaxel
không nên tái sử dụng docetaxel.
Các nhản ứng trên da:
Hổng ban khu trú ở cảc chi (lòng bản tay vả lòng bản chân) cùng với phủ sau khi tróc vảy đã
được ghi nhận ở bệnh nhân điều trị bằng docetaxel. Cảo phản ứng nặng như phát ban sau khi
tróc vảy dẫn đến phải ngừng sử dụng docetaxel đã được ghi nhận (xem mục Liều lượng và
cách dùng).
@…
Bệnh nhân có biến hiện gỉữ nước nặng như trản dịch mảng phổi, trản dịch mảng tim v cổ
trướng cần được giám sảt chặt chẽ. ,
Bênh nhân suỵ gan
Ở bệnh nhân được điếu trị bằng docetaxel 100 mg/m2 liếu duy nhất có nồng độ transaminase
huyết thanh (ALT vả/hoặc AST) cao hơn 1,5 lần giới hạn trên bình thường (ULN) kèm theo
nông độ phosphatase kiềm cao hơn 2,5 lần ULN, nguy cơ tiển triến cảc phản ứng bất lợi
nghỉêm trọng như tử vong do nhiễm độc bao gồm nhiễm khuấn mảu vả xuât huyết tiếu hóa
gây tử vong, sốt do giảm bạch cầu trung tính, nhiễm khuẩn, giảm tiếu cầu, viêm miệng và suy
nhược tăng lên. Do đó, liếu docetaxel đề nghị sử dụng cho những bệnh nhân nảy là 75 mg/m2
vả cần tỉến hảnh kiếm tra chức năng gan trước khi dùng thuốc và trước mỗi lẫn dùng thuốc
(xem mục Liều lượng và cảch dùng).
Với bệnh nhân có nồng độ bilỉrubin huyết thanh > ULN vả/hoặc ALT vả AST > 3,5 lần ULN
cùng với phosphatase kiếm > 6 lần ULN, không khuyến cảo giảm liếu và không được sử dụng
docetaxel trừ khi có chỉ định nghiêm ngặt.
Trong nghiên cứu lâm sảng sử dụng phối hợp với cisplatin vả S-fluorouracil để điều trị cho
những bệnh nhân ung thư biểu mô tuyến dạ dảy, những bệnh nhân có ALT vả/hoặc AST > 1,5
lần ULN kèm theo phosphatase kiềm > 2,5 lần ULN vả bilirubin > ULN đến bị loại khỏi
nghiên cứu. Vởi những bệnh nhân nảy, không khuyến cảo giảm liếu, vả không được sử dụng
docetaxel trừ khi có chỉ định nghiêm ngặt. Chưa có dữ liệu về việc hiệu chỉnh liền ở bệnh
nhân suy gan được điếu trị bằng docetaxel trong các chỉ định khác.
Bếnh nhân suỵ thân:
Chưa có dữ liệu về việc sử dụng docetaxel cho những bệnh nhân suy thận nặng.
Hè thằn kinh:
Nếu bệnh nhân gặp các triệu chứng nhiễm độc thần kinh ngoại vi nặng, cần giảm liếu
docetaxei (xem mục Liều lượng vả cảch dùng).
Nhiễm đôc tim:
Suy tim đã được ghi nhận ở bệnh nhân sư dụng docetaxel phối hợp với trastuzumab, đặc biệt
lả sau khi sử dụng dẫn chất anthracyclin (như doxorubicin hoặc epirubicỉn). Tinh trạng suy
tim’có thế ở mửc độ vừa hoặc nặng và có thể gây tử vong (xem mục Tác dụng không mong
muôn).
Nếu bệnh nhân cần phải sử dụng phối hợp docetaxel cùng với trast _ầĩb'ẵẫẫtiớồđiịh giá
trước năng tim của bệnh nhân trước khi dùng thuốc. Chức năng tim _eungCuằn Cđữợc Ịĩ—ềR tục
theo dõi trong suốt quá trinh điều trị (chẳng hạn sau mỗi 3 thảng) đế 1111p piíắFhiẬh sỆtình
t
/
trạng giảm chức năng tim. Thông tin chi tiết hơn có thể tham khảo tmg Wiẳf'đặỡ
phấm trastuzumab. \ỀO;DDUY TÂẸíỔ/ỵ
Những lưu V khảo:
Cả nam gíới vả nữ giới đếu phải sử dụng các biện phảp trảnh thai trong quá trình điếu trị bằng
docetaxel. Riêng nam gíới phải tỉếp tục sử dụng cảc biện pháp trảnh thai trong ít nhất 6 thảng
sau khi ngừng điều trị (xem mục Sử dụng cho phụ nữ có thai và cho con bủ)
Những lưu Ý khi sử dung docetaxel đế điếu tri ung thư vú:
Biến chứng do ,qiảm hach cẳu trungv tính.
Nếu bệnh nhân gặp cảc biến chứng do giảm bạch cầu trung tính (như gíảm bạch cầu trung tính
kéo dải, sốt hoặc nhiễm khuẩn do giậm bạch cầu trung tính), cẳn sử dụng G-CSF để dự phòng
vả giảm liếư docetaxel (xem mục Liều lượng và cảch dùng)
Các Dhản ứng rrên đường tiêu hóa
Cảc triệu chứng như đau bụng xuất hiện sớm, ia chảy có hoặc không kèm theo giảm bạch cấu
trung tính có thế là nhưng biếu hỉện sởm cùa tình trạng nhiễm độc tiêu hóa và cân được kiếm
tra cũng như điếu trị kịp thời.
Suv !zm sung huvết
Cần theo dõi eảc triệu chứng suy tim sung huyết trong suốt quá trình điếu trị và sau khi ngừng
thuốc
Bẽnh bach cẳu ÁM'Á1/
Ở những bệnh nhân sử dụng phối hợp cả docetaxei, doxorubicin vả cyclophosphamỉd, nguy
cơ măc đị sản tùy xuất hiện muộn hoặc bệnh bạch cẩu dạng tùy có thề tảng lến, do đó cân theo
dõi chặt chế tình trạng huyết học cùa bệnh nhân.
Bênh nhân có trên 4 hach dương tính:
Nguy cơílợi ich cùa việc sử đụng phối hợp docetaxel, đoxorubicỉn vả cycloph05phamid chưa
được đảnh giá đầy đủ (xem mục Cảc đặc tính dược lực học).
Bênh nhân cao tuổi:
Chưa có dữ liệu về việc sử dụng phối hợp docetaxel cùng với doxorubicin vả
cyclophosphamid cho những bệnh nhân từ 60 tuổi trở lên.
Trong một nghiên cứu trên 333 bệnh nhân được điếu trị bằng docetaxel sau mỗi 3 tuần để
điếu trị ung thư tiến liệt tuyến, 209 bệnh nhân ở độ tuồi từ 65 trở lên vả 68 bệnh nhân ở độ
tuối trên 75 Trong số bệnh nhân được điếu trị bằng docetaxel sau mỗi 3 tuần, tỷ lệ biến đổi
móng do đùng thuốc ở nhóm bệnh nhân từ 65 tuồi trớ lến cao hơn > 10% so với ở bệnh nhân
trẻ tuổi hơn Tỷ lệ sốt, ỉa chảy, chản ăn vả phù ngoại vi ở nhóm bệnh nhân từ 75 tuồi trờ lên
cao hơn so với ở bệnh nhân đưới 65 tưổi.
Một nghiên cứu khảc trên 300 bệnh nhân (221 bệnh nhân trong nghiến cứu pha III và 79 bệnh
nhân trong nghiên cửu pha II) được điếu trị bằng docetaxel phối hợp với cisplatin và 5-
fiuorouracil để điều trị ưng thư dạ dảy, 74 bệnh nhân ở độ tuổi từ 65 trở lên và có 4 bệnh nhân
từ 75 tuối trở lên. Tần suất các bỉến cố bắt lợi nghiêm trọng ở nhóm bệnh nhân cao tuôi cao
hơn so với ở bệnh nhân trẻ tuổi hơn. Tần suất các phản ứng bất lợi như ngủ lịm, viêm miệng,
nhiễm khuẩn do giảm bạch cầu trung tính ở nhóm bệnh nhân từ 65 tuổi trở lên cao hơn 2 10%
so vởi ở bệnh nhân trẻ tuồí hơn.
Bệnh nhãn cao tuổi điếu trị bằng đocetaxel phối hợp với cisplatin vả S-fiuorouracil cần được
theo dõi chặt chẽ.
Tương tác với các thuốc khác vả các dạng tương tảc khác:
Các nghiến cửu ín vítro cho thấy quá trình chuyến hóa của docetaxei có thế bị biến đổi khi sử
dụng đồng thời với cảc thuốc gây cảm ứng, ức chế hoặc được chuyến hóa (v` ặỂễ<`mthe ức
chế cạnh tranh) bởi cytochrom P450- 3A như cyclosporin, terfenđđhg’; ketoeọnaủ
`J1n_
erythromycỉn vả troleandomycin. Do đó, cần thận trọng khi sử dụng đồng ẵời daqetạgqi c
với cảc thuốc nảy. ị`*ị DƯOC pHẢM *i
Tỷ lệ docetaxel gắn protein huyết tương cao (> 95%) Mặc dù nguy c \,ẵìảy faitươngltacỄzởị
vivo giữa docetaxel với cảc thuốc khảc chưa được nghiên cứu đầy đủ, tườn t__acU … v_rltò C`giữa
"111. x_.JY`Ệ,
docetaer với cảc thuốc khảo gắn mạnh với protein huyết tương như erythromycin,
diphenhydramin, propranolol, propafenon, phenytoin, salicylat, sulfamethoxazol và natri
valporat không lảm ảnh hưởng đến mức độ liên kết với protein huyết tương cùa docetaxel.
Dexamethason không ảnh hướng đến tỷ lệ gắn protein huyết tương của docetaxel. Docetaxel
không lảm ảnh hưởng đến liên kêt giữa digitoxin với protein.
Dược động học của docetaxel, doxorubicin vả cyclophosphamid không bị ảnh hướng khi sử
dụng đồng thời. Dữ liệu chưa đầy đủ từ một nghiên cứu đơn lẻ không được kiếm soát cho
thấy nguy cơ xảy ra tương tảc thuốc giữa docetaer vả carboplatin. Khi sử dụng đồng thời
cùng với docetaxel, tôc độ thanh thải carboplatin cao hơn khoảng 50% so với khi sử dụng
carboplatỉn đơn độc
Dược động học của docetaer khi có mặt prednỉson đã được nghiên cứu trên bệnh nhân ung
thư tiến liệt tuyến di căn. Docetaxel được chuyến hóa bới CYP3A4 còn prednỉson lá thuốc
gây cảm ứng CYP3A4 Chưa ghi nhận ảnh hướng có ý nghĩa lâm sảng cùa prednỉson đến
dược động học cùa docetaxel.
Cần thận trọng khi sử dụng docetaer cho những bệnh nhân đang được điều trị bằng cảc thuốc
có khả năng gậy ức chế CYP3A4 (chẳng hạn cảc thuốc ức chế protease như ritonavir, các
thuốc chống nâm dẫn chất azol như ketoconazol hay itraconazol) Một nghiên cứu về tương
tác thuốc được tiến hảnh trên bệnh nhân sử dụng đồng thời ketoconazol vả docetaer cho thấy
tốc độ thanh thải docetaer giảm xuống một nứa khi có mặt ketoconazol. Tình trạng nảy có
thế là do docetaer được chuyến hóa chủ yếu bời CYP3A4. Tốc độ thanh thải docetaer cũng
giảm khi sử dụng cùng với ketoconazol, ngay cả khi dùng liếu thấp.
Sử dụng cho phụ nữ có thai và cho con bú:
Chưa có thông tin về việc sử dụng docetaer cho phụ nữ mang thai. Docetaxel gây độc cho
phôi vả thai khi thử nghiệm trên thở và chuột cũng như lảm giảm khả nãng sinh sản cùa
chuột. Tương tự như cảc thuốc gây độc tế bảo khác, docetaer có thể gây hại cho thai khi sử
dụng cho phụ nữ mang thai. Vì vậy, không được dùng docetaer trong thai khi trừ khi có chỉ
định rõ rảng.
Phụ nữ trong độ tuổi mang thaỉ/tra'nh thai:
Cần yêu câu phụ nữ trong độ tuổi mang thai sử dụng docetaer tránh mang thai và phải thông
báo ngay cho bác sĩ nếu bệnh nhân có thai khi đang dùng thuốc.
Cần’ ap dụng cảc biện phảp tránh thai thích hợp trong quá trình đỉếu trị bằng docetaxel.
Trong một nghiến cứu, docetaer gây độc với di truyền và có thế lảm thay đối khả năng sinh
sản cùa nam giới. Do đó, nam giới đang được điếu trị bằng docetaer không nên có con trong
khi dùng thuốc và tới 6 thảng sau khi ngừng điếu trị cũng như nên lưu giữ tinh trùng trước khi
sử dụng docetaxel.
Phụ nữ cho con bú:
Docetaxel lá thuốc có cấu trúc thân dầu nhưng chưa rõ thuốc có được tiết vảo sữa mẹ hay
không. Do thuốc có thể gây ra nhiều tác dụng bất lợi cho trẻ bú mẹ, người mẹ cần ngừng cho
con bú trong quá trình điếu trị bằng docetaxel.
Ấnh hưởng đến khả nãng lái xe và vận hânh mảy móc:
Chưa có nghỉên cứu đầy đủ về ảnh hướng cùa thuốc đến khả năng lải xe và vận hả.nh máy
móc. Tuy nhiên, vì có thể gặp các tảo dụng không mong muốn như chóng mặt, giảm thinh
lực, giảm huyết’ ap v. v.. ,bệnh nhân nên thận trọng khi lải xe và vận hảnh mảy móc.
Tác dụng không mong muốn:
Các tác dụng bắt lợi hay gặp nhât khi sử dụng Docetaxel Teva đơn độc lả '
Mức độ nghiêm trọng của cảc phản ứng bất lợi có thể tăng lến khi sử dụng đồng thời
Docetaxel Teva cùng với cảc hóa chắt điếu trị ung thư khảo.
Các phản ứng dị ứng sau đây có thể xuất hiện trong khi truyền docetaer (xảy ra với tần suất
> 1/10):
0 Bốc hỏa, cảc phản ứng trên da, ngứa
o Tức ngực, khó thở
o Sốt hoặc ớn lạnh
0 Đau lưng
o Hưyết áp thấp
Cảc phản ứng nặng hơn có thể xảy ra.
Nhân viên y tế cần theo dõi chặt chẽ tinh trạng bệnh nhân trong quá trình điếu trị. Bệnh nhân
cần thông bảo ngay cho bác sĩ nếu phát hiện thấy cảc triệu chứng nảy.
Khi truyền tĩnh mạch Docetaxel Teva, có thể gặp cảc phản ứng bất lợi sau. Tần suất của cảc
phản ứng nảy có thế khảc nhau tùy theo cảc thuốc dùng phối hợp.
Rất hay gặp (tần suất > 1/10)
0 Nhiễm khuắn, giảm số lượng hồng cầu (thiếu máu), bạch cầu (là tác nhân quan trọng trong
việc chống lại nhiễm khuấn) hoặc tiếu cầu.
Rụng tóc trong thời gian ngắn (ở hầu hết bệnh nhân, tóc sẽ mọc lại bình thường sau đó)
Sưng đỏ lòng bản tay hoặc lòng bản chân, có thể gây tróc da (tình trạng nảy cũng có thể
xuất hiện ơ cánh tay, mặt vả toản thân)
Thay đổi mảu sắc móng, có thể gây bong móng
Đau cơ, đau lưng hoặc đau xương
Thay đếi hoặc mất kinh
Sưng bản tay, bản chân, cẳng chân
Mệt mỏi hoặc các triệu chứng giả cúm
Tăng hoặc giảm cân
Hay gặp (tần suất < mo vả › mom
Nhiễm nấm Candida ở miệng
Mất nước
Chóng mặt
Giảm thính lực
Giảm huyết ảp, nhịp tim bất thường hoặc nhanh
Suy tim
Viêm thục quản
O Sốt: nêu bệnh nhân bị sốt, phải thông bảo ngay cho bác sĩ
o Cảo phản ứng dị ứng đã liệt kê ở trên
0 Giảm cảm gỉác thèm ăn (chản ăn)
o Mất ngủ
0 Cảm giảc tế hoặc kim châm, đau ở khớp hoặc cơ
0 Đau đầu
0 Thay đổi vị giảc
o Viêm mắt hoặc tăng tiết nước mắt
0 Sưng do iỗi dẫn lưu mạch bạch huyết
o Thở gấp
0 Dẫn lưu mũi, viêm họng và mũi, ho
o Chảy mảu mũi
O Đau miệng
o Rối loạn dạ dảy, bao gồm buồn nôn, nôn vả ia chảy, táo bón
O Đau bụng
o Khó tiêu
0
O
Khô miệng
Khó nuốt hoặc nuốt đau
Xuất huyết
Tăng men gan (do đó cần xét nghiệm mảu thường xuyên)
It gặp (tần suất > 111000 vả < 1l100)
O Choáng ngất
o Cảc phản ứng trên da tại vị trí truyền, víêm hoặc sưng tĩnh mạch.
o Vìêm kết trảng, ruột non, thùng một
0 Cục nghẽn mạch
Nếu bất kỳ phản ứng bất lợi nâo trờ nến nghỉếm trọng, hoặc nếu bệnh nhân ghi nhận tác dụng
không mong muôn nảy chưa được kê ở trên, cân thông bảo ngay cho bác sĩ hoặc dược sĩ bệnh
viến.
Thông báo cho bác sỹ những tác dụng không mong maốn gặp phải khi sử dụng thuốc.
`OOOO
Quả liêu:
Chỉ mới có một số báo cáo về tình trạng quá liếu docetaxel. Chưa có thuốc giải dộc đặc hiệu
trong trường hợp xảy ra quá lìếu. Khi xảy ra quá liếu, cần giữ bệnh nhân ở đơn vị chưyên
khoa và giám sảt chặt chẽ các chửc nảng sỏng. Các biến chứng chính có thể dự đoản khi xảy
ra quả lỉếu bạo gồm suy tủy xương, nhiễm độc thằn kinh ngoại vi vả viêm niêm mạc. Bệnh
nhân cần sử dụng G— CSF ngay khi có thế sau khi phát hiện quá liếu. Cần ảp dụng các biện
pháp điếu trị triệu chứng thích hợp. Ấ,Jư/
Tương kỵ: _ , ’ _ _ .
Không được trộn lân đocetaxei yới bât kỳ thuôc nảo khảo trừ các thuôc được kê đên ở mục
Những lưu ý đặc biệt khi pha chế và xử lý ioại bỏ.
Nhũng lưu ý đặc biệt khi pha chế và xử lý loại bỏ:
Docetaxel lá thuốc khảng ung thư nến giông như cảc thuốc có khả năng gây độc khác, cần
thận trọng trong việc sử dụng và pha chế dịch truyền. Phải sử dụng gảng tay khi tiếp xúc với
thuốc
Nếu dung dịch Docetaxel Teva đậm đặc trước khi pha thảnh dịch truyền tiếp xúc với da, cằn
rứa ngay vả rứa kỹ vùng da tiếp xúc với thuốc bằng xã phòng và nước sạch. Trường hợp
Docetaxel Teva đậm đặc tiếp xúc với niêm mạc, cân rứa ngay vả rứa kỹ bằng nước sạch.
Pha chế dung dich truyền tĩnh mach
a) Chuẩn bi dung dich Docetaxel Teva n'ền trỏn (10 mg docetaxel/ml)
Nếu lọ đựng thuốc được bảo quản lạnh, cần lẳy ra khỏi tủ lạnh vả để ở nhiệt độ phòng (dưới
25°C) trong vòng 5 phút.
Sử dụng kỹ thuật vô trùng, lật nghiếng lọ đtmg dung môi, dùng một bơm kim tiêm để rút toản
bộ lượng dung môi trong lọ dung môi rồi bom dung môi trong bơm tiếm vảo lọ Docetaxel
Teva.
Rút bơm kím tiếm và dùng tay lật đi lật lại lọ trong ít nhất 45 giây. Không được lắc.
Giữ yên lọ ở nhiệt độ phòng (dưới 25°C) trong 5 phút và kiếm tra sự đồng nhất vả độ trong
của dung dịch (bọt thường xuât hiện sau 5 phút do trong công thức chế phầm có chứa
poiysorbat 80).
Dung dịch sau khi pha có nồng độ docetaer 10 mg/ml vả cần pha loãng tiế .
3^ ’T'ĩsỷv—
dung dịch có thế ón định về mặt hóa học và vật lý trong vòng 8 giờ khi Ẹ'ảEg tãiiặnởựfflì'ễt'đ
2—°C 8°C hoặc ở nhiệt độ phòng (dưới 25°C). Ứề; CỐ pHẢN ' ’
ẹfC-Ệ
*
DUOc PHAM ),
b) Pha chế dích truvền
Có thế cần phải sử dụng nhiếu hơn một lọ để pha chế dịch truyền chứa đủ liều điếu trị cho
bệnh nhân. Tùy theo liếu cần thiết cho mỗi bệnh nhân tính theo mg, sử dụng kỹ thuật vô
trùng, dùng bơm kim tiêm để rút một thể tích tương ứng dung dịch tiến trộn docetaer 10
mglml. Chăng hạn, vởi lỉếu 140 mg docetaxel, thể tích dung dịch docetaxei tiền trộn cần rủt là
14 ml.
Bơm toản bộ lượng dung dịch tiến trộn vừa rút vảo tủi truyền (không lảm bằng chất liệu PVC)
có thể tích 250 ml chứa sẵn dung dịch glucose 5% hoặc dung dịch natri clorid 9 mng
(0,9%)
Nếu lỉều docetaer cần dùng lớn hơn 200 mg, phải sử dụng bao bì có dung tích lớn hơn để
đảm bảo dịch truyền sau khi pha có nồng độ docetaer không được vượt quá 0,74 mglml.
Trộn kỹ túi hoặc chai đựng dịch truyền bằng cách dùng tay đảo nhẹ.
Dịch truyền Docetaxel Teva cần phải sử dụng trong vòng 4 giờ sau khi pha và truyền tĩnh
mạch 1 giờ ở nhiệt độ phòng (dưới 25°C) trong điếu kiện ảnh sáng bình thường.
Giống như cảc chế phấm tiếm truyền khảc, phải kiếm tra cảm quan của dung dịch Docetaxel
Teva tiến trộn và dịch truyền trước khi sử dụng. Nếu dung dịch có kết tủa, phải loại bỏ.
Bất kỳ phần thưốc nảo không sử dụng phải được loại bỏ theo đủng hướng dẫn của cơ sở điếu
tn.
Hạn dùng: '
18 thảng kê từ ngảy sản xuât.
Bảo quản:
Bảo quản tại 2— 25°C, trong bao bì gốc để tránh ánh sáng.
Đóng gỏi: ,
Docetaxel Teva 20 mg: Hộp chứa 1 lọ thuộc 0,72mL & 1 lọ dung môi 1,28mL
Docetaer Teva 80 mg: Hộp chứa 1 lọ thuôc 2,88mL & 1 lọ dung môi 5,12mL
Tiêu chuẩn chất lượng:
Nhà sản xuất
Sản xuất bởi:
Teva Pharmaceutical Works Private Limited Company
Tancsics Mihaly ut 82, H-2100 Godollo, Hungary
PHÓ cuc TRUỞNG
JVyayẫn "Í/âm W
CỔ PHẨN
DƯỢC PHẢM
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng