










Hosplra - Australia
Mnúnnw zHooz
… osuvscmacn
CunpmmlTwr om:
Dlmunímn 475 : 11.5 x us …
AM… |
Mưmnav mom:
uugnu… iu
I m…c
I MITIICMM
I musocm
I FUNISCM
l…lõw s ……
uwdumro
uadsou
zz sr
uMq/gố M ’ “"
BỘ Y TẾ
cục QUẢN LÝ DUỢC
ĐÃ PHÊ DUYỆT
Lẩn đấuẮQ/Ắ/ỈO'Ữ
VĂN PHQNG
ĐẬl DIẸN _
TẬI THÀNH PHỐ
HỒ cní MlNH
M: - -
| 3 …… ….n..ủ…n …… ...,ợ,
Concemmte for Solution bt Oxaltplưhn slngh-m vIds - Dbcud
Iníusucn Hospỉm 5 m m| umnđ … uppmpfiơHY
ẫẵỗh ml l4olẫll cmlisloins Concentroie or SOnn hnbw wc
""""""""""""" mg om' ơtin mglml! … om: …
mmrlc ocld. sodium hyởoxide SOlƯNOI'I f_Of In_fusmn h udỞẵ m Omm w“
und Woleư Ior hp 15 mglm². Tuy nhiên, không
có ảnh hưởng trên sự sinh sản được ghi nhận ở loải chuột đực vả cải ở những liều lên tới
12 mg/mz/ngảy/trong 5 ngảy/chu kỳ.
Sử dụng trong thời kỳ mang thai
Loại Df À
Những nghiên cứu vê độc tính trên khả năng sinh sản không cho thấy hoạt tính gây quái thai trên
loải chuột hoặc thở khi dùng tương ứng liều truyền tĩnh mạch ở 6 vả 9 mg/m2 /ngảy (1/20 của lỉều
lâm sảng tối đa được khuyến cảo, dựa trên diện tích da co thế) Tuy nhiên sự gia tăng tử vong trên
bảo thai, sự giảm trọng lượng phôi thai và sự trì hoãn hóa xương đã được ghi nhận trên loải chuột.
Những hợp chất có liên quan với cơ chế tảc động tương tự được ghi nhận gây quải thai Không có
nghiên cứu đầy đủ và kiêm chứng tốt trên phụ nữ mang thai. Nếu thuốc nảy được dùng trong lủc
mang thai, hoặc nếu bệnh nhân có thai trong khi dùng thuốc nảy, bệnh nhân phải được cho biết về
khả năng gây nguy hiểm cho bảo thai. Oxalỉplatin dường như độc cho bảo thai người ở liều điều trị
khuyến cáo, vả như vậy chống chỉ định dùng trong lủc mang thai.
' Loại D: những thuốc gây. nghi có gây hoặc có thẻ gây . rỷ lệ gía tãng dị tật trên bờo thai ngưởi hoãc tốn xhương không hồiphục .
Những thuôc nảy cũng có Ihẽ có tác dụng dược lý có hại.
Trang 4
_)f7PÓJ
Cũng như đối vơi những thuốc độc tế bảo khác, những biện pháp trảnh thai hữu hiện phải được ảp
dụng cho bệnh nhân có khả năng sinh sản trước khi khởi đằu hóa trị với oxaliplatin
Sử dụng trong iúc cho con bú
Không có dữ iiệu về sự bải tiết oxalipiatin trong sữa ioải vặt hoặc người. Oxalipiatin chống chỉ định
trên phụ nữ đang cho con bú.
Trẻ em
Oxalipiatin không được khuyến cảo sử dụng cho trẻ em vì đặc tính an toản và hiệu quả chưa được
xác định trong nhóm bệnh nhân nảy.
Người cao tuổi
Không thấy tăng độc tính nặng khi dùng oxaliplatin như lả. đơn iiệu phảp hay khi kết hợp vởi
tiuorouracil trên những bệnh nhân trên 65 tuổi. Như vậy là không cần điếu chinh liểu trên bệnh
nhân cao tuổi.
Tương tảc với những thuốc khác
Trên những bệnh nhân dùng đơn liều 85 mgi’zm oxaliplatin, ngay trước khi dùng fluorouracil,
khong có thay đổi mức độ nguy cơ cùa fiuorouracil Tuy nhiên, trên bệnh nhân dùng fiuorouracil
môi tuần và oxaliplatin 130 mg/m2 mỗi 3 tuần có ghi nhận gia tăng 20% fiuorouracil huyết tương.
In vitro, ít hoặc không có hiện tượng cạnh tranh gắn kết với protein huyết tương vởi các chất sau:
erythromycỉn, salicylates, granisetron, paclitaxel, vả sodium valproate.
Oxalipiatin tương tảc với dung dịch chứa chloride và những dung dịch kiềm (kể cả fiuorouracíl), đo
đó oxaliplatỉn không được hòa tan vởi những dung dịch đó hoặc truyền đồng thời qua cùng bộ dây
truyền. Không có dữ liệu về sự tương thich với những thuốc khác
Vì không có sự chuyến hóa qua trung gian rCytochrome P450 nên ợxalipiatin có thế không điếu
chinh sự chuyên hóa qua P450 của những thuôc cùng dùng theo cơ chế cạnh tranh.
Lời khuyên cho Bệnh nhân
Bệnh nhân phải được thông bảo đầy đủ về nguy cơ tiêu chảy Ínôn và giảm bạch cầu trung tính sau
khi dùng oxaliplatỉn/fiuorouracìl để họ có thế liên hệ ngay với bảo sĩ điều trị để xử lý thích họp.
Bệnh nhân và những người săn sóc phãi được thông báo về nhũpg phản ứng phụ có thể xãy
ra của oxalipiatỉn vả, đặc bỉệt bệnh nhân nên được khuyên bảo đê:
- Tránh những thức ăn vả nước uống lạnh và che phủ cơ thể trước khi tiếp xúc vởi nơi lạnh trong
thời gian hoặc trong vòng 48 giờ sau khi dùng oxaliplatin, vì tác dụng thần kinh có thể xảy ra
nhanh hơn hoặc gia tăng khi bị lạnh.
- Thông bảo ngay với bác sĩ khi có sốt đặc biệt phối hợp vởi tiêu chảy kéo dải hoặc có dấu hiện
nhiễm trùng vì tình trạng nảy có thế cho biết lả số lượng tế bảo máu thấp.
. Thông bảo với bác sĩ nếu nôn kéo dải, tiêu chảy, dấu hìệu mất nước, ho hoặc khó thở hoặc dấu
hiệu có phản ứng dị ửng .
PHẨN ỨNG có HẠI
Thẩn kỉnh
Hỗ trợ Tiễn xa
Rẫl thóng thường: Bệnh ly thân kinh cảm Bệnh lý thân kinh cảm giác ngoại biên đâu
giác ngoại biên tiên (như mât phản xạ gân cơ, loạn cảm,
Trang 5
_Jt’fỎ/
dẩu hiệu dị cảm của Lhermitte)
Thông rhường: Lọạn cảm họng-hầu, co thắt hảm, cảm giác
bât thường vùng lưỡi, cảm giác nặng ngực
Hiếm : Loạn vận ngõn
Những phản ứng có hại về thần kinh có độc tính phụ thuộc liều lượng. Bệnh lý thần kinh cảm giác
ngoại biên xuất hiện trên 85% đến 95% bệnh nhân. Những triệu chứng nảy thường xảy ra sau 2 giờ
truyền dịch oxaliplatin hoặc trong vòng it giờ sau, giảm đi trong những giờ hoặc ngảy kế tiếp, và
thường tái diễn trong những chu kỳ tiếp theo. Chủng có thế xảy ra mau hơn hoặc nặng hơn khi bệnh
nhân nhiễm lạnh hoặc tiếp xúc với vật lạnh. Chúng có thế biều hiện như một di cảm thoáng qua một
loạn cảm vả giảm cảm giác. Có thể có rối loạn ohức năng như khó thực hiên cảc động tảo tế nhị
Thời gían tồn tại cùa các triệu chứng nảy gia tăng theo sô lần cảc chu kỳ điều trị. Cảo triệu chứng
thường giảm đi giữa các chu kỳ điều trị.
Nếu những triệu chứng kéo dải hoặc nếu đau hay rối loạn chức năng xuất hiện, nên giảm liều hoặc
ngưng điêu trị (Xem Liên dùng và Cảch sữ dụng).
Trong điều trị hỗ trợ, đối với liều cộng Jdổn là 850 mgltn2 (10 chu kỳ) nguy cơ xuất hỉện những triệu
chứng kéo dải là 10% và đối với liếu cộng dồn là 1020 mg/m2 (12 chu kỳ) nguy cơ xuất hiện lả
20%.
Trong điều trị tiến xa, trong EFC 2962,16% bệnh nhân dùng oxaliplatin + FU/FA biến hiện dị cảm
và rôỉ loạn chức nãng phối hợp kéo đải trên hai tuần, sau một liếu oxaliplatin cộng dồn trunng binh
là 874 mglm². Hai phần trăm ra khỏi điều trị do dị cảm tồn tại (nghĩa lả tồn tại giữa các iần điều trị),
sau liều cộng dồn oxaliplatin in 759…1 mo mg/rn².
Trong phần lớn trường hợp, các dấu hiệu và triệu chứng thần kinh sẽ cải thiện khi ngưng điều trị.
Phân tich bệnh nhân trong EF C 2962 cho thấy trong 34 bệnh nhân có bệnh lý thần kinh Grad 3
(grad tối đa trong nghiên cứu nảy), 25 (73 5%) có cải thỉện triệu chứng trong một thời gian trưng
bỉnh là 13, 2 tuần. 8 trên 34 bệnh nhân (23%) có triệu chửng hoản toản thoải lui Thời gian kéo dải
trung bình của độc tính thần kinh Grad 3 là 13,6 tuần. Liều cộng dồn trung bình của oxaliplatin khi
khởi đầu là 913. 6 mg/m2 (phạm vi :.169 7- 1713.15 mg/m2 ) Thời gỉan theo dõi trung bỉnh của 34
bệnh nhân nảy là 55,71 tuần.
Một hội chứng rối loạn cảm giác vùng hẩu họng cấp tính đã được ghi nhận trên 1% đến 2% bệnh
nhân. Hội chứng nảy thường xuất hiện khi bệnh nhân nhiễm lạnh và khi có những thay đối nhiệt độ.
Hội chửng nảy biếu hiện bẳng cảm giảc chủ quan nuốt khó và khó thở, cảm giác ngộp thớ mả
không có bằng chứng khách quan về rối loạn hô hẳp (không thiếu oxy, co thẳt họng, co thắt phế
quản).
Những triệu chửng khảo thỉnh thoảng được ghi nhận, đặc biệt là rối loạn dây thần kinh sọ não có
thể phối hợp với những triệu chứng khảo, hoặc cũng có thể xảy ra đơn độc, như sa mi mắt, nhin
đôi, mất tiếngzr chứng khó phát âm/ khan tiểng, thỉnh thoảng được mô tả như líệt dây thanh am, cảm
giác bất thường vùng lưõi hoặc loạn vận ngôn, thinh thoảng được mô tả như chứng mất ngôn ngữ,
đau dây thần kinh sinh bai đau mặt/ đau vùng mắt, giảm thị lục, rối loạn thị trường Ngoải ra,
những triệu chímg sau đây đã được ghi nhận: co oứng hảm/ co thắt oơ/ co cơ không chủ tâm/ co gỉật
cơ] giật rung cơ, sự phối hợp bắt thường/ dảng đi bắt thường/ mắt điếu vận/ rối loạn thăng bằng, co
thắt họng hoặc ngực/ cảm giảc đè nặng! khó chịu/ đau.
Hưyễt học
Trang 6
_Jh'iĩì/
lư .l
Hỗ trợ Tiến xa
Chảy mảu cam, thiếu mảu (mọi Thiếu mảu (mọi mức độ), giảm
mức độ), giảm bạoh cầu trung bạch cầu trung tính (mọi mức độ),
tính (mọi mức độ), giảm tiếu câu giảm tiếu cầu (mọi mức độ)
(mọi mức độ)
Rất thông thường:
Trong điều trị ung thu cá giai đoạn hỗ trợ và tiến xa, phối hợp oxaliplatin với fiuorouxacil vả folinic
acid:
' Về thực chất gia tăng tỷ lệ giảm bạch cầu trung tính và giảm bạoh cầu trung tính nặng (bạch cầu
trungtính <1.0x109/L)vả
' Về thực chất gia tăng tỷ lệ giảm tỉểu cầu (Bảng 8- 9).
Tiêu hóa
Hỗ trợ Tiến xa
Tiêu chảy, buồn nôn, nôn, viêm Tiêu chảy, buồn nôn, nôn, viêm
miệng, chản ăn, đau bụng, viêm miệng, chản ăn, đau bụng, viêm
nỉêm mạc, táo bón. niêm mạc, mất nước, tắc ruột, hạ
kali huyết, nhiễm acid chuyến
Rất thông thường:
hóa, táo bón.
Thông thường : Chứng khó tiêu
Hiếm : Viêm ruột, kể cả tiêu chảy do
Closiridíum difflcile
Phối hợp oxaliplatin vởi f1uorouracil vả folinic acid:
0 Gia tăng tỷ lệ buồn nôn nặng, nôn, tiêu chảy, và viêm miệng, trong giai đoạn điều trị hỗ trợ (xem
Bảng 8) và về thực chất gia tăng những tảo dụng nảy trong điều trị giai đoạn tiến xa. (xem Bảng
9).
Gan mật
’ Hỗ trợ Tiểu xa
Rât ihỏng thường: Tăng transamỉnases và hoạt tính
alkaline phosphatase
Rất hiếm :
Bộ Cơ Xưong
Rất thông thường:
Phản ứng liên quan đến hội ohứng
tắc nghẽn xoang gan, bao gôm
ban xuất huyết, tăng sản tải tạo
bướu nhỏ, xơ quanh xoang, và
tăng huyết ảp tĩnh mạch cứa.
Hỗ trợ
Phản ứng liên quan đến hội
chứng tắc nghẽn xoang gan, bao
gôm ban xuất huyết, tăng sản tải
tạo bưởu nhò, xơ quanh xoang, và
tăng huyết ảp tĩnh mạch cửa.
Tiến xa
Đau hmg*, đau khởp
* Dau lưng. Phải nghiên cứu kỹ nếu phối hợp với tản huyết, hiếm khi được bảo cảo.
Quá mẫn
Hỗ trợ ` Tiến xa `
Rất thông thường: Mân da (đặc biệt mê đay), viêm Mân da (đặc biệt mê đay), viêm
kêt mạc, viêm mũi. kêt mạc, viêm mũi.
T hông thường : Co thắt phế quản, cảm giảc đạn Co thắt phế quản, cảmgiảc đạu
ngực, phù mạch, hạ huyết ảp, sôc ngực, phù mạch, hạ huyêt ảp, sôc
phản vệ. phản vệ.
Các giáo quan
’ Hỗ trợ Tiến xa
Rât thông thường .' Rôi loạn vị giác
Thông thường .— Viêm kết mạo
Bất Ihường: Độc tính với tai
Hiếm: Điếc, viêm thần kinh mắt, mất thị
lực.
Thận
Hỗ trợ Tìến xa
Thông thường : Suy chức năng thận
Rất hiếm .- Hoại tử ống thận
Trong nghiên oửu lâm sảng và sau marketing: rất hiếm bệnh lý thận ống — kẽ cấp dẫn đến suy thận
Â
cap.
Hô hẩp
Hỗ trợ Tiến xa .
Thông thường Viêm mũi, khó thở
' . . . U
Hiêm: Bệnh phôi kẽ câp, xơ phôi 3
O
Hệ miễn nhiễm ,
’ Hỗ trợ , Tiến xa , ỉ
Rát thông thường .' Nhiễm trùng, sôt, lạnh run. Nhiêm trùng, sôt, lạnh run. _:
Thông thường : Sốt giảm bạch oầu trung tinh Sốt giảm bạch cầu trung tính -
Hiếm .- Thiếu mảưtán huyết tự miễn vả '
giảm tiêu câu
Da
Hỗ trợ Tiến xa
Rât thông thường .' Rụng tóc, nôi mân
Trang 8
_WỔ/
Thông thường : Rụng tớc, nổi mẳn
Rụng tóc vùa đã được ghi nhận ở 2% bệnh nhân dùng oxaliplatin đơn liệu pháp, sự phộỉ hợp của
oxaliplatin vả fluorouracil không gia tảng tỷ lệ rụng tóc ghi nhận vởi fiuorouracii đơn thưân.
Thận trọng tại vị trí tiêm truyền
Trản ngoải mạch mảu có thể gây đau tại chỗ và viêm có thể nặng và dẫn tởi biến chửng, bao gồm
hoại tử. Phản' ưng tại ohỗ tiêm, gôm đỏ, sưng vả đau, đã được ghi nhận
Bảng sau đây cung cẩp những phản ứng có hại ghi nhận trong nghiên cứu theo thứ tự tằn số giảm
dằn trong phối hợp oxaliplatin vả FU/F A truyền
Bảng 8: FUIFA :1: Oxalỉplatỉn trong điều trị hỗ trợ ung thư đại trâng - EFC3313 (MOSAIC),
tẩt cả các grad và độc tính grad 3-4 — tẩt cả chu kỳ - % bệnh nhân
Nhảnh A Nhảnh B
FOLFOX4 FU/FA
N=1108 N=lll 1
Tẩt cả Gr 3 Gr 4 Tẩt cả Gr 3 Gr 4
Xét nghiệm
'Giảm bạch cầu hạt 78.9 28.8 12.3 39.9 3.7 i 1.0
`Giảm tiếu cầu 77.4 1.5 0.2 19.0 0.2 0.2
'Thiếu mảu 75.6 0.7 0.1 66.9 0.3 -
r Phân ứng có hại
`Dị cảm 92.0 12.4 NA 15.6 0.2 [ NA
'Buèm nôn 73.7 4.8 0.3 61.1 1.5 0.3
Tiêu chảy 56.3 8.3 2.5 48.4 5.1 1.5
ỊNôn 47.2 5.3 0.5 24.0 0.9 0.5
fViếm miệng/ viêm niêm mạc 42.1 2.8 0.1 39.7 2.1 0.2
ĨRối loạn da 31.5 1.4 0.6 35.5 1.7 0.7
"Rụng tóc 30.2 NA NA 28.1 NA NA
`sỏr 27.3 0.7 0.3 12.2 0.4 0.2
'Nhiẽm trùng 25.2 3.3 0.7 24.9 2.3 0.6
Ệphản ứng tại vị trí tiêm 11.1 2.6 0.5 10.4 3.1 0.2
ịPhán ửng dị ứng 10.3 2.3 0.6 1.9 ị 0.1 0.1
`Huyết khối/ viêm tĩnh mạch 5.7 1.0 0.2 6.5 1.7 0.1
ỊNhiẻm trùng huyết giảm bạch cầu 1.1 0.6 0.4 0.1 … 0.1
`Sốt giảm bạch cầu 0.7 0.7 - 0.1 0.1 ị -
Bảng sau đây cung cấp những phản ứng có hại ghi nhận trong nghiên oứu (xem NGHIÊN CỬU
LÂM SÀNG) theo thứ tự tần sô giảm dấn trong phối hợp oxaliplatin vả FUfFA truyền trên bệnh
nhân ung thư đại trực trảng tiến xa chưa được điều trị.
Trang 9
Jì°ó/
.' Jf²-
Z 11 'Í r. .
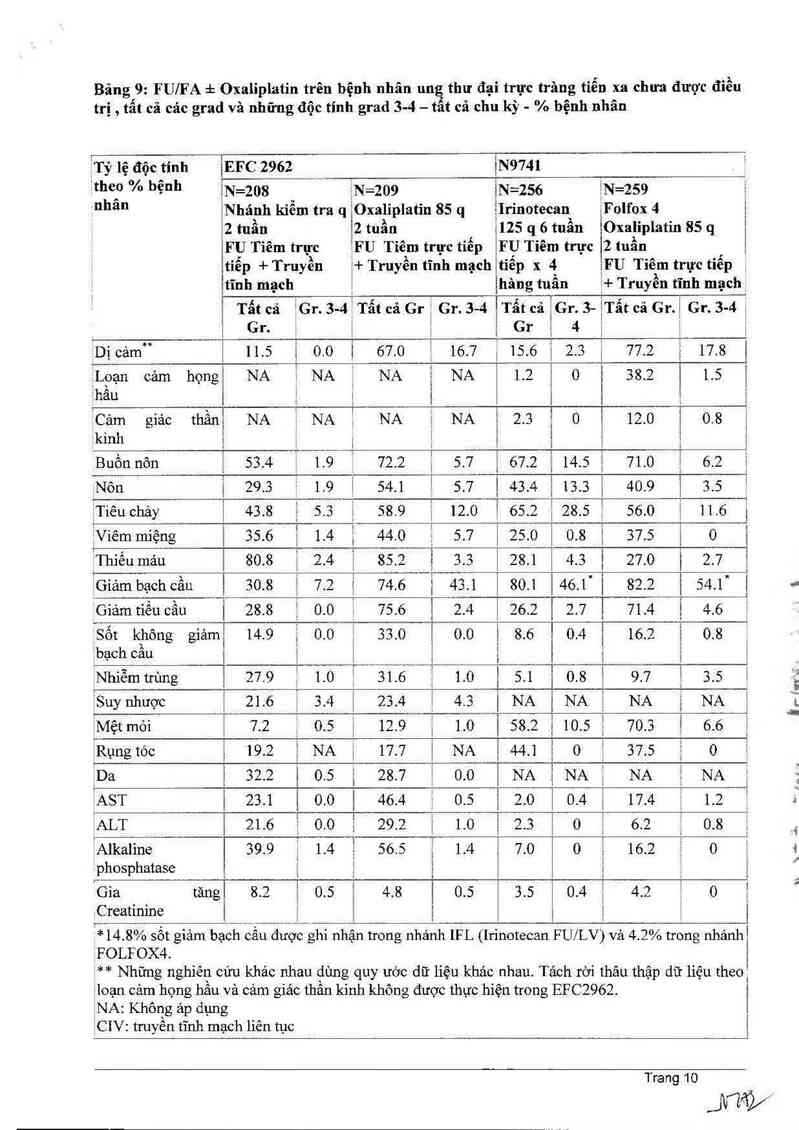
Bảng 9: F UJFA :1: Oxalipiatin trên bệnh nhân un thư đại trực trâng tiến xa ohưa được điều
trị , tất cả các grad và những độc tính grad 3-4 — tat cả ohu kỳ - % bệnh nhân
ĨCIV: truyền tĩnh mạch liên tục
`Tỷ lệ độc tính EFC 2962 N9741
`the…° % bệnh N=208 g =209 =256 ịN=259
nhan Nhảnh kiếm tra q ỉOxaliplatìn 85 q Irinotecan` Folfox 4
2 tuân 2 tuẫn 125 q 6 tuân Oxalipiatin ss q ;
FU Tiêm trực FU Tiếm trực tỉếp F U Tiêm trực 2 tuần ' ị
tiếp + Truyền + Truyến tĩnh mạch tiêp x 4 FU Tiêm trực tiêp .
tĩnh mạch . hãng tuân + Truyền tĩnh mạoh_
Tất cả iGr. 3-4' Tất cả Gr : Gr. s…4 Tẩt cã Gr. s- Tắt cã Gr.Ị Gr. 3-4 ,
Gr. _ Ị Gr 4 ị
Dị cảm“ 11.5 i 0.0 67.0 ! 16.7 15.6 2.3 77.2 ' 17.8
jL_oạn cảm họng NA NA NA * NA 1.2 0 38.2 1.5
ỉhâư
@… giảc thần NA i NA . NA NA 2.3 0 12.0 0.8
kinh ị
Buồn nôn 53.4 1.9 ' 72.2 } 5.7 67.2 14.5 71.0 6.2
Nôn 29.3 1.9 ị 54.1 5.7 43.4 13.3 40.9 3.5
Tiêu chảy 43.8 5.3 ị 58.9 1 12.0 65.2 28.5 56.0 11.6
Viêm miệng 35.6 1.4 ặ 44.0 ế 5.7 25.0 0.8 37.5 0
Thiếu mảu 80.8 2.4 ị 85.2 3.3 28.1 4.3 27.0 2.7
Giảm bạch cầu 30.8 ị 7.2 { 74.6 ị 43.1 80.1 46.1“ 82.2 54.1“
Giảm tiếu cẩu 28.8 ỉ 0.0 75.6 2.4 26.2 2.7 71.4 4.6
Sốt không giảm 14.9 0.0 33.0 0.0 8.6 0.4 16.2 0.8
.bạch câu
Nhiễm trùng 27.9 1.0 i 31.6 _ 1.0 5.1 0.8 9.7 3.5 1
lSuy nhược 21.6 3.4 23.4 Ị 4.3 NA NA NA NA ị
'Mệt mỏi 7.2 . 0.5 12.9 ' 1.0 58.2 10.5 70.3 i 6.6
ĨRụng tóc 19.2 F NA 17.7 NA 44.1 0 37.5 0
IDa 32.2 0.5 28.7 0.0 NA NA NA NA
ỂAST 23.1 0.0 46.4 Ế 0.5 2.0 0.4 17.4 1.2
`ALT 21.6 , 0.0 29.2 ị 1.0 2.3 0 6.2 0.8
'Aikaiine 39.9 ị 1.4 56.5 1.4 7.0 0 16.2 0
phosphatase
'Gia tăng 8.2 0.5 4.8 0.5 3.5 0.4 4.2 0
=Creatinine
*14.8% sốt giảm bạch cầu được ghi nhận trong nhánh lFL (Irinotecan FU/LV) và 4.2% trong nhảnhỊ
FOLFOX4.
** Những nghiên cửu khác nhau đùng quy ước dữ liệu khác nhau. Tảch rời thâu thập dữ liệu theo
ểloạn cảm họng hâu và cảm giảc thân kinh không được thực hiện trong EFCZ962.
NA: Không ảp dụng
Trang 10
JWiỳ
Írim'.í-
Ghi chú:
Rất thông thường: a mo (2 10%)
Thông thường: 21/100 and <1/10(21% and < 10%)
Bất thường: 2 1/1000 and < moc (ả 0.1% and < 1.0%)
Hiếm: a mo,ooo and < 1/1000<2 o.om and < 0.1%) ậ
Rất hiếm: < 1/10,000(< 0.01%) 1
LIÊU DÙNG VÀ CÁCH SỬ DỤNG
Liều dùng:
Trong phối hợp vởi fiuorouracii vả folinic acid liều khuyến cáo điều trị ung thư đại trực trảng tiến
xa iả 85 mg/m2 truyền tĩnh mạch mỗi 2 tuần
Trong phối với fluorouracil vả folinic acid liếu khưyến cáo điều trị hỗ trợ là 85 mg/m2 truyền tĩnh
mạch mỗi 2 tuân trong 12 chu kỳ (6 tháng).
Thay đỗi liễu lượng:
Trước mỗi chu kỳ điều trị, bệnh nhãn nên được đảnh giả về độc tính cùa thuốc và điếu chỉnh liếu
oxaliplatìn cho thích hợp.
Độc tính Thần kinh:
Nếu phản ửng thần kinh cắp xảy ra, ví dụ loạn cảm họng hầu cấp, tăng thời gian truyền oxaliplatin
từ 2 giờ lên đến 6 giờ. Như vậy sẽ giảm 30% Cmax và có thế giảm bởt những độc tính cấp.
Nếu mất cảm giặc hay dị cảm kéo dải trên 7 ngảy hoặc tương tảo với chức năng (độc tỉnh grad 2),
nên giảm 25% lìêu oxaliplatin.
Nếu mất cảm giảc hay dị cảm tương tảo với những sinh hoạt hảng ngảy (độc tính građ 3), phải
ngưng oxalỉplatin.
Đôc tính huyết học .
Nếu độc tính huyết học xảy ra (bạch cầu trung tính < 1 5 x 10 9!L hay tiếu cầu < 75 X 10911.) trước
khi khởi đầu điều trị hoặc trước đợt điếu trị kế tiếp:
- Nên trì hoãn đợt đìềư mị cho đến khi bạch cầu trung tính 2 1.5 x 10% và tiểu cầu ; 75 x 109/L
and
. Giảm líều oxalỉplatin từ 86ng…² xuống 75 ngm² mỗi 2 tuần và giảm 20% liều FU (điều trị hỗ
trợ).
' Giảm liều oxaiiplatin từ 85mg/m2 xuống 65 mg/m2 mỗi 2 tuần và gỉám 20% iiều FU (điều trị
tiến xa).
Đôc tính đường tiêu hóa:
Nếu phản ứng tỉêu hóa grad 3-4 xảy ra, như đã được đảnh giả theo tiêu chuẩn cùa Viện Ung Thư
Quốc Gia Hoa Kỳ:
Trì hoãn điều trị cho đểu khi những phản ứng có hại thoải lui.
* Giảm liều oxaliplatin từ 8Smg/m2 xuông 75 mg/m2 mỗi 2 tuần và giảm 20% liều FU (điều trị hỗ
trỢ)
~ Giảm lìếu oxalipiatin tù SSmgfm² xuống 65 mg/m² mỗi 2 tuần vả giảm 20% liều FU (đỉều trị
tiên xa).
Độc tính gắn với fluorouracil:
Cũng phải điều chỉnh liếu đối với độc tỉnh gắn với f1uorouracìl (xem thông tin sán phấm lỉên quan).
Trang 11
Oxaliplatin phải được dùng trước fluorouracil.
Oxalipiatin được dùng truyền tĩnh mạch từ 2 đến 6 giờ trong 250 đến 500 mL glucose 5% tiêm.
Chuẩn bị và Sử dụng :
Những thận trọng đặc biệt để sử dụng:
' KHỘNG dùng bất cứ vật liệu tiêm nảo có chứa aluminium.
~ KHÔNG được dùng khi chưa pha loãng.
' KHÔNG được pha lẫn hoặc dùng với sodium chloride tiêm hoặc bất cứ dung dịch nảo khảo chứa
chlorid
' KHÔNG pha lẫn với bất cứ thuốc nảo khảo hoặc dùng đồng thời cùng một dây truyền (đặc biệt
fiuorouracỉl vả folinic acid). Có thể dùng óng Y (xem Truyền dịch).
- CHỈ DÙNG chất pha loãng được khuyến cảo (xem duới đây).
Không được dùng bất cứ dung dịch nảo đã hoản nguyên cho thấy dấu vết kết tủa và phải hủy dung
dịch.
Thao tác:
Cũng như đối với những hợp chất khảo có khả năng gây độc, phải thận trọng khi thao tảo và chuẩn
bị dung dịch oxalỉplatin.
Việc nhân viên y tế thao tảo tác nhân gây độc tế bảo nảy đòi hòi mọi thận trọng để đảm bảo sự bảo
vệ người thao tảo và môi trường chung quanh. Cần dùng quằn ảo bảo vệ thích hợp, gồm kính bảo
hộ, khăn che mặt và găng tay. Phụ nữ mang thai phải được căn dặn trảnh thao tảo những tảo nhân
độc tế bảo. Nếu oxaliplatin đậm đặc, dung dịch pha sẵn hoặc dung dịch truyền tiếp xúc với da, niêm
mạc hoặc mắt, nên rửa ngay và thật kỳ với nước.
Chuẩn bị dung dịch truyền
Lọ tiêm Oxaliplatin không chứa chất bảo quản và chỉ dược dùng một lần thôi. Hãy vứt bỏ bất
cử những phần oòn iại.
Pha Ioãng trước khi truyền
Dung dịch hoản nguyên,` được pha loãng trong một dung dịch truyền chứa 250— 500 mL
glucose 5% dạng tiêm. Về mặt vi sinh học và hóa học, dung dịch truyền nảy phải được dùng
ngay. Hãy quan sảt kỹ lọ thuốc trưởc khi dùng. Chỉ những dung dịch trong suốt không có cặn
mới được sử dụng. Sản phâm chỉ được dùng một lần thôi. Hãy vứt bỏ bất cử những phần còn
lại. KHÔNG BAO GIỜ dùng dung dịch sodium chloride đề hoản nguyên hoặc pha loãng.
Tiêm truyền:
Không cần bù nước trước khi dùng oxaliplatin. Oxaliplatin pha loãng trong 250 - 500 mL dung dịch
glucose 5% tiêm phải được tiêm truyền hoặc qua đường tĩnh mạch trung ương hoặc tĩnh mạch
ngoại biên trong 2 - 6 giờ. Khi oxaliplatin được dùng với fluorouracil, phải tiêm truyền oxalipiatin
trưởc t1uorouracỉ].
Oxaliplatin có thể được truyền cùng vởi folinic acid tiêm truyền dùng ống Y đặt ngay trước vị trí
tiêm. Cảo thuốc không được pha ohung trong cùng một túi truyền dịch. Folinic acid phải được pha
loãng dùng dung dịch truyền đẳng trương như dung dịch glucose 5% nhưng KHÔNG dùng dung
dịch sodium ohloride hoặc những dung dịch kiềm.
Rừa đường dây sau khi dùng oxaliplatin.
Trang 12
JWỐ/
\ i'."iiĨ `
\
\\ Am
Mặc dù có rất ít hoặc không oó khả năng gây giộp da, khi thuốc thoảt ra ngoải mạch có thể gây đau
vả viêm tại chỗ có thể nặng và dẫn đến những biên chứng đặc biệt khi oxaliplatin được tiêm truyền
qua tĩnh mạch ngoại biên. Trường hợp oxaliplatin bị thoát ra ngoải mạch, phải ngưng tiêm truyền
ngay tức thì và khới đầu điều trị tại chỗ thông thường.
Để giảm nguy cơ vi sinh sau khi hoản nguyên nên pha loãng vâo dịch truyền để dùng ngay. Nếu
chưa được sử dụng ngay thi dung dịch nảy phải được bảo quản ở 2° - 8°C không quá 24 giờ.
Loại thải:
Tất cả những vật liệu dùng để hoản nguyên, pha loãng và sử dụng phải được hùy theo nhu cầu quy
định địa phương.
QUÁ LIÊU
Không có thuốc giải độc cho oxaliplatin. Trường hợp quá liều, cảc phản ứng có hại có thể trầm
trọng hơn. Theo dõi các thông sò huyết học và điểu trị triệu ohứng.
DẠNG TRÌNH BÀY
Oxalipiatin được cung cấp dưới dạng dung dịch tiêm truyền đậm đặc vô trùng 50 mg/IOmL và
100 mg/20mL và 200 mg/40mL.
Hộp ] lọ 40m1 dung dịch đậm đặc dùng để pha tìêm truyền
BẢO QUẢN
Bảo quản ở nhiệt độ không quá 30°C, trảnh ảnh sảng, tránh đông lạnh. Dung dịch sau khi pha bảo
quản ở ngăn mát ở nhiệt độ 2- 8°C và không quá 24 giờ.
HẠN SỬ DỤNG: 18 tháng kế từ ngảy sản xuất.
TIÊU C1_iUẨN CHẤT LƯỢNG
Tiêu chuân nhả sản xuât
Thông báo cho Bảo sĩ khi xảy ra các tác dụng ngo_
Đế thuốc trảnh xa tầm tay trẻ em. ' ' Q. CỤC TRUỜNG
Không dùng thuốc quá hạn dùng. P.TRUỜNG PHÒNG
Tên và địa chỉ nhà sản xuất: Ấỷayen Jẳlẩ JẳInấ
Zydus Hospỉra Oncology Private Limited
Pharmez Special Economic Zone, Plot number 3, Sarkhej Bavla Highway, Matoda, Taluka San
Ahmedabad, In-382210, Ấn Độ.
/
1
Trang 13
,MẮ/
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng