










rutmcn…h … «
/ Illlllll )(
|…0L/ỒWOS naMâqần
uueldiiexo
hc_
& Yhubc bln meo uc…
Oxaliplatin
“Ebewe" 50mg/10m1
Bưcmg dung Tném intvèn iình
mach
50mg
BỘ Y TẾ
cuc QUÁN LÝ nược
ĐÃ PHÊ DL'YỆT
Lân t1âuz...íiẫi…Aẩạl…Ziỉif
n-- 1
& orncnprioo o…g
Oxaliplatin
“Ebewe" 50mg/tom! W
Ad… …svubon. lf'llavenoul me
nnly nhu mcnnsftlunnr
50mg
illllil
65408i
911111
Oxaliplatin
“Ebewe" 50mg/10111l
ỉ _ harma Ges.m.h.H. th.KG
† Hlllll 7` Mondseestraũe 11
\ I '4866 Unlerach/Austna
" ~ — Tel 07666781230
WVm
,, … … am
ĩ Oncmuc Prurwu
Farben: ỌỂẽDỊQẸĐ 185 C_
gỆamone 469_Ọ
Code: 425 _
Faltschachtel OI Faltschachtelzuschnltt: O
Artikelnummer: 743194-ffl (inld. Klischeevermerk):
Format: ỉ x Ẻ_ x Ẹme FS-Norm: _ _
. G_cạg_HKS 92K
Schmuckfarbe Spannung ủber 1.1 ja ²0 | neinO
Besonderheit:
mmzmn mua
n
“"
LG 510qu Oml 1 … wtlF It,—fflhiiiiji ĩ Ễ
' powđet contains f›unq ~ `_ *
' ~ `xvthplat-i- anđ :mcsc ?
Oxahplatm ………t :
11111 nt veixrịliiuteii .
“Ebewe” SũmgHOn-1l muthw _… i
cmhplattr «een … 17111 3
_ ___.___._, reach anti sint'0l ẳ
. fhildian '
l.V. use only after … 11nq11 iạt …
~ - Hecnnztimm ~rciưrtnn
reconshtut1on. _,m c, ,, , ,,v _ _
- ~ mmedmipi ² :
Oxalnplattn 50mg ' _,
Ê
snn …a1 va đong got so zảp ta` : __
Oncotec Pham): Produktien GmbH ụ(imư “'
Đong gò1mư cip va xoa. xuớng 151 Ủ-
Ebmuc Fhuma GmbH Nin KG | … .… ,
`V :
.KG
F EBEWE Pharma Ges m.b.H. ng
' => Be 11
Mundse..sira
4866 UntetachlAustna
Tet : 0766518123—0
Etikette AMP O IDST O
CARINI-Standard 2007
Artikelnummer: 734089 -ffl(inkl. Klischeevermerk):
Format: 71 x 31 mm
Farben:ọPantone 185 C . Schwarz C
gPantơne 469 C .
Eindruckfeld rechts: 6mm 0 8 mm I
Code: 2254 Seite: rechts(DSTffl links (AMP) O
Stellung: M4
7340 - .
09 ntvahmoớ 1 @ 22.05.2010 00:46:28
Wifi lhgt
TỜ HƯỚNG DẨN SỬ DỤNG THUỐC
Rx_ Thuốc bán theo đơn
Oxaliplatin “Ebewe“ SOmg/lOml
Oxaliplatin “Ebewe“ 100mg/20m1
Dạng bảo chế Bột đông khô pha dung dịch tiêm truyền
Đường dùng Tiêm truyền tĩnh mạch
Thảnh phần Oxalipiatin “Ebewe” 50mg/10m1
Mỗi lọ dựng bột thuốc đông khô chứa 50 mg oxalipiatin. Một mi dung
dịch tải tạo lại chứa 5 mg oxalipiatin là hoạt chất tác dụng.
Tá dược: Iactose monohydrat
Oxalipiatin “Ebewe” 100mg/20m1
Mỗi lọ đựng bột thuốc đông khô chứa 100 mg oxaliplatin. Một ml dung
dịch tải tạo lại chứa 5 mg oxaliplatin 18) hoạt chẩt tảo dụng.
Tá dược: Iactose monohydrat
Chỉ định điều trị: Ổ\vỵ
Oxalipiatin kết hợp với 5 — fiuorouracil (5 - FU) vả acid folinic (FA) được chỉ định:
- Trong liệu phảp bổ trợ trong trường hợp ung thư đại trảng giai đoạn 111 (Duke“s C) sau
khi dã phẫu thuật cắt bỏ hoản toản khối u tiên phảt. %
- Điều trị ung thư đại - trực trảng đã di cãn. "
Đường dùng:
Oxalipiatin được dùng theo cảch tiêm truyền tĩnh mạch.
Việc dùng oxaliplatin không đòi hỏi phải tiểp nhiếu nước. Hoả tan oxaiiplatin vảo 250
đến 500 ml dung dịch glucose 5% để tạo ra một dung dịch có nồng độ không thấp hơn 0,2 mglml
và được tiêm truyền vảo một tĩnh mạch trung tâm hay tĩnh mạch ngoại vi trong thời gian từ 2 đến
6 giờ. Việc tiêm truyền oxalipatin bao giờ cùng phải thực hiện trước việc tiêm 5 — tiuorouracil.
EBEWE ":
41
Trong trưởng hợp tiêm ra ngoải tĩnh mạch, phải ngừng ngay việc tiêm.
Cảc điều hướng dẫn khi dùng;
Oxaliplatin phải được tải tạo (tức là hoả vảo một ít dung môi), sau đó được pha loãng
trước khi dùng. Chỉ những dung môi đã được khuyến nghị để tải tạo và để pha loãng sản phẳm
dã đông khô thì mới được sử dụng.
EBEWE Pharma Ges.m.b.H. NIg.KG
MondseestraBe 11
4866 Unterach/Austria
Tel.: 0766518123—0
Liều dùng, cách dùng: Chỉ dùng cho người lớn
Liều dùng oxaliplatin dược khuyến nghị cho trường hợp dùng 1iệu phảp bổ trợ là 85
mg/m2 theo đường tiêm tĩnh mạch, hai tuần dùng một lân, dùng tât cả 12 lân (6 thảng).
Liều dùng oxaliplatin được khuyến nghị trong điều trị ung thư dại - trực trảng đã di căn là
85 mglm², tiêm tĩnh mạch, hai tuần một lần
Liều lượng nói trên cần được hiệu chinh theo mức dung nạp của bệnh nhân (Xem “Thận
trọng dùng khi dùng thuốc“).
Oxalzịzlatín bao giờ cũng dùng Irước các fiuoropyrỉmidin.
Oxaliplatin được tiêm truyền trong thời gian 2 đến 6 giờ theo dường tĩnh mạch, với thể
tích 250 đến 500m1 trong dung dịch glucose 5%.
Oxalipiatin chủ yếu được dùng cùng với 5 - fiuorouracil theo chế độ tiêm truyền liên tục,
trong chế độ điều trị 2 tuần một lần thi 5 - tiuorouracii dùng theo chế độ tiêm nhanh, kết hợp với
việc tiêm truyền liên tục.
Đối với những quẳn thề dăc biêt
- Bệnh nhân có bệnh thận
Chưa nghiên cứu việc dùng oxaliplatin cho người có bệnh nặng về thận (xem “Chống chỉ
định“). ,
Đối với những bệnh nhân có bệnh hận với mức độ vừa phải, có thể bắt đẩu diều trị
với lỉều bình thường được khuyến nghị (xem “Thận trọng dùng khi dùng thuốc 45). Đối với những
bệnh nhân có rổi loạn chức năng thận nhẹ, không cần thiết phải hiện chinh liều lượng.
- Bệnh nhân thiếu năng gan.
Chưa nghiên cứu việc dùng oxaliplatin cho người oó bệnh nặng về gan. Đối với phân
nhóm các bệnh nhân mà cảc test thứ về chức năng gan lúc ban đầu là không binh thường, không
thấy độc tính cấp cùa oxaliplatin tăng lên. Trong việc phảt triến sử dụng trên lâm sảng, không
cẩn việc hiệu chỉnh iiểu dùng riêng cho những bệnh nhân có test thứ về chức năng gan không
binh thường.
Bệnh nhân lớn tuối
Không thấy tăng những biếu hiện độc tính nghiêm trọng khi oxaiiplatin được dùng riêng
hay dùng kết hợp với 5 - tiuorouracil ở những bệnh nhân trên 65 tuổi. Vì vậy, không cần hiệu
chinh liều dối với những bệnh nhân iớn tuổi.
Chổng chỉ định:
Chống chỉ định dùng oxaliplatin đối với những bệnh nhân sau:
. Có tiên sử quá mẫn cảm với oxaliplatin
— Cho con bú
— Có sưy tuỳ trước khi bắt đầu liệu trình thứ nhất, được minh chứng theo số đếm bạch cầu
trung tính < 2 x 10°7L vả/ hoặc số đếm tiểu cẳu < 100 x10°71…
… Có tới loạn chức nãng thẳn kỉnh cảm giác ngoại biên trước bắt đầu liệu trình thứ nhắt.
' Có rối loạn chức năng thận nặng (độ thanh thải creatinin thẳp hơn 30 mVphủt) (xem
mục Đặc tính dược động học).
Thận trọng dùng khi dùng thuốc:
Oxalipiatin chỉ được dùng ở những khoa chuyên về ung thư, và phải được đặt dưới sự
giảm sát cùa một chuyên gia về ung thư có kỉnh nghiệm.
Suv thân:
Do hãy còn có ít thông tin về tính an toản đối với những bệnh nhân có bệnh về thận ở
mức độ vừa phải, chỉ sử dụng thuốc nảy sau khi đã có sự cân nhắc, đảnh gỉả thich hợp về lợi
ích/nguy cơ với bệnh nhân. Trong trường hợp nảy, cần theo dõi chặt chẽ chức năng thận, và hiệu
chinh iìều dùng theo độc tính thuốc.
Phản ứng di ứng:
Các bệnh nhân có tiển sứ dị ứng với hợp chất của platin, phải theo dõi những triệu chứng
về dị ứng. Khi có phản ứng giống phản vệ với oxalipiatin, phải ngừng lập tức việc tiêm truyền và
bắt đầu tiến hảnh ngay vỉệc điếu trị cảc triệu chứng thích hợp. Việc dùng tiếp oxaliplatin 1o
chống chi dịnh. Phản ứng chéo, đỏi khi gây tử vong, đã được bảo cáo với tất cả cảc hợp chất
platin. W’
Trong trường hợp tỉêm oxaliplatithĩo thoảt mach. phải ngừng lập tức việc tiếm truyền. vả
bắt đầu ngay điều trị tại chỗ các triệu chứng.
Triẽu chứng thần kinh:
Cần phải theo dõi chặt chẽ độc tỉnh cùa oxaiiplatin trên thần kinh, đặc biệt khi dùng với
cảc thuốc khác độc với thần kinh. Việc thăm khám về thần kinh phải được thực hiện trước mỗi
iần tìêm thuốc và định kỳ sau đó.
Đối với những bệnh nhân có xuất hiện ioạn cảm gỉảc hạ hầu cẳp tính (xem ““Các tảo dụng
không mong mưốn“) trong thời gian tiêm truyền 2 giờ, hoặc sau đó vải giờ, thì việc tiêm truyền
oxaiỉpiatin iân tiêp sau phải tiến hảnh kéo dải trong 6 gỉờ.
Thần kinh ngoai bỉên:
Nếu những triệu chứng thần kinh (ioạn cảm, dị cảm) xuất hiện, thì việc hiệu chỉnh liều
[ượng oxalipiatin phải dựa vảo mức độ nghiếm trọng và thời gian kéo dải cảc hiện tượng nảy.
- Nếu cảc triệu chứng nảy kéo dải trên bảy ngảy và gây nhiều phiền hả, thì giảm Iỉều
oxaiiplatin xuống từ 85 đến còn 65 mg/m2 (trong trường hợp ung thư dì căn), hoặc còn 75
mg/m2 (trong liệu phảp bổ trợ). '
- Nếu có triệu chứng dị cảm nhưng không lâm rối loạn chức năng, và kéo dải cho đên tận
iẫn tiêm tiếp sau, thì giảm liều oxaliplatin từ 85 xuống còn 65 rnglm2 (trong trường hợp
ung thư di cãn) hoặc còn 75 mglm² (trong liệu phảp bổ trợ).
- Nếu có triệu chứng dị cảm kèm theo rối ioạn chức năng kéo dải cho đến tận lần tiêm tiếp
sau, thì ngừng dùng oxaiiplatin.
- Nếu các triệu chứng trên được cải thiện sau khi ngừng thưốc, có thể xem xét việc sử dụng
lại thuốc nảy.
Các bệnh nhân phải được thông bảo trước về khả năng có những triệu chứng về bệnh
thẩn kinh cảm gìảc ngoại biên kéo dải sau khi đã hoản thảnh đọt điều trị. Có những trường hợp
dị cảm mức độ vừa phải khu trú hoặc dị cảm gây rối ioạn các hoạt động theo chức nãng kéo dải
tới 3 năm sau khi ngừng điều trị trong biện phảp bổ trợ.
Hôi chứng bênh não chắt trắng có thế ghuc hồi (Reversible Posterior Lcukoencephaionathv
SVndrome - RPLS):
Các trường hợp bệnh não chất trắng có thể phục hồi (RPLS cũng được biểt đến như hội
chửng bệnh lý năo có thể phục hồi PRES-Posterior Reversible Encephalopathy Syndrome) đă
được ghi nhận trên bệnh nhân dùng oxaiiplatin trong hóa trị liệu phối hợp. RPLS hỉếm gặp, có
thể phục hồi, nhanh chóng phảt triển thảnh cảc triệu chứng thần kinh, có thể bao gỗm co giật,
tăng huyết ảp, đau đẩu, lù iẫn, mù mắt và cảc rối loạn thị giảc và thần kinh khảc (xem mục ““Các
tảc dụng không mong muốn”). Chẳn đoản RPLS dựa trên hình ảnh não, chủ yếu iả hinh ảnh chụp
cộng hưởng từ hạt nhân.
LÍ
Buôn nôn. nôn. tiêu chảv. mât nước và thay đôi vê h1Ệtẩh/oc:
vè độc tính đối với dạ dảy - ruột, thế hiện 6 các triệu chứng buồn nôn vả nôn, đòi hói
phải có biện phảp dự phòng vả/hoặc liệu phảp chống nôn (Xem “Các tác dụng không mong
muốn“).
Có thể xảy ra các hiện tượng mất nước, tắc ruột, hạ knli huyết, nhiễm acid chuyến hoá,
suy thận do hiện tượng nôn/ia chảy nặng, đặc biệt khi kết hợp oxaiipiatin với 5 - fiuorouraci].
Nếu xuất hiện độc tính với mảu (bạch cầu tnmg tính (<1,5 x 10971, hay tiếu cẩu <50 x
10°7L), thì cần hoãn lại 1ần tiêm tiếp sau cho đến khi cảc thông số huyết học trở về những giá trị
chấp nhận được khi đó phải thực hiện đếm máu toản bộ, có phân loại bạch cầu trưởc khi tiêm lại,
và cũng thực hiện như vậy mỗi lần tiêm tiếp sau.
Cảo bệnh nhân cần được thông bảo đầy đủ về nguy cơ ia chảy/nôn, nguy cơ viêm niêm
mạc/viêm mỉệng và giảm bạch câu trung tinh sau khi tiêm oxalíplatin và 5 — fiuorouraci] để họ
có thế gặp ngay bảo sỹ điếu trị, kịp có những chăm sóc cẩn thiết.
`I th
Nếu có hiện tượng viêm niêm mạc/viêm miệng có kèm theo hay không kèm theo giảm
bạch cầu trung tính, thì lần tiêm thuốc tiếp sau cẳn được hoãn lại cho đến khi hiện tượng viêm
niêm mạc/viêm miệng hồi phục lại trở về mức độ 1 hoặc mức dộ thắp hơn vả/hoặc đến khi số
đếm bạch cầu trung tính đạt tới 1,5 x 109/L.
Khi dùng liệu pháp kết hợp với 5 -fluorouracil (có kèm hay không kèm acid folinic), thì
cần hiệu chinh liều thường dùng cùa 5 - iiuorouracil theo những độc tính xuất hiện.
Nếu xuất hiện ỉa chảy mức độ 4, giảm bạch cầu trung tính mức độ 3 - 4 (số đếm bạch cầu
trung tính < 1.0 x 10°7L), giảm tiểu cầu mức độ 3 - 4 (số đếm tiều cẳu < 50 x 10°7L), thì phải
giảm liếu oxalipiatin từ 85 mglm2 xuống còn 65 mg/m2 (trong trường hợp ung thư di căn) hoặc
xuống còn 75 mglm² (trong liệu phảp bổ trợ), thêm vảo đó là giảm liều 5 - fluorouracii theo đòi
hỏi.
Phối:
Nếu gặp trường hợp có những triệu chứng hô hấp không rõ nguyên nhân như ho khan,
khó thờ, thờ có tiểng lép bép, X quang có thâm nhiễm ở phổi, cần phải ngừng dùng oxalipiatin
cho đến khi khảm bệnh phối loại trừ bệnh phổi kẽ (xem ““Các tác dụng không mong muốn“).
ủa
Trong trường hợp cảc kết quả xét nghiệm chức nãng gan bất thường hoặc tãng ảp tĩnh
mạch cửa không rõ rảng do di căn gan, trường hợp rất hiếm gặp rối loạn mạch mảu gan do thuốc
cần dược xem xét.
Phu nữ có thai
Sử dụng thuốc cho phụ nữ có thai, xem mục “Phụ nữ có thai vả cho con bú”.
Khả nãng sinh sản cỷ
Độc tính trên gen cùa oxaliplatin đã đ _c quan sải thấy trong cảc nghiên cứu tiền 1âm
sảng. Do đó, bệnh nhân nam giới diều trị bằng oxaiipiatin được khuyên không nên có con trong
thời gian điều trị và trong vòng 6 thảng sau khi điều trị. Cảc bệnh nhân nảy nên được tư vấn về
việc bảo quản tinh trùng trước khi bẳt dầu diều trị do oxaiiplatin có thể lảm mất khả năng sinh
sản và tảc dụng nảy có thể không hồi phục.
Phụ nữ không nên có thai trong thời gian điều trị bằng oxaliplatin và nên sử dụng biện
pháp trảnh thai có hiệu quả (xem mục “Phụ nữ có thai vả cho con bủ”).
Phụ nữ có thai và cho con bú
Cho đến nay, chưa có đủ thông tin về tính an toản của thuốc khi dùng cho phụ nữ mang
thai. Trong các nghiên cứu trên động vật, độc tính trên khả nãng sinh sản đã được ghi nhận. Do
đó, oxaliplatin không được khuyến cáo sử dụng trong thời kỳ mang thai và trên phụ nữ có khả
năng mang thai không sử dụng cảc biện pháp trảnh thai.
Chỉ nên sử dụng oxalỉplatin sau khi đã có những đảnh giá thỉch hợp trên bệnh nhân về
nguy cơ trên thai nhi và được sự đống ý cùa bệnh nhân.
Phải sử dụng cảc biện phảp trảnh thai thích hợp trong thời gỉan đỉều trị và sau khi ngừng
điều trị trong khoảng thời gian 4 thảng đối với phụ nữ vả 6 thảng dối với nam giới.
Việc thải trừ thuốc qua sữa chưa được nghiên cứu, nên chống chỉ định dùng oxaliplatin
đối với phụ nữ cho con bú.
Oxalipiatin có thế lảm mắt khả nãng sinh sản (xem mục “Thận trọng khi dùng thuốc”).
Ảnh hưởng trên khả năng lải xe và vận hảnh mảy móc
Chưa có cảc nghiên cứu về ảnh hưởng cùa thuốc trên khả năng 1ải xe và vận hảnh máy
mỏc. Tuy nhiên, điều trị bằng oxaliplatin lảm tãng nguy cơ gây chóng mặt, buồn nôn, nôn và các
triệu chứng thần kinh khảo ảnh hưởng đến khả năng đi lại và cân bằng dẫn đến những ảnh hưởng
ở mức độ nhẹ hoặc trung bình dến khả năng 1ái xe và vận hảnh máy móc.
Rối loạn thị giảc, đặc biệt là mất thị lực thoảng qua (có thể hồi phục sau khi ngừng điều
trị), có thể ảnh hưởng đến khả năng iải xe và sử dụng mảy móc của bệnh nhân. Do đó, nên cảnh
báo bệnh nhân về nguy cơ xuất hiện các biến cố nảy trên khả năng iải xe và sử dụng mảy móc.
Tương tác thuốc:
Với những bệnh nhân có dùng một liều oxaliplatin lả 85mg/m2 ngay trước khi dùng 5 -
tiuorouracil, thì không thấy có thay đối gì về cảc thông số dược động học của 5 - fiuorouracil. In
vitro, không thấy oxaliplatin bị đấy khỏi mối liên kết với cảc protein của huyết tương khi dùng
cùng với cảc thuốc sau: erythromycin, salicylat, granisetron, paciitaxel và natri valproat.
Các tác dụng không mong muốn:
Tảo dụng có hại hay gặp nhất của oxaliplatin dùng kết hợp với 5 - fluorouracil/acid
folinic (5 - FU/FA) lá trên dạ dảy - ruột (ia chảy, buồn nôn, vả viếm niêm mạc) là độc với mảu
(giảm bạch cầu trung tính, giảm tiếu cầu) và là độc với thần kinh (tảo dụng trên thẩn kinh cảm
gỉác ngoại biến cấp tính và do thuốc tích Iuỹ). Nói chung, cảc tác dụng có hại nảy khi dùng
oxaliplatin cùng với 5 - FUIFA là hay gặp hơn và nghiêm trọng hơn trường hợp chỉ dùng 5 -
FU/FA.
Tần suất xuất hiện cảc tảo dụng phụ nảy ở bảng dưới đây là rủt ta từ những nghiên cứu
lâm sảng trong trường hợp ung thư di cãn và trong liệu phảp bổ trợ (trong đó nhóm dùng
oxaliplatin + 5 FU/FA đối với ung thư di căn có 416 bệnh nhân, và đối với liệu pháp bổ trợ có
1108 bệnh nhân) và từ những kinh nghiệm trong điều trị thu được sau khi thuốc đã được đưa ra
thị trường.
Mức độ của tần suất được định nghĩa theo quy ước như sau:
—ơẶ_g_
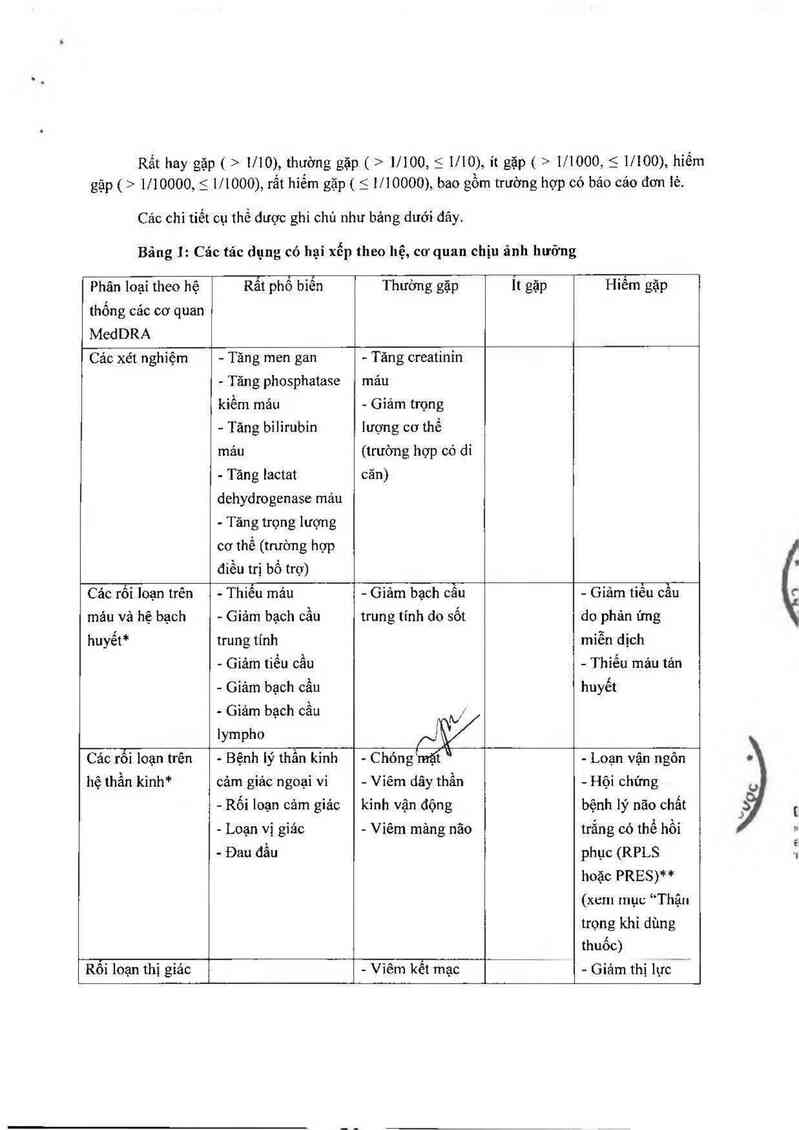
Rẳt hay gặp ( > 1/10), thường gặp ( > 1/100,51110),1tgặp(>1/1000,51/100), híếm
gặp ( > 1/10000, S 1/1000), rẩt hiếm gặp ( S 1/10000), bao gồm trường hợp có báo cảo đơn !ẻ.
Các chi tiết cụ thể được ghi chủ như bản g dưới đây.
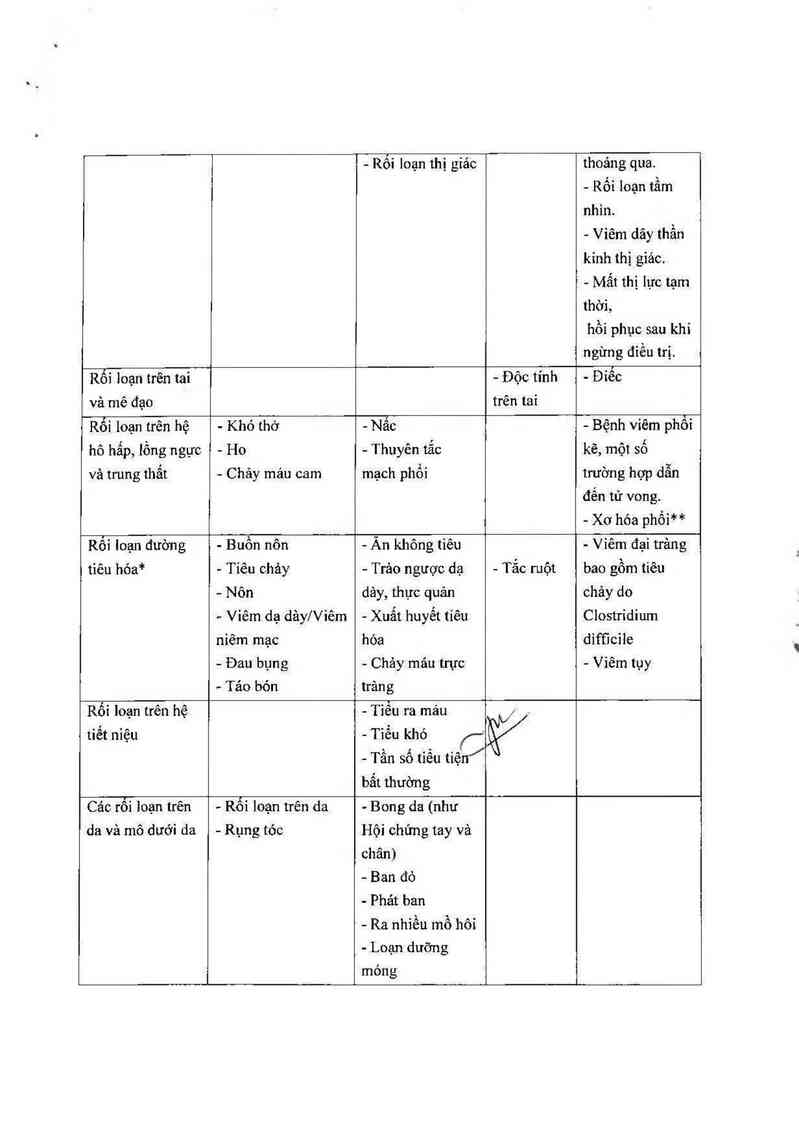
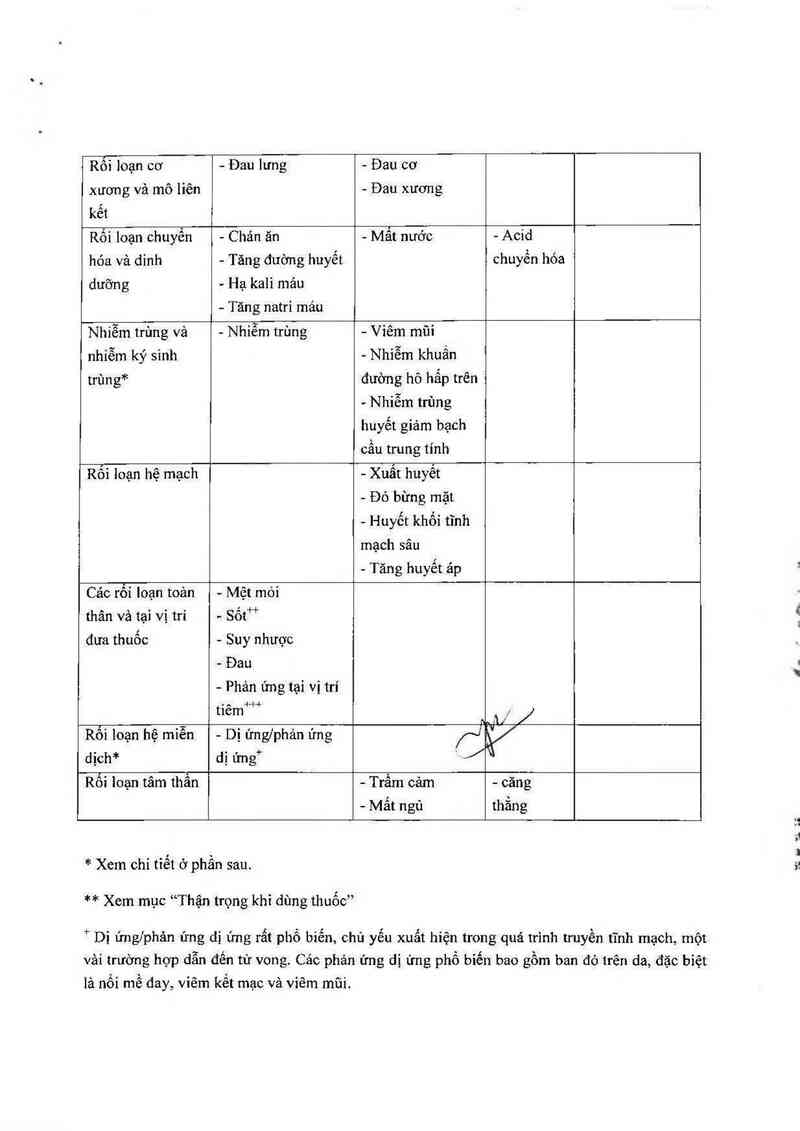
Bảng ]: Các tác dụng có hại xếp theo hệ, cơ quan chịu ảnh hưởng
Phân loại theo hệ
thống cảc cơ quan
MedDRA
Rất phố bỉến
Thường gặp
Ít gặp
Hiếm gặp
Cảo xét nghiệm
- Tăng men gan
- Tăng phosphatase
kiềm mảu
- Tăng bilirubin
mảu
- Tăng iactat
dehydrogenase máu
- Tăng trọng iượng
cơ thể (trường hợp
điều trị bổ trợ)
— Tăng creatinin
máu
- Giảm trọng
lượng cơ thể
(trường hợp có di
cãn)
Cảc rối loạn trên
mảu và hệ bạch
huyết*
- Thiếu mảu
— Giảm bạch cầu
trung tính
- Giảm tiếu cầu
- Gìảm bạch cầu
- Giảm bạch cẳu
lympho
- Giảm bạch cẫu
trung tính do sốt
- Giảm tiếu cầu
do phản ứng
mỉễn dịch
- Thiếu mảu tản
huyết
Các rôi loạn trên
hệ thân kinh*
- Bệnh iý thần kinh
cảm giảc ngoại vi
- Rối loạn cảm giảc
- Loạn vị gỉảc
- Đau đẩu
418
— Chóng'mậĨ
- Viêm dây thẳn
kinh vận động
- Viêm mảng não
Rối loạn thị giác
- Viêm kết mạc
- Loạn vặn ngôn
- Hội chứng
bệnh lý não chất
trắng có thể hồi
phục (RPLS
hoặc PRES)**
(xem iriỤc “Thận
trọng khi dùng
thuốc)
- Giảm thị iực"
.'mụ-n
- Rối loạn thị giảc
thoảng qua.
- Rối loạn tầm
nhỉn.
- Viêm dây thần
kinh thị giảc.
- Mất thị lực tạm
thời,
hồi phục sau khi
ngừng điếu trị.
Rối ioạn trên tai - Độc tinh - Điếc
vả mê đạo trên tai
Rối loạn trên hệ - Khó thớ - Nấc — Bệnh viêm phổi
hô hẳp, iổng ngực - Ho - Thuyên tắc kẽ, một số
vả trung thẩt — Chảy mảu cam mạch phổi trường hợp dẫn
đến tử vong.
- Xơ hóa phốỉ* *
Rối ioạn đường - Buồn nôn - Ăn không tiêu - Viêm đại trảng
tiêu hóa* - Tiêu chảy - Trảo ngược dạ - Tắc ruột bao gồm tiếu
- Nôn dảy, thực quản chảy do
- Viêm dạ dảy/Viêm - Xuất huyết tiêu Clostridium
niêm mạc hóa difficiie
- Đau bụng - Chảy máu trực - Viêm tụy
- Táo bón trảng
Rối loạn trên hệ - Tiểu ra mảu
tiết niệu - Tìếu khó K-ẦV
— Tần số tỉểu tiện/
bẩt thường
Các rối ioạn trên - Rối loạn trên da - Bong da (như
da vả mô dưới da - Rụng tóc Hội chửng tay vả
chân)
- Ban đò
- Phảt ban
… Ra nhiêu mồ hôi
- Loạn dưỡng
móng
Rối loạn cơ - Đau lưng - Đau cơ
xưong và mô iiên - Đau xương
kết
Rối loạn chuyền - Chém ăn - Mất nước - Acid
hóa và dinh - Tăng đường huyết chuyền hóa
dưỡng - Hạ kali mảu
- Tăng natri máu
Nhiễm trùng và - Nhiễm trùng - Viêm mũi
nhiễm ký sinh
trùng*
… Nhìễm khuằn
đường hô hấp trên
- Nhiễm trùng
huyết giảm bạch
cẩu trung tính
Rôi ioạn hệ mạch
- Xuất huyết
- Đỏ bừng mặt
- Huyết khối tĩnh
mạch sâu
- Tăng huyết áp
Cảo rôi loạn toản
thân và tại vị trí
đưa thuôc
— Mệt mỏi
… SổtH
- Suy nhược
- Đau
- Phản ửng tại vị trí
. h 4—1+
tiem
Rôi loạn hệ mỉên
dịch*
- Dị ửng/phản ứng
dị ứng'(
Rối ioạn tâm thần
- Trầm cảm
- Mất ngủ
* Xem chi tiết ở phần sau.
'f.’
** Xem mục “Thận trọng khi dùng thuốc”
* Dị ửng/phản ứng dị ứng rất phổ bỉến, chủ yếu xuất hiện trong quá trình truyền tĩnh mạch, một
vải trường hợp dẫn đến tử vong. Cảo phản ứng dị ửng phổ biến bao gồm ban đỏ trên đa, đặc biệt
là nổi mề đay, vỉẽm kết mạc và vỉêm mũi.
Phản ứng phản vệ thường gặp bao gồm co thắt phế quản, phù mạch, hạ huyết áp, cảm giảc đau
ngực vả sôc phản vệ.
1“LRẳtphổ biến gổrn sốt, run, hoặc do nhiễm trùng (có kèm theo hoặc không kèm theo giảm bạch
cầu trung tinh có sôt) hoặc có thế do cơ chế miễn dịch.
"*Phản ứng tại vị trí tiêm bao gổm đau tại chỗ tỉẻm, đò, sưng và huyết khối đã được báo cáo. Sự
thoảt mạch cũng có thể là kết quả đau vả viêm tại chỗ tiêm bao gồm cả hoại tữ, đặc bỉệt khi
oxaliplatin được truyền qua tĩnh mạch ngoại vi (xem mục “Thận trọng khi dùng thuốc”).
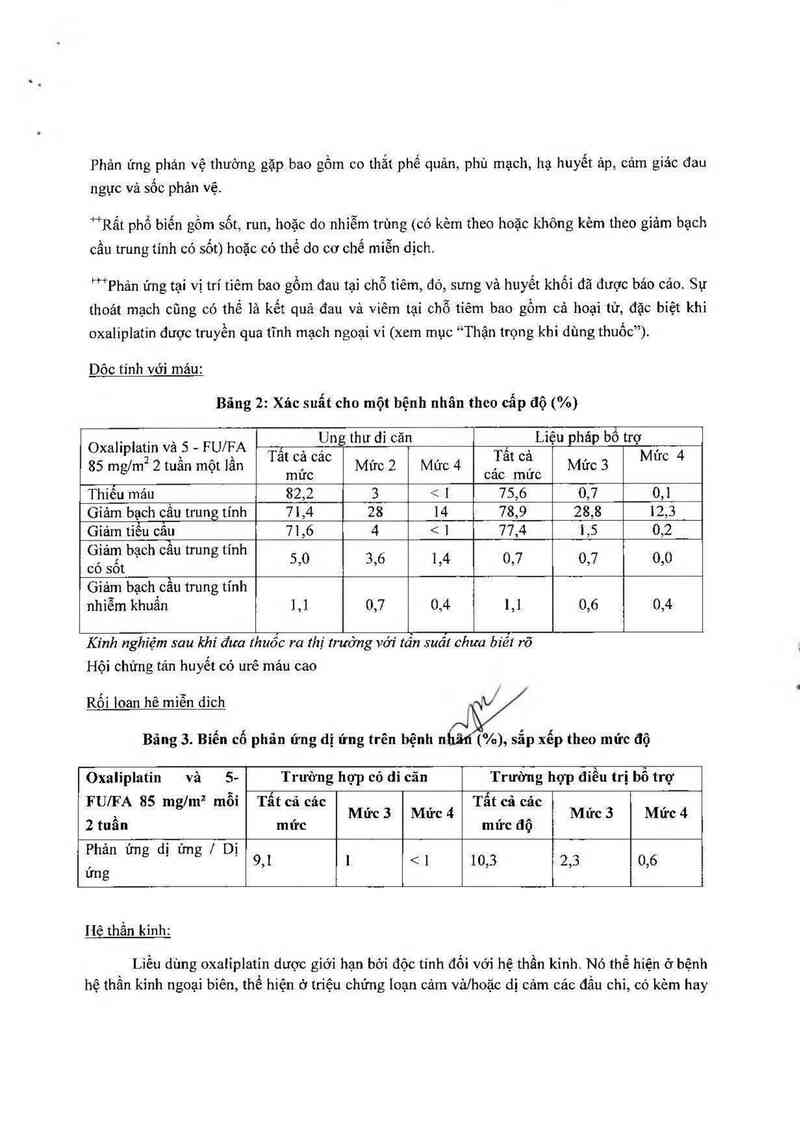
Dôc tỉnh với mảu:
Bãng 2: Xác suất cho một hệnh nhân theo cẩp độ (%)
Oxalipiatin và 5 _ FU/FA TẮt , IIJn thư di can T“ \ Lieu phap bo trợM ' 4
85 mg7m² 2 tuần một lằn a °Ề’ cac Mức 2 Mức 4 . m ²8 Mức 3 “°
mưc C'dC mưc
Thiểu máu 82,2 3 < 1 75,6 0,7 0,1
Giảm bạch cẩu trung tinh 71,4 28 14 78,9 28,8 12,3
Giảm tiếu cân 71,6 4 < 1 77,4 1,5 0,2
(J'tam bạch cau trung t1nh 5ỉ0 3,6 1,4 057 037 030
co sot
Giảm bạch cầu trung tính
nhiễm khuẳn 1,1 0,7 0,4 1,1 0,6 0,4
Kinh nghiệm sau khi đưa thuốc ra thị rrường với tần suất chưa biết rõ
Hội chửng tán huyết có urê máu cao
: . e .; . /
R01 loan he mien dich \z
Bãng 3. Biến cố phân ửng dị ứng trên bệnh ní1ẵđí (%), sẳp xếp theo mức độ
Oxalipiatin và 5- Trường hợp có di căn Trường hợp điều trị bổ trợ
FU/FA 85 mglm² mỗi Tẩt cả các Tẩt cả eác
, , Mức 3 Mức 4 _ Mức 3 Mức 4
2 tưan mưc mửc đọ
Phản ứng dị ứng 7 Dị
, 9,1 1 < 1 10,3 2,3 0,6
ưng
Hệ thần kinh:
Liều dùng oxaliplatin dược gỉớì hạn bởi độc tinh đối với hệ thần kỉnh. Nó thế hiện ở bệnh
hệ thần kinh ngoại biên, thế hiện ở triệu chứng ioạn cảm vả/hoặc dị cảm cảc đẩu chỉ, có kèm hay
không kèm chuột rút, thường khớí phát khi gặp lạnh. Cảo triệu chứng nảy xuất hiện không quá
25% bệnh nhân điều trị. Thời gian xảy ra các triệu chứng nảy thường giám dân trong thời gian
giữa hai lần tiêm thuốc, và tăng lền theo số chu kỳ đỉêu trị.
Sự xuất hiện đau vả/hoặc rối loạn chức năng iả nguyên nhân đòi hỏi phải hiệu chỉnh iiều
dùng, thặm chí là ngừng thuốc, tuỳ thuộc vảo mức độ kéo dải các triệu chứng nảy (xem “Thận
trọng dùng khi dùng thuốc“).
Sự rối loạn chức năng bao gỗm khó khăn khi thực hiện cảc thao tảc tinh vỉ, và có thế lả
do rối loạn cảm gỉảc gây ra. Nguy cơ xuất hiện cảc triệu chứng vĩnh viễn do tích luỹ thuốc khi
dùng liều 850 mg7m² (10 chu kỳ) 1ả vâo khoảng 10%, còn khi dùng liều 1020 mg7m² (12 chu kỳ)
thì nguy cơ lả vảo khoảng 20%.
Trong đa số trường hợp, cảc dấu hiệu và triệu chứng thẩn kinh sẽ được cải thiện hoặc
hoản toản bỉnh phục sau khi ngừng điều trị. Trong trường hợp dùng biện pháp bổ trợ cho ung thư
đại trảng, sau khi ngừng điều trị được 6 thảng, 87% số bệnh nhân không còn triệu chứng gì hay
chi có triệu chứng rất nhẹ. Sau 3 năm theo dõi sau khi ngừng đỉều trị, có khoảng 3% số bệnh
nhân có hiện tượng dị cảm khu trú dai dẳng mức độ vừa phải (2,3%) hay dị cảm có gây rối ioạn
các hoạt động chức năng (0,5%).
f,“
Đã có những bảo cảo vè cảc biểu hiện cấp tính thần cảm giảc (xem “Dữ liệu an toản
tiền lâm sảng“). Các biếu hiện nảy xuất hiện trong vòng vải gỉờ sau khi tiêm thuốc, và hay gặp
khi bệnh nhân bị lạnh. Chúng có thể là cảc triệu chứng dị cảm, loạn cảm, giảm cảm gỉác thoảng
qua. Hội chúng cẳp tính cùa loạn cảm hẳn thanh quản nảy có tỷ lệ vảo khoảng 1% đến 2% được
đặc trưng ở cảm giác chủ quan thấy khó nuốt hay khó thở/cảm giác nghẹt thở mã không có một
bằng chứng cụ thể nảo về suy hô hẳp (không có hiện tượng xanh tím hay thiếu oxy) hay về co
thẳt thanh quản hay co thắt phế quản (không có tiếng thở rít hay thở khờ khê). Cũng đã quan sát
thấy co cứng hảm, cảm giác lạ ở lưỡi, loạn vận n gôn, vả cảm gìảc tức ngực. Mặc dù trong những
trường hợp nảy cảc thuốc khảng histamin và thuốc iảm gỉãn phế quản thường được dùng, nhưng
cảc triệu chứng nảy thường hồi phục nhanh ngay khi không điều trị gi. Việc kéo dải thời gian
tiêm truyền (tỉêm chậm lại) giúp iảm giảm hội chứng nảy (xem “Thận trọng khi dùng thuốc“).
Đôi khi quan sảt thấy cảc triệu chứng khảo như co cơ hảm/ chuột rủt/ co giật cơ | rung gìật cờ,
phối hợp bắt thường 7 dáng đi bất thường 7 mắt điếu hòa 7 rối loạn sự cân bằng, đau cổ họng hoặc
tức ngực 7 ảp lực 7 khó chịu 7 đau. Ngoài ta, rối loạn chức năng dây thần kỉnh sọ não có thể liên
quan đến cảc biến cố nêu trên, hoặc cũng xảy ra như một biến cố đon iè như sa mi mắt, nhìn đôi,
mắt tiếng 7 khản giọng, đôi khi được mô tả như tê liệt dây âm, cảm gỉác lưỡi bất thường hoặc
loạn vận ngôn, đôi khi được mô tả như mất ngôn ngữ , đau mặt! dây thần kinh sinh ba lđau mắt,
giảm thị 1ực, rối loạn tầm nhìn.
Các triệu chứng về thần kinh khảo như loạn vặn ngôn, mắt phản xạ gân xưong vả dắu
hiệu Lhermỉte đã được bảo cảo trong thời gỉan điều trị với oxaliplatin. Cũng có ca lẻ tẻ về vỉêm
thần kỉnh thị giác được báo cáo.
Kinh nghiệm sau khi đưa thuốc ra thị trường với lần suất chưa rõ
Co giật
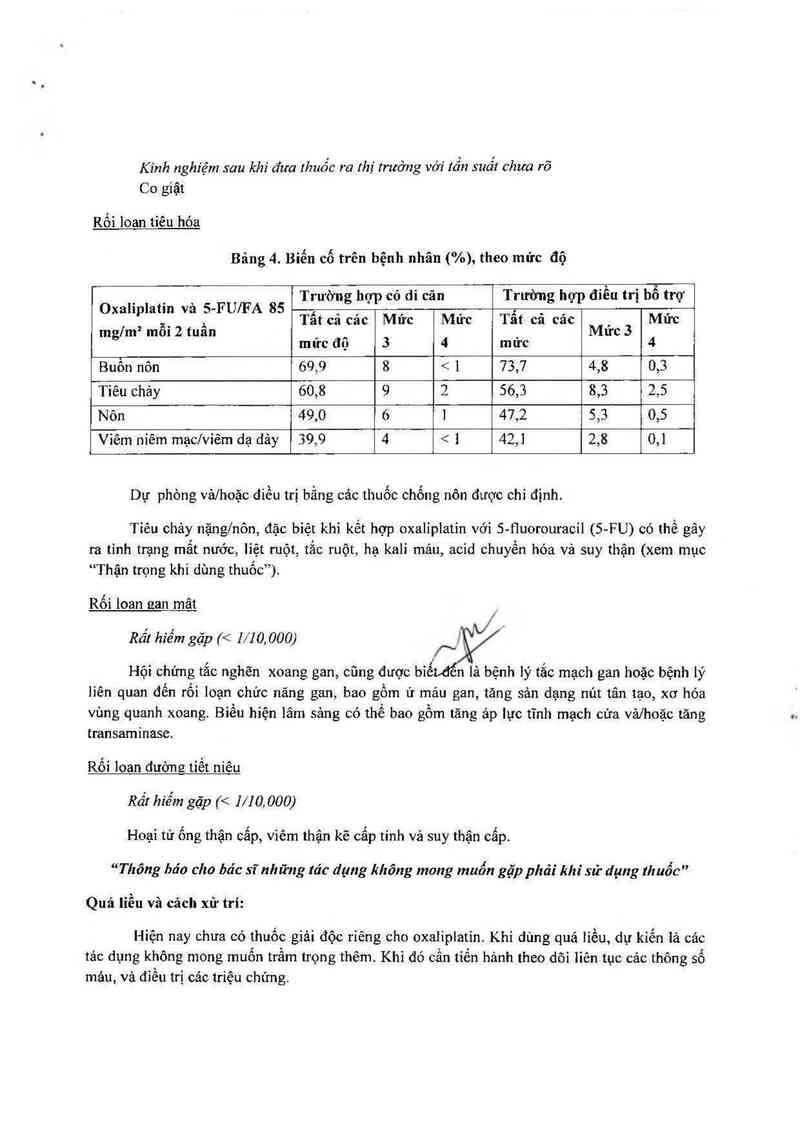
Rối loan tiêu hóa
Bảng 4. Bỉến cố trên bệnh nhân (%), theo mức độ
Trường hợp có di căn Trường hợp điều trị bổ trợ
Oxalipiatin vã 5-FUÍF A 85 ,, , , , , _, _ _ ,
- , Tat ca cac Mưc Mưc Tat ca cac , Mưc
mglm² môi 2 tuân , _ _ Mưc 3
mưc đọ 3 4 mưc 4
Buồn nôn 69,9 8 < 1 73,7 4,8 0,3
Tiêu chảy 60,8 9 2 56,3 8,3 2,5
Nôm 49,0 6 1 47,2 5,3 0,5
Viêm niêm mạc/viêm dạ dảy 39,9 4 < 1 42,1 2,8 0,1
Dự phòng vả/hoặc điều trị bằng các thuốc chống nôn được chi định.
Tiêu chảy nặng/nôn, đặc biệt khi kết hợp oxaliplatin với 5—fiuorouracíl (5-FU) có thể gây
ra tỉnh trạng mất nước, liệt ruột, tắc ruột, hạ kali mảu, acid chuyển hóa vả suy thận (xem mục
“Thận trọng khi dùng thuốc”).
Rôi loan ean mât
Rất hiếm gặp (< 1710, 000) Fi
Hội chứng tắc nghẽn xoang gan, cũng được bỉễbđễn là bệnh lý tắc mạch gan hoặc bệnh iý
]iẽn quan đến rối loạn chức nãng gan, bao gồm ứ mảu gan, tăng sản dạng nút tân tạo, xơ hóa
vùng quanh xoang. Biểu hiện lâm sảng có thế bao gồm tăng áp lực tĩnh mạch cừa vảlhoặc tăng
transaminase.
Rối loan đường tiết niên
Rất hiểm gặp (< 1710, 000)
Hoại từ ống thận cắp, vìêm thận kẽ cẳp tỉnh vả suy thận cẩp.
“T hông băo cho bác sĩ những tác dạng không mong muốn gặp phâi khi sử dụng thuốc”
Quá Iiếu vả cảch xử tri:
Hiện nay chưa có thuốc giải độc riêng cho oxaiipiatin. Khi dùng quá liều, dự kiến là cảc
tảo dụng không mong muốn trầm trọn g thêm. Khi đó cần tiến hảnh theo dõi iiên tục cảc thông số
mảu, vả đỉêu trị cảc triệu chứng.
Đặc tính dược lực học:
Mã ATC: LOl XAO3 Chắt kim tế bảo (L: chất chống ung thư và điều biến miễn dịch - các
hợp chất platin).
Oxalipiatin là một thuốc chống ung thư, thuộc một họ hợp chất mới cùa platin, trong đó
platin được tạo phức với 1 - 2 diaminocyclohexan (“DACH“) và với nhóm oxalat.
Oxalipiatin iả chất đổng phân đối hình đơn, (SP-4-2)-[(1R,2R)-Cyciohexane-l,2-
diamine—kN, kN’] [ethanedioato(Z-)-kOI , k02] piatinum.
Oxaliplatin có phổ tác dụng rộng về hai mặt: độc tính với tế bảo in vitro, vả hoạt tính
chống khối u in vivo. Trong nhiếu mô hình ung thư khác nhau, trong đó có mô hinh ung thư đại -
trực trảng ở người.
Oxalipiatin cũng thế hiện có hoạt tính in vỉtro trên nhiều mô hình ung thư kháng một số
hợp chất cisplatin khảc nhau.
Đã nhận xét thấy có tảc dụng hiệp đồng khi kết hợp với 5 - tiuorouracil in vitro cũng như
in vivo về độc tính với tế bảo.
Tuy những công trình nghiên cứu về cơ chế tác dụng cùa oxaliplatin chưa đi đển kết luận
hoản toân rõ rảng, nhưng cũng đã cho thấy là những dẫn chứng tạo thảnh qua quá trinh chuyển
dạng sinh học của oxaliplatỉn sẽ tường tương tác với DNA dế tạo ra những liên kểt bắt chéo giữa
hai chuỗi hoặc trong nội bộ một chuỗi, do đó ngăn cản việc tổng hơp DNA, từ đó trở thảnh độc
vởi tế bảo, và có tảc dụng chống ung thư.
Ở những bệnh nhân ung thư đại - trực trảng di căn, 1ệu quả cùa oxaliplatin (với iiều 85
mglm2 hai tuần một lần) kết hợp với 5 - t]uorouracillfolinic acid (5 - FUIFA) đã được ghi nhận
trong ba công trình nghỉên cứu trên lâm sảng.
- Công trinh nghiên cứu với những bệnh nhân lẩn đầu tiên được điều trị trước đó, và
kháng với kết hợp thuốc irinotecan (CPT - 11) + 5 - FU/FA
- Công trình thuộc giai đoạn 111 (Rothenbery, ML và cộng sự, 2003) gồm 82] bệnh nhân,
được phân ngẫu nhiên thảnh 3 nhỏm: một nhóm chỉ dùng riêng 5 - FU/FA (nhóm LV5 FU2. N =
275), nhóm thứ 2 dùng riêng oxalipiatin (N = 275) và nhóm thứ 3 dùng oxaliplatin với 5 -
FU/FA (Nhóm FOLFOX 4 - N = 271).
Cuối cùng là một công trinh không có đối chứng thuộc giai đoạn 11 (Andre“,T. và cộng
sự, 1999), thu nhận những bệnh nhân dã kháng riêng 5 - FU/FA và họ được dùng 5 - FU/FA kết
hợp với oxaiiplatin (nhóm FOLLFOX 4 - N = 57).
Hai công trình có dối chứng: Công trình với bệnh nhân lần đầu được diều trị ung thư (dc
Gramont. A và cộng sự) và công trinh đã có điếu trị trước đó (Rothenberg ML, và cộng sự), đã
ivr…ư
cho thấy là có tỷ lệ đảp ứng cao, tỷ lệ giữa thời gian sổng sót mả bệnh không tiền triến (PFS)
chia cho thời gian bệnh có tiền triển là lớn hơn khi so sảnh với tỷ lệ đó ở những bệnh nhân chi
đỉều trị bằng 5 - FU/FA. Trong công trình của Rothenberg vả cộng sự trên những bệnh nhân đã
có điều trị và khảng thuốc, thì sự sai khảo về thời gian sổng sót t…ng bình (OS) của nhỏm dùng
kết hợp oxaiipiantin + 5 - FU/FA so với nhóm chỉ dùng 5 - FUIFA chưa có ý nghĩa thống kê.
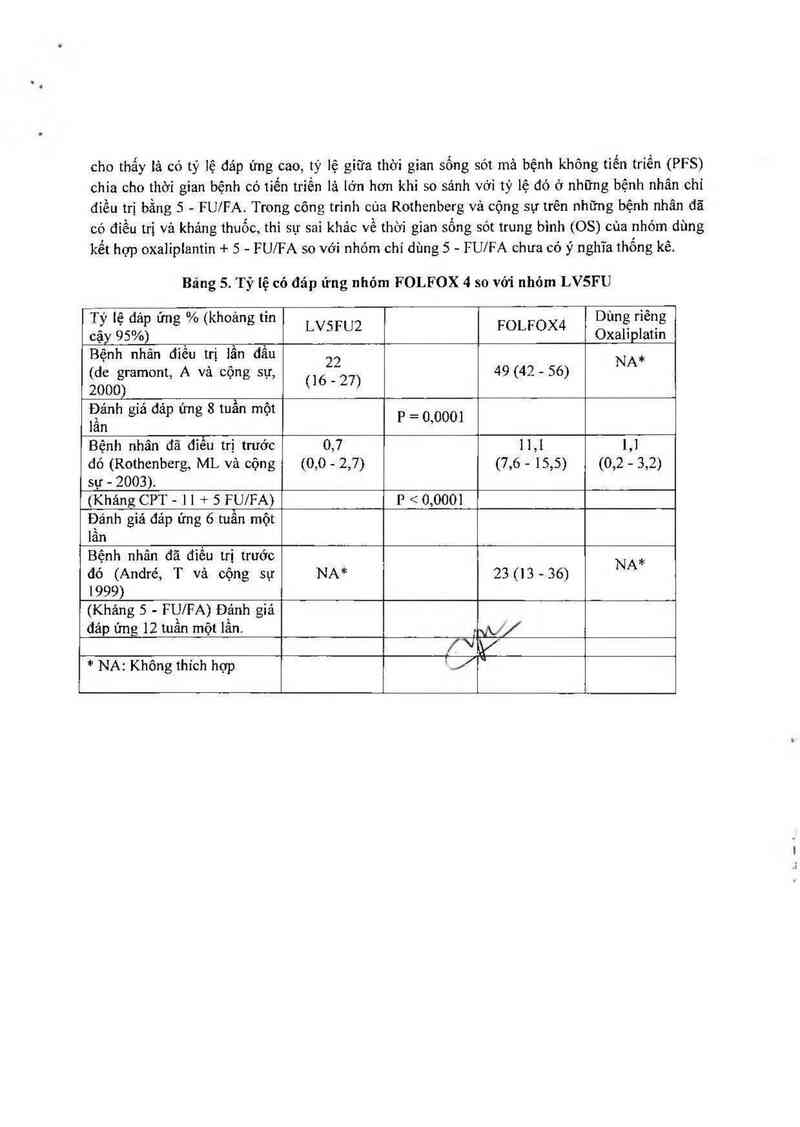
Bảng 5. Tỷ lệ có đáp ứng nhỏm FOLFOX 4 so với nhóm LVSFU
ỉTỷ 1ệ đảp ứng % (khoảng tin
cậy 95%)
LVSFU2
FOLFOX4
Dùng riêng
Oxalipiatin
Bệnh nhân điều trị iần đầu
(de gramont, A và cộng sự,
2000)
22
(]6-27)
49 (42 … 56)
NA*
Đánh giá đáp ửng 8 tuần một
iân
P = 0,000]
Bệnh nhân đã tĩễu trị trước
đó (Rothenberg, ML và cộng
sự - 2003).
0,7
(0,0 - 2,7)
11,1
(7,6 - 15,5)
1,1
(0,2 - 3,2)
(Khảng CPT - 11 + 5 FU/FA)
P < 0,000]
Đảnh giả đảp ứng 6 tuần một
lần
Bệnh nhân đã điếu trị trước
đó (André, T và cộng sự
1999)
NA*
23 (13-36)
NA*
(Kháng 5 - FỤ/FA) Đậnh giả
đáp ứng 12 tuân một lân.
/
* NA: Không thich hợp
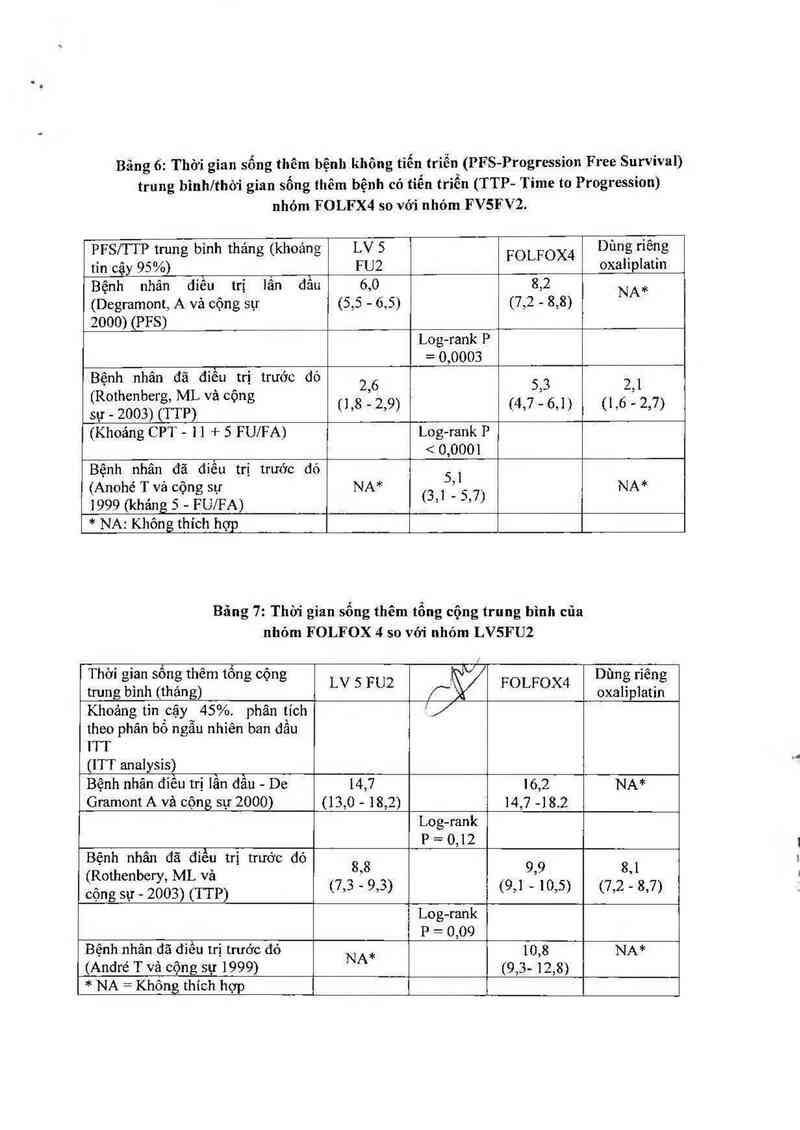
Bảng 6: Thời gian sống thêm bệnh không tiến triễn (PFS—Progression Free Survival)
trung bình/thòi gian sống thêm bệnh có tiến trìển (TTP- Time to Progression)
nhóm FOLFX4 so với nhóm FVSFV2.
PFS/TTP trung bình thảng (khoảng LV 5 FOLFOX4 Dùng riêng
tỉn cậy 95%) FU2 oxahplatm
Bệnh nhân điếu trị lẩn đẳu 6,0 8,2 NA*
(Degramont, A vả cộng sự (5,5 - 6,5) (7,2 - 8,8)
2000) (PFS)
Log-rank P
= 0,0003
sự _ 2003) (TTP) (1,8 - 2,9) (4,7 - 6,1) (1 ,6 - 2,7)
(Khoảng CPT - 11 + 5 FU/FA) Log-rank P
< 0,000]
Bệnh nhân đã điều trị trước đó 5 1
(Anohé T vả cộng sự NA* (3 1 i 5 7) NA*
1999 (khảng 5 - FU/FA) ’ ’
* NA: Khôn g thích họp
Bảng 7: Thời gian sổng thêm tổng cộng trung bình cũa
nhóm FOLFOX 4 so với nhỏm LVSFUZ
Thời gian sống thêm tổng cộng
Dùng riêng
trung bình (thảng) LV 5 FU2 /` FOLFOX4 oxaliplatin
Khoảng tin cậy 45%. phân tich ’/
theo phân bố ngẫu nhỉền ban đầu
ITT
(ITT analysis)
Bệnh nhân đỉếu trị lần đầu - De 14,7 16,2 NA*
Gramont A vả cộng sự 2000) (13,0 - 18,2) 14,7 —18.2
Log—rank
x P = 0,12
Bênh nhân đã đieu tri trưởc đó
' , ' 8 8 9 9 8 1
(Rothenbery, ML va ’ ’ ’
cộng sự _ 2003) (TTP) (7,3 - 9,3) (9,1 - 10,5) (7,2 - 8,7)
Log—rank
P = 0,09
Bệnh nhân đã điều trị trưởc đó NA, 10,8 NA*
(André T và cộng sự 1999) (9,3- 12,8)
* NA = Không thích hợp
Ở những bệnh nhân trước dó đã được đìều trị (Rothenberg, ML và cộng sự, 2003) mà khi
vảo nghìên cứu, triệu chứng lúc đầu có thể hiện bên ngoảì, thì số được cải thỉện. Cảc triệu chứng
1iên quan đến bệnh đó ở những trường hợp dùng oxaliplatín kết hợp vởi s - FUJFA là nhiều hơn
rõ rệt so với những trường hợp chỉ đùng riêng 5 - FUIFA (27,7% so với 14,6% p = 0,0033).
Ở những bệnh nhân trước đó chưa được đỉều trị (de Gramont. A và cộng sự, 200) không
có sự khảo nhau có ý nghĩa thống kê về cảc mặt cùa chất 1ượng cuộc sống gỉữa hai nhóm điều trị.
Tuy nhiên điểm số về tỉnh hỉnh sức khoẻ nói chung, và về đau đởn trong chất lượng cuộc sống,
thì nhóm đối chứng có tốt hon chút ít, và nếu xét mặt phản ứng buồn nôn vả nôn, thì nhóm dùn g
oxaliplatin lả xấu hơn.
Ở những bệnh nhân dùng ìiệu phảp bổ trợ, công trình nghiên cứu so sảnh thuộc giai đoạn
111 MOSAIC, đã phân phối ngẫu nhỉên 2246 bệnh nhân (vảo công trình Duke B2/bệnh mức 11)
899 bệnh nhân và (vảocông trình Duke C/bệnh mức 1 1347 bệnh nhân; Tất cả bệnh nhân sẽ được
cẳt bò hoản toản khối ung thư tỉên phảt ở đại trảng, và được dùng riêng 5 … FUIFA (LVSFU2 - N
= 1123, trong đó BZ/C = 448/675) hoặc được dùng kểt hợp oxaliplatin vả 5 - FO/FA (FOLFOX4,
N = 1 123 trong đó B2/C = 451/672).
Bảng 8. Nghiên cứu MOSAIC — Tỷ lệ bệnh nhân sống trên 3 năm mà bệnh không
tiểu tríễn (phân tích ITT (phân tích theo phân bổ ngẫu nhiên ban đầu) trên tổng số bệnh
nhân)
Nhộm đíều trì LVSFU2 , FOLEOX4
Tỷ lệ bệnh nhận sông trên 3 năm mà bệnh 73,3 " 78,7
không tiên triền (khoảng tin cậy 95%). (70,6 ~ 75,9) /`11 (76,2 - 81,1)
Nguy cơ tương đối (khoảng tin cậy 95%) + (16417Ễ 89)
P = o,ooos
* Thời gian theo dõi trung bình 44,2 tháng (tất cả cảc bệnh nhân được theo dõi ít nhẳt 3 năm).
Nghiên cứu trên cho thấy lợi ích đảng kể về khả năng sống thêm không có bệnh tìến triển
trong 3 năm do liệu pháp oxaliplatin kết hợp vởỉ 5 FU/FA mang lại (nhóm FOLFOX 4) khi so
sảnh với lỉệu pháp dùng rỉêng 5 - FU/FA (nhóm LVS FU2).
Bảng 9. Nghiên cứu MOSAIC. Tỷ lệ bệnh nhãn sổng trên 3 năm
mà hệnh không tiến tríễn (phân tích lTT)* trên số bệnh nhân
theo từng mức độ bệnh
, . . Bênh mức 11 Bênh mức 111
Mưc đọ hẹnh (Duke`s 132) (Duke“s C)
Nhóm điêu lrị LV 5 FU2 FOLFOX4 LVSFU2 FOLFOX4
Tỷ lệ bệnh nhân sống
trên 3 năm mà bệnh 84’3 87’4 65’8 72’8
không tìển
triến (khoảng tin cậy (80,9 — 87,7) (84,3 — 90,5) (62,2 - 69,5) (69,4 - 76,2)
95%).
Nguy cơ tương đối + 0,79 0,75
(khoảng tỉn cậy 95%) (0,57 - 1,09) 0,62 - 0,90
P=0,151 P=0,002
* Thời gìan theo dõi trung bình 44,2 tháng (tắt cả các bệnh nhân theo dõi 3 năm trở lên).
+ Nguy cơ tương đối: Xem chú thích ở bảng 8.
Thời gỉan sống thêm tồng cộng - Phân tích ITT ( phân tích theo phân bổ ngẫu nhiên ban
đẩu).
Ở thời điếm phân tích chỉ tìêu: sống thêm 3 năm mả không có bệnh tiến triển, và đó lả chí
tìêu đầu tỉên của công trình nghiên cứu MOSAIC, thì ở nhóm FOLFOX vẫn còn 85,1% bệnh
nhân sống sót trong khi ở nhóm LV SFU2 còn 83,8%. Điểu đó có nghĩa 1ả nguy cơ tử vong giảm
đi được 10% ở nhóm FOLFOX4, nhưng chưa có ý nghĩa thống kê (nguy cơ tương dối = 0,90).
Nếu phân theo từng phân nhỏm theo mức độ bệnh, thì phân nhóm bệnh nhân giai đoạn II
(Duke`s B2), thì tỷ lệ trên sẽ lả 92,2% so với 92,4% (nguy cơ tương đối là 1,01) và phân nhóm
bệnh nhân ở gìaì đoạn 111 (Dukesc C) thì tỷ lệ sẽ là 80,4% so với 78,1% (nguy cơ tương đối lả
0,87) (con số trước là phân nhóm dùng FOLFOX4, con số sau ứng vởi nhóm dùng LV4SFUZ).
Đặc tinh dược động học:
Dược động học của từng chất có hoạt tính cụ thể chưad'ược nghiên cứu rõ. Dược động
học của platin trong huyết tưong lọc qua siêu lọc, là của một hỗn hợp nhiều hợp chất cùa platín
có hoạt tính hay không có hoạt tính, thực hiện tíêm truyền trong 2 gĩờ 130 mg/m2 oxaliplatin 3
tuần tiêm truyền một 1ần, tiêm tất cả 5 chu kỳ, hoặc theo chế độ tíêm 85mg7m² oxalíplatin cử hai
tuần một lẳn, tiêm tắt cả 3 chu kỳ - Thởi gỉan tỉêm truyền là 2 gìờ ở cả hai chế độ. Kết quả như
sau.
Bảng 10. Tóm tắt cảc thông số dược động học cũa platin qua sỉêu lọc sau nhiều lần dùng
oxaliplatỉn fỉSmg/m2 hai tuần một lần hay 130 mgím2 ba tuần một lần.
Liều Cmax AUC0 - 48 AUC tllla t1720 t1rzy Vss CL
ụg/ml ụg.hlml ụg.hfml h h h L th
85 mglm2
Trung bình 0,814 4,19 4,68 0,43 16,8 391 440 17,4
Đọ ẵẹCh 0,193 0,647 1,40 0,35 5,74 406 199 6,35
chuan
130 mglm2
Trung bình 1,21 8,20 11,9 0,28 16,3 273 582 10,1
Đọ 'Ể°h 0,10 2,40 4,60 0,05 2,90 19,0 261 3,07
chuan
Các số liệu về trưng bình A1JCg.qg_ và c.… được xảo định 0 chu kỳ 5 (85mgim²) hay ở
chu kỳ 5 (130mg7m²).
Cảo số ]ỉệu AUC, v,,, CL vả CLR028 được xảc định ở chu kỳ 1.
Cảc số liệu Cmax, AUC, AUCo-48, Vss vả CL được xảo định theo phương pháp phân tích
không phân ngãn.
Cảc số liệu t…… tm, hn, được xảo định thoc phương phảp phân tích có phân ngãn (kết
hợp cảc chu kỳ 1-3).
Sau khi kết thúc việc tiêm truyền trong 2 giờ, 15% platin tiêm vảo nằm trong máu, 85%
còn lại được phân bố nhanh vảo cảc các mê hoặc được đảo thải qua nước tiều. Do việc liên kết
giữa platỉn với hồng cẩu vả với huyết tương là bất thuận nghịch, nên thời gian bản hùy của cảc
chất ban đầu liên hệ chặt chẽ vởi vòng đời tự nhiên của các albumin huyết tương và của hồng
cầu. Không thấy có hỉện tượng tích luỹ ở nước huyết tưong siêu 1ọc sau mỗi lần tiêm 85mg/m2
hai tuần lễ một lần, hay 13Otng/m2 ba tuần lễ một lần và trạng thái ốn định được thiểt lập ngay ở
chu kỳ 1 ở cảc chất nền đó. Sự thay đối bên trong vả bên ngoảỉ tế bảo nhìn chung là chậm
Nghiên cứu sự biến đối sinh học in vítro, cho thẳy có sự thoải biến cùa thuốc không thông qua
enzym, và không có bằng chứng là sự chuyển hoá của vòng diamino cyclohexan (DACH) có
thông qua cytochrom P450.
Ở bệnh nhân, oxaliplatinđược chuyển hóa đảng kể, vả không phảt hiện được thuốc còn
nguyên vẹn trong dịch huyết tương siêu lọc sau 2 giờ tiêm truyền. Đã xảo định được một số chất
chuyến hỏa gây độc vởi tế bảo, trong đó bao gồm monocloro, đicloro và các dạng chẳt dìaquo -
DACH của platỉn vả ở thời điếm cuối lả cảc chất chuyển hóa không hoạt động đã được phân lập
trong tuần hoản ở trong mảu cùng với nhỉều chất 1iên hợp không có hoạt tính ở những thời điểm
muôn hơn.
, . ^,
Platin chủ yêu được đảo thải qua nước tiêu, thanh thải lởn trong vòng 48 giờ sau khi
tiêm.
Đến ngảy thứ 5, khoảng 54% liều tiêm vảo được tìm thấy trong nước tiếu và dưới 3%
thấy ở phân.
Có sự giảm đảng kể về độ thanh thải khi suy thân, từ 17,6:t2,18 L/giờ xuống còn
9,952,91 L/giờ, kèm theo sự giảm một cảch có ý nghĩa thống kê về thể tích phân bố, từ 330i40,9
xuống còn 241i6,1L. ảnh hưởng có tinh trạng suy thận nặng lên sự thanh thải platin còn chưa
dược nghiên cứu.
Hướng dẫn sử dụng và xử lý
Cần đặc biệt thận trọng khi pha chế và xử lý dung dịch oxalìplatin được khuyến cảo cho
tất cả các thuốc gây độc tế bảo. Oxaiiplatìn phải được hoản nguyên vả pha loãng trước khi sử
dụng. Việc pha chế thuốc phải được thực hiện bởi người có chuyên môn đã được đảo tạo, dưới
cảc điều kiện đảm bảo việc bảo vệ môi trường vả người xử lý thuốc.
Chỉ nên sử dụng nước cất pha tiêm hoặc dung dịch glucose 5% để pha chế dung dịch:
-Oxaliplatin 50 mg: thêm 10 ml đến 20 ml dung môi vảo bột thuốc đông khô để được
nồng độ cuối cùng tương ủng từ 5 mglml đến 2,5 mg/ml oxaliplatin;
-Oxaliplatin 100 mg: thêm 20 ml đển 40 ml dung môi vảo bột thuốc đông khó dễ được
nồng độ cuối cùng tương ứng từ 5 mglml đển 2,5 mg/ml oxalỉplatin.
Dung dịch nảy cần tiếp tục dược pha loãng với 250 ml hoặc 500 ml dung dịch glucose 5%
để thu được dịch truyền. Dung dịch sau khi pha chế nên sử dụng ngay.
Cảc khuvến cáo đãc biêt
Không nên sử dụng bất cứ dung dịch pha chế nảo có xuất hiện kểt tủa và nên hùy bỏ thuốc
theo cảc quy trình hướng dẫn xử lý cảc chất thải gây độc tế bảo
Trong trường hợp dung dịch oxaliplatin đậm đặc hoặc dung dịch sau khi đã được pha
loãng để truyền tiếp xúc vởi da hoặc niêm mạc, cảc vùng tiếp xúc cẳn phải được rừa và lâm sạch
ngay lập tức dưới dòng nước.
Không được kết hợp oxaliplatin vởi cảc thuốc hoặc dung dịch có tinh kiềm hoặc với cảc
clorid, bao gồm natri clorìd ở bất cứ nồng độ nảo.
Không trộn lẫn oxaliplatỉn với bất cứ thuốc nâo.
Oxaliplatin có thể bị phân hủy nếu tiếp xúc với nhôm.
Đọc kỹ hướng dẫn sử dụng trước khi dùng.
Nếu cần thêm thông tin xin hỏi ý kiến bác sỹ.
Thuốc nây chi dùng theo đơn của bác sỹ.
Để xa tầm tay trẻ em. n,/
Trình bây và đóng gói: hộp 1 lọ 50mg/1 Oml ; hộp ] IọCTỈẬríg/ZO ml.
Bảo quản: Không bảo quản trên 30°C.
Tiêu chuẩn chẩt lượng: Tíêu chuẩn nhà sản xuất
Hạn dùng: 24 thảng kế từ ngảy sản xuất.
Tên cơ sở sản xuất và đóng gói sơ cấp:
Oncotec Pharma Produktion GmbH
Am Pharmapark, 0686] Dessau-Rossiau, Đức.
Tên cơ sở đỏng gói thứ cẩp và xuất xưởng:
Ebewe Pharma GmbH Nfg KG
Mondseestrasse 11, 4866 Unterach am Attersee, Áo.
TUQ. CỤC TR UỐNG
P.TRUỜNG PHÒNG
.Ảỷụfyẫn nĨfíịlkz/ ẨÍfíìnỵ
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng