


















.4
cục QUẢN LÝ nược CARTON
ỉJẶ_PẸE-DUỸÊ_T ' = - =
ị , I ___ẵèot3 - ceạeu tablet ntains 5. 58 mg saxagliptin nyơroomortơa (anhyttous) equivalent to 5 mg saxagliptin.
` h . op out ot rcach of chltdren.
[
___'___L - ẺỘYTỂ PRODUCT: ONGLYZA5mg 4Ỹ/q_ 884
See accompanying insert tcr inclinations and dosing intormation
@ 2013 BristoI-Myers Squibb and AstraZeneca ~~~~~~
weewea
Onegza ts a tradetmrk ot Btistol—Myets Squibb Company.
1 ~ _ _
T | _
“Ẹ ễ. Ẹ— ị Mõl viên nẻn bao phim thửa 5,58 mg saxagliptin hydrochloride (dạng khan) tương ủng vút 5 mg saxagltptin.
ẵ Ễ ẳ'ẫ Wẽn nén bao phim. Hộp 2 le 14 vtèn.
ị Ễ Ễ (hỉđịnh, ca'chdùng, chõng thi dịnh vảcát thông tin khác:nhdọctờHưfflgDănSửũụng Thuõt. ' '
zị ; Báoquántnhiệtđộdưiiiưt Ề
tuuõc BAN tqu oơu.ot xa TÃM … mt m.
ị oọc nnuơne otu sử nụumươt nu otms. …
Sảnxuãt bởi|Manufađutcd by: Bristol-Myers Squibb, 4601 Highwayó2 East.
Mount Vetaon, Indiana 47620, USA.
Đóng gói bởll Packaged by: Bristol-Myers Squibb S.r.l. (ontnda Fontana del Cetaso. 031112qu im, miy.
i Xuẩtxt'tziAỹ. “"
SĐK: XX—XXXX-XX
56 lô SX, NSX, H D: xem ”Lot". “Mfg”. "Exp“ trên bao bì.
Cơ sở dãng ký | MAN: Asttaleneca Slngapore Pte., ttd.
DNNK:Công 1y Cỡ Phân Dược Ltệu TW2, 24 Nguyên Thị Nghĩa, 01— Tp. 116 Chi Minh.
AstraZenecaỄ \
PalladioZannini Anlgni (Fr) AT ONGLYZA sms 1294163A1
lndumie GraũcheCưtotecniche S.p.A. zx14TAB 1 37Ẩ 3CK
Artwom DevelopmuưâPreptesstlepaưment VN __ ZI.’ 0119416301 (ITF)
{- ` _ …suu _ 77x30x132mm
Cyan - Magenta — - Black —
& m … am nm !ẳI'J m ram m ID
Ill05/2013
I.Knsttc
PRODUCT: ONGLYZA s mg
B LISTE R
Scale: 75%
%
.'“ _Ẹ _ _ 'Aý \ f _ `
( Am2gnemử MAH' AslmZeneca Smgapote Pte.. Lm I | mmâ MAH Aslraleneca Smgnpme Ple.. uu. \
onợyza’ onglyza’ onegn' onglyza’ onegza' onglyza' onglyza' onegza’ onglyn onan
J (samgiplim ĩẳw] 50 mL/phút).
Sử dụng ONGLYZA ở liều 2,5 mg 1 lầnlngảy cho bệnh nhản suy thận ở mức trung bình hay
suy thặn nặng vả cả suy thận ở giai doạn cuối cần phải thẳm phân mảu (độ thanh thải creatinin
[CrCI] 550 mL/phút) [Xem mục Dược lý lâm sèng]. Nên sử dụng ONGLYZA sau khi thấm phân
mảu. Chưa có nghiên cứu về việc sử dụng ONGLYZA trên bệnh nhản thấm phân phúc mạc
Do liều cùa ONGLYZA cần hạn chế ở mừc 2.5 mglngảy dưa trên chức nảng thặn, vì thế cần
đánh giá chức nảng thận trưởc khi bắt đầu điều trị với ONGLYZA vả sau đó cần theo dỏi chức
nặng thận định kỳ Chưc nảng thận có thể ước lượng từ nồng độ creatinin trong huyết thanh
bằng cảch sử dụng công thưc Cockcroft- Gault hay cỏng thức MDRD (Modification of Diet In
Renal Disease. Điều chỉnh chế độ ản cho bệnh nhân suy thận). [Xem mục Dươc!ỷlâm sáng].
Sử dụng cùng lúc vởi các thuốc ức chế mạnh CYP3A4!5
Liều sữ dụng của ONGLYZA là 2,5 mg 1 lần/ngảy khi sử dụng cùng lúc với các thuốc ưc chế
mạnh cytochrom P450 3A4/5 (CYP3A4IỔ) như: ketoconazoL atazanavir, clarithromycin
indinavir, itraconazol, nefazodon, nelfinavir, ritonavir. saquinavir vả telithromycin [Xem mục
Tương tác thuốc vả Dược lý lâm sáng].
2/28
Sử dụng cùng lúc vởi các thuốc kich thich tiết insulin {như sulfonylurẽ) hoặc với insulin
Khi sử dụng ONGLYZA cùng lùc với các thuốc i 20%. Dữ liệu sau khi điêu trị tăng cướng khộng được sử dụng cho cảc phản tỉch chinh về
hiệu quả.
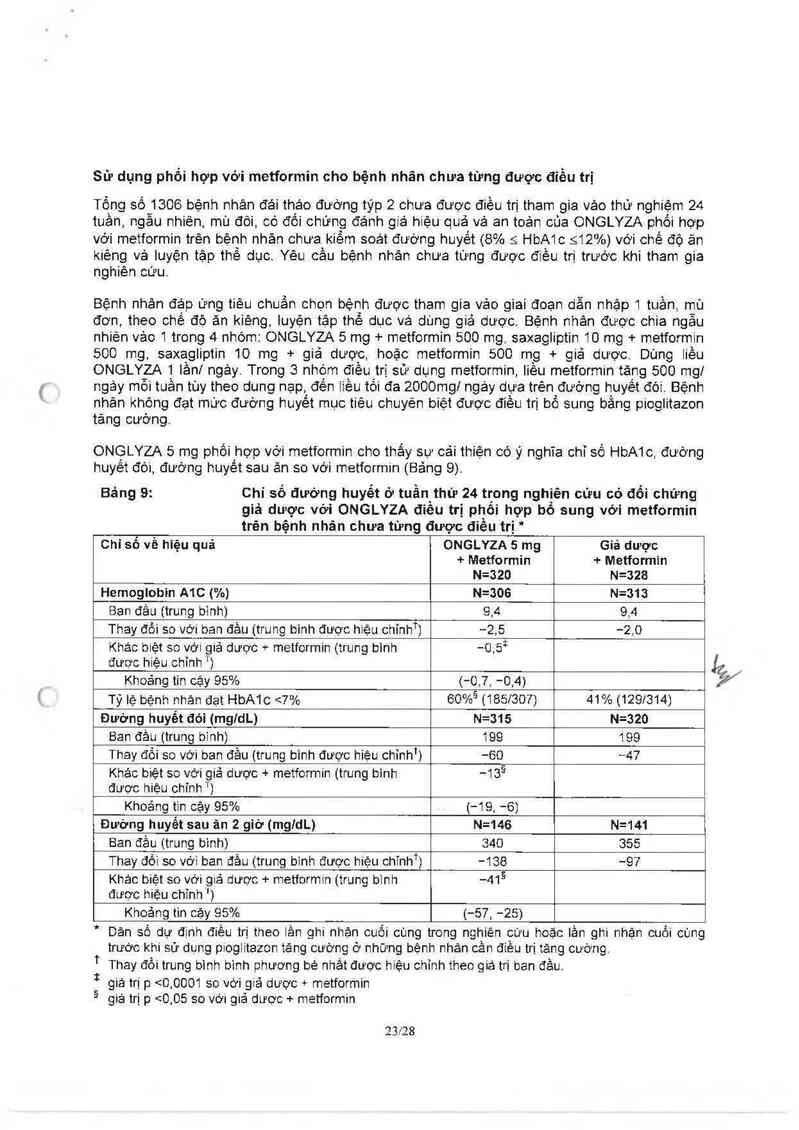
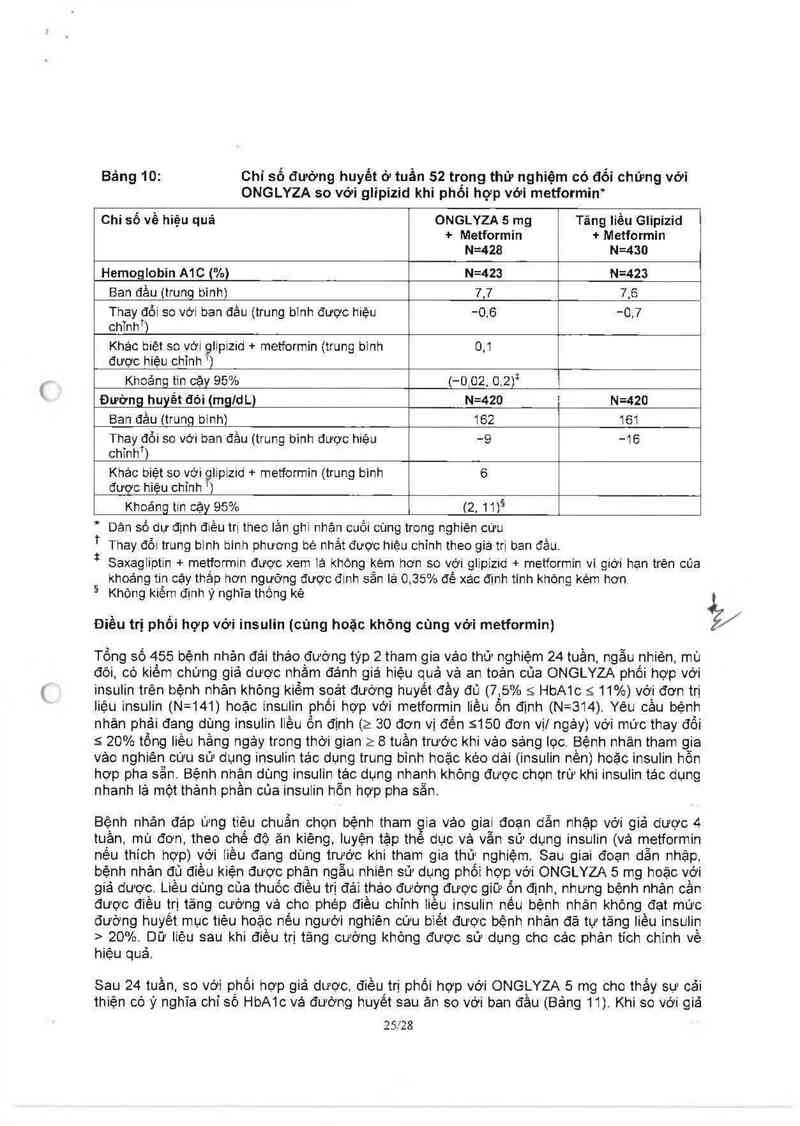
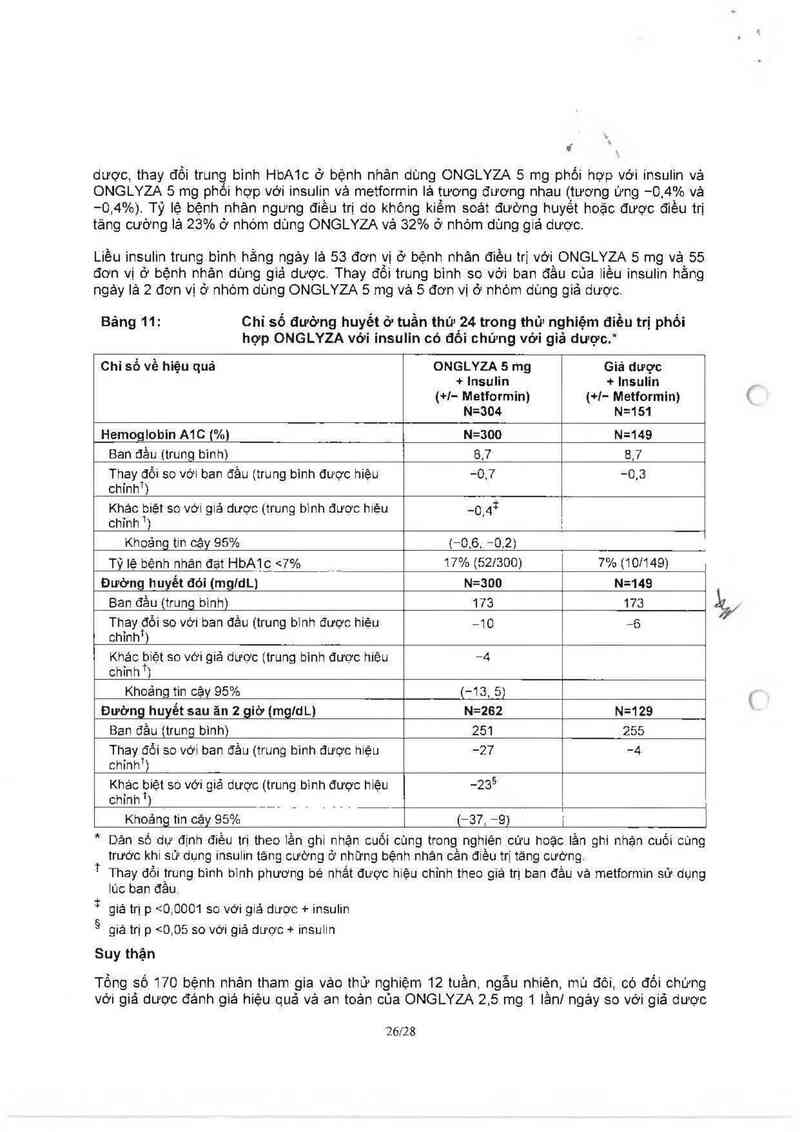
Sau 24 tuần, so với phối hợp giả dược. điêu trị phối hợp với ONGỊ.YZA 5 mg cho thắy sự oải
thiện có ý nghĩa chỉ số HbA1c vả đướng huyết sau ăn so với bản đầu (Bảng 11). Khi so với giá
25728
f ,
dược, thay đồi trung bình HbA1c ở bệnh nhân dũng ONGLYZA 5 mg phối hợp với insulin vả
ONGLYZA 5 mg phối hợp với insulin vả metformin lả tương đương nhau (tương ứng -0,4% vả
—0,4%). Tỷ lệ bệnh nhân ngưng điều trị do không kiềm soát đướng huyết hoặc được điều trị
tảng cướng lả 23% ở nhóm dùng ONGLYZA vả 32% ở nhóm dùng giả dược.
Liều insulin trung binh hằng ngảy lả 53 đơn vị ở bệnh nhản điều trị vớiONGLYịZA 5 mg vả_ 55
đơn vị ở bệnh nhân dùng giả dược. Thay đôi trung bình so với bạn đâu cùa liêu insulin hăng
ngảy lả 2 đơn vị ở nhóm dùng ONGLYZA 5 mg vả 5 đớn vị ở nhóm dũng giả dược.
Bảng 11: Chỉ số đướng huyết ở tuần thứ24 trong thử nghiệm điều trị phối
hợp ONGLYZA với insulin có đôi chứng với giả dược.*
Chỉ số về hiệu quả ONGLYZA s mg Giả được
+ Insulin + lnsuiin
(+i- Metformin) (+I- Metformin)
N=304 N=151
Hemoglobin A1 C (%) N=300 N=149
Ban đằu (trung binh) 8,7 8,7
Thay đối so với bản đầu (trung bình được hiệu -0,7 —0,3
chinh“)
Khảo biệt so với giả dược (trung binh được hiệu -o_4x
chỉnh 1)
Khoảng tin cậy 95% (-0.6, —0,2)
Tỷ lệ bệnh nhản đạt HbA1c <7% ___ 17% (527300) 7% (107149)
Đường huyết đói (mgidL) N=300 N=149
Ben đằu (trung bình) 173 173
Thay đồi so với ban đảu (trung binh được hiệu —10 —6
chỉnh')
Khác biệt so với giả dược (trung binh được hiệu —4
chinhi)
Khoảng tin cậy 95% (—13, 5)
Đường huyết sau ản 2 giờ (mgldL) N=262 N=129
Ban đầu (trung bình) 251 255
Thay đối so với ban đầu (trung bình được hiệu -27 -4
chĩnhi)
Khảo biệt so với giả dược (trung binh được hiệu -23s
ohinh †) _ _ _ _ , _
Khoảng tin cặy 95% (—37, —9) (
Dản số dự định điều trị theo iần ghi nhận ouối cùng trong nghiên cứu h0ặc lần ghi nhặn ouối cùng
trước khi sử dụng insụlin tảng cướng ở những bệnh nhản cản điêu trị tãng cướng.
Thay đồi `trung binh binh phương bé nhảt được hiệu chinh theo giá trị ban đảu Vả metformin sử dụng
lúc ban đâu.
giả trị p <0,0001 so với giả dược + insulin
giá trị p <0,05 so với giả dược + insuiin
Suy thặn
Tồng số 170 bệnh nhản tham gia vảo thử nghiệm 12 tuần, ngẫu nhiện, mũ đôi, có đối ohứng
với giả dược đảnh giả hiệu quả và an toản của ONGLYZA 2,5 mg 1 lảnl ngảy so với giả dược
267'28
!
/"
,x
trên bệnh nhân đái thảo đướng týp 2 bị suy thặn trung bỉnh (n=90), suy thặn nặng (n=41) hoặc
suy thận giai đoạn cuối (ESRD) (n=39). Trong thử nghiệm nảy, 98% bệnh nhân sử dụng thuốc
điều trị đải thảo đường nền (75% sử dụng insulin vả 31% sử dụng thuốc điều trị đái tháo đường
đường uống, đa số là sulfonylurẽ)
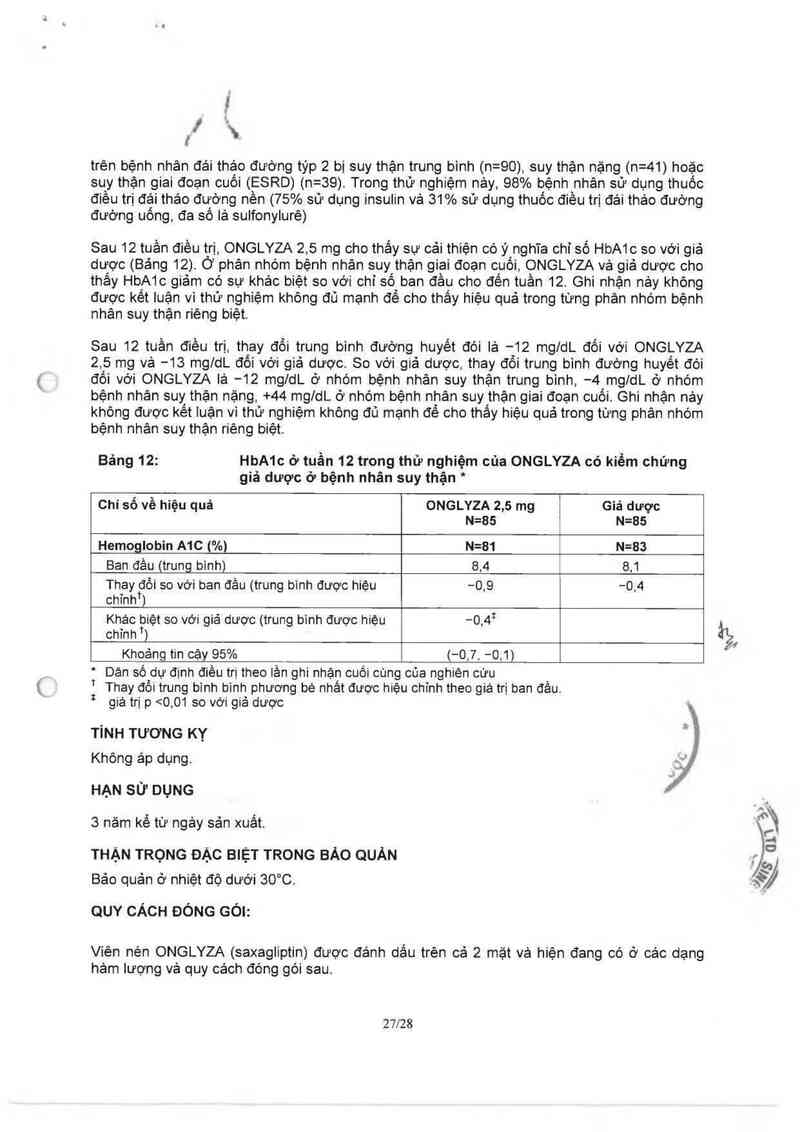
Sau 12 tuần điều trị, ONGLYZA 25 mg cho thấy sự cải thiện cóỷ nghĩa chỉ số HbA1c so với giả
dược (Bảng 12). Ở phân nhòm bệnh nhân suy thặn giai đoạn cụối, ONGLYZA vả giả dược cho
thắy HbA1c giảm có sự khảo biệt so với chỉ số ban đầu cho đẻn tuần 12. Ghi nhận nảy không
được kết luận vi thử nghiệm không đủ mạnh để cho thấy hiệu quả trong từng phản nhóm bệnh
nhân suy thận riêng biệt.
Sau 12 tuần điều trị. thay đồi trung binh đường huyết đói lả -`12 mgldL đối với ONGLYZA
25 mg vả -13 mg/dL đối với giả dươc. So với giả dược. thay đôi trung bình đường huyết đói
đối với ONGLYZA lẻ -12 mg/dL ở nhóm bệnh nhân suy thận trung bình, -4 mgldL ở nhóm
bệnh nhân suy thận nặng, +44 mg/dL ở nhóm bệnh nhân suy thận giai đoạn cuối. Ghi nhận nảy
không được kết luận vi thử nghiệm không đủ mạnh để cho thảy hiệu quả trong từng phân nhóm
bệnh nhân suy thận riêng biệt.
Bảng 12: HbA1c ớ tuần 12 trong thử nghiệm của ONGLYZA có kiềm chứng
giả dược ở bệnh nhân suy thận *
cm số về hiệu quả ONGLYZA 2,5 mg Giả dược
sts N=85
Hemoglobin A1C (%) N=81 N=83
Ban đầu (trung binh) 8,4 8.1
Thay đồi so với ban đầu (trung binh được hiệu —0,9 —0,4
chĩnh’)
Khác biệt so với giả dược (trung binh được hiệu -o,4²
chinh T)
Khoảng tin cậy 95% (-0,7, -0.1)
' Dãn số dự định điêu trị theo lần ghi nhận cuối cùng của nghiên cứu
' Thay đối trung bình binh phương bé nhảt được hiệu chĩnh theo giá trị ban đảu.
² giá tri p
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng