












589qu! WIWJ'WIU
ã…@@g «…JenexaN
Dow vvuc
DIRNFI' MW … PiRESEN'II'ATDN IIS NƯIT DIDIIIIG
pun etssuos mm
Ptntom: 2718. 1255.
TAUZN 16990
1 ~ get
Ơ N exa va ri… 2 OOmg
\Ễ fiIm-coated tablets Ìấ
sorafem'b (as tosylate)
" n' ma use
Reaci eansec leaf1el befOie t.se
Each iabiet cunia ns 200 mg Swatcmh 1`dE towta!O…
iỄli Thuốc bán theo đơn
. N ex a va !“ ẫ2 @@mg fiIm-coated tablets
!)eđc r;i pt. _ tt 51,60, 10 men _;ii piescrt iJ
Keep modicameni out ot reach ot chitdren.
Sfth
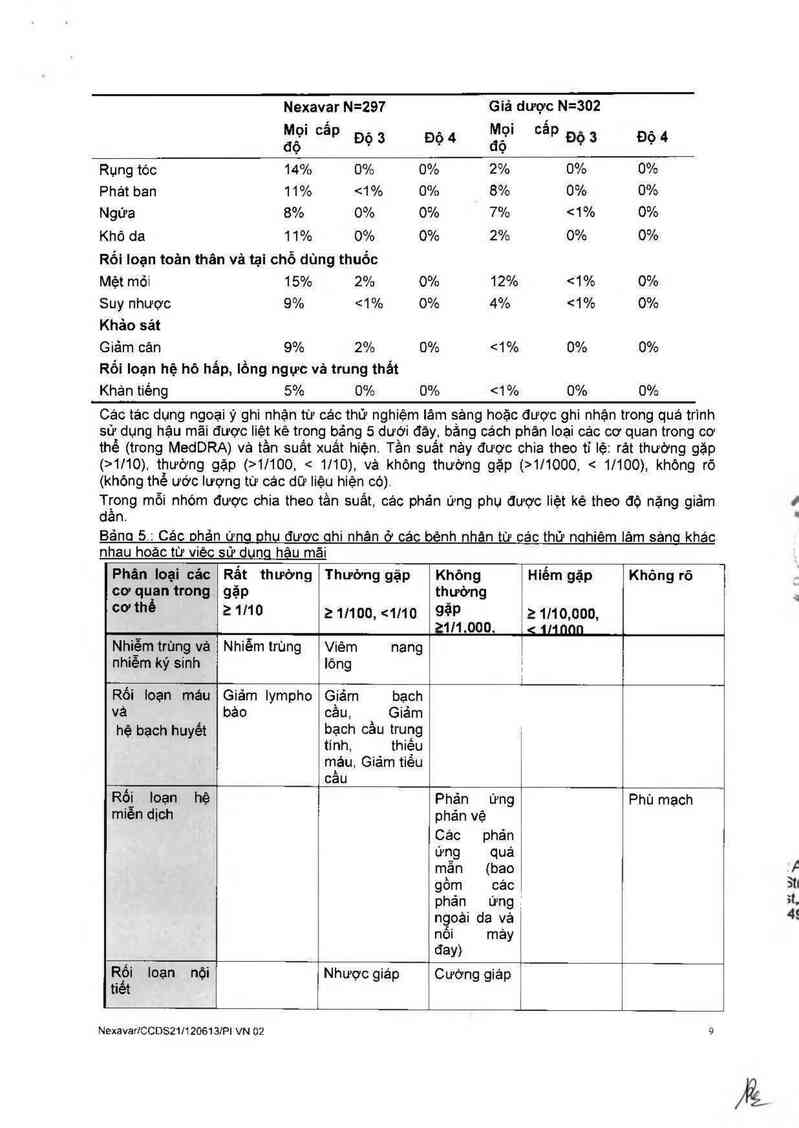
Mến vie— … (.iiua zni rv~g Snm'eivii |1l10) thường gặp (>1/100 < 1110), và không thường gặp (>111000 < 1/100), không rõ
(khỏng thể ước lượng từ các dữ liệu hiện có)
Trong mỗi nhóm được chia theo tần suất các phản ứng phụ được liệt kê theo độ nặng giảm
dần.
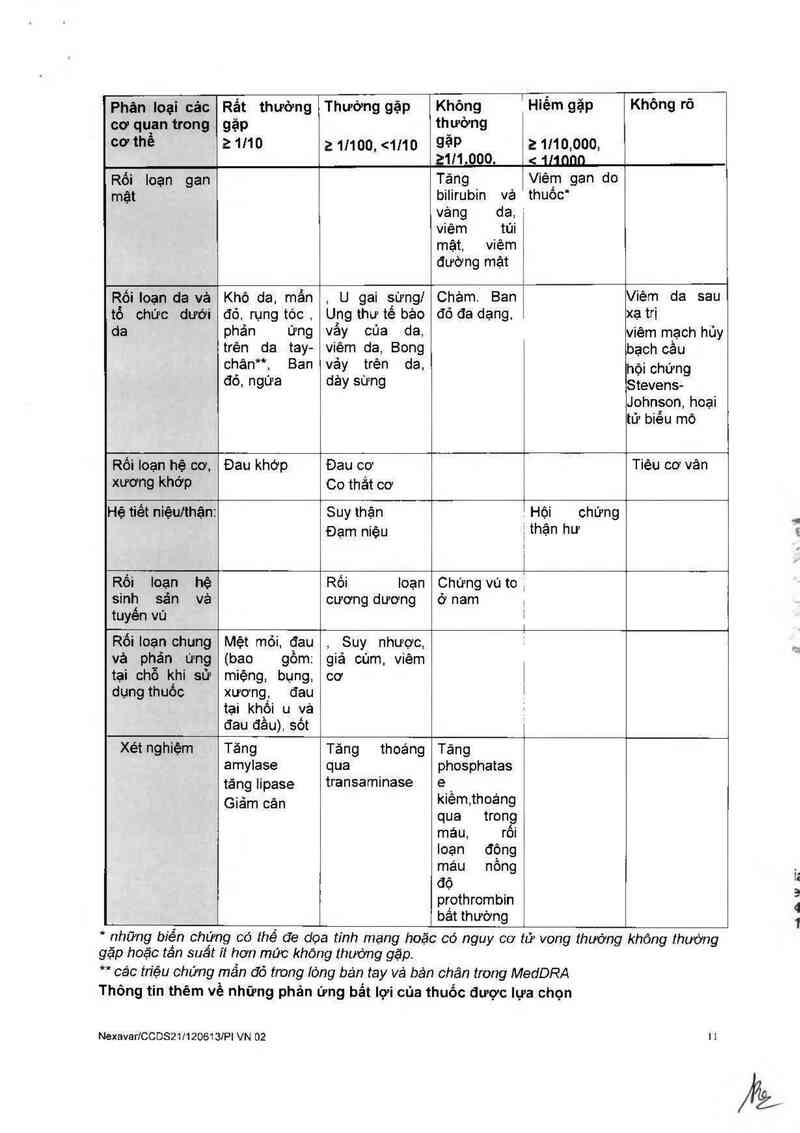
Báno S.: Các ohản ứnc nhu đươc ohi nhân ở các bẻnh nhân từ các thử nohiêm lâm sảno khác
nhau hoăc từ viêc sử dunq hâu măi
Phân loại các Rẩt thường Thường gặp Không Hiếm gặp Khôngrõ
cơ quan trong gặp thường
°°'thề 21110 211100, <1110 gạp z1l10,ooo,
Ễ'II'I.OOO. < 1I1HQỊI
Nhiễm trùng vả Nhiễmtrùng Viêm nang
nhiễm ký sinh lông
Rối Ioạn máu Giảm lympho Giảm bạch
va bảo cầu, Giảm
hệ bạch huyêt bạch cầu thfJ9
tỉnh, thieu
máu. Giảm tiếu
câu
Rối loạn hệ Phản ứng Phù mach
miễn dich phản vệ
Các phản
ứng quả
mẫn (bao
gòm các
phản ứng {
ngoải da vả
nối mảy
đay)
RỄi loạn nội Nhược giáp Cường giáp
tiet
NexavarlCCDSZ1/1ZOGỦIPI VN 02
ẫtl
ìt.
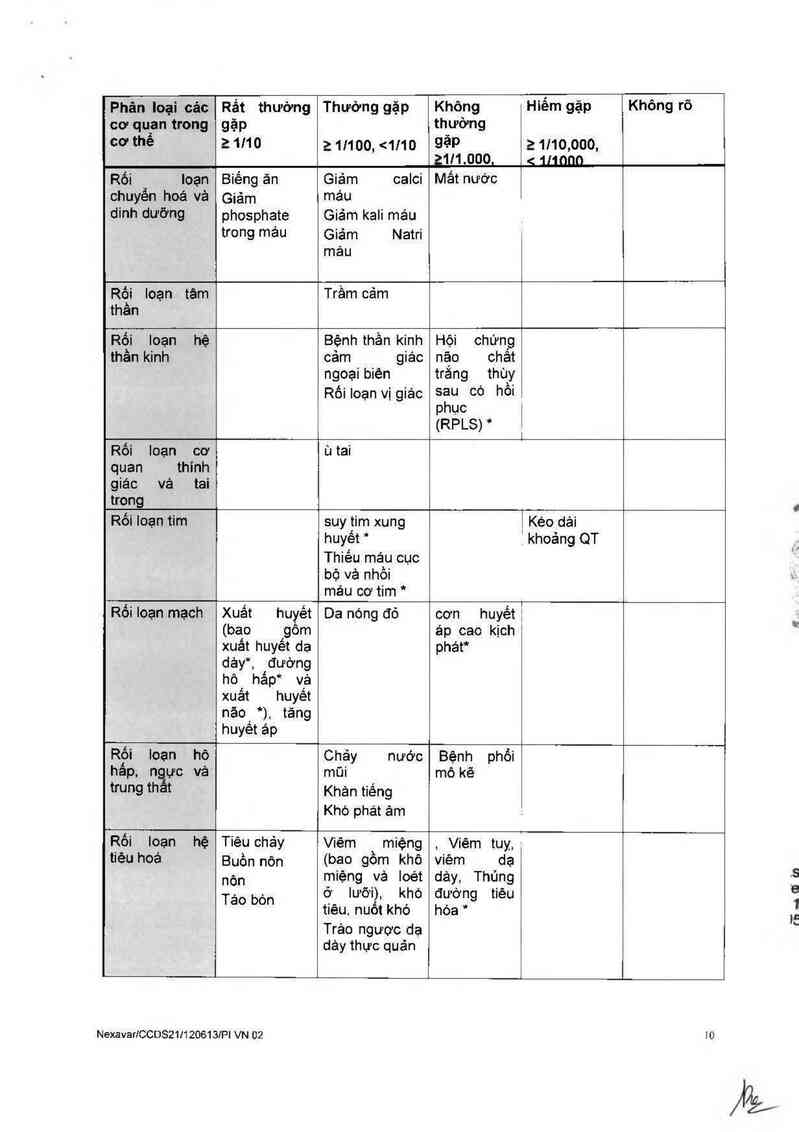
Phân loại các Rất thường Thường gặp Không Hiếm gặp Khõngrõ
cơ quan trong gặp thường
cơthễ 21110 zmoo,500
msec sau khi theo dõi bằng ECG sau khi điêu trị. (xem phần Cảc cảnh báo vả thận trọng)
Đặc điềm dược động học
Hắp thu vả phân bố
NexavarICCDSZ1HZOfflSIPI VN 02 12
Sau khi sử dụng thuốc viên sorafenib, sinh khả dụng tương đồi trung bình đạt được vảo khoảng
38— 49% so vơi sử dụng dung dịch uống. Sau khi uống. sorafenib đạt tới nồng độ đỉnh trong
huyêt tương trong khoặng 3 giờ Khi sử dụng cùng bữa ăn với lượng mỡ vưa phải, sinh khả
dụng tương đương với sử dụng khi đói. Với bữa ăn có lượng mỡ cao, sinh khả dụng của
sorafenib giảm đi khoảng 29% so với sữ dụng khi đói.
Trên in vitro, gắn kết của sorafenib với protein trong huyêt tương lả 99,5%.
Chuyến hoá vả thải trừ
Sorafenib được chuyến hoá chủ yếu trong gan thòng qua quá trinh oxi hoá vả được hoạt hoá
bởi CYP3A4 cũng như phản ứng liên hợp glucuronic được hoạt hoá bời UGT1A9
Sorafenib Iiẻn hợp có thể được tách ra trong ông tiêu hóa bới cảc hoạt động glucoronic hóa cũa
vi khuẩn, cho phép tải hâp thu thuôo ở dạng không liên hợp. Sử dụng đồng thời với neomycin
sẻ Iảm ảnh hưởng tới quá trình nảy, Iảm giảm sinh khả dụng trung bình của sorafenib tới 54%.
Khi uống dung dịch smafenib liều 100mg, 96% iiều dùng được thải trừ khỏi cơ thể trong vòng
14 ngảy, với 77% lièu dùng được bải tiêt qua phân và 19% Iièu dùng được bải tièt qua nước
tiểu dưới dạng chuyền hóa glucuronidate Sorafenid dạng không chuyển hóa, chiêm 51% liêu
dùng, được tim thấy trong phân mã không có trong nước tiếu
Thời gian bán thải của Sorafenib trong khoảng từ 25-48 giờ.
Các thóng tin khác trên các đối tượng đặc biệt
Các nghiên cứu về út chế men trén in vitro
Các nghiên cứu với vi lạp thể của gan ở người cho thắy sorafenib lả một chất ưc chê cạnh tranh
của CYP2C19 CYP2D6 vả CYP3A4. Uộng đồng thơi với midazolam dextromethorphan, vả
omeprazoie, những thuốc chuyển hóa lần lượt bởi các cytochromes CYP3A4 CYP2D6 vả
CYP2C19, sau khi uống sorafenib 4 tuần khòn Iám thay đối sự hâp thu của cảc thuốc náy.
Điều nảy cho thắy rằng sorafenib không ức che cũng như khòng kich thích các men xúc tác
cytochrome P450.
ln invitro dữ liệu cho thắy sorafenib ức chế phản ứng lièn hợp giucoronic thông qua con đường
UGT1A1 (Ki =1 ịJM) vả UGT1A9 (Ki=2 uM). Khi sử dụng với irinotecan, mà bị chuyển hoá đầu
tiên bởi SN38 và sau đó được chuyền hoá bời con đường UGT1A1, có sự gia tăng AUC cùa
SN— 38 từ 67-120%. Sự hâp thu toản thân của cảc thuốc chuyền hóa bởi UGT1A1 vá UGT1A9
có thể tăng lẻn khi sử dụng đồng thời với sorafenib
Sorafenib ức chế CYP2Bõ vả CYP2C8 trèn in vitro với giá trị Ki tương ứng lả 6 vả 1- 2 uM.
Uông đồng thời sorafenib vởi paclitaxel Iảm tảng, thay vì giảm, sự hấp thu của 6-OH paclitaxel,
chảt chuyển hóa đâu tiên của paclitaxel được hình thảnh bởi CYP2CB. Những dữ liệu nảy gợi ý
sorafenib có thể không phải lá chât ức chế CYP2CB trong in vivo.
Uống đồng thời sorafenib với cyclophosphamide lam giảm nhẹ hấp thu cyclophosphamid,
nhưng khỏng lảm giảm hấp thu toản thân của 4-OH cyclophosphamide lá chảt chuyển hoá có
hoạt tinh cùa cycloph05phamid được hình thảnh chủ yêu bởi CYPZBG. Những dữ liệu nảy gợi ý
rằng sorafenib có thế khỏng gây ức chê CYPZBG trên in vivo.
Các nghiên cứu trên microsomes trong gan người cho thây sorafenib là một ức chế cạnh tranh
của CYPZCS với gia' tri K. 7- 8 uM. Sorafenib có thể tác động đến cảc thuốc chuyển hóa bởi
CYPZC9 đă được ghi nhận ở những bệnh nhân sử dụng sorafenib hoặc giả dược kêt hợp với
warfarin. Những thay đối trung bình so với mức ban đầu của PT-INR không cao hơn khi so
nhóm bệnh nhản sorafenib với nhóm bệnh nhản giả dược. cho tháy răng sorafenib có thể
không ức chế CYP2C9 trên in vivo
Tác động ức chế CYP3A4
Ketoconazole (400 mg) được dùng mỗi ngáy một lần trong 7 ngảy cho các tình nguyện nam
khoẻ mạnh không lam thay đồi AUC của một iiều đơn 50 mg sorafenib. Do đó. dường như
Khỏng có cảc tương tác dược lý Iám sảng của sorafenib và các thuốc ức chế CYP3A4
Tác đóng lên các thuốc kích thich CYP
Hoat tỉnh của CYP1A2 vả CYP3A4 không bị thay đổi sau khi uông sorafenib trên các tế báo gan
trên người được nuôi cắy, cho thay rảng sorafenib gần như khỏng phải lả chât kich thích
CYP1A2 vá CYP3A4. Uống liên tục sorafenib vá rifampỉcin lám giảm trung binh 37% AUC
sorafenib. Cảo chảt kich thich hoạt tính CYP3A4 khảc (như Hypericum perforatum hay được goi
Nexavarlccoszmzosisipi VN 02 13
lả St. John's wort, phenytoin, carbamazepine, phenobarbital, vả dexamethasone) có thể cũng
tảng chuyên hóa sorafenib vá do đó Iảm giảm nông độ sorafenib.
Kết hơp với các thuổc chổng ung thư khác
Trong các nghiện cứu lâm sảng, sorafenib được sử dụng đồng thời với cảc thuốc chống ung
thư khác với liều điều trị bao gồm: gemcitabine, cispiatin, oxaiiplatin paclitaxel, carboplatin,
capecitabine, doxorubicin. irinotecan vả cyclophosphamide. Sorafenib không ảnh hưởng liên
quan đến lâm sảng đển dược động học của gemcitabine, cisplatin, oxaliplatin hoặc
cyclophosphamid.
Paciitaer/Carboplatin
Sử dụng paclitaxel (225 mglm²) vả carboplatin (AUC= 6) với uống sorafenib (< 400 mg 2
lân/ngảy), uống sorafenib cho đên khi nghỉ 3 ngảy trước khi sử dụng paclitaxellcarbopiatin, kêt
quả không ảnh hưởng lớn đén dược động học của paclitaxel.
Sử dụng cùng lúc paclitaxel (225 mglm², mỗi 3 tuần) vả carboplatin (AUC= 6) với sorafenib (400
mg 2 lần/ngảy, không có khoảng ngưng thuốc) kết quả tảng 47% hắp thu sorafenib, vả tảng
29% hấp thu paclitaxel vả tảng 50% hắp thu 6- OH paclitaxel. Dược động học cúa carboplatin
khỏng bị ảnh hưởng.
Những dữ liệu nảy cho thảy không cần điều chỉnh liều khi điều trị đồng thời paclitaxel vả
carboplatin với sorafenib, mả sorafenib phải ngưng 3 ngảy trước khi điều trị cho chu kì sau.
Ý nghĩa lâm sảng cúa việc tăng hắp thu sorafenib vả paclitaxel, sau khi điều trị đổng thời khỏng
có khoảng nghỉ, lả chưa rõ.
Capecitabíne
Uống đồng thời với capecitabine (750- -1050 mglm² 2 lầnlngảy, ngảy 1 14 mỗi 21 ngảy) vả
sorafenib (200 hay 400 mg 2 lần/ngảy, uống Iiẻn tuc) kêt quả không lảm thay đổi lớn sự hắp thu
của sorafenib, nhưng táng 15- 50% hảp thu của capecitabine vả 0-5 52% tăng hắp thu 5- FU. Ý
nghĩa Iảm sảng của việc tảng nhỏ không đáng kể hấp thu của capecitabine vả 5-FU khi uống
đồng thời với sorafenib lả chưa rõ.
Doxorubicin/lrinotecan
Đìèu trị đồng thời với sorafenib Iảm tăng lên 21% AUC của doxorubicin. Khi sử dụng với
irinotecan, mã được chuyền hoá đầu tiên bởi SN38 và sau đó được chuyền hoá bời con đường
UGT1A1, có sự gia tăng AUC của SN- 38 từ 67— 120% và tảng 26-42% AUC của irinotecan. Ý
nghĩa |ảrh sảng của những phát hiện nảy lá chưa rõ rảng (xem phần Cảo cảnh báo đặc biệt vả
thận trọng khi sử dụng).
Docetaxel
Docetaxel (75 hoặc 100 mglm² 1 lần mỗi 21 ngảy) khi sử dụng đồng thời với sorafenib (200 mg
ngảy 2 lần hoặc 400mg ngảy 2 lần sử dụng từ ngáy thứ 2 đền 19 của chu kỳ 21 ngả ). sau đó
ngưng dùng thuốc trong 3 ngảy, kêt quả là AUC của docetaxel tảng từ 36-8 0% và nong độ tối
đa Cmax của docetaxel tăng từ 16-3 2% Cần thận trọng khi sử dụng đồng thời sorafenib vả
docetaxel (xem phần Các cảnh báo đặc biệt và thận trọng khi sử dụng).
Kểt hợp với các kháng sinh khác
Neomycin
Sử dụng đồng thời với neomycin, một tảc nhân diệt khuẩn không tác đụng toán thân, được sử
dụng để diệt khuấn tại đướng tiêu hóa, sẽ Iảm ảnh hướng đên chu trinh gan ruột của sorafenib
(xem phần Dược lý lâm sảng chuyển hóa vả thải trừ). dẫn đên lảm giảm hấp thu sorafenib
Trên những người tình nguyện khỏe mạnh với phác đồ điều trị 5 ngảy sử dụng neomycin Iảrn
giảm sinh khả dụng trung binh của sorafenib 54%. Ý nghĩa iâm sảng cùa những kết quả nảy
vẫn chưa rõ. Ành hướng của các kháng sinh khác vẳn chưa đươc nghiên cứu, nhưng gân như
phụ thuộc vảo khả nảng của chúng lảm giảm hoạt động cùa glucoronidase
Dược động học đối với một số nhóm bệnh nhán đặc bíệt
Người giả (trên 65 tuổi) vả giởi tính
Các phân tích dựa trên số liệu nhản khấu học cho thây khỏng cần thiết điêu chỉnh liêu dùng đồi
với yêu tố tuối tác vả giới tính
Trẻ em. Không có số liệu về dược động học đối với nhóm bệnh nhân nhi khoa.
NexavarlCCDSZ1/120ôiSiPl VN oz 1“
/i£
Suy gan Sorafenib được đảo thải chủ yếu qua gan
Ở những bệnh nhân ung thư tè báo biểu mô gan có suy gan nhẹ (Child Pugh A) hoặc suy gan
vừa (Child- Pugh B), giá trị tiếp xúc trong phạm vi đã quan sát ở những bệnh nhân không suy
gan. Dược động học (PK) của sorafenib ở bệnh nhân Chiid- Pugh A vả Child- P-ugh B khỏng ung
thư gan tương tự như PK ở những ngưới tinh nguyện khoẻ mạnh Dược động học của
sorafenib chưa đươc nghiên cữu trèn những bệnh nhân suy gan nặng (Child- Pugh 0) (xem
phần Cảnh báo đặc biệt vả thặn trọng vả phần Liều dùng vả cách dùng thuốc)
Suy thận: Trong một nghiên cứu dược iỷ iảm sảng, dược động học của sorafenib được đánh
giá dựa trên lièu dùng duy nhất lả 400mg đối với những đối tượng có chức nảng thận bình
thuờng, các đối tượng suy thận nhẹ (CrCL 50-80 mllphút), suy thặn vừa (CrCL 30 đến < 50
mllphút) hoặc suy thận nặng (CrCL <30 mllphút) nhưng không cần phải lọc máu. Không ghi
nhận được mối liên quan giữa việc sử dụng sorafenib vả chức năng thặn. Không cần thiêt phái
điêu chỉnh liều dùng dựa trên mừc đó suy thặn nhẹ, Vừa hoác nặng mả chưa lọc máu (xem
phần Liều dùng và cách dùng thuốc).
Dữ liệu an toản tiền Iám sảng
Các số liệu về an toản tiền lâm sảng của sorafenib đă được đảnh giá trên chuột, chó vả thỏ.
Độc tinh toản thân
Các nghiên cứu về liêu độc nhắc lại cho thảy những thay đối từ nhẹ đên vừa (thoái hoá vá tái
sinh) tại các cơ quan khác nhau trèn cơ thể.
Sau khi sử dụng liều dùng nhắc lại đôi với chó con vá chó đã trưởng thảnh, các ảnh hưởng đến
xương và răng đã đươc ghi nhận Những thay đối bao gôm sự dảy lèn bắt thường ở đia sụn
đầu xương đùi khi sử dụng liều dũng sorafenib 600 mglm² diện tích bề mặt cơ thế- BSA (tương
đương với 1 ,2 lần liều khuyên dùng trẻn lâm sáng ia 500 mglm² BSA), giảm hoạt tính tế bảo
trong tuý xương dẫn đên thay đối sự trường thảnh cùa đĩa sụn đầu xương với liều dùng lá
200mg/m²lngảy. sự thay đồi của thảnh phần men răng cũng xảy ra ở liều dùng 600 mglm²lngảy.
Tuy nhiên không thảy có ảnh hưởng đối với chó trưởng thảnh.
Có tác động gáy đột biên gien được ghi nhận đối với sorafenib trong một thử nghiệm với tế bèo
trên invitro cùa động vặt có vú (buồng trứng chuột hamster Trung Quốc) để tim ra thực bảo gây
đột biên (nhiễm sảc thể bắt thường) được biẻu hiện qua sự chuyên hoá phóng xạ _Trong một
thử nghiệm với tế bảo vi khuẩn trên in vitro (thử nghiệm Ames), một hoạt chât cuối cùng của
thuôo (
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng