












osw 0
sxa;qez paưoa-uuụ … x sman z ;o xoa
f @… os unduũeuS)
…ọcgnuor
HO
.ffl
Ế}
\\
/1_ ẵ ễ Ễ ffl ,
ẳ Thuốc ban theo đơn
_ _n — 0
:=: ' …
je Jơnwĩ Ệ
ẵỄẵ Box of 2 blisters x 14 fìlm-coated zablets
: :
\Í Ộ wuso
___fJ
n
Jcnuv`ỉô…
(sỉtagliptin so mg]
Box of 2 blisters x 14 film-coated tablets
“@ "9'1
dVG
v
ELLĂÒEI
lv
V
Doi… A1 rwnò :)
a
.LHĂIÌ(I HH
V
JVỔmem’ĩml`Ốĩ
Each fiIm-coated tablet contains 6425 mg
sitagliptin monohyd rate phosphate
equivalent to 50 mg sitagliptin.
For Indications. Contưaindicatìons. Dosage
and Administration, and other information:
see package insert.
Store below 30°C (86'F).
Keep out of reach of children
Săn xuấì bời/Manufactured by:
Mnrck Shlrp & Dohme le.
Shonen tane. Cramlington. Nonhumberland,
NE23 31U. United Klngdom (Anh)
0 MSD
SĐKIREGJ XX-XXXX-XX
ot xa TẨM mv mt em
Đọc KỸ uuơne nAu sử
DỤNG mươc KHI DONG
Mòi vlèn nẻn bao phim 50 mL/ phút, gần tương
ửng vởi creatinine huyết thanh < 1,7 mg/dL ở nam vả < 1,5 mgldL ở nữ), không cân chinh liếư
JANUVIA.
me
Đối vởi bệnh nhân suy thận trung binh (CrCl > 30 đển < 50 mL/phủt, gẩn tương ứng với
creatinine huyết thanh > 1,7 đến < 3,0 mg/dL ở nam và > 1, 5 đến < 2 ,5mg/dL ở nữ), liều
JANUVIA là 50 mg ngảy 1 lần.
Đối với bệnh nhân suy thận nặng (CrCl <30 mL/phút, tương ứng với creatinine huyết thanh
khoảng >3, 0 mgldL ở nam và >2, 5 mg/dL ở nữ) hoặc có bệnh thận giai đoạn cuối cân thẩm tách
mảu hoặc thẩm phân phủc mạc, liếư JANUVIA là 25 mg ngảy 1 lần. Có thể dùng JANUVIA bất
kỳ lúc nảo, không liên quan đến thời điếm thẩm tảch máu
Vì có sự chỉnh liếư dựa vảo chức năng thận, theo khuyến cảo nên đảnh giả chức năng thận trước
khi khời đầu điêu trị và sau đó kiêm tra định kỳ.
CHỐNG cui ĐỊNH
Chống chỉ định dùng JANUVIA ở pẹnh nhân quả mẫn với bất kỳ thảnh phần nảo cùa thuốc
(xem THẬN TRỌNG, Phản ứng mân cảm vả TAC DỤNG PHỤ, Kinh nghiệm hậu mãz),
THẶN TRỌNG
Tống quát
Không nên dùng JANUVIA ở bệnh nhân đái thảo đường týp } hoặc để điểu trị nhiễm acid
ceton ở bệnh nhân đái tháo đường.
Viêm tụy. Đã có cảc bảo cảo về viêm tụy cấp, bao gồm viêm tụy xuất huyết hoặc hoại từ gây tử
vong vả không gây tử vong (xem TÁC DỤNG PHỤ) ở bệnh nhân dùng sitagliptin. Nên cho
bệnh nhân biểt triệu chứng đặc tnmg của viêm tụy câp là đau bụng dữ dội và liên tục. Viêm tụy
được ghi nhận hồi phục sau khi ngưng dùng sitagliptin. Nếu nghi ngờ viêm tụy, nên ngưng
dùng JANUVIA vả các thuốc khảc có thế liên quan
Sử dụng ở bệnh nhân suy Ihận: JANUVIA được đảo thải qua thận. Để đạt nồng độ JANUVIA
trong huyết tương tương tự như ở bệnh nhân có chức năng thận bình thường, nến giảm liều
thuốc ở bệnh nhân suy thận trung bình và nặng, cũng như ở bệnh nhân có bệnh thận giai đoạn
cuối (ESRD) cần thẩm phân máu hoặc thấm phân phủc mạc (xem LIÊU LƯỢNG VÀ CÁCH
DÙNG, Bệnh nhân suy thận. )
Hạ đường huyết khi dùng liệu pháp kết họp vởi sulfamide hạ đường huyết hoặc insulin. Trong
cảc thử nghiệm lâm sảng với JANUVIA theo đơn trị liệu và theo trị liệu kểt hợp với các thuốc
được biểt rõ không gây hạ đường huyết (như metformin hoặc chất chủ vận PPARy
(thiazolìdinedỉones)), tỷ lệ cảc bảo cảo hạ đường huyết khi dùng .FANUVIA tương tự như ớ
bệnh nhân dùng placebo Giống như cảc thuốc trị tãng đường huyết khác, đã quan sảt thấy hạ
đường huyết khi dùng JANUVIA kết hợp vởi ìnsulin hoặc sulfamide hạ đường huyết (xem
TẢC DỤNG PHỤ). Do đó, để giảm nguy cơ hạ đường huyết do SU vả insulin, có thể xem xét
giảm liếư SU hoặc insulin (xem LIÊU LƯỢNG VÀ CÁCH DÙNG).
Phản ứng quá mẫn. Đã có cảc bảo cảo hậu mãi về những phản ứng quả mẫn nghiêm trọng ở
bệnh nhân dùng JANUVIA. Cảo phản ứng nảy bao gôm phản ứng phản vệ, phù mạch và cảc
bệnh lý tróc da kể cả hội chứng Stevens—Johnson. Vì cảc phản ưng nảy được bảo cảo tự nguyện
từ dân số chưa biết rõ cỡ mâu, nên thường không thể ước tinh chẳc chắn tần suất hoặc xảo lập
mối quan hệ nhân guả với việc sử dụng thuốc. Các phản ứng nây bắt dầu xuất hiện trong 3
thảng đầu sau khi băt đầu điếu trị với JANUVIA, vởỉ vải bảo cáo xảy ra sau liều đầu tỉên. Nếu
nghi ngờ có phản ứng quá mẫn, phải ngưng dùng JANUVIA, đánh giá cảc nguyên nhân tiềm
tảng khác vả bắt đầu cảc trị liệu thay thể vẽ bệnh đải tháo đường. (xem CHỐNG CHỈ ĐỊNH
vả TÁC DỤNG PHỤ, Kinh nghiệm hậu mã1).
JmpÒ/
ũt
PHỤ NỮ có THAI
Sitagliptin không có khả năng gây quải thai ở chuột cống khi dùng Iỉều đến 250 mg/kg hoặc ở
thỏ vởi liếư đến 125 mgfkg trong giai đoạn hình thảnh cảc cơ quan (tương ứng đến 32 lần và 22
lần, lượng dung nạp ở người dựa theo liếư đề nghị hâng ngảy ở người lớn là 100 mg/ngảy). Ở
chuột công, tỷ lệ biến dạng xương sươn thai nhi (không có xương sườn, xương sườn giảm sản vả
chuỗi hạt sườn) tăng nhẹ được ghi nhận khi chuột mẹ dùng liếư ] 000 mg/kglngảy (khoảng 100
lần lượng dung nạp ở người dựa theo liếư đề nghị hảng ngảy ở người lớn lả 100 mg/ngảy) Khi
chuột công mẹ dùng liếư uông ] 000 mg/kg/ngảy, cân nặng trung bình của chuột con cả 2 giống
đực và cải trước khi thôi bú vả sự tăng cân của chuột đục con sau khi thôi bú đếu giảm nhẹ. Tưy
nhiên, nhủng nghiên cứu về sự sinh sản ở động vật không phải lức nảo cũng dự đoản được đảp
ứng ở người.
Vì không có những nghìên cứu đầy đủ và đối chứng tớt ở phụ nữ có thai, nên chưa biết rõ tính an
toản cùa JANUVIA ở phụ nữ có thai. Như các thuốc uông trị tăng đường huyết khảo, không
khuyến cảo sử dụng JANUVIA trong thai kỳ
PHỤ NỮ CHO CON BÚ
Sỉtaglìptỉn được bải tiết vảo sữa chuột cống mẹ. Vẫn chưa bỉểt rõ sitagliptin có bải tỉết vảo sữa
người hay không. Do đó, không nên dùng JANUVIA cho phụ nữ đang cho con bú.
SỬ DỤNG ở TRẺ EM
Chưa xác lập tính an toản và hiệu lực của JANUVIA ở bệnh nhi dưới 18 tuổi.
SỬ DỤNG ớ NGƯỜI CAO TUỔI
Trong cảc nghiên cứu lâm sảng, tính an toản và hiệu lực cùa JANUVIA ở người cao tuổi (> 65
tuổi) tương tự như ở bệnh nhân trẻ tuồi hơn (<65 tuổi). Không cần chỉnh liếư theo độ tuốỉ. Bệnh
nhân cao tuối có nhiếư khả nãng Suy thận hơn; như cảc bệnh nhân khác, có thế cần chỉnh liếư khi
có suy thận đáng kể (xem LIÊU LƯỢNG vẨ CÁCH DÙNG, Bệnh nhán suy lhận).
TƯỜNG TÁC THUỐC
Trong cảc nghiên cứu tương tác thuốc, sìtagliptin không gây tảc động có ý nghĩa lâm sảng lên
dược động học cùa các thuôo sau đây: metformin, rosiglitazone, glyburide, sỉmvastatin, warfarin
và viên uông trảnh thai. Dựa vảo cảc dữ liệu nảy, sitagliptin không ức chế cảc isozyme CYP tả“
CYP3A4, 2C8, hoặc 2C9. Dựa vảo dữ liệu in ví,tro người ta cho răng sitagliptin cũng không có
tác dụng ức chế CYP2D6, 1A2, 2C19 hoặc 2B6, hoặc cảm ứng CYP3A4
Dùng metformin ]ìểu lặp lại ngảy 2 lần cùng với sitagliptin không iảm thay đổi có ý nghĩa-dược ~
động học của sitagliptin ở bệnh nhân đái tháo đường týp 2.
Cảo phân tích dược động học theo dân số đã được tiến hảnh ở bệnh nhân đái thảo đường týp 2.
Những thuốc dùng đổng thời không gây tảc dụng có ý nghĩa lâm sảng lẽn dược động học cùa
sitagliptin Những thuốc được đánh giả là thuốc dùng phổ biến ở bệnh nhân đái thảo đường tỷp
2, bao gôm các thuốc trị tảng cholesterol mảu (như statins, fibrates, ezetimibe), thuốc khảng tiếu
cầu (như clopỉdogrel), thuốc trị tăng huyết ảp (như thuốc ức chế men chuyền, chẹn thụ thể
angiotensin, chẹn beta, ức chế kênh canxi, hydrochlorothiazide), thuốc giảm đau và kháng viếm
không steroid (như naproxen, diclofenac, celecoxib), thuốc trị trầm cảm (như bupropion,
fiuoxetine, sertraline), khảng histamỉne (như cetirỉzine), ửc chế bơm proton (như omeprazole,
!ansoprazole), và các thuốc trị rối loạn cương dương (như sildenaftl)
Diện tích dưới đường cong và trung binh nồng độ đinh của digoxin tăng nhẹ (AUC, ll% vả
Cmax, 18%) khi dùng cùng sitagliptin, mức độ tăng nảy không được xem lả có ý nghĩa lâm sảng.
4
_j\ỨỌỒ/
\\ .\ ẳ "~.ỉạ—ả /:Jl
Nên giảm sảt bệnh nhân đang dùng digoxin cho thỉch hợp. Không khuyến cáo điếu chĩnh liếư
digoxin hay JANUVIA
Khi cho đối tượng nảy uống một liều đơn JANUVIA 100 mg cùng với một liều đơn cyclosporin
600 mg, vốn lả chẳt ức chế mạnh p-glycoprotein, AUC vả Cmax của sitagliptin tảng xâp xi 29%
và 68 % Những thay đối năy trong dược động học của sitagliptin được xem không có ý nghĩa
ìâm sảng. Không khuyến cáo điếu chỉnh liếư JANUVIA khi dùng chung vởi cyclosporine hoặc
cảc chẳt ức chế p-glycoprotein khác (như ketoconazole).
TÁC DỤNG PHỤ
Tóm tắt về tính an toản cùa thuốc
Cảo tác dụng phụ nghìêm trọng bao gồm viêrn tụy và cảc phản ứng quá mẫn đã được báo cảo.
Hạ đường huyêt đã được báo cảo khi dùng kêt hợp với sưlphOnylurea (4,7%-13,8%) vả insulin
(9,6%) (xem THẶN TRỌNG).
Bảng liêt kê các tảo dung phu
Cảo tác đụng phụ được liệt kê dưới đây (Bảng 1) theo hệ cơ quan và tần suất Tần suất được xảo
định như sau: Rất thường gặp (> ƯIO); thường gặp (> 1/100 to < 1110); it gặp (>1/1,000 to <
1/100); hỉếm gặp (> ]/10, 000 to < 1/1,000); rât hiêm gặp (< 1/10 ,000) và chưa biết (không thế
tiên đoán được từ dữ liệu hiện có)
Bảng ]. Tẩu suất các tác dụng phụ được xảc định từ cảc nghiên cửu lãm sâng có đối chứng
placebo với sitagliptin đơn trị liệu và kinh nghiệm hậu măi
Tảo dụng phụ Tần suất tác dụng phụ
Rôi loạn hệ miễn dịch
Các phản ứng quá mẫn bao gổm phản ứng phản Chưa xảo định tần suất
vệ
Rối loạn chuyến hóa vả dinh dưỡng
Hạ đường huyếtjr ThƯỜỮE gặp
Rối Ioạn hệ thẩn kinh
Đau đầu Thường gặp
Rối loạn tiêu hóa
Tảo bón Thường gặp
Nônt Chưa xảo định tần suất
Viêm tụy cấpỰ ': Chưa xảo định tần suất
viêm tụy xuất huyết vả hoại tử gây tử vong và Chưa xác định tần suất
không gây tử vong
Rối loạn da và mô dưới da
Ngứa' ít gặp
_m4)
XV/
Ê
\\Ỹ
ln
Phù mạchtỈ Chưa xảo định tần suất
Phảt ban” Chưa xảc định tần Suất
Mảy đay'er Chưa xảc định tần suất
Viêm mao mạch*~* Chưa xác định tần suất
Cảc bệnh lý gây tróc da kể cả hội chửng Chưa xảc định tần suất
Stevens-Johnson'jf
Bóng nước pemphigoỉd' Chưa xác định tằn suất
Rối loạn cơ xương và mô liên kết
Đau khởp' Chưa xảo định tẩn SUấI
Đau cơ* Chưa xác định tằn suất
Đau lưng” Chưa xác định tẩn suất
Rối loạn thận và tiểt niệu
Suy thận cẳp’ Chưa xác định tần suất
'Tác dụng phụ được xảo định qua giám sảt hậu mãi.
" Xem Thận trọng.
² Xem nghiên cứu TECOS đánh giá tính an toản trên tim mạch bẽn dưới.
Mô tả môt số tảc dung phu chon lOc
Ngoài các tác dụng phụ liên quan đến thuốc được mô tả ở trên, cảc tác dụng phụ đã được béo
cảo bất kể mối quan hệ nhân quả với thuốc và xảy ra ở ít nhất 5% và nhiều hơn ở bệnh nhân
đang điếu trị với sitagliptin bao gôm nhiễm trùng đường hô hắp trên vả viêm mũi họng. Các tảc
dụng phụ bổ sung sau đây đã được bảo các bất kể môi quan hệ nhân quả với thưốc vả xảy ra
thường xuyên hơn ở bệnh nhân điếu trị với sitagliptin (dưới 5%, nhưng tỷ lệ xảy ra với
sitagliptin cao hơn 0,5% so với nhóm đối chửng) bao gôm viêm xương khớp vả đau ơ chì.
Một số tác dụng phụ được quan sát thấy thường xưyên hơn ở cảc nghiên cứu sử dụng sitagliptin
với các thuốc điều trị đái thảo đường khảo hơn so với các nghiên cửu sử dụng sitagliptin đơn trị
liệu. Bao gồm hạ đường huyết (tần suất rẩt thường gặp khi dùng kết họp với sulphonylurea vả
metformin), cúm (thường gặp khi dùng vởi insulin (có hoặc không có metformin), buồn nôn vả
nôn (thường gặp khi dùng với metformin), đầy hơi (thường gặp khi dùng với metforming hoặc
pioglitazone), táo bón (thường gặp khi dùng kết hợp với sulphonyiurea vả metfonnin), phù ngoại
biên (thường gặp khi dùng với pioglitazone hoặc phối hợp với pioglitazone vả metformin), vả
tìêu chảy (ít gặp khi dùng với metformin)
Nghiên cứu T ECOS đánh giá linh an toản lrên tim mạch
Nghiên cứu lâm sảng đánh giá tảc động của sítagliptin trên tim mạch (TECOS) tiến hảnh trên
7 332 bệnh nhân điều trị với sitagliptin, 100 mg mỗi ngảy (hoặc 50 mg môi ngảy nểu tốc độ lọc
cấu thận > 30 vả < 50 lephủt/1,73 m²), và 7. 339 bệnh nhân dùng placebo trong quần thể có ý
định điều trị. Cả hai trị liệu được thêm vảo chế độ chăm sóc thông thường nhằm kiểm soát mức
HIbAIc theo tìêu chuẩn khu vục vả cảc yếu tố nguy cơ trên tim mạch. Dân số nghiên cứu bao
gôm 2.004 bệnh nhân > 75 tuối (970 bệnh nhân điếu trị với JANUVIA và 1.034 bệnh nhân dùng
6
ffl4'V
\.“
giả dược). Tần suất các tảc dụng phu nghiêm trọng ở những bệnh nhân điểu trị với sitagliptin
tương tự như bệnh nhân dùng placebo Đánh giả về các biến chứng liên quan đến bệnh đái tháo
đường là tương đương giữa cảc nhóm bao gôm nhiễm trùng (18, 4% ở bệnh nhân điều trị với
JANUVIA và 17,7% ở bệnh nhân dùng giả dược), và suy thận (l, 4% ở bệnh nhân điếu trị với
JANUVIA và 1,5% ơ bệnh nhân dùng giả dược). Các tảo đụng phụ ở bệnh nhân > 75 tuổi nhìn
chung tương tự với toản bộ dân sô nghiên cứu.
Trong quần thể có ý định điếu trị, trong số những bệnh nhân đang sử dung insulin vả/hoặc một
sulfonyurea, tỷ lệ hạ đường huyết nặng là 2,7% ở bệnh nhân điểu trị với sitagliptin vả 2, 5% ở
bệnh nhân dùng placebo; trong sô các bệnh nhân đang không sử dụng insulin vả/hoặc một
sulfonylurea, tỷ lệ hạ đường huyết nặng lả 1 ,0% ởbệnh nhân điếu trị với sitagliptin và 0, 7% ở
bệnh nhân dùng placebo. Tần suất biến chứng viêm tụy đã được xảc nhận là 0, 3% ở bệnh nhân
điếu trị với sitagliptin và 0,2% ở bệnh nhân dùng placebo. Tần suất biến chứng khối u ác tính dã
được xảc nhận là 3, 7% ở bệnh nhân điều trị với JANUVIA vã 4, 0% ở bệnh nhãn đùng plac’ebo
THÔNG BÁO C_HO BÁC_ SỸ HOẶC qUợc SỸ NHỮNG TÁC DỰNG KHÔNG MONG
MUÔN GẶP PHAI KHI sư DỤNG THUOC.
Các phát hiện về xét nghỉệm
Tần suất các tác dụng bất lợi về kết quả xét nghiệm ở bệnh nhân dùng JANUVIA 100 mg tuong
tự ở bệnh nhân dùng placebo Trong cảc nghiên cứu lâm sảng chéo (across clinical studies),
lượng bạch cầu tăng nhẹ (khảc biệt xẩp xỉ 200 tế bảo bạch câu /microL so với placebo; lượng
bạch cầu trung bình ban đầu xâp xỉ 6 600 tế bảo/microL) đo tăng bạch cầu trung tính. Điếu nèy
được phảt hiện ở hầu hết nhưng không phải ở tất cả cảc nghiên cứu Sự thay đối cảc thông số xét
nghiệm nảy được xem không liên quan đến lâm sảng.
TÁC ĐỌNG CÙA THUỐC LÊN KHẢ NĂNG LÁ] XE vÀ VẶN HÀNH MÁY MÓC
Chưa thực hiện cảc nghiên cứu về tảo động của JANUVIA iẽn khả năng Iải xe vả vận hânh mảy
móc. Tuy nhiên, người ta cho rằng JANUVIA không ảnh hướng đến khả năng lải xe và vận hảnh
mảy móc.
DƯỢC LỰC HỌC
Cơ chế lác động
JANUVIA thuộc nhóm thuốc uống trị tăng đường huyết, gọi lả chất ức chế dipeptidyl peptidase
4 (DPP— 4) có tác dụng cải thiện đường huyết ở bệnh nhân đải thảo đường tỷp 2 bằng cách lảm
tăng nông độ các hormone incretin thể hoạt động Các hormone incretin bao gồm peptide giống
glucagon ] (glucagon—like peptide- ]: GLP-l) vả polypeptide kích thích tiết insulin và phụ thuộc
vảo glucose (glụcose- dependent ỉnsulinotropic polypeptide: GIP), được phóng thích từ ruột suốt
ngảy, vả tăng nông độ đảp ứng với bữa ăn. Các hormone incretin nảy lả thảnh phần của hệ thống
nội sinh tham gia vảo sự điểu hòa sinh lý tình trạng cân bằng nội môi glucose Khi nống độ
glucose binh thường hoặc tăng cao, GLP-I and GIP Iừm tăng sựtổng hợp và phóng thích insư1'm
tù cảc tế bảo beta tuyến tụy qua cảc đường truyền tín hiện nội bảo liên kết với AMP vòng.
Người ta dã chứng minh việc điếu trị với cảc chất ức chế GLP- ] hoặc với DPP- 4 cảc mô hình
động vật bị dải tháo đường tỷp 2 đã 1ảm cải thiện đáp ứng của tế bảo beta đối với giucose và
kích thích sinh tống hợp vả phóng thích insulin. Sự hấp thu và sử dụng glucose tại mỏ gia tăng
khi nổng độ insulin cao hơn. Ngoài ra, GLP- ] lảm giảm tiết glucagon từ tế bảo alpha tuyến tụy.
Nồng độ glucagon giảm cùng với nông dộ insulin cao hơn dẫn đến giảm sản xuất glucose tại
gan, gây giảm nông độ glucose trong máu. Các tảc dụng nảy của GLP- ] vả GIP phụ thuộc vảo
glucose, vì vậy khi nổng độ glucose trong mảu thẳp, sự kích thích phỏng thích insulin vả ức chế
7
W
/Ắ~ẳ²ẳN
tiết glucagon do GLP- ] không xảy ra. Đối với cả hai GLP— 1 và GIP, khi nồng độ glucose cao
hơn mức bình thường thì sự kích thích phóng thích insulin gia tăng. Hơn nữa, GLP 1 không 1ảm
suy giảm đáp ứng bình thường của glucagon đối với tinh trạng đường huyết thấp. Hoạt tính của
GLP—l vả GIP bị hạn chế bới enzyme DPP-4, đây là enzyme nhanh chóng thùy phân các
hormone incretin thảnh cảc chẩt không hoạt tính Sitagliptin ngăn ngừa DPP-4 thủy phân các
hormone incretin, do đó lảm tăng nổng độ cảc dạng hoạt tính cùa GLP- 1 vả GIP trong huyết
tương. Bằng cảch tăng nồng độ incretin dạng hoạt động, sitagliptin lảm tăng phóng thích insulin
vả giảm nông độ glucagon theo cảch thức phụ thuộc vâo glucose. Ở bệnh nhân đái thảo đuờng
tỷp 2 có tình trạng tăng đường huyết, sự thay đối nông độ insulin vả glucagon nảy dẫn đến giảm
nông độ hemoglobin A1c (HbAlc) và nông độ glucose lúc. đói vả sau khi ăn. Cơ chế phụ thuộc
vảo glucose nảy khảc biệt với cơ chế tảc dụng của cảc Sulfamid hạ đường huyết; cảc sulfamid hạ
đường huyết Iảm tăng tiết insulin ngay cả khi nồng độ glucose thẩp và có thể dẫn đến hạ đườn
huyết ở bệnh nhân đải thảo đường tỷp 2 và ở đối tượng binh thuờng. Sitagliptin lả ] chất ức chế
mạnh, chọn lọc cao trên enzyme DPP-4 vả không ức chế cảc enzyme liên quan gẳn lả DPP-8
hoặc DPP- 9 ở cảc nổng độ điếu trị.
Dược lực học
Tổng quát
ớ bệnh nhân đải tháo đường týp z, cảc liếu đơn JANUVIA dẫn đến ức chế hoạt tính của DPP-4
trong 24 giờ, gây tăng nồng độ GLP—l vả GIP thể hoạt động trong máu đển 2-3 lần, tăng nổng độ
insulin vả C—peptide trong huyết tương, giảm nồng độ glưcagon, giảm gìucose h'tc đỏi, vè giảm
dung nạp glucose sau khi uống glucose hoặc sau bữa ăn.
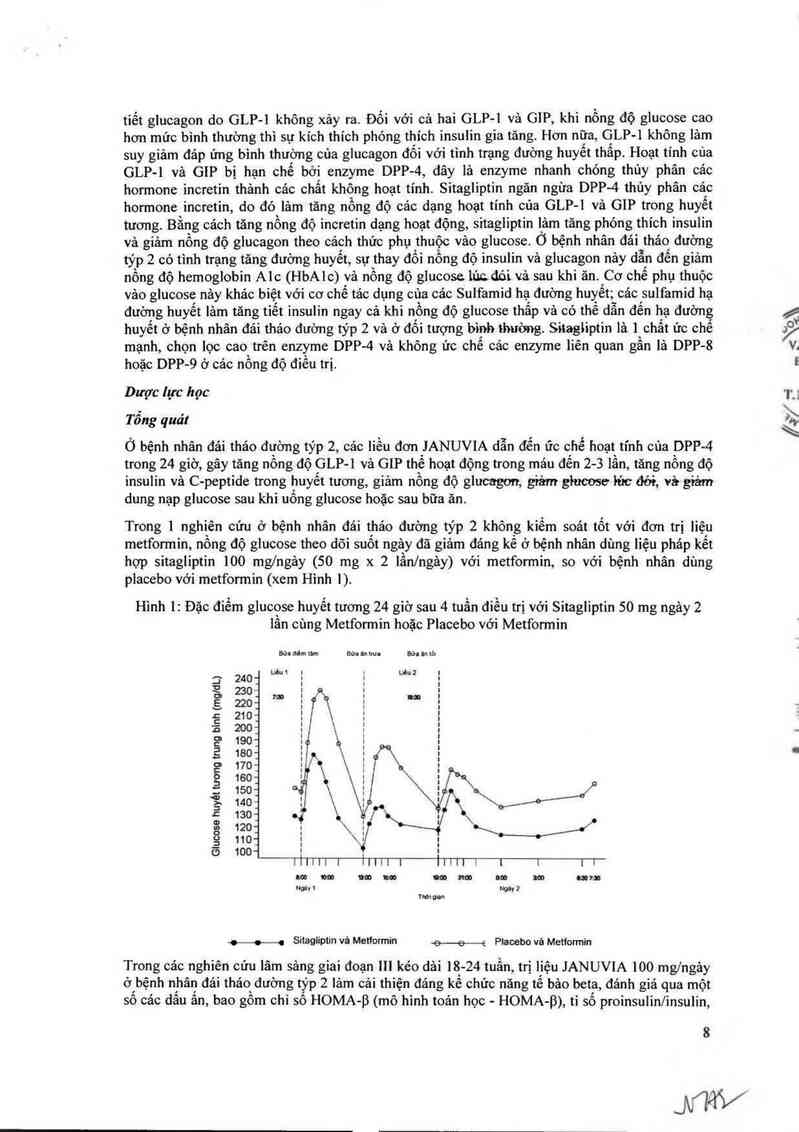
Trong ] nghiên cứu ở bệnh nhân đải thâo đường týp 2 không kiềm soát tốt với đơn trị liệu
metformin, nông độ glucose theo dõi suốt ngảy đã giảm đáng kể ở bệnh nhân dùng liệu phảp kết
hợp sitagliptin 100 mg/ngây (50 mg x 2 Iần/ngảy) với metformin, so với bệnh nhân dùng
placebo với metformin (xem Hình 1).
Hình 1: Đặc điềm glucose huyết tương 24 giờ sau 4 tuần điếu trị với Sitagliptin 50 mg ngây 2
lẩn cùng Metformin hoặc Placebo với Metformin
Bù: dlm um Bửu b tru: Bửu In tót
Glucose huyêt tương trung bình (mgldL)
f—-O—f Sitagliptin vả Metformin -e——e—e Ptacebo vả Mettonnin
'1`rong cảc nghiên cứu lâm sảng giai đoạn 111 kéo dải 18- 24 tuần, ttị liệu JANUVIA 100 mg/ngảy
ở bệnh nhân đái thảo đường typ 2 Iảm cải thiện đảng kề chức năng tế bảo beta, đánh giả qua một
số cảc dấu ản, bao gồm chi sô HOMA- -0 (mô hinh toản học- HOMA- B), tỉ số proinsulin/insulin,
8
_m4V
… .<"x"%\\
_j
//ấ/ ~ .
vả đảnh giả đáp ứng của tế bảo beta từ xét nghiệm dung nạp bữa ãn với mẫu máu lấy thường
xuyến.
Trong cảc nghỉên cứu giai đoạn II, hiệu lục gỉảm đường huyết không tăng thêm khi dùng
JANUVIA 50 mg ngảy 2 lần so với liều 100 mg ngảy ] lần.
Một nghiên cứu ngẫu nhiên, đối chứng placebo, mù đôi, mù dạng thuốc, nhóm bắt chéo 4 giai
đoạn ở cảc đối tượng người lớn khóe mạnh đã đảnh giả cảc tảc dụng lên nồng độ huyết tương
sau bữa an của GLP- l toản phần và GLP- ] thể hoạt động, cũng như nỗng độ glucose sau khi
uống sitagliptin kết hợp vởi metformin so với sau khi uông sitagliptin đơn độc, metformin đơn
độc, hoặc placebo trong 2 ngảy Sự gia tăng nổng độ trung bỉnh của GLP-l thể hoạt động do 4
gỉờ sau bữa an đã tăng gần 2 lần sau khi dùng hoặc sitagliptin đơn độc hoặc metformin đơn độc,
so với placebo Tảc dụng lên nồng dộ GLP- 1 thể hoạt động sau khi dùng sitagliptin cùng
metformin đã tăng cộng lực, với nông độ GLP-l thể hoạt động tăng xấp xỉ 4 lẫn so với dùng
placebo. Sitagliptin đơn trị liệu chỉ lảm tăng nồng độ GLP- ] thể hoạt động, phản ảnh sự ức chế
DPP-4, trong khi đó metformin đơn độc ]ảm tăng nồng độ GLP- l toản phần và thể hoạt động ở
mức độ như nhau. Các dữ liệu nảy phù hợp với những cơ chế khảc nhau vẽ sự gia tãng nông độ
GLP- 1 thể hoạt động. Kết quả từ nghiên cứu nảy cũng chứng mỉnh sitagliptin, chứ khỏng phải
metformin, lảm tăng nồng độ GIP thể hoạt động.
Trong các nghiên cứu ở đối tượng khỏe mạnh, JANUVIA không lảm giảm thấp đường huyết
hơn mức độ binh thường hoặc gây hạ đường huyết, điếu nảy gợi ý các tác động kích thích tiết
insulin vả ức chế glucagon cùa thuốc nảy hoản toản phụ thuộc vảo glucose.
Tác dụng lên huyểt áp
Trong một nghiên cứu ngẫu nhiên, đối chứng placebo, nhớm bắt chéo ở bệnh nhân tăng huyết ảp
đang dùng một hoặc nhỉều thuốc trị tăng huyết ảp (bao gồm cảc các thuốc ức chế men chuyến
angiotcnsin, thuốc đối khâng angỉotensin—il, ủc chế kênh canxin, chẹn beta và lợi tiểu),
JANUVIA dùng chung với cảc thuốc nảy thường dung nạp tốt. Ở cảc bệnh nhân nảy, JANUVIA
có tảc dụng giảm huyết ảp vừa phải; JANUVIA liếư 100 mgz'ngảy lảm gỉảm mức huyết' ap tâm
thu trung bình đo di động suốt 24 giờ đến gần 2 mmHg, khi so vởi placebo Tác đụng giảm
huyết’ ap nảy không xảy ra ở đối tượng có huyết' ap bỉnh thường.
Đìện Iỉm
Trong một nghỉên cứu ngẫu nhiên, đối chứng placebo, nhớm bắt chéo trên 79 đối tượng khóe
mạnh dùng một liếư đơn JANUVIA 100 mg, JANUVIA 800 mg (8 lẩn liếư khuyến cáo) và
placebo. Ó liếư khuyến cáo 100 mg, không xảy ra tảc động lến khoảng QTc khi thuốc đạt nông
độ đinh trong huyết tương, hoặc vảo bắt kỳ thời điếm khảo trong nghiến cửu. Sau khi dùng 1ỉều
800 mg, mức độ tăng tối đa về sự thay đối trung bình khoảng QTc hìệu chỉnh theo placebo so
vởi mức ban đầu sau 3 giờ uống thuốc lá 8, 0 msec Sự gia tăng nhỏ nảy không được xem có ý
nghĩa lâm sảng Ở lìều 800 mg, nồng độ đỉnh của sitagliptin huyết tương cao hơn gần 1 1 lần so
vởi nông độ đinh cứa liều 100 mg.
Ở bệnh nhân đái tháo đường týp 2 dùng JANUVIA 100 mg (N=8l) hoặc JANUVIA 200 mg
(N=63) mỗi ngảy, khoảng QTc thay đối không có ý nghĩa dựa theo dữ lỉệu ECG tại thời điểm
đạt nông độ đỉnh thường gặp trong huyết tương.
nƯợc ĐỘNG HỌC
Dược động học của sitagliptin dược nghiên cứu sâu rộng ở đối tượng khỏe mạnh và ở bệnh nhân
đái thảo đường tỷp 2. Ở dối tượng khỏe mạnh uống dùng ] liều 100 mg, sitagliptin được hấp thu
nhanh chóng đạt nồng dộ đỉnh trong huyết tương (trung vị Tmax) 1—4 giờ sau khi uống thuốc.
AUC cùa sitagliptin trong huyết tương gia tãng tường ứng theo ]ỉều dùng. Ở người tình nguyện
9
ffl®/
khỏe mạnh sau khi uống ] liếư đon 100 mg, AUC trung bình của sitagliptin trong huyết tương lả
8, 52 ụMơgiờ, Cmax là 950 nM, vả nứa đời thải trừ cuôi cùng bỉếu kiểu (tm) lả 12,4 gìờ AUC
cùa sitagliptin huyết tương tăng xấp xỉ 14% sau khi dùng cảc liều 100 mg ở trạng thải bến vững
so với dùng liều đầu tiên. Hệ sô tương quan về AUC của sitagliptin ơ từng đối tượng vả giữa cảc
đối tượng đều nhỏ (5, 8% so với 15,1%). Dược động học cùa sitagliptin nói chung đến giống
nhau' ơ đối tượng khỏe mạnh vả ở bệnh nhân đải thảo đường týp 2
Hẩp thu
Sinh khả dụng tuyệt đối của sitagliptin khoảng 87%. Do uống thuốc trong bữa an nhỉếu chẳt bẻo
không ảnh hướng đến tác động lên dược động học của JANUVIA dùng cùng 1ức, nên có thể
dùng JANUVIA cùng hoặc không cùng với thức an (lúc bụng no hoặc bụng đới)
Phân phổi
Thế tich phân phối trung bình ở trạng thải bến vững sau khi dùng 1 liếư đơn sỉtagliptin 100 mg
đường tĩnh mạch ở đối tượng khỏe mạnh thì khoảng 198 lít. Tỷ lệ sitagliptin găn kết thuận
nghịch với cảc protein huyết tương thì thẳp (3 8%).
Chuyển hóa
Sitagliptin được đảo thải chủ yếu trong nước tiểu ở dạng không thay đối vả một phẫn nhỏ qua
đường chuyến hóa. Gần 79% sitagliptin được thải trong nước tiếu ở dạng khõng thay đối.
Sau khi uống 1 liếư sỉtagliptin có đánh dẳu [ C], khoảng 16% chẳt có tinh phớng xạ lả cảc chẳt
chuyến hóa của sitagliptin. Sáu chắt chuyến hóa nảy được phát hiện ở nồng độ vết vả được cho
là không Iỉên quan đến hoạt tính ức chế DPP-4 huyết tương của sitagliptin. Nhũng nghỉên cứu in
vitro đã chứng minh enzyme chủ yếu chịu trảch nhiệm cho sự chuyến hóa hạn chế của sitagliptin
lả CYP3A4, với sự góp phần của CYP2C8.
Thải trừ
Sau khi cảc đối tượng khỏe mạnh uống 1 liếư sitagliptin [ C], khoảng 100% chất có tính phóng
xạ được thải trong phân (13%) hoặc nước tiếu (87%) trong 1 tuần dùng thuốc. Nửa đời thải trừ
cuối cùng biếu kiến sau khi uống ] liều sitagliptin 100 mg thì xẳp xỉ 12, 4 giờ vả sự thanh thải
qua thận khoảng 350 mL/phút.
Sitagliptin được đảo thải chủ yếu qua thận với sự bải tiết chủ động qua ống thận. Sitagliptin là 1
chất nên đối với chắt chuyên chở anion hữu cơ 3 ở người (human organic anion transporter-3:
hOAT- -,3) vốn lả chẳt có thể tham gia vảo sự thải trừ sitagliptin qua thận. Vẫn chưa xác định
được sự liên quan lâm sảng cùa hOAT-3 trong vận chuyến sitagliptin. Sitagliptin cũng lả ! chắt
nền cùa p- glycoprotein, mả chất nảy cũng có thể tham gia vảo quá trình đảo thải sitagliptin qua.
thận. Tuy nhiên, cyclosporìne, một chất ức chế p—glycoprotein khỏng ]ảm gìảm sự thanh thải
sitagliptin qua thặn.
Các đặc !z'nh ở bệnh nhân
Suy thận: Một nghỉên cứu mở liếư đơn, nghiên cứu mở được tiến hảnh để đánh giá dược động
học của JANUVIA (liếư 50 mg) ở các bệnh nhân suy thận mãn tính với các mửc độ khác nhau so
với đối tượng khỏe mạnh, chức nãng thặn bình thường ở nhóm chứng. Nghiên cứu nảy gồm các
bệnh nhân phân loại suy thận phân theo dựa vảo hệ số thanh thải creatỉnỉne: nhẹ (50- <80
lephủt), trung bình (30- <50 mL/phút) vả nặng (<30 mL/phủt), cũng như các bệnh nhân có
bệnh thận giai đoạn cuôi đang được thẳm phân mảu. Hệ sỏ thanh thải creatinine được đo qua sự
thanh thải creatinine trong nước tỉếu 24 giờ hoặc được tính từ nồng độ creatinine hưyết thanh
theo cỏng thức Cockcroft-Gault:
10
MW
[140 - tuổi (năm)] x thể trọng (kg) {x 0,85 đối với bệnh nhãn nữ}
CrCl =
[72 x creatininc huyết thanh (mg/dL)]
Bệnh nhân suy thận nhẹ không tăng nồng độ sìtagliptin huyết tuơng có ý nghĩa lâm sảng, so với
đối tượng khóe mạnh, bình thường ở nhóm chưng. AUC của sitagliptin huyết tương đã tăng
khoảng 2 lần ở bệnh nhân suy thặn trung bình, và tăng khoảng 4 lần ở bệnh nhân suy thặn nặng
và ở bệnh nhân có bệnh thận giai đoạn cuối đang được thấm phân mảư, khi so với đối tượng
khóe mạnh, bình thường ở nhóm chứng Sitagliptin được loại bỏ vừa phải qua thẩm phân máu
(13,5% sau 3-4 giờ thẩm phân mảu, bắt đầu thẳm phân sau khi uống thuốc được 4 giờ). Để đạt
nông độ sitagliptin trong huyết tương tương tự như ở bệnh nhân có chức năng thận bình thường,
nên dùng liếư thấp hơn ở bệnh nhân suy thận trung bình và nặng, cũng như 0 cảc bệnh nhân có
bệnh thận giai đoạn cuối cần thẳm phân mảu (xem LIÊU LƯỢNG VÀ CÁCH DÙNG, Bệnh
nhản suy thận).
Suy gan: Ở bệnh nhân suy gan trung bình (điếm số Chìld-Pugh 7 - 9), giá trị trung bình AUC
vả Cmax của sitagliptin tãng, lần lượt, khoảng 21% và 13%, so với các nhỏm chứng tương ứng
khỏe mạnh sau khi dùng 1 liếư đơn JANUVIA lOOmg. Cảo khảo biệt nảy được xem không có ý
nghĩa lâm sảng. Không cần chỉnh liếư JANUVIA đối với bệnh nhân suy gan nhẹ hoặc trung
bình.
Không có kinh nghiệm lâm sảng ở bệnh nhân bị suy gan nặng (điếm số Child-Pugh > 9). Tuy
nhiên, vì sitagliptin chủ yêu được đảo thải qua thận, nên theo đự đoản sưy gan ưặrrg không tác
động lên dược động học cùa sìtagliptin.
Người cao tuổi: Không cần chỉnh liếu theo tuổi. Tuổi tảo không gây tác động oó ý nghĩa lâm
sảng lẽn dược động học cùa sìtagliptin dựa theo 1 phân tích dược động học theo dãn sô tứ dữ
lìệu giai đoạn I và giai đoạn 11. Đối tượng cao tuôì (65- 80 tuổi) có nông độ sìtagliptỉn huyết
tương cao hơn 19% so với đối tượng trẻ tuôi hơn.
Trẻ em: Chưa có nghỉên cứu JANUVIA tiến hảnh ở trẻ em.
Giới tính: Không cẩn chĩnh lỉều theo giới tỉnh. Gìới tính khộng gây tảc động có ý nghia lâm
sảng lên dược động học của sitagliptin dựa theo 1 phântích tông hợp từ các dữ liệu duợc động
học giai đoạn ] vả theo 1 phân tich dược động học dân sô từ dữ liệu lâm sảng gíaĩ đoạn lvả II.
Chủng tộc: Không cần chỉnh liếư theo chùng tộc. Chùng tộc không gây tảo động có ý nghĩa
lâm sảng lên dược động hợc cùa sitagliptin dụa theo 1 phân tỉch tổng hợp từ các dữ liệu dược
động học giai đoạn I vả theo 1 phân tích dược động học dân số từ dữ lỉệu lâm sảng giai đoạn I
và H, bao gôm các đối tượng người da trắng, Tây Ban Nha, da đen, da vâng Châu Á và cảc
nhóm chùng tộc khảo.
Chỉ số khổi cơ thể (BMI): Không cần chĩnh liếư theo BMI. Chỉ số khối cơ thể không gây tác
động có ý nghĩa lâm sảng lên dược động học cũa sitagliptin dựa theo 1 phân tich tống hợp từ
cảc dữ liệu dược động học gìaỉ đoạn I vả theo ] phân tỉch dược động học dân số từ dữ lỉệu lâm
sảng giai đoạn I vả II.
Đải thảo đường týp 2: Dược động hợc của sitagliptin ở bệnh nhân đải thảo đường tỷp 2 thường
tương tự như ở đỏỉ tượng khỏe mạnh.
SỬ DỤNG QUÁ LIÊU
Trong những thử nghiệm lâm sảng có đối chứng người khóc mạnh, JANUVIA liếư đơn đến 800
mg được dung nạp tốt. Trong một nghiên cứu dùng liếư 800 mg JANUVIA, khoảng QTc tăng rắt
ỉt vẻ không liên quan đến lâm sảng (xem DUỢC LÂM SÀNG, Dược lực học, Điện lim). Chua
Il
Jvflđ’ẵ/
L ổ Íf/Í
`xỀn\l : '
có kinh nghiệm`sứ dụng cảc liếư cao hơn 800 mg ở người. Trong các nghiên cứu giai đoạn 1 về
chế độnhiếu liêu trong ngảy, người 'ta không tim thẩy các phản ứng bât lợi trên lâm sảng liên
quan đên liêu khi dùng JANUVIA đên liêu 600 mg/ngảy trong 10 ngảy vả 400 mg/ngảy đên 28
ngảy.
Trong trường hợp quá liếư, nên ảp dụng các biện phảp hỗ trợ thường dùng, như loại bỏ chất chưa
kịp hâp thu khội đường tiêu hóa, theo dõi trên lâm sảng (bao gôm lâm đỉện tâm đổ) vả trị liệu
nâng đỡ, nếu cân.
Sitagliptin có thể được thẩm'tách vừa phải. Trong nghiên cứuỌlâm sảng, khoảng 13,5% liếư dùng
được loại bỏ sau 3-4 giờ thâm phân_mảu. Có thế xem xét thêm phân máu kéo dải nêu phù hợp
trên lâm sâng. Vẫn chưa biêt rõ thâm phân phúc mạc oó thê thâm tách được sitagliptin hay
không.
BẢO QUẢN
Bảo quản ở nhiệt độ dưới 30°C (86°F).
HẠN DÙNG
36 tháng kế từ ngảy sản xuất.
DẠNG TRÌNH BÀY
JANUVIA 25 mg: Hộp 2 vì x 14 viên nén bao phim.
JANUVIA 50 mg: Hộp 2 vì x 14 viên nén bao phim.
JANUVIA 100 mg: Hộp 2 ví x 14 viên nén bao phim.
THUỘC NÀY cní DÙNG THEQ ĐON CỦA BÁC sỹ. ĐỌC Kỹ HƯỘNG DÃN sử DỤNG
T1ịƯOQ KHI punẹ, NỊGAYẦCA Klj1 BẠN ĐÃ DUNG mụoc NAY THEO ĐON CÙA
BAC sv TRƯOC ĐO. NEU CAN THEM THONG TIN, XIN HOI Y KIẺN BÁC SỸ.
XIN LƯU Ý RĂNG TỤUÔC NÀY Đ_ƯỌC cni ĐỊNH CHO_ CẢ N11ÂN BAN. KHÔNG
ĐƯỢC ĐƯA THUỘC NAY CHO NGƯOI KHAC sư DỤNG. ĐE XA TAM TAY TRẺ EM.
Sản xuất bởi:
Merck Sharp & Dohme Limited
Shotton Lane, Cramlington, Northumberland, NE23 3.1 U, United Kingdom (Anh)
TUQ. C_ỤC TRUỘNG
P.TRUỜNG PHONG
Jiỷayễn Jẳty Jfểìnẵ
12
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng