




























Label size:60x24m m ,.ịf 1 _)
colorzlP1szc IP2685c IK ịẹ ' \
i . ;... ,,m
llsọtera _Ễẫ …ỂWỆ
…ẹgẵẺ ²ỆỄ…Ệ…L.ẸnãẸ
azermm M
32...—
; =s
Ị"'Lz. '_ẸP“ u—n—
_ _Iờl __
1…âw oz amiuaẻuoa
. JĐJO lI
BOX suze: 82x53x50mm
color:lP152c IP2685c IK ; "H
. vỡ
ợ’ R .lmzư cmzn
K . .`: _ `… lsotera Rx Thuỏc bán tth dơn :Bẫm'ịơvn: lmlseetiẵcnotm mmm
ISOTERA lNJECTION CONCENTRATE 2DMGIML 21 um CNUỦ m D exd 2ung)
so e ra lnicction Concutrzle 20 mglnư om du … … … u… mb … …… -Rem d Ammmẵm; mmmiẵiuễcziẵ
' ' Dooetuel trih rlte . . ~Stonnu Common … bdow '
ỈII ectnon COI'ICGI'IỪỦG 20 mg/mL ( yd ) :ẵ'iẵhiiẵllinẵmẩệẵẵ'x'ẵi'iiiizmm'M u…u «… nuomu .: Smm … h on'ơml pm:qu in … to
cm M ua lun.. oh; alalnh … Ion |mng nn…l ulu … nunl. pm mm lith
IỒIB BK.NSI.ND ln… 'Itho '. 'MIIIIIÝIHqu Euto', `Elullilll nut
MI IDODI
Dooetaxel trihydraie lll| l|l ã“.ĩfflỉỉĩẩiỉềĩẵỉểầíồỉẫiầìĩffl…
l5'll Ị 91. NMobnnll' nnmumnmnmuulcu un nu ou nmụ u.,hmll
lìlhll DII Tdhm CIy WIMI {R D 60
lưnm lMu cunmunuạmmvtmw-mnlnhmon.
A #::ứnz: mmmnw=……
20mg/ 1mL …… ủimmg cumhnụnlhkdnghlunu ungúhưnngslnnbiun gmmn unm…ũiih
lỰHÙIM uon _u unnu _. —nnn
ngp u81
d ya
…...J. .../…n
QC! ẸIH
OOHCI A1 NVHÒ ofta
ỌEI
_ẸLẢ
.LỆẮ
LỄ/m l;
Osmm
R. Thuốc bản theo đơn
lsotera Injection Conccntrate 20 mglml
El HOẠT CIIÁT
Mỗi ml chứa:
Docctaxcl trihydrat .............................. 21,34 mg
(tương dương với Docctaxct ....................... 20 mg)
Cl HÀM LƯỢNG
Mỗi lọ 1 ml chứa 21,34 mg docctaxel trihydrat tương đương với 20 mg docctaxel.
[ a dươc. Polysorbat 80, Ethanol tuyệt đối 395,0 mg, Acid hydrochloric.
Mỗi lọ 4 ml chửa 85,35 mg docctaxcl trihydrat tương đương với 80 mg docctaxcl.
Tá dươc: Polysorbat 80, Ethanol tuyệt dối 1580,0 mg, Acid hydrochloric
Cl MÔ TẢ
Docctaxel là một thuốc chống ung thư thuộc họ taxoid, dược bảo chế bằng phương phảp
bản tổng hợp bắt đầu bằng một tiền chất chiết xuất từ sinh khối kim tải tạo của cây thủy
tùng. Tên hóa học của docetaxcl lả (2R, 3S)—N- carboxy-3— phenylisoserine, N-tert- -butyl
ester, l3-cstcr with 5]? —- 20 — epoxy - l, 2ơ., 4, 713, 10,6, l3a - hexahydroxytax -l l-en—9-
one 4—acetatc 2—bcnzoatc, trihydrat.
Docetaxcl có công thức cấu tạo như sau:
Docctaxcl iả bột mảu trắng dến gần như trắng với công thức tối giản lả C43H53N014° 3H20
vả trỌng lượng phân từ 861, 9. Docctaxcl rất ưa mỡ và thực tế không tan trong nước.
Isotcra Injection Concentratc là một dung dịch nhớt trong suốt, mảu vảng nhạt đến hoi nâu
vảng. Lọ đơn liều vô khuần, không gây sốt, chứa 20 mg ( 1 ml) hoặc 80 mg (4 ml) docetaxel
(khan)
Mỗi ml chứa 20 mg docetaxcl (khan) trong 0,54 g polysorbat 80 và 0,395 g dung dịch cổn
khử nước.
/,
Íĩ
ti
.1 i
v`ẵ
El CHỈ DỊNH (dược sử dụng bời bảo sĩ)
Ung thư vú . Ung thư phổi không tế bảo nhỏ . Ung thư tuyển tỉền liệt , Ung thư bỉếu mô
tuyến dạ dảy vả Ung thư dầu vả cô.
[Ung thư vú]
`fJ
Docctaxcl kết hợp với doxorubicin vả cyclophosphamid dược chi dịnh để điểu trị bổ trợ
cho bệnh nhân bị ung thư vú có hạch bạch huyết dương tính có thề phẫu thuật và bệnh nhân
bị ung thư vú có hạch bạch huyết am tính có thế phẫu thuật. Đối với những bệnh nhân bị
ung thư vú có hạch bạch huyết am tính có thế phẫu thuật, điều trị bổ trợ nên được giới hạn
chỉ ở những bệnh nhân dù diều kiện dề dược dùng hóa trị liệu theo các tiêu chuẩn quõc tế
dược xảc định đề diều trị ban đầu ung thư vú giai đoạn sớm.
Docctaxei kết hợp với doxorubicin được chỉ định đề diều trị bệnh nhân bị ung thư vú tiến
triến tại chỗ hoặc di căn trước dây chưa dược dùng liệu phảp gây độc tế bảo dối với tình
trạng nảy.
> Docctaxcl đơn trị liệu dược chỉ định để điền trị bệnh nhân bị ung thư vú tiến triến hoặc di
căn sau khi thât bại với liệu phảp gây dộc tế bảo.
> Docctaxcl _kết hợp với trastuzumab dược chỉ định dế diều trị bệnh nhân bị ung thư vú di
cản mả khôi u có biêu hiện quá mức HER2 và những người trước đây chưa được dùng hóa
trị liệu dôi với bệnh di căn.
› Docctaxcl kết hợp với capccitabin dược chỉ dịnh dể diều trị bệnh nhân bị ung thư vú tiến
triên hoặc di căn sau khi thất bại vởi hóa trị liệu gây dộc tế bảo. Điêu trị trước dó nên bao
gôm một anthracyclin.
[Ung thư phổi không tế bảo nhòl (Di
/
› Docetaxel được chỉ định dễ điều trị bệnh nhân bị ung thư phổi không tế bảo nhỏ tiến triến
tại chỗ hoặc di căn sau khi thất bại với hỏa trị líệu trưởc đó.
Docctaxcl kết hợp với cisplatin dược chi dịnh để diều trị bệnh nhân bị ung thư phồi không
tế bảo nhỏ tiến triến tại chỗ hoặc di căn không thể cắt bỏ, ở những bệnh nhân trước đây
chưa được dùng hóa trị liệu cho tình trạng nảy. Docctaxcl kết họp vói carboplatin dại diện
cho một lựa chọn diều trị đối với trị liệu dựa trên cisplatin.
[Ung thư tuyến tiền liệt]
> Docctaxcl kết hợp với prcdnison hoặc prednisolon dược chi dịnh để điều trị bệnh nhân bị
ung thư tuyến tiển iiệt di căn kháng trị với hormon.
{Ung thư biếu mô tuyến dạ dảyl
» Docctaxcl kết hợp với cisplatin vả 5-fìuorouracil dược chi dịnh dế diều trị bệnh nhân ung
thư bìều mô tuyến dạ dảy dì căn, bao gồm cả ung thư biều mô tuyến của chỗ nối dạ dảy-
thực quán là những người chưa dược dùng hóa trị liệu trước đó đối với bệnh di căn.
[Ung thư đầu và cổ]
> Docctaxel kết hợp với cisplatin vả 5- Huorouracil được chỉ định để điều trị ban đầu cho đối
với bệnh nhân ung thư biêu mô tế bảo vảy đầu và cổ tiến triến tại chỗ
D LIÊU LƯỢNG VÀ CÁCH DÙNG (được sử dụng bởi bảo sĩ)
Việc sử dụng docctaxel nên được giới hạn chỉ ở các đơn vị chuyên sử dụng hóa trị liệu gây
dộc tế bảo vả nó chỉ nên dược dùng dưới sự gìám sát cùa một bác sĩ có trình độ trong việc
sử dụng hóa trị liệu chông ung thư.
KLiều khuyến cáo]
)— Đối vởi ung thư vú, ung thư phổi không tế bảo nhỏ, ung thư dạ dảy, ung thư dầu và cổ,
thuốc chuẩn bị trước gôm một corticosteroid đường uỏng, như dexamethason 16 mglngảy
(ví dụ 8 mg, 2 lần/ngảy) trong 3 ngảy, bắt đầu trước khi dùng docetaxel [ ngảy, trừ khi bị
chống chỉ dịnh, có thế sử dụng yêu tố kích thích dòng bạch câu hạt (G- CSF) dự phòng để
lâm giảm nguy cơ độc tính vô huyết học. Đối với ung thư tuyến tiến liệt, nêu sử dụng dồng
thời prednison hoặc prednisoion, chế độ dùng thuốc chuẩn bị trước được khuyến cáo là
dcxamcthason 8 mg, uống l2 giờ, 3 giờ và 1 giờ trước khi truyền docetaxcl.
`» Docctaxcl dược sử dụng truyền ] giờ mỗi 3 tuần. (D1
[Ung thư vú] '
> Trong dỉếu trị bổ trợ ung thư vú có hạch bạch huyết dương tinh có thế phẫu thuật và ung
thư vú có hạch bạch huyết am tinh có thế phẫu thuật, liếư khuyến cáo của docetaxel lả 75
mg/m2 dùng 1 giờ sau khi dùng doxorubicin 50 mg/m2 vả cyclophosphamid 500 mglm2
mỗi 3 tuần trong 6 chu kỳ (xem thêm Điều chỉnh liếư trong khi điều trị). Đối vởi việc diếu
trị bệnh nhân bị ung thư vú tiến triển tại chỗ hoặc di căn, liều khuyến cáo của docetaxel lả
IOO mg/m2 duới dạng dơn trị liệu. Trong điều trị dầu tay, docetaxel 75 mg/m2 dược dùng
trong liệu phảp kết hợp với doxorubicin (SO mg/m2).
>> Khi kết hợp với trastuzumab, líồu khuyến cáo cùa docetaxel là 100 mg/m2 mỗi 3 tuần, với
trastuzumab dùng hảng tuần "lrong một nghiên cứu then chốt, việc truyền lìểu docetaxcl
khời dầu dược bắt đầu vảo ngảy sau liếư trastuzumab đầu tiên. Cảc lỉều docetaxel tiếp theo
dược truyền tĩnh mạch ngay sau khi hoản thảnh việc truyền trastuzumab, nêu liếư
trastuzumab trưởo dó dược dung nạp tốt. Về liếư lượng và cách dùng trastuzumab, xem tóm
tắt đặc tính sản phầm cùa trastuzumab.
> Khi kết hợp với capccitabin, liếư khuyến cảo của docetaxel là 75 mg/m2 mỗi 3 tuần, kết
họp với capccitabin ở liếư 1250 mgm2, 2 lần/ngảy (trong` vòng 30 phút sau bữa ãn) trong
2 tuần, tiếp theo là một khoảng thời gian nghỉ 1 tuần. Về cách tính iiều capecỉtabin theo
diện tích bề mặt cơ thế, xem tóm tắt đặc tinh sản phấm của capecitabin.
IUng thư phổi không tế bảo nhỏ]
> Ở những bệnh nhân chưa tùng được dùng hóa trị liệu điều trị ung thư phối không tế bảo
nhỏ (NSCLC), chế dộ liếư dùng khuyến cáo là docctaxel 75 mg/m2, tíếp theo ngay sau đó
lả cisplatỉn 75 mglm2 trong 30- 60 phủt. Đối vởi điều trị sau khi thất bại với hóa trị liệu dựa
trên platin trước đó, iiều khuyến cảo là 75 ngm² dưới dạng thuốc đơn độc.
[Ung thư tuyến tiến liệt]
> Liều khuyến cảo của Docetaxel lả 75 mglm². Prednispn hoặc prednisolon 5 mg, 2 lầnlngảy
dường uỏng dược dùng liên tục. (Xem CAC ĐẶC TINH DƯỢC LỰC HỌC)
[Ung thư biếu mô tuyến dạ dảy]
)— Liều khuyến cảo cùa docctaxcl là 75 mg/m2 truyền trong 1 giờ, tiếp theo lá cispiatin 75
ngm², truyền từ 1—3 gỉờ (cả hai thuốc chỉ dùng vảo ngây thứ nhất), sau đó lả s-
tìuorouracil 750 mglm²lngảy dược dùng truyền liên tục trong 24 giờtrong 5 ngảy, bắt đầu
vảo iúc kết thúc truyền cisplatin. [ ặp lại điều trị mỗi 3 tuần. Bệnh nhân phải được dùng
thuốc chuẩn bị trước bắng thuốc chống nôn vả bù nước thích hợp để dùng cisplatin. Điếu
trị dự phòng bằng G- CSF nên dược sử dụng để lảm giảm nguy cơ độc tinh vê huyết học.
(Xem DlẺU CHỈNH LIẺU TRONG KHI ĐIÊU TRỊ)
[Ung thư dầu và cổ]
› Bệnh nhân phải được dùng thuốc chuẩn bị trước bằng thuốc chống nôn và bù nước thích
hợp (trước và sau khi dùng cisplatin). Điều trị dự phòng bằng G-CSF nên được sử dụng để
lâm giảm nguy cơ dộc tính về huyết học. Tất cả các bệnh nhân ở nhóm dùng docetaxel
trong cảc nghiên cứu 'I`AX 323 vả TAX 324 đều được dùng kháng sinh dự phòng.
1. Hóa trị liệu ban đầu, tiếp theo lá xạ trị (TAX 323) Ơị1
Về diếu trị ban dầu dối vởi ung thư biếu mô tế bâo vảy dầu và cố tìến triến tại chỗ (SCCHN)
không thế phẫu thuật, liếư khuyến cảo của docetaxel là 75 mg/m2 truyền trong 1 giờ, tiểp
theo lá cisplatỉn 75 mg/m2 trong 1 giờ, vảo ngảy thứ nhất, sau đó là 5- f1uorouracil truyền
liên tục ở liều 750 mg/mzlngảy trong 5 ngảy. Chế độ điếu trị nảy được sử dụng mỗi 3 tuần
trong 4 chu kỳ. Sau hóa trị liệu, bệnh nhân nên được xạ trị.
2. Hóa trị lỉệu ban đầu, tiếp theo lá hóa xạ trị liệu (TAX 324)
Về điếu trị ban đẩu đối vói bệnh nhân bị ung thư biếu mô tế bảo vảy đầu vả cổ tiến triển
tại chỗ (SCCI IN) (về kỹ thuật không thể cắt bò, xác suất chữa khỏi bằng phẫu thuật thấp
và nhằm mục đích bảo tồn cơ quan), liếu khuyến cáo cùa docetaxel là 75 mg/m2 truyền
tĩnh mạch trong ] gíờ vảo ngảy thứ nhắt, tiếp theo lá cisplatin 100 mg/m2 truyền trong 30
phút dến 3 giờ, sau đó lả 5- Huorouracil 1000 mglm²lngảy truyền liên tục từ ngây thứ nhất
đến ngảy thứ 4. Chế dộ điều trị nảy được sử dụng mỗi 3 tuần trong 3 chu kỳ. Sau hóa trị
liệu, bệnh nhân nên được dùng hóa xạ trị liệu.
Về vìệc diều chinh liếư cisplatin vả 5-fluorouracil, xem tỏm tắt đặc tính sản phẩm tương ứng.
0 DIỀU CHỈNH LIÊU TRONG KHI ĐIỀU TRỊ
[Chung]
"» Nên dùng Docctaxel khi số Iưọng bạch cẩu trung tính 2 I.500 tế bảo/mmẵ
JJ.\Ỉ "
uOl
> Ở những bệnh nhân bị giảm bạch cầu trung tính có sốt, số lượng bạch cẩu trung tính < 500
tế bảo/mm3 trong hơn một tuần, cảc phản ứng da nặng hoặc phản ứng da tich lũy hoặc bệnh
thần kinh ngoại biên nặng trong khi điều trị bằng docctaxel nên giảm liều docetaxel từ 100
mglm2 xuống 75 mglm2 vâ/hoặc 75 mg/m² xuông 60 mg/m². Nếu bệnh nhân tiếp tục gặp
cảc phản ứng ở liều 60 mg/m² nến ngừng điều trị.
[Các nhóm bệnh nhân đặc biệt]
? Bệnh nhân suy gan
Dựa trẽn các dữ liệu dược dộng học với docetaxel 100 mg/m² dưới dạng thuốc đơn độc, đối
với những bệnh nhân có tảng cả transaminase (ALT vảlhoặc AST) lớn hơn 1,5 lân giới hợn
trên cùa mức binh thường (U I.N) vả phosphatase kiềm lớn hơn 2,5 lằn ULN, liều khuyên
cáo của docctaxcl là 75 ngm² (xem CÁNH BẢO VÀ THẬN TRỌNG ĐẶC BIỆT KHI
SỬ DỤNG). Dối với nhũng bệnh nhân có nồng độ bilirubin huyết thanh › ULN vảfhoặc
ALT vả AST › 3,5 lần ULN kết hợp với nồng dộ phosphatase kiềm › 6 lần ULN, không
khuyến cáo gỉảm lỉếu và không nên sử dụng docetaxel trừ khi có chi dịnh nghiêm ngặt.
> Kết hợp với cisplatin vả 5-fluorouracil trong điếu trị bệnh nhân bị ung thư biếu mô tuyến
dạ dây.
Nghiên cứu lâm sảng then chốt đã Ioại trừ những bệnh nhân có ALT vả/hoặc AST > 1,5
iần ULN kết hợp với phosphatasc kiềm > 2,5 lần ULN, vả bilirubin > ] lần ULN; dối với
những bệnh nhân nảy, không khuyến cảo giảm liều và không nên sử dụng docetaxel trừ khi
được chỉ định nghiêm ngặt. Không có dữ liệu ở những bệnh nhân suy gan được điểu trị
bằng docctaxcl kết hợp trong cảc chỉ định khảo.
> Nhóm bệnh nhân trẻ em ĨDJ
'
! . Dộ an toản và hiệu quả của docctaxcl trong ung thư biều mô mũi họng ở trẻ em từ 1 thảng
đên dưới 18 tuôi chưa được xác dịnh.
2. Không có sử dụng thich hợp cùa docetaxel ở nhóm bệnh nhân trẻ em trong cảc chỉ định
ung thư vú, ung thư phổi không tế bảo nhỏ, ung thư tuyến tiến liệt ung thư biểu mô dạ dảy =;
vả ung thư dầu và cô, không bao gồm ung thư biều mô mũi họng type Il vả III ít biệt hóa "
0
> Người cao tuối Ẹ
l. Dựa trện phân tích dược động học quần thế, không có hướng dẫn sử dụng dặc biệt ở người p
cao tuôi. _
2
2. Dối với bệnh nhân từ 60 tuồi trở lên, khi kết hợp với capecitabin, khuyến cảo giảm liếư
khởi dâu cùa capecitabin còn 75%. (Xem tóm tăt đặc tính sản phâm cùa capecitabin)
[Điếu trị bổ trợ dối với Ung thư với
Nên nem xét đìếu trị dự phòng ban đầu bằng G—CSF ớ những bệnh nhân dược đỉếu trị bổ
trợ băng docctaxcl, doxorubicin vả cyclophosphamid (DAC) đối với bệnh ung thư vú.
Nhũng bệnh nhân bị giảm bạch cầu trung tính có sốt vảlhoặc nhiễm trùng giảm bạch cầu
trung tính nên dược iảm liếư docctach xuống còn 60 ngm² trong tất cả các chu kỳ sau
đó (xem CẢNH BAO VÀ T HẬN TRỌNG DẶC BIỆT KHI SỬ DỤNG vả TẢC
DỤNG Ki IÔNG MONG MUÔN). Những bệnh nhân bị viêm miệng độ 3 hoặc 4 nên được
giảm liều còn 60 mglm².
Kết hợp vởi cisplatin
Đối với nhũng bệnh nhân dược dùng thuốc khới đầu với liều docetaxel 75 mglm² kết h p
với cisplatin vả những bộnh nhân có số lượng tiếu cầu ở mức thấp nhất trong liệu trình đieu
trị trước đó là < 25. 000 tế bảolmm3 hoặc ở những bệnh nhân đã bị giảm bạch cầu trung tính
có sốt, hoặc ở những bệnh nhân bị nhiễm độc nghiêm trợng không phái vế huyết học, nên
giảm Iỉếu docctach trong chu kỳ tiểp theo còn 65 mg/m². Về việc điếu chỉnh lỉều cisplatin,
xem tóm tắt đặc tính sản phẩm tương ứng.
Kết hợp với capecitabin
Về việc diều chinh liếư capecitabin, xem tóm tắt đặc tinh sản phấm của capecitabin.
Đối với những bệnh nhân phát sinh biếu hiện dầu tiên cùa độc tính độ 2 kéo dải tại thời
diếm điều trị tiếp theo bằng docctaxcllcapccitabin, trì hoãn điếu trị cho đến khi được giải
quyết về dộ 0- 1 và diếu trị trở lại ở mức 100% cùa liều ban dầu.
. Đối với những bệnh nhân phát sinh biếu hỉện thứ hai của; độc tính độ 2 hoặc biếu hiện đầu
tiên của dộc tinh độ 3 vâo bât ky lủc nảo trong chu kỳ điêu trị, trì hoãn điêu trị cho đên khi
được giải quyêt vê dộ 0-1 và diêu trị trở lại bãng docctaer 55 mg/m².
. Đối với bất kỳ biều hiện cùa độc tính tiếp theo nảo hoặc bất kỳ độc tinh độ 4 nảo, ngừng
liếư docctaxcl.
Kết hợp với trastuzumab ffl1
;
Về việc diếu chinh liều trastuzumab, xem tóm tắt đặc tinh sản phẩm cùa trastuzumab.
Kết hợp vói cisplatin vả 5-i`luorouracil
Nếu một giai doạn giảm bạch cầu trung tính có sốt, giảm bạch cầu trung tính kéo dải hoặc
nhiễm trùng giảm bạch cầu trung tính xảy ra mặc dù sử dụng G- CSF, nên giảm liều
docctach từ 75 mglm² xuống 60 mg/m². Nêu cảc giai đoạn giảm bạch cầu trung tính phức
tạp xáy ra sau dỏ, nến giảm iiều docctaer từ 60 mglm² xuông 45 mg/m². Trong trường hợp
giảm tiểu cầu độ 4, nên giảm liếư docctaer từ 75 mglm² xuông 60 mg/m². Bệnh nhân không
nên dược điếu trị trở lại với các chu kỳ docctaer tiếp theo cho đến khi bạch câu trung tính
phục hồi về mức > | 500 tế bảo/mm3 vả tiểu cầu phục hồi về mức > 100. 000 tể bảo/mmẵ
Ngừng điều trị nếu các độc tính nảy kéo dải (xem CẢNH BÁO VÀ THẬN TRỌNG
ĐẶC BIỆT KHI SỬ DỤNG).
Điếu chinh liếư khuyến cảo do độc tính ở những bệnh nhân được đỉều trị bằng docctaer
kêt hợp với cisplatin vả 5—ÍÌuorouracỉl (S-FU):
ÍN Ỉi
\9..\ & 'f.
Dộc tính Diều chỉnh liếư
Tiêu chảy độ 3
Giai doạn dầu tiên: giảm liếư s-nuorouraeii còn 20%. Giai đoạn thứ
hai: sau dó giảm liêu docctach 20%.
'I`iêu chảy dộ 4
Giai doạn dầu tiên: gỉảm liếư docctaer vả 5-fiuorouracii 20%. Giai
đoạn thứ hai: ngừng điêu trị.
Viêm mỉệng/viếm
niêm mạc dộ 3
Giai doạn dầu tiến: giảm liếư 5-fiuorouracii còn 20%. Giai đoạn thứ
hai: chỉ ngừng 5-fluorouracil ở tất cả cảc chu kỳ sau đó. Giai đoạn
thứ ba: giảm liều docctaer 20%.
Giai doạn dầu tiên: chỉ ngừng 5—fluorouracil ở tẳt cả các chu kỳ sau
Vìêm miệnglviêm đó
niêm mạc độ 4 '
Giai doạn thứ hai: giảm liều docctaer 20%.
Về việc điếu chinh liếư cisplatin vả 5-f1uorouracil, xem tóm tắt đặc tính sản phẩm tương
ứng.
l`rong cảc nghiên cứu then chốt về ung thư biều mô tế bảo váy dầu và cố tiến triến tại chỗ
(SCCHN) ở những bệnh nhân bị giảm bạch cầu trung tính phức tạp (bao gồm giảm bạch
câu trung tính kẻo dải, giảm bạch câu trung tính có sôt, hoặc nhiễm trùng), khuyến cáo sử
dụng G-CSF dế dem lại dộ bao phù dự phòng (ví dụ ngảy thứ 6-15)ờ tất cả các chu kỳ tỉếp
theo.
Ci TƯỚNG TẤC THUỐC (31
>
"7
;
Các nghiên cứu in vitro đã cho thấy sự chuyển hóa cùa docctaer có thế bị biến đổi do việc
sử dụng dồng thòi các hợp chất cảm ứng, ức chế hoặc dược chuyến hóa bới cytochrom
P450- 3A (vả do đó có thể ức chế cạnh tranh enzym) như cyclosporin, terfcnadin
kctoconazol, crythromycin vả trolcandomycin. Do dó cân thận trọng khi điều trị đồng thời
những thuốc nảy cho bệnh nhân vì có khả năng tương tác đáng kế.
Docctaxel gắn kết cao với protein (> 95%). Mặc dù tương tác có thế có in vivo của docctach
với thuốc dùng dồng thời chưa dược nghiên cứu chính thức, các tương tác in vitro vởi các
thuốc gắn kết chặt với protein như erythromycin, diphenhydramin, propranolol, propafenon,
phenytoin, salicylat, sulfamethoxazol và natri valproat không ảnh hướng đến sự gắn kết
protein cùa docetaxel. Ngoài ra, dcxamcthason không ảnh hưởng đến sự gắn kết protein
cùa docctaxcl. Docctaxci không ảnh hưởng đến sự gắn kết của digitoxin
Dược động học của docctaxcl, doxorubicin vả cyclophosphamid không bị ảnh hưởng bởi
việc dùng các thuốc nảy đổng thời. Dữ lỉệu giói hạn từ một nghiên cứu đơn không đối
chứng gợi ý sự tương tác giữa docctach vả carboplatin. Khi kết hợp với docctaxcl, dộ thanh
thải cùa carboplatin cao hơn khoảng 50% so với các trị số trước dó được báo cáo dối với
dơn trị liệu bằng carboplatin.
Dược động học của Docetaxcl khi có sự hiện dìện của prednison đã được nghíên cứu ở
bệnh nhân bị ung thư tuyến tiền liệt di căn. Docetaxcl dược chuyến hóa bời CYP3A4 vả
prednison dã được bỉết lả gây cảm ứng CYP3A4. Không quan sảt thấy tác dụng nảo cùa
prednison có ý nghĩa thống kế đối với dược động học cùa docetaxel.
Cần thận trọng khi dùng docctaxcl ở những bệnh nhân đang dùng đồng thòi với các thuốc
ức chế mạnh CYP3A4 (ví dụ thuốc ức chế protcasc như ritonavir, thuốc kháng nấm nhóm
azol như ketoconazoi hoặc itraconazol). Một nghiên cứu về tương tác thuốc dược thực hỉện
).i c
\\ Ổ'Ă' - /.x `l/
ờ nhũng bệnh nhân đang dùng ketoconazol vả docctaer cho thấy dộ thanh thải cùa
docctaer giảm đi một nứa do ketoconazol, có lẽ do sự chuyển hóa của docctaer liên quan
dến CYP3A4 như là một đường chuyến hóa chính (duy nhất) Giảm dung nạp docctaer có
thể xảy ra, ngay cả ở Iiểu thấp hơn.
Có thế phải giảm 50% lỉếu nếu dùng chung với các thuốc ức chế mạnh CYP3A4 như azolc
kháng nâm, ritonavỉr, một sô macrolide (clarithromycin, telythromycin).
CI CHỐNG cni i›ịNii
>
>
>
›
Quả mẫn với hoạt chất hoặc với bất kỳ tá dược nảo của thuốc.
Bệnh nhân có số lượng bạch cầu trung tính ban đầu < 1.500 tế bảolmm².
Bệnh nhân suy gan nặng. (xem LIỂU LƯỢNG VÀ CẢCH DÙNG vả CẢNH BÁO VÀ
THẬN TRỌNG DẬC BIỆT KHI SƯ DỤNG)
Chống chi dịnh đối với cảc thuốc khảo cũng áp dụng, khi được kết hợp với docctaxcl.
C] CẢNH BÁO VÀ THẶN TRỌNG ĐẶC BIỆT KHI sử DỤNG
noe kỹ hướng dẫn sử dụng trước khi dùng. Nếu cần thêm thông tin, xin hỏi ý kiến bác sỹ
Thuốc chỉ dùng theo sự kế đơn của bác sỹ.
[Dối với ung thư vú và ung thư phổi không tế bảo nhỏ] {91
>
f
Thuốc chuẩn bị trước gồm một corticosteroid đường uống, như dexamethason 16 mglngây
(ví dụ 8 mg, 2 iầnlngảy) trong 3 ngây bắt đầu ] ngảy trước khi dùng docctaxcl, trừ khi có
chống chỉ định, có thế lảm giảm tỷ lệ mắc và mức độ nặng của tinh trạng ứ dịch cũng như
mức dộ nặng của phản ứng quá mẫn. Dối với ung thư tuyến tiển liệt, thuốc chuẩn bị truớc lả
dcxamethason 8 mg, uống lúc 12 giờ, 3 giờ và 1 giờ trước khi truyền docctaer (xem LIÊU
LU'ỌNG VÀ CÁCH DÙNG).
Illuyết học]
›
>
Giảm bạch cầu trung tính là phản ứng bất lợi thường gặp nhất của docctaxcl. Bạch cầu
trung tính ở mức thấp nhất đã xảy ra với thời gỉan trung binh 7 ngảy nhưng khoảng thời
gian nảy có thế ngắn hơn ở những bệnh nhân nặng dã được điếu trị trước đó. Phải tiến hảnh
theo dõi thường xuyên số lượng huyết cầu toản phần ở tất cả các bệnh nhân được điều trị
bầng docctaxcl. Bệnh nhân cần dược điều trị trở lại bằng docctaer khỉ bạch cầu trung tính
phục hồi về mức 2 1.500 tể bảo/mm3 (xem LIỂU LƯỢNG VÀ CÁCH DÙNG).
Trong trường hợp giảm bạch cầu trung tính nặng (< 500 tế bãtolmm3 trong 7 ngảy hoặc
nhiến hơn) trong một liệu trình diều trị docctaxcl, khuyến cảo giảm liều cho liệu trình điếu
trị tiếp theo hoặc sử dụng cảc biện phảp điều trị triệu chứng thích hợp (xem LiỂU LƯỢNG
VÀ CẢCH DÙNG).
Ở những bệnh nhândược điếu trị bằng docctaer kết hợp với cisplạtin vả 5-f1uorouracil
(ỌCF), giảm bạch câu trung tính có sột và nhiễm trùng giảm bạch câu trung tính xảy ra ở
tôc độ thâp hơn khi bệnh nhân dược điêu trị dự phòng băng G-CSF. Những bệnh nhân được
\x'th. « n
điều trị bằng DCF nên dược dỉếu trị dự phòng bằng G-CSF đề Iảm giảm nguy cơ giảm bạch
cầu trung tính phức tạp (giảm bạch cầu trung tính có sốt, giảm bạch cầu trung tính kéo dải
hoặc nhiễm trùng giảm bạch cầu trung tính). Cần theo dõi chặt chế những bệnh nhân được
điều trị bằng DCF (xem LIÊU LUỢNG VÀ CẢCH DÙNG vả TẢC DỤNG KHÔNG
MONG MUON).
> Ở những bệnh nhân được điếu trị bằng docctach kết hợp vởi doxorubicin vả
cyclophosphamid (DAC), giảm bạch cẫu trung tính có sốt vả/hoặc nhiễm trùng giảm bạch
câu trung tính xảy ra ở tốc độ thẳp hon khi bệnh nhân dược điếu trị dự phòng ban đầu bằng
G- CSF. Nên xem xét diều trị dự phòng bằng G- CSF ở nhũng bệnh nhân được điều trị bô
trợ bắng DAC đối với ung thư vú dế lảm giảm nguy cơ giảm bạch cầu trung tính phức tạp
(giảm bạch cầu trung tính có sốt, giảm bạch cầu trung tính kéo dải hoặc nhiễm trùng giảm
bạch cầu trung tính). Cần theo dõi chặt chẽ những bệnh nhân được điếu trị bẳng DAC (xem
LIỂU LƯỢNG VÀ cÁcn DÙNG vả TÁC DỤNG KHÔNG MONG MUỐN).
[Phán ứng quá mẫn]
> Cần theo dõi bệnh nhân chặt chẽ về các phản ứng quả mẫn, đặc biệt là trong các lần truyền
dẩu tiên và thứ hai. Phản ứng quá mẫn có thể xảy ra trong vòng vải phút sau khi bắt đẩu
truyền docctaxcl, do đó phải có sẵn các phương tiện để diều trị hạ huyết ảp và co thắt phế
quản. Nếu phản ứng quá mẫn xảy ra, các triệu chứng nhẹ như đỏ bừng hoặc phản ứng da
khu trú không cần phải giản đoạn đỉều trị. Tuy nhiên, cảc phản ứng nặng như hạ huyết ảp
nặng, co thắt phế quản hoặc nồi ban/ban đỏ toản thân đòi hỏi phải ngừng docctaer ngay
lập tức vả điều trị thich hợp. Nhũng bệnh nhân bị phản ứng quả mẫn nặng không được điếu
trị trở lại bằng docctaxcl.
[Phản ứng da] ffl1
> Ban đò da khu trú ờcác chỉ (lòng bản tay vả lòng bản chân) với phù nề, sau đó tróc vảy da
đă được qụan sát thây. Đã có bảo cáo các triệu chứng nặng như phảt ban, sau đó lặ trỏc vảy
da` dẫn đên gián đoạn hoặc ngững điều trị docctaer (xem LIEU LƯỢNG VA CACH
DUNG).
tÚ’ dịch]
> Những bệnh nhânứ dịch nặng như trản dịch mảng phổi, trản dịch mảng ngoải tim và trản
dịch mảng bụng cân được theo dõi chặt chẽ.
lBệnh nhân suy gan]
> Ở những bệnh nhân dược đỉều trị bằng docctaer với liếư 100 mglm² dưới dạng thuốc đơn
độc có nổng độ transaminase huyết thanh (ALT vả/hoặc AST) lớn hơn 1,5 lần giới hạn trên
của mức binh thường (ULN) đồng thời có nồng độ phosphatase kiếm trong huyết thanh lớn
hon 2, 5 lần ULN, có một nguy cơ cao hơn phảt sinh các phản ứng bất lợi nặng như tử vong
do nhiễm độc bao gổm nhiễm khuấn và xuất huyết dạ dảy ruột có thể gây tử vong, giảm
bạch cầu trung tính có sốt, nhiễm trùng, giảm tiêu cầu, vìêm miệng và suy nhược. Vì vậy,
liều khuyến cáo cùa docctach ớ những bệnh nhân có kết quả xét nghiệm chức năng gan
(LFT) lăng là 75 mglm² và xét nghiệm chức năng gan cần dược đảnh giả lúc ban đẩu vả
trước mỗi chu kỳ điều trị (xem LIÊU LƯỢNG VÀ CÁCH DÙNG).
> Đối với những bệnh nhân có nổng độ bilirubin huyết thanh > ULN vả/hoặc ALT vả AST >
3, 5 lần U 1 N, dồng thời có nồng dộ phosphatnse kiếm > 6 lần ULN, không khuyến cáo giảm
liếư và không nến sử dụng docctach trừ khi có chỉ định nghiêm ngặt.
> Khi kết hợp với cispiatin và 5- [iuorouracil trong điếu trị bệnh nhân ung thư biếu mô tuyến
dạ dảy, cảc nghiên cứu tâm sảng then chốt đã loại trừ nhũng bệnh nhân có ALT vả/hoặc
AST > ! ,5 lằn ULN kết hợp với phosphatase kiếm > 2, 5 lần ULN, vả bilirubin > 1 lần
ULN; dối với những bệnh nhân nảy, không khuyến cáo giảm liếư và không nến sử dụng
docctach trừ khi được chỉ định nghiếm ngặt. Không có dữ lỉệu ở những bệnh nhân suy gan
được diếu trị bằng docctaer kết hợp trong các chi dịnh khác.
[Bệnh nhân suy thận]
> Chưa có dữ liệu ở bệnh nhân suy chức năng thận nặng được diếu trị bằng docctaxcl.
mẹ thần kinh]
› Sự phát sinh dộc tính thần kinh ngoại biên nặng dòi hòi phải giảm liều.
[Độc tính dối với iiml -
> Suy tim đã dược quan sát thấy ở những bệnh nhân dùng docctaer kểt hợp với trastuzumab,
dặc biệt Iậ sau khi dùng hóa trị liệu chứa anthracyclin (doxorubicin hoặc epirubicin). Suy
tim có thẻ có mức độ từ trung bình dên nặng và dã có liên quan với tử vong.
> Khi bệnh nhân là các dối tượng để điếu trị bằng docctaer kết hợp với trastuzumab, họ sẽ
được đánh giá về tim ban dầu. Cần theo dõi thêm về chức năng tim trong khi diều trị (ví
dụ mỗi 3 tháng) dề giúp xảo dịnh những người có thế phảt sinh rối Ioạn chức nãng tim. Để
biết thẽm chi tiết, xem tóm tắt đặc tính sản phẩm của trastuzumab
ISuy hô hấp]
> Hội chứng suy hô hấp cắp, viêm phổi kẽ l viêm phổi, bệnh phổi kẽ, xơ hóa phổi và suy hvô
hấp dã dược bảo cáo và có thế liên quan vởi kêt quả gây tử vong. Các trường hợp viêm phôi
do tia xạ đã được báo cáo ở những bệnh nhân được xạ trị dồng thời.
> Nếu các triệu chửng ở phối phát triến thêm hoặc trở nến xấu đi, bệnh nhân cần dược theo
dõi chặt chẽ, kỉếm tra kịp thời và diển trị thích hợp. Điếu trị gián doạn docctaer được
khuyến cảo cho dến khi có kết quả chẩn đoản. Dùng sớm cảc bỉện pháp chăm sóc hỗ trợ có
thể giúp cải thiện tình trạng nảy. Lợi ich của bắt dằu lại việc điều trị bằng docctach phải
dược đảnh gìả cẳn thận.
[Độc tính trên mắt]
Phù hoảng điếm (CMO) đã dược bảo cảo ở những bệnh'nhân được điếu trị với docctaxcl.
Bệnh nhân bị suy giảm thị lưc nên trải qua một cuộc kiêm tra nhãn khoa nhanh chóng và
dằy dù. 'l`rongjrường hợp dược chẩn doản bị phù hoảng điếm, nên ngừng đỉếu trị với
docctaer vả băt đâu với phương phảp diêu trị thích hợp hơn.
10
[Các phản ứng khảo]
?
Phải thực hiện cảc biện phảp trảnh thai ở cả nam giới và phụ nữ trong khi điều trị vả đối
với nam giới ít nhất là 6 tháng sau khi ngừng điếu trị (xem PHỤ NỮ CÓ THAI VÀ CHO
CON BU)
[Thận trọng bổ sung trong điếu trị bổ trợ ung thư vú]
tư
7
ỵr
Giảm bạch cầu trung tính phức tạp
Dối với những bệnh nhân bị giảm bạch cầu trung tính phức tạp (giảm bạch cẩu kéo dải,
giảm bạch câu trung tính có sôt hoặc nhiếm trùng), nên xem xét dùng G- CSF và giảm liếư
(xem ! IÊU LƯỢNG VÀ CÁCH DÙNG).
Phản ứng về tiêu hóa
Cảc triệu chứng như đau bụngqvả nhạy c_ảm dau ở bụng sóm, sốt, tiêu chảy, có hoặc không
giảm bạch câu trung tinh có thế là các biêu hiện sóm cùa nhiễm độc đường tiêu hóa nghiêm
trọng, cân được đảnh giả và điều trị kịp thòi.
Suy tỉm sung huyết Ơỉi
Cần theo dõi bệnh nhân về các triệu chứng suy tim sung huyết trong khi điều trị và trong
thời gian theo dõi.
Bệnh bạch cầu
Ở những bệnh nhân được điều trị bằng docctaxcl. doxorubicin vả cyclophosphamid (DAC),
nguy cơ loạn sản tùy chậm hoặc bệnh bạch cầu dòng tủy đòi hỏi phải theo dõi vế huyểt học.
Bệnh nhân có hạch bạch huyết giai đoạn 4+
Tỷ lệ lợi ích/nguy cơ đối với DAC ò bệnh nhãn có hạch bạch huyết giai đoạn 4+ chưa được
xảc định đầy đủ vảo lúc phân tích tạm thời (xem Các ĐẶC TỈNH DU ỌC LỰC HỌC).
Người cao tuối
. Chưa có dữ liệu nảo ở bệnh nhân > 70 tuổi đang sử dụng docctaer kết hợp với doxorubicin
vả cyclophosphamíd.
Trong số 333 bệnh nhân dược diếu trị bằng docctach mỗi 3 tuần trong một nghiến cứu về
ung thư tuyến tiến liệt, 209 bệnh nhân từ 65 tuổi trở lên và 68 bệnh nhân trên 75 tuối. Ở
những bệnh nhân được diều trị bằng docctaer mỗi 3 tuần, tỷ lệ thay đổi ở móng liên quan
xảy ra với một tỷ lệ 2 10% ở những bệnh nhân từ 65 tuối trờ lến so với những bệnh nhân
trẻ. Tỷ lệ sốt, tiêu chảy, chản ăn và phù ngoại biên iiên quan xảy ra ở mức > 10% ở những
bệnh nhân từ 75 tuổi trở lên so với bệnh nhân dưới 65 tuổi.
Trong số 300 bệnh nhận (221 bệnh nhân ở phần pha 111 của nghiên cứu và 79 bệnh nhân ở
phần pha li) được điếu trị bằng docctaer kết hợp với cisplatin và 5 fluorouracil trong
nghiên cứu ung thư dạ dảy, 74 bệnh nhân tù 65 tuôi trở lên và 4 bệnh nhân từ 75 tuổi trở
l]
z'
lên. Tỷ lệ mắc các tác dụng bất lợi nghỉếm trọng cao hơn ở những bệnh nhân cao tuổi so
vởi những bệnh nhân trẻ. Tỷ lệ cảc tảc dụng bất lợi sau đây (tẩt cả cảc cấp độ): ngủ lịm,
viếm miệng, nhiễm trùng giảm bạch cầu trung tinh xảy ra ở tỷ lệ_ > 10% ở những bệnh nhân
từ 65 tuồi trở lến so với những bệnh nhãn trẻ. Cần theo dõi chặt chẽ các bệnh nhân cao tuồi
được điếu trị bằng DCF.
[Thảnh phần có chứa ethanol]
Thảnh phần có chứa ethanol: Dã ghi nhận được báo cảo về ngộ độc liến quan đến một số
chế phẩm chúa docctach do có chứa ethanol. Lượng ethanol trong một liếư thuốc tiếm
docctaer có thể gây tảc dộng lên hệ thẫn kinh trung ương vả cần cân nhắc khi kế đơn cho
những bệnh nhân: tránh hoặc hạn chế đưa cthanol vảo cơ thế. Cân nhắc về hảm lượng
ethanol trong chế phẩm docctaer dạng tiêm tới khả năng lải xe, vận hânh mảy móc ngay
sau khi dùng thuốc.
Phụ nữ có thai và cho con bú
Không có thông tin về việc sử dụng docctaer ở phụ nữ mang thai. Docetaxel đã cho thấy
gây độc cả cho phôi vả thai ở thở và chuột cống và lâm giảm khả năng sinh sản ở chuột
cống. Cũng như với các thuốc gây dộc tế bâo khảc, docctaer có thể gây nguy hiếm cho
thai khi dùng cho phụ nữ mang thai Vì vậy, không được dùng docctach trong khi mang
thai trừ khi có chỉ định rõ rảng.
Phụ nữ có khả năng sinh dẻlthụ thai: ÒĨ
Những phụ nữ trong độ tuổi sinh đẻ nên được khuyến tránh mang thai, và thông bảo cho
bác sĩ điều trị ngay lập tức nếu mang thai xảy ra. Nên sử dụng một phương phảp tránh thai
có hiệu quả trong khi diếu trị. lrong cảc nghiến cứu tiến lâm sâng, docctaer có tác dụng
gây độc gen và có thề lảm thay đổi khả năng sinh sản ở nam giới (xem CẢC DỮ LIỆU AN
TOÀN "] [ỂN LÂM SÀNG). Vì vậy, nam giới đang được điếu trị bằng docctaer nên được
khuyên không nên có con trong và lên đến 6 tháng sau khi điếu trị và nến tìm kiếm lời
khuyến về việc bảo tồn tinh trùng trước khi diếu trị.
Phụ nữ cho con bú:
Docetaxcl tả một chất ưa mở nhưng chưa rõ liệu nó có dược bải tiết qua sữa mẹ hay không.
Vì vậy,`do khảmăng có các phản ứng bẩt lợi ở trẻ bú mẹ, phải ngưng cho con bú trong thời
gian dìếu trị bãng docctaxcl.
Tác động trên khả năng iái xe vả vận hânh máy mỏc
>
>
Chưa có nghiến cún vế tảo động trên khả năng lải xe và vận hảnh máy móc được thực
hiện.
Lượng ethanol trong chế phấm Isotcra Injection Concentratc 20 mglml có thế Iảm giảm
khả năng lái xe hay vận hảnh mảy mớc.
12
`
uJo |
Cl TÁC DỤNG KHÔNG MONG MUÔN
>
Các phản ứng bất lợi được cho là có thế liên quan hoặc có khả năng liên quan đến việc
dùng docctaer đã thu được ớ:
1312 và 12] bệnh nhân đã dược diếu trị tương ửng bằng docctaer 100 mglm² vả 75 mg/m²
như một thuốc đơn dộc.
258 bệnh nhân dã dược diểu trị bằng docctaxel kết hợp với doxorubicin.
406 bệnh nhân dã được diếu trị bằng docctach kết hợp với cisp1atin.
92 bệnh nhân dã dược dỉếu trị bằng docctaer kết hợp với trastuzumab.
255 bệnh nhân dã dược diều trị bằng docctaer kết hợp với capecitabin. …
332 bệnh nhân dã dược diồu trị bằng docctaer kết hợp với prednison hoặc prednisolon (cảc
phản ứng bất lợi quan trọng trên lâm sảng liến quan đến điếu trị được trình bảy).
1276 bệnh nhân (744 trong nghiên cứu TAX 316 vả 532 trong nghiên cứu GEICAM 9805)
đã dược điều trị băng docctaer kêt hợp với dogorubicin vả cyclophosphamid (các phản
ứng bẩt lợi quan trọng trên lâm sảng lìến quan đên điêu trị được trình bảy).
300 bệnh nhân bị ung thư biếu mô tuyến dạ dảy(22l bệnh nhân ớ phầnpha … của nghiên
cứu và 79 bệnh nhân ở phân pha1 1) đã được điêu trị băng docctaer kêt hợp với cisplatin
vả S-f1uorouracil (cảc phản ứng bât lợi quan trợng trên lâm sảng liên quan đên điêu trị dược
trình bảy).
174 và 251 bệnh nhân ung thư dầu và cổ đã dược điếu trị bằng docctaer kết hợp với
cisplatin vả 5—i1uorouracil (các phản ứng bât iợi quan trọng trên lâm sảng liên quan dên
diêu trị được trinh bây).
Những phản ứng nảy dã được mô tả sử dụng Tiêu chuẩn dộc tinh chung của Viện Ung thư
quốc gia Mỹ (NCI) (độ 3= G3; độ 3 -4= G3l4; độ 4= G4) và các thuật ngữ của COSTART
vả MedDRA. T an suất được định nghĩa lả: rất thường gặp (> 1/10), thường gặp (> 1/100
đến < 1/10); ít gặp (> 1/1.000 dến < 1/100);h1ếm gặp (> 1/10. 000 đến < 1/1.0;00) rât hiếm
gặp (< 1/ 10 000); không rõ (không thể ước tính từ cảc dữ liệu hiện có).
Trong mỗi nhóm tầnsuất, cảc tảc dụng không mong muốn được trinh bảy theo thứ tự độ
nghiêm trọng giảm dân.
Cảc bảo cáo bất iợi dược báo cáo thường gặp nhất cùa docctaer dùng đơn độc lâ: giảm
bạch cầu trung tính (có hồi phục và không tich lũy; số ngảy trung bình dẫn đến mức bạch
cẩu trung tính thấp nhắt là 7 ngảy và thời gian trung bình bị giảm bạch cầu trung tính nặng
(< 500 tế bảo/mm²) là 7 ngảy), thỉếu máu, rụng tóc, buồn nôn, nôn, viêm miệng, tỉêu chảy
vả suy nhược. Mức dộ nặng cùa cảc phản ứng bất lợi của docctaer có thể tăng khi docctach
được dùng kết hợp với cảc thuốc hóa trị liệu khảo.
V
VI
Khi kết hợp với trastuzumab, các phan ứng bất lợi (tất cả cấp độ) được báo cáo > 10% được
trinh bảy. Có một tỷ 1ệ tăng các phản ứng bất lợi nghỉếm trọng (SAE) (40% so với 31%) và
phản ứng bắt lợi (AE) độ 4 (34% so với 23%) ở nhóm dùng kết hợp với trastuzumab so với
docctaxcl đơn trị liệu.
Khi kết hợp với capecitabin, các tác dụng không mong muốn thường gặp nhẩt liên quan
đến điếu trị (> 5%) được bảo cảo trong một nghiến cứu pha 111 ở những bệnh nhân bị ung
thư vú thất bại với điếu trị bẳng anthracyclin được trinh bảy (xem tỏm tắt đặc tính sản
phấm của capecitabin).
Cảc phản ứng bất lợi sau đây thường được quan sát với docctaxcl:
. Rối loạn hệ miễn dịch
Phản ứng quá mẫn thường xảy ra trong vòng vải phứt sau khi bắt đầu truyền docctaer vả
thường từ nhẹ đến trung binh Các triệu chứng thường gặp nhất lá đỏ bừng mặt, nổi ban có
hoặc không ngứa, tức ngực, dau lưng, khó thờ và sốt hoặc ớn lạnh Cảo phản ứng nặng
được đặc trưng bới hạ huyết áp vả/hoặc co thắt phế quản hoặc nối banlban đò toản thân
(xem CẢNH BÁO VÀ THẶN TRỌNG DẶC BIẸT KHI sư DỤNG).
Rối loạn hệ thẳn kinh OĨ1
Sự xuất hiện dộc tính thần kỉnh ngoại biên nặng đòi hỏi phải giảm iiều. Cảc dấu hiệu thần
kinh cảm giảc từ nhẹ đến trung bình được dặc trưng bời dị cảm, loạn cảm hoặc đau bao
gồm cả nóng rát. Cảo phán ứng thần kinh vận động chủ yếu được đặc trưng bời yếu (xem
LIỂU LƯỢNG VÀ CÁCH DÙNG vả CẢNH BÁO VÀ THẬN TRỌNG ĐẶC BIỆT KHI
SỬ DỤNG).
Rối loạn da và mô dưới da
Phản ứng da có hổi phục dã được quan sảt thấy và được thường được xem là nhẹ dến trung
bình. Phản ứng nảy được đặc trưng bời phát ban bao gồm phảt ban khu trú chủ yếu trên bản
chân vả bản tay (bao gồm cả hội chứng bản tay bản chân nặng) nhưng còn gặp ở cảnh tay,
mặt hoặc ngực và thường đi kèm với ngứa. Phát ban thường xảy ra trong vòng 1 tuần sau
khi truyền docctaxcl. it gặp hơn, cảc trìệu chứng nặng như phát ban tiếp theo lá tróc vảy da
hiếm khi dẫn đến gián đoạn hoặc ngừng điều trị bằng docctach đã dược báo cáo (xem
11ÊU LƯỢNG VÀ CẢCH DÙNG vả 1`ẢC DỤNG KHỎNG MONG MUÔN). Rối loạn
móng nặng dược đặc trưng bời giảm sắc tế hoặc tăng sắc tố, đôi khi đau và bong mỏng.
Rối loạn toản thân và tinh trạng tại chỗ tiêm truyền
Phản ứng tại chỗ truyền thường nhẹ và bao gồm tãng sắc tố, viêm, đó hoặc khô da, viêm
tĩnh mạch hoặc thoát mạch và sưng tĩnh mạch.
Ú dịch bao gồm các phản ứng như phù ngoại biến và ít gặp hơn gồm trản dịch mâng phối
trản dịch mảng ngoải tim, có trướng và tăng cân. Phù ngoại biên thường bắt dầu ở chi
dưới và có thể trở thảnh phù toản thân với mức tăng cân từ 3 kg trở lên. Ử dịch tích lũy
về tỷ 1ệ mắc và múc dộ nặng (xem CÀNH BẢO VÀ THẬN TRỌNG ĐẶC BIỆT KHI
sư DỤNG).
14
— g;,_
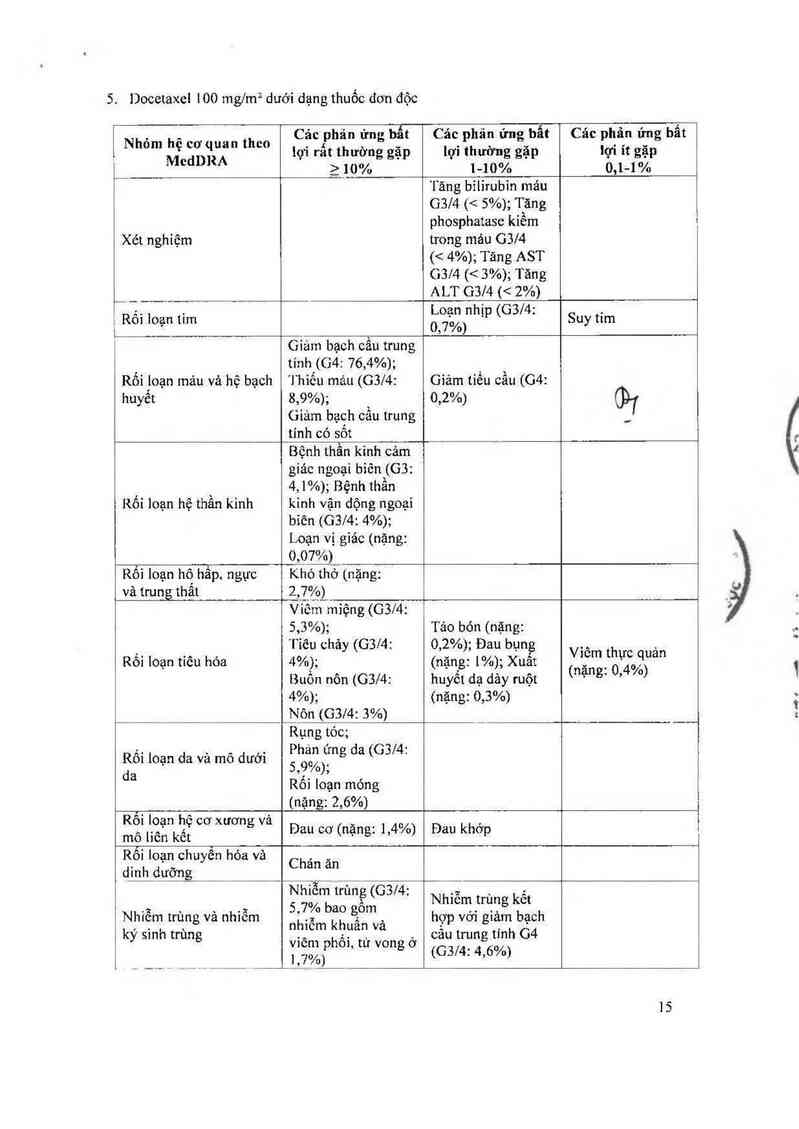
s. Docetaxei mo mg/m² dưới dạng thuốc đơn độc
Nhỏm hệ cơ quan theo
MedDRA
Các phản ửng bẩt
iợi rất thường gặp
2 10%
Cảc phản ứng bất
lợi thường gặp
1-10%
Các phản ứng bẩt
lọi ít gặp
0,1—l %
i
Xét nghiệm
Tãng bilirubin máu
G314 (< 5%);11ăng
phosphatase kiêm
trong máu 63/4
(< 4%); Tăng AST
G3/4 (< 3%); Tăng
ALT G3/4 (< 2%)
Rối loạn tim
Loạn nhịp (G3/4:
0,7%)
Suy tim
Rối _loạn mảu và hệ bạch
huyêt
Giám bạch cẩu trung
tính (G4: 76,4%);
'l'hỉếu máu (63l4:
8,9%); ;
Giảm bạch câu trung
tính có sốt
Giảm tiếu cằn (G4:
0,2%)
Rối loạn hệ thần kinh
Bệnh thần kinh cảm
giảc ngoại biến (63:
4,1%); Bệnh thẳn
kinh vận dộng ngoại
biên (GB/4: 4%);
Loạn vị giác (nặng:
Rối loạn hộ hẳp. ngực
và trung thât
0,07%)_
Khó thở (nặng:
Rối loạn tiêu hóa
5,3%);
Tiêu chảy (G3/4:
4%);
Buổn nôn (0314:
4%);
Nôn (03/4: 3%)
Tảo bón (nặng:
0,2%); Đau bụng
(nặng: 1%); Xuất
huyết dạ dảy ruột
(nặng: 0,3%)
Viêm thực quản
(nặng: 0,4%)
Rối loạn da và mô dưới
da
Rụng tóc;
Phan ứng da (G3/4:
5,9%);
Rối loạn móng
(nậng: 2,6%)
Rối Ioạn hệ cơ xương và
mô liến kêt
Đau cơ (nặng: 1,4%)
Đau khởp
Rối loạn chuyến hóa vả
đinh dưỡng
Chán ăn
Nhiễm trùng và nhiễm
ký sinh trùng
Nhiễm trùng (G3/4:
5,7% bao gồm
nhiễm khuẳn vả
vỉếm phối, từ vong ở
1,7%)
Nhiễm trùng kết
hợp vởi giảm bạch
cầu trung tính 64
(G3/4: 4,6%)
15
~—x
i Hạ huyết áp; Tăng
Rối loạn mạch huyết' ap;
Xuất huyết ,
i 1 1
Á. . .z . Qua man (G3/4:
ROI loạn hẹ micn dịch 5,3%)
m . , ; ~ %
Rối ioan toản thân và U d1Ch (nặng: Phan ưng tại cho
. ' . z .. 6,5%); truyền; Đau ngực
tinh trạng tại cho tiem _ . .
truyền Suy nhược (nặng. khong do tim
1 1,2%); Đạụ (nặng: 0,4%) _
Rối loạn máu vả hệ bạch huyết
Hiếm gặp: Các giai đoạn xuất huyết kết hợp với giảm tiếu cầu độ 3/4.
0 Rối loạn hệ thẩn kinh
Hiện có dữ liệu vế khả năng hồi phục ớ 35,3% các bệnh nhân xưất hiện độc tính thần kinh
sau khiđiếu trị băng docctaer ở liêu 100 mglm² dưới dạng thuôc đơn độc. Các phản ứng
dã tự hôi phục trong vòng 3 thảng.
o Rối Ioạn da và mô dưới da CD’J
Rất hiếm gặp: Một trường hợp rụng tóc không hổi phục vảo cuối cuộc nghiên cứu. 73%
các phản ứng ớ da có thế hồi phục trong vòng 21 ngảy.
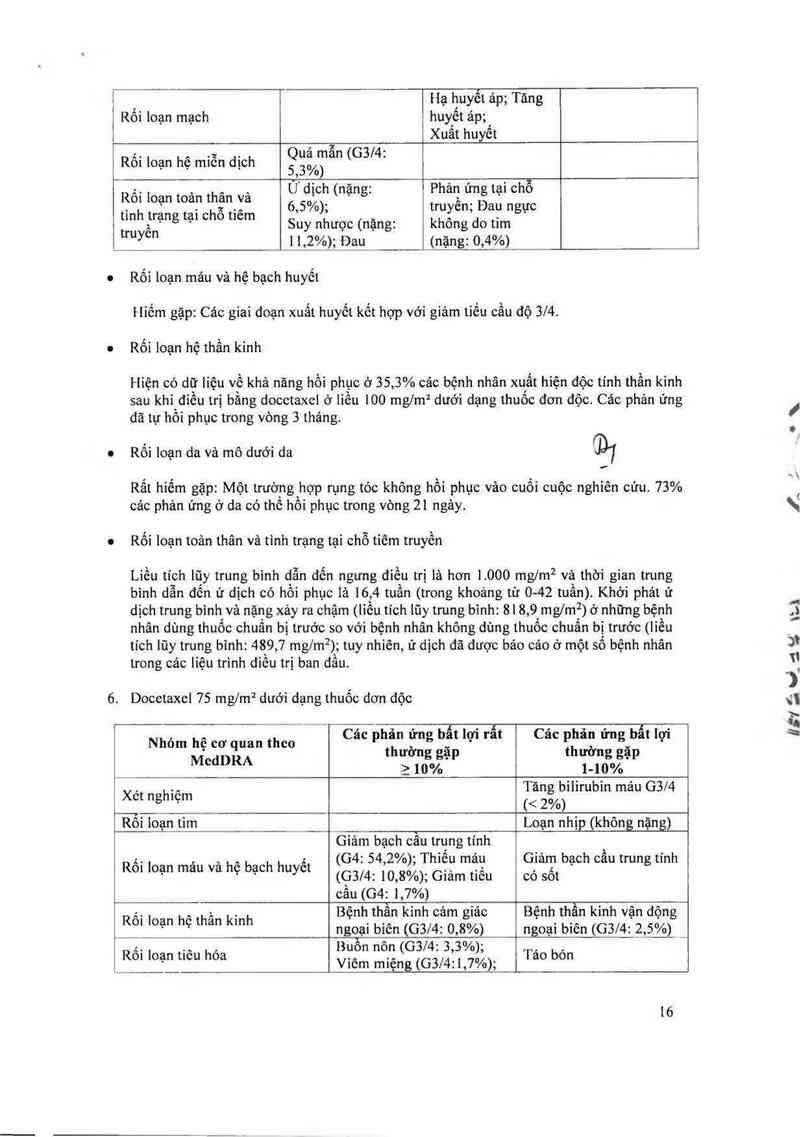
o Rối loạn toản thân vả tình trạng tại chỗ tiêm truyền
Liều tích lũy trung binh dẫn đến ngưng điếu trị là hơn 1.000 mglm² và thời gian trung
bình dẫn đến ứ dịch có hồi phục là 16,4 tuần (trong khoảng từ 0- 42 tuần). Khởi phát ứ
dịch trung binh và nặng xảy ra chậm (liếư tích lũy trung binh: 818,9 mglm²) ở những bệnh
nhân dùng thuốc chuẩn bị trước so vởi bệnh nhân không dùng thuốc chuẩn bị trước (liều
tich lũy trung binh: 489, 7 mglm²); tuy nhiên, ứ dịch đã dược bảo cảo ở một số bệnh nhân
trong các liệu trinh điếu trị ban dầu.
6. Docetaxel 75 mg/m² dưới dạng thuốc dơn độc
Nhỏm hệ cơ quan theo
Cảc phản ứng bất lợi rất
Các phản ửng bất lợi
thường gặp thường gặp
MedDRA 210% uo%
, .. Tăng bilirubin máu G3l4
ỂíĨỉ'ỉễh'ẹm << 2%›
Roi ioạn tim Loạn nhịp (không nặng)
Rối Ioạn mảu vả hệ bạch huyết
Giảm bạch cầu trung tính
(G4: 54,2%); Thiếu máu
(G3/4: 10,8%); Giảm tiếu
cầu (G4: 1,7%)
Giảm bạch cầu trung tính
có sôt
Rối loạn hệ thần kinh
Bệnh thần kinh cảm giác
ngoại biên (GB/4: 0,8%)
Bệnh thần kinh vận dộng
ngoại biên (G3/4: 2,5%)
Rối loạn tiêu hóa
Buồn nôn (G3/4: 3,3%);
Viêm miềịng (G3/4: 1,7%);
Táo bón
16
% \LI
Ụ_ A
Ilổ'l 2
Nôn (G3l4: 0,8%);
Tiêu chảy (G3l4: 1,7%) ,
g. ' , - . Rụng tóc; Phản ứng đa Rôi loạn móng (nặng:
Êm Ioạn dd va mo dướị da (G314: 0,8%) 0,8%)
IỄỉ>ị 1oẵn hẹ cơ xương va mo Dau c ơ
11en ket, ` , __
R01 loạn chuyen hoa va dmh Chán ăn
dưỡng
.1 _ 4 4 »; . …
Ẹẵằịm trung va nh1em ky smh Nhiễm trùng (G3/4: 5%)
Rối loạn mạch Hạ huyết áp
Rối Ioạn toản thận và tình trạng S’uy nhược (nặng: 12,4%);
tại chỗ tiêm truyền Ư dịch (nặng: 0,8%); Đau
Rối loạn hệ mìễn dịch Quá mẫn (không nặng)
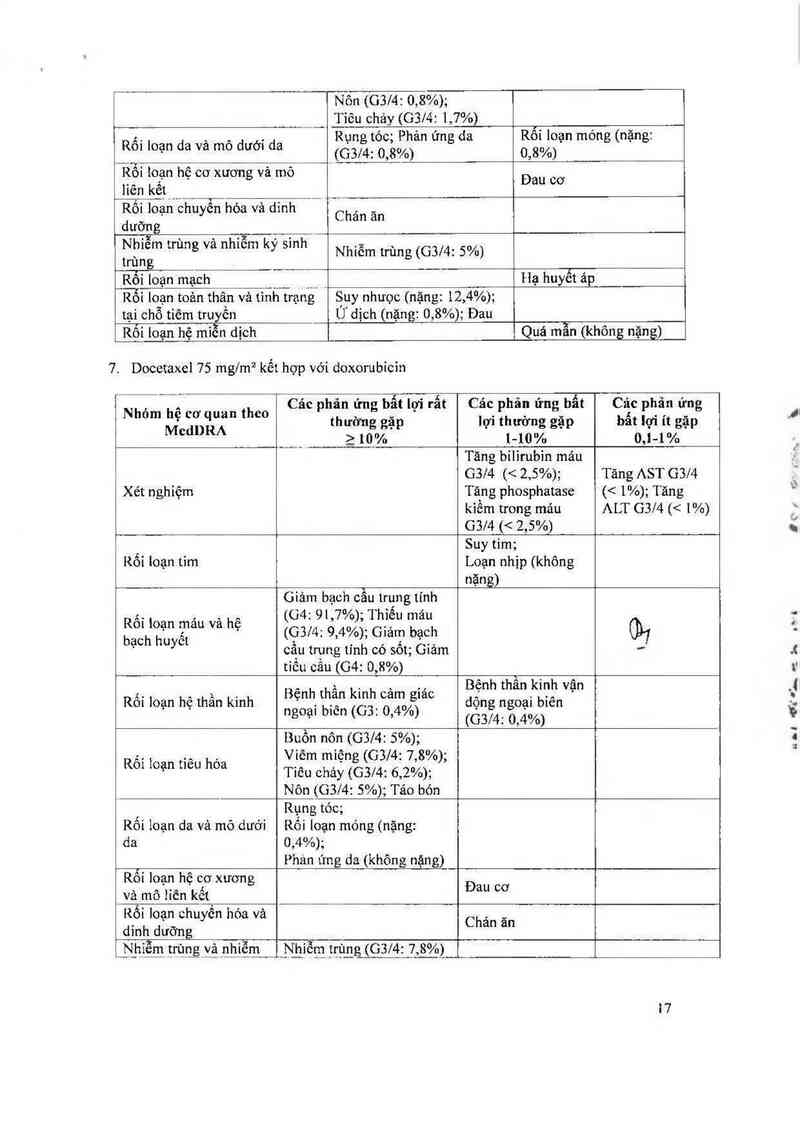
7. Docetaxel 75 mg/m² kết hợp với đoxorubỉcin
Nhỏm hệ cơ quan theo
Các phản ứng bất lợi rất
Các phản ửng bất
Cảo phãn ứng
Rối Ioạn tỉm
Loạn nhịp (không
nặng)
thườn ặ lợi thường gặp bất lợi ít gặp
MCdDRA z 10g0Ễ p 1-10% 0,1-1%
Tăng bỉlìrubỉn máu
G3/4 (< 2,5%); Tăng AST GB/4
Xét nghiệm Tăng phosphatase (< 1%); Tăng
kỉểm trong mảu ALT 63/4 (< 1%)
GBI4 (< 2,5%)
Suy tim;
Rối loạn máu vả hệ
bạch huyêt
Giám bạch cầu trung tính
(G4: 91,7%); Thìếu mảu
(G314: 9,4%); Gỉảm bạch
cầu trung tính có sốt; Giảm
tiếu cẩu (G4: 0,8%)
Rối loạn hệ thẫn kinh
Bệnh thần kinh cảm giác
ngoại biên (G3: 0,4%)
Bệnh thần kinh vận
dộng ngoại bíẽn
(G3/4: 0,4%)
Rôi Ioạn tỉẽu hóa
Buổn nôn ((13/4: 5%);
Viêm miệng (G3/4: 7,8%);
Tìêu chảy (GSÍ4: 6,2%);
Nôn (G3Í4: 5%); Táo bón
Rối loạn da và mô dưới
da
Rụng tóc;
Rối loạn móng {nặng:
0,4%);
Phán ứng da (không nặng)
Rối loạn hệ cơ xương
và mô lỉên kêt
Đau cơ
Rối loạn chuyến hỏa và
dỉnh dưỡng
Chản ăn
LN.h ĩễ_m_ _trùrẸ xả JẺiỄHL…
NỀễÊl _trịịl_qg (G3/4: 7,8%)
17
l` 'C`J
uh] lơi... 0% k
kỷ sỉnh trùng
Rôi loạn mạch
Hạ huyết áp
Rối loạn toản thân và
tình trạng tại chõ tíêm
S'uy nhược (nặng: 8,1%);
Ư dịch (nặng: 1,2%); Dau
Phản ửng tại chỗ
truyên
Rối loạn hệ mỉễn dịch
Quá mẫn (G3/4:
1,2%)
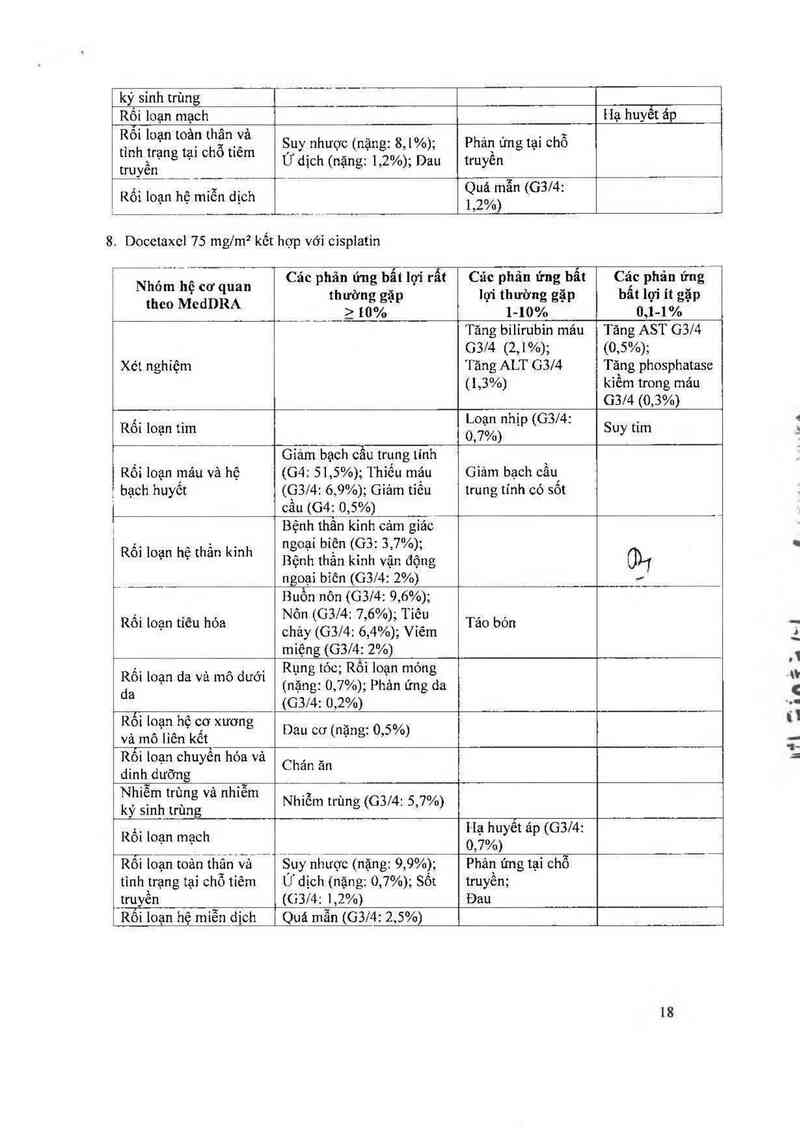
8. Docetaxcl 75 mglm² kết hợp với cỉsplatin
Nhóm hệ cơ quan
Các phân ứng bẩl lợi rẩt
Các phản ứng bẩt
Các phản ứngiụ
th ườn ặ lợi thường gặp bât lợi ít gặp
theo MedDRA 2 1 ỗẳ,ẳ p 1-1 0% 0,1-1%
Tăng bilirubin mảu Tăng AST G3/4
(3374 (2, 1 %); (0,5%);
Xét nghiệm Tăng ALT G3/4 Tăng phosphatase
(1,3%) kỉềm trong máu
G37'4 (0,3%)
Rối loạn tim ầỄĨổnhịp (G3l4` Suy tím
Rối loạn mảu và hộ
bạch huyêt
Giảm bạch cầu trung tính
(64: 51,5%); Thỉếu mảu
(G3/4: 6,9%); Giảm tỉểu
cằu (G4: 0,5%)
Giảm bạch cầu
trung tính có sôt
.
Rối loạn hệ thần kỉnh
Bệnh thẩn kinh cảm giác
ngoại bíên (G3: 3,7%);
Bệnh thần kinh vận động
ngoại bỉẽn (G3/4: 2%)
Buồn nôn (G3/4: 9,6%);
Nôn (G3/4: 7,6%); Tiêu
Ro1 loạn tléu hoa chảy (G3/4: 6,4%); Viêm Tao bon
miệng (G3l4: 2%)
Rối loan da vả mô đưới Rụng tóc; Rôi loạn móng
da ' (nặng: 0,7%); Phản ứng da
(G3/4: 0,2%)
Rối loạn hệ cơ xương , _ _,
và mô liên kết Dau cơ (nặng. 0,5 Á:)
R.OI Ioạ.n~ chuyen hoa va Chán ăn
dmh dương
Nhiễm trùng vả nhỉễm .g _ , _ ,,
ký sinh trùng Nh1cm Lrung (0374. 5,7/o)
,. Hạ huyết áp (G3/4:
RO' IOỈ'ỆỀỀh_… ___… __ 0,7%› __
Rôì loạn toản thỂm vả S'uy nhược (nặng: 9,9%); Phảụ ứng tại chõ
tình `trạng tại chõ tiêm Ư dịch (nặng: 0,7%); Sôt truyền;
truyên ((13/4: 1,2%) Đau
'11731 loạn hệ miễn dịch
Quá mẫn (6374: 2,5%)
18
9. Docetaxel 100 mg/m² kết hợp với lrastuzumab
Các phản ứng bẫt lợi
Cảc phản ứng bẩt lợi
Nhòm hệ cơ quan theo McdDRA rẩt thường gặp thường gặp
2 10% 1-10%
Xét nghỉệm Tăng cân
Rôi loạn tim Suy tim
Rối Ioạn máu và hệ bạch huyết
Gỉâm bạch cầu trung tinh
(G314: 32%);
Giảm bạch cẳu trung tinh có
sốt (bao gồm giảm bạch cầu
trung tính kết họp với sốt và sử
dụng kháng sinh) hoặc nhiễm
khuẳn gíảm bạch cầu trung
tính
Rối loạn hệ thần kinh
Dị cảm; Nhức đầu; Loạn vị
giảc; Giảm cảm giác
Rôì Ioạn măt
T ãng chảy nước măt; Viêm
kêt mạc
Rốj loạn hô hắp, ngực và trung
thãt
Chảy mảu cam; Dau họng-
thanh quản; Viêm mũi họng;
Khó thở; Ho; Chảy nước mũi
Rối loạn tỉêu hóa
Buồn nôn; Tiêu chảy; Nôn;
Tảo bón; Viêm mỉệng; Khó
tìêu; Dau bụng
Rối Ioạn da và mô dưới da
Rụng tóc; Ban đò; Ban; Rối
loạn móng
Rối Ioạn hệ cơ xương vả mô lỉên
kết
Đau cơ; Đau khởp; Dau ở chi;
Đau xương; Đau lưng
Rỗi loạn chuyến hóa và dinh
dưỡng
Chán ăn
Rôi loạn mạch
Phù bạch huyết
Rối Ioạn toản thân và tình trạng tại
chõ tíêm truyền
Suy nhược; Phù ngoại bíẽn;
Sốt; Mệt mỏi; Vìêm níêm mạc;
Dau; Bệnh gỉống cứm; Đau
ngực; Ón lạnh
Ngủ lịm
Rối loạn tâm thần
Mất ngủ
Rối loạn mảu và hệ bạch huyết
Rất thuờng gặp: Độc tính về huyết học tảng lên ở nhũng bệnh nhân được điều trị bằng
trastuz.umab vả docctaxcl so với docctaxcl đon dộc (gỉảm bạch cầu trung tính đó 3/4 32%
so vởỉ 22%, sử dụng I`ỉêu chuẩn độc lính chung của Viện Ung thư quõc gìa Mỹ (NCI- CTC)
Lưu ý rãng dìều nảy có thế là một sự dánh giá thẩp vì đocetaxel dùng đon dộc ở liều 100
mgfm² dã dược biết là dẫn dến gỉảm bạch câu trung tinh ở 97% bệnh nhân, 76% độ 4 dựa
trên số luợng thẩp nhắt trong mảu. Tỷ lệ giảm bạch cầu trung tính có sốt/nhiễm khuấn giảm
bạch trung tính củng tảng lên ở những bệnh nhân dược diếu trị bằng Herccptin cộng vởi
docctaxcl (23% so vởi 17% đối với bệnh nhân được dỉều trị bằng docetaxel đon độc).
19
' ^7.
\wL\ Z #
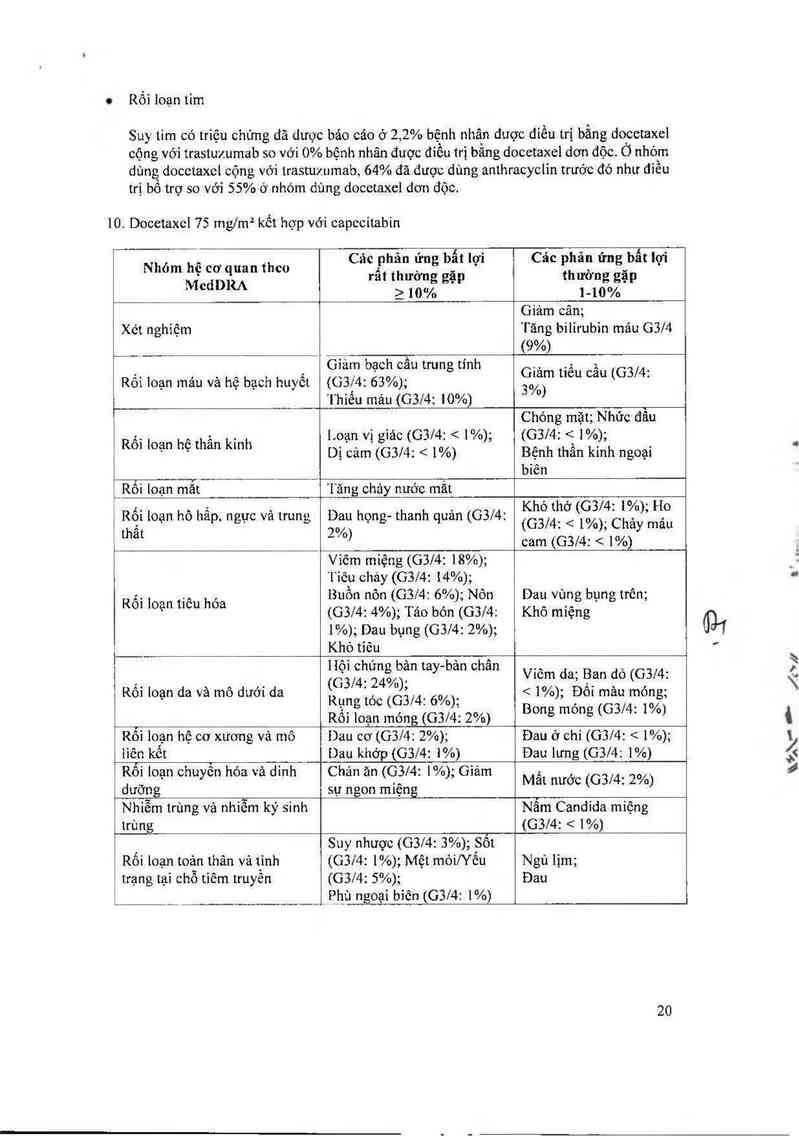
Rối loạn tim
Suy tim có triệu chửng dã dưọc bảo cáo ở 2, 2% bệnh nhân duợc điểu trị bằng docctaer
cộng với trastuzumab so với 0% bệnh nhân được đỉều trị bằng docetaxel dơn độc. Ở nhóm
dùng docctach cộng vởi lrastuvumab, 64% đã được dùng anthracyclỉn trước đó như diều
trị bổ trợ so vởỉ 55% ở nhóm dùng docctaxel đơn độc.
10. Docetaxcl 75 mglm² kết hợp với capccitabin
Nhóm hệ cơ quan theo
Cảc phản ứng bẩt lợi
Các phân ứng bất 1ọ1
\ rẩt thường gặp thường gặp
Mcdl)RA 210% 1_10%
Giảm cân;
Xét nghiệm Tăng bilirubin mảu 63/4
(9%)
Rối loạn máu và hệ bạch huyết
Giảm bạch cẩu trung tinh
(G374: 63%);
Thiêu máu (GẫÍ4I 10%)
Giảm tiều cầu (6374:
3%)
Rối Ioạn hệ thẩn kinh
I.oạn vị gỉác (Gấl4: < 1%);
Dị cảm (G314: < 1%)
Chóng mặt; Nhức đẫu
(G3/4: < 1%);
Bệnh thần kinh ngoại
biên
LRôi Ioạn măt
'I`ảng chảy nước mắt
Rối loạn hô hấp. ngực vả trung
thât
Dau họng- thanh quản (G3/4:
2%)
Khó thớ (G3/4: 1%); Ho
(G3/4: < 1%); Chảy máu
cam (G3l4: < 1%)
Rối loạn tiêu hóa
Viêm miệng (G314: 18%);
Tiêu chảy (6374: 14%);
Buồn nôn (6374: 6%); Nôn
(G3/4: 4%); Tảo bón (G314:
1%); Đau bụng (G3/4: 2%);
Khó tiêu
Dau vùng bụng trên;
Khô miệng
Rối Ioạn da và mô dưới da
Hội chứng bản tay-bản chân
((13/4: 24%);
Rụng tóc (G374: 6%);
Rối loạn móng (6374: 2%)
Viêm da; Ẹan dò ((33/4:
< 1%); Đôi mâu móng;
Bong móng (G314: 1%)
Rôi loạn hệ cơ xương và mô
liên kêt
Dau cơ (0314: 2%);
Dau khớp (G3/4: 1%)
Đau ở chi (G3/4: < 1%);
Đau lưng (G3/4: 1%)
Rối loạn chuyến hóa và dinh
dưỡng
Chán ăn (G3l4: 1%); Gìảm
sự ngon miệng
Mất nước (6374: 2%)
Nhiễm trùng và nhiễm ký sinh
lrùng
Nẫm Candida miệng
(G374: < 1%)
Rối loạn toản thân vả tinh
trạng tại chõ tìêm truyền
Suy nhược (6374: 3%); Sốt
(6374: 1%); Mệt mỏi/Yếu
(6374: 5%);
Phù ngoại bỉên (6374: 1%)
Ngủ lịm;
Đau
20
\9A\d .' Íc`ll
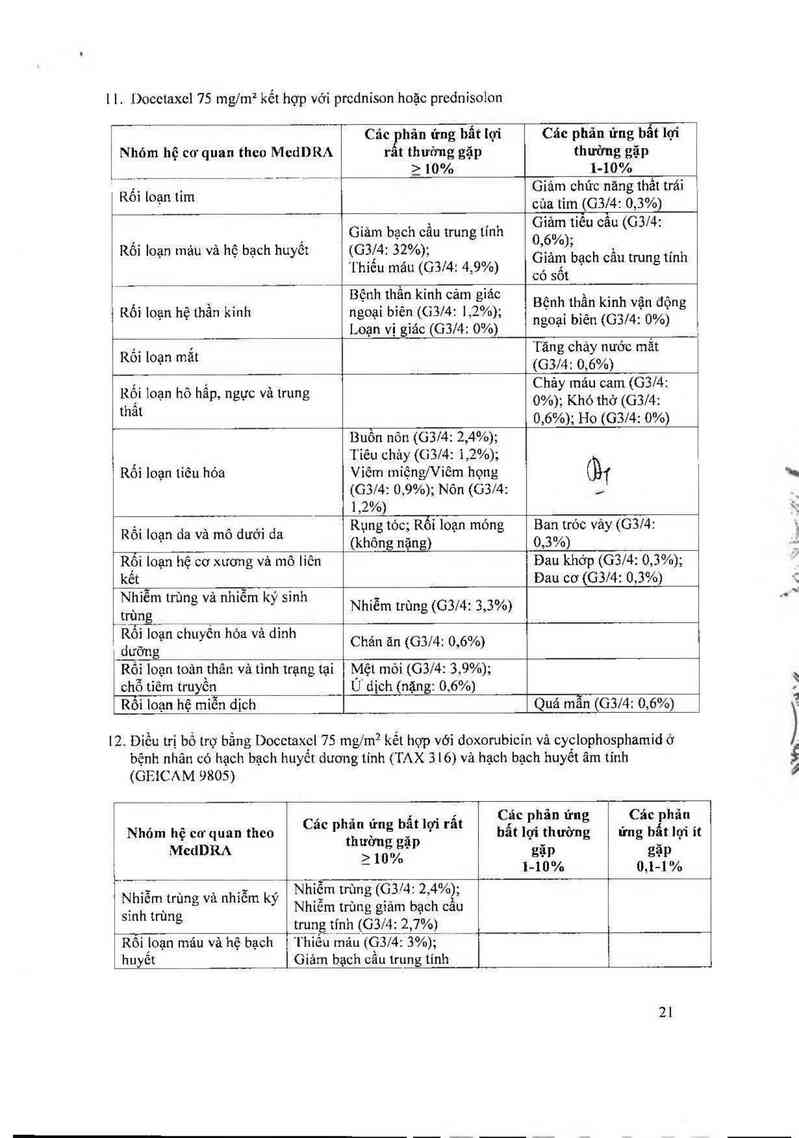
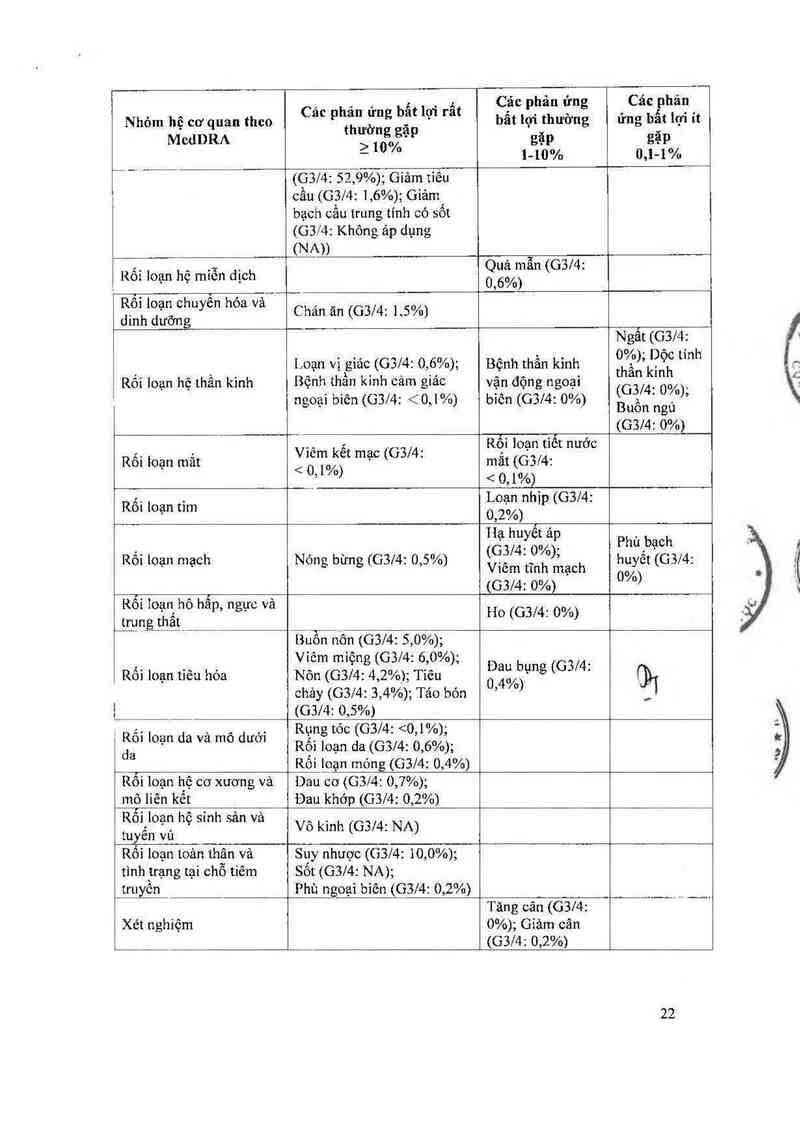
1 l. Docctaxcl 75 mglm² kết hợp vởi prednison hoặc prednisolon
Rôì loạn tim
Nhỏm hệ co' quan theo MedDRA
Các phản ứng bắt lợi
rất thường gặp
2 10%
Các phản ứng bẩt lợi
thường gặp
1-10%
Giảm chức năng thắt trái
cùa tim (G3/4: 0,3%)
Rối loạn mảu và hệ bạch huyết
Giảm bạch cầu trung tính
(G374: 32%);
Thiêu máu (G37'4: 4,9%)
Giảm tiêu cẩu (6374:
0,6%);
Giảm bạch cầu trung tính
có sốt
Rối loạn hệ thần kinh
Bệnh thần kinh cảm gỉảc
ngoại bỉẽn ((13/4: 1,2%);
Loạn vị giác (G314: 0%)
Bệnh thần kinh vận động
ngoại biên (GBÍ4: 0%)
Rối loạn mắt
Tăng chảy nước mắt
(63/4: 0,6%)
thất
Rối loạn hô hấp, ngực và trung
Chảy máu cam (6314:
0%); Khó thở (G3/4:
0,6%); Ho (G374: 0%)
Rối loạn tiêu hóa
Buồn nôn (6374: 2,4%);
Tiêu chảy ((ì3/4: 1,2%);
Viêm míệng/Viêm họng
(6374: 0,9%); Nỏn (6374:
CỀ(
f
1,2%)
:. , , Rụng tóc; Rối loạn móng Ban tróc vảy (G3/4:
R01 Ioạn da va mo duơ1 da (không nặng) 03…
Rội loạn hệ cơ xương và mô liên Đau khởp (G3/4: 0,3%);
kêt Đau cơ (G314: 0,3%)
Rối loạn tim
Cảc trường hợp hiếm gặp về nhồi máu cơ tim đã được báo cáo.
Rối loạn mắt
%
I
Các trường họp rất hiểm gặp về rối ioạn thị giảc thoáng qua (lóc sảng, ánh sáng nhấp nháy,
ám điếm) thường xảy ra trong khi truyền thuốc nảy vả kểt hợp với phản ứng quả mân dã
được báo cáo. Những phản ứng nảy có hồi phục khi ngừng truyền thuốc. Các trường hợp
chảy nước mắt có hoặc không có viêm kết mạc, như trường hợp tắc ống lệ đạo dẫn đến
chảy nước mắt trản trụa hiếm gặp dã được bảo cảo.
Rối loạn máu vả hệ bạch huyết
Ức chế tủy xương và các phản ứng bất lợi về huyết học khác đã được bảo cáo. Đông mảu
rải rác trong lòng mạch (DIC), thường kết hợp với nhiễm khuẩn hoặc suy nhiếu cơ quan đã
được báo cáo.
Rối Ioạn hệ thần kinh
Các trường hợp hiếm gặp về co giật hoặc mất ý thức thoáng qua đã được quạn sát thấy khi
dùng docctaxcl. Những phán ửng nảy đôi khi xuât hiện trong khi truyền thuôo nảy.
27
Rối ioạn tai và mô đạo
Những trường hợp hiếm gặp về độc tính đối với tai, suy giảm thinh giảc vả/hoặc mất thính
giảc dã được báo cảo.
Rối loạn hô hấp, ngực và trung thất
llội chứng suy hô hấp cẳp, viêm phổi kẽ/viêm phổi, bệnh phổi kẽ, xơ hóa phổi, suy hô hấp
và hiện tượng nhớ lại bức xạ hiếm gặp đã dược bảo cảo và có thế Iiẽn quan với kết quả gây
tử vong. Nhũng trường hợp hiếm gặp về viêm phối do tia xạ đã được bảo cảo ở những bệnh
nhân được xạ trị đồng thời.
Rối loạn tiêu hóa
Mất nước hiếm gặp như là hậu quả cùa phản ứng dạ dảy ruột, thủng dạ dảy ruột, viêm đại
trảng do thiếu mảu cục bộ, viêm dại trảng và viêm ruột giảm bạch cầu trung tính đã được
báo cảo. Những trường hợp hiếm gặp vô tắc ruột đã dược bảo cảo.
Rối Ioạn da và mô dưới da
Những trướng hợp rất hiếm gặp về Iupus ban dó ở da và phát ban bóng nước như ban đó
đa dạng, hội chứng Stevens—Johnson, hoại tứ, biếu bi nhỉễm độc đã được bảo cáo với
doeetaxel. '1`rong một sô trường hợp, các yêu tô đông thời có thế đã góp phân vảo sự phát
triên của nhũng tảc dụng nảy. Thay đôi dạng cứng bị thường có phù bạch huyêt ngoại biên
trước do dã được bảo cảo với doeetaxel.
Khối u lảnh tinh, ảc tính vả không xảc định (bao gồm nang và polyp) -
Những trường hợp rất hiếm gặp về bệnh bạch cầu cấp dòng tùy vả hội chứng loạn sản tùy
đã được bảo cáo liên quan với docctaxci khi được sử dụng kêt hợp với các thuôc hóa trị
khảc vả/hoặc xạ trị.
Rối loạn mạch
Biến cố thuyên tắc huyết khối tĩnh mạch hiểm gặp đã được bảo cảo.
Rối Ioạn toản thân và tình trạng tại chỗ tiêm truyền
Hiện tượng nhớ lại bức xạ hiếm gập dã dược: bảo cáo.
Ú dịch không kèm theo dợt cấp cùa thiếu niệu hoặc hạ huyết áp. Mất nước vả phù phối
hiếm gặp dã được báo cảo
Rối Ioạn hệ miễn dịch
Một số trường hợp sốc phản vệ, đôi khi gây tử vong, đã được báo cảo.
Rối Ioạn gan mật
Những trường hợp rất hiếm gặp về viêm gan, dôi khi gây tử vong, chủ yếu ở những bệnh
28
nhân bị rối loạn gan trước dó, đã được báo cảo.
Thông bảo cho bác sỹ những tác dụng không mong muốn gặp phải khi dùng thuốc
C] QUÁ LIÊU
Có một vải bảo cảo về quá iiếu Không có thuốc giải độc nảo được biết đối với quá liều
docctach Trong trường hợp quá liều, bệnh nhân cân được chăm sóc trong một đơn vị
chuyên khoa và theo dõi chặt chẽ cảc chức năng sống. Trong trường hỌp quả iiều, đợt cấp
của cảc tảo dụng bất iợi được dự kiến sẽ xảy ra. Cảo biến chứng dự đoán chính cùa quả liếu
bao gồm ức chế tùy xương, độc tính thần kinh ngoại biên và vỉếm niêm mạc. Bệnh nhân
cần được điều trị bằng G- CSF cảng sóm cảng tốt sau khi phảt hiện quá liều. Cẩn thực hiện
các biện pháp điếu trị triệu chúng thích hỌp, khi cẳn thiết
[] CÁC ĐẶC TÍNH DƯỢC LÝ
[Các đặc tinh dược lực học]
> Nhóm dược lý trị iỉệu: Thuốc chống ung thư %
(
› Dữ liệu tiền lâm sảng
1. Docetaxel là một thuốc chống ung. thư tác đụng bằng cảch thủc đấy sự tập hợp cảc tubulin
thảnh các vi ống ổn dịnh vả ức chế sự tháo ra cùa chúng dẫn đến gỉảm đáng kể tubulin tự
do. Sự gắn kết cùa docctaer với các vi ống không lảm thay đối sô lượng cảc nguyên sợi
(prototilament).
2. Docetaxel đã được chứng minh in vitro iảm phá vỡ mạng lưới vì ống trong tế bảo mà đó lả
yếu tố cần thiết cho cảc chức năng sống cùa tế bảo trong gian kỳ và gián phân.
3. Docetaxel được tim thấy gây độc tế bảo“ … vỉtro chống lại cảc dòng tế bảo khối u khác nhau
cùa chuột công vả người và chống lại cảc tế bảo khối u của người mởỉ được cắt trong thử
nghiệm tạo dòng (clonogenic). Docetaxcl đạt nổng dộ cao trong tế bâo với thời gian lưu iại
1âu trong tế bảo. Ngoài ra, docctach được tìm thấy có hoạt tính đối với một số nhưng không
phải tất cả các dòng tế bảo qua biếu hiện p-glycoprotein được mã hóa bới các gen khảng đa
thuốc. In vivo, docctach không phụ thuộc vảo lịch trình dùng thuốc và có phố hoạt tính
chống khối u rộng trong thực nghiệm chống lại các khối u ghép tiến triến của chuột cống
vả ngưòi.
> Dữ liệu lâm sảng
1. Ung thư vú
o Docetaxel kết hợp vởi doxorubicin vả cyclophosphamid: điều trị bổ trợ
Dữ iiệu từ một nghiên cứu da trung tâm, nhăn mở, ngẫu nhiên hỗ trợ việc sử dụng đocetaxel
đề điểu trị bổ trợ cho những bệnh nhân bị ung thư vú có hạch bạch huyết dương tinh có thế
phẫu thuật và tinh trạng hoạt động cơ thể theo thang diếm Karnofsky (KPS) z 80%, từ 18
đến 70 tuổi. Sau khi phân tầng theo số lượng hạch bạch hưyết dương tính (1-3, 4+), 1491
bệnh nhân được chọn ngẫu nhiên dễ được điều trị hoặc băng docctaer 75 mglm² tiêm !
29
âJ
.nỰdv
..(l
giờ sau khi dùng doxorubicin 50 mg/m2 vả cyciophosphamid 500 mglm² (nhóm DAC),
hoặc bằng doxorubicin 50 mglm², tiếp theo 1ả i1uorouracil 500 mg1m² vả cyclosphmphamid
500 mg/m² (nhóm FAC). Cả hai chế dộ điếu trị được dùng một iần mỗi 3 tuân trong 6 chu
kỳ. Docctaxel được dùng truyền trong 1 giờ, tất cả các thuốc khác được dùng tiêm bolus
tĩnh mạch vảo ngảy thứ nhất. G- CSF được dùng để điếu trị dự phòng thứ phát cho những
bệnh nhân bị giảm bạch cầu trung tính phức tạp (giảm bạch cầu trung tính có sốt, giảm bạch
cầu trung tinh kéo dải hoặc nhiễm trùng). Những bệnh nhân ở nhóm DAC được điếu trị
kháng sinh dự phòng bằng ciprofloxacin 500 mg, uống 2 lẫn/ngây trong 10 ngảy bắt đẩu
vâo ngảy thứ 5 cùa mỗi chu kỳ, hoặc tương đương. Ở cả hai nhóm, sau chu kỳ cuồi cùa hóa
trị iỉệu, những bệnh nhân có thụ thể estrogcn dương tính vả/hoặc thụ thể _progcsterone
dương tính được điếu trị bằng tamoxifen 20 mg/ngảy trong 5 năm. Xạ trị bổ trợ được kê
don theo hướng đẫn tại chỗ tại các viện tham gia nghiên cứu và đã được sử dụng cho 69%
bệnh nhân được điều trị bằng DAC và 72% bệnh nhân được điếu trị bằng FAC.
Một phân tich giữa kỳ dưọc thực hiện với thời gian theo dõi trung bình 55 tháng. Tỷ lệ
sông còn không bệnh dải hơn có ý nghĩa đối với nhóm DAC so với nhóm FAC đã được
chứng minh. Tỷ lệ tải phảt sau 5 năm đã được giảm xuống ở bệnh nhân được đỉếu trị bằng
DAC so với những người dược điều trị bằng FAC (25% so vởi 32%, tương ứng) tức là giám
nguy cơ tuyệt dối 7% (p= 0 ,.001) Thời gian sống còn toản bộ 5 năm cũng tăng có ý nghĩa
với DAC so vởi FAC (87% so với 81%, tương ứng) tức là giảm tuyệt đoi vê nguy cơ tử
vong 6% (p= 0 ,0.08)
Các phân nhóm bệnh nhân được điều trị bằng DAC theo các yếu tổ tiên iượng quan trọng '
được xảc dịnh theo thời gian đã được phân tích:
Thời zian sống còn không bệnhl Thời gian sống còn toảu bộ
Phân nhóm bệnh sỏ bệnh Tỷ số K.hOả.ng _ Tỷ số Khoan _
nhân nhân nguy cơ* t1n cạy p _ nguy cơ* tm cạy p _
(C1) 95% (CI) 95%
Số hạch bạch huyết
đưong tính
'l`oản bộ 745 0,72 0,59-0,88 0,001 0,70 0,53-0,91 0,008 ị
1-3 467 0,61 0,46—0,82 0,0009 0,45 0,29-0,70 0,0002 !
4+ 278 0,83 0,63-1,08 0,17 0,94 0,66-1,33 0,72 ;
' tỷ số nguy cơ dưới 1 cho thấy DAC có liên quan với một thòi gian sống còn không bệnh và
thời gian sông còn toân bộ dải hơn so với FAC.
Tác dụng có lợi cùa DAC chưa được chứng minh ở những bệnh nhân có hạch bạch huyết
dương tính giai đoạn 4 trở lên (37% của nhóm đối tượng nghiên cứu) trong giai đoạn phân
tích giữa kỳ. Hiệu quả dường như it rõ rệt hơn ở những bệnh nhân có hạch bạch huyết
dương tính giai đoạn 1-3.'1`ỳ1ệ lợi íchlnguy cơ chưa được xác định đầy đủ trên những bệnh
nhân có hạch bạch huyết dương tính giai đoạn 4 trở lên ở giai doạn phân tích nảy.
Bênh nhản bi ung Ihư vú có hach bach huyết âm tỉnh có Ihế phẫu lhuát đủ điều kién đế
đươc dùng hóa m“ liêu (GEICA M 9805 )
Dữ 1iệu từ một thử nghiệm da trung tâm, nhãn mớ, ngẫu nhiên hỗ trợ việc sử dụng docctaer
đế điếu trị bổ trợ cho bệnh nhân bị ung thư vú có hạch bạch huyết am tính có thề phẫu thuật
đủ điếu kiện để được đùng hóa trị liệu. 1060 bệnh nhân được chọn ngẫu nhiên đề được điều
30
trị hoặc bằng docctaxci 75 mg/m² tiếm 1 giờ sau khi dùng đoxorubicin 50 mglm² vả
cyciophosphamid 500 mgfm² (539 bệnh nhân ở nhóm DAC), hoặc bằng doxorubicin 50
mglm², tỉêp theo lá fluorouracil 500 mglm² vả cyclosphosphamid 500 mglm² (521 bệnh
nhân ở nhóm FAC) như lá diếu trị bổ trợ cho bệnh nhân bị ung thư vú có hạch bạch huyết
âm tinh có thế phẫu thuật vởi nguy cơ tải phát cao theo tiêu chuẩn St. Gallen 1998 (khối 11
có kich thước > 2 cm vảJhoặc thụ thể estrogcn (ER) vả thụ thể progestcron (PR) am tinh
vá/hoặc cấp độ cao về mô học/nhân (độ 2-3) vảlhoặc < 35 tuổi). Cả hai chế độ điếu trị được
dùng một iằn mỗi 3 tuần trong 6 chu kỳ. Docctaxei dược dùng truyền trong 1 giờ, tất cả cảc
thuếc khác được dùng tiêm tĩnh mạch vảo ngảy thứ nhắt mỗi 3 tuan. Điếu trị dự phòng ban
đẩu bằng G- CSF đã được thực hiện bắt buộc ở nhóm DAC sau khi 230 bệnh nhảm được
chọn ngân nhiến Ty 1ệ giảm bạch cầu trung tinh độ 4 iảm bạch cầu trung tinh có sốt và
nhiễm trùng giảm bạch câu trung tính đã được giảm xuong ở những bệnh nhân dược điếu
trị dự phòng ban đẩu bằng G-CSF (xem "1 ÁC DỤNG KIIỎNG MONG MUỐN). Ở cả hai
nhóm sau chu kỳ cuỏi cùa hỏa trị liệu, bệnh nhân bị khối 1.1 có thụ thể estrogen đương tính
(ER’) vả1hoặc thụ thể progestcron dương tính (PGRỔ) được điều trị bằng tamoxifcn 20 mg,
] lầningảy cho đến 5 năm Xạ trị bổ trợ được dùng theo hướng dẫn tại chỗ tại cảc viện tham
gia nghiên cứu và đã đuợc sử dụng cho 57, 3% bệnh nhân được điếu trị bằng DAC và 51, 2%
bệnh nhân được điếu trị bằng Ĩ`AC. Thò1 gian theo đõi trung bình 1ả 77 tháng. Tỷ lệ sống
còn không bếnh dải hơn có ý nghĩa đối với nhóm DAC so với nhóm FAC đă đuợc chứng
minh. Những bệnh nhân đuợc điêu trị bằng DAC đã giám 32% về nguy cơ tái phát so với
những người điều trị bằng I`AC (tỷ số nguy cơ= 0,68, khoảng tin cậy (CI) 95% (0, 49- 0 ,93),
p = 0,01). Thời gian sống còn toản bộ (OS) cũng dải hon ở nhóm DAC với các bộnh nhân
được điều trị bằng DAC có giảm 24% về nguy cơ tử vong so với nhóm FAC (tỷ số nguy cơ
= 0,76, khoảng tin cậy (CI) 95% (0,46—1,26, p = 0,29). Tuy nhiên, sự phân bố thời gian
sống còn toản bộ (OS) không khác biệt có ý nghĩa giữa 2 nhóm.
Các phân nhóm bệnh nhân được diều trị bằng DAC theo các yếu tổ tiên lượng quan trọng
được xảc định theo thời gian dã được phân tich (xem bảng dưới đây): ffl'1
Phân tich phânnhóm-Điều trị bổ trợ trong nghiến cứu ở những bệnh nhân bị ung thư vú có
hạch bạch huyêt âm tính (Phân tích theo ý định điêu trị — Intention-To-Trcat, ITT)
; . . Tỷ lệ sông eòn không bệnh
Phân nhủm bệnh nhân Ễonlitỉ'tẺ E'Ẩ'ẻ' Tỷ số Khoảng tin cậy
nguy cơ* (CI) 95%
Toản bộ 539 0,68 0,49-0,93
Nhóm tuổi 1 “' "
, < 50 …ồi 260 0,67 0,43…1,05
( ì 50 tuồi 279 0,67 0,43-1,05
) Nhóm tuổi 2
<3510ô1 42 0,31 0,11-0,89
>_— 35 tuồi 497 0,73 0,52-1,01
Thụ thề hormon
Ấm tinh 195 0,7 0,4511
Dương tính 344 0,62 0,4-0,97
Kich thước khôi 11
S 2 cm 285 0,69 0,43-1,1
> 2 cm 254 0,68 0,45-1,04
ỉátìẹtneéhto , ___ ___ ******
31
i Độ [ (bao gồm cả cấp dộ không
, dược dánh giá) 64 0,79 0,24-2,6
Dộ 2 2I6 0,77 0,46-1,3
i _D_ộ3 _ _ 259 0,59 0,39-0,9
'l`ìhh trạng mãn kinh
'l`iền măn kinh 285 0,64 0,40-1
Hậu mãn kinh 254 0,72 0,47-1,12
* tỷ số nguy cơ (DAC/FAC) dưới I cho thẩy DAC có liên quan với một tỷ lệ sống còn không
ii.
bệnh vả tỷ lệ sống còn toản bộ dải hon so với FAC.
Phân tich phận nhóm thăm dò về tỷ lệ sống còn không bệnh dối với những bệnh nhân đáp
ứng tiêu chuân hóa trị liệu St. Gallcn 1998 - (nhóm ITT) đã dược thực hiện và trình bảy
dưới đây
. — _ Tỷ sỂnguy cơ 1
, _ DAC FAC mACIFAC) ,
Phân nhóm (n=539) (n=521) (KĨỄĨỄIỄỄỀZĨạy Trị sô p—
ảD—áp—ứng chi dịnh tưong
đối về hóa trị liệu _
| Không i872i4 (8,4%) 267227 (11,5%) 0,796 (0,434 — I,459) 0,4593 _
1 Có 487325 (14,8%) 697294 (23,5%) 0,606_(0,42 - 0,877) 0,0072 i
DAC = docctaxcl, doxorubicin vả cyclophosphamid FAC = 5—fluorouraeil, doxorubicin vả
cyclophospamid Cl = khoảng tin eậy (coníidcnce interval) ER = thụ thể estrogen (estrogen
receptor) PR = thụ thể progestcron (progesterone receptor).* ER/PR âm tinh hoặc độ 3 hoặc
kích thước khối u > 5 cm
Tỷ số nguy cơ ước tính đã sử dụng mô hình cảc nguy cơ tương xứng Cox với nhóm diều
trị là hệ sô.
Docetaxel dưới dạng thuốc đơn độc ffl1
2 nghiên cứu so sánh, ngẫu nhiên, pha … bao gồm tống cộng 326 bệnh nhân bị ung thư vú
di căn thất bại với thuôo alkyl hóa hoặc 392 bệnh nhân bị ung thư vú di căn thât bại với
anthracyclin, đã dược sử dụng docctaer ở liều khuyến cáo và chế độ liều dùng 100 mg/m²
mỗi 3 tuần.
Ở những bệnh nhân thất bại với thuốc alkyl hóa, docctaer đã được so sánh với doxorubicin
(75 mglm² mỗi 3 tuần). Không có ảnh hướng dến thời gian sống còn toản bộ (docctaer 15
tháng so với doxorubicin 14 thảng, p = 0,38) hoặc thời gian dẫn dển tiến triến bệnh
(docctach 27 tuần so vởi doxorubicin 23 tuần, p = 0,54), docctaer đã lảm tăng tỷ lệ đảp
ứng (52% so với 37%, p = 0,01) vả rủt ngắn thời gian dẫn đến đáp ứng (12 tuần so với 23
tuần, p = 0,007). 3 bệnh nhân được diều trị bằng docctaer (2%) ngưng điều trị do ứ dịch,
trong khi i5 bệnh nhân được đỉều trị bằng doxorubicin (9%) ngưng điều trị do độc tinh đối
với tim (3 trường hợp suy tim sung huyết gây tử vong).
Ở những bệnh nhân thất bại với anthracyciin, docctaer được so sảnh với dạng kết họp
mitomycin C vả vinblastỉn (12 mg/m² mỗi 6 tuần và 6 mglm² mỗi 3 tuân). Docetaxel lảm
32
vì
Ivl
…:-e'”
tăng tỷ lệ đảp ứng (33% so với 12%, p < 0 ,,0001) kéo dải thời gian dẫn đến tiến triền bệnh
(19 tuân so với 1 1 tuần, p= 0 ,0004) và kéo dải thời gian sống còn toản bộ (11 thảng so với
9 thảng, p= 0 ,.01)
Trong 2 nghiên cửu pha III nảy, hồ sơ an toản cùa docctaxcl đồng nhất với hồ sơ an toân
được quan sát thẩy trong cảc nghiên cứu pha 11 (xem TÁC DỤNG KHÓNG MONG
MUÔN).
Một nghiên cứu pha 111, nhãn mở, đa trung tâm, ngẫu nhiên đã được tiến hảnh để so sảnh
docctach don trị liệu và paclitaxel trong điều trị ung thư vú tiến triến ở những bệnh nhân
có diều trị trước dó bao gôm một anthracyclin. Tổng cộng có 449 bệnh nhân được chọn
ngẫu nhỉên đế được điều trị hoặc bằng docctach đơn trị liệu 100 mg/m² truyền trong
1 giờ hOặc paclitaxel 175 mg/m² truyền trong 3 giờ. Cả hai chế độ điều trị được dùng mỗi
3 tuần.
Không ảnh hưởng dến tiêu chí đảnh giá chính, tỷ lệ đảp ửng chung (32% so với 25%, p —
0,10), docctaer kéo dải thời ẹian trung bình dẫn đến tiến triến bệnh (24, 6 tuần so với 15,6
tuần; p < 0,01) vả thòi gian song còn trung bình (15,3 thảng so với 12,7 thảng; p= 0 ,0.3)
Cảc phán ứng bất 1ợi dộ 374 dược quan sát thấy nhiều hơn đối với đơn trị liệu bằng docctaer
(55,4%) so với paclitaxcl (23,0%). (D1
Docetaxel kết hợp với doxorubicin
Một nghiên cứu lớn pha 111, ngẫu nhiên bao gồm 429 bệnh nhân bị bệnh di căn, trước đó
chưa dược điều trị, dã dược thực hiện với doxorubicin (50 mglm²) kểt hợp với docctaer
(75 mg/m²) (nhóm AD) so với doxorubicin (60 mglm²) kết hợp với cyclophosphamid (600
mglm²) (nhóm AC). Cả hai chế độ điều trị được dùng vảo ngảy thứ nhất mỗi 3 tuần.
Thời gian dẫn đến tiến triến bệnh (’ITP) dải hơn có ý nghĩa ở nhóm AD so với nhóm AC,
p = 0,0138. Thời gian trung bình dẫn đện tìên triên bệnh là 37,3 tuân (khoảng tin cậy (CI)
95%: 33,4-42,1) ở nhóm AD vả 31,9 tuân (khoảng tin cậy 95%: 27,4-36,0) ở nhóm AC.
Tỷ lệ đáp ứng chung (ORR) cao hơn có ý nghĩa ở nhỏm AD so với nhóm AC, p = 0,009.
Tỷ lệ đáp ứng chung là 59,3% (khoảng tin cậy (CI) 95%: 52,8-65,9) ở nhỏm AD so với
46,5% (khoảng tin cậy 95%: 39,8-53,2) ở nhóm AC.
Trong nghỉôn cứu nảy, nhóm AD cho thắy một tỷ lệ cao hơn về giảm bạch cầu trung tính
nặng (90% so với 68 ,,6%) giảm bạch câu trung tính có sốt (33, 3% so với 10%), nhiễm trùng
(8% so với 2,4%), tiêu chảy (7, 5% so với 1,4%), suy nhược (8,5% so với 2 4%) và đau
(2,8% so với 0%) so với nhóm AC. Mặt khác, nhóm AC cho thấy một tỷ lệ cao hơn về thiếu
máu nặng (15,8% so với 8,5%) so với nhỏm AD. Ngoài ra, một tỷ lệ cao hơn về độc tinh
dối với tim nặng: suy tim sung huyết (3,8% so với 2,8%), giảm phâp số tống máu thất trái
(1 VE1` ) tuyệt đôi > 20%(13,1% so với 6,1%), giảm LVEF tuyệt đôi > 30% (6, 2% so với
1 ,.I%) | ư vong do nhiễm độc xảy ra ở 1 bệnh nhân ở nhóm AD (suy tim sung huyết) và 4
bệnh nhân ở nhóm AC (! do sốc nhỉễm khuấn và 3 do suy tim sung huyết).
Ở cả hai nhóm, chất lượng cuộc sống được đảnh giá bằng Bảng câu hòỉ theo Tổ chức
Nghiên cứu và Điều trị Ung thư châu Âu (EORTC) tương đương nhau và ổn định trong quá
trình điều trị và theo dõi.
33
o Docctaxcl kết hợp vởi trastuzumab
Docctaxel kết hợp với trastuzumab dã được nghiên cứu trong điếu trị bệnh nhân bị ung thư
vú di căn mả khối u có biểu hiện quá mức HER2 và những người trước đây chưa được dùng
hóa trị liệu đối với bệnh di cãn. 186 bệnh nhân được chọn ngẫu nhiên đề được điểu trị bằng
docctaer (100 mglm²) có hoặc không có trastuzumab; 60% bệnh nhân được dùng hóa tri
liệu bổ trợ dựa trên anthracyclin. Docctaxcl cộng với trastuzumab có hiệu quả ở những
bệnh nhân dù họ có được điếu trị trước bằng anthracyciin hay không. Phương pháp thử
nghiệm chính dược sử dụng để xảc định HER2 dương tinh trong nghiên cứu then chốt nảy
là hóa mô miễn dịch (11 1C). Một số ít bệnh nhân đã được thử nghiệm sử dụng kỹ thuật lai
huỳnh quang tại chỗ (FISH). Trong nghiên cứu nảy, 87% bệnh nhân bị bệnh có IHC 3+ và
95% bệnh nhân được đưa vảo nghiến cứu bị bệnh có IHC 3- + vả/hoặc FISH dương tính Kết
quả về hiệu quả được tóm tắt trong bảng sau:
› Docetaxcl cộng với Docetaxcl'
Thông số trastuzumabl n = 94
, _ n = 92
1 Tỷ lệ dảp ứng (khoảng tín cậy (Ci) , _ , _
95%) 61A›(50 71) 34/o (25 45)
Thời gian dáp ứng trung bình (thảng) _ _
Ịkhoảngtiilẵcẳy 95%2 † … 11,—4 (9,2 15,0) 5,1 (4,4 6,2)
Thời gian d n dcn tiến triễn bệnh ('1“1`P) _ _
trugg binh (thảng) (khoảng tin cậy 95%) 10’6 (7’6 12’9) 5’7 (5’0 6’5)
'I`hòi gian sống còn trung bình (tháng) 2 _ 2 _
_(khoảng tỉn cậy 95%) 30,5 (26,8 nc) 22,1 (17,6 28,9)
1TP = Thời gỉan dẫn dến tiến triến bệnh (time to progression); “nc” chi ra rằng không thể
ước tính hoặc chưa dạt dược.
lBộ phân tich đầy dù (theo )? dịnh diễu trị) ² Thời gian sống còn trung binh ước tính
0 Docctaxcl kết hợp với capecitabin 071
Dữ 1iệu từ một nghiên cứu lâm sảng pha 111, đa trung tâm, ngẫu nhiên, có đối chứng hỗ trợ
việc sử dụng docctach kết hợp với capccitabin để điều trị bệnh nhân bị ung thư vú tiến
triến tại chỗ hoặc di căn sau khi thất bại với hóa trị iiệu gây độc tế bảo, bao gồm cả
anthracyclin. Trong 2nghiến cứu nảy, 255 bệnh nhân được chọn ngẫu nhiên dễ điều trị bằng
docctaer (75 mg/m2 truyền tĩnh mạch trong 1 giờ mỗi 3 tuần) và capecitabin (1250 mglm²,
2 lần/ngảy trong 2 tuần, tiếp theo là một thời gian nghỉ 1 tuần). 256 bệnh nhân được chọn
ngẫu nhiến đề điếu trị bằng docctach đơn độc (100 mg/m2 truyền tĩnh mạch trong | giờ
mỗi 3 tuần). Thời gian sông còn trội hơn ở nhóm dùng kết hợp docctach + capecitabin (p
= 0 ,0.126) I`hời gian sống còn trung bình là 442 ngảy (docctaer t capecitabin) so với 352
ngảy (docctach dơn độc). Tỷ lệ dáp ứng mục tiêu chung trong tất cả nhóm nghiến cứu được
chọn ngẫu nhiên (đảnh giả của nhả nghiên cứu) lả 41,6% (docctach + capecitabin) so với
29, 7% (docctach đơn dộc); p= 0, 0058. Thời gian trung bình dẫn đến tiến triển bệnh cao
hơn ở nhóm dùng kết hợp docctach + capecitabin (p < 0 ,0001) Thời gian trung bình dẫn
dến bệnh tiến triên là 186 ngảy (docctaer + capecitabin) so với 128 ngảy (docctach đơn
dộc).
34
2.
Ung thư phổi không tế bảo nhỏ
Bệnh nhân trước đó được điều trị bằng hóa trị liệu có hoặc không có xạ trị
Trong một nghiên cứu pha 111 ở những bệnh nhân được điều trị trước đó, thời gian dẫn đến
tiến triến bệnh (12,3 tuần so với 7 tuần) và thời gỉan sống còn toản bộ dải hon có ’nghĩa
đối với docctaer ở lỉều 75 mg/m² so với chăm sóc hỗ trợ tốt nhất (BSC). Tỷ lệ sông còn
1 năm cũng dải hơn có ý nghĩa đối với docctaer (40%) so với chăm sóc hỗ trợ tốt nhất
(16%). Có sự sử dụng ít hơn về thuốc giảm đau morphin (p < 0 ,,01) thuốc giảm đau không
morphin (p < 0 ,,01) các thuốc khác liên quan đến bệnh (p= 0,06) và xạ trị (p < 0 0,1) ở
những bệnh nhân được điều trị bằng docctaer 75 mg/m² so với những người được chăm
sóc hỗ trợ tốt nhất Tỷ lệ đảp ứng chung lả 6, 8% ở những bệnh nhân có thế đảnh giả, và
thòi gian đảp ứng trung bình là 26,1 tuần.
Docetaxel kết hợp với thuốc platin ở bệnh nhân chưa từng được dùng hóa trị liệu 0Ễ1
T rong một nghiên cứu phalll, 1218 bệnh nhân bị ung thư phối không tế bảo nhỏ (NSCLC)
giai đoạn 11113 hoặc IV không thể cắt bò, với tình trạng hoạt động cơ thể theo thang điềm
Karnofsky (KPS) 70% hoặc cao hơn, và những nguời chưa được hóa trị liệu trước đó đổi
với tinh trạng nảy, được chọn ngẫu nhiên hoặc được điểu trị bằng docctaer (D) 75 mg/m2
truyền trong 1 giờ, tiếp theo ngay bằng cisplatin (Cis) 75 mg/m2 trong 30— 60 phút mỗi 3
tuần (DC15), docctach 75 mg/m2 truyền trong 1 giờ kết hợp với carbopiatin (AUC 6 mg]
ml. phút) trong 30-60 phủt mỗi 3 tuần, hoặc vinorelbine (V) 25 mg/m2 tiếm trong 6- 10 phút
vảo các ngây 1, 8, 15, 22, tiếp theo lá cisplatin 100 mg/m2 tiêm vảo ngảy thứ nhất cùa cảc
ehu kỳ, được lặp lại mỗi 4 tuần (VCis).
Dị: lỉệu về thời gian sống còn, thời gian trung bình dẫn đến bệnh tiến triến và tỷ lệ đảp ứng
đôi vói 2 nhóm của nghiên cứu được trinh bảy trong bảng sau:
DCis n = 408 VCis n = 404 Phân tích thống kê
1
Thời gian sỗng còn toản bộ
(Tiêu chí đảnh giá chinh):
Thời gỉan sống còn trung
bình (tháng)
11,3
10,1
Tỷ số nguy cơ: 1,122
[Khoảng tin cậy (CI)
97,2%: 0,937; 1,342]*
Sống còn 1 năm (%) 46 41 Khảo biệt về điều trị: 5,4%
[Khoảng tin cậy 95%: -1,1;
' 12,0] 1
Sông còn 2 năm (%) 21 14 Khác biệt về điều trị: 6,2% 1
[Khoảng tin cậy 95%: 0,2;
12,3]
, .. . , 'x 7 Tỷ số nguy cơ: 1,032
1 hơi gian trung binh dan đen . . ,
.7 .i , A _ 22,0 23,0 [Khoang tin cạy 95%:
mm truen bẹnh (tuan). 0,876; 1,216]
Khảc biệt về điểu trị: 7,1% ,
Tỷ lệ đảp ứng chung (%): 31,6 24,5 [Khoảng tin cậy 95%: 0,7;
13,5]
:Hiệu chinh đối với so sảnh bội số và điều chinh các hệ số phân tẩng (giai đoạn bệnh và vùng
diều trị), dựa trên nhóm bệnh nhân có thế đánh giá.
35
`
iif.ì f _
Cảc tiêu chi phụ bao gồm thay đổi vê đau, đánh giá chung về chẳt lượng cuộc sống theo
thang điềm EuroQoL- 5D, thang đỉếm triệu chứng ung thư phối và nhũng thay đối vê tình
trạng hoạt dộng cơ thể theo thang điếm Karnofsky. Kết quả vê nhũng tiêu chí nảy đến hổ
trợ kết quả vế tiếu chí đảnh giả chính
Đối với sự kểt họp đocctaxel/carboplatin, không có hìệu quả tương đương và cũng không
có hiệu quả thua kém nảo có thể được ehứng mỉnh so vởi VCìs là dạng kết hợp điểu trị
tham chiêu
Ung 11… tuyến tiến liệt
Độ an toản và hiệu quả của docctaer kết hợp với prednison hoặc prednisolon ở bệnh nhân
bị ung thư tưyến tiền liệt di cãn kháng trị vởi hormon đă được đánh gìá trong một nghiên
cứu pha 111, ngẫu nhiên, đa trung tâm. Tổng cộng có 1006 bệnh nhân với KPS > 60 được
chọn ngẫu nhiên vảo cảc nhóm diều trị sau đây: O)T
;
Docetaxel 75 mg/m² mỗi 3 tuần trong 10 chu kỳ.
Docetaxel 30 mg/m2 tìêrn hảng tuần trong 5 tuần đầu tiên ở một chu kỳ 6 tuần trong 5 chu
kỳ.
Mitoxantrone 12 mg/m2 mỗi 3 tuần trong 10 chu kỳ.
Tẩt cả 3 chế độ điếu trị được dùng kết hợp với prednison hoặc prednisolon 5 mg, 2 lẩnlngảy,
iiẽn tục.
Nhũng bộnh nhân dược diều trị bằng docctaer mỗi 3 tuần đã cho thấy thời gian sống còn
toản bộ dải hơn có ý nghĩa so với những người điếu trị bằng mitoxantrone. Sự tâng thời
gian sống còn được thấy ở nhóm dùng docctaer hảng tuần không có ý nghĩa thống kê so
với nhóm đối chứng đùng mitoxantrone. Tiếu chi vế hiệu quả đối với nhóm docctaer so
với nhóm đối chứng được tóm tắt trong bảng sau:
Tiêu chí Docetaxel mỗi 3 tuần Docetaỉtel mỗi Mit23tantrfnơ:
tuan m013 tuan
Sô bệnh nhân 335 334 337
Thời gian sống còn 18.9 17,4 16.5
trưng binh (tháng)
Khoảng tin cậy (CI) (17,0~21,2) (15,7-19,0) (14,4~18,6)
95%
Tỷ số nguy cơ 0,761 0,912 …
Khoảng tin cậy 95%; (0,619-0,936); 0,0094 (0,747-1,113); —-' --
'i`rị số p~i* 0,3624
sớ bệnh nhân 291 282 300
Tỷ lệ đáp ứng đối với 45,4 47.9 31.7
PSA** (%) (39,5-51,3); 0,0005 (41,9-53,9); (26,4-37,3) ; -—
Khoảng tỉn cậy 95%; < 0,0001
( 'l`rị số p*
1 Số bệnh nhân ' 153 154 157
( Tỷ lệ đảp ứng dôi vói 34.6 31,2 21,7
36
An 'A.\ ` A—
đau (%)
Khoáng tin cậy 95%; (27,1-42,7); 0,0107 (24,0-39,1); 0,0798 (15,5-28,9); --
Trị sô p*
, 86 bệnh nhân ' 141 134 137
Tỷ lệ đảp ứng dôi với 12,1 8,2 6,6
khối u (%)
Khoảng tin cậy 95%; (7,2-18,6); 0,1 1 12 (4,2-14,2); 0,5853 (3,0-12,1); --
Trổ…
7 Kiếm định log rankphân tầng *Ngưỡng có ý nghĩa thống kê = 0,0175 ** PSA: Kháng
nguyên đặc hiệu tuyên tiến 1iệt(Prostate-Specific Antigen)
Do thục tế là docctaer dùng mỗi tuần thể hiện một hồ sơ an toản tốt hơn một chút so với
docctaxcl mỗi 3 tuần, có khả năng lả một số bệnh nhân có thế có lợi từ việc dùng docctaer
mỗi tuần.
Không có sự khảc biệt về mặt thống kê được quan sát thấy giữa các nhóm điều trị về chất
lượng cuộc sống nói chung.
4. Ung thư biều mô tuyến dạ dảy CĐ)
Một nghiến cứu da trung tâm, nhãn mở, ngẫu nhiên đã được tiến hảnh đế dánh giá độ an
toản và hiệu quảẫ của docctaer trong điểu trị cảc bệnh nhân bị ung thư biểu mô tuyến dạ
dảy dì căn, bao gồm cả ung thư chỗ nôi dạ dảy-thực quản, chưa được dùng hóa trị liệu trưởc
đó đối với bệnh di căn. Tông cộng có 445 bệnh nhân với KPS > 70 đã được điều trị hoặc
bằng docctaer (D) (75 mg/m2 vảo ngảy thứ nhất) kết hợp với cisplatin (C) (75 mg/rri2 vảo
ngảy thứ nhắt) vả 5-11uorouracil (F) (750 mg/m²lngảy trong 5 ngảy) hoặc cisplatin (100
mg/m2 vâo ngảy thứ nhất) và 5-fluorouracil (1000 mglm²lngảy trong 5 ngảy). Thời gian
cùa một chu kỳ điếu trị là 3 tuần đổi vói nhỏm DCF vả 4 tuần đối với nhóm CF. Số lượng
chu kỳ trung bỉnh sử dụng cho mỗi bệnh nhân lả 6 (vởi phạm vi từ 1-16) đối với nhóm DCF
so với 4 (với phạm vi từ 1—12) đối với nhóm CF. Thời gian dẫn đến tiến triển bệnh (TTP)
là tiêu chí đánh giá chinh. Sự giảm nguy cơ tiến triển là 32,1% và có liên quan với thời gian
dẫn dến tiển triền bệnh dải hơn có ý nghĩa (p = 0,0004) thiến về nhóm DCF. Thời gian sống
còn toản bộ cũng dải hơn có ý nghĩa (p = 0,0201) thiên về nhóm DCF với một sự giảm
nguy cơ tử vong 22,7%. Kết quả về hiệu quả được tóm tắt trong bảng sau:
Hiệu quả của docctach trong diếu trị bệnh nhân bị ung thư biều mô tuyến dạ dảy
Tiêu chí DCF, n = 221 CF, n = 224
Thời gian trung bình dẫn đến tiến triển bệnh _ _
(tháng); (Khoảng tin cậy (Cl) 95%) 5’61(4186'5'91) 317’ (3145'4’47)
Tỷ số nguy cơ; (Khoảng tin cậy 95%); *Trị số p 1,473; (1 ,189-1,825); 0,0004 |
Thòi gian sống còn trung bình (thảng); (Khoảng 9,2; (8,38- 8,6; (7,16-9,46); '
tỉn cậy 95%); ước tính 2 năm (%) 10,58); 18,4 8,8
, Tỷ số nguy cơ; (Khoảng tỉn cậy 95%); *Trị số p 1,293, (1,041-1,606); 0,0201
Ê lệ đảp ứng chung (CR+PR) (%) Trị số p 36,7 [ 25,4
0,0106
Bệnh tỉến triến dưới dạng đáp ứng chung tốt 16,7 25,9
, phât__(%)
37
,Ìh'ì
* Kiếm định logrank phân tầng
Phân tich phân nhóm theo tuồi, giởi tính và chủng tộc dều đổng nhất thiên về nhóm DCF
so với nhóm CF.
Một phân tích cập nhật về sự sống còn được tiến hảnh với thời gian theo dõi trung bình
41, 6 thản khôn còn cho thấy sự khảo biệt có ý nghĩa thống kế mặc dù [uôn 1uônthiên về
chế dộ điếu trị băng DCF và cho thấy lợi ich eùa DCF hơn CF được quan sát thấy rõ rảng
giữa 18 thảng và 30 thảng theo dõi.
Nhìn chung, chẩt lượng cuộc sống (QOL) và kết quả lợi ích lâm sảng luôn cho thấy sự cải
thiện thiến về nhóm DCF. Nhũng bệnh nhân được đỉều trị bằng DCF đã có một thời gian
dải hơn dẫn đến 5% suy giảm rõ rảng về tình trạng sức khỏe chung theo Báng câu hỏi QLQ-
C30 (p 0 ,0121) và một thời gỉan dải hon dẫn đến sự xấu đi rõ râng vô tình trạng hoạt
động cơ thể theo thang diểm Karnofsky (p= 0 ,0088) so với bệnh nhân được điều trị bằng
CF.
5. Ung thư dầu và cổ fflĨ
'
o Hỏa trị liệu ban đầu, tiếp theo lá xạ trị (TAX3Z3)
Độ an toản và hiệu quả cùa docctaer trong điều trị ban đầu ở bệnh nhân ung thư biều mô
tế bảo vảy dầu và cố (SCCHN) đã được đánh giá trong một nghiên cứu pha III, đa trung
tâm, nhãn mớ, ngẫu nhiện (TAX323). Trong nghiên cứu nảy, 358 bệnh nhân bị ung thư biểu
mô tế bảo vảy đằu và cố tiên triến tại chỗ không thế phẫu thuật và tình trạng hoạt động co
thể theo W1 10 (Tổ chức Y tế thế giới) là 0 hoặc 1, dược chợn ngẫu nhiên vảo một trong hai
nhóm điều trị Bệnh nhân ở nhóm docctach được điều trị bằng docctaer (D) 75 mg/m²,
tiểp theo lá cisplatin (P) 75 mglm², sau đó là 5- fiuorouracil (F) 750 mglm²lngảy truyền lỉên
tục trong 5 ngảy. Chế độ điều trị nảy đă đuợc sử dụng mỗi 3 tuần trong 4 chu kỳ trong
trường hợp quan sát thấy ít nhẩt một dảp ứng nhỏ (giảm_ > 25% kích thước khối u được do
2 chiều) sau 2 chu kỳ. Vảo cuối cùa gìai đoạn hóa trị liệu, vói một khoảng cảch tối thiều 4
tuần vả một khoảng cách tối đa 7 tuần, những bệnh nhân với bệnh không tỉến triền đã được
xạ trị (RT) theo hướng dẫn của viện nghiến cứu trong 7 tuần (DPF/RT). Những bệnh nhân
ở nhóm so sánh dược điếu trị bằng cisplatin (P) 100 mglm², tiếp theo là 5- fiuorouracil (F)
1000 mglm²/ngảy trong 5 ngảy. Chế dộ diều trị nảy đã được sử dụng mỗi 3 tuần trong 4
chu kỳ trong trường hợp quan sát thấy ít nhắt một đảp ứng nhỏ (giảm_ > 25% kich thước
khối u được đo 2 chiều) sau 2 chu kỳ. Vảo cuối cùa giai đoạn hóa trị lìệu, với một khoảng
cách tối thiếu 4 tuần và một khoảng cảch tối đa 7 tuần, những bệnh nhân với bệnh không
tiến triến dã được xạ trị (RT) theo hưởng dẫn của viện nghiên cứu trọng 7 tuần (PF/RT).
Diều trị tại chỗ— —vùng với tia xạ đã dược thực hiện, hoặc vởỉ một phân liều nhớ thông thường
(1, 8 Gy- 2 ,O Gy 1 lần/ngảy, 5 ngảy/tuần đối với tổng 1iểu 66- 70 Gy), hoặc một chế độ xạ
trị đa phân liều và gia tôc (2 iần/ngảy, với một khoảng cảch giũa cảc phân liều tối thiếu 6
gỉờ, 5 ngảy/tuần). Tống cộng có 70 Gy được khuyến cáo cho chế độ điều trị gia tốc và 74
Gy đối với kế hoạch da phân liều. Phẫu thuật cắt bỏ được cho phép sau hóa trị liệu, trước
hoặc sau khi xạ trị. Các bệnh nhân ở nhóm DPF được điều trị kháng sinh dự phòng bằng
ciprofioxacin 500 mg, uống 2 lần/ngây trong 10 ngảy bắt đầu từ ngảy thứ 5 cùa mỗi chu
kỳ, hoặc tương dương. Thời gian sông còn không tiến triến bệnh (PFS)— tiêu chí đánh giá
chinh trong nghỉến cứu nảy, dải hơn có ý nghĩa ở nhóm DPF so với nhóm PF, p = 0,0042
(PFS trung bình: | 1,4 tháng so với 8,3 thảng tương ứng) với thời gỉan theo dõi trung bình
38
vế tống` thế là 33, 7 tháng. Thời gian sống còn toản bộ trung bình cũng dải hơn có ý nghĩa
thiên vê nhóm DPF so với nhóm PF (thòi gian sống còn toản bộ trung binh: 18, 6 thảng so
với 14,5 thảng tương ứng) với giảm 28% vê nguy cơ tử vong, p= 0, 0128. Kết quả vê hiệu
quả đuợc trình bây trong bảng dưới đây:
lliệu quả của đocetaxcl trong điều trị ban đầu ở ung thư biểu mô tế bảo vảy đầu và cổ
(SCCI IN) tiến triến tại chỗ không thể phẫu thuật (Phân tich theo ý định điều trị)
T`iếu chí Doeetaxel + Cis + 5— . ___
FU, n = 177 C1s + 5-FU n 18]
Thời gian sống còn trung bình 1 1 4 8 3
không tiến triến bệnh (thảng) (10,1-14,0) (7’4_9’1)
(Khơảng tin cậy (CI) 95%)
Tỷ sô nguy cơ điếu chỉnh (Khoảng
- 9 '
tin cậy 95%) ; *Trị sô p 0,70 (0,55 0,8 ), 0,0042
Thời gian sông còn trung bình 18,6 (15,7_2410) 14’5 (11,6-18,7)
, (tháng) (Khoảng tin cậy 95%)
Tỷ sô nguy cơ (Khoảng tin cậy
?5°/01 ,, Fri sô p 0,72 (0,56-0,93); 0,0128
' Đáp ứng chung tốt nhẩt với hớa trị 67,8 53,6
liệu (%) (Khoảng tin cậy 95%) (60,4-74,6) (46,0-61,0)
1 ***Trị số p 0,006
Dảp ứng chung tốt nhẫt vởi thuốc 72 3 58,6
điều trị của nghiên cứu [hóa trị liệu (65,1-78,8) (51,0—65,8)
+/- xạ trị] (%) (Khoảng tin cậy 95%)
***Trị số p 0,006
Thời gian đáp ứng trung binh với = 128 11 = 106
hóa trị liệu +. xạ trị (tháng) 15,7 1 1,7
(Khoảng tỉn cậy 95%) (13,4—24,6) (10,2~17,4)
Tỷ số nguy cơ (Khoảng tin cậy
95%) ; **Trị số p 0,72 (0,52-0,99); 0,0457
Tỷ số nguy cớ dưới 1 thiên về docctaer + cisplatin + S-FU * Mô hình Cox (điều chinh đối
với vị trí khôi u ban đâu, cảc giai đoạn lâm sâng T và N và tình trạng hoạt động cơ thế theo
WHO - PSWHO) ** Kiềm định logrank *** Kiêm định chi bình phương
Thỏmz số về chất lương cuỏc sống %
Những bệnh nhân được điều trị bằng DPF bị suy giảm ít có ý nghĩa về điếm số sức khòe
chung so với những người diếu trị băng PF (p = 0,01, sử dụng thang điếm EORTC QLQ-
C30).
'1'hóng số về lơi ích lâm sảng
Thang điếm tinh trạng hoạt động … thế, thang điếm phụ đối với đầu và cổ (PSS-HN) được
thiết kế dê đánh giá khả năng hiếu lời nói, khả năng ăn nơi công cộng và chế độ ăn uông
binh thường là có ý nghĩa thiến về nhóm DPF so với PF.
Thời gian trung bình dẫn dến sự suy giảm đẩu tiên về tình trạng hoạt động cơ thể theo WHO
dải hơn có ý nghĩa ở nhóm DPF so với PF. Điếm số về cường độ đau cải thiện trong khi
điêu trị ở cả hai nhóm cho thấy việc điều trị đau là đầy đù.
39
Hóa trị liệu ban đầu, tiếp theo là hóa xạ trị liệu (TAX324)
Dộ an toản và hiệu quả eủa docctaer trong điều trị ban đầu đối với bệnh nhân ung thư biếu
mỏ tế bảo vảy đầu và cổ tiến triền tại chỗ (SCCHN) đã dược đánh giá trong một nghiên
cứu pha 111, ngẫu nhiên, da trung tâm, nhãn mớ (' FAX324) 'lrong nghiên cứu nảy, 501 bệnh
nhân bị ung thư biểu mô tế bảo vảy đầu và cổ tiến triền tại chỗ và tinh trạng hoạt động cơ
thể theo WHO là 0 hoặc !, dược chợn ngẫu nhiến vảo một tron hai nhớm. Nhóm nghìên
cứu bao gồm những bệnh nhân có bệnh về kỹ thuật không thế eăt bỏ, những bệnh nhân có
xác suất chữa khói bằng phẫu thuật thấp và những bệnh nhân nhằm mục dích bảo tồn cơ
quan. Dảnh giả về hỉệu quả vả độ an toản chỉ hướng dến cảc tiêu chi về sống còn và sự
thảnh công cùa việc bảo tồn cơ quan đã không được nhắm đển một cách chính thức. Cảc
bệnh nhân ở nhóm docctach dược diếu trị bằng docctaer (D) 75 mg/m2 truyền tĩnh mạch
vảo ngảy thứ nhất, tiếp theo lá cisp1atin (P) 100 mglm² truyền tĩnh mạch trong 30 phủt đên
3 giờ, tiếp theo là truyền tĩnh mạch liên tục 5—11uorouracil (F) 1000 mglm²lngảy từ ngảy
thứ nhất đến ngảy thứ 4. Cảo chu kỳ được lặp lại mỗi 3 tuần trong 3 chu kỳ. Tất cả những
bệnh nhân không có bệnh tiến triến được dùng hóa xạ trị liệu (CRT) theo dể cương
(DPF/CRT) Các bệnh nhân ở nhóm so sánh được điều trị bằng cisplatin (P) 100 mglm²
truyền tĩnh mạch trong 30 phủt dến 3 giờ vảo ngảy thứ nhất, tiếp theo là truyền tĩnh mạch
liên tục 5-11uorouracil (F) 1000 mglm²lngảy từ ngảy thứ nhất dên ngảy thứ 5 Cảc chu kỳ
được lặp lại mỗi 3 tuần trong 3 chu kỳ. Tất cả những bệnh nhân không có bệnh tiến triến
dược dùng hóa xạ trị liệu (C RT) theo dề cương (PF/CRT). (DT
Các bệnh nhân ở cả hai nhớm diếu trị đã nhận dược 7 tuần hóa xạ trị liệu sau hóa trị liệu
ban dầu với một khoảng cảch tối thìếu là 3 tuần vả không quá 8 tuần sau khi bắt dầu chu
kỳ cuối cùng (ngảy thứ 22 đến ngây thứ 56 của chu kỳ cuối cùng). Trong thòi gian xạ trị,
carboplatin (AUC (diện tích dưới đường cong) - 1 ,5) đã được dùng hảng tuần đưới dạng
truyền tĩnh mạch trong một giờ cho tối đa 7 liều. Tia xạ dã được cung câp bằng thiết bị xạ
trị megavolt sử dụng phân liếư 1 iần/ngảy (2 Gy/ngảy, 5 ngây/tuần trong 7 tuân, cho một
tổng liếư 70 72 Gy). Phẫu thuật ở vị trí ban đầu của bệnh vả/hoặc cô có thế dược xem xẻt
bất cứ lủc nảo sau khi hoản thảnh hóa xạ trị liệu (CRT) Tất cả cảe bệnh nhân ở nhóm
nghiên cứu dùng docctach dược điều trị bằng khảng sinh dự phòng. Thời gian sống còn
toản bộ (OS) - tiêu chí chính về hiệu quả trong nghiên cứu nảy, dải hơn có ý nghĩa (kiểm
dịnh log-rank, p = 0,0058) vói chế dộ điếu trị bầng docctaer so với PF (Thời gian sống
còn toản bộ trung bình: 70,6 tháng so với 30,1 tháng tương ứng), với giảm 30% về nguy cơ
tử vong so với PP (tỷ số nguy eơ (HR)= 0, 70, khoảng tin cậy (CI) 95% = 0, 54- 0 ,90) và
thòi gian theo dõi trung bình vê tống thế là 41,9 tháng. Tiêu chỉ phụ là thời gian sống còn
không tiến triến bộnh (PFS) cho thấy giảm 29% về nguy cơ tìến tríển hoặc tử vong vả một
sự cải thiện 22 tháng về thòi gian sông còn trung bình không tiểu triển bệnh (35,5 tháng
đối với DP1` vả 13,1 tháng dối với PF). Diều nảy cũng có ý nghĩa thống kẽ với tỷ số nguy
cơ (HR) 0,71; khoảng tỉn cậy 95% 0, 56- 0, 90; kiểm dịnh log- -rank p= 0,004. Kết quá vô
hiệu quả dược trình bảy trong bảng dưới đây:
Hiệu guả củq dơccta›ch trong điếu trị ban đầu dối với bệnh nhân ụng thư biếu mô tế bảo
vảy đâu và cô tiên triên tại chỗ (SCCHN) (Phân tích theo ý định điêu trị)
Tiếu chí Docetaxel + Cis + 5- Cis + 5-FU,
, ___ ___ __r _ _ _ FULn -255 11 =246
Thời gian sông còn toản bộ trung binh _ _ _
(thảng); (khoảng tin cậy (Cl) 95%) 7016Ẩ49’0 NA 30~11(20’9'51’5)
40
Tỷ ỂỔ ngy cơ; (khoảng tin cậy 95%); 0,70; (0354-090); 0,0058
*Trị so p ,
'1ihời gian sống còn trung bình không tiên N 13 1; 10, 6 _ 20 2
triến bệnh (tháng); (khoảng tin cậy 95%) 35 5ẵ (19 3 A) ( , )
Ĩ,ỷ Số "ẵuy ““ (kh°à"g ti" cử 95%); 0, 71, (0, 56— o ,;90) 0, 004
1 ri so p
Đáp ứng chung tốt nhất (CR + PR) với 71,8; (65,8-772) [ 64,2;(57,9-70,2)
hóa trị 1iệu (%) (khoảng tin cậy 95%) ; 0,070
***Trị số p ; ,
Dảp ứng chung tốt nhẳt (CR -1 1’1Ĩ) với 1 '
thuốc diều trị của nghiến cứu lhóa trị liệu _ _ 71 5 65 5_77 1
+/— hóa xạ trị liệu] (%);( khoảng tin cậy 76’5’ (70’8 81’5) ' ’ ( ’ ’ )
95%)
***Trị số p 0,209
Tỷ số nguy cơ dưới 1 thiên về docctaer + cisplatin + fiuorouracỉl *Kiếm định log—rank
không diếu chinh
** Kiếm định log-rank không điếu chỉnh, không điều chinh đốivởi so sảnh bội số ***Kiếm
định ehi bình phương, không diếu chinh đôi với so sảnh bội sô
NA: không ảp dụng (not applicable)
1:1 CẢC DẶC TỈNH DƯỢC DỌNG 11ọc 0Ễ1
> Dược động học cùa docctach đã dược dánh giả ở những bệnh nhân ung thư sau khi dùng
20-1 15 mg/m2 trong các nghiên cứu pha 1. Đường biếu diễn động học của docctaer không
phụ thuộc iiếu dùng vả phù hợp với mô hinh được động học ba ngăn với thời gian bán hùy
đối với pha 6 lá 4 phút, pha 0 là 36 phút và pha y là 11,1 giờ. Pha cuối lả do, một phần, sự
thoát ra tương đối chậm của docctaer từ khoang ngoại biên. Sau khi dùng một liều 100
mg/m2 truyền trong một giờ, nồng dộ đinh trung binh trong huyết tương đạt được là 3,7
ụg/ml với diện tích dưới dường cong (AUC) 4,6 gỉờ.pg/ml tương ứng. Giá trị trung binh
eủa độ thanh thải toản thân 1ả 21 Iít/giờ/m2 và thể tích phân bố ở trạng thải ốn định lả 113
iít. Sự thay đổi giữa các cá nhân về dộ thanh thải toản thân khoảng 50%. Docetaxel gắn kết
hơn 95% với protein huyết tương.
> Một nghiên cứu về MC-docetaxel dã được tiến hảnh ở 3 bệnh nhân ung thư. Docetaxel được
thải trừ trong cả nước tiếu vả phân sau sự ehuyển hóa oxy hóa cùa nhóm este tert-butyl qua
trung gian cytochrom P450 trong vòng 7 ngảy, sự bảỉ tiết qua nước tiếu chiếm khoảng 6%
và bải tiết qua phân chiếm Ikhoảng 75% chất đánh dấu phóng xạ đã dùng. Khoảng 80% chất
dánh dấu phóng xạ tim thấy trong phân được bải tiết trong 48 giờ đầu dưới dạng một chắt
ehuyến hóa chính không có hoạt tính và 3 chất chuyến hóa nhỏ không eó hoạt tính và số
lượng rẩt thấp của thuốc ở dạng không thay đổi.
> Một phân tích dược động học quần thể đã được thực hiện với docctach ở 577 bệnh nhân.
Cảe thông số dược động học dược ước tính theo mô hình rất gần với các thông số dược ước
tính từ cảc nghiên cứu pha !. Dược động học của docctaer đã không bị thay đối theo tuồi
hoặc giới tính cùa bệnh nhân. Ở một số lượng nhỏ bệnh nhân (11 = 23) với dữ liệu hóa học
lâm sảng gợi ý suy chức năng gan nhẹ đến trung bình (ALT, AST > 1,5 lần giói hạn trên
cùa mức bình thường (ULN) kết hợp với phosphatase kiềm > 2, 5 lần ULN), tổng độ thanh
thái giám trung binh 27% (xem 1.1ỂU LƯỢNG VÀ CÁCH DÙNG). Độ thanh thải eủa
41
Doeetaxel không thay dối ở bệnh nhân ứ dịch nhẹ đến trung bình và không có dữ liệu ở
bệnh nhân ứ nước nặng.
Khi sử dụng kết hợp, docctaer không ảnh hưởng dến độ thanh thải của doxorubicin và
nồng dộ trong huyết tương cùa doxorubicinol (một chất chuyền hóa của doxorubicin) Dược
dộng học cùa docctaxcl, doxorubicin vả cyclophosphamid không bị ảnh hướng bới việc sử
dụng đồng thòi.
Nghiên cứu pha 1 dánh giá hiệu quả eủa capecitabin về dược động hợc của docctaer và
ngược lại cho thấy capecitabin không có ảnh hướng nảo dến dược động học của docctaer
(nồng dộ cao nhẩt trong huyết tương (Cmax) vả AUC) vả docetaxel không có ảnh hưởng
nảo đến dược dộng học của 5'- DFUR là chất chuyến hóa cùa capecitabin liên quan.
Dộ thanh thải của docctach trong diều trị kết hợp vởi cisplatin tương tự như dược quan sát
thây sau khi dùng đơn trị liệu. Đường biểu diễn dược dộng học của cisplatin sử dụng ngay
sau khi truyền docetaxcl tương tự như dược quan sát thấy khi dùng cisplatin đơn độc.
Việc sử dụng kết hợp docctaxel, cisplatin vả 5-fluorouracil ở 12 bệnh nhân có khối u rắn
không ảnh hưởng đến dược dộng hợc cùa từng thuôo riêng biệt.
Ành hưởng của prednison đến dược dộng hợc của docctaer dược dùng với thuốc chuẩn bị
trước lả dexamethason đã dược nghiến cứu ờ42 bệnh nhân. Không quan sảt thây ảnh hưởng
nảo của prednison dên dược dộng học của docctaxcl.
CI CẢC DỮ LIỆU AN TOÀN TIÊN LÂM SÀNG (Dữ liệu từ y văn) ffl1
>
>
[]
Khả năng gây ung thư của docctach chưa được nghiên cứu. ’
Doeetaxe! đã được chứng minh là gây đột biến trong cảc thử nghiệm vi nhân vả thử nghiệm
sai 1ạc nhiễm sắc thể in vilro ở tế bảo Ci 10- Kl vả trong thử nghiệm vi nhân ín v1'vo ở chuột
nhắt. Tuy nhiến, docctaer không gây dột bỉến trong thử nghiệm Ames hoặc thử nghiệm
đột biến gen CHOII IGPRT. Những kết quả nảy phù hợp với hoạt tính dược lý cùa docctaxcl.
Các tác dụng không mong muốn trên tinh hoản dược quan sát thấy trong cảc nghiên cứu về
dộc tính ở loải loải gặm nhấm cho thấy docctaer có thề lảm giảm khả năng sinh sản ở nam
giới.
'l`ƯƠN G KY
Không dược trộn lẫn thuốc nảy vói cảc thuốc khảo, ngoại trừ những thuốc được đề cập
trong phấn 1`11ẬN 1 `RỌNG DẶC BIỆT KHI HỦY BÒ VÀ XỬ LÝ KHÁC).
IIẠN DÙNG
Lọ chưa mờ: 2 năm
Sau khi mơ:
Mỗi lọ chỉ sử dụng một lần và phải dược sử dụng ngay lập tức sau khi mớ. Nếu không sử
dụng ngay lập tức, thời gian bảo quản trong khi dùng vả điếu kiện bảo quản lả trách nhiệm
cùa ngưòi sử dụng.
42
TÍNH cnÁfr VÀ DUNG LƯỢNG CỦA BAO BÌ DÓNG GÓI
Một khi đã thếm vảo túi truyền
1 heo quan diểm vi sinh vật học, việc pha/pha loảng phải được thực hiện trong điều kiện
dược kiếm soát và vô khuấn vả thuốc phải được sử dụng ngay lập tức. Nếu không sử dụng
ngay lập tức, thòi gian bảo quản trong khi dùng và diếu kiện bảo quản là trảch nhiệm cùa
người sử dụng. Một khi đã thêm vảo tủi truyền theo khuyến cáo, dung dịch truyền docctaer
ôn định trong 8 giờ nếu dược bảo quản dưới 25°C. Cần sử dụng dung dịch trong vòng 6 giờ
(kể cả 1 giờ truyền tĩnh mạch) Ngoài ra, độ ổn định lỷ-hóa trong khi sử dụng cùa dung
dịch truyền được chuẩn bị theo khuyến cáo đã được ehứng minh trong túi không PVC lên
đến 48 gìờ khi được bảo quản từ 2 8°C. Dung dịch truyền docctaer quả bão hòa, do đó có
thế kết tinh theo thời gian Nếu có tinh thể xuất hiện, không được sử dụng dung dịch đó
nữa và phải loại bỏ.
Không dùng thuốc quá hạn sử dụng.
Dế xa tầm tay trẻ em.
THẬN TRỌNG DẶC BIỆT KHI BẢO QUẢN
Bảo quản trong bao bì gốc để tránh ảnh sáng.
Bảo quản dưới 30°C. %
Lọ 20 mg/1 ml vả lợ 80 mg/4 ml.
Mỗi hộp ehứa 1 lọ.
’I`IIẬN TRỌNG DẶC BIỆT Km IIỦY BÒ VÀ xử LÝ KHẢC
Dung dịch đậm đặc pha tịếm isotcra lá thuốc chống un thư và eũng như cảc hợp chất eó
khả năng gây độc khảo, cân thận trọng khi xử lý và ehuân bị dung dịch docctaxcl. Khuyến
nghị nên sử dụng găng tay.
Nếu dung dịch dậm đặc pha tiếm lsotcra hoặc dung dịch truyền tiếp xúc với da, rửa ngay
lập tức và kỹ lưỡng bằng xã phòng và nước. Nếu thuốc Isotera Injection Concentrate hoặc
dung dịch truyền tiếp xúc với nỉếm mạc, rứa ngay lập tức và kỹ lưỡng bằng nước.
Chuẩn bị dùng đường tĩnh mạch
. Chuẩn bị dung dịch truyền
KHÔNG sử dụng eác thuốc docctaer khác gồm 2 lọ (đậm đặc và dung môi) với thuốc nảy
(isotera Injection Concentrate, 20 mg/ 1 ml và 80 mg/4 ml lả Ioại thuôo chỉ chứa 1 lọ).
lsotera lnjectỉon Concentrate 20 1ng/ 1 ml và 80 mgl4 ml KHÔNG cần phải pha Ioãng trước
với một dung môi và săn sảng đế thêm vảo dung dịch truyền.
Mỗi 1ọ chỉ dùng một lần và phải được sử dụng ngay lập tức.
43
Nếu bảo quản các 1ọ thuốc trong tủ lạnh, để số lượng hộp dung dịch đậm đặc pha tiêm
Isotcra cần dùng dưới 25°C trong 5 phủt trưởc khi sử dụng. Có thể cần hơn 1 lọ đung dịch
đậm dặc pha tiếm Isotera đế có được liều cần thiết cho bệnh nhân. Sử dụng kim tiêm cỡ 21
gaugc, trong diều kiện vô khuẩn rủt số lượng Isotera Injection Concentrate cần đùng, sử
dụng một ống tiêm đã được hiệu chuẩn.
Trong lọ lsotera Injection Conccntrate 20 mg/1 ml và 80 mg/4 mi, nồng độ của docctaer
là 20 mg/ml.
. Thể tích Isotera Injection Concentrate cần dùng phải được bơm vảo một tủi truyền 250 ml
hoặc chai chứa dung dịch giucose 5% hoặc dung dịch tiêm natri chlorid 9 mng (0,9%).
. Nếu cần một liều docctaer lớn hơn 200 mg, sứ dỤng một thể tích chất dẫn để truyền thuốc
lớn hon đề không vượt quá nông độ docctaer 0,74 mg/ml.
. Trộn tứi truyền hoặc chai bằng tay bằng cảch sử dụng chuyền động lắc.
. Dung dịch trong túi truyền phải được sử dụng trong vòng 6 giờ dưới 25°C kể cả 1 giờ
truyến cho bệnh nhân.
. Cũng như với tất eả các thuốc tiếm khác, Isotera Injection Concentrate cần dược kiếm tra
băng măt trước khi sử dụng, dung dịch có chứa chât kêt tủa phải được loại bò.
Bất kỳ phần thuốc nảo không dùng hoặc vật liệu thải đi phải được hủy bỏ theo quy định
của địa phương.
NIIÀ SẢN XUẤT ,
NangKuang Pharmaceutical Co., Ltd.
Địa ch1: No. 1001, Zhongshan Rd., Xinhua Dist., Tainan City, Taiwan (R.O.C.)
Điện thoại: 886-6—5984121 Fax: 886-6-5981845
TUQ. CỤC TRUỞNG
RTRUỞNG PHÒNG
—Ấỷayễn JfỄ7y Jfíìnấ
44
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng