

















Illlllllll
Atuouommms
ĐẠI DIẸN
1A1
\
VAN PHONG
Keep out of the reach ofchildren.
Sán xua't bờl/Manufattured by Read the padage leaflet befom use.
A;
TE
ANLÝDUỢC
ÊDUYÊT
BỎY
292…1…7…2113’
CỤCQU
ĐÃPH
Lẩu đẩu
Lllmutoilu MOlú Shilp lv Each 20 mt Vlil contatns enapenem
°°"’“° -chihm. a°“'² * Wm'i sodium equivalent to enapenem 1g,
Riom. F _ 63963 Clemont-Ferrand. ,
cedu 9, Pháp Product be stored in Vnet Nam:
between z'c-a'c .
Doanh nghiệp nháp khẩu:
' 111
muõc BÁN THEOĐơN.
INVẢNZ®
lỡ—
19
Powdef for concentnte
for solution for Infuslon.
Sỉnợe Dose via! for
Intnvenous OI
Intrimuscular Injection
Ồ MSD 1
L— __ ụ
For Posỉtlon ỉnly
0 00000 00Ị100
\, llllllllll
For Positởon Only K
ĐỂ ›… TẨM TAY TRẺ EM. 1
lllllll
/ L…LL-L
| L… |
\
oọc KỸ uươuc DÃN sử ,
DỤNG mươc KHI oùuc. l
Chiđịnh. cảch dùng. chóng ch1 i
đinh vả các thông tin khác: vui
lòng xem tờ huang dản sử dung
dtnh kèm.
Bột pha dung dịch tiêm truyền
tỉnh mạch hoác tiẻm bảp,
Hòpt lọ bỏt pha tiêm. 1
Mòi lo 20 mL chửa ertapenem nam
tương dương 1 g enapenem
dườL' dạng góc acid tự du.
Bảo quản ở Vlệt Nam ở nhiệt
dộ 2'C>B°C
SĐKIREG.z VN-Lotxx-Lnt
W
VIAL LABEL 20 ML
ĐẠI DIỆN
Ono
múuzr.
_
Enapenem tq Las enapenem sodium)
… Illllllll HHXI-I HU
'I'Ạl
, 'r.r HÀ NỘI
nolutlou M Intuclon
Intravenous use
Read the paekage leatIet
betore use.
For single use only.
n…Jì
lì/ti1'èư
VIAL LABEL 20 ML
ộuu
Luláuzr.
Eriapenem Lg Las enapenem sodium)
… mu…x
Pmựr toc concomntn tot
tot… tot Intunlon
lntravenous use
Read the packaoe Ieatlet
beíore use.
For single use only.
lllllX-l uu
dW
`Đffl/XSN
MẢẮunupp
ẨAMumpp
xxx: HJwas 0195
Sân xuất bòưManufactured by.`
leouloiru Muck Shup I
Dohme -Chian Rnute de MarsaL,
Riom, F ~ 63963 Clemont-Ferrand.
c…… 9, Pháp
Doanh nqhiêp nháp khăn:
DAIIHỆN
lllllll
lllllX-l
Nu
Keep outof Lhe reach ofchildren.
Read tbe package Ieaũet before use.
Each 15 ml. vial contains enapenem
sodium eqưvalenthoertapenem Lg,
Product be stored in V1et Nam4
between TC—B'C.
]
\\".ll' HU
LNM4ẾL`®
0—
19
Powder for 30 mL/phủt/l ,73 m thì không cằn2 đỉểu chinh 1iều.Nhưng vởi người lớn suy thận
đang tiến triền (độ thanh lọc creatinin S30 mL/phut/ 1 ,73 m 2) bao gốm người đang được thẳm phăn máu, thì
liều mỗi ngảy cân là 500 mg Không có dữ 1iệu về sử dụng thuốc ơ bệnh nhi bị suy thận.
Vởi người đang được Lhầm phân máu: trong một nghỉên cứu lâm sảng, sau khi truyền tĩnh mạch một liều
duy nhất 1 g enapenem trưởo khi thẩm phân, có khoảng 30% lỉếu được tìm thẳy trong dịch thẳm phân. Khi
dùng INVANZ 1iểu 500 mg/ngảy trong vòng 6 gỉờ trước thẩm phân ở bệnh nhân người lớn, nẻn bổ sung
thêm liều 150 mg sau khi thẩm phân xong. Nhưng nếu đã dùng INVANZ ít nhắt 6 giờ trước khi thẩm phân,
thì không cẩn liểu bổ sung. Chưa có dữ liệu ở người bệnh lọc máu hoặc thấm phân mảng bụng. Chưa có dữ
lỉệu ở bệnh nhi được thẳm phân máu.
Nếu chi có nồng độ creatinin-mảu thì dùng công thức Cockcroft vả Gault để xác định độ thanh lọc
creatinin. Khi đó, nồng độ creatinin-mảu có thể tương ứng với trạng thái òn định của chức nãng thận:
thể trọng (kg) x (140 — tuối theo năm)
(721 x creatinin huyết thanh ng7100 mL)
Nam:
Nữ: 0,85 x gỉá trị cũa nam (tính theo công thức trên)
Không cẳn chỉnh liều vởi người suy gan. (Xem CÁC ĐẶC TÍNH DƯỢC ĐỘNG HỌC, Đặc điếm của người
bệnh, Suy gan)
Liều dùng INVANZ không phụ thuộc tuổi (13 tuốỉ hoặc lớn hơn) hoặc gỉớỉ tính.
HƯỚNG DÃN CÁCH DÙNG
Bênh nhân 15 tuổi ỊI_ỌỄC lớn IỆ
Chuẩn bi dung dich iruvển Lĩnh mach
ĐUNG TRỌN LẢN HAY CỦNG TRUYỀN INVANZ VỚI CÁC THUỐC KHÁC
ĐỪNG HOÀN NGUYÊN VỚI CẤC DUNG DỊCH CÓ CHỬA DEXTROSE (ct- D—GLUCOSE)
CÀN HOÀN NGUYÊN VÀ PHA LOÃNG INVANZ TRU ỚC KHI TIÊM.
]. Dùng 10 mL của một trong các dung môi sau, bơm vảo lọ INVANZ 1 g đế hoản nguyên: nước pha tiêm,
dung dịch tiêm NaCl 0,9% hoặc nước pha tiêm có chẳt kiềm khuẩn.
2 Lắc kỳ để hòa tan hết, sau đó chuyến ngay sang lợ chứa 50 mL dung dịch tiêm NaCI 0,9%
3 Hoản tắt truyền tĩnh mạch trong vòng 6 gỉờ sau hoản nguyên.
CLLuá'n bi qunz dich tiệm bẳQ
CAN HOAN NGUYEN INVANZ TRƯỚC KHI TIÊM.
Công thủc Cockcrofì vả GaulL: Cockcrofì DW, Gauit MH Dự tinh độ thanh lọc creatinin đựa trên cteatinin- mảu. Thận hoc. 1976
gWỪ'
MK0826-VNM-2015-011140
S-WPC-MKOSZó-IVI lM-062015
l. Hoản nguyên lo 1 g INVANZ với 3 ,2 mL dung dịch tỉêm lidocain HCl 1% hoặc 2% (không chứa
epinephrỉne). Lắc kỹ lọ để hòa tan hết thuốc.
2. Rút ngay dung dịch vừa pha và tíêm bắp sâu vảo nơi có khối cơ lớn (như cơ mông hoặc phần bên đùi)
3 Nên dùng dung dịch đã pha để tiêm bắp trong vòng 1 giờ sau khi hoản nguyên.
Chủ ỷ: Tuyệt đối không được truyền tĩnh mạch dung dịch nây
Bênh nhi từ 3 tháng đến 12 tuổi
Chuẩn bi dung dich truvền tĩnh mach , _ ’
ĐÙNG TRỌN LẦN HAY CÙNG TRUYỀN INVANZ VỚI CAC THUOC KHAC
ĐỪNG HOÀN NGUYÊN VỚI CÁC DUNG DỊCH có CHỬA DELLTRO_SE (OL-D-GLUCOSE)
CẨN HOÀN NGUYÊN VÀ PHA LOĂNG INVANZ TRƯỚC KHI TIEM.
1. Dùng 10 mL của một trong cảc dung môi sau bờm vảo lọ INVANZ 1 g đề hoản nguyên: nước pha tiêm,
dung dịch tiêm NaCi 0,9% hoặc nước pha tiêm có chất kỉềm khuẩn.
2. Lắc kỳ để hòa tan hết, sau đó rút một thể tỉch tương đương với 15 mg/kg thể trọng (không quá ] g/ngảy)
hòa vảo dung dịch tiêm NaC] 0,9% để đạt được nông độ cuối cùng là 20 mg/mL hoặc thấp hơn.
3. Hoản tất truyền tĩnh mạch trong vòng 6 giờ sau khi hoản nguyên.
Chuẩn bt“ dung dich Liêm bắp
CẨN HOÀN NGUYÊN INVANZ TRƯỚC KHI TIÊM.
1. Hoân nguyên lọ 1 g INVANZ với 3 ,2 mL dung dịch tiêm iiđocain HCl 1% hoặc 2% (không chứa
epinephrine). Lắc kỹ lọ để hòa tan hết thuốc
2. Rút ngay dung dịch vừa pha một thể tích tương đương 15 mg/kg thể trọng (không quá ] g/ngây) vả tiêm
bắp sâu vảo nơi có khối cơ lớn (như cơ mông hoặc phần bên đùi)
3. Nên dùng dung dịch đã pha đế tiêm bắp trong vòng 1 giờ sau khi hoản nguyên
Chú ý: T uyet đổi không được tiêm truyền tĩnh mạch dung dịch nảy.
Thuốc tiêm cần được kiểm tra kỹ bằng mật xem cớ vật lạ hoặc đồi mảu trước khi sử dụng. Dung dịch
INVANZ là từ không mảu tởi vảng nhạt. Nêu thay đôi mảu trong phạm vi nảy thi không có ảnh hưởng tới
hiệu lục của thuôo.
CHỐNG CHỈ ĐỊNH
Người quả mẫn vởi cảc thảnh phần cùa INVANZ hoặc vởi cảc khảng sinh cùng nhóm hoặc ở người bệnh đã
có phân ứng phản vệ với [3-Iactam.
Do sử dụng dung môi lidocain HCl pha dung dịch tiêm bắp, nên chống chỉ định tiêm bắp INVANZ cho
người được biết quá mẫn với Lhuốc tê nhóm amid vả ở người bệnh bị sôc nghiêm trọng hoặc blốc tim (xin
tham khảo thỏng tin kê đơn vởi lidocain HCl).
THẬN TRỌNG
Đã có nhũng bảo cảo phản ứng quả mẫn nghiêm trọng, có khi từ vcmg (phản vệ) ở người bệnh dùng khảng
sinh {3- -lactam. Những phản ứng nảy dễ gặp hơn ở người đã có tiển sủ mân cảm với nhiều loại dị nguyên. Đã
có những bảo cảo vê người bệnh có tiền sử quá mân với penicillin thì cũng có những phản ứng quá mẫn
nghiêm trọng khi dùng cảc [3- lactam khảo. Vì vậy, trưởc khi dùng INVANZ, cần điều tra kỹ người bệnh về
cảc phản ứng quả mẫn trước đãy với cảc penicillin, cephalosporìn, các B-lactam khảc và với những dị
nguyên khảc. Nếu gặp phản ứng dị ứng với INVANZ, phải ngừng thuốc ngay Cần đỉều trị cấp cứu kịp
thời các phản ửng phản vệ nghiêm trọng
Co giật và cảc tác dụng phụ khảo trên hệ thống thần kinh trung ương (CNS) đã được báo cáo trong quá trình
điều trị với TNVANZ (xem Tác dụn lphụ). Trong giai đoạn nghiên cứu lâm sảng ở bệnh nhãn người lón
được điều trị bằng INVANZ (1 g moi ngảy một lẩn), cảc cơn co giặt, bắt kế có liến quan tới thuốc hay
không, xảy ra ở 0,5% bệnh nhân trong thời gian điều trị vả 14 ngảy theo dõi sau đó. Những tảo đụng phụ nảy
" x… tham khảo thôngtin kê toa của L.Ldocain HC]
/W1)2
MKOSZG-VNM-ZOIS-Ol 1 140
S—WPC-MKOSZG-IV/IM-OóZO] 5
xảy ra phố biển nhất ở những bệnh nhân bị rối Ioạn thần kinh trung ương (ví dụ, tổn thương não hoặc có tiến
sử động kinh) vảlhoặc chức năng thận bị tổn hại. Khuyến nghị tuân thủ chặt chẽ theo phác đồ khuyến cáo,
đặc biệt ở những bệnh nhận có các yếu tố được coi là dẫn đến co giật. Liệu pháp chống co giật nên được tiểp
tục ở những bệnh nhân rối loạn co giật đã biểt Nếu có run khu trú, rung giật cơ, hoặc co giật xảy ra, bệnh
nhân cân được đánh giá về mặt thẩn kinh và kiểm tra lại liều lượng INVANZ đề xảc định liệu có nên giảm
hoặc chấm dứt điều trị hay không.
Những bải viết trên y văn về cảc trường hợp riêng lẻ cho thấy rằng sử dụng carbapenems, bao gồm
ertapenem đồng thời với acid valproic hoặc divalproex sodium sẽ 1ảm giảm nông độ acid valproic Nồng độ
acid valproic có thế bị giảm thẩp hơn nồng độ trị liệu do tương tảo nảy, do đó lâm tăng nguy cơ bộc phát cơn
co giật. Tăng liều acid valproic hoặc divalproex sodium có thể không dù khắc phục được tương tác nảy.
Nhìn chung, không khuyến cảo dùng acid valproic/divalproex sodium chung với ertapenem. Có thể dùng các
khảng sinh khác ngoải carbapenems để trị cảc bệnh nhiễm khuẩn ở cảc bệnh nhân đang được kiềm soát tốt
cơn co giật với acid valproic hoặc divalproex sodium. Nếu cần thiết phải dùng INVANZ, nên xem xét dùng
thêm một liệu phảp chống co giật khác (xem TƯỢNG TÁC THUỐC).
Cũng như các kháng sinh khảc, dùng INVANZ kéo dâi sẽ lảm Lãng sinh cảc chùng vi khuẩn không nhạy cảm
với kháng sinh nảy. Cần phải đảnh giá liên tục tình trạng bệnh. Nếu bội nhiễm xảy ra trong khi điều trị, cần
có biện phảp điều trị thích hợp.
Đã có cảc bảo cảo về viêm ruột kểt mảng giả, từ nhẹ tới ảnh hưởng tới tính mạng với hầu hết các thuốc
khảng sinh kể cả ertapenem. Vì vậy, cần nghĩ đến biến chứng nảy khi chẩn đoản người bệnh bị tiêu chảy sau
khi dùng thuốc khảng khuẩn. Các nghỉên cứu cho thấy một độc tố tiết ra từ CIostridium difflcile lá nguyên
nhân hảng đẩu cùa “viêm ruột kểt do khảng sinh”.
Cần thận trọng khi tiêm bắp INVANZ, đế trảnh vô tinh tiêm vảo mạch máu (xem LIÊU LƯỢNG VÀ CÁCH
DUNG).
Lidocaíne HCl là dung môi dùng để tiêm bắp INVANZ. Xin tham khảo thông tin kê đơn lidocaine HCl.
KHI MANG THAI
Chưa có những nghiên cứu đầy đủ và có đối chứng tốt trên phụ nữ mang thai. Chỉ dùng INVANZ trong thai
kỳ nếu lợi ích điều trị hơn hẳn nguy cơ có thể xảy ra cho mẹ vả cho thai.
KHI cno CON BỦ
Ertapenem bải tiết qua sữa mẹ (xem CÁC ĐẶC TÍNH DƯỢC ĐỘNG HỌC, Phân phối). Thận trọng khi
dùng INVANZ cho bả mẹ đang cho con bL'L.
TRẺ EM
Tinh an toân và hiệu lực của INVANZ ở bệnh nhi từ 3 tháng đến 17 tuổi đã được chứng minh qua tải liệu từ
các nghiên cửu đằy đủ và có đối chứng tốt ở người lớn, các dữ liệu Dược động học ở bệnh nhi, và cảc dữ
liệu bổ sung từ cảc nghiên cứu dùng các thuốc khảo đối chứng ở bệnh nhi từ 3 thảng đến 17 tuổi có cảc
nhiễm trùng sau đây (xem CHỈ ĐỊNH vả CÁC ĐẶC TÍNH DUỌC ĐỘNG HỌC, Đặc điềm của người bệnh,
Bệnh nhỉ)
o Nhiễm khuẩn o bụng có biến chứng
. Nhiễm khuẩn da vả cảc tổ chức da có biến chứng
› Viêm phối mắc phải tại cộng đồng
n Nhiễm khuấn đường tiểt niệu có biến chứng
o Nhiễm khuẩn vùng chậu cắp
o Nhiễm khuẩn huyet
Không khuyến cáo sử dụng INVANZ ở trẻ em dưới 3 thảng tuối vì không có dữ liệu.
/1\_/1aì/
²7 %]
MKOSZỏ-VNM-ZOIS—Ol ] 140
S-WPC-MKOSZG-IV/lM-OóZO] 5
NGƯỜI CAO TUỔI
Trong nghiên cứu lâm sảng, tinh an toân và hiệu lực của INVANZ ở người cao tuổi (265 tuổi) cũng tương
đương như ơ người trẻ tuổi hơn (<65 tuổi).
TƯỢNG TÁC THUỐC
Khi phối hợp ertapenem với probenecid, probenecid cạnh tranh dẫn đến ức chế sự đảo thải chủ động
ertapenem qua ông thận, nên lảm tăng tuy ít nhưng có ý nghĩa thống kê về thời gian bản thải (tăng 19%) vả
nồng độ cùa ertapenem ương cơ thể (25%). Không cần điều chinh liều ertapenem khi phối hợp với
probenecid. Vì tác dụng không đảng kể tới thời gìan bản thải của ertapenem, nên không khuyến cáo dùng
phối hợp probenecid để kéo dải thời gian bán thải cùa ertapenem.
Nghiên cứu in vitro cho thấy ertapenem không ức chế sự vận chuyển digoxin hoặc vinblastin qua trung gian
P-glycoprotein vả ertapenem không phải là chất nền dùng trong sự vận chuyển qua trung gian P-
glycoprotein. Nghiên cứu in vitro trên microsom gan người thẩy ertapenem không ức chế chuyến hóa của
thuốc khảc qua xúc tảc của 6 đồng dạng cytochrom p450 (CYP) chủ yếu lả: 1A2,2C9,2C192D6,2151 vả
3A4 Chưa chẳc có tương tảc thuốc với ertapenem qua cơ chế' ưc chế thanh thải thuốc qua trung gian của P-
glycoprotein hoặc qua xúc tảc của cytochrom p450 (xem CÁC ĐẶC TỈNH DƯỢC ĐỘNG HỌC, Phân phối
và Chuyển hóa)
Ngoài probenecid, chưa thực hiện cảc nghỉên cứu chuyên biệt khảc về tương tảc trên lâm sảng.
Những bải viết trên y văn về cảc trường hợp riêng lẻ cho thấy sử dụng carbapenems, bao gồm ertapenem
đồng thời với acid valproic hoặc divalproex sodium sẽ lảm giảm nông độ acid valproic. Nồng độ acid
valproic có thế bị gìảm thắp hơn nồng độ trị liệu do tương tảc nảy, do đó lảm tăng nguy cơ bộc phát cơn co
giật. Mặc dù cơ chế của tương tác nây chưa được biết rõ, đữ liệu từ các nghiên cứu trên động vật và in vitro
cho thấy carbapenems có thể ức chế sự thủy phân chất chuyển hóa glucuronide của acid valproic (VPA-g)
thảnh acid valproic, do đó lảm gỉảm nồng độ huyết thanh của acid valproic (xem THẬN TRỌNG).
ẢNH HƯỞNG CỦA THUỐC LÊN KHẢ NĂNG LÁ] XE VÀ VẶN HÀNH MÁY MÓC
Không có dữ liệu cho thấy INVANZ ảnh hưởng lên khả năng lái xe và vận hânh mảy mỏc.
TÁC DỤNG PHỤ
N ườilơ’n
Trong các nghiên cứu lâm sảng, tổng số người bệnh dùng ertapenem là hơn 1900, trong đó hơn 1850 người
dùng INVANZ liều ] g Phần lớn những phản ứng bẩt lợi được báo cảo trong nghiên cứu lâm sảng có mức
độ nhẹ tới trung bình Những phản ứng có liên quan đến ertapenem chiếm khoảng 20% số người bệnh được
điếu trị bằng eưapenem. Ngừng thuốc do phản ứng liên quan đển thuốc thường gặp ở 1,3% sô người bệnh.
Những phản ứng lỉên quan đến thuốc hay gặp nhất trong khi dùng ertapenem dạng tiêm nảy lả tiêu chảy
(4, 3%), biến chứng ở tĩnh mạch tại chỗ tiêm (3,9%), buồn nôn (2,9%), nhức đầu (2,1%).
Sau khi tiêm ertapenem, đã gặp ở người bệnh những phản ứng sau đây có liên quan tới dùng thuốc:
- Hay gặp (2… 00, <1/10) Rối loạn hệ thần kinh Nhức đầu
Rối loạn mạch mảu Bíến chứng ở tĩnh mạch tại chỗ tiêm, viêm
tĩnh mạchl viêm tĩnh mạch huyêt khôi
Rõi ioạn tiêu hóa Tiêu chảy, buôn nôn, nôn
- Ỉt gặp (>1/1000, <… 00) Rối loạn hệ thần kinh Choáng vảng, buồn ngủ, mất ngủ,
co giật, lù lân
, /,ỰV1V
,V
\Ị-i
\
MKOSZó—VNM-2O 1 5-01 1 140
S-WPC-MKOSZG-ỈV/lM-OGZOI 5
Rối loạn tim mạch Hạ huyết ảp, thoát mạch
Rối loạn hô hấp, ' Khó thớ
Lông ngực và trung thât
Rối loạn tiêu hóa Nhiễm nắm Candỉđa miệng, táo bón, trảo
ngược dịch vị, tiêu chảy liên quan đên
C.dịfflcile, khô miệng, khó tiêu, chản ăn
Rối loạn da và mô dưới da Ban đò, ngứa
Rối loạn chung Đau bụng, rối loạn vị giảc, suy nhược/ m'ệt
vảtìnhtrạng tại nơitiêm mòi, nhiêm nâm Candida, phùfsưng, sôt,
đau, đau ngực
Rối loạn hệ sỉnh dục và vũ Ngứa âm đạo
Trong cảc nghiên cửu lâm sảng, cảc phản ứng co giật có thể gặp sau khi tiêm là 0,2% người dùng ertapenem,
ở 0,3% người dùng piperacillin/tazobactam vả ở 0% người dùng ceftriaxione.
Trong phần lớn cảc nghiên cứu lâm sảng, khảng sinh dạng tiêm được tiếp nối bằng khảng sinh dạng uống
(xem CÁC ĐẶC TÍNH DƯỢC LỰC HỌC, Các nghiên cứu lâm sâng). Trong suốt thời kỳ điều trị và thời kỳ
14 ngảy theo dõi sau điểu trị, những phản ứng liên quan đến thuốc INVANZ bao gổm những phản ứng đã
nêu ở trên, cũng như phát ban vả viêm âm đạo có tỷ lệ 21,0% (hay gặp) và cảc phản úng dị ứng, khó chịu và
nhỉễm nắm có tỷ lệ >0, 1% nhưng <1,0% (ít gặp).
Trong một nghỉên cứu lâm sảng về điều trị nhiễm trùng bản chân do đái tháođường ở 289 bệnh nhân người
lớn bị đải thảo đường được điểu trị với ertapenem, đặc tính vê phản ứng bât lọi liên quan đên thuốc nhìn
chung tương tự như cảc phản ứng đã quan sát trong các thử nghiệm lâm sảng trước đó.
Trong một nghiên cứu lâm sảng về sử dụng [NVANZ trong dự phòng nhiễm trùng tại chỗ sau phẫu thuật đại
trực trảng theo chương trình trên 476 bệnh nhân người lớn dùng 1 g ertapenem trưởo khi phẫu thuật, chi có
chậm nhịp xoang là phản ứng bất lợi liên quan đến thuốc duy nhất không thẩy trong cảc thử nghiệm lâm
sảng trước đó đã được báo cảo với tỷ lệ >0, 1% nhưng <1, 0% (L't gặp).
Bệnh nhé
Có tông cộng 384 bệnh nhi được điều trị với ertapcnem trong cảc thử nghiệm lâm sảng. Đặc tỉnh an oản
chung của thuốc ở trẻ em thì tương tự như người lớn. Trong cảc thử nghiệm lâm sảng, phản' ưng bẩt lợi
lâm sảng liên quan đến thuốc phổ biến nhẳt trong suốt trị lỉệu được bảo cảo lả tiêu chảy (5, 5%), đau tại 11
tiêm (S, 5%) và ban đô tại nơi tiêm (2, 6%)IJO1
Cảc phán ứng bẩt lợi liên quan đến thuốc sau đây được bảo cảo trong thời gian bệnh nhi điểu tfịr
ertapcnem:
Hav găp (>1/100. <1/10)
Rối loạn tiêu hóa: tiêu chảy, nôn
Cảc rối loạn chung và tình trạng tại nơi tiêm: ban đó tại nơi tiêm, đau tại nơi tiêm, vỉếm tĩnh mạch tại nơi
tiêm, sưng tại nơi tiêm.
Cảo rổi loạn da vả mô dưới da: phảt ban
Cảc phản ứng bắt lợi liên quan đên thuốc đã được báo cáo trong lủc điếu trị (trên >0 ,5% nhưng <1,0% số
bệnh nhân dùng INVANZ trong cảc thử nghiệm lâm sảng) bao gổm: chai cứng tại nơi tiêm, ngứa tại nơi
tỉẽm, viêm tĩnh mạch và nóng tại nơi tỉêm.
Trong cảc nghiên cứu lâm sảng trên bệnh nhi phần lởn các bệnh nhân được điều trị với khảng sinh đường
tỉêm sau đó chuyến sang khảng sinh dường uống thích hợp Trong suốt thời gian điều trị và thời gian theo
6 /ỰViừ
MKOS26-VNM-20] 5-01 1 140
S-WPC—MKOS2ó-IVIIM-OỔZOÌ 5
dõi 14 ngảy sau trị liệu, các phản ứng bất lợi liên quan đến thuốc ở các bệnh nhân dùng INVANZ cũng
tương tự như cảc phản ứng dược liệt kê phía trên.
Kinh nghiệm hậu mãi
Những phản ứng bất lợi sau đây đã được bảo cảo khi thuốc dùng trên thị trường:
Hệ miên dịch.- phản vệ bao gổm cả các phản ứng dạng phản vệ
Rối loạn tâm Lhần: thay đôi trạng thải tâm thân (bao gôm kích động, hung hăng, mê sảng, mất phương
hướng, cảc thay đối trạng thải tâm thẩn)
Rối Ioạn hệ thần kinh. giảm ý thức, Ioạn vận động, bất thường về dảng đi, ao giác, giật mng cơ, run
Rối Ioạn dạ dảy- ruột. Lâm xăng xỉn mảu.
Rối Ioạn da và mô dưới da. ngứa, phảt ban do thuốc với tãng bạch cầu ưa acid và những triệu chứng toản
thân ( hội chứng DRESS).
Rối Ioạn cơ xương khóp và mô Iién kết: Yếu cơ
BÁO NGAY cno BÁg: sĩ HOẶC pưog sĩ CỦA BẠN NÊU GẶP BẤT cứ TRIỆU CHÚNG BẤT
THƯỜNG NÀO KẺ TREN HAY KHAC NƯA.
Xét nghiệm cận lâm sâng
Ngư_ời Iởn
Nhũng bất thường hay xảy ra nhất có liên quan tới thuốc khi dùng INVANZ lả Lãng enzym gan (ALT, AST),
phosphatase kiềm vả sô lượng tiếu cầu.
Trong phần lớn các nghiên cứu lâm sảng, tiêm INVANZ được tiếp nối bằng khảng sinh đưòng uống thich
hợp (xem CÁC ĐẶC TÍNH DƯỢC LỰC HỌC, Các nghiên cứu Iám sảng). Trong suốt thời kỳ điều trị và 14
ngảy theo dõi sau điều trị, những bất thường về kểt quả xét nghiệm có liên quan tới thuốc ở người dùng
INVANZ không khác với những bất thường đã nêu ở trên
Những bất thường khác về kết quả xét nghiệm có liên quan tới thuốc bao gổm: tăng bilirubin trực tiểp trong
huyết thanh, tăng bilirubin toản phần huyết thanh, tăng bạch cầu ưa eosin, bilirubin giản tiếp huyết thanh,
thời gian co cục mảu, vi khuẩn niệu, nitơ u-rê mảu, creatinin huyết thanh, glucose huyêt thanh, bạch cầu đơn
nhân, tế bảo biếu mô trong nước tiểu, hồng cẫu niệu; lảm giảm bạch cầu phân thùy, bạch cầu đa nhân trung
tính, hemoglobin, hematocrit vả số lượng tiếu cẩu.
Trong một nghiên cứu lâm sảng trên 289 bệnh nhân điều trị nhiễm trùng bặn chân do đải tháo đường với
ertapenem, nhin chung, các bất thường vê kêt quả xét nghiệm liên quan đên thuôo tương tự như các bât
thường đã quan sảt thây trong các thử nghiệm lâm sâng trước dó.
Trong một nghiên cứu lâm sâng trên 476 bệnh nhân điều trị dự phòng nhiễm trùng tại chỗ sau phẫu thuật đại
trực trảng theo chương trình với 1 g ertapenem trước phẫu thuật, không có thêm cảc bất thường khảo về kết
quả xét nghiệm trong quá trình điều trị được bảo cáo
Bẽnh ___n_hi
Các bất thường xét nghiệm liên quan đến thuốc phổ biến nhẩt dược quan sảt thấy ở bệnh nhân sử dụng
INVANZ là giảm bạch câu trung tính.
Các bất thường xét nghiệm khảo liên quan đển thuốc trong suốt quá trinh điều trị và 14 ngây theo dõi gồm
có: tăng ALT, AST, giảm bạch cẩu, tăng bạch cầu eosin.
cÁc ĐẶC TÍNH DƯỢC LỰC nọc
Enapenem có tác dụng in vilro chống nhỉều vi khuẩn ưa khí và kỵ khí, cá gram dương và gram ãm. Tảo
dụng díệt khuấn của enapenem là do ức chế tống hợp vảch vi khuẩn: ertapenem gắn vảo cảc protein gắn
penicillin (PBP). Ó E.coli, ertapenem có ái lực mạnh với cảc PBP la, lb, 2, 3, 4 vả 5, chủ yếu là với PBP2
vả PBP3. Ertapenem rẩt bền vững, không bị thuỷ phân bởi phần lởn cảc Ioại B— lactamase, kể cả cảc
penicillinase, cephalosporinase vả các B-lactamase phố rộng nhưng không chống được metallo-B—lactamase.
LĩVÔỎ/
...z
\%_\x
\
o /"
Il -
Il . .’/l . '
Ọ\
MKO8Zó-VNM-ZOI 5-01 1 ]40
S-WPC-MKOSZó-ỈV/IM-OÓZOI 5
INVANZ có hoạt tính chống được hầu hết cảc chủng cùa những vi khuẩn sau đây cả in vitro và trong nhiễm
khuẩn lâm sảng (xem CHI ĐỊNH):
VL KHUẨN GRAM DƯONG ƯA KHÍ VÀ KY KHÍ KLLóNG BÀT BUỘC:
Staphylococcus aureus - tụ cầu vâng (bao gồm chủng tiêt penicillinase)
Streptococcus agalactiae
Streptococcus pneumoniae
Streptococcus pyogenes
Chú thích: Tụ cầu khảng methicillin kháng INVANZ. Nhiều chủng Enterococcusfaecalis vả hầu hết chủng
Enterococcusfaecium cũng khảng INVANZ.
VI KHUẨN GRAM ẨM ƯA KHÍ VÀ KY KHÍ KHÔNG BĂT BUỘC:
Escheria coIi
Haemophilus injluenzae (bao gồm chủng tiết B-lactamase)
Klebsiella pneumoniae
Moraxella catarrhalis
Proteus mirabilis
VL KHUẨN KY KHÍ
Bacteroídesftagílis vả cảc loải khảc trong nhóm B. fragilis
Loải CIostridium (trừ C . dịfflcile)
Loải Eubaclerium
Loải Peptostreptococcus
Porphyromonas asaccharolylica
Loải Prevolella
Nhĩmg dữ liệu in vitro sau đây hiện có sẵn, nhưng chua rõ ỵ' nghĩa lâm sâng.
Nồng độ ức chế tối thiểu (MIC) in vitro của INVANZ lả 90%) các chùng cùa
Streptococcus bao gồm Streptococcus pneumoniae, nồng dộ <0, 5 mcg/mL chống được phần lớn (>90%)
chùng của Haemophilus. <2 mcg/le chống được phần lớn (>90%) chủng vi khuẩn ưa khí và kỵ khí không
bắt buộc và nồng độ <4 mcg/mL chống được phần lớn (>90%) chủng cảc vi khuẩn kỵ khi bắt buộc trong
danh sảch dưới đây; tuy nhiên, hiệu lực và tính an toản của INVANZ trong điều trị cảc bệnh nhỉễm khuẩn
trên lâm sảng do nhiễm cảc vi khuẩn nêu trên thì chưa chửng minh được trong cảc nghiên cứu lâm sảng có
đối chứng tốt và thích hợp:
VI KHUÁN GRAM DƯONG ƯA KHÍ VÀ KY KHÍ KHÔNG BẨT BUỘC:
Staphylococcus, coagulase âm tính, nhạy cảm vởi methicillin.
Streptococcus pneumoniae khảng penicillin
Cảo Streptococcus viridans.
Chú thích: Tụ cầu khảng methicillin khảng INVANZ. Nhiều chủng Enterococcus faecalis và hầu hết các
chùng Enterococcusfaecium cũng khảng INVANZ.
VI KHUẨN GRAM ÂM ƯA KHÍ VÀ KY KHÍ KHÔNG BẢT BUỘC:
C ilrobacter freundii
Enterobacter acrogenes
Enterobacter cloaceae
Escherichia coIi tiết ESBL
Haemophilus parainjĩuenzae
Klebsiella oxytoca
Klebsiella pneumoniae tỉết ESBL
Morganella morgam'í
Proteus vngaris
Serratia marcescens
l."^./ :.… .
MKOS26-VNM-ZO ] 5-01 1 140
S-WPC-MKOSZG-lV/IM-OõZOI 5
Chú thích: Nhiều chủng của cảc vi khuẩn nêu trên có đa đề kháng với các kháng sinh khảc, như các
penicillin, cephalasporin (bao gồm thế hệ thứ ba) và cảc aminogiycosid nhưng lại nhạy cảm với INVANZ.
VI KHUẨN KY KHÍ
Loâi F usobacterium
Xét nghiệm tính nhgỵ cảm với khang sinh
Khi có những kết quả in vưro vê tính nhạy cảm với khảng sinh của vi khuẩn, nên báo cáo định kỳ cho thầy
thuốc, trong đó mô tả đặc tính nhạy cảm của vi khuẩn gây bệnh ở bệnh vỉện và lây nhiễm ở cộng đồng.
Những bảo các nảy sẽ giúp thầy thuốc lựa chọn được khảng sinh hiệu quả nhất.
Kỹ thuật pha Ioãng
Dùng cảc phương phảp định lượng để xảc đinh nồng độ ức chế tối thiếu (MIC). Những trị số MIC nảy sẽ
cung cap trị sô uớc tỉnh về tính nhạy cảm cùa vi khuấn đối vởi khảng sinh. MIC được xảo định bằng một
quy trinh chuẩn hoá. Quy trình chuẩn hoá dựa vâo phương phảp pha loãng (canh cấy hoặc thạch) hoặc
tương đương với nổng độ chuẩn hóa cùa chẩt cấy truyền và nồng độ chuẩn hoá của bột eưapenem Phân tich
cảc trị số MIC theo các tiêu chí được cung cấp ở Bảng 1.
Kỹ thuật khuếch tán
Những phương pháp định lượng đo đường kính của vòng vô khuẩn cũng cung cấp những trị số ước tính có
thể lặp lại về tinh nhạy cảm của vi khuẩn đối yới cảc kháng sinh Một quy trình chuẩn hoá như thể ** đòi hỏi
sử dụng những nồng độ chuẩn hoá của chất cấy truyền. Kỹ thuật nảy dùng những1đ”a giấy tròn thấm 10 mcg
ertapenem để thử tính nhạy cảm của vi khuấn đối với enapenem. Những chi tiêu biếu thị sự khuếch tản của
thuôo tâm vảo đ" a giấy được cung cấp ở Bảng I.
Kỹ thuật kỵ khí:
Vởi vi khuẩn kỵ khi, có thể xác đinh tính nhạy cảm với ertapenem qua MIC với một phương pháp thử
nghiệm chuẩn hoá mẻ .Phân tích các trị số MIC thu được theo cảc tiêu chí được cung câp ở Bảng 1.
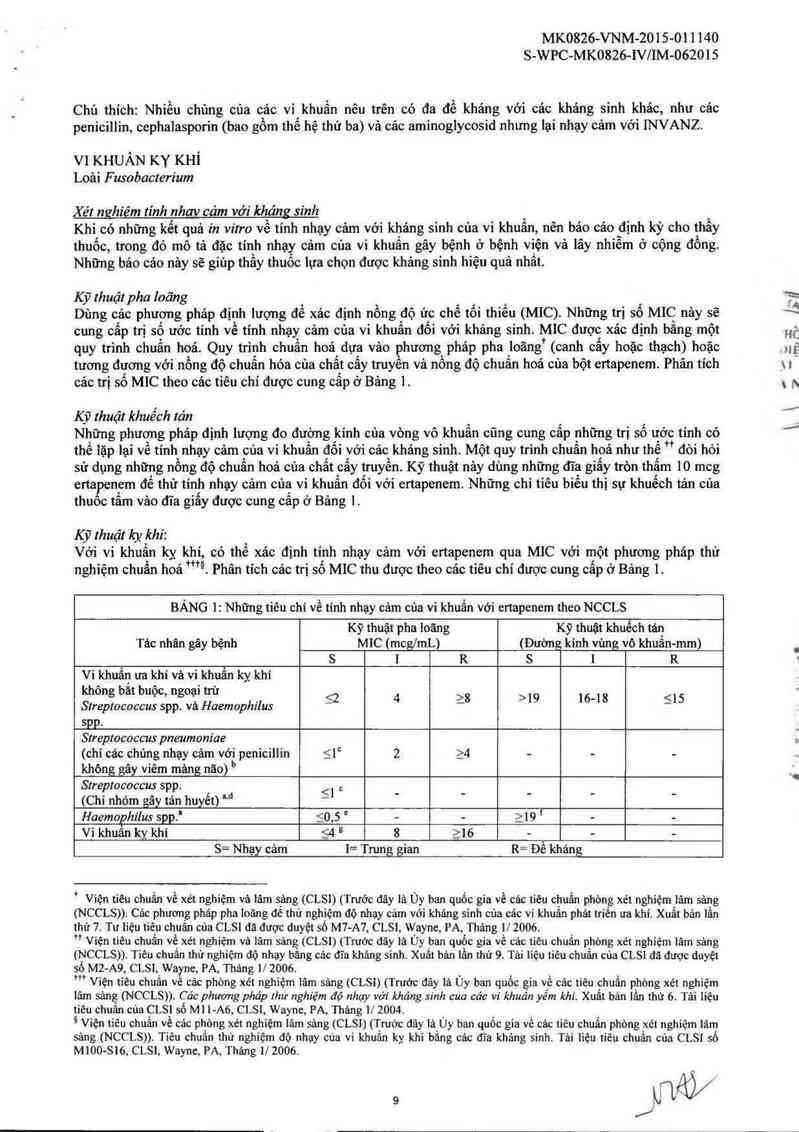
BÀNG !: Những tiêu chí về tính nhạy cảm cùa vi khuẩn với enapenem theo NCCLS
Kỹ thuật pha loãng Kỹ thuật khuếch tản
Tác nhân gãy bệnh MIC (mcg/mL) (Đườn kinh vùng vô khuẳn-mm)
S ! R S ! R
Vi khuẩn ưa khí vả vi khnẩn kỵ khí
khôn băt buôc, n oại trừ
StrepỀococcus sppể vả Haemophilus 52 4 >8 >19 16-18 515
spp.
Streptococcus pneumoniae
(chi cảc chùng nhạy cảm với penicillin 51° 2 24 - - -
khỏnggây viêm mảngỵão) "
Streptococcus spp. <] ,
(Chi nhóm gây tản huyết) ~“ - ’ ' ' ' ’
Haemophilus spp.’ _<_0,5 ' — - 219 { — -
Vi khuẩn kỵ khi 54 ² 8 2 L 6 - - -
S= Nhạy cảm l= Trung gian R= Đề kháng
Viện tiêu chuẩn về xét nghỉệm và lâm sâng (CLSI) (Trước đây là Ủy ban quốc gia về các tiêu chuẩn phòng xẻt nghiệm lâm sảng
(NCCLS)). Cảc phương phảp pha loãng đế thử nghiệm độ nhạy cảm với kháng sinh của các vi khuẩn phát triên ưa khi Xuất bản lẩn
thứ 7. Tư liệu tiêu chuẩn cùa CLSI đã được duyệt số M7-A7, CLSI, Wayne, PA, Tháng 1/ 2006.
” Viện tiêu chuẩn về xét nghiệm vả lâm sảng (CLSI) (Trước dây lả Ủy ban quốc gía về các tiêu chuẩn phòng xét nghiệm lâm sảng
(NCCLS)). Tiêu chuẩn thử nghiệm độ nhạy băng cảc đĩa khảng sinh. Xuất bản lẩn thứ 9 Tái liệu tiêu chuẩn của CLSi đã được duyệt
số M2 A9, CLSI Wayne, PA, Tháng Il 2006.
… Viện tiêu chuẩn về cảc phòng xét nghiệm lâm sảng (CLSI) (Trước đây là Ủy ban quốc gia về các tiêu chuẩn phòng xét nghiệm
lâm sảng (NCCLSD Các phương phảp Lhư nghiệm độ nhạy vởi kháng sinh của căc w" khuần yếm khi. Xuất bản lần thứ 6 Tải liệu
tiêu chuẩn của CLSI số Mll -,A6 CLSI, Wayne, PA, Thảng II 2004
Ổ Viện tiêu chuẩn về các phòng xét nghiệm lâm sảng (CLSI) (Trước dây là Uy ban quốc gia về các tiêu chuẩn phòng xét nghiệm lâm
sảng (NCCLS)). Tiêu chuẩn thu nghiệm dộ nhạy cùa vi khuẩn kỵ khi bằng các đĩa kháng sinh. Tải liệu tiêu chuẩn của CLSI số
M… 816 CLSI Wayne PA Tháng 1l2006
9 ý Ồ
MKO8ZỔ-VNM-20iS-Oi I ]40
S-WPC-MKOSZõ-IVllM-OÓZO l 5
' Hiện nay, không có nhũng dữ liệu về cảc chủng kháng thuốc nên khỏng xảc định bắt cứ phân ioại nảo khác ngoải "nhay cảm (S)".
Nếu cảc chủng vi khuẩn cho những kểt quả về MIC khảc với chủng nhạy cảm cần phải thư thêm ở một phòng Lhi nghiệm khác để
đối chiến.
” Streptococcus pneumonỉae nhạy cảm vởi pcniciilin (đường kinh vòng kháng khuẩn >20 mm đổi với đĩa tấm ! mcg oxacilline) có
thế xcm lả nhạy cảm với ertapcncm. Nên thử lại tinh nhạy cảm với ertapencm bằng phương phảp đo nồng dộ L'Lc chế tối thiếu nểu
chùng phân lập có kich thước vòng khảng khnẩn 519 mm với dĩa Lắm oxacillinc ] mcg
° StrepLocor;cus pneumoniae hạy cảm với penicillin (MIC 50,06 mcg/mL) vả Slreptococcus spp. ngoại trừ S. pneumoniae nhạy cảm
vởi pcnĩcillin (MIC 50, 12 mcg/mL) có thể xem là nhạy cảm với cnapenem Không cân thư tinh nhay cảm với eưapenem dối với các
chủng phân lặp kháng hoản toản hoặc kháng trung gian với penicillin vi không có cảc tiêu chuẩn đáng tin cậy biện giải độ nhạy cảm
với ertapcnm.
đ Streptococcus spp. gây tản hưyết nhỏm li nhạy cảm với penicillin (vòng khảng khuẩn >24 mm với dĩa tẩm 10 dơn vị penicillin) có
thể xem lá nhạy cảm với enapenem. Nên thử lại tinh nhạy cảm với crtapenem bằng phương phảp đo nổng độ ức chế tối thiều nểu
chủng phân lập có kích thưởc vòng khảng khuẩn <24 mm với đĩa tẩm 10 đơn vị pcnicillin. Không cần thừ tinh nhạy cảm vởi
enapcncm đối với Streptococci viridans vì khỏng có các tiêu chnẩn đáng tin cậy bíện giải độ nhạy cảm với pcnicỉllin.
' Những tiêu chuẩn nảy có thề ảp dụng cho quy trinh vi pha loãng canh cấy, dùng môi trường thử nghiệm Haernophilus (H' IM]
đuợc cấy truyền với một dịch treo khuẩn iạc trực tiễp vả L`L trongphòng' ơ 35°C trong 20- 24 giờ
' Những dướng kỉnh vòng vô khuẩn nảy có thể áp dụng cho. các thử nghiệm bằng kỹ_thuặt khuếch tán trên đĩa thạch, dùng mỏi
truờng thạch thử nghiệm Haemophilus (HTM) được cây Lruyên với mõt dịch treo khuân lạc trực tiêp vả ủ trong 5% COz ở 35°C
trong 16-18 giò.
² Những tiêu chuẩn biều thi nảy chi có thề ảp dụng cho kỹ thuật pha loãng tIong thạch dùng thạch Brucella có bổ sung hcmỉn,
vìtamin Ki và 5% mản cừu dã loại bỏ iibrin hoặc mảu đã lv giải được cấy truyền với mỏt dìch treo khuần lac truc tiếp hoặc một mẻ
cẳy mởi tứ 6 đến 24 giờ trong môi trường chứa nhiến thioglycolal: được ủ trong một bỉnh hoặc buồng u yếm khi ở 35- 37°C trong 42-
48 giờ.
Một bảo cảo gợi lả "Nhạy cảm" nếu tảo nhãn gây bệnh có thế bị ủc chế ở nồng độ khảng sinh thử nghiệm
thường đạt được trong mảu Một báo cảo gọi là "Trung gian“ nếu kết quả được xem khỏng rõ rảng và nên vi
khuẩn không hoản toản nhạy cảm đối vởi những thuốc khảo được xem là nhạy cảm trên lâm sảng, thì cần lặp
lại xét nghiệm Phân loại nảy cho biết vân có thể dùng thuốc trên lâm sảng nếu những vị trí cùa cơ thể có
nồng độ phân bố thuốc cao hoặc trong trường hợp có thể dùng thuốc vởi liều cao Phân loại nảy cũng cung
câp một vùng đệm nhắm ngăn ngừa những yêu tô sai sót kỹ thuật nhỏ có thể gây nên những khác biệt lởn
khi phân tích kết quả. Một báo cáo gọi lả' 'Khảng" nểu tảc nhân gây bệnh có thể khỏng bị ức chế 0 nồng độ
kháng sinh thử nghiệm thường đạt được trong máu; do đó cần lựa chọn iiệu phảp khảc.
Kzếm tra chất Iuợng
Những quy trình chuẩn hóa thư nghiệm tính nhạy cảm chuẩn hoá cần dùng những chủng vi khuẩn chuẩn đối
chứng nhằm kiếm tra những mặt kỹ thuật của quy trình thử nghiệm. Bột ertapcncm chuẩn cung cắp cảc gíá
trị nồng độ ghi ở bảng 2 dưới đây Cảo vi khuẩn chuẩn dối chứng là những chùng vi khuẩn đặc hiệu có
những tinh chất sinh học nội tại. Những chủng chuẩn đối chứng phâi rất ôn định, luôn cho mô hình nhạy
câm có tinh chuẩn mực và có tịnh lặp lại Những chủng đặc hiệu dùng trong kiềm tra chất lượng xét nghiệm
vi sinh học không có ý nghĩa về mặt lãm sâng.
BÀNG 2: Phạm vi nồng độ có thể chắp nhận của vi khuẩn chuẩn đối chửng đối với ertapenem
. , À .: , .. _ Thử nghiệm khuếch tản đĩa—
Chung dung đe kLcm tra Thư n hLẹm ha loan . . , . z
chẳt lượng ATCC® (Mngtheo LiicglmL)g (đương kmh vằnrẳìvo khuan theo
Enterococcus faecalis 29212 4-16 Không ảp dụng
Tụ cãu vảng 29213 0,06-0,25 Không ảp dụng
Tụ cẩu vảng 25923 Không ảp dụng 24-31
Streptococcus’pneumoniae h 49619 0,03-0,25 1 28-35
EscheriChia coli 25922 0,004-0,016 29-36
JIaemophilus influenzae 49766 0,016-0,06J 27-33 '“
Pseudomonas aerugz'nosa 2'7853 2-8 13-21
Bacteroides fragilis 25285 0,06-0,25 ' (0,06-0,25) "' Không ảp dụng
Bacteroides thetaiotaomicron 2974] 0,25-1,0 '{0,5-20) "' Khỏng ảp dụng
E ubacteríum Ientum 43055 0,5-2,0 ] ( 0,5-0,4) '“ Không áp dụng
10 1
²' “' ò/ev/
\; "
MKO826-VNM-20l 5-01 1 140
S-WPC—MKOSZÓ-IVIIM—OóZOI 5
" Vi khuẩn nây được dùng để kiểm tra chất lượng xét nghiệm tính nhạy cảm của Slreplococcus pneumoniae vả Streptococcus spp.
' Những nồng độ chuẩn, đối chửng nảy có thế ảp dụng cho nhũng thử nghiệm với Streptococcus pneumoniae ATCC 49619 bằng kỹ
thuật vi pha loãng canh cấy với canh thang Mueller—Hinton đã điều chỉnh cation chứa 2- 5% mảu ngựa ly giải đuợc cấy tmyền với
một dịch treo khuẩn lạc trực tiếp và ủ trong phòng 0 35°C trong 20-24 giờ.
’ Những nồng độ chuẩn, đối chửng nảy có thể ảp dụng cho cảc thử nghiệm với Haemophilus L'ndLLenzae ATCC 49766 bằng kỹ thuật
vi pha loãng canh cắy với mõi trường thử nghiệm Haemophilus (HTM) được cẩy truyền với một dịch treo khuấn lạc trực tiểp vả LL
trong phòng 0 35°C trong 20-24 giờ
'“ Những nồng dộ chuẩn, dối chửng nây có thế âp đụng cho cảc thử nghiệm với Haemophilus induenzae ATCC 49766 bằng ky thuật
khuếch tán đỉa với môi trường thạch thử nghiệm Haemophilus (HTM) được cây truyện với một dich trco khuẩn lạc trực tiep vả ủ
trong 5% COz ớ 35°C trong 16- 18 giờ
' Những nồng độ chuẩn, đối chứng nây chi có thế áp dụng cho kỹ thuật pha loãng ttong thach, với thạch Brucella bổ sung hcmin,
vitamin Kl và 5% mảu cừu đã loại bỏ tibrin hoặc máu bi ly giải, được cấy truyền với một dịch treo khuân lạc trực tiêp hoac một mẻ
cắy mởi từ 6 tới 24 giờ trong môi trường chứa nhìẽu thioglycolat và được ủ trong một bình hoặc buổng ủ yểm khi ở 35-37°C trong
42-48 giờ.
"’ Những nồng dộ chuẩn, đối chứng nảy có thể ảp dụng cho kỹ thuật vi pha loãng canh cắy
Cảc nghiên cứu lâm sảng
Người lớn
Enapenem đã được đảnh giả trong một thử nghiệm lâm sâng ở 665 người lớn điều trị nhiễm khuấn trong ổ
bụng có biến chứng: so sảnh ertapenem (mỗi ngảy một iần 1 g truyền tĩnh mạch) với piperacillinltazobactam
(truyền tĩnh mạch 3, 375 g môi 6 giờ), dùng trong 5- 14 ngảy. Tại thời điểm 1-2 tuần sau thời kỳ điều tri, tỷ lệ
thảnh công về lâm sảng và vi sinh là 89,6% (190l212) với ertapenem và 82,7% (162/196) với
piperacillin/lazobactam; sau khi điều trị 4-6 tuần (đảnh giả khỏi bệnh), tỷ lệ thảnh công là 86, 7% (l76/203)
với ertapenem và 81,3% (157/193) với piperacillin/tazobactam
Trong thử nghiệm lâm sảng, đảnh giả eưapenem ở 540 người lớn điều trị viêm da và cấu trúc da có biến
chứng, so sánh ertapenem (mỗi ngảy truyền tĩnh mạch một lần 1 g) với piperacillin/tazobactam (truyền tĩnh
mạch mỗi 6 giờ; môi lẳn 3,375 g) dùng trong 7- 14 ngảy, bao gồm nhiễm khuẩn chi dưới do đải thảo đường
đường,’ ap-xe sâu mô mếm, nhiễm khuẩn vẽt thương sau chấn thương, viêm mô tế bảo đang dẫn lưu mủ. Tỷ
lệ thảnh công trên lâm sảng vảo 10- 21 ngảy sau thời kỳ điều trị (đảnh giá khỏi bệnh) là 82, 2% (152l185) với
enapenem và 84,5% (1471174) với piperacillin/tazobactam.
Ertapenem được đánh giá hiệu quả trong điều trị nhiễm trùng bản chân do đái tháo đường trong một thử
nghiệm lâm sảng có đối chứng, mù đôi, đa trung tâm, phân nhóm ngẫu nhiến. Nghiên cứu nảy so sảnh (1 g
IV ngảy 1 lần) với piperacillin/tazobactam (3,375 g IV môi 6 giờ) trên 586 bệnh nhân. Cả 2 phác đồ điếu trị
đều cho phép chuyên sang liệu pháp amoxicillin/clavucianate dường uống với thời gian điều trị tông cộng là
5- 28 ngảy (cả đường tiêm và dường uống). Tỷ lệ thảnh công trên lâm sảng trong vòng 10 ngảy sau trị liệu 1ả
87, 4% (180l206) đối vởi ertapenem và 82, 7% (162/196) đối với piperacillin/tazobactam.
Trong hai thử nghiệm lâm sảng trên 866 người lớn điều trị viêm phổi mắc phải tại cộng đồng, ertapenem
(mỗi ngảy tiêm một lần 1 g) được so sánh với ceftriaxone (mỗi ngảy tiêm một lần 1 g). Cả hai phảc đồ đểu
cho phép chuyến sang liệu pháp amoxicillin/clavulanate đường uống với thời gian điêu trị tổng cộng là 10-
14 ngảy (cả tiêm vả uổng) Tỷ lệ thảnh công trên lâm sảng (gộp 2 nghiên cứu) vảo 7- 14 ngảy sau thời kỳ
điểu tri (đánh giá khỏi bệnh) lả 92% (335/364) với ertapenem và 91, 8% (270/294) với ceftriaxone.
Trong hai thử nghiệm lâm sảng trên 850 người lớn điếu trị viêm đường tiết niệu có biến chứng, bao gồm
viêm thận- bế thận, ertapenem (mỗi ngảy tiêm ] lần 1 g) được so sánh với ceftriaxone (mỗi ngảy tiêm một
lần 1 g). Cả hai phảc đồ đều cho phép chuyến sang liệu pháp ciprofioxacin đường uống (500 mg, ngảy uông
2 iần) với thời gian điều trL tống cộng lả 10-14 ngảy (cả tiêm và uống). Tỷ lệ thảnh công vê vi sinh học (gộp
2 nghiên cứu) vảo 5- 9 ngảy sau thời kỳ điều trị (đánh giá khỏi bệnh) là 89, 5% (229/256) với ertapenem vả
91,1% (204/224) với ceftriaxone
11
/fflpỒ/
MKOSZG-VNM-ZO 1 5-01 1 140
S-WPC-MKOSZó-IVIĨM-OỐZOI 5
Trong một thử nghiệm lâm sảng, đảnh giá ertapenem (] g truyền tĩnh mạch, ngây 1 lần) so với
piperacillin/tazobactmn (3,375 g tiêm tĩnh mạch mỗi 6 giờ) dùng trong 3- 10 ngây trong đìếu trị vỉếm vùng
chậu câp trên tống cộng 412 người lớn bao gôm 350 ngưới nhiễm trùng lL'Lc sinh] sau khi sinh và 45 người
nạo thai nhiễm khuẩn Tỷ lệ thảnh cõng trên lâm sảng vảo 2- 4 tuần sau thời kỳ điếu trị (đảnh giá khỏi bệnh)
là 93,9% (153/163) với ertapenem và 91,5% (140/153) với piperacillinltazobactam.
Một thử nghiệm đa trung tâm, mù đôi, phân nhóm ngẫu nhiên đánh giá hiệu quả dự phòng trong phân thuật
trên 1002 người lớn, so sánh 1'NVANZ IV (1 g) với cet'otetan N (2 g) tiêm truyền kéo dải 30 phút vảo 1giờ
trước khi phẫu thuật đại trực trảng theo chương trình. Tỷ lệ đảp ứng lâm sỉmg có lợi nới chung vảo 4 tuân
sau phẫu thuật (tiêu chí chủ yểu đảnh giá hiệu quả) là 72,0% cho nhóm bệnh nhân dùng ertapenem (N= —338)
và 57, 2% ở nhóm dùng cefotetan (N=334) (khảc biệt 14,8%, [95% C1 lẻ 7 ,5%-21 ,9%]), cho thấy hiệu quả
vượt trội cùa ertapenem so với thuốc đối chứng trong điếu trị dự phòng cho cảc bệnh nhân phẫu thuật đại
trực trảng theo chương trình.
Trẻ em
Enapenem dược đảnh giá trong hai thử nghiệm lâm sảng đa trung tâm, mù đôi, phân nhóm ngẫu nhiên trên
các bệnh nhi từ 3 tháng đến 17 tuổi. Thử nghỉệm đầu tỉẽn kết nạp 404 bệnh nhi, so sảnh ertapencm (IS
mgfkg truyền thh mạch mỗi 12 giờ trên bệnh nhi từ 3 tháng đến 12 tuổi và 1 g truyền tĩnh mạch ngảy 1 lần
cho bệnh nhi tử 13 tuồi đến 17 tuối) với ceftriaxone (SO mg/kg/ngây truyền tĩnh mạch chia 2 lần trên bệnh
nhi từ 3 thảng đến 12 tuổi và 50 mg/kg/ngảy truyền tĩnh mạch ngảy ] iẩn trên bệnh nhi từ 13 tưỗi đến 17
tuối) trong điêu trị nhiễm khuẩn tiết niệu có biến chứng, nhiễm khuẩn da vả mô mềm hoặc viêm phổi mắc
phải tại cộng đồng. Cả hai phác đồ đều cho phép chuyền sang dạng uống amoxicillin/ciavulanate với thời
gian điều trị tông cộng 14 ngảy (tiêm và uống). Tỉ lệ thảnh công vẽ vi khuẩn học được đánh giá trong một
phân tich dựa trên protocol ở các bệnh nhi nhiễm khuẳn tiểt niệu có biến chứng cho thấy là 87,0% (40/46)
đối với ertapenem và 90, 0% (18/20) đối với ceftriazone. Tỉ lệ thảnh công trong một phân tích dựa trên
protocol ở các bệnh nhi được điếu trị nhiễm khuẩn da vả mô mềm là 95, 5% (64/67) đối với ertapenem vả
100% (26/26) đối với ceftriaxonc vả ở các bệnh nhân được điếu trị viêm phối mãc phải tại cộng đồng lả
96,1% (74/77) đối với ertapencm và 96, 4% (27/28) đối vởi ceftriaxone
Thử nghiệm thứ hai kết nạp ] 12 bệnh nhi vả so sảnh ertapenem (15 mglkg truyền tĩnh mạch mỗi 12 giờ trên
cảc bệnh nhi từ 3 thảng đểu 12 tuổi vả lg truyền tĩnh mạch ngảy 1 iần trên bệnh nhi từ 13 tuổi đến 17 tuối)
với ticarcỉllin/clavulanate (50 mg/kg đối với bệnh nhi <60 kg hoặc 3, 0 g đối với bệnh nhi >60 kg, ngảy 4
hoặc 6 lần) trong thời gian 14 ngảy tr0ng điều trị nhiễm khuấn ố bụng có biến chứng và nhiễm khuẩn vùng
chậu cấp Trên các bệnh nhi được điều trị nhiễm khuẩn 0 bụng có biến chứng (lả những bệnh nhi trước đây
có lỗ dò hoặc viêm ruột thùa có biển chứng) tỉ lệ thânh công trên lâm sảng là 83,7% (36/43) đối với
ertapenem và 63, 6% (7/11) đối với ticarcillin/clavulanate trong một phân tích dựa trên protocol. Trên các
bệnh nhi được đỉếu trị nhiễm khuẩn vùng chậu cấp (hậu phẫu hoặc viêm nội mạc tử cung sản khoa tự phát
hoặc phá. thai nhiễm trùng) ti iệ thảnh công lâm sảng là 100% (23123) đối với ertapenem và 100% (4/4) đối
với đối vởi ticarcillin/ciavulanate trong một phân tich dựa trên protocol.
CÁC ĐẶC TỈNH DƯỢC ĐỘNG HỌC
Hắpthu
Thuốc tiêm ertapenem pha với dung dịch tiêm lidocain HCl 1% (Dược điếu Mỹ) pha trong nước muối
không có epinephrine, rất dễ hẳp thu sau khi tiêm bắp với 1iếu khuyến cảo ] g. Sinh khả đụng trung bình
khoảng 92%. Sau khi tiêm bắp liều 1 glngảy, nồng độ đinh trung bình trong huyết tương (Cmax) đạt sau
khoảng 2 giờ (T,…)
Phân phối
Ertapenem gắn kết nhiến vởi protein huyết tượng Ở người 1ởn trẻ tuổi khoẻ mạnh, mức độ gắn kết protein
cúa ertapenem sẽ giảm khi nồng độ trong huyết tương tăng. Khi nồng độ huyết tương <100 mcg/mL thi găn
khoảng 95% nhưng khi nồng độ huyết tương khoảng 300 mcglmL thì chi găn khoảng 85%
/LL’)<Ồ/
12
6
of.
MKOS26-VNM-ZOl 5-01 1 140
S-WPC-MKOS2ó-IVỉlM-OÓZOI 5
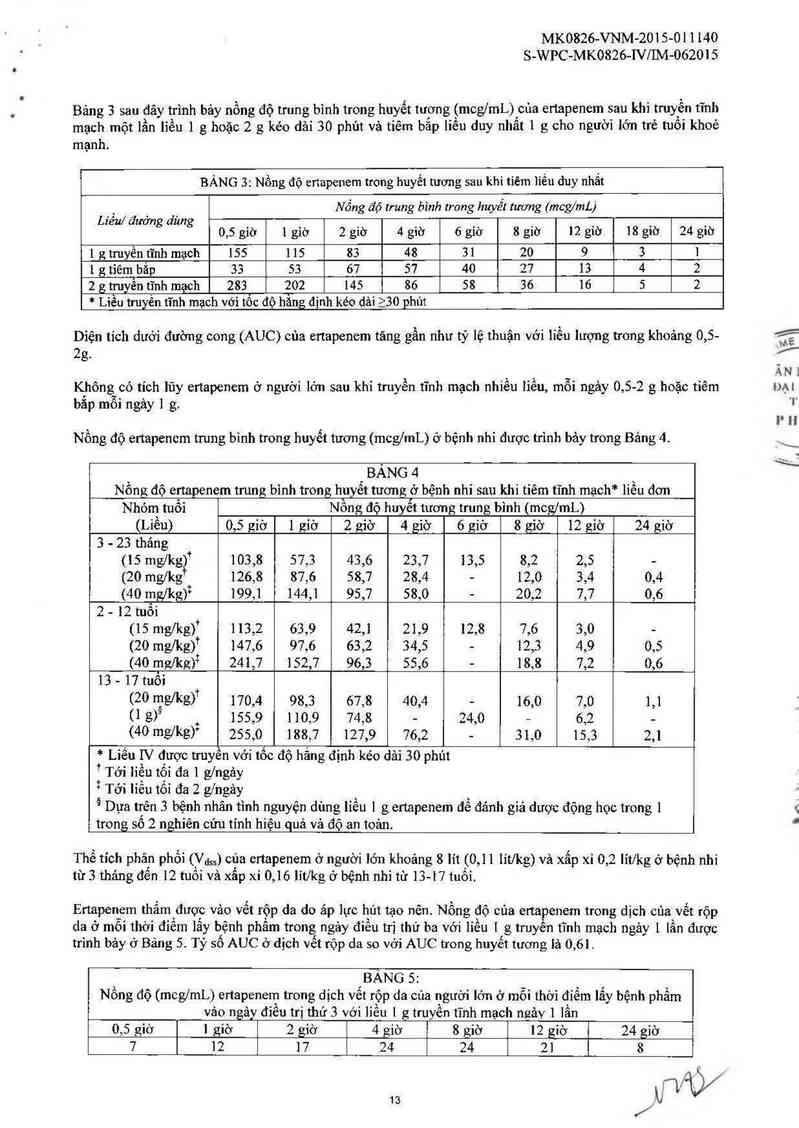
Bảng 3 sau đây trình bảy nổng độ trung bỉnh trong huyết tương _(mcg/mL) cùa eLtapenem sau khi truy_ến tĩnh
mạch một lần liếư ] g hoặc 2 g kéo dải 30 phút vả tiếm bắp liếư duy nhất 1 g cho người iớn trẻ tuổi khoẻ
mạnh.
BÀNG 3: Nồng độ enapenem trong huyết tương sau khi tiêm liếư đuy nhất
, Nồng độ trung bình trong huyềt tương (mcg/ml.)
LL'éu/ đường dùng _ _ __ _ _ Ợ '
0,5 giờ 1 giờ 2 gLờ 4 giờ 6 giơ 8 gLờ 12 giờ 18 gLờ 24 gLờ
L g truyền tĩnh mạch 155 1 15 83 48 31 20 9 3 L
1 g tiêm bắp 33 53 67 57 40 27 13 4 2
2 g trưyền tĩnh mạch 283 202 145 86 58 36 16 5 2
* Liễu truyền tĩnh mạch với tốc độ hỂng định kẻo dải 230 phút
Diện tích đưới đường cong (AUC) cùa ertapencm tăng gần như tỷ lệ thuận với líếu lượng trong khoảng 0,5-
2g.
Không có tích lũy ertapenem ở người lớn sau khi truyền tĩnh mạch nhiều Iiếu, mỗi ngảy 0,5-2 g hoặc tiêm
bắp mỗi ngảy ] g.
Nồng độ ertapencm trung binh trong huyết tương (mcg/mL) ở bệnh nhi được trinh bảy trong Bảng 4.
BANG 4
Nồng độ ertapenem trung bình trong huyễt tương ở bệnh nhi sau khi tiêm tĩnh mạch* liếư đơn
Nhóm tuổi Nồng độ huyễt tương trung binh (mcg/mL)
(Liễn) 0,5 giờ 1 giờ 2 giờ 4 giờ 6 giờ 8 giờ 12 giờ 24 giờ
3 - 23 thảng
(15 mg/kgỹ 103,8 57,3 43,6 25,7 13,5 8,2 2,5 …
(20 mg/kgi 126,8 87,6 58,7 28,4 - 12,0 3,4 0,4
(40 mg/kgỹ 199,1 144,1 95,7 58,0 - 20,2 7,7 0,6
2 - 12 tuối
(15 mg/kgỹ' 113,2 63,9 42,1 21,9 12,8 7,6 3,0 -
(21) mglkg)’r 147,6 97,6 63,2 34,5 - 12,3 4,9 0,5
(40 mg/kg)I 241,7 152,7 96,3 55,6 - 18,8 7,2 0,6
13 - 17 tuổi
(20 mg/kgỹ 170,4 98,3 67,8 40,4 - 16,0 7,0 1,1
(1 8)ã _ 155,9 1 10,9 74,8 … 24,0 … 6,2 …
(40 mglkgr 255,0 188, 7 127,9 76 2 - 31,0 15,3 2,1
* Liều IV được truyẻn vởi tốc độ hắng định kéo dải 30 phủt
Tới iiều tối đa 1 g/ngây
t Tới liều tối đa 2 g/ngảy
Ổ Dựa trên 3 bệnh nhân tinh nguyện d_ùng lỉều 1 g ertapenem đế đảnh giá dược động học trong 1
trong số 2 nghiên cứu tính hiệu quả vả độ an toản.
Thế tich phân phối (Vdss) của crtapenem ở người lởn khoảng 8 lit (0,11 lít/kg) vả xẫp xỉ 0 ,2 lítlkg ở bệnh nhi
từ 3 thảng đến 12 tuốí vả xấp xỉ 0,16 lit/kg ơ bệnh nhi từ 13- 17 tuồi.
Ertapenem thẩm được vảo vết rộp da do’ ap lực hút tạo nên Nồng độ của enapenem trong dịch của vết rộp
da ơ môi thời điểm iấy bệnh phấm trong ngảy điều trị thứ ba vởi liều [ g truyền tĩnh mạch ngảy 1 lần được
trình bảy ở Bảng 5. Tỷ số AUC ơ dịch vết rộp da so với AUC trong huyết tương 18) 0,61.
BẢNGS:
Nồng độ (mcg/mL) ertapenem trong dịch vết rộp da cùa người lớn ở mỗi thời điếm lấy bệnh phẳm
vảo ngảy điều trị thứ 3 với liều 1 ;; truyền tĩnh mạch ngảv 1 lần
0,5 giờ 1 giờ 2 giờ 4 giờ 8 giờ 12 giờ 24 giờ
7 12 ]7 24 24 21 8
ợđV
13 b
_/,
ìn..
MKOSZó-VNM-ZOI 5-01 1 140
S-WPC-MKO8Zó-IV/ 1M-06201 5
Hâm lượng enapenem trong sữa mẹ, thu thập ở 5 bả mẹ cho con bú được đo ở các thời điểm chọn ngẫu
nhiên trong ngảy, xét nghiệm liên tục 5 ngảy sau khi truyền tĩnh mạch liếư enapenem cuối cùng. Nổng dộ
của ertapenem trong sữa của cả 5 bả mẹ vảo ngảy điều trị cuối cùng (5- 14 ngảy sau khi sinh) là 65 tuổi lả
khoảng 39% vả 22%, cao hon một chút so với người lớn trẻ tuối (<65 tuổi). Không cần điếu chinh liều lượng
ở người cao tuối.
Bênh _nhi
Nồng độ huyết tương của ertapenem ở bệnh nhi 13- 17 tuổi tương đương với người lớn dùng liều 1 g tiêm
truyền tĩnh mạch ngảy ] lần.
Giá trị cảc thông số động học ở bệnh nhi từ 13- 17 tuốỉ khi dùng liếư 20 mglkg (tối đa 1 g) nhìn chung tương
tự ở người lớn trẻ khóe mạnh. Ba trong số sảu bệnh nhân từ 13- 17 tuổi dùng lỉều ít hơn 1 g. Đế ước tính cảc
dữ liệu dược động học khi tắt cả cảc bệnh nhân trong nhóm tuổi nảy đểu dùng liền 1 g, dữ liệu dược động
học được điều chinh theo liếư ] g, với giả định tuyến tinh theo Iiếu dùng. So sảnh các kết quả cho thấy các
bệnh nhân từ 13- 17 tuổi dùng liều 1 g enapenem ngảy ] lần đạt được các đặc tính dược động tương đương ở
người lớn. Tỷ số (nhỏm 13- 17 tuổi/ người lớn) của cảc giá trị AUC là 0, 99, nồng độ ngay khi kết thúc tiêm
truyền là 1,20 vả nồng độ tại điểm giữa của khoảng cảch các 1iều là 0,84.
Nồng độ huyết tương tại điềm giữa của khoảng cảch cảc liếư khi tiêm tĩnh mạch ertapene_m liều dơn
15 _mg/kg cho bệnh nhi từ 3 thảng đến 12 tuối thì tương đương với nồng độ huyết tương tại đíếm giữa cùa
khoảng cách cảc liều khi tiêm tĩnh mạch Iỉếu 1 g ngảy 1 lần ở người 1ởn (xem Phân phối) Độ thanh thải
… ,W
/.ả/l
lỆh
\ 8\ .3. '
MKO826-VNM—ZO 1 5-01 1140
S-WPC—MKO82Ó- 1VlIM-OôZO 1 5
ertapenem tại huyết tương (lephủt/kg) ở bệnh nhi từ 3 thảng đến 12 tuốí cao hơn xắp xi 2 lần ở người lớn
Khi dùng liều 15 mg/kg, giá trị AUC (gắp đôi đối với chế độ điều trị 2 lầnlngặy, nghĩa là 30 mg/kg/ngảy) ở
bệnh nhi từ 3 tháng đển 12 tuổi thì tương tự giá trị AUC ở người lớn trẻ tuôi khỏe mạnh được truyền tĩnh
mạch liểu đơn 1 g extapenem.
.S_uy_ga_n
Chưa xảc đinh dược động học cùa ertapenem ở người suy gan Do thuốc nây it chuyến hoả qua gan, nên
động học cùa thuốc rất có thế không bị ảnh hướng khi suy gan. Vì vậy, không cân chinh 1iều khi suy gan.
Suv thân
Sau khi truyền tĩnh mạch một liều đơn 1 g ở người lón, AUC ở người suy thận nhẹ (độ thanh lọc creatinin từ
60- 90 mL/phủt/l ,73 m 2) tương đương với AUC ở 11 ười khoẻ mạnh (25- 82 tu_ối). Nhưng ở người suy thận
vừa (độ thanh lọc creatinin từ 31- 59 lephủt/l ,73 m ), AUC tăng khoảng 1 ,5 lẩn so với ở người khoẻ mạnh.
Ở người suy thận tiến triển (độ thanh 1ọc creatinin từ 5- 30 mL/phut/ 173 m ), AUC tăng khoảng 2 ,6 lần so
với người khoẻ mạnh. Ở người suy_ thận giai đoạn cuối (độ thanh iọc creatinin <10 mL/phủt/ 1,73 m²), AUC
tảng khoảng 2, 9 lần so với ở người khoẻ mạnh. Sau khi truyền tĩnh mạch một liều 1 g ngay trước khi '
phân máu, khoảng 30% liếư dùng được tim thẩy trong dịch thẩm phân. Không có dữ liệu ở bệnh nhi bầ_
thận.
Cần chinh liếư eLtapenem ở người lớn bị suy thận tiến triến hoặc ở giai đoạn cuối (xem LIÊU LƯỢNG
CÁCH DÙNG). ẩọ'ù
QUẢ LIÊU
Không có thông tin đặc biệt về điếu trị quá liều INVANZ. Hầu như không có trường hợp cố tinh dùng quá
liều INVANZ. Không thấy có độc tính đảng kế trên người tinh nguyện trướng thảnh khỏe mạnh tiêm tĩnh
mạch mỗi ngảy 3 g INVANZ, dùng trong 8 ngảy. Trong nghiên cứu lâm sảng ở người 1ớn, vô tinh dùng mỗi
ngảy tới 3 g không gây phản ứng quan trọng trong lâm sảng. Trong cảc nghiên cửu lâm sảng ở trẻ em, tiêm
tĩnh mạch một liều đơn 40 mgfkg đến liều tối đa là 2 g cũng không gây độc tinh.
Nếu sử dụng quá liều, cẩn ngừng INVANZ vả điếu trị hỗ trợ chung tới khi thuốc đảo thải được qua thận.
Có thế thải INVANZ nhờ thẩm phân máu; tuy nhiên, chưa có thông tin về sử dụng thẫm phân mảu để điều
trị quá liều thuốc nảy.
DẠNG TRÌNH BÀY
INVANZ được cung ửng dưới dạng bột dông khô vô khuẩn dùn_ _~ . tr_uyến tĩnh mạch hoặc tiêm bắp,
mỗi lọ chứa 1 g ertapenem gốc acid tự do Mỗi hộp chứa một 1 . '
Trước khi hoân nguyên
Bảo quản ở Việt Nam ở nhiệt độ 2°C-8°C.
Dung dịch đã hoân nguyên để truyền _ .
Sau khi hoản nguyên, pha Ioãng_ ngay_ dung dịch thuốc với dung 1 - ' , 0 (xem LIEU LƯỢNG
VÀ CÁCH DÙNG, HUÓNG DÃN SỬ DỤNG), và có thế sử dụng trong vòng 6 giờ khi bảo quản ở nhiệt độ
phòng (25°C) hoặc bảo quản 24 giờ trong tủ iạnh ở nhiệt độ 5°C vả dùn tron vòng\4 0 sau khi lấy ra khỏi
tủ lạnh. Khõng được lảm đông đã dung dịch INVANZ. gTUỔẺ C,ỤL ử
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng