















\-
1~“` YTẾ
chQL
4LÝDUỌC
ĐẨỈHÊ DUYỆT
15 -1111- 1011
L_ẩn đau/l
iS-NDv-ll-viil
3lU
0000000000
ọ2702/36t
Each vìai contains ertapenem
Product be stored in Viet Nam:
between 2-8°C .
sodium equivalent to enapenem ig.
fflintuóc BẤN THEOĐơN.
LNMúNZ®
9—
1 0
Powder for injection.
Single Dose via! for
Intravenous or
Intramuscular injection
£ặma›
ĐỂ xa TẨM TAY TRẺ EM.
ĐỌC KỸ HƯỚNG DẦN sử
DỤNG rnươc KHI DÙNG.
Chỉ định, cách dùng, chóng ch1
đinh và các thông tin khác: vui
lòng xem tờ hưởng dản sử dụng
đính kèm.
Bột pha dung dịch tiem tiuyèn
tĩnh mạch hoảc tiêm báp.
Hộp 1 iọ bột pha tiêm.
Mòi lọ chứa ertapenem natri
tương dương 1 g ertapenem
duởi dạng gõc acid tự do.
Bảo quán ở Viêt Nam ở nhiẻt
dô 2—8”C.
SĐK/REG.: VN-xxxx-xx
ĐẠI DIỆN
TẠ!
T.P HÀ NỘI
Sản xuãt bời:
Labuutciưes Merck Sharp &
Dchmc —chlbm. Route de Mavsat.
Riom, F — 63963 CiemonL-Fenand,
Cedex 9, Pháp
Đòng gói bời:
PT Mcrclt Sharp Doth Pharma TblL.
Ji. Raya Pandaan Km 48, Pandaan,
Pasuruan. lawa Tưnur. Indonesia
Doanh nghiệp nhập khẩu:
Cỏng ty cổ phản dươc liệu TW 2.
24 Nguyên Thị Nghia. Q. 1.Tp. Hô
Chí Minh
111111
L
F Wimmpp axaton
xmx .LOVXSỸIỸS
(hi el_nh, cảch dùng. dìdna
dtiđịnh vả cá: Lhònọ lln k i'c
vui lòng mm lờ hưứìg dln
sửdụng đính kèm.
Đóng gái bă: PT Murd: Shin
lỉuhme Fhamu Thu. Lndnuuna
0
0
ỆỆỆ ỂẳèỂl
ềẽ ỈS
ẳầ iz
ẵ9 Il~l
ẻỄ °
'Ẻ
!
—L
@
Mỏi lo rhùa ơtapenem
nmi Ian đưưẩ 1 ;
empenem dưđ ang gõc
add Lự do
Sán xuất bói:
mom
CMIIRET. Pháp
510 qlún 0 Viet Nu
ngl 00 2-l'C
MK0826-VNM—2016-012255
S-WPC-MKO8Zỏ—IV/IIVI—WZOM
THÔNG TIN SÁN PHẨM
LNVANZ®
(Ertapenem dùng để tiêm)
NHÓM THUỐC
INVANZ (Eriapenem dùng dễ tiêm) là 1- 13 methyl-carbapenem tổng hợp, vô khuần, dùng đường tiêm, có tảo
dụng kéo dải và có câu trúc dạng beta-iactam, như là peniciliin vả cephalosporin, có hoạt tính chống lại
nhiều vi khuẩn kỵ khí và ưa khí, cá gram âm và gram dương
THÀNH PHÀN
INVANZ được cung đng dưới dạng bột đông khô vô khuấn để pha truyền tĩnh mạch hoặc tiêm bắp. Mỗi lọ
chứa 1 g crtapenem gôc acid tự do.
Mỗi lọ INVANZ còn chứa cảc tá dược sau: 175 mg bicarbonat natri và hydroxid natri để điều chỉnh pH tới
7,5.
CHỈ ĐỊNH
Điếu tri
INVANZ được chỉ định để điều trị cảc bệnh nhiễm khuẩn từ trung binh tởi nghiêm trọng do các vi khuấn
nhạy cảm vởi khảng sinh nảy, cũng như điều trị khởi đầu theo kinh nghiệm trưởc khi xảc định được vi khuấn
gây bệnh trong cảc bệnh nhiễm khuẩn sau:
Nhiễm khuẩn ồ bụng có biến chửng Ỹx/
Nhiễm khuẩn da và tổ chức da có biến chứng, bao gồm nhiễm khuần chi dưới vả bản chán do đái tháo
đường
Viêm phồi mắc phải tại cộng đồng
Nhiễm khuẩn đường tiết niệu có bìến chúng bao gồm viêm thận- bế thận
Nhiễm khuẩn vùng chậu cẩp, bao gồm víêm nội mạc-cơ tử cung sau sinh nạo thai nhiễm khuẩn, nhiễm
khuẩn phụ khoa sau mô.
ơ Nhiễm khuấn huyết
Dư phòng 7 ~ _ _ _
INVANZ được chỉ định đê dự phòng nhiêm trùng tại chõ phân thuật ở ngưòi 1ởn trong phân thuật đại trực
trâng theo chương trinh mồ phiên.
LIÊU LƯỢNG VÀ CÁCH DÙNG
Liều thường dùng của INVANZ ở bệnh nhân từ 13 tuổi trở iên là 1 g, ngảy 1 lẩn. Líều thường dùng cùa
INVANZ ở bệnh nhi từ 3 thảng đến 12 tuồi là 15 mg/kg, ngảy 2 lần (không quá 1 gl ngảy).
Có thể truyền tĩnh mạch hoặc tiêm bắp. Nếu dùng đưòng tĩnh mạch, thời gian truyền tĩnh mạch phải hơn 30
phút.
Có thế tiêm bắp thay vì truyền tĩnh mạch INVANZ, để điều trị cảc nhiễm khuẩn chỉ cần tiêm bắp.
cỔẦỀP R
OSZG-VNM—20] 6—012255
S-WPC—MKOS26— lV/IM-O7ZO ] 4
Thời gỉan điều trị với INVANZ thông thường là 3- 14 ngảy, nhưng thay đổi tùy theo loại bệnh nhiễm khuấn,
vả vi khuẩn gây bệnh (xem CHỈ ĐỊNH). Nếu có chỉ định 1âm sảng, có thể chuyền sang kháng sinh đường
uống khi thấy có cải thiện về lâm sảng.
Trong cảc nghiên cứu lâm sảng có đối chứng, người bệnh được điều trị từ 3 tới 14 ngảy Thời gian điều trị
kéo dải bao lâu là do bác sĩ điều trị quyết định dựa vảo vị trí và mức độ nghiêm trọng cùa nhiễm khuấn vả
vảo đảp ứng lâm sảng cùa người bệnh. Trong một số nghiên cứu, bác sĩ quyết định chuyến điều trị sang
khảng sinh đường uỏng sau khi thấy có cải thiện về lâm sảng.
Dự phòng nhiễm trùng tại chỗ ở người lớn sau phẫu thuật đại trực trảng theo chương trình mo phiên: để
ngãn ngừa nhiễm trùng tại chỗ sau phẫu thuật đại trực trảng theo chưong trình, liều khuyến cáo là 1 g truyền
tĩnh mạch, dùng liều duy nhất 1 giờ trước khi phẫu thuật.
Với người suy thận: có thể dùng INVANZ đizều trị bệnh nhiễm khuẩn cho người suy thận. Với người bệnh có
độ thanh lọc creatinin >30 mL/phut/ 173 m2 thì không cần2 điều chinh 1iều.Nhưng với người lớn suy thận
đang tiến triễn (độ thanh lọc creatinin S30 mL/phủtll ,73 m 2) bao gồm người đang được thầm phân máu, thì
liều mỗi ngảy cần iả 500 mg. Không có dữ liệu vê sử dụng thuốc ở bệnh nhi bị suy thận.
Với người đang được thầm phán máu. trong một nghiên cứu lâm sảng, sau khi truyền tĩnh mạch một liều
duy nhất 1 g ertapenem trước khi thầm phân, có khoảng 30% liều được tìm thấy trong dịch thấm phân Khi
dùng iNVANZ liều 500 mg/ngảy trong vòng 6 giờ trước thẩm phân ở bệnh nhân người lớn, nên bổ sung
thêm liều 150 mg sau khi thẳm phân xong. Nhưng nếu đã dùng INVANZ ít nhất 6 giờ trước khi thẩm phân,
thì không cần liều bổ sung. Chưa có dữ liệu ở người bệnh lọc máu hoặc thẩm phân mảng bụng. Chưa có dữ
liệu ở bệnh nhi được thẩm phân mảu.
Nếu chỉ có nồng độ creatinỉn-máu thì dùng công thức Cockcroft vả 'Gault" để xác định độ thanh lọc
creatinin. Khi đỏ, nông độ creatinin-máu có thế tương ứng với trạng thải ôn định của chức năng thận:
Nam_ thể trọng (kg) x (140 - tuổi theo năm) (ỹ/
' (72) x creatinin huyêt thanh (mgl 100 mL)
Nữ: 0,85 x giá trị của nam (tính theo công thức trên)
Không cần chỉnh liều vởi người suy gan. (Xem CÁC ĐẶC TÍNH DƯỢC ĐỘNG HỌC, Đặc điểm của người
bệnh, Suy gan)
Liều dùng INVANZ không phụ thuộc tuổi (13 tuối hoặc lớn hơn) hoặc giới tinh.
HƯỚNG DẨN CÁCH DÙNG
Bênh nhân 13 tuổi hoãc lớn hơn
Chuẩn bi dung dích truvền tĩnh mach
ĐỪNG TRỌN LÃN HAY CÙNG TRUYỀN iNVANZ VỚI CÁC THUỐC KHÁC
ĐỪNG HOÀN NGUYÊN vót CÁC DUNG DỊCH có CHỬA DEXTROSE (oc-D—GLUCOSE)
CÀN HOÀN NGUYÊN VÀ PHA LOÃNG INVANZ TRƯỚC KHI TIÊM.
1. Dùng 10 mL của một trong cảc dung môi sau, bơm vảo lọ INVANZ 1 g đế hoản nguyên: nước pha tiêm,
dưng địch tiêm NaCi 0,9% hoặc nước pha tiêm có chất kiềm khuẩn.
2. Lảc kỹ'đê hòa tan hêt, sau đó chuyên ngay sang lọ chứa 50 mL dung dịch tiêm NaCl 0,9%.
3. Hoản tât truyền tĩnh mạch trong vòng 6 giờ sau hoản nguyên.
Chuẩn bi cịung dich tiệm bắg _
CAN HOAN NGUYEN INVANZ TRƯỚC KHI TIEM.
" Công thửc Cockcrotì vá Gault: Cockcroft DW, Gault MH. Dự tính dộ thanh 100 creatinin dưa Lrên creatinin- máu Thân hoc. 1976
__ S. \`2\\
0826-VNM—2016-012255
S-WPC—MKOSZó—IV/IM—O7ZOM
1. Hoản nguyên lọ ] g INVANZ vởi 3,2 mL dung dịch tiêm lidocain HCl 1% hoặc 2% … (không chứa
epinephrine). Lắc kỹ lọ để hòa tan hết thuốc.
2. RL’Lt ngay dung dịch vừa pha và tiếm bắp sâu vảo nơi có khối cơ lớn (như cơ mông hoặc phần bên đùi)
3. Nên dùng dung dịch đã pha đế tỉêm bắp trong vòng 1 giờ sau khi hoản nguyên.
Chủ ỷ: Tuyệt đối không được truyền tĩnh mạch dung dịch nây.
Bênh nhi từ3 tháng đễn 12 tuổi
Chuẩn bi dung dich truvên tĩnh mach
ĐỪNG TRỌN LĂN HAY CUNG TRUYỀN INVANZ VỚI CÁC THUỐC KHÁC
ĐỪNG HOÀN NGUYÊN VỚI CÁC DUNG DỊCH có CHỬA DEXTROSE (oc-D—GLUCOSE)
CẨN HOÀN NGUYÊN VÀ PHA LOÃNG INVANZ TRƯỚC KHI TIÊM.
1. Dùng 10 mL của một trong cảc dung môi sau bơm vảo lọ TNVANZ ] g đế hoản nguyên: nước pha tiêm,
dung dịch tiêm NaCI 0,9% hoặc nước pha tiêm có chất kiềm khuẩn.
2. Lắc kỳ để hòa tan hết, sau đó rủt một thể tích tương đương với 15 mglkg thể trọng (không quả 1 glngảy)
hòa vảo dung dịch tiêm NaCl 0,9% để đạt được nông độ cuối cùng là 20 mg/mL hoặc thấp hơn
3. Hoản tất truyền tĩnh mạch trong vòng 6 giờ sau khi hoản nguyên.
Chuẩn bi cịung dich tìêm bẳQ '
CAN HOAN NGUYEN INVANZ TRƯƠC KHI TIEM.
1. Hoản nguyên lọ ] g TNVANZ với 3, 2 mL dung dịch tiêm lidocain HC] 1% hoặc 2% (không chứa
epinephrine). Lắc kỹ lọ để hòa tan hết thuốc.
2. Rút ngay dung dịch vừa pha một thể tích tương đương 15 mg/kg thể trọng (không quá 1 g/ngảy) và tiêm
bắp sâu vảo nơi có khối cơ lởn (như cơ mông hoặc phân bên đùi).
3. Nên dùng dung dịch đã pha đế tiêm bắp trong vòng 1 giờ sau khi hoản nguyên.
Chú ý: Tuyệt đối không được tỉêm truyền tĩnh mạch dung dịch nây.
Thuốc tiêm cần được kiếm tra kỹ bằng mắt xem cớ vật lạ hoặc đồi mảu trước khi sử dụng. Dung dịch
INVANZ 1ả từ không mảu tởi vảng nhạt. Nêu thay đôi mầm trong phạm vi nảy thi không có ảnh hưởng tởi
hiệu iực của thuôo.
CHỐNG CHỈ ĐỊNH i
Người quá mẫn với các thảnh phần của INVANZ hoặc với các kháng sinh cùng nhóm hoặc ở người bệnh đã
có phản ứng phản vệ với B-lactam.
Do sử dụng dnng môi_lidocain H_CI pha dung dịch tiêm bắp, nên chống chỉ định tiêm bắp INVANZ cho
người được biêt quá mâu với thuôo tê nhóm amid vả ở người bệnh bị sốc nghiêm trọng hoặc blốc tim (xin
tham khảo thông tin kê đon với lidocain HCl).
THẬN TRỌNG
Đã có những bảo cảo phản ứng quá mẫn nghiêm trọng, có khi tử vong (phản vệ) ơ người bệnh dùng kháng
sinh 13- lactam. Những phản ứng nảy dễ gặp hon ở người đã có tiền sử mẫn cảm với nhiều loại dị nguyên. Đã
có những bảo cảo vê người bệnh có tiên sử quá mân vởi penicillin thì cũng có những phản ứng quá mẫn
nghiêm trọng khi dùng cảc [3- lach khảc Vì vậy, trước khi dùng INVANZ, cần điều tra kỳ người bệnh về
các phản ứng quả mẫn trưởo đây với cảc penicíiiin, cephalosporin, các [3- lactom khác và với những dị
nguyên khảc. Nếu gặp phản ứng dị ứng với INVANZ, phải ngừng thuốc ngay. Cần điếu trị cẩp cứu kịp
thời các phản ứng phản vệ nghỉêm trọng.
Những bải viết trên y văn về các trường họp riêng kê cho thấy rằng sử dụng carbapenems, bao gồm
ertapenem đồng thòi với acid valproic hoặc divalproex sodium sẽ lảm giảm nông độ acid valproic. Nồng độ
acid valproic có thể bị giảm thấp hơn nồng độ trị liệu do tương tảo nảy, do đó lảm tăng nguy cơ bộc phảt cơn
co giật. Tăng liều acid valproic hoặc divalproex sodium có thể không đủ khắc phục được tương tác nây.
ss #
Xin tham khảo thông tin kẽ toa của Lidocain HCl
0826—VNM—201 6—012255
S-WPC-MKO82ó-IV/IM—O72O ] 4
Nhin chung, không khuyến cáo dùng acid vaiproic/divaiproex sodium chnng với ertapenem. Có thể dùng các
khảng sinh khảo ngoải carbapenems dể trị các bệnh nhiễm khuẩn ở các bệnh nhân đang được kiếm soát tốt
con co giật với acid valproic hoặc divaiproex sodium. Nếu cần thiết phải dùng INVANZ, nên xem xét dùng
thêm một liệu phảp chống co giật khảc (xem TƯỜNG TẢC THUỐC).
Cũng như cảc khảng sinh khảc, dùng INVANZ kéo dải sẽ lảm tăng sinh cảc chủng vi khuấn không nhạy cảm
với khảng sinh nảy. Cần phải đảnh giá liên tục tinh trạng bệnh. Nêu bội nhiễm xảy ra trong khi điêu trị, cân
có biện phảp điều trị thích hợp.
Đã có các báo cáo về viêm ruột kết mảng giả, từ nhẹ tới ảnh hướng tới tính mạng với hầu hết cảc thuốc
khảng sinh kể cả ertapenem. Vì vậy, cân nghĩ đến biến chứng nảy khi chấn đoán người bệnh bị tiêu chảy sau
khi dùng thuốc khảng khuẩn Cảo nghiên cứu cho thấy một độc tố tiết ra từ Clostrỉdium difflcile lá nguyên
nhân hảng đầu của “viêm ruột kết do khảng sính”.
Cần thận trọng khi tiêm bắp INVANZ, đế trảnh vô tinh tiêm vâo mạch mảu (xem LIÊU LƯỢNG vA cÁcn
DUNG).
Lidocaine HCl là dung môi dùng để tiêm bắp INVANZ. Xin tham khảo thông tin kê đơn lidocaine HC].
KHI MANG THAI
Chưạ có những nghiên cứu đầy đủ và có đốichứng tốt trên phụ nữ mang thai. Chỉ dùng INVANZ trong thai
kỳ nêu lợi ích điêu ttj hơn hăn nguy cơ có thế xảy ra cho mẹ vả cho thai.
… CHO CON BỦ
Ertapenem bải tiết qua sữa mẹ (xem CÁC ĐẶC TÍNH DƯỢC ĐỘNG nọc, Phân bố). Thận trọng khi dùng
INVANZ cho bả mẹ đang cho con bú.
TRẺ EM 31
Tính an toản vả hỉệu lực của INVANZ ơ bệnh nhi từ 3 thảng đến 17 tuổi đã được chứng minh qua tải liệu từ
các nghiên cứu đầy đủ vả có đối chứng tốt ở người lởn, cảc dữ liệu Dược động học ở bệnh nhi, và các dữ
liệu bổ sung từ các nghiên cửu dùng cảc thuốc khác đối chứng ở bệnh nhi từ 3 thảng đến 17 tnổi có các
nhiễm trùng sau dây (xem CHỈ ĐỊNH vả CÁC ĐẶC TÍNH DƯỢC ĐỘNG HỌC, Đặc điếm của người bệnh,
Bệnh nhi)
o Nhiễm khuẩn ổ bụng có biến chứng
Nhiễm khuẩn da và cảc tổ chửc da có biến chứng
Viêm phổi mắc phải tại cộng đồng
Nhiễm khuẩn đường tíết niệu có biến chứng
Nhiễm khuẩn vùng chậu câp
Nhiễm khuẩn huyet
Không khuyến cáo sử dụng INVANZ ở trẻ em dưới 3 tháng tuồi vi không có dữ liệu.
NGƯỜI CAO TUỔI
Trong nghiên cứu lâm sảng, tính an toản vả hiệu lực của INVANZ ở người cao tuổi (265 tuối) cũng tương
đương như ở người trẻ tuổi hơn (<65 tuối).
TƯO'NG TÁC THUỐC
Khi phối hợp ertapenem với probenecid, probenecid cạnh tranh dẫn đến ức chế sự đảo thải chủ động
ertapenem qua ông thận, nên lảm Lãng tuy it nhưng có ý nghĩa thống kê về thời gian bán thải (tăng 19%) và
nồng độ cùa ertapenem trong cơ thể (25%). Không cần điều chỉnh liều ertapenem khi phối hợp vởi
probenecid. Vì tảc dụng không đáng kể tới thời gian bản thải của ertapenem, nên không khuyến cảo dùng
phối hợp probenecid để kéo dải thời gian bản thải cùa ertapenem.
0826—VNM-2016-012255
S-WPC-MKOS2õ—[V/IM—O7ZO 14
Nghiên cứu in vitro cho thấy ertapenem không ức chế sự vận chuyến digoxin hoặc vinblastin qua trung gian
P—glycoprotein vả ertapenem không phải là chất nền dùng trong sự vận chuyền qua trung gian P-
glycoprotein. Nghiên cứu in vitro trên microsom gan người thấy ertapenem không ức chế chuyền hỏa của
thuốc khác qua xúc tảc cùa 6 đồng dạng cytochrom p450 (CYP) chủ yêu lả: 1A2, 2C9, 2C19, 2D6, 2E1 vả
3A4. Chưa chẳc có tương tác thuốc vởi ertapcnem qua cơ chế ức chế thanh thải thuốc qua trung gian của P-
glycoprotein hoặc qua xúc tảo của cytochrom p450. (xem CẢC ĐẶC TÍNH DƯỢC ĐỘNG HỌC, Phân bố
và Chuyến hóa).
Ngoài probenecid, chưa thực hiện cảc nghiến cứu chuyên biệt khảc về tương tác trên lâm sảng.
Những bải viết trên y vản vế cảc trưòng hợp riêng iẻ cho thấy sử dụng carbapenems, bao gồm ertapencm
đồng thời với acid valproic hoặc divalproex sodium sẽ lảm giảm nông độ acid valproic. Nồng độ acid
vaiproỉc có thể bị giảm thấp hơn nông độ trị liệu do tương tảc nảy, đo đó lảm tăng nguy cơ bộc phảt cơn co
giật. Mặc dù cơ chế của tương tảo nảy chưa được biết rõ, dữ lỉệu từ các nghiên cứu trên động vật vã in vitro
cho thấy carbapenems có thế ức chế sự thủy phân chất chuyến hóa glucuronide của acid valproic (VPA—g)
thảnh acid vaiproic, do đó lảm giảm nồng độ huyết thanh cùa acid valproic (xem THẬN TRỌNG).
ẨNH HƯỞNG CỦA THUỐC LÊN KHẢ NĂNG LÁ] XE VÀ VẶN HÀNH MÁY MÓC
Không có dữ liệu cho thấy lnvanz ảnh hưởng lên khả năng iái xe và vận hảnh mảy móc.
TÁC DỤNG PHỤ q/
Người lớn _ '
Trong cảc nghiên\cứu lâm sậng, tông sô người bệnh đùng ertapenem là hơn 1900, trong đó hon 1850 ngưòi
dùng INVANZ liêu 1 g. Phân lớn những phản ứng bât lợi được báo cảo trong nghiên cứu lâm sảng có mức
độ nhẹ tới trung binh. Những phản ứng có liên quan đến ertapenem chiếm khoảng 20% số người bệnh được
điêu trị băng ertapenem. Ngừng thuôc do phản ứng liên quan đến thuốc thường gặp ở 1,3% sô người bệnh.
Những phản ứng liên quan đến thuốc hay gặp nhất trong khi dùng ertapenem dạng tiêm nảy là tiêu chảy
(4, 3%), biến chứng ở tĩnh mạch tại chỗ tiêm (3,9%), buồn nôn (2,9%), nhức đầu (2,1%)
Sau khi tiêm ertapenem, đã gặp ở ngưòi bệnh những phản ứng sau đây có iiên quan tới dùng thuốc:
- Hay gặp (217100, <1/10) Rối loạn hệ thần kinh Nhức đẩu
Rối loạn mạch máu Biến chứng 6 tĩnh mạch tại chỗ tiêm, viêm
tĩnh mạchl viêm tĩnh mạch huyêt khôi
Rối ioạn tiêu hóa Tiêu chảy, buồn nôn, nôn
- Ỉt gặp (›1/1000, <1/100) Rối ioạn hệ thần kinh Choáng vảng, buồn ngù, mất ngủ,
co giật, lù lân
Rối loạn tim mạch Hạ huyết áp, thoát mạch
Rối loạn hô hấp, Khó thở
Lồng ngực và trung thất
Rối loạn tiêu hóa Nhiễm nấm Candida miệng, tảo bón, trảo
ngược dịch vị, tiêu chảy liên quan đên
C.difflcile, khô miệng, khó tiêu, chản ăn
Rối loạn da và mô dưới da Ban đó, ngứa
OSZó-VNM—20l 6-0 12255
S-WPC-MKOSZỏ—IV/IM—O7ZO14
Rối loạn chung Đau bụng, rối loạn vị giác, suy nhượcl mệt
vả tinh trạng tại nơi tiêm mỏi, nhiêm nâm Candỉda, phù/sưng, sôt,
đau, đau ngực
Rối loạn hệ sinh dục và vú Ngứa âm đạo
Trong cảc nghiên cứu iâm sảng, cảc phản ứng co giật có thể gặp sau khi tiêm là 0,2% người dùng ertapenem,
ớ 0,3% người dùng pìperacillin/tazobactam vả ở 0% người dùng ceftriaxione.
Trong phần lớn cảc nghiên cứu lâm sảng, khảng sinh dạng tiêm được tiếp nối bằng khảng sinh dạng uống
(xem CÁC ĐẶC TÍNH DƯỢC LỰC HỌC, Các nghiên cứu lâm sảng). Trong suốt thời kỳ điếu trị và thời kỳ
14 ngảy theo dõi sau điều trị, những phản ứng liên quan đến thuốc INVANZ bao gồm những phản ứng đã
nếu ở trên, cũng như phát ban và viêm âm đạo có tỷ lệ 21,0% (hay gặp) vả cảc phản ứng dị ứng, khó chịu và
nhiễm nấm có tỷ lệ ›0,19o nhưng <1,09o (ít gặp).
Trong một nghiên cứu lâm sảng về điều trị nhiễm trùng bản chân do đải tháo đường ở 289 bệnh nhân người
1611 bị đải thảo đưòng được điêu trị với ertapcnem, đặc tính vê phản ứng bât iợi 1iến quan đên thuôc nhin
chung tương tự như cảc phản ứng đã quan sát trong cảc thử nghỉệm lâm sảng trước đó.
Trong một nghiên cứu lâm sảng về sử dụng INVANZ trong dự phòng nhiễm trùng tại chỗ sau phẫu thuật đại
trực trảng theo chương trình trên 476 bệnh nhân người lớn dùng 1 g ertapenem trước khi phẫu thuật, chỉ có
chậm nhịp xoang là phản ứng bẩt iợi liên quan đến thuốc duy nhắt không thấy trong cảc thử nghiệm lâm
sảng trước đó đã được bảo cáo với tỷ lệ >0,1% nhưng <1,0% (ít gặp).
Bệnh nhỉ
Có tổng cộng 384 bệnh nhi được điều trị với ertapenem trong các thử nghiệm lâm sảng. Đặc tinh an toản
chung của thuốc ở trẻ em thì tương tự như người Ión. Trong các thử nghiệm lâm sảng, phản ứng bất lợi Lrên
lâm sảng liên quan đến thuốc phổ biến nhẩt trong suốt trị liệu được bảo cáo là tiêu chảy (5,5%), đau tại noi
tiêm (5,5%) và ban đó tại nơi tiêm (2,6%).
Cảc phản ứng bất lợi liến quan đến thuốc sau đây được bảo cáo trong thời gian bệnh nhi điều trị với
ertapenem:
Hav căn (>1/100. <1/10)
Rối loạn tiêu hóa: tiêu chảy, nôn
Các rối loạn chung và tinh trạng tại nơi tiêm: ban đó tại nơi tiêm, đau tại nơi tiêm, viêm tĩnh mạch tại nơi
tiêm, sưng tại nơi tiêm.
Cảo rối loạn da và mô dưới da: phát ban
Cảc phản ứng bất lợi liên quan đến thuốc đã được bảo cảo trong lúc điều trị (trên ›0,5% nhưng <1,0% số
bệnh nhân dùng INVANZ trong cảc thử nghiệm lãm sảng) bao gồm: chai cứng tại nơi tiêm, ngứa tại nơi
tiêm, viêm tĩnh mạch và nóng tại nơi tiêm.
Trong cảc nghiên cứu lâm sảng trên bệnh nhi, phần lớn các bệnh nhân được điều trị với khảng sinh đường
tíếm sau đó chuyến sang khảng sinh đưòng uống thích hợp. Trong suốt thời gian điếu trị và thời gian theo
dõi 14 ngảy sau trị liệu, các phản ứng bất lợi liên quan đến thuốc ở các bệnh nhân dùng INVANZ cũng
tưong tự như các phản ứng được liệt kê phía trên.
Kinh nghiệm hậu mãi
Những phản ứng bất lợi sau đây đã được báo cáo khi thuốc dùng trên thị trường:
Hệ miễn dịch: phản vệ bao gồm cả cảc phản ứng dạng phản vệ
Rối loạn tâm thần: thay đổi trạng thải tâm thần (bao gồm kích động, hung hăng, mê sảng, mất phương
hướng, cảc thay đổi trạng thái tâm thần)
Rối loạn hệ thẳn kinh: giảm ỷ thửc, loạn vận động, bắt thường về dảng đi, ảo giảc, giật rung cơ, run
Rối loạn dạ dảy — ruột: Lâm xăng xỉn mảu.
Rối loạn da và mô dưới da: ngứa, phát ban do thuốc với tăng bạch cầu ưa acid và những triệu chứng toản
thân ( hội chứng DRESS).
0826-VNM-201 6-012255
S-WPC-MKO82ó-IV/LM-O7ZO 1 4
Rối Ioạn cơ xương khớp vá mô liên kết: Yếu cơ
BÁO `NGAY`CHOABÁQ sĩ HOẶC pƯỌg sĩ CỦA BẠN NÊU GẶP BẨT CỨ TRIỆU CHÚNG BÁT
THƯỢNG NAO KE TREN HAY KHAC NƯA.
Xét nghiệm cận lâm sảng
N…4ươ—wóv . ,
Những bât thường hay’xảy ra nhật cớ liên quan tới thuôo khi dùng INVANZ là tăng enzym gan (ALT, AST),
phosphatase kiêm vả sô lượng tiêu câu.
Trong phần lớn cảc nghiên cứu lâm sảng, tiêm INVANZ được tiếp nối bằng khảng sinh đường uống thích
hợp (xem CÁC ĐẶC TINH DƯỢC LỰC HỌC, Các nghiên cứu lâm sảng). Trong suốt thời kỳ điều trị và 14
ngảy theo dõi sau điếu trị, những bất thường về kết quả xét nghiệm có liên quan tới thuốc ở người đùng
INVANZ không khảo với những bất thường đã nêu ở trên.
Những bất thường khác về kết quả xét nghiệm có lỉên quan tới thuốc bao gồm: tăng bilirubin trực tiếp trong
huyết thanh, tãng bilirubin toản phần huyết thanh, tảng bạch cầu ưa eosin, bilirubin giản tiếp huyết thanh,
thời gian co cục máu, vi khuẩn niệu, nitơ u-rê mảu, creatinin huyết thanh, glucose huyet thanh, bạch cầu đơn
nhân, tế bảo biểu mô trong nước tiếu, hồng cầu níệu; lảm giảm bạch cầu phân thùy, bạch cẩu đa nhân trung
tính, hemoglobin, hematocrit và số lượng tiếu cầu.
Trong một nghiên cứu lâm sảng trên 289 bệnh nhân điều trị nhiễm trùng bặn chân do đải thảo đường với
ertapenem, nhin chung, cảc bất thường về kết quả xét nghiệm liên quan đên thuôo tương tự như các bât
thưòng đã quan sảt thây trong các thử nghiệm lâm sảng trước đó. 3/
ổ au phẫu thuật đại
Trong một nghiên cứu lâm sâng trên 476 bệnh nhân điều trị dự phòng nhiễm trùng tại ch `
trực trảng theo chương trình với 1 g ertapencm trước phân thuật, không có thêm cảc bât thường khảc vê kết
quả xét nghiệm trong quá trình điêu trị được bảo cáo.
Bénh nhí
Các bất thường xét nghiệm liên quan đển thuốc phổ biến nhất được quan sát thấy ở bệnh nhân sử dụng
ÍNVANZ là giảm bạch câu trung tính.
Cảo bất thường xét nghiệm khảo liên quan đến \thuốc trong suốt quá trình điều trị và 14 ngảy theo dõi gồm
có: tăng ALT, AST, giảm bạch cầu, tăng bạch câu eosin.
CÁC ĐẶC TÍNH DƯỢC LỰC HỌC
Enapenem có tác dụng in vitro chống nhiều vi khuấn ưa khí và kỵ khí, cá gram dương và gram âm. Tảc
dụng diệt khuẩn c_ùa ertapenem lả do ức chế tổng hợp vảch vi khuẩn: ertapenem gắn vảo cặc protein gắn
penicillin (PBP). O E.coli, ertapenem có ải lực mạnh với cảc PBP la, lb, 2, 3, 4 vả 5, chủ yêu 1ả với PBP2
vả PBP3. Ertapenem rất bền vững, không bị thuỷ phân bởi phần Iởn cảc loại B-lactamase, kể cả cảc
penicillinase, cephalosporinase vả cảc B-lactamase phố rộng nhưng không chống được metallo-B-lactamasc.
INVANZ có hoạt tính chộng được hầu hết cảc chùng của những vi khuấn sau đây cả in vỉtro và trong nhiễm
khuẩn lâm sảng (xem CHI ĐỊNH):
VL KHUẨN GRAM DƯONG ƯA KHÍ VÀ KY KHÍ KHÔNG BẨT BUỘC:
Staphylococcus aureus - tụ cầu vâng (bao gồm chủng tiết penicillỉnase)
Streptococcus agalactiae
Streptococcus pneumoniae
Streptococcus pyogenes
Chú thich: Tụ cầu kháng methicillin khảng iNVANZ. Nhiều chủng Enterococcusfaecalis vả hẩu hết chủng
Enterococcusfaecium cũng khảng INVANZ.
0826—VNM—201 6—012255
S—WPC-MKOSZó—IV/IM-O7ZO 14
VI KHUẨN GRAM ÂM ƯA KHÍ VÀ KY KHÍ KHÔNG BẤT BUỘC:
Escherìa coIí
Haemophilus injluenzae (bao gổm chùng tiết B-lactamase)
Klebsiella pneumoniae
Moraerla catarrhalis
Proteus mirabilis
VI KHUẤN KY KHÍ
Bacteroidesftagilis vả cảc loải khác trong nhóm B. fiagílis
Loải Clostridium (trừ C . dijìcile)
Loải Eubacterium
Loải Peptostreptococcus
Porphyromonas asaccharolylica
Loải Prevotella
Những dữ liệu in vitro sau đây hiện có sẵn, nhưng chua rõ ý nghĩa lâm sảng.
Nồng độ ức chế tối thiểu (MiG) in vitro của INVANZ 1ả 90%) các chủng của
Streptococcus bao gồm Streptococcus pneumoniae, nồng độ <0, 5 mcg/mL chống được phần lớn (>90%)
chủng của Haẹmophilus, <2 mcg/mL chống được phần lớn (290%) chủng vi khuẩn ưa khí và kỵ khí không
bắt buộc và nông độ <4 mcg/mL chống được phần lớn (>90%) chủng cảc vi khuẩn kỵ khi bắt buộc trong
danh sảch dưới đây; tuy nhiên, hiệu lực và tính an toản của INVANZ trong điều trị cảc bệnh nhiễm khuẩn
trên lâm sảng đo nhiễm cảc vi khuẩn nêu trên thì chưa chứng minh được trong cảc nghiên cứu lâm sảng có
đối chứng tốt và thích hợp:
VI KHUẨN GRAM DƯO'NG ƯA KHÍ VÀ KY KHÍ KHÔNG BẨT BUỘC: W
Staphylococcus, coagulase âm tính, nhạy cảm với methicillin.
Streptococcus pneumoniae khảng penicillin
Cảc Streptococcus viridans.
Chú thích: Tụ cầu kháng methicillin kháng INVANZ. Nhiếu chủng Enterococcus faecalis và hầu hết các
chủng Enterococcusfaecium cũng kháng INVANZ.
VI KHUẨN GRAM ÂM ƯA KHÍ VÀ KY KHÍ KHÔNG BẦT BUỘC:
Citrobacterfreundii
Enterobacter acrogenes
Enterobacter cloaceae
Escherichia coIi tiết ESBL
Haemophilus parainjluenzae
Klebsiella oxytoca
Klebsiella pneumoniae tiết ESBL
Morganella morganii
Proteus vulgaris
Serratia marcescens
Chú thích: Nhiều chùng cùa cảc vi khuấn nêu trên có đa để khảng với cảc khảng sinh khảo, như các
penicillin, cephalasporin (bao gồm thế hệ thứ ba) và cảc aminoglycosid nhưng lại nhạy cảm với INVANZ.
VI KHUÂN KY KHÍ
Loải F usobacterium
Xét nghiêm tính nhav cảm với kháng sinh
Khi có những kết quả in vitro về tính nhạy cảm với khảng sinh cùa vi khuấn, nên báo cáo định kỳ cho thầy
thuốc, trong đó mô tả đặc tính nhạy cảm cùa vi khuẩn gây bệnh ở bệnh viện và 1ây nhiễm ở cộng đồng.
Những báo cảo nảy sẽ giúp thầy thuốc lựa chọn được khảng sinh hiệu quả nhất.
Kỹ thuật pha Ioãng
0826—VNM-2016-012255
S-WPC-MKOSZó—IV/M—O7ZO ] 4
Dùng các phương phảp dịnh lượng để xảc định nồng độ ức chế tối thiếu (MIC) Những trị số MIC nảy sẽ
cung cấp trị số ước tinh về tính nhạy cảm cùa vi khuẩn đối với khảng sinh MIC đuợc xảo định bằng một
quy trình chuẩn hoá Quy trình chuẩn hoá dựa vảo phương phảp pha loãng (canh cấy hoặc thạch) hoặc
tương đương với nồng độ chuẩn hóa của chắt cấy truyền và nông độ chuẩn hoá cùa bột ertapenem Phân tỉch
các trị sô MIC theo các tiếu chí đuợc cung cấp ở Bảng 1.
Kỹ thuật khuếch tản
Nhng phương phảp dịnh lượng do đưòng kính cùa vòng vô khuẩn cũng cung cấp những trị số ước tính có
thế lặp lại về tính nhạy cảm của vi khuẩn đối với cảc kháng sinh. Một quy trinh chuẩn hoá như thếH' đòi hòi
sử dụng những nồng độ chuẩn hoá của chất cấy truyền Kỹ thuật nảy dùng những đĩa giấy tròn thấm 10 mcg
ertapenem đế thứ tính nhạy cảm của vi khuẩn đối vởi ertapenem. Những chi tiêu biến thị sự khuếch tán của
thuốc tâm vảo đĩa giấy được cung cẳp ở Bảng 1.
Kỹ lhuậi kỵ khí:
Với vi khuẳn kỵ khí, có thế xảo định tính nhạy cảm với extapenem qua MIC với một phương phảp thử
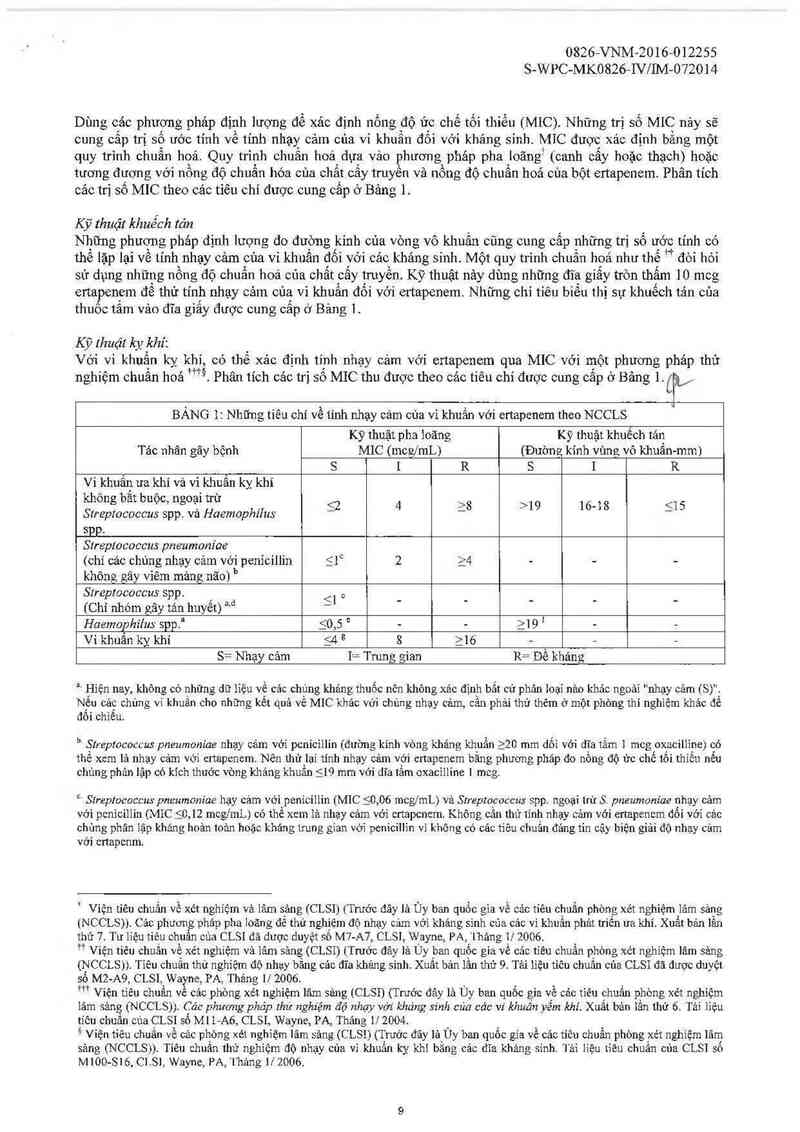
nghiệm chuẩn hoá ứẻ Phân tích các trị số MIC thu được theo các tiêu chí được cung cẳp ở Bảng 1. .ỉPị/
BẢNG 1 Những tiêu chí về tính nhạy cảm cùa vi khuẩn với ertapenem theo NCCLS
Kỹ thuật pha loãng Kỹ thuật khuếch tản
Tác nhân gây bệnh MIC (mcg/mL) (Đường kinh vùng vô khuẩn-mm)
S 1 R S [ R
Vi khuẩn ưa khi và vi khuẩn kỵ khí
khong bat buọc, ngoại trư _ 52 4 28 >19 16-18 515
Sưeplococcus spp. va Haemophzlus
spp.
Sireplococcus pneumoniae
(chỉ các chúng nhạy cảm với penicillin 51° 2 24 - - -
không gây viếm mảng não) "
Sireplococcus spp. <1 , _ _ _ _ _
(Chỉ nhóm gây tán hnyết) ²~ d “
Haemophiíus spp. _<_0,5 ° - - 219 1 - —
Vi khuẩn kỵ khi 54 , 8 216 - - -
S= Nhạy cảm 1= Trung gian R= Dế khảng
a~ 1_-Iiện nay, không có những dữ iiệu vệ cảc chưng kháng thuốc nên không xác định bắt cứ phân ioại nản khảo ngoảỉ "nhạy cảm ( S)".
Nếu các chủng vi khuân cho những kết quả về MIC khác với chủng nhạy cảm, cân phải thử thêm ở một phòng thí nghiệm khảc đê
đôi chiêu.
b Ẹireptococcus pneumoníae nhạy cảm vởi pcnicillin (đường kính vòng kháng khuẩn 220 mm dối với dĩa tằm 1 mcg_oxncillỉpe) có
thế xem là nhạy cảm với cnapenem. Nên thừ_lại tinh nhạy cảm với eitapcnem băng phương pháp đo nông độ ức chế tôi thíên nêu
chùng phân lập có kích thước vòng khảng khuân 519 mm với dĩa iảm oxacilline 1 mcg.
“ Slreptococeus pneumoniae hạy cảm vởipenícillin (MIC 50,06 mcgímL) vả Streptococcus spp. ngoại lrừ S. pneumoniae nhạy cảm
với pcnicillin (MIC 50,12 mcg/mL) có thế xem 113 nhạy cảm với crtapcncm. Không cân thừ tính nhạy cảm với ertapencm đôi với các
chủng phân iập kháng hoản toỉm hoặc kháng trung gian với penicillin vi không có cấu: tiêu chuân đảng tin cậy biện giải độ nhạy cảm
với crtapcnm.
ỷ Viện tiêu chuẩn về xét nghíệm và lâm sảng (CLSI) (Trước đây iả Ủy ban quốc gia về cảc tiêu chuẩn phòng xét nghiệm lâm sảng
(NCCLS)) Các phương pháp pha loãng để thử nghịệm độ nhạy cám với kháng sinh của các vi khuẩn phát triền ưa khí. Xuất bản lần
thứ 7. Tư liệu tiếu chuẩn cùa CLSI đã được dnyệt số M7-A7, CLSI, Wayne, PA, 'lhâng 1/ 2006.
" Viện tiêu chuẩn về xét nghiệm và 1ãm sảng (CLSI) (Trước đây lả Ủy ban quốc gia về cảc tiêu chnấn phòng xét nghiệm lâm sảng
(NCCLSD. Tiêu chuẩn thử nghiệm độ nhạy bằng các đĩa kháng sinh Xuất bản iần thứ 9. Tải iiệu tiêu chuẩn cùa CLSI đã được duyệt
số M2-A9, CLSI Wayne PA Tháng II 2006.
… Viện tiêu chuẩn về cảc phòng xét nghiệm lâm sảng (CLSI) (Trước đây là Ủy ban quốc gia về cảc tiêu chuẩn phòng xét nghiệm
lăm sâng (NCCLSD Các phương pháp thử nghiệm độ nhạy vm kháng sinh của các vi hhuần yểm khí. Xuất bản iần thứ 6 Tái liệu
tiêu chuẩn cùa CLSI số M11 —,A6 CLSI, Wayne, PA, Thảng 1! 2004.
ễ Viện tiếu chuẩn về các phòng xẻt nghiệm lâm sảng (CLSI) (Trước đây là Ủy ban quốc gía về các tiêu chuẩn phòng xẻt nghiệm lâm
săng (NCCLS)). Tiêu chuẩn thử nghiệm độ nhạy của vi khuẩn kỵ khi bằng cảc dĩa kháng sinh. 1211 liệu tiếu chuẩn của CLS] số
M 100-316, C1 SI, Wayne, PA, "ihz'mg 1/ 2006.
OSZó-VNM—ZOI 6—012255
S—WPC-MKO82ó-W/lM—O7ZO 14
d Streptococcus spp. gây tản huyết nhớm B nhạy cảm với penicillin (vòng khảng khuẩn >24 mm với dĩa tấm 10 đơn vị penicillin) có
thể xem là nhạy cảm với ertapcnem Nên thử lại tính nhạy cảm với eriapenem bằng phương pháp đo nồng dộ ức chế tối thiều nểu
chùng phân ìặp có kich thước vòng khảng khuẩn <24 mm với đ“ a tẩm 10 đơn vị penicillin Không cần Lhừ tính nhạy cảm với
ertapenem đối với Streptococci vỉridans vi không có các tiêu chuẩn đáng tin cậy biện giải độ nhạy cảm với penicillin
° Những tiêu chuẩn nây có thể áp dụng cho quy trình vi pha ioãng canh cấy, dùng môi trường thử nghiệm Haemophilus (HTM)
được cấy truyền với một dich treo khuẩn lạc trực tiểp vả ủ trong phòng ở 35°C trong 20-24 giờ
f Những đường kinh vòng vô khuẩn nảy oó thế áp dụng cho cảc thử nghiệm bằng kỹ thuật khuếch tản trên dĩa thạch, dùng môi
truờng thạch thử nghiệm Haemophilus (HTM) dược cấy truyền với một dịch treo khuẩn 1ạc trực tiếp vả ủ trong 5% CO; ờ 35°C
trong 16- 18 giờ.
®“ Nhũng tiêu chuẩn biền thị nảy chi có thế ảp dụng cho kỹ thuật pha loãng trong thạch, dùng thạch _Brucella có hồ sung hemín,
vitamin Kl và 5% mảu cừu đã loại bỏ fỉbrin hoặc rnảu đã ly giải được cấy truyền với một địch tren khuân lạc trực tiêp hoặc một mẻ
cấy mới từ 6 đên 24 giờ trong mỏi trường chửa nhiêu thioglycolat được ủ trong một bình hoặc buông ù yêm khí ở 35-37°C trong 42-
48 giờ.
Một báo cảo gọi là "Nhạy cảm" nếu tác nhân gây bệnh có thể bị ức chế ở nổng độ kháng sinh thử nghiệm
thường đạt được trong máu. Một bảo cảo gọi là "Trung gian" nếu kết quả được xem không rõ râng và nếu vi
khuấn không hoản toản nhạy cảm đối với những thuốc khác được xem là nhạy cảm trên iâm sâng, thì cần lặp
lại xét nghiệm. Phân loại nảy cho bỉết vân có thể dùng thuốc trên lâm sảng nếu những vị trí cùa cơ thể có
nồng độ phân bố thuốc cao hoặc trong trưòngl họp có thể dùng thuốc với liều cao. Phân loại nảy cũng cung
câp một vùng đệm nhằm ngăn ngừa những yêu tố sai sót kỹ thuật nhỏ có thể gây nên những khảo biệt lớn
khi phân tích kết quả. Một báo cáo gọi là "Kháng" nếu tảo nhân gây bệnh có thể không bị ức chế ở nồng độ
kháng sinh thử nghiệm thường đạt được trong mảu; do đó cần lựa chọn liệu phảp khảc. Ữ/
Kìếm tra chầt lượng
Những quy trình chuẩn hóa thử nghiệm tính nhạy cảm chuẩn hoá cần dùng những chùng vi khuẩn chuẩn đối
chứng nhằm kiểm tra những mặt kỹ thuật của quy trình thử nghiệm. Bột enapenem chuẩn cung cấp các giá
trị nông độ ghi ở bảng 2 dưới đây. Các vi khuẩn chuẩn đối chứng là những chùng vi khuẩn đặc hiệu có
những tính chất sinh học nội tại. Những chùng chuẩn đối chứng phải rất ốn định, luôn cho mô hình nhạy
cảm có tính chuẩn mực và có tính lặp lại. Những chủng đặc hiệu dùng trong kiếm tra chất lượng xét nghỉệm
vi sinh học không có ý nghĩa về mặt lâm sảng.
BÀNG 2: Phạm vi nồng độ có thể chấp nhận của vi khuẩn chuẩn đối chứng đối với ertapenem
Chim dùn để kìểm tra ® Thứ n hiệm ha loãn Th“ “glẾ'ẹm kh“eĩh ta"Lđĩa "
gchấẵượng ATCC (Mlcgtheo rỄchmLLg (đường kmh vằrịÌg)Vơ khuan theo
Enterococcus faecalis 29212 4-16 Không ảp dụng
Tụ cầu vảng 29213 0,06-0,25 Không ảp dụng
Tụ cầu vảng 25923 Không ảp dụng 24-31
Streptococcus pneumoniae " 49619 0,03-0,25 ' 28-35
Escherichia coli 25922 0,004-0,016 29—36
Haemophilus injluenzae 49766 0,016-0,06J 27-33 k
Pseudomonas aeruginosa 27853 2-8 13-21
Bacteroides ứagilis 25285 0,06-0,25 ' (0,06-0,25) '" Không áp dụng
Bacteroides thetaiotaomicmn 29741 0,25-1,0 ' (0,5-20) … Không áp dụng
Eubacterium lentum 43055 0,5-2,0 ' (0,5-0,4) `" Không ảp dụng
h Vi khuẩn nảy được dùng để kiếm tra chất lượng xẻt nghiệm tính nhạy cảm cùa Streptococcus pneumoniae vả Streptococcus spp.
* Nhũng nồng độ chuẩn, đối chứng nây có Lhẻ ảp dụng cho nhửngthứ nghiệm với Srreptococcus pneumonỉae ATCC 49619 bằng kỹ
thuật vi pha loãng canh cây với canh thang Mucller-Hinton dã điêu chinh cation chứa 2-5% máu ngựa ly giải được cấy truyền với
một dịch treo khuân 1ạc trực tỉêp vả ủ trong phòng ở 35°C trong 20-24 giờ.
’ Những nồng độ chuẩn, đổi chứng nảy có thể ap đụng cho cảc thừ nghỉệm vởí Haemophilus injluenzae ATCC 49766 bằng kỹ thuật
vi pha loãng canh cắy với môi trường thử nghiệm Haemophtlus (HTM) duợc cấy truyền với một dich treo khuẩn lạc trực tiêp vả ủ
trong phòng ở 35°C trong 20-24 giờ.
10
OSZõ—VNM-ZOló-O ] 2255
S-WPC—MKOBZõ-IV/IM-O7ZO 1 4
k Những nồng độ chuẩn, đối chứng nảy có thế ảp dụng cho cảc thử nghiệm với Haemophílus L'njluenzae ATCC 49766 bằng Ềỹ thuật
khuếch tán đ” a vởi môi trường thạch thử nghiệm Haemophilus (HTM) được cây truyên với một dịch treo khuẩn lạc trực tL p và ủ
trong 5% CO; ở 35°C trong 16-18 giờ
' Những nồng độ chuẩn, dối chứng nảy chi có thể áp dụng cho kỹ thuật pha loãng trong thạch, với thạch Brucella bổ sung hemin,
vitamin Kl vả 5% máu cừu dã loại bỏ f ban hoặc mảu bi ly giải, được cấy truyền với một dich treo khuấn lạc trực tiếp hoặc một mẻ
cắy mới từ 6 tới 24 giờ trong môi Lrường chứa nhiều thioglycolat vả được` u trong một bình hoặc buồng u yếm khi ở 35- 37“C trong
42-48 giờ.
"" Những nổng độ chuẩn, đối chứng nảy có thể áp dụng cho kỹ thuật vi pha loãng canh cấy
Cảo nghiên cứu lâm sản
Nguời lớn
Ertapenem đã được đánh giá trong một thử nghiệm lâm sảng ngẫu nhỉên, đa trung tâm, mù đôi, có đối chứng
ở 665 người lởn điều trị nhiễm khuẩn trong ô bụng có bỉến chứng: so sảnh ertapenem (mỗi ngảy một lẩn ] g
truyền tĩnh mạch) với piperacillin/tazobactam (truyền tĩnh mạch 3,375 g môi 6 giờ), dùng trong 5- 14 ngảy
Tại thời điếm 1—2 tuần sau thời kỳ điếu trị, tỷ lệ thảnh công về lâm sảng và vi sinh là 89, 6% (190/212) với
ertapenem và 82, 7% (162/196) với piperacillin/Iazobactam; sau khi điều trị 4- 6 tuần (đảnh giá khói bệnh),tỳ
lệ thảnh công là 86,7% (176/203) với crtapenem và 81,3% (157l193) với piperacillin/tazobactam.
Trong thử nghiệm lâm sảng, đảnh giá ertapenem ở 540 người lớn điều trị viêm da vả cấu trúc da có biến
chứng, so sánh ertapenem (mỗi ngây truyền tĩnh mạch một lần 1 g) với piperacillin/tazobactam (truyền tĩnh
mạch mỗi 6 giờ; môi lần 3,375 g) dùng trong 7- 14 ngảy, bao gồm nhìễm khuấn chi dưới do đải thảo đường
đường, áp— xe sâu mô mếm, nhiễm khuẩn vết thương sau chấn thương, viêm mô tế bâo dang dẫn lưu mù. Tỷ
lệ thảnh công trên lâm sảng vảo 10—21 ngảy sau thời kỳ điều trị (đảnh giả khỏi bệnh) là 82,2% (152/ 185) với
ertapenem và 84,5% (147/ 174) với piperacillin/tazobactam.
Ertapenem được đánh giá hiệu quả trong điều trị nhiễm trùng bản chân do đải thảo đường trong một thử
nghiệm lâm sảng có đối chứng, mù đôi, đa trung tâm, phan nhóm ngẫu nhiên Nghiên cứu nây so sảnh (1 g
IV ngảy 1 lần) với piperacillin/tazobactam (3,375 g IV môi 6 giờ) trên 586 bệnh nhân Cả 2 phảc đồ điều trị
đều cho phép chuyến sang liệu pháp amoxicillin/clavuclanate đường uống vởi thời gian điều trị tống cộng là
5—28 ngảy (cả đường tiêm vả đưòng ưống). Tỷ lệ thảnh công trên lâm sảng trong vòng 10 ngảy sau trị liệu là
87,4% (180/206) đối vởỉ enapenem và 82,7% (162/196) đối với piperacillin/tazobactam.
Trong hai thử nghiệm lâm sâng trên 866 người lớn điều trị viêm phổi mắc phải tại cộng đồng, ertapenem
(mỗi ngảy tiêm một lần 1 g) được so sảnh với ceftriaxone (mỗi ngảy tiêm một lẩn 1 g). Cả hai phảc đồ đều
cho phép chuyền sang liệu phảp amoxicillin/clavulanate đường uống vởi thòi gỉan điều trị tống cộng là 10-
14 ngảy (cả tiêm và uống). Tỷ lệ thânh công trên lâm sảng (gộp 2 nghiên cứu) vảo 7-14 ngảy sau thời kỳ
điều trị (đánh gỉá khỏi bệnh) là 92% (335/364) vởi eLtapenem và 91,8% (270/294) với ceftriaxone.
Trong hai thử nghiệm lâm sảng trên 850 người lớn điều trị viêm đường tiết niệu có biến chứng, bao gổm
vìêm thận-bể thận, ertapenem (mỗi ngảy tiêm 1 lần 1 g) được so sánh với ceftriaxone (mỗi ngảy tiêm một
lần 1 g). Cả hai phác đồ đều cho phép chuyến sang liệu pháp cíprofioxacin đường uống (500 mg, ngây uống
2 lần) với thời gian điếu trị tổng cộng là 10-14 ngảy (cả tiêm và uống). Tỷ lệ thảnh công về vi sinh học (gộp
2 nghiên cứu) vảo 5-9 ngảy sau thời kỳ điều trị (đánh giá khỏi bệnh) là 89,5% (229/256) với ertapenem và
91 ,] % (204/224) với ceftriaxone.
Trong một thử nghiệm lâm sâng, đảnh giả ertapenem (1 g truyền tĩnh mạch, ngảy 1 lần) so vởi
piperacillinltazobactam (3,375 g tiêm tĩnh mạch môi 6 giờ) dùng trong 3- 10 ngảy trong điều trị viêm vùng
chậu câp trên tổng cộng 412 ngưòi lớn bao gôm 350 người nhiễm trùng lúc sínhl sau khi sinh và 45 người
nạo thai nhíễm khuẩn. Tỷ lệ thảnh công trên iâm sâng vảo 2-4 tuần sau thời kỳ điều trị (đảnh giả khỏi bệnh)
là 93, 9% (153l163) với ertapenem và 91,5% (140/ 153) với piperacillin/tazobactam.
Một thử nghiệm đa trung tâm, mù đôi, phân nhóm ngẫu nhiên đảnh giá hiệu quả dự phòng trong phẫu thuật
trên 1002 người lớn, so sảnh INVANZ IV (] g) vởi cefotetan IV (2 g) tiêm truyền kéo dải 30 phủt vảo lgiờ
trước khi phẫu thưật đại trực trảng theo chương trình. Tỷ lệ đáp ứng lâm sảng có lợi nói chung vảo 4 tuần
11
OSZô-VNM-20ló-O1Z2SS
S-WPC-MKO8Zó—IVJIM-O72OI 4
sau phẫu thuật (tìêu chí chủ yếu đảnh giá hiệu quả) là 72,0% cho nhóm bệnh nhân dùng crtapencm (N=338)
và 57 2% ở nhóm dung cefotetan (N=334) (khác biệt 14,8%, [95% CI là 7, 5%— 21 ,9%]), cho thấy hiệu quả
vượt trội của ertapencm so với thưốc đối chng trong điều trị dự phòng cho cảc bệnh nhân phẫu thuật đại
trực trảng theo chương trình.
Trẻ em
Ertapenem được đảnh giả trong hai thử nghiệm lâm sảng đa trưng tâm, mù đôi, phân nhóm ngẫu nhiên trên
các bệnh nhi từ 3 tháng đến 17 tuổi. Thử nghiệm đẳu tiên kết nạp 404 bệnh nhi, so sảnh ertapenem <15
mglkg truyền tĩnh mạch mỗi 12 giờ trên bệnh nhi từ 3 tháng đến 12 tuổi và lg truyền tĩnh mạch ngảy L lần
cho bệnh nhi từ 13 tuối đến 17 tuổi) với ceftriaxone (SD mg/kg/ngảy truyền tĩnh mạch chia 2 lần trên bệnh
nhi từ 3 tháng đển 12 tuồi và 50 mg/kg/ngảy truyền tĩnh mạch ngảy 1 lần trên bệnh nhi từ 13 tuổi đến 17
tuối) trong điếu trị nhiễm khuẩn tiết niệu có bỉến chứng, nhỉễm khuẩn da và mô mềm hoặc viêm phồì mắc
phải tại cộng dồng. Cả hai phác đồ dền cho phép chuyển sang dạng ưống amoxicillin/clavulanatc vởi thời
gian điếu trị tống cộng 14 ngảy (tiếm và uống). Tỉ lệ thảnh công về vi khuẳn học được đánh gỉá trong một
phân tich dựa trên protoco] ở các hệnh nhi nhiễm khưẩn tiết niệu có biến chứng cho thắy lả 87, 0% (40/46)
đối với ertapenem và 90,0% (18/20) đối với ceftriazone. Tỉ lệ Lhảnh công trong một phân tích dựa trên
protocol ở cảc bệnh nhi được điếu trị nhiễm khuẩn da và mô mềm là 95, 5% (64/67) đối với ertapenem và
100% (26/26) đối với ceftriaxone và ở các bệnh nhặn được điều trị viếm phổi măc phải tại cộng đỗng là
96,1% (74/77) đối với crtapencm và 96, 4% (27/28) đối vởi ceftriaxone
Thử nghiệm thứ hai kết nạp 112 bệnh nhi và so sảnh crtapenem (IS mg/kg truyền tĩnh mạch mỗi 12 giờ trên
cảc bệnh nhi từ 3 thảng đến 12 tuốí và 1 g truyền tĩnh mạch ngảy ] lẩn trên bệnh nhi từ 13 tuốí đến 17 tuồi)
với tỉcarcillin/clavulanate (SO mg/kg đối với bệnh nhi <60 kg hoặc 3, 0 g đối với bệnh nhi >60 kg, ngảy 4
hoặc 6 lần) trong thời gian 14 ngảy trong điều trị nhiễm khuẩn ỏ bụng có biến chứng vả nhiễm khuẩn vùng
chậu cẩp. Trên các bệnh nhi được điều trị nhiễm khuấn ổ bụng có biến chưng (là những bệnh nhi trưởo đây
có lỗ dò hoặc viêm ruột thừa có biến chửng) ti 1ệ thảnh công trên lâm sảng lả 83, 7% (36/43) đối với
ertapenem và 63,6% (7/11) đối với ticarciilin/clavulanate trong một phân tích dưa trên protocol. Trên cảc
bệnh nhi dược điều trị nhiễm khuẳn vùng chậu cẩp (hậu phẫu hoặc viêm nội mạc tử cung sản khoa tự phải;
hoặc phá thai nhiễm trùng) tỉ lệ thảnh công lâm sảng là 100% (23123) đối với ertapenem và 100% (4/4) đối
với đối với ticarcillin/clavưlanate trong một phân tích dựa trên protocoi.
CÁC ĐẶC TÍNH DƯỢC ĐỘNG HỌC
Hấpthu
Thuốc tiêm ertapcnem pha vởỉ dung dịch Líêm lidocain HCl 1% (Dược điến Mỹ) pha trong nước muối
không có epinephrinc, Tẳt dễ hẫp thu sau khi tiêm bắp với iiều khuyến cáo L g. Sinh khả dụng trung bình
khoảng 92%. Sau khi tiêm bắp liếư ] g/ngảy, nồng độ đinh trung bình trong huyết tương (C,…) đạt sau
khoảng 2 giờ (Tmax).
Phân bố
ELtapenem gắn kết nhiến vớiprotein huyết tương. Ở người lớn trẻ tuổi khoẻ mạnh, mức độ gắn kết protein
của ertapenem sẽ giảm khi nông độ trong huyêt tương tăng. Khỉ nông độ huyêt tương <100 mcg/mL thì găm
khoảng 95% nhưng khi nông độ huyêt tưng khoảng 300 mcg/mL thi chỉ găn khoảng 85%.
Bảng 3 sau đây trình bảy nồng độ trung bình trong huyết tương (mcg/mL) của ertapenem sau khi truyền tĩnh
mạch một lần 1ỉều 1 g hoặc 2 g kéo dải 30 phút và tiêm bắp liều duy nhắt 1 g cho người lớn trẻ tuồi khoẻ
mạnh.
BÁNG 3: Nồng độ ertapenem trong huyết tương sau khi tiêm liếư duy nhất
_ Nống độ Lrung bình ưong huyết tương (mcg/mL)
Liêu/ đường dùng
o,s giờ 1 giờ 2 giờ 4 giờ 6 giờ 8 giờ 12 giờ 18 giờ 24 giờ
1 gtruyền tĩnh mạch 155 115 83 48 31 20 9 3 l
1 g tiêm băp 33 53 67 57 40 27 13 4 2
12
0826-VNM—2016—012255
S-WPC—MKOS2õ-IV/IM-O72O l 4
2gtruyểntĩnhmạch| 283 ] 202 ] 145 | 86 [ 58
1_36|16|5|2
* Liều truyền tĩnh mạch với tôc độ hằng định kéo dải ặ30 phút
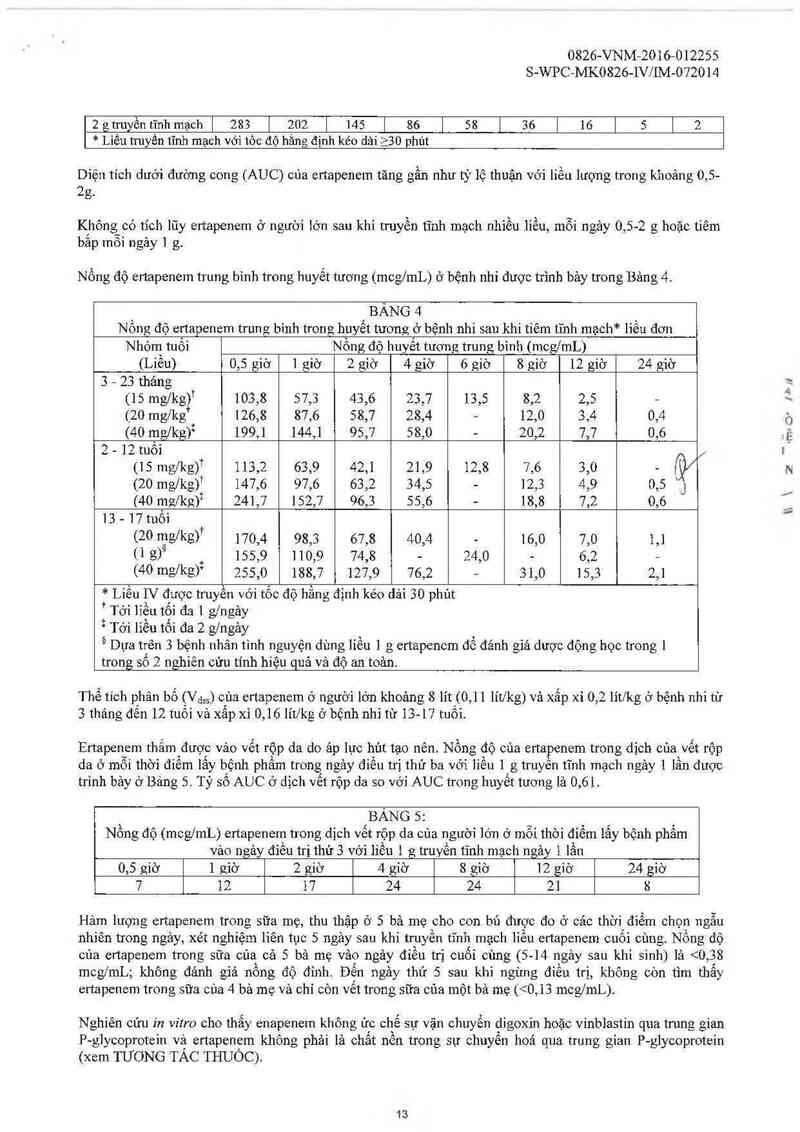
Diện tích dưới đưòng cong (AUC) cùa crtapenc-m tăng gần như tỷ lệ thuận với iiểu Iưọng trong khoảng 0,5-
2g.
Không có tích lũy ertapencm ở ngưòi iớn sau khi truyền tĩnh mạch nhiều liều, mỗi ngảy 0, 5-2 g hoặc tiêm
bắp môi ngảy 1 g.
Nồng độ enapenem trung bỉnh trong huyết tương (mcg/mL) ở bệnh nhi được trình bảy trong Bảng 4.
BANG 4
Nồng độ crtapencm trung bình trong huyết tương ở bệnh nhi sau khi tiêm tĩnh mạch* liều đơn
Nhỏm tuồì Nồng độ huyết tương trung binh (mcgltnL)
(Liều) 0,5 giờ 1 giờ 2 giờ 4 giờ 6 giờ 8 giờ 12 giờ 24 giờ
3— 23 thảng
(15 mglkgỹ 103,8 57,3 43,6 23,7 13,5 8,2 2,5 —
(20 mg/kg 126,8 87,6 58,7 28,4 — 12,0 3,4 0,4
(40 mg/kg)“ 199,1 144,1 95,7 58,0 - 20,2 7,7 0,6
2 - 12 tưôi .
(15 mg/kgỹr 113,2 63,9 42,1 21,9 12,8 7,6 3,0 - ffl/
(20 mg/kgỹ 147,6 97,6 63,2 34,5 - 12,3 4,9 0,5 J
(40 mglkg)I 241,7 152,7 96,3 55,6 - 18,8 7,2 0,6
13—17tuổỉ
(20 mglkg) 170,4 98,3 67,8 40,4 - 160 7,0 1,1
(1 g) _ 155,9 110,9 74,8 - 24,0 - 6,2 -
(40 mgfkgỹ 255, 0 188, 7 127 9 76 2 , 31,0 15,3 2,1
* Liều ĨV được truyền với tốc độ hằng định kéo dải 30 phút
Tới lỉếu tối đa 1 g/ngây
' Tới liều tối đa 2 g/ngảy
Ễ Dựa trên 3 bệnh nhân tình nguyện dùng liếư ] g ertapencm đế đảnh giả dược động học trong 1
trong số 2 nghiên cửu tính hiệu quả và độ an toản.
Thể tích phân bố (V,;,,) của crtapcnern ở người lớn khoảng 8 lít (0 11 lit/kg) vả xấp xỉ 0, 2 lỉt/kg ơ bệnh nhi từ
3 thảng đến 12 tuỏi vả xấp xỉ 0,1611t/kg ơ bộnh nhi từ 13- 17 tuối.
ELtapenem thấm được vảo vết rộp da do’ ap lực hút tạo nên. Nồng độ của e1tapenem trong dịch cùa vết rộp
da ở môi thời điếm lấy bệnh phẩm trong ngảy điều trị thứ ba với liều 1 g truyền tĩnh mạch ngảy ] lần được
trình bảy 0 Bảng 5. Tỷ số AUC ơ địch vết rộp da so với AUC trong huyết tương là 0,61.
BẢNG 5:
Nổng độ (mcg/mL) ertapenem trong dịch vết rộp da cùa người lớn ở mỗi thòi đíểm lắy bệnh phẩm
vảo ngảy điêu trị thứ 3 vởi liêu 1 g truyền tĩnh mạch ngảy 1 lần
0,5 giờ
1 giờ
2 giờ
4 giờ
8 giờ
12 giờ
24 giờ
7
12
17
24
24
21
8
Hảm lượng ertapenem trong sữa mẹ, thu thập ở 5 bả mẹ cho con bú được đo ở cảc thời điếm chọn ngẫu
nhiên trong ngảy, xét nghiệm liên tục 5 ngảy sau khi truyền tĩnh mạch liếư ertapenem cưối cùng. Nồng độ
của ertapenem trong sưa của cả 5 bả mẹ vảo ngảy điều trị cuối cùng (5- 14 ngảy sau khi sỉnh) lả <0 ,38
mcglmL; không đảnh giả nồng độ đỉnh. Đến ngảy thứ 5 sau khi ngùng điều trị, không còn tìm thấy
ertapencm trong sữa cùa 4 bả mẹ vả chi còn vết trong sữa cũa một bà mẹ (<0, 13 mcg/mL).
Nghiên cứu in vitro cho thẫy enapenem không ưc chế sự vận chuyển digoxin hoặc vinblastin qua trungg ơian
P-glycoprotein vả ertapcnem không phải là chắt nền trong sự chuyến hoả qua trung gian P- g-lycoprotcin
(xem TƯONG TÁC THUỐC).
13
Lf’i`LO' Ma
7..
\\
0826-VNM-2016-012255
S-WPC—MKOS2ó-IV/IM-O7ZO ] 4
Chuỵển hoá
Ở người lởn trẻ tuổi khoẻ mạnh sau khi truyền tĩnh mạch 1 g ertapenem đảnh dấu phóng xạ, tinh phóng xạ
trong huyết tương chủ yểu lả cùa ertapenem (94%). Chất chuyến hoá chính của ertapenem lả dẫn xuất có
vòng [3- lactam mở sau khi vòng nảy bị thuỷ phân.
Nghiên cửu in vitro trên microsom tế bảo gan người cho thấy ertapenem không ức chế sự chuyến hoá của
những thuốc qua xúc tác của 6 đồng dạng cytochrom P450 (CYP) chủ yêu là 1A2, 2C9, 2C19,2D6,2E1 vả
3A4 (xem TƯONG TÁC THUỐC)
Đảo thải
Ertapenem đảo thải chứ yếu qua thận. ó người lớn trẻ tuối, khoẻ mạnh và người bệnh từ 13-17 tuổi, thời
gian bản thải trong huyêt tương khoảng 4 giờ và khoảng 2,5 giờ ở bệnh nhi từ 3 thảng đên 12 tuôi.
Sau khi truyền tĩnh mạch ] g ertapenem đảnh dấu phóng xạ, khoảng 80% thải qua nước tiểu, 10% theo phân.
Trong 80% liếu thuốc tìm thấy trong nước tiểu, thì khoảng 38% thuốc ở dạng không đổi và khoảng 37% là
chất chuyến hoá có vòng |3— lactam mở.
Ở người lớn trẻ tuổi khoẻ mạnh truyền tĩnh mạch 1 g, nồng độ trung bình ertapenem trong nước tiểu vượt
quá 984 mcg/mL trong 0-2 giờ sau khi tíêm và vượt quá 52 mcg/mL trong 12-24 giờ sau khi tìêm.
Đăc điếm của người bênh
Giới ƠÌ/
Nong đọ ertapenem/huyet tương khong phụ thuọc gLơL.
N2ười cao tuổi
Nồng độ trong huyết tương sau khi truyền tĩnh mạch ] g và 2 g eưapenem cho người cao tuổi 265 tuối là
khoảng 39% và 22%, cao hơn một chủt so với người lớn trẻ tuổi (<65 tuổi). Không cần điều chỉnh Liều lượng
ở người cao tuổi.
Bênh nhi
Nồng độ huyết tương cùa` enapenem ở bệnh nhi 13-17 tuổi tương đương với người lớn dùng liều 1 g tiêm
truyền tĩnh mạch ngảy ] lân.
Giá trị cảc thông số động học ở bệnh nhi từ 13- 17 tuổi khi dùng liếư 20 mg/kg (tối đa 1 g) nhin chung tương
tự ở người lớn trẻ khỏe mạnh. Ba trong số sáu bệnh nhân từ 13- 17 tuối dùng liều ít hơn 1 g. Để ước tính cảc
dữ liệu dược động học khi tất cả các bệnh nhân trong nhóm tuối nảy đều dùng liều ] g, dữ liệu dược động
học được điều chỉnh theo liều 1 g, với giả định tuyển tính theo liều dùng. So sánh cảc kết quả cho thấy cảc
bệnh nhân từ 13-17 tuổi dùng liều ] g ertapenem ngảy 1 lần đạt được cảc đặc tính dược động tương đương ở
người lớn. Tỷ số (nhóm 13-17 tuổi/ người lởn) của các giá trị AUC là 0,99, nồng độ ngay khi kết thủc tiêm
truyền là 1,20 và nồng độ tại điếm giữa của khoảng cảch cảc liều là 0,84.
Nồng độ huyết tương tại điềm gỉữa cùa khoảng cảch các liều khi tiêm tĩnh mạch ertapenem liếư đơn
15 _mg/kg cho bệnh nhi từ 3 tháng đến 12 tuồi thì tương đương với nồng độ huyết tương tại điềm giữa của
khoảng cảch các lỉều khi tiêm tĩnh mạch liều 1 g ngảy ] lần ở người lớn (xem Phân bố). Độ thanh thải
ertapcnem tại huyết tương (lephủtlkg) ở bệnh nhi từ 3 tháng đến 12 tuốì cao hơn xấp xỉ 2 lần ở người lớn.
Khi dùng liếư 15 mg/kg, giá tn_ AUC (gấp đôi đối với chế độ điều trị 2 lầnlngảy, nghĩa là 30 mg/kg/ngảy) ở
bệnh nhi từ 3 tháng đến 12 tuối thì tương tự giá tn AUC ở người lớn trẻ tuổi khỏe mạnh được truyền tĩnh
mạch liều đơn 1 g ertapenem.
Suv gan , ’
Chưa xảo định dược'động hvọc của ertapcncm ở người suy gan. Do thuôo nảy` ít chuyênhoá qua gan, nên
dộng học cùa thuôo rât có thế không bị ảnh hưởng khi suy gan. Vì vậy, không cân chỉnh liêu khi suy gan.
Suỵ thân
14
\\ 'Ax—
O826-VNM-2016-012255
S-WPC-MKOSZõ-IV/IM-O7ZO 1 4
Sau khi truyền tĩnh mạch một liều đơn 1 g ở người 1ớn,AUC ở người suy thận nhẹ (độ thanh lọc creatinin từ
60—90 mL/phút/l, 73 m 2) tương đương vởi AUC ở người khoẻ mạnh (25- 82 tuổi). Nhưng ở người suy thận
vùa (độ thanh lọc creatinin từ 31- 59 mL/phut/ 173 m ), AUC tãng khoảng 1, 5 lần so vởi ở người khoẻ mạnh.
Ở người suy thận tiến triển (độ thanh lọc creatinin từ 5— 30 mL/phut/ 173 m ), AUC tăng khoảng 2, 6 lần so
vởi người khoẻ mạnh. Ở người suy thận giai đoạn cuối (độ thanh lọc creatinin <10 mL/phut/ 173 m ), AUC
tăng khoảng 2, 9 lần so vởi ở nguời khoẻ mạnh. Sau khi truyền tĩnh mạch một liều ] g ngay trước khi thẩm
phân mảu, khoảng 30% liều dùng được tìm thấy trong dịch thẫm phân. Không có dữ lĩệu ở bệnh nhi bị suy
thận.
Cần chinh liều ertapenem ở người lớn bị suy thận tiến triển hoặc ở gỉai đoạn cuối (xem LIÊU LƯỢNG VÀ
CÁCH DÙNG).
QUÁ LIÊU
Không có thông tin đặc biệt về điều trị quá liều INVANZ. Hầu như không có trường hợp cố tình dùng quá
lìều INVANZ. Không thấy có độc tính đảng kể trên người tình nguyện trưởng thảnh khỏe mạnh tiêm tĩnh
mạch mỗi ngảy 3 g INVANZ, dùng trong 8 ngảy. Trong nghỉên cứu lâm sảng ở người lớn, vô tình dùng mỗi
ngảy tới 3 g không gây phản ửng quan trọng trong lâm sảng. Trong các nghiên cứu lâm sảng ở trẻ em, tiêm
tĩnh mạch một liều đơn 40 mglkg đến liều tối đa là 2 g cũng không gây độc tính.
Nếu sử dụng quá liều, cằn ngừng INVANZ và điều trị hỗ trợ chung tới khi thuốc đảo thải được qua thận. ) ,
Có thế thải INYANZ nhờ thẩm phân mảu; tuy nhiên, chưa có thông tin về sử dụng thẩm phân máu để điềíỂ
trị quả liêu thuôo nảy.
DẠNG TRÌNH BÀY
INVANZ được cung ứng dưới dạng bột đông khô vô khuẩn dùng để pha truyền tĩnh mạch hoặc tiêm bắp,
mỗi lọ chứa 1 g ertapenem gốc acid tư do. Mỗi hộp chứa một lọ.
BẢO QUẢN ỔỀ/
Trước khi hoản nguyên
Bảo quản ở Việt Nam ở nhiệt độ 2-8°C.
Dung địch đã hoân nguyên để truyền
Sau khi hoản nguyên, pha loãng ngay dung dịch thuốc với dung dịch tiêm NaCl 0,9% (xem LIÊU LƯỢNG
VÀ CÁCH DÙNG, HƯỚNG DÃN SỬ DỤNG), và có thế sử dụng trong vòng 6 giờ khi bảo quản ở nhiệt độ
phòng (25°C) hoặc bảo quản 24 giờ trong tủ lạnh ở nhiệt độ 5°C và dùng trong vòng 4 giờ sau khi lấy ra khỏi
tủ lạnh. Không được lảm đông đã dung dịch INVANZ.
HẠN DÙNG
24 thảng kế từ ngảy sản xuất.
Đọc KỸ LiUÓNG DẨL_~L SỬ DỤNG TRƯỚC KHI DÙNG
ĐE XA TAM TAY TRE EM.
Sãn xuất tại Merck Sharp & Dohme- Chibret
“ NG
R t đ M rs t Ri F-63963,C1ermont-Ferrand Cedex9,France TRUƠ
ou e e a a, om, (lễhặầc ỤNGPHÒNG
Đóng góitại ./1fauyền líùợ Ífiìng
PT Merck Sharp Dohme Pharma Tbk.,
Jl. Raya Pandaan Km 48, Pandaan, Pasuruan, Jawa Timur, Indonesia
15
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng