















ĐÃPHÊ
Lân đẩusz …..
BỘ Y TẾ
CỤC QUẢN LÝ DƯỢC
DUYỆT
…..…..J…ửủỉ
I4I IIỈÌII \\
\_———unỂ
lllnm'lllniũwllmffl
ulllĩffl
…qwmmm
fflẵ
'“Ưư
. b.mumè
ẹnnuamr
i Janssen7
i
IMMMWWI
W
nr.
JMũq SM. … c. J….
Bup & … mon LỦI MIIHIIHO
Út-lỉiand'-MCMS~IDũS
Ở lNTELENCE'
® compfimb orlux
Etravirinezoomg
parcompởné
Liudmi'mtnlnnelim
thnmw-d-nncm'c.
…mnumcm
ũllhbmhmllthtthmi
dhdthđoIW
IhIIUIDIHIWH_WH
HlùhulủllpơlndnmhrỤ
DU WD'AGCẺB
i
A… mv…
cmmnvntntncum
~'J INTELENCF
® onl hbloh
Ettavirine²ơJ mg
pertnblet
Fơ6lncmbrm
m……cwm
Dondmmffl’lì.
Mhthncwm
Kluhhulowwmnm
upmmmdm.
Dommnumpum,
Kandrnchdctủm.
FOR mm… Il …
OWNTB ULV
i
Ụ(
|
"1INTELENCE'
h , mừ mu bn
masuce“
MM
m…mm u Iu
cunmummhmỤnnekuqn
#… nnmmncmnin
IAYAITAVMH ưc
luutơơúlmed nincmimgu
ẫ__augaùndmh Munưu
- n-n n
mmmcmu tm’zm
muhni mulluutuu vuc …
tums…ị mmmULv
SAesl,tu.ttmhúm llnmEơ’ymu
ẵTIuắiunuunmotu'nnmú—i
sa_ … _mm :
SP_Intetence_ĩab 200mg_v2
| SENSI DI SVOLGIMENTO
— IN uso PRESSO
ị LA CARLUCCI SPA
. f'Tv _ 4
1 `1INTELENCEo
Ễễ @
ỉf UMllủgdzgzlphldĩlỉnhurnclđnonl
Etmvirlnc 200 mg per tablot
Ettava zoo mg por comprlmido
Etmirlnc 200 mg par oomprtmó
".ắ'ă
»…
…
10…
:Ợ
_mM
ẵ
i
l
s
ẵ
ễ
PP_lntelence_Tab 200mg_v2
iNTELENCE®
Thuốc nảy chỉ dùng theo đơn của bác sỹ.
Dọc kỹ hướng dẫn sử dụng trước khi dùng.
Nếu cần thêm thông tin xin hỏi ý kiến bác sỹ.
THÀNH PHẦN
Viên nén IN'I`ELENCE 200 mg: mỗi vỉên chứa 200 mg ctravirìn.
Viên nén iN'I`ELENCF. IOO mg: mỗi viên chứa i00 mg etravirin.
l`á dược:
lntclence 200 mg: hypromcllosc, ccllulosc vi tinh thể thấm silic dioxyd, ccllulose vi tinh
thế, silica dạng kco khan, natri croscarmciiosc, magnesi stearat.
lntclcncc 100 mg: hypromcllosc, ccllulosc vi tinh thể, silica dạng keo khan, natri
croscarmciiosc magnesi stcarat, lactose monohydrat.
Ciii DỊNII
Người lớn
IN i` El ENCE phối hợp với cảc thuốc khảng rctrovirus khác để điều trị virus gậy suy giảm
miễn dịch ở người týp ! (IilV- I) cho những bệnh nhân người lớn dã từng điều trị khảng
rctrovirus bao gôm các bệnh nhân xuât hiện dễ kháng với ít nhất một NNRTI (thuốc ức
chế mcn sao chép ngược không nucleosid) và kháng ít nhất với một rctrovirus khác.
Chỉ dịn__h nảy được dựa trên cảc phân tích kết quả ở tuần 48 cùa 2 thử nghiệm pha Hi mù
dôi ngẫu nhỉên, có dối _chứng với giả dược trên những bệnh nhân dã khảng thuốc NNRT I
(qua sảng iọc vả/hoặc hồi cưu) và kháng với thuốc ức chế mcn protcasc (Pi), trong đó tỷ iệ
bệnh nhân có tải lượng virus đạt dưới mức phải hiện dược (< 50 phiên bản HIV l
RNA/mi ) và số lượng tế bảo CD4 tăn so với ban dầu cao hơn có ý nghĩa thống kê ở
nhóm bộnh nhân u_ông IN' l` ELLENCE ket hợp với chế độ đỉều trị cơ bản (BR) so với nhóm
bênh nhân dùng giả dược kết hợp vởỉ chế dộ điều trị cơ bản (BR) (xem Đậc tính dược lực
học).
'lất cả cảc bệnh nhân
Cần có hướng dẫn sử dụng lN1EI ENCE dựa vảo tiền sử diễu trị và xét nghiệm khảng
thuốc nểu có. Khuyến cáo không dùng phối hợp lNTELENCE chi với N(t)RI`I ở những
bệnh nhân dã thất bại virus học với phác dỗ điều trị có chứa thuốc ửc chế mcn sao chép
ngược không nucleosid (NNR'H) vả thuốc ức chế mcn sao chép ngược nucleosid hoặc
nucleotid (N[tJRT [).
LIÉU DÙNG VÀ CẢCII DÙNG
INTELENCE iuôn Iuôn phải dược dùng phối hợp với các thuốc kháng rctrovirus khác.
Người lớn
I ỉêu IN' l`ìl [ l` N_CE khuyến cáo cho người lớn là mỗi lấn 200 mg (! viên 200 mg hoặc 2
viên IOO mg), uống 2 iần/ngảy, sau bữa ăn (xem Dặc lính dược động học).
Các đối tượng đặc biệt
Người cao tuổi
'l`hông tin vẫn còn hạn chế cho dối tượng nảy (xem Thông lin lăm sảng — Canh bảo và lhận
lrọng vù Dặc lính dược động học).
Page I of 24
l’l Inlefenư lí)llmỵ .’fNImg (Y'I)X IlUimJU/5 vl
Phụ nữ có thai
Không dòĩ hói phải diều chinh tiều cho p_hụ nữ dang mang thai vả sau khi sinh Do phơi
nhiễm với ctravirin tăng khi mang thai, cân thận trọng ở những bệnh nhân mang thai cẩn
dùng các thuốc dồng thời hoặc có các rối ioạn có thế iảm tãng khả năng phơi nhiễm với
ctravirin
S uy thân
Không yêu câu phải dỉều chinh liều cho các bệnh nhân suy thận (xem ]hông tin lảm xảng—
( ánh báo và [hận trọng và Dặc lính dược động học).
Suy gan
Không yêu cẩu phải đỉồu chinh liều cho các bệnh nhân có suy gan nhẹ hoặc trung binh
(Chĩld-Pugh mức A hoặc B). Chưa có nghiên cứu dược động học cùa ĨNTELENCE ở
những bệnh nhân suy gan nặng (ChiId-Pugh mức C) (xem Thông tin lâm sảng — Cảnh băo
và thận lrọng vả Dặc tính dược động học)
Quên không aống thuốc
Nếu bộnh nhân quê_n không uống một liồu INT ELENCẸ trong vòng 6 gỉờ so vởi thời gian
dã dịnh thi phải uỏng lN'ILL ENCF cảng sởm cảng tốt sau bữa ăn và sau dó uống liếu
IN' I`ít LENCE tiếp theo dùng như thòi gian trong lịch dùng thuốc dã dịnh. Nếu bệnh nhân
quên không uống một lỉếu iN'l`ELENCE quá 6 giờ so với thời gian dã dịnh, thì bệnh nhân
không cẩn phải uống bù liều dã quẻn và chỉ uống thuốc theo iịch uống thuốc đã định.
Cảch dùng
Bệnh nhân nôn được hướng dẫn uống cả viên thuốc TNTELENCE với một chất lỏng như
nước. Những bệnh nhân không thế nuốt cả viên thuốc thì có thể phân lán thuốc vâo một
cốc nước. Huởng dẫn bệnh nhân Iảm theo các bưóc sau:
«› thả viên thuốc vảo 5 mL nước (1 thìa cả phê), hoặc ít nhất phải đủ để nước ngập
viên thuốc,
* khuấy dếu dễn khi nuớc trông giống như sũa,
ơ nêu muốn, thêm một ít nuớc hoặc thay bằng nuớc cam hoặc sữa (bệnh nhân không
nôn thả thuoc vảo nước cam hoặc sủa trước khi thả thuốc vảo nuớc),
o uống th_uốc nga_y,
o tráng cốc vải lần với nuớc, nước cam, hoặc sũa và uống hết sau mỗi lần tráng đế
dảm bảo bệnh nhân dã uống hết thuố_c.
Iránh sư dụng nuớc ấm (> 40°C) hoặc dỗ uống có ga.
CIIÓNG cui DỊNII
Mẫn cảm vói ctravỉrin hoặc với bất kỳ tả dược nảo cùa thuốc.
CÁNH nẨơ VÀ 'I`IIẶN TRỌNG
Bộnh nhân cẩn phải dưọc thông báo là liệu phảp khảng retrovirus hiện hảnh không chũa
khòỉ đuợc [HV và không thể _ngăn ngùa đuợc sụ lan truyền I-IIV cho ngươi khác qua đuờng
máu hoặc dường tinh dục. Cần tiếp tục thục hỉện cảc biện phảp phòng ngừa thích hợp.
Nhũng nghiên cứu iâm sảng trên lrẻ cm dưới 6 tuổi nhỉễm I-IIV-l dang dược thực hiện.
Phân ứng mẫn cảm và nhãn ủng da nghiêm trong
Ghi nhận các phản ủng da nghiêm trọng, có thổ do dọa tính mạng vả gây tử vong khi dùng
iN"ẺIiIENCE; hội chứng Stcvcns-Johnson hoại tử biều bì do nhiễm độc hiểm xảy ra
(< 0,1%) Ghi nhận cảc phản úng quá mẫn bao gồm hội chúng DRESS (phảt ban kòm tăng
bạch câu ua cosin vả cảc triệu chửng toản thân) đuọc mô tả như phát ban, cảc dấu hiệu thế
Page 2 uf 24
P! Inlelenre IUlnng .?lfflmg f'(`.`DS 10.11m20/5 v!
’ì
tạng, và rối loạn chức năng cơ quan hiếm gặp, bao gồm suy gan (xem Thỏng tin lâm sảng—
7'ác dụng khỏng mong muôn).
Ngừng sử dụng INTELENCE ngay khi có các dấu hỉệu hoặc triệu chứng cùa phản ứng da
nghiêm trọng hoặc xuất hiện cảc phản ửng quả mẫn (bao gốm nhưng không giới hạn như
phát ban nặng hoặc phát ban kèm theo sốt, khó chịu, mệt mòi, dau cơ hoặc khớp, bòng rộp,
tốn thương miệng, vỉêm kết mạc, viêm gan, tăng bạch cầu ưa cosin). Nên theo dõi tình
trạng lâm sảng bao gồm mcn gan và bắt đầu liệu pháp diếu trị thích hợp Việc trì hoãn
ngừng dìều trị bằng iNTEI t`NCE sau khi bị phảt ban nặng có thể dẫn dến một phản ứng
dc dọa tính mạng.
Phát ban
Phát ban khi dùng INT ELlỉ NClỉ dã dược bảo cảo. Hầu hết thường gặp phát ban ở mức độ
nhẹ tới trung binh, xảy ra trong tuẫn thứ 2 của trị liệu và không thường gặp sau tuần 4.
Phảt ban hầu hết tự giới hạn vả hồi phục hoản toản trong vòng 1 đến 2 tuần khi tiếp tục
diều trị. l`ỷ lệ phảt ban cao hơn ở nữ giới (xem Thông lin lảm sảng— Tác dụng khóng
mong muốn).
Người cao tuổi ,
Kỉnh nghỉệm trôn những ngưòi cao tuổi còn hạn chê: trong các thử nghiệm pha 3, 6 bệnh
nhân từ 65 tuối trở Iôn và 53 bệnh nhân ở dộ tuổi 56-64 tuối dùng INTELENCE. Loại và tỷ
lệ các biến cố bất lợi ở những bệnh nhân trên ss tuổi là tương dương với những bệnh nhân
trẻ hon (xem Thông Iin lán: sảng — Tác dụng khỏng mong muốn và Đặc lính dược động
học).
Bệnh nhân có các bệnh khác kèm theo
Bệnh gan
Không yêu cầu diểu chinh liều lượng ở những bệnh nhặn suy gan nhẹ hoặc trung binh
(Child-Pugh mức A hoặc B). Chưa có nghiên cứu dược dộng học cùa INTELENCE ở
những bệnh nhân suy gan nặng (Chỉld-Pugh mức C) (xem T hỏng Iin Iảm sảng — Liều dùng
vả cảch dùng và Dặc lính dược động học).
Bệnh lhận
t)ộ thanh lọc qua thặn cùa etravirin lá không dáng kể (< 1,2%), nên không nhận thấy giảm
dộ thanh lọc cùa toản bộ cơ thể ở bộnh nhân suy thặn. Không cần thận trọng đặc biệt hoặc
diễu chinh liếư đối vởi bệnh nhân suy thận Vì ctravirin gắn chặt vảo protein huyết tương
nên không chắc thuốc nảy dược Ioạỉ khỏi cơ thể bằng lọc mảu hoặc thấm phân phủc mạc
(xcm Thỏng Iin lâm sảng— Liều dùng và cách dùng và Dặc lính dược động học).
Tái phân bố mỡ
! iệu pháp khảng rctrovirus phối họp (CAR' t“) liên quan với tải phân bố mỡ cùa cơ thể
(lipodystrophy) ở nhũng bệnh nhân nhiễm HIV. Hậu quả lâu dải cùa cảc hiện tuợng nảy
hiện chưa rõ. lliếu biết về cơ chế còn chưa dẳy đù. Sự liên quan giữa bệnh u mỡ nội tạng
vả thuốc ức chế mcn protcasc (Pls) và hiện tượng teo mỡ và thuốc ức chế sao chép ngược
nucleosid (NR [` !) chi lả giả thuyết. Nguy cơ cao về loạn dưỡng mỡ lìén quan đến cảc yêu
tố cá thế như tuối giả và cảc yêu tô liên quan đến thuốc như thời gian điều trị kháng
rctrovírus dải hơn và các rối loạn chuyến hóa liên quan. Khám lâm sảng cân bao gốm dánh
giả các dấu hìệu thực thế về tái phân bố mỡ (xem Thóng lin lâm sảng— Tác dụng không
mong muốn)
Hội chủng phục hồi miễn dịch
0 bệnh nhân nhiễm IIIV có suy giảm miễn dịch nghiêm trọng vảo thời diếm dùng liệu
phản (CAR' i ), dảp t'mg viêm dối với các mầm bệnh cơ hội không triệu chứng hoặc còn tồn
Page 3 of 24
1²! lnlelenư IUUmg 200mg (`(“DS IOJunJỦ/j vl
dư có thể gia tảng hoặc gây nên tinh trạng lâm sảng nghỉêm trỌng, hoặc iảm nặng lên các
triệu chứng. Diễn hinh, những phản ứng như vậy thấy được trong tuấn đầu hoặc thảng dầu
khi khỏi dầu liệu pháp CAR'Ii Cảo ví dụ liên quan lả viêm vỏng mạc do vi rủt cụ bảo,
nhỉễm khuấn lao cục bộ vả/ hoặc toản thân vả viêm phổi do Pneumocyalisjt'roveci. Bất kỳ
trỉệu chúng viêm nảo cũng cằn duợc dảnh giả và diều trị khi cần thiết. Cảo rối loạn tụ mỉễn
như bệnh (]ravcs duợc báo cáo xảy ra trong phục hồi miễn dịch; tuy nhiên, thời gian khời
phát biến dối, vả có thể xảy ra nhiều tháng sau khi khởi đằu đỉổu trị (xem Thóng tín lâm
sang Tác dụng khỏng mong muốn).
"lương tác vởí các thuốc khác
l`hông tin về tuong tảc thuốc dược xem Thóng tin lám sảng Tương tác vót cảc lhuốc khác
và cảc ỉoại lmmg rác khác.
TƯONG TÁC VỚI CẢC TIIUỐC KHÁC VÀ CÁC LOẠI TƯỜNG TÁC KHÁC
Câc thuốc ảnh hưởng đễn nồng độ etravirỉn
Etravirin dược chuyến hóa bằng cytochrom P450 (CYP) 3A, CYP2C9 vả CYP2CI9 sau dó
dược glucoronat hóa bởi men vận chuyến uridín diphosphat glucuronosyl transferasc
(UDPGT). Cảo thuốc gây cảm ứng CYP3A, CYP2C9, hoặc CYP2C]9 có thế lảm tãng độ
thanh thải của ctravirin, dẫn dến lảm giảm nồng độ của ctravirin huyết tương. Việc dùng
phối hợp INTELENCE với các thuốc ửc chế CYP3A, CYP2C9, hoặc CYP2C19 có thế
giảm độ thanh thải cưa ctravirin vả lảm tăng nồng độ của etravirin trong huyết tương.
_’I_`fflJjngPt_ảc thuốc … Dùng phối hợp ctravirin với các thuốc khảng retrovỉrus
Liên của ' _ _
' thuõc phôi Thuỏc được
Thuỏc phối họp hợp (mg) đánh giá AUC Cm;n
'lhuốc ức chế men sao chép ngược không nucleosid (NNRTI)
NNRTI (ví dụ cfavircnz, Khuyến cảo không dùng phối hợp INTELENCE với cảc
ncvirapin, dclavirdin, NNRTI.
rilpivirin)
Thuốc ức chế mcn sao chég_ngược nucleosid hoặc nucleotid (NRTIs/NItIRTI)
` [)idanosin 400 q.d. didanosin 4—› ND
__ etravirin H …
Có thế dùng phối họp lN'l` ELENCE vả dỉdanosin mả không
cần hiệu chính lỉều. Vì didanosin được chi dịnh uống túc dói,
nên dùng didanosin một giờ trước hoặc hai gỉờ sau khi dùng
tN'i`ELI'ỉNCE vi INTELENCE được chỉ định uống sau ãn).
'I`cnofovir đisoproxi] 300 q.d. tenofovir <—› } ĩ19%
fumarat
ctravirin 119% 118%
Có thê dùng phối hợp IN I ELENCE vả tcnofovir disoproxi]
fumarat mã không cân hỉệu chinh liếư.
` Các NR'I`I kiẵ’c Do cảc thuốc NR l“I nây (ví dụ: abacavir, cmtricitabin,
tamivudin, stavudin vả zidovudin) thặi trừ chủ yếu qua thận,
nên không có tương tác gỉữa các thuôo nảy vả tNTELENCE.
q.d.: l lần/ngảy
ND: khõng xảo dịnh
Các thuốc bị ãnh huỏng do dùng ofetravirin
tỉtravirin lá thuốc gây cảm ứng yêu với CYP3A. Dùng phối họp cùa INTELENCE với các
thuốc dược chuyền hóa dẫu tiên bởi CYP3A có thề tảm giảm nồng độ của các thuốc đó
lrong huyết tuơng, do dót âm giảm hoặc rút ngắn hìệu quả diểu trị cùa thuốc Etravỉrỉn lả
Page 4 of 24
Pi lnlclence l(lllmg_2ớflmg CCDS I tUun2tJlĩ_vl
'A !
\`..
thuốc có tinh ủc chế yếu đối vói CYP2C9 vả CY 1’2C19. Etravirin cũng ức chế yếu đối với
P-glycoprotcin khi không lả co chất. Dùng phối hợp với các thuốc bị chuyến hóa đầu tiên
bời CYP2C9 hoặc CYP2CI9 hoặc dược vận chuyền bởi P-giycoproteìn có thế lảm tăng
nồng độ cùa các thuốc nảy trong huyết tuơng, do đó có thể lảm tăng hoặc kéo dải hiệu quả
điều trị hoặc cảc phản ứng phụ của thuốc
Cảc tương tảc dã biết hoặc trên lý thuyết vởi cảc thuốc khảng rctrovirus vả với các thuốc
không khảng retrovirus chọn lọc dược liệt kê trong bảng dưới dây.
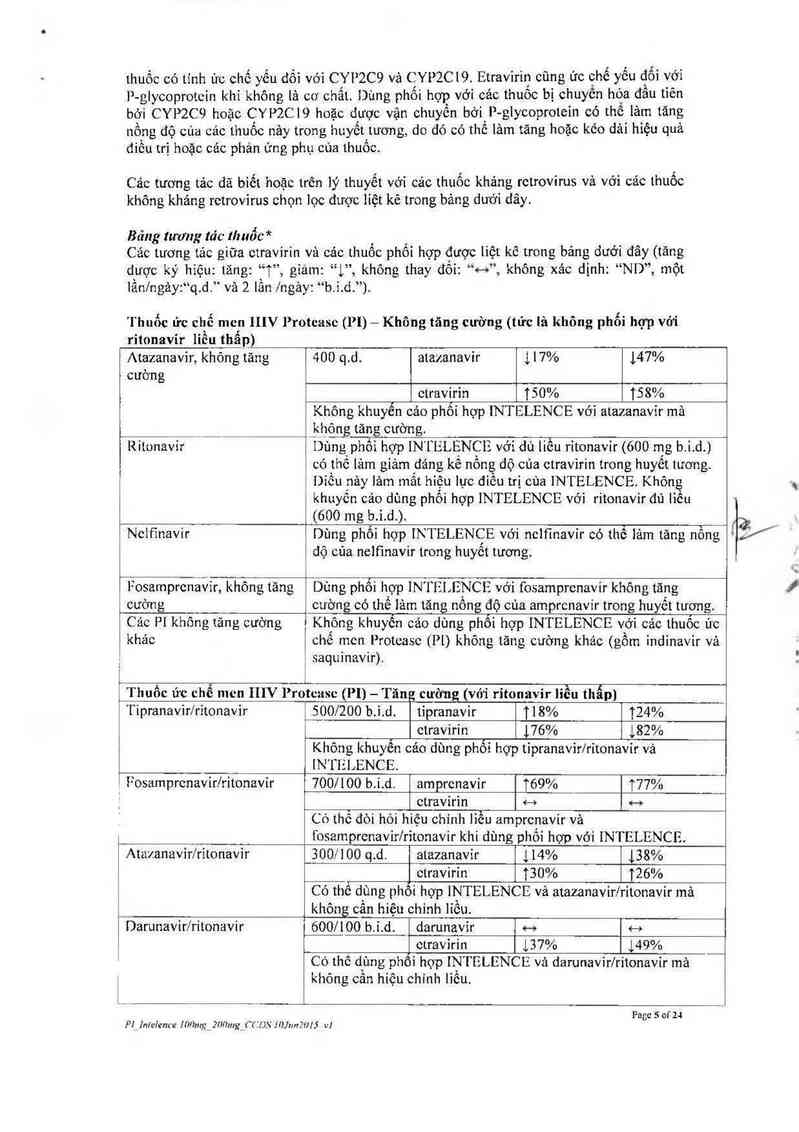
Bảng tương ta'c thuốc *
Các tuơng tảc giữa ctravirin và các thuốc phối hợp được liệt kê trong bảng dưới đây (tăng
duợc ký hiệu: tăng: “”,T giám: “1”, không thay đổi: ~“ .không xảc dịnh: “ND”, một
lần/ngây:“q.d." và 2 lần |ngảy: “b.ỉ.d.”).
Thuốc ức chế mcn IIIV l’rotease (PI) — Không tăng cường (tức là không phổi hợp với
ritonavir liêu thâp)
Atazanavỉr, không tăng 400 q.d. atazanavỉr 117% 147%
cường
ctravirin 150% TS 8%
Không khuyến cáo phối hợp iNTELENCE với atazanavir mã
không tăng cường.
Ritonavir Dùng phối hợp IN' [ IìLENCIE vởỉ dù liều ritonavir (600 mg b. 1. d. )
có thể 1ảm giảm dáng kể nồng dộ cúa ctravirin trong huyết tương.
Diều nảy lâm mât hiệu lực điều trị cùa INTELFNCF. Không
khuyến cảo dùng phối hợp INTELENCE với ritonavir đú Iiồu
(600 mg b i. d ).
Ncifinavir Dùng phối họp 1N1 ELENCE với ncifinavỉr có thẻ Iảm tăng nồng
dộ cúa nelfinavir trong huyỗt tương.
Fosamprcnáiìỉr, khỏng tăng Dùng phối họp IN I`Iì I ENCE với fosamprcnavir không tăng
cường cu ờng có thề 1ảm tăng nổng độ của amprcnavir trong huyết tu ơng.
Các PI không tăng cường Không khuyên cáo dùng phổi hợp IN' I`ELENCE vởi các thuốc úc
khảo chế mcn Protcasc (Pi) không tăng cường khác (gồm indinavir vả
| saquinavir).
L
Thuốc ức chế men IIIV l’rotcase (l’l) — Tăng cường (với ritonavir liều thẩp)
Tipranavir/rỉtonavỉr ' 500/200 b.ỉ.d. tipranavir 118% 124%
ctravirin 176% 182%
Không khuyến cảo dùng phôi hợp tỉpranavir/ritonavỉr vả
INTELENCE.
Fosamprcnavirlritonavir 700/100 b.ỉ.d. amprcnavỉr T69% T77%
) ctravirìn <-› …
Có thể đòi hỏi hiệu chỉnh liễu amprcnavir và
I fosamprcnavir/rìtonavir khi dùng phôi hợp vỏi INTELENCE.
Atazanavirlritonavỉr 300/100 q.d. atazanavir 114% 138%
ctravirỉn ĩ30% T26%
Có thế d_ùng phôi hợp INTELENCE vả atazanavir/ritonavir mả.
không cân hiệu chỉnh lỉêu.
Darunavir/ritonavir 600/100 b.ỉ.d. darunavĩr o-› +-›
ctravirin 137% 149%
1 Có thế dùng phôi họp 1N' I`ELENCE vả darunavir/ritonavỉr mả
khõng cân hiệu chỉnh liều.
Page 5 of 24
Pl Jm'eỈerưe' Hllhng_ .?Hflmgj'fClJS IOJun2Fl/5 vl
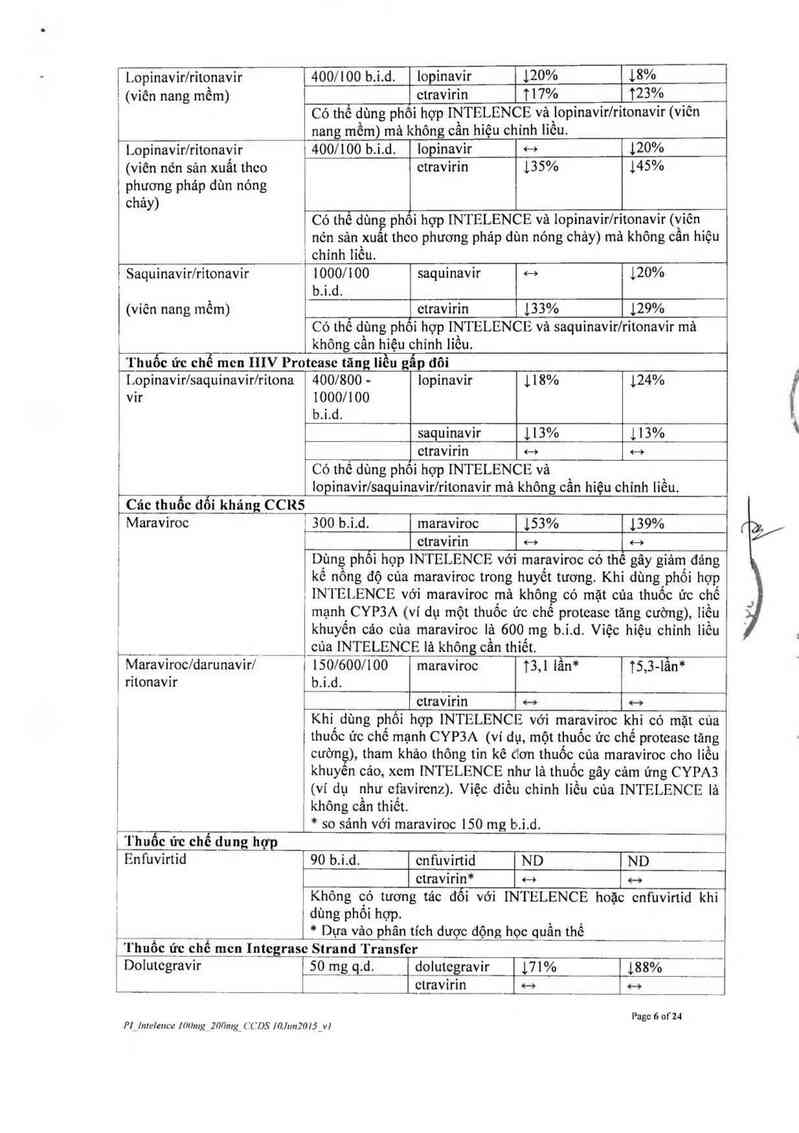
(viên nang mềm)
Lopinavir/ritonavir
400/100 b.ỉ.d. Iopìnavỉr 120% 18%
etravirin T 17% 123%
Có thể dùng phôi hợp TNTELENCE vả lopinavỉr/ritonavir (viên
nang mềm) mã không cần hiệu chỉnh liều.
Lopinavir/ritonavir
400/100 b.“ !. d. lopinavir <—› 120%
(viên nẻn sản xuất theo
phương phảp dùn nóng
chảy)
ctravirin 135% 145%
Có thể dùng phôi hợp INTELENCE vả lopinavir/ritonavir (viên
nén sản xuất theo phương phảp dùn nóng ehảy) mà không cần hiệu
' chinh liồu.
Saquinavir/ritonavir 1000/100 saquinavir <—+ 120%
' b.ỉ.d.
(viên nang mồm) ctravirin 133% 129%
Có thế d`ùng phôi hợp INTELENCE vả saquinavir/ritonavir mã
không cân hiệu chỉnh lỉồu.
Thuốc ức ehế men IIIV Pro
tease tăng liều gấp đôi
I.opinavirlsaquinavir/ritona
vir
400/800 - lopinavir 118% 124%
1000/100
b.ỉ.d.
saquinavir 113% 113%
etravirin «» H
Có thể dùng phôi hợp INTELENCE vả
lopinavir/saquinavir/ritonavir mã không cần hiệu chinh liều.
Các thuốc dối kháng ccns
Maraviroc
j aoo b.ỉ.d. maraviroc 153% 139%
H 4—›
etravirin
Dùng phối họp lNTELENCE vởi maravìroc có thẻ gây giảm đáng
kể nông độ của maraviroe trong huyết tương. Khi dùng phối hợp
. 1N1 FLENCE với maraviroe mã không có mặt của thuốc ức chế
mạnh CYP3A (ví dụ một thuốc ức chế protease tãng cường), liều
khuyến cáo của maravỉroc là 600 mg b.' 1. d. Việc hìệu chinh liều
cùạ_ lNTELENCE lá không cần thiết.
Maraviroc/darưnavir/ 1 lSO/óOOI 100 maraviroc T3, ] lẩn* TS,3-iẳn*
ritonavir b. 1. d.
etravirin ~—› e—o
Khi dùng phối hợp lNTELENCE với maraviroc khi có mặt của
thuốc ức chế mạnh CYP3A (ví dụ, một thuốc ức ehể protease tãng
› cường), tham khảo thông tin kê đơn thuốc của maraviroe cho liều
khuyên cảo, xem INTELENCE như lá thuốc gây cảm ứng CYPA3
(ví dụ như efavirenz). Vìệc điều chinh liều eủa INTELENCE lả
' không cần thiết.
1 * so sánh với maraviroc 150 mg b.ỉ.d.
, Thuốc ức chế dung hợp
11 Enfuvirtid 90 b.ỉ.d. enfuvirtid ND ND
etravirin* 4-> H
1 Không có tương tác đổi với INTELENCE hoặc enfuvìrtid khi
1 dùng phối hợp.
1 * Dựa vảo phân tích dược động học quần thể
Ị'l lhuốc ức chế mcn Intgg_r3se Strand T ransfer _ `—
1Dolutegravir _ặ_0___mg q. d. dolutegravir 171% 188%
__ _ etravirin o-› …
PagcỏofN
PI hneleure IOUmg 200mg (.'CDS l0Jun2
0l5_vl
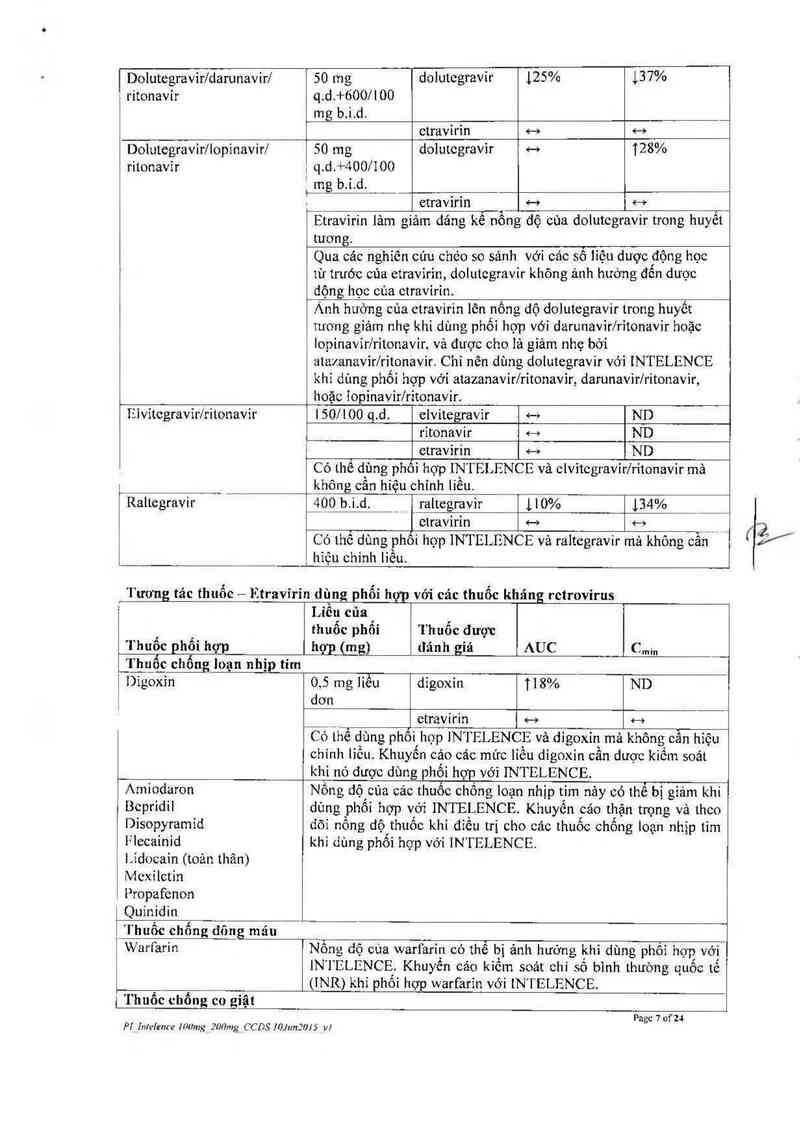
Dolotegravirldarunavirl 50 mg dolutegravir 125% 137%
ritonavir q.d.+6001100
mg b.ỉ.d.
etravírìn e—› e—›
Dolotegravir/lopìnavir/ 50 mg dolutegravir <-› 128%
ritonavir . q.d.+400l100
'ịng b.ỉ.d.
' etravìrin <—› <—+
Etravirin lầm giảm đảng kế nỗng độ cùa dolutegravir trong huyết
tương.
Qua các nghiên cúu chéo so sảnh với eáe sỗ iiệu dược động học
tù truớc cùa etravirin, dolutegravir không ảnh hưởng đến dược
dộng học eùa etravirỉn.
Anh hưởng của etravirin lẻn nống dộ dolutegravir trong huyết
tương giảm nhẹ khi dùng phối họp với darunavìr/ritonavir hoặc
lopinavirfritonavir. vả được cho 1ả giảm nhẹ bởi
atazanavir/ritonavir. Chi nẻn dùng dolutegravir với INTELENCE
khi dùng phổi hợp với atazanavir/ritonavir, darunavir/ritonavir,
hoặc Iopinavir/ritonavir.
Iỉlvitegravir/ritonavir
1501100 q.d. elvitegravir <—› ND
ritonavir «—› ND
etravirin … ND
Có thể dùng phôi hỌp IN I El. FNCE vả etvỉtcgravir/ritonavir mã
không cân hiệu chinh liều
Raltcgravir
110%
H
_400 b.ỉ.d. raltegravỉr
etravirin
C ó thể dùng phôi hợp INTELENCE vả raltegravir mà không cẫh
hiệu ehinh liều
134vs
1—>
Tương tác thuốc — Etravỉrin dùng` phối hợp với eác thuốc khán retrovirus
Liều của
thuốc phối Thuốc được
1muốcphốinợp hợp(mg) aánhgm ALKI c,,in __
Thuốc chống loạn nhịp tim
Digoxin 0,5 mg liều digoxin 118% ND
dơn
etravirin o—› 4-9
Có thể dùng phôi hợp IN I` FLENCE vả digoxin mả không Cần hiệu
ehinh tiổu. Khuyến cản eảc mức liêu digoxin cẳn dược kiếm soát
khi nó được dùng phối họp với INT ELENCE.
Amindaron
Bepridil
Disopyramid
I²1ecainid
Lidoc-ain (toản thân)
Mexi lctin
Propafenon
Quinid in
Nông dộ cùa các thuốc ehống ioạn nhịp tỉm nảy có thể bị giảm khi
dùng phối hợp vởi INTELENCE. Khuyến eảo thặn trọng và theo
dỏỉ nông dộ thuốc khi đỉều trị eho các thuốc chống loạn nhịp tìm
khi dùng phối hợp với IN T FLENCE.
Thuốc chống dõng mảu
Warfarin
Nồng dộ eùa warfarin có thể bị ảnh hướng khi dùng phối hợp vởi
INI`ELENCE. Khuyển cáo kìếm soát ehi số bình thường quôe tế
(INR) khi phối hợp warfarin với tN' I` ELENCE.
1 Thuốc chống co giật
Page 7 of24
Pỉ_lnlelence lflOmg 200mg C CDS IOJJmỆOIJ' vi
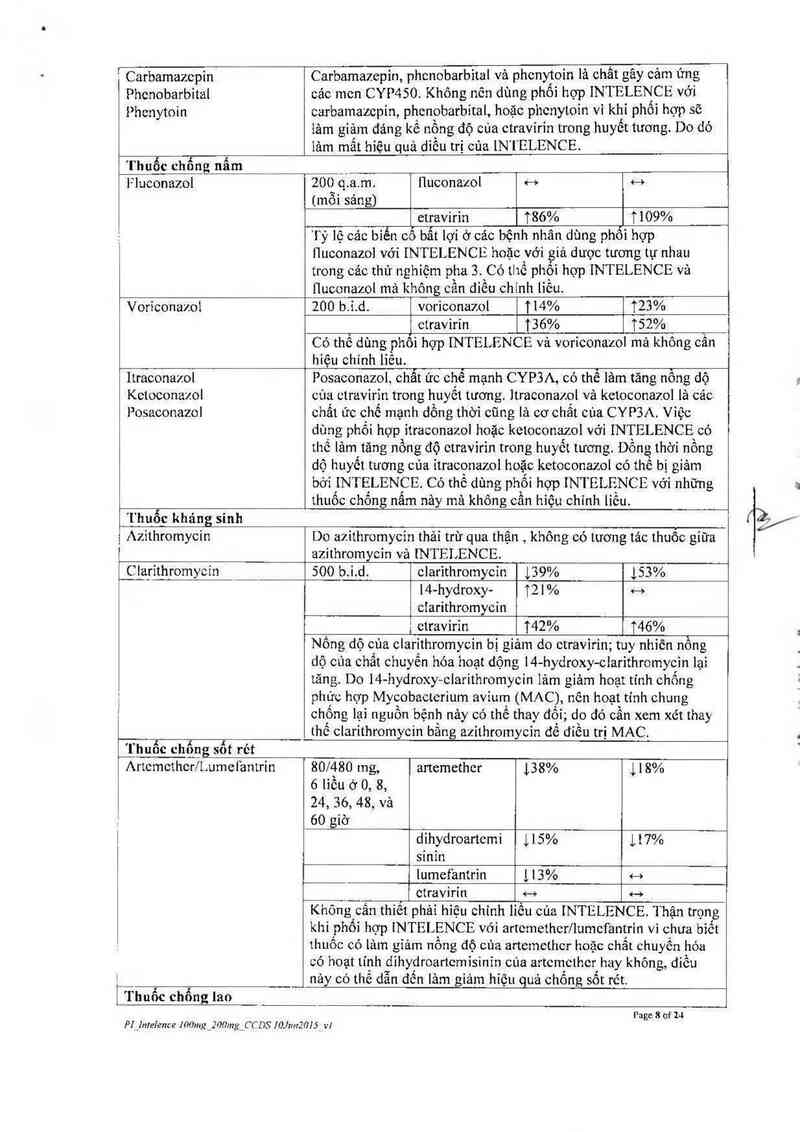
Carbamazepin
Phenobarbital
Phenytoin
Carbamazepin, phcnobarbital vả phenytoin lả ehắt gây cảm ứng
các men CYP450 Không nên dùng phối hợp INTELENCE với
carbamazepin, phenobarbital, hoặc phenytoin vi khi phổi hợp sẽ
iảm giảm đáng kể nông độ eủa etravirin trong huyết tương. Do đó
iảm mất hỉệu quả diều trị cùa IN [ ELENCE.
1 v Ă A A
lhu0c ehonp, nam
l-“luconazol
200 ấ.a.m. iluconazol <—› 4—>
(mỗi sáng)
etravirin 186% 1109%
Tỷ lệ cảc biến eô bẩt lợi ở các bệnh nhân dùng phôi hợp
Huconazol vởi INTELENCE hoặc yới _giả dược tương tự nhau
trong các thử nghiệm pha 3. Có thế phôi hợp INTELENCE vả
Iluconazol mà không cần điều chinh lỉều.
Voriconazoi 200 b.ỉ.d. vorỉconazol 114% 123%
etravirin 136% 152%
Có thể dùng phôi hợp [NTELENCE vả voriconazol mã không cấn
hiệu chinh liều.
Itraconazol Posaconazol, chẫt ức ehễ mạnh CYP3A, eó thể lảm tăng nồng dộ
Ketoconazol eủa etravirỉn trong huyết tương. ]traeonazol vả ketoconazol lá các
Posaconazol ehất ức chế mạnh dồng thời cũng là eơ chất của CYP3A. Việc
dùng phối hợp itraeonazol hoặc ketoconazol với INTELENCE có
thế lảm tăng nồng độ etravỉrin trong huyết tương. Đồng thời nồng
dộ huyết tương cúa itraconazol hoặc ketoconazol có thể bị giảm
bởi INTELENCE. Có thể dùng phối hợp INTELENCE vởi những
thuốc ehống nấm nảy mả không cẩn hiệu chỉnh liều.
Thuốc kháng sinh
Azithromycin
Do azithromycin thải trừ qua thận , không eó tương tảe thuốc gíữa
azithromyeỉn vả INTELENCE.
_C1_aịrĩthromycin 500 b.ỉ.d. ciarithromycỉn 139% 153%
l4-hydroxy- 121% «-›
ctarithromycin
ị etravirin 142% 146%
Nống dộ của clarithromycin bị giảm do ctravirin; tuy nhiên nồng
dộ của chẩt chuyến hóa hoạt dộng 14- -hydroxy-clarithromycỉn lại
tăng Do 14- -hydroxy—elarithromycin lảm giám hoạt tính chống
phức hợp Mycobactcrium avium (MAC), nên hoạt tính chung
chống lại nguõn bệnh nảy Có thể thav đối; do đó cần xem xét thay
thế clarithromyein bằng azithromycỉn để điều trị MAC.
! ~: K Ả Ả :
lhuoc ehong sot ret
Artcmcther/Lumefantrin
Thuốc chống lao
80/480 mg, artemether 138% 118%
6 liều ở 0, 8,
24, 36, 48, vả
60 giờ
dihydroartemi 115% 117%
sinin
lumefantrin 113% <—›
etravirin … v-›
Không cần thiết phải hiệu chinh liều của iNTLLENCE. T hận trọng
khi phối hợp INTELẸNCE với artemether/lumefantrin vì chưa biểt
thuốc có tảm gỉảm nồng độ cùa artemether hoặc chắt chuyên hóa
có hoạt tính dihydroartemisinỉn của artemether hay không, diều
nảy có thể dẫn dến iảm giảm hiệu quả chống sốt rẻt.
l’age 8 of 24
Pi _Infelence IOUmg_JOỦmg_CCDS lOJr/nZỮIS_ vỉ
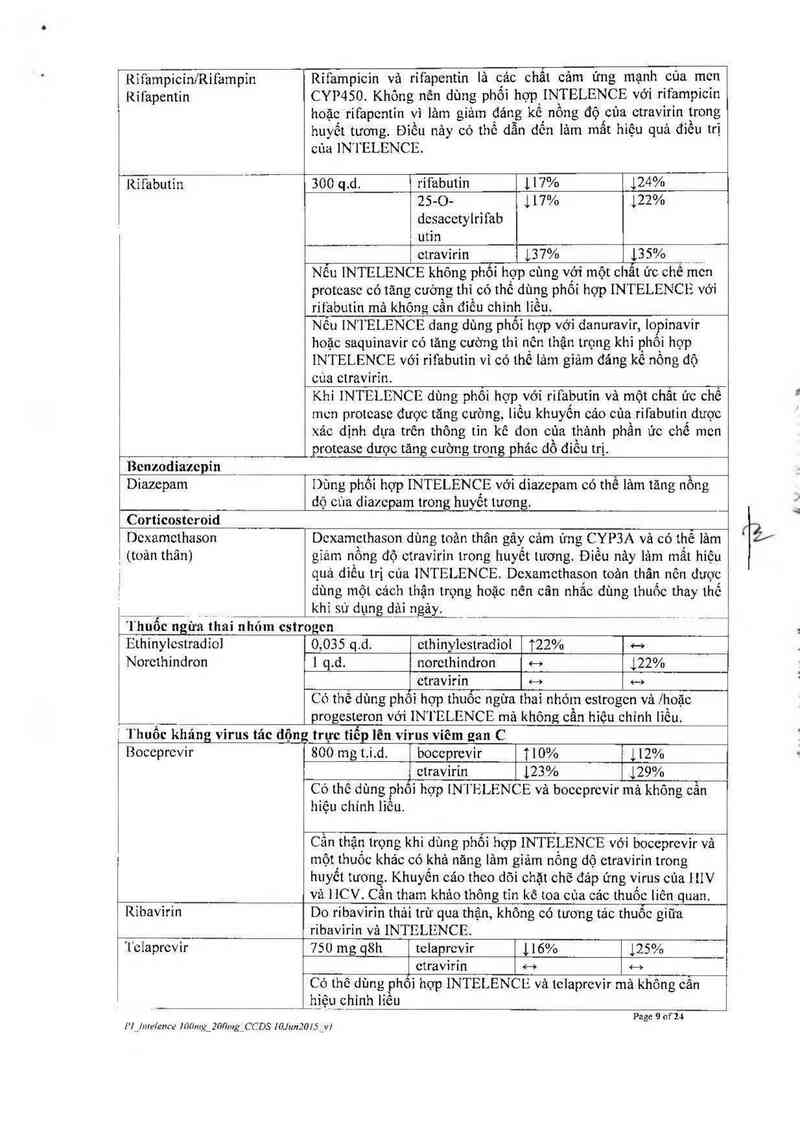
Ridepicin/Rifampin
Rifapentin
Rífampicin vả rifapentin lả eác chất eảm ứng mạnh của men
CYP4SO Khỏng nẻn dùng phối họp INTELENCE với rifampicin
hoặc rifapentin vì lảm giảm đáng kể nồng độ eủa etravỉrin trong
huyết tương. Đìều nảy eó thể dẫn dến lảm mẩt hiệu quả điều trị
của IN ] ELENCE.
Rifabutin
11741
117vz
12496
12224
rifabutin
25-0-
desaeetylrifab
utin
etravirin 137% 135%
Nếu INTELENCE không phối họp cùng vở1' một chẳt uc ehê nten
protcase có tăng cường thì có thể dùng phối hợp INTELENCE với
_rit`abutin mã không cần đỉều ehỉnh liều.
Nêu IN I` ELENCE dang dùng phối hợp với đanuravir, Iopinavir
hoặc saquìnavir có tăng cường thì nên thận trợng khi phôi hợp
INTELENCEVớHHủmfianÓƯỔlmngfflmđủgkổnỡụdộ
của ctravirĩn.
Khi INTELENCE dùng phôi hợp với rifabutin và một chắt ủc chế
men protease được tăng cưòng, liều khuyến cáo cúa rifabutin dược
xác dịnh đụa trôn thông tin kê đon của thảnh phần ửc chế men
protease dược tăng cường trong pháo dỗ diều trị.
300qd.
Benzodiazepỉn
Diazepam
Dùng phối hợp INTELENCE với diazepam có thế lảm tăng nồng
dộ cùa diazepam trong huyêt tương.
Corticosteroid
Dexamethasm
. (toản thân)
Dexamethason dùng toản thân gây cảm ủng CYP3A và có thể lâm
giảm nồng độ ctravỉrin trong huyết tuong. Điều nảy lảm mất hiệu
quả diểu trị cùa INTELENCE. Dexamethason toân thân nôn dược
dùng một cách thận trọng hoặc nên cân nhắc đùng thuốc thay thế
khi sử dụng dải ngảy.
'l`huốe ngừấthai nhóm estr
Ethinylestradiol
Norethindron
ogen
0,035 q.d. ethinylestradiol 122% <—›
1 q.d. norethindron «—› 122%
etravirin e—› …
Có thể dùng phôi hợp thuốc ngứa thai nhóm estrogen vả /hoặe
progesteron vởi INTELENCE mã không cân hiệu chỉnh lìêu.
Í 'I`huổỄĨchảng virus tác động trực tiếp ]ẽn virus viêm gan C
Boceprevir
1800 mg t.i.d. boceprevir 110% 112%
etravirin 123% 129%
Có thế dùng phôi hợp 1N I` ELENCE vả boecprevir mà không cần
hiệu chỉnh liều.
Cẩn thận trọng khi dùng phối hợp INTELENCE vói boceprevir vả
một thuốc khảo có khả năng lảm giảm nồng dộ etravirin trOng
huyết tuong. Khuyến cáo theo dõi chặt chẽ đảp ứng virus cúa IllV
vả HCV Cần tham khảo thông tỉn kê toa eủa các thuốc liên quan.
Ribavirin Do ribavirỉn thải trù qua thận, không có tuong tác thuốc giũa
ribavirin vả INTELENCE.
'1'etaprcvir 750 mg q8h telaprevir 116% 125%
etravirin +—+ 4—›
1’ỉ _lnưlence IOng_20ng_CCDS I 0.11an
Có thê dùng phôi hợp INTELENCE vả telaprevir mã không cần
_hịệ_u chỉnh liều
Page 9 of 24
0.15 _v/
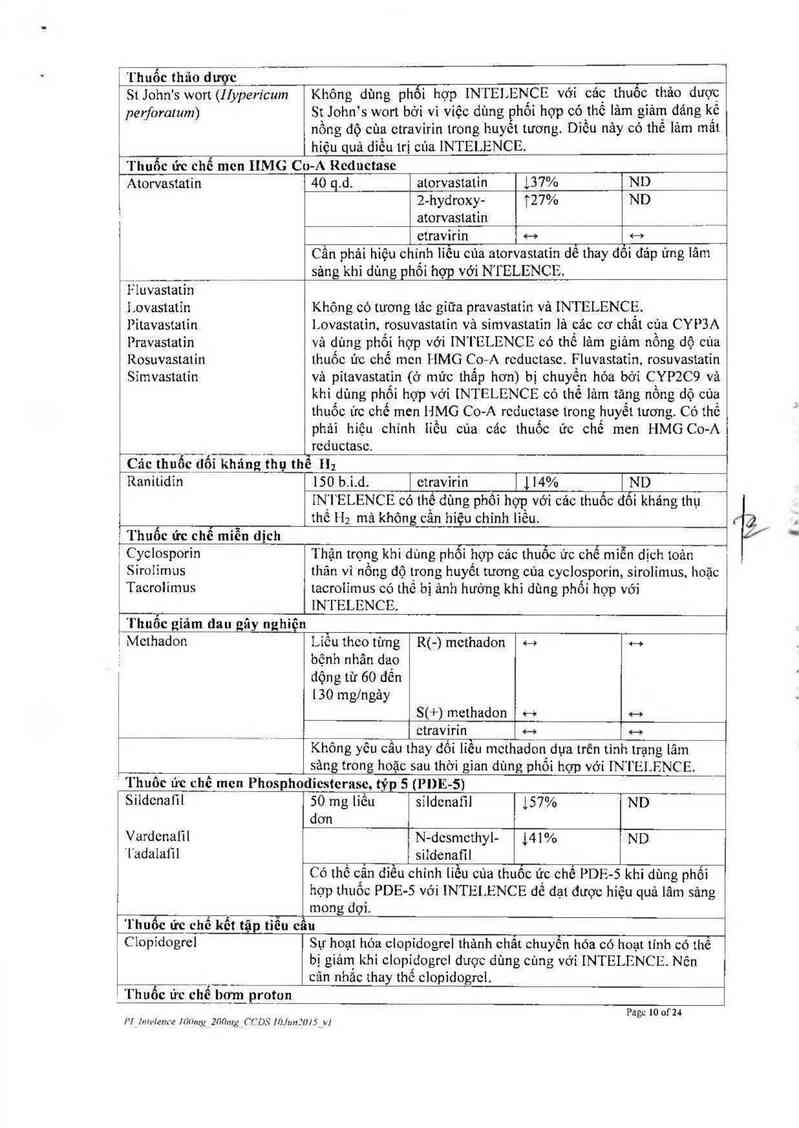
| Thuốc thăo dược
' St John's wort (Ilypericum
perforalum)
Không dùng phối hợp IN TE! ENCE vởi các thuôo thảo dược
St John s wort bới vi vìệe dùng phối hợp có the lảm giảm dáng kế
nồng dộ cùa etravirin trong huyết tương. Dìều nảy có thế lảm mất
hiệu quả diều trị của INTELENCE.
Thuốc ức chế men IIMG Co-A Reductase
Atorvastatin 40 q.d. atorvastatin 137% ND _
2-hyđroxy— 127% ND
atorvastatin ___
etravirin o—+ <——›
Cần phải hiệu chỉnh liều cùa atorvastatin dể thay đôi đáp ứng lâm
sảng khi dùng phôi hợp Với N'I`ELENCE.
1²1uvastatin
1 ,ovastatin
l’itavastatin
Pravastatin
Rosuvastatin
Simvastatin
Không có tương tảo giữa pravastatin vả INTELENCE.
Lovastatin, rosuvastatin vả simvastatin lả eảe cơ chẳt của CYP3A
và dùng phối hợp với IN'I`ELENCE có thề lảm giảm hòhg dộ eủa
thuốc ức chế men I-IMG Co—A reductase. Fluvastatin, rosuvastatin
vả pitavastatỉn (ở mức thấp hơn) bị chuyến hóa bởi cvpzcọ và
khi dùng phối hợp với INTELENCE có thề lảm tăng nồng dộ của
thuốc ức chế men H MG Co-A reductase trong huyết tương. Có thế
phải hiệu chinh tiều cùa eác thuốc ức chế men HMG Co-A
reductase.
Các thuốc“ủối kháng thụ thể
II;
Ran itidin
ISO b.ỉ.d. 1 etravirin 1 114% | ND
tN_TELENCE có thể dùng phối hợg với eác thuốc đỗi khảng thụ
thê 112 mã không cân hiệu chinh liêu.
' v A , ã .z .
. lhuoc ưe che mten dịch
i Cyclosporin
Siroiimus
Tacrolimus
Thận trọng khi dùng phối hợp các thuốc ức chế miễn dịch toản
thân vì nông độ trong huyết tương eủa eyclosporin, sirolimus, hoặc
tacroiỉmus có thế bị ảnh hướng khi dùng phối họp với
INTELENCE.
Thuốc giảm dau gây nghiện
1 Methadon
Liễu theo từng R(-) methadon … …
bệnh nhân dao
động từ 60 đển
130 mg/ngảy
S(+) methadon e—› ...
etravirỉn H …
Không yêu cầu thay đối iỉều methadon dụa trên tình trạng lâm
sảng trong hoặc sau thời gian dùng phối hợp vởi IN l` L`I FNCE.
’ Thuốc ức chế men Phospho
diesterasc, týp S (PDE- 5)
Sitdenatìl 50 mg tỉều sĩldenaíil 157% ND
dơn
Vardenaiil N-desmethyl- 141% ND
'l'adaiaiìl siIdenaf'tl
Có thể cẳn điều chính liều eủa thuốc’ ưc chế PDF -5 khi dùng phối
hợp thuốc PDE-5 với INTEI ENCE đế dạt được hiệu quả lâm sảng
mong đọỉ
Thuốc ức chế kết tập tiễu cau
Clopidogrel
Sụ hoạt hóa clopidogrel thảnh chất ohuyễn hóa có hoạt tính có thể
bị giảm khi ctopidogrel được dùng cùng với INTELI-I NCL. Nên
cân nhắc thay thế clopidogrel.
: 4 A . Á“—
Ihuoe u~c che bơm proton
P! hwlem~e Hlíhuỵ 200mg C`t`DS llì.lunJ
Page 10 of 24
ms_w
ị ()meprazol 40 q ớĨ ] etravirin \ T41% ịND
Có thể dùng phỗi hợp TN TELENCE với các thuốc ức chế bơm
proton mà không cân hiệu chỉnh liều
Í’Ỉ`hịuốc ú~c chế tải hẩp thu Serotonin chọn lọc (SSRls)
Paroxetin 20 q.d. paroxetin <—› 113%
etravirin «—› 4—+
Có thê dùng phôi hợp INTELENCE với paroxetin mã không eần
hiệu chinh liều.
* lrong eảc nghiên cứu tương tác thuốc, eông thức bâo chế khảc nhau vả/hoặc liều dùng khác
nhau cùa IN 1`ỉ1 I ENCF dền cho nhũng nông dộ tuong tự, do đó cảc tướng tảc Iìên quan dến
một công thức bâo chế nảy cũng sẽ liên quan đến công thức bảo chế khảc.
PHỤ NỮ có 'I`IIAI, CHO CON BÚ VÀ KHẢ NĂNG SINH SẢN
Phụ nữ có thai
Chưa có nghiên eửu dầy dù và có kiếm soát chặt chẽ về ctravirin ở phụ nữ có thai. Những
nghiên cứu trẻn dộng vật cho thấy không eó bằng chứng độc tính trên sự phảt triền hoặc
ảnh huởng lên chửc năng sỉnh sản vả khả năng thụ thai (xem Thóng u'n n'ền lâm sảng).
Một nghiên cúu dánh giả IN i`ELENCE (200 mg x 2 lần/ngảy) dùng phối hợp với cảc thuốc
kháng retrovirus khác trong 3 tháng gỉữa và 3 tháng cuỏi cùa thai kỳ ở 15 phụ nữ mang
thai và sau khi sinh, eho thấy phơi nhiễm với etravirin toản phần trong khi mang thai nhìn
chung eao hơn so với sau khi sinh, và phơi nhiễm với etravirin không gắn kết ít hon (xem
Dặc linh dược động học). Không thấy kết luận tương quan lâm sảng ở mẹ hoặc ở trẻ sơ
sỉnh trong thử nghiệm nảy.
INTELENCE chi dược dùng cho phụ nữ có thai nễu lợi ich lởn hơn nguy cơ.
Cho con bú
Chưa rõ etravirin có bải tiết qua sữa mẹ hay không. Do eả nguy cơ lây truyền HIV vả nguy
cơ có các biển cố bất lợi cho tre bú mẹ, cảc bả mẹ không cho con bú khi dùng
[N I`ìl [ [ `NClĩ.
Khả năng sinh sân
Không có dữ lỉệu về ảnh hướng eủa ctravirin lên khả năng sinh sản cùa người. Trỏn chuột
cõng, IN'I'1! F NCFJ không ảnh hướng lên sự giao phối hoặc khả nãng sinh sản (xem Thóng
It'n !iền Íám sảng).
ẢNH nu'ớnc TRÊN KHẢ NÂNG LÁ] XE VÀ VẬN HÀNH MẤY MÓC
IN' FELENCF. có thể gây rối loạn thị giác (nhìn mờ) hoặc rối ioạn thính gĩác vả tai trong
(chóng mặt), đo vậy cân phái hết sức thận trọng khi dùng thuốc
'I`ẢC DỤNG KHÔNG MONG MUÔN
Các phản ứng bất lợi dược trình bảy trong mục nảy. Các phản ứng bất lợi lả eác biến eố bất
lợi có môi quan hệ nhân quả vói vỉệc dùng ctravirin dựa trên đảnh giả toản diện thông tin
biển cố bắt lọi sẵn có. Mối quan hệ nhân quả cùa etravirỉn không thê thìết lập một cảch tin
cậy dựa trôn từng trường họp cả thề. Hơn nữa, cảc thử nghiệm lâm sâng được tiến hảnh
trong cảc diồu kỉộn khác nhau, tỷ lệ các phản ứng bất 1ợi quan sảt được trong cảc thử
nghiệm lâm sảng cùa một thuốc không thể so sảnh trực tiếp vói tỷ iệ trong các thử nghiệm
lâm sảng eoa thuốc khác vả có thế không phản ánh tỷ lộ quan sát dược trong thực hânh lâm
sảng.
Những phản ứng bất lợi trong eảc thử nghiệm lâm sảng trên bệnh nhân người lớn
Fagc 11 nf 24
Pi Imefenrc Illílmỵ 2'00mg í`(`[JS leunJU/5 vl
Dánh giá tính an toản dưa vâo tắt cả cảc dữ liệu của 1203 bệnh nhân trong thử nghỉệm pha
3 có dối chứng giả dược DUE"—l 1 và DUET -2 trôn những bệnh nhân trướng thảnh bị nhìễm
111V-1 dã diều trị với thuốc kháng retrovỉrus, trong số đó có 599 người dược dùng
IN I`~11 I 1: NCL (200 mg b.` i. d) (xem Dặc tính dược lực học). 1`rong cảc thử nghiệm gộp nảy,
trung vị thời gian điều trị cùa nhóm INTELENCE và nhóm giả dược lằn lượt là 52, 3 và
51,0 tuần.
Các phản ứng bắt lợi eủa thuốc hay gặp nhất (AR) (2 5%) mà mức độ nghiêm trọng thâp
nhẳt ở mức dộ 2 là phát ban (10, 0% ở nhóm INTFLENCE và 3, 5% ở nhóm giả duợc), tiêu
chảy (7 0% ở nhóm 1NTELENCE vả 1 1,3% ở nhóm giả dược), tãng triglyeerid máu (6, 3%
ò nhóm IN 1` ELENCF. vả 4, 3% ở nhóm giả dược) vả buồn nôn (5,2% ở nhóm
INTELF.NCF và 4.8% ở nhóm giả dược) (xem bảng dưới).
Phần lớn các phán ứng bất lợi của thuốc dược ghi nhận trong suốt thời gian điếu trị vởi
1N'I`FLIỉNCE lả ớ mức dộ 1—2. Phản ứng bất iợi mức độ 3 hoặc 4 dươc báo cảo lả 22,2%
vả 17,2% tương ứng cho nhóm 1NTELENCE vả nhòm giả dược. Phản ứng bât lợi mức dộ
3 hoặc 4 thường được ghi nhận nhắt lả tãng triglycerid mảu (4,2% ở nhóm INTELENCE
và 2,3% ở nhóm gỉả dược), tăng cholesterol máu (2,2% ở nhóm INTELENCE vả 2,3%ớ
nhóm giả dược), suy thận (2,0% ở nhóm INTELENCE vả 1,2% ở nhóm giả dược) vả thỉêu
mảu (1,7% ở nhóm INTELENCF. vả 1,3% ớ nhóm giả dược). Nhũng bắt thường trong xót
nghiệm cận lâm sảng do diều trị (mức dộ 3 hoặc 4) được ghi nhận iớn hon hoặc bằng 2% ở
các bệnh nhân dược diều trị với INTELENCE, xem bảng “Những bất thường trong xẻt
nghiệm do dỉều trị”. Tắt cả các phản ứng bất lợi mức 3 vảfhoặc 4 khác được ghi nhận nhớ
hơn 1,5% trong số các bộnh nhân được điều trị với iNTELENCE. 5,2% trong số bệnh
nhân cùa nhóm tN'I`ELIỉNCE phải tạm ngừng đỉểu trị do phản ứng bất lợi so với 2,6 %
trong số bệnh nhân eùa nhóm giả dược. Các phản ứng bất lợi thường gặp nhất dẫn dển
ngừng điều trị là phát ban (2,2% ở nhóm INTELENCE so với 0% ở nhóm giả dược).
Phát ban hay gặp nhất là từ mức nhẹ đến trung bình, thường ở dạng vết dến sần hoặc ban
dò, hay xảy ra trong tuẳn diẽu trị thứ 2 và ít gặp hơn sau tuần 4. Ban thướng tự giới hạn và
nhìn chung phục hồi trong vòng 1-2 tuần khi tiếp tục diều trị (xem Thông tín lâm sảng ~
(. ảnh báo và l'hận trọng). Tỷ lệ phảt ban ở phụ nữ eao hơn so với nam giới trong nhóm
dùng INTIỉLENCIỉ trong các thử nghiệm DUET (phát ban 2 mức 2 gặp ở 9160 [15,0%]
phụ nữ so với 51/539 {_9,5%] nam giới; ngừng thuốc do phảt ban dược bảo cáo ở 3/60
[5,0%] phụ nữ so vởi 10/539 [1 .9%] nam giới) (xem Thông tỉn lám sảng- Cảnh báo vả
'I'hận trong) () nhũn0 bênh nhân có tiền sử bị phát ban liên quan với NNR' I`I, không thẳy
có sự tăng nguy cơ xuất hỉện phảt ban do INTFLENCE so vởi các bệnh nhân không có tiên
sư bị phát ban do NNR' 1'1.
Các phản ứng bất lợi ở múc trung bình hoặc nặng hơn (> mức 2) vả được ghi nhận > 1%
trong sô các bệnh nhân diều trị vởỉ 1N'1` FLF NCL dược tồng kết trong bảng dưới dây. Các
phản ửng bất lợi dược iiệt kê theo Ioại eơ quan (SOC) vả tằn suất. Nhũng bất thuòng trong
xét nghiệm dược cân nhắc là phản ứng bất lợi duợc tỏm tắt trong bảng dưới dây (xem
Nhũng bẩt thường mửc 3 dến 4 trong xót nghiệm do diều trị ghi nhận > 2% trong số các
bệnh nhân)
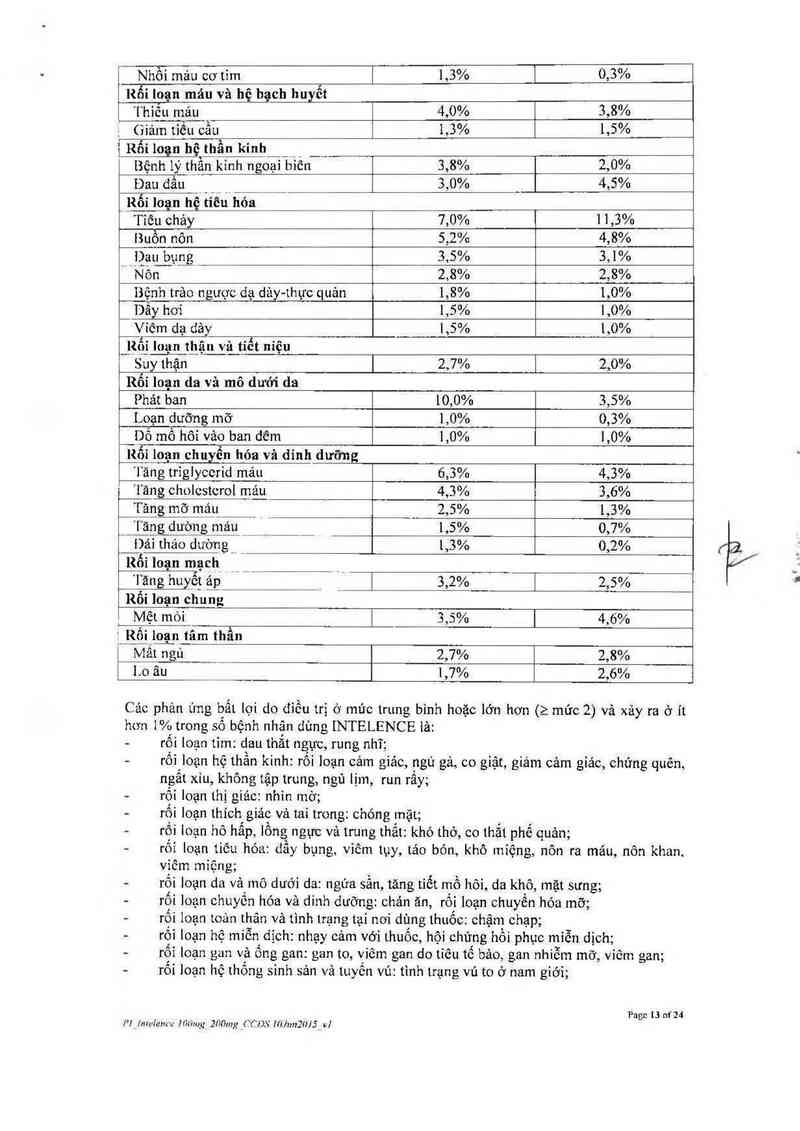
C ác phán úng bất lợi mức trung bình hoặc nặng htm (_ mức 2) và được ghi nhận
> 1% ô cảc bệnh nhân truồng thânh điều trị với IN'I FLENCF.
lhủ nghiệm DUI< "~l 1 và DUE"—I 2
IN'I'ELENCE + Điều Giả dược + diều trị cơ
Phân loại eo; quan (SOC) trị cơ hãn (BR) bản (BR)
- Phản ứn bãt lơi của thuốc N=599 =604
Rôi loạn tim
Page 12 uf 24
Pi hươlence IUflmg—V .200mg_ f`(ỈDS 10.11012015 vl
Nhồi máu cơ tỉm 1,3% 0,3%
Rối loạn máu và hộ hạch huyết
Thiếu máu 4,0% 3,8%
- Giảm tỉếu cẫu 1,3% 1,5%
1 Rối logn hệ thần kinh
Bệnh 1ý thần kinh ngoại biến 3,8% 2,0%
Đau đẩu 3,0% 4,5%
Rối loạn hệ tiêu hóa
“ " Tiêu chảy 1,0% 1 1,3%
Buồn nôn 5,2% 4,8%
Dau bụng 3,5% 3,1%
"' 'ixiòĩ“ 2,8% 2,8%
Bệnh trảo ngược dạ dảy-thụ'c quản 1,8% 1,0%
Dẩy hơi 1,5% 1,0%
Viêm dạ dảy 1,5% 1,0%
Rôỉ loạn t_hật_i_ vả tỉết niệu
Suy thận 2,7% 2,0%
Rối logt da và mô dưới da
Phát ban 10,0% 3,5%
Loạn dưỡng mỡ 1,0% 0,3%
__Dồ mồ hôi vảo ban dêm 1,0% 1,0%
Rối loạn chuyển hóa và dinh dưỡng
Tăng triglyccrid máu 6,3% 4,3%
Tăng cholesterol mẳư 4,3% 3,6%
Tăng mỡ mảu 2,5% 1,3%
Táng_Ếòng mảu _ __ 1,5% 0,7%
Dái tháo duòng _ 1,3% 0,2%
Rối loạn mạch _ _
'Iang huyêt" a_p _ _ | 3,2% 1 2,5%
Rối loạn ehung
, Mệt mỏi | 3,5% | 4,6%
ỊJỀố_i_lo_ạn tâm thần
Mât ngủ _ 2,7% 2,8%
Lo âu 1,7% 2,6%
Cảc phản ửng bất lọi do điều trị ở múc trung bình hoặc lớn hơn (2 mức 2) và xảy ra ở ít
hơn 1% trong số bệnh nhân dùng INTELENCE iả:
rối loạn tim: dau thắt ngực, rung nhĩ;
rối loạn hệ thần kinh: rôi loạn cảm giác, ngủ gả, co giật, giảm cảm giảc, chứng quên,
ngất xỉu, không tập trung, ngũ Iịm, run rây;
rội Ioạn thị giảe: nhỉn mờ;
rối loạn thích giác vả tai trong: chóng mặt;
rối loạn hô hấp, lồng ngục vả trung thất: khó thớ, co thẳt phế quản;
rối toạn tiêu hóa: đầy bụng, viêm tụy, táo bón, khô miệng, nôn ra máu, nôn khan
viêm mỉộng;
rối loạn da vả mô duới da: ngứa sần, tăng tiễt mồ hôi, da khô, mặt sưng;
rối loạn chuyến hóa và dinh dưỡng: chản ăn, rối toạn chuyến hóa mỡ;
rối loạn toản thân và tình trạng tại nơi dùng thuốc: chậm ehạp;
rối loạn hệ miễn dịch: nhạy eảm với thuốc, hội chứ ng hồi phục mỉễn dịch;
rối loạn gan và ống gan: gan to, viêm gan do tiêu tế bảo, gan nhiễm mỡ, viêm gan;
rối loạn hệ thống sinh sản và tuyến vú: tinh trạng vú to ở nam giới;
Page 13 nf2d
P! lmulem~e IHI`lmg_ 200mg_(Y`DS !llltm2í'tlj v]
- rối loạn tãm thần: rối loạn giấc ngù, mơ bẫt thường, tình trạng lẫn, mât phương
hướng, nớng nảy, ảc mộng.
Các phán úng bất lợi bổ sung của thuốc it nhất ở mức trung bình còn gặp ở trong eảc
nghiên cún khác như loạn dưỡng mỡ, phù nề thần kinh mạch, ban đó đa dạng và đột quỵ
do xuất huyêt, moi loại đuợc ghi nhận trong không quá 0,5% cùa số bệnh nhân. Hội chủng
Stevens-Johnson (hiêm gặp; < 0 ,1%) vả hoại tử biền bì nhìễm độc (rất hiếm gặp; <0 ,01%)
được báo Cảo trong phát trìền lâm sảng của 1N’1 ELENCE.
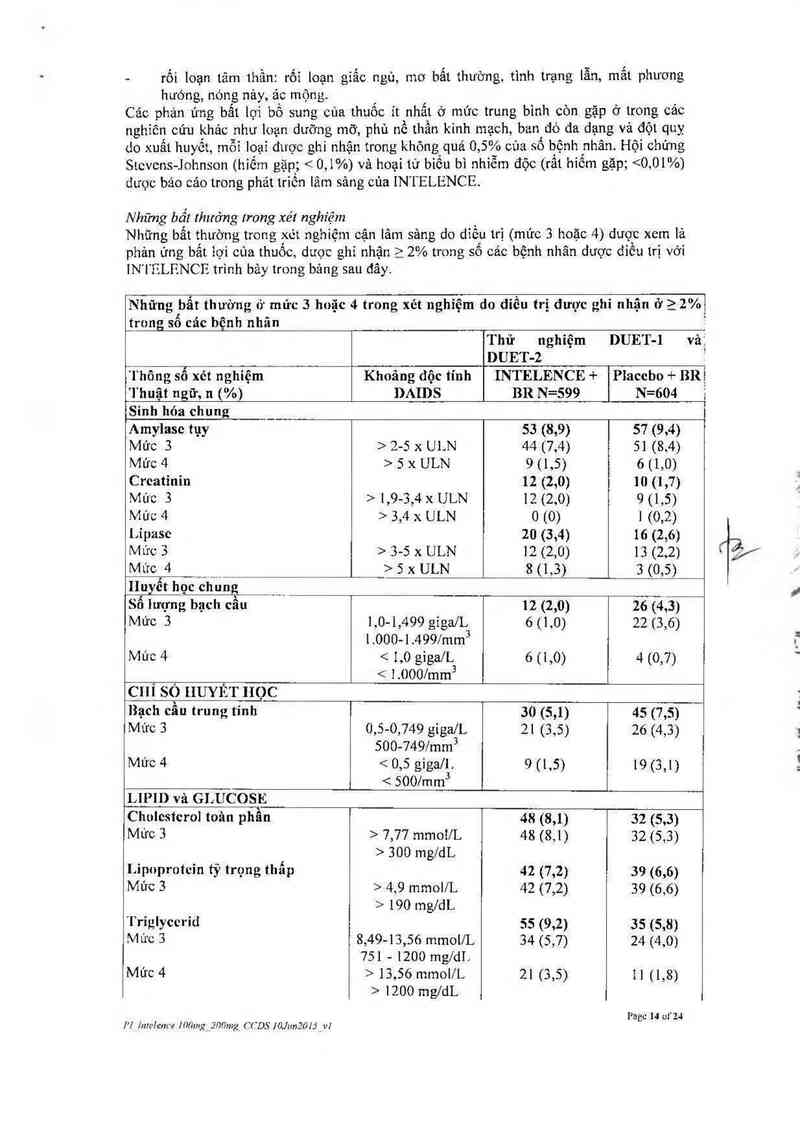
Những bất thường lrong xét nghiệm
Những bất thường trong xét nghiệm cận lâm sảng do diều trị (mức 3 hoặc 4) dược xem lả
phản ứng bắt iợi của thuốc, dược ghi nhận > 2% trong số các bệnh nhân dược diều trị vởi
IN 1 F.LF.NCF trình bảy trong bảng sau đây
trong số các bệnh nhãn
Nhũng bẩt thuờng ớ múc 3 hoặc 4 trong xét nghiệm do diều trị đươc ghi nhận ở > 2%1
Thử nghiệm
DUET-l vảị
I’J' lnlelenfe l0(1111g_200111g C(`DS lOJi/nZÚIJ v]
DUET-2
Thông số xét nghiệm Khoảng dộc tính INTELENCE + Placcbo + BRị
Thuật ngữ, 11 (%) DAIDS BR N=599 N=604 '
Sinh hỏa chung
Amylase tụy 53 (819) 57 (9s4)
Mức 3 > 25 x ULN 44 (7,4) 51 (8,4)
Mức4 >5xULN 9(1,5) 6(1,0)
Creatinin 12 (2,0) 10 (1,7)
Mức 3 › 1,9-3,4 x ULN 12 (2,0) 9 (1,5)
Mức 4 > 3,4 x ULN o (0) 1 (0,2)
Lípase 211 (3,4) 16 (2,6)
Mức 3 › 35 x ULN 12 (2,0) 13 (2,2)
Mức 4 > 5 x ULN 8 (1,3) 3 (0,5)
Huyết học chung
Số lượng bạch cẩu 12 12,01 2614.31
Mức 3 1,0-1,499 giga/L 6 (1,0) 22 (3,6)
1 000 1 499/mm²
Mức 4 < 1,0 giga/L3 6 (1,0) 4 (0,7)
_ < 1 .3000/mm
_cỵí sò [IUYÉT HỌC
Bạch cẩu trung tính 30 (5,1) 45 (7,5)
Mức 3 o, 5 0, 749 gigafL 21 (3,5) 26 (4,3)
500- 749/mm
Mức4 7,77 mmoi/L 48 (8,1) 32 (5,3)
> 300 mgldL
Lỉpoprotein tỷ trọng thấp 42 (1,2) 39 (6,6)
Mức 3 > 4,9 mmol/L 42 (1,2) 39 (6,6)
> 190 mg/dL
'l`riglyccriđ 55 (9,2) 35 (5,8)
Mức 3 8,49-13,56 mmoi/L 34 (5,7) 24 (4,0)
751 - 1zoo mg/dL
Mức 4 > 13,56 mmol/L 21 (3,5) 11 (1,8)
> 1200 mg/dL
Page 14 ot`24
Mức Glucose tăng 21 (3,5) 14 (2,3)
Mức 3 13,89-27,75 mmol/L 21 (3,5) 13 (2,2)
251—500 mg/dL
Mức 4 > 27,75 mmol/L 0 (0) 1 (0,2)
> 500 mg/dL
Cảo thông số về gan
Men Alanin amino transferasc 22 (3,7) 12 (2,0)
Mức 3 5,1-10 x ULN 16 (2,7) 10 (1,7)
Mức 4 > 10 x ULN 6 (1,0) 2 (0,3)
Men Aspartat amino transferase 19 (3,2) 12 (2.0)
Mức 3 5,1-10 x ULN 16 (2,7) 10 (1,7)
Mức 4 > 10 x ULN 3 (0,5) 2 (0,3)
UI.N= Giới hạn trên cúa mức bình thường
Loạn dưỡng mỡ , ,
[.iệu pháp kháng rctrovirus phối hợp) dã gây nên sự tái phân bõ mỡ trong cơ thể (loạn
dưỡng mỡ) ở bộnh nhân 111V, bao gôm hao hụt mỡ duởi da ngoại biên vả mặt, tăng mỡ
trong bụng vả mỡ lạng, tăng mở ở ngực và lích mở ở lưng vả cố (bưởu trâu) (xem Thóng
tin lăm sòng— Cảnh báo vả Thận lrọng).
Hỏi chzmg phục hồi mỉễn dịch
Ở những bệnh nhân nhiễm 111V có suy gỉảm mỉỗn dịch nghiêm tfọrìg vảo lúc khỏi đầu
dùng liệu phảp kháng rctrovirus phối hợp, phản ùng viêm vởi các nhiễm trùng cơ hội
không triệu chứng hoặc nhiễm trùng cơ hội sỏt lại có lhế tăng (hội chúng phục hồi mìỗn
dịch). Dã gặp cảc rối loạn tự miễn như bệnh Grach trong hội chứng phục hồi miễn dịch
(xem T hông Iin lâm sảng — Canh báo và Thận trỌng).
[ hong lz'n bo sung o'~ cảc đối l1rọng đặc biệt
Iìênh nhận bi dổne nhiễm vói vỉrus vỉêm ean B vả/hoãc viêm ean C
'1rong số cảc bệnh nhân bị đồng nhiễm (n= 139) trong phân tích gộp của thử nghiệm
DUET-l vả DUE'I—2, AST tăng lên mức 3 hoặc 4 ở 9, 7% trong số 72 bệnh nhân thuộc
nhóm dùng INTELENCE vả 6, 0% trong số 67 bệnh nhân thuộc nhóm giả dược vả tăng
ALT lên mức 3 hoặc 4 ở 1 1,1% trong số bệnh nhân thuộc nhóm dùng INTI~J LENCE và
7,5% trong số bệnh nhân thuộc nhóm gỉả dược. Trong số cảc bệnh nhân có đồng nhiễm,
1 4% các bệnh nhận đỉếu trị vói IN’I` 131 ENCE và 3 ,0% bộnh nhân ở nhóm gĩả duợc bị
ngừng diều trị do rối loạn hệ lhống gan hoặc mật.
Cần xem xót dẩy dù vỉệc lheo dõi lâm sảng chuẩn mục ở những bệnh nhân bị vỉôm gan
mạn tính
Dữ liêu hâu mãi
Ngoài các phản ứng bất lọ1 gặp 1rong cảc nghiên cứu 1âm sảng dược lỉệt kê ở trên, dã gặp
các phản úng bất lợi dưới đây trong kinh nghỉệm hậu mãi. "Iần Suắt dưọc qui ước như sau:
Rẳt Lhuờng gặp > 1/10 (_ 10%)
'l`hường gặp ì 17100 vả <1110(a 1% vả <10%)
1'1gặp ì1/1000vả<1/100(ìO,l%vả100 ụM.
Page lũ of2al
Pi ỉnrelanre fflrlmg 21'JIsz (.`(ẺILS'II'JJ1m2WÃ vl
Nồng dộ ECso cùa clravỉrỉn lăng lên 5,8 bởi nhân tố trung gian khi có cùa huyết thanh
người.
Không thấy có sụ đối kháng giữa elravirin và bất kỳ thuốc kháng rctrovirus dã nghiên cún
nảo. Elravỉrin thể hiện hoạt tinh khảng virus bổ sung khi dùng kết hợp với cảc Pl nhu
amprcnavir, alazanavir, darunavir, indinavir, lopinavir, neiíinavir, ritonavir, tipranavir vả
saquinavir; các thuốc N(t)R"ll như zaicitabin, didanosin, stavudin, abacavir vả tcnofovỉr~
các thuốc NNRTI như cfavỉrcnz, đolavỉrdin vả nevirapin; thuốc ủc chế sự dung họp
cnt`uvirtìd; thuốc ức chế mcn ỉmcgrasc strand transfer raỉtcgravir và thuốc dối kháng CCRS
maraviroc. Ltravirin còn 1hổ hiện hoạt tính kháng virus hiệp đồng khi phối hợp vởi các
lhuốc NRI` 1 cmtricitabin, lamivudin vả zidovudin.
nè kháng _
I`rong panci tạo bởi 65 chùng 111V- 1 khác nhau do thay thê một amino acid đơn tại vị trí
RT liên quan dến khảng NNRI`L bao gồm cả những chủng thường gặp như K103N vả
YISlC, ctravirin có hoạt tính kháng virus tiềm ân vởi 56 trong số cảc chủng dó. Sự thay
thế amino acid dẫn dến sự dễ kháng cao nhẩt đối vói ctravirin trong nuôi cấy tế bảo là
chùng Y1811 (giá trị 13 Cso thay đổi 13 lần) và Y181V (giá trị ECso thay đối 17 lần) Hoạt
tính khảng vỉrus của ctravỉrin trong nuôi cây tế bảo khảng 1ại 24 chùng HIV- 1 có thay thế
nhiều amino acid liên quan dến sự đề kháng vói N(l)R [ I vả/hoặc P] có thễ so sảnh vói hoạt
tính khảng virus khảng 1ại chùng 111V-1 hoang dại.
Vỉệc chọn lọc in vilro cúa cảc chùng khảng lại etravìrin có nguồn gốc từ chủng HIV- ]
hoang dại từ cảc chùng gốc và cảc phân týp khác nhau cũng như HỈV- 1 kháng NNRTl
dược thục hiện ở nông độ virus cao vả thẳp. Ở nồng độ virus cao, sự xuất hiện cảc chủng
có dễ khảng với chùng HIV- ] hoang dại bị trì hoãn hoặc bị ngăn ngừa ở nồng độ 40 nM
hoặc 200 nM. Hiện tượng nảy cũng quan sảt thấy ở những chủng đề kháng lả nhũng dột
biên K103N vả Y181C liên quan đến khảng NNRTI đơn. Bắt kế cách thức thử nghiệm vả
chùng 111V- 1 gốc, sự xuất hiện dễ khảng clravirỉn đòi hỏi các dột biến kép lrong RI`, trong
đó có các chủng sau hay gặp: 1 1001,E138K,13138G, V1791, Y181C vả M2301.
"1rong cảc thử nghỉệm pha 3 DUET- 1 và DUE1` 2, các đột biến hay gặp trong những bệnh
nhân thắ1 bại vởi phác đồ điều trị có INTELENCF lả V179F, V1791, vả YISIC, chúng
thưòng 121 cơ sở cùa các đột biến liên quan đến đề kháng kép NNR 11 khác (RAM). 1`rong
lất cả cảc nghiên cứu 1iến hảnh với IN' IFLENCE trên những bệnh nhân nhiễm 111V- 1 cảc
dột biến hay gặp lả: 11001, 13138G, V1791, V1791, Y181C vả1.1221Y
Dễ kháng chéo
[1 có đề khảng chéo giũa clravirỉn vả cfavircnz được quan sát thấy … vilro ở 3 trong số 65
chùng dột biễn 111V-1 trực tiềp chứa các dột biến liôn quan đến sư dề kháng NNR".II Đối
với các chùng khảc, cảc vị trí amino acid lỉên quan dến giảm tính nhạy cảm với ctravirin vả
ci`avircnz iả khảc nhau Ftravirin có giá trị ECso < 10 nM trong 83% cùa 6171 các chùng
phân lập trôn lâm sâng dã kháng vởỉ dciavírdin, cfavỉrenz vả/hoặc ncvirapin Không
khuyến cảo chế dộ diển trị có ctravirin cho những bệnh nhân đã thất bại vởỉ delavirdin,
cí’avircnz hnặc nevirapin.
Nghiên cún lâm sảng
Bệnh nhân nguời lớn dã điều tr_1 tru ~ớc đó
Băng chửng về hiệu quả cùa 1N [`FLENCE đuợc dựa trên cảc phân 11'ch số liệu 48 1uần của
2 thứ nghìệm pha 3 I)UE'-l` 1 vả [)UETÍ2 ngẫu nhiên, mù kép, dược dối chứng vởi giả
dưọc. Các thử nghiệm nảy giống nhau về thiết kế nghiên cứu vả cho kết quả tương tư về
hỉệu quả của 1N'1`Ẻ1 I ENClS. Các kết quả dưới dây là dữ liệu tổng hợp cùa hai thủ nghiệm.
Page 17 of 24
l’l lnlcÌem-c10(1171g_2(Ifhng_íf`t”DS 10J11r12015 vi
Những bệnh nhân bị nhiễm 111V-1 dã diều trị trước đó có > 5000 phiên bản 1-11V-1
ARN/mì trong huyễt tương vả có 1 hoặc nhiều dột bỉến lỉẽn quan đến khảng thưốc NNR 11
trong xét nghiệm sảng lọc hoặc qua phân tích kiến gen trước dó (như khảng tich lũy) duợc
lụa Lhọn. Những bệnh nhân nảy cũng có tù 3 hoặc nhỉổu hon trong sô các đột biến Pi chính
sau: D3ON, V321, L331, M4611L, 147A/V, G48V, ISOL/V, V82A/1 /L/SIT, 184V, NSSS
hoặc L9OM khỉ sảng lọc và dã qua chế độ điểu trị kháng retrovirus ổn định it nhất là 8
tuần. Tinh ngẫu nhiên cùa nghiên cứu dược sắp xếp qua việc sử dụng thuốc enfuvỉrtid
(ENF) trong chế dộ diều tri cơ bân (BR), đã từng sử dụng thuốc darunavin'ritonavir trước
dây vả tải lượng virus khi sảng lọc. Phân tích nảy gôm 612 bệnh nhân trong thử nghiệm
1)111"1`-1 và 591 hệnh nhân trong thử nghiệm I)UEI`,-2 iả những người dã kết thúc 48 tuấn
diều trị dược hoặc dã ngùng diều trị sởm hơn.
"Iại tuần 48, tỷ lệ dáp ứng virus học duợc dảnh giá trên những bệnh nhân dùng
INFELI NC1ĩ(ZOOmg, 2 ìần/ngảy) phối hợp vởĩ chế dộ dìềư trị cơ bản so với nhũng bẹnh
nhân dùng giả dược phối hợp với dìếu trị cơ bản. Chế độ điều trị cơ bản gồm
darunavirlritonavir 600/100 mg x 2 lằm’ngảy vả thôm it nhất là 2 thuốc khảng rctrovirus
khác do điểu tra viên lua chỌn (N[t]RTI có hoặc không có ENF). 45, 6% trong số bệnh
nhân ở nhóm dùng N 1 F..1 1² NCE và 46, 9% lrong sô bệnh nhân ở nhóm dùng giả dược có
sử dụng ENF trong điều 1rị kháng rctrovirus 25,5% trong số bộnh nhân của nhóm
IN 1' LLFNCE dã sử dụng ENF lấn dầu (de novo), so vói 26, 5% bệnh nhân cùa nhóm giả
dược. 20,0% bệnh nhân trong nhóm IN'I`ELENCE tải sử dụng ENF, so vởi 20,4% bệnh
nhân của nhóm giả dược. Dáp ứng virus dược xảo định qua việc dạt dược tải 1UỌng virus
dưới mức phảt hiện dược (<50 phiên bản 111V-1 ARN/mL).
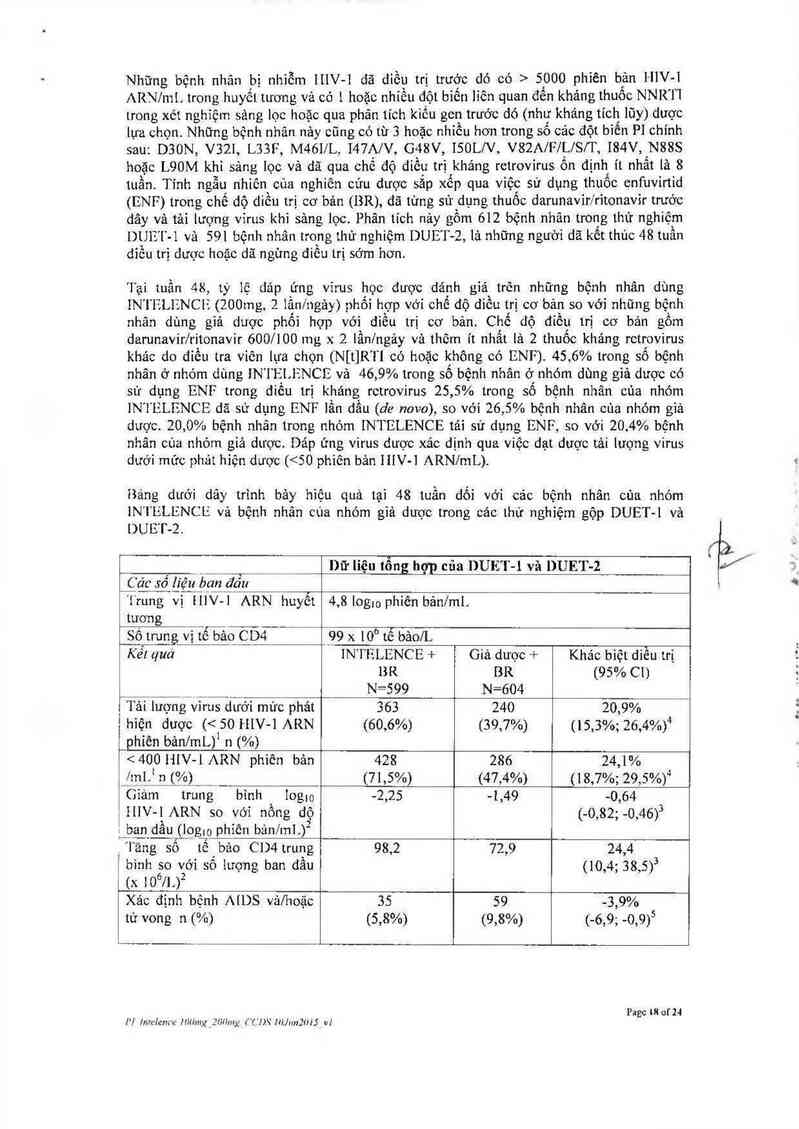
Báng dưới dây trình bảy hiệu quả tại 48 tuần đối vởi cảc bệnh nhân của nhóm
1N’1`ELENCE vả bệnh nhân cùa nhóm giả dược trong nảc lhử nghiệm gộp DUET-l vả
[)UET-2.
Dữ liệu tổng_h_ơp cũa DUET-l vả DUET-2
_Các số h'ệu bạn đảu
1…ng vị 111v-1 ARN huyễt 4,81og…phiênbánme
phiên ban/mL)l n (%)
tương _
56 trung vị lễ bảoỆD4 09 x 10° tễ bảo/L
Kết qua IN'I`ELENCE + Giá dược + Khác biệt diễu tri
B R BR (95% CI)
_ N=599 N=604
_ Tải lượng virus dưới mức phát 363 240 20,9%
hiện dược (< 50 HIV-l ARN (60,6%) (39,7%) (15,3%; 26,4%)4
<400111V-1ARN phiên bản 428 286 24,1%
J1ụ_1.jn (%) _ (71,5%) (47,4%) (18,7%; 29,5%)“
Giảm trung bình ioglo -2,25 -1,49 -0,64
,111v IARN so với nồng dộ (0,82;-0,46)3
ban dầu (log… phỉên bản/ml )2
_'láng số lễ bảo CIJ4 trung 98,2 72,9 24,4
bình so với số iưọng ban dầu (10,4; 38,5)3
(x 10"71 )²
Xác định bệnh AIDS vảlhoặc 35 59 -3,9%
111 vong 1) (%) (5,8%) (9,8%) (4,9, 0,9)5
l’l' inrcỉem~c Hing_2ffflmg ("CD.S` IHJMNZUI5 v)
Page 111 0124
\1
1` ính theo thuật toán 1'LOVR.
Những người không hoản thảnh điều trị được cho lả thất bại: những bệnh nhân ngừng
diều trị sớm dược coi là có thay đối bằng 0 lại mọi thời diểm sau khi ngùng
Sự khác hỉêt trong diểu trị tính thon cách tính trung bình theo bình phương tối thiếu dựa
trên mô hình ANCOVA bao gồm cảc yếu tố phân tầng. Giá trị P < 0, 0001 đối với giảm
trung bình 111V- 1 RNA; gỉả trị P =0, 0006 đối với thay dối trung bình của số tế bảo
CD4.
Khoảng lin cậy gần với những khảc biệt có thể nhận thấy cùa tỷ iộ đáp ứng; giá trị P
< 0, 0001 tính lhco phương pháp hồi quy bao gồm cả cảc yêu tố phân tầng.
Khoảng tin cặy gần với những khác biệt có thể nhận thấy của tỷ lệ đảp ứng; giá trị P
- —0, 0408.
Kể 111 khi phát hiện dược hiệu quả lương tác giữa điều trị vả ENF, dã tỉến hảnh phân tích
ban dầu cho 2 nhóm FNF (bệnh nhân tái sử dụng ENF hoặc không sử đụng 1ỉNF so Với
bộnh nhân sử dụng iỉNF lần dầu)
Kết quả từ các phân tích tồng hợp ở 48 tuần cùa DUET- 1 vả DUEF—2 chứng minh rằng
nhóm IN "511 LENCL vưọt trội so vởi nhóm giả đuợc bất kể ENF dược sử dụng lần dầu hay
không. Trong nhóm bệnh nhân hoặc 121 tải sử dụng hoặc không sử dụng ENF, tỳ 1ệ bộnh
nhân có < 50 phiên bản 1-11V-1 ARN /mL 121 57,0% ở nhóm INTELENCE vả 33,0% ở
nhóm giả dược (khác bỉệt 24,0%, p <0.0001). ở nhóm câc bệnh nhân sư dụng ENF lần
dầu, 71,2% trong nhóm IN'1`ELENCE cỏ < 50 phiên bản 1-11V-1 ARN/mL so vởỉ 58,5%
trong nhóm giả dược (khảc biệt 12,7%, p=0,0199).
ở tuần 48. số bệnh nhân 11 hơn dáng kể trong nhóm INTELENCE (35 bệnh nhân, 5,8%)
dạt Liêu chi lâm sảng (xác định 1ả A1DS hoặc tử vong) so vởi nhóm giả dược (59 bệnh
nhân, 9,8%) (10% 0,0408).
Kểt quả rrụ~c !iểp trên bệnh nhân
Trong cảc thử nghiệm gộp DUET, các bệnh nhân trong nhóm IN 'llẫ 1 FNCF đã chứng tỏ
răng việc diều trị 48 tuần mang lại những cải thỉộn tốt dáng kể so với ban dầu về thể trạng
dược đánh giá dựa theo bộ câu hòi “Dảnh giả chức nảng của nhìỗm virus gây suy giảm
miễn dịch ở nguời” (F A1- 11). Sự cải thiện thể trạng nảy tốt hơn đảng kế có ý nghĩa lhống kê
ở những bệnh nhân dùng INTEI ENCF so với bệnh nhãn trong nhóm giả dược. Dối với
thang thế lrạng chung và chức nãng, không thấy sự khảc biệt có tính lhống kê.
Kiểu gen Imy kiểu hinh brm dầu và phân n'ch kể! quả về virus
'l`rong DUL`T—l vả DUET-2, sự có mặt cùa 3 hoặc nhiều hon nhũng dột biến sau tại thời
điẽm ban dằu: V901 A98G, 11001K10113, 141011², V1061, V179D,V179F,Y181C,
Y1811,Y181V, Gl9OA và 61908 (INTELENCE RAM) có iiên quan với giảm đáp ứng
cứa virus dối với IN ] El ENCE (xem báng dưới dây) Cảc đột biến đơn 1è dã xảy ra trong
sự có mặt cùa các NNRTI RAM khảo V1791` không bao giờ hiện diện mà không có
Y181C.
Tỷ lệ bệnh nhan củ < 50 phiên hân IllV-l ARN/mL ở tuần 48 theo sỗ lượng các đột
hiến liên quan dến kháng IN TELENCE (lN1 ELENCE RAM) ở các dối tưọng không
dùng V_F trong Lác nghiên cúu gộp DUET
Tỷ lệ bệnh nhân tải sử dụng hoặc không sử dụng
enfuvirtid
I’! Jnmlem~e IUllmg 200111g ( `CDS 10.111r120|5_v1
số các đột biễn INTELENCE + BR Giả dược + BR
INTELENCE RAM %; (n/N) %; (an)
0 74, 1 0/0 42,70/o
(117/158) (611143)
Page 19 of 24
61,3% 38,6%
' (737119) (597153)
“ 64,1% 26,2%
² ___ (41/64) (16761)
“ > 3 38,3% 28,2%
(23760) (1 1739)
n = số bệnh nhãn được thco dõi; = tông số bệnh nhân
Đối tượng được phân tích 111 tất cả cảc bệnh nhân ngoải những nguời bị ngừn diều trị vì
1ý do khảo với lý do về thất bại virus được phân tích (loại trừ dối tượng that bại vỉrus
học)
K103N lả chùng dột bỉến NNRTI thường gặp nhất trong nghiên cứu DUET- 1 vả DUET-2
tại thòi diồm ban dầu, khỏng dược xác dịnh lả chùng đột biến liên quan dến dề kháng với
INTEI 1` NC1. Sự có mặt cùa dột biến nảy không ảnh hướng đến dảp ứng trong nhóm
lN'FELIỉNCE.
Kiến hình (Phenotypc) etravirin ban đầu (thay đối tính nhạy cảm so vởi chùng đối chiếu)
dược xem như là yếu tố dự doản của kểt quả về virus. Tỷ lệ đáp ứng được đánh giá theo
kiếu hinh ctravirin ban đầu dược trình bảy trong bảng dưới đây. Cảc nhóm kiều hinh ban
đầu dựa trên việc lựa chọn nhóm các bệnh nhân trong thử nghiệm DUET- 1 và DUET—2 vả
khỏng dại diện cho cảc diểm cẳt nhạy cảm lân) sảng cuối cùng của INTELENCE Cảo dữ
1iộu đuợc cung cấp cho các bảo sĩ thông tỉn về khả năng có hiệu quả dối với virus dựa trên
tính nhạy cảm truớc diều trị với ctravirin ở bệnh nhân đã từng điều trị.
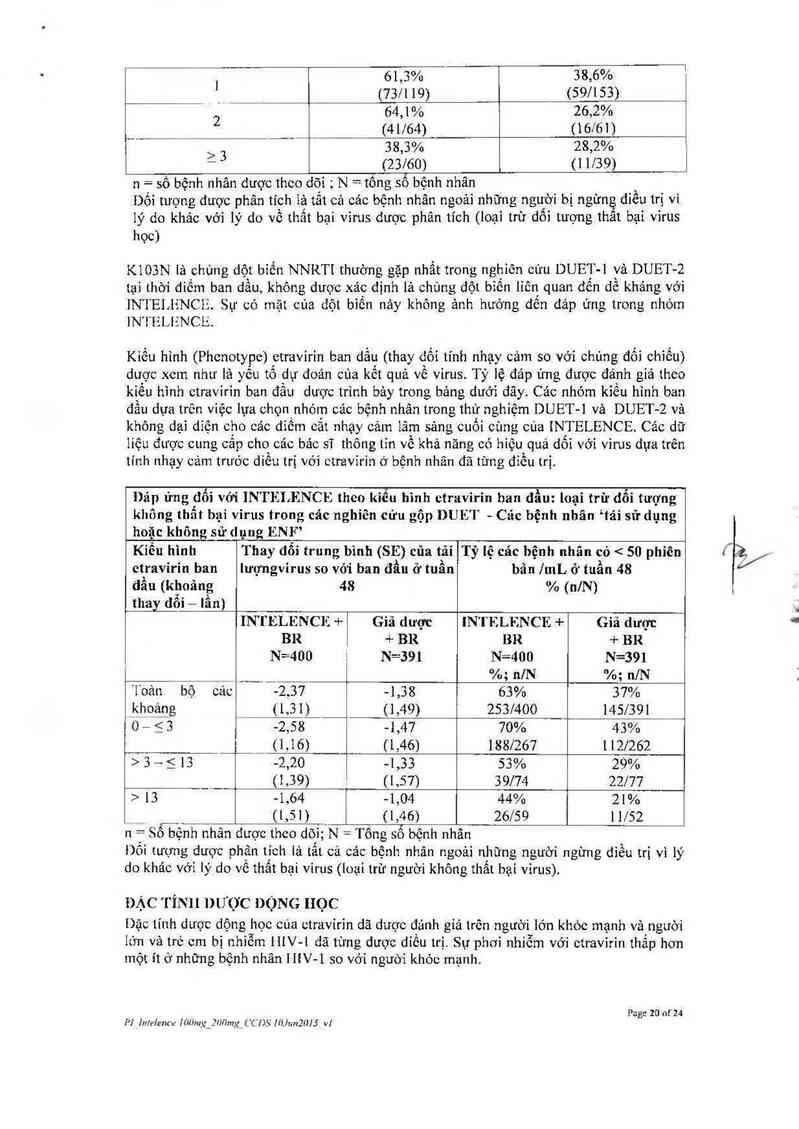
Dáp ứng đôi với INT F LENCE theo kiêu hình ctravirin han đẩu: Ioại trừ dỗi tượng
khong thẫt bại virus trong các nghiên cứu gộp DUEF - Các bệnh nhân ²táỉ sử dụng
hoặc không sử dụng ENF’
Kiểu hình Thay đỗi trung bình (SE) của tãi Tỷ lệ các bệnh nhãn cỏ < 50 phiên
ctravỉrin ban Iượngvirus so với ban đầu ở tuần bãn lmL ở tuần 48
đầu (khoảng 48 % (nlN)
thay đỗi —— lần)
INTELENCF. + Giá dược lN'I`ELENCE + Giá dược
BR + BR 1312 + BR
N=400 N=391 N=400 N=391
…_ %; n/N %; n/N
Toản bộ các -2,37 -1,38 63% 37%
khoảng _ (1,31 )_ (1,49) 2537400 1457391
0 — S 3 -2,58 -1,47 70% 43%
_ (1,16) (1,46) 1887267 1127262
> 3 ~ 5 13 -2,20 -1,33 53% 29%
(1,39) (1,57) 39774 22777
› 13 -1,64 -1,04 44% 21%
(1, 51) (1, 46) 26/59 11752
n = So bệnh nhân dược theo dõi; N= Tông số bệnh nhân
Doi iương dược phân tích lả tất cả cảc bệnh nhân ngoải nhũng người ngùng diều trị vì lý
do khác với lý do vê thất bại virus (loại trừ người không thất bại vỉrus)
1)ẬC TỈNH DƯỢC DỌNG nọc
Dật: lính duoc dộng học của ctravirin dã dược đảnh gỉá trên người lớn khỏe mạnh và ngưòi
lớn và trẻ cm bị nhíỗm 111V-1 đã tùng dược dỉều trị. Sự phơi nhiễm với ctravirin thấp hơn
một ít ở những bệnh nhân 111V- 1 so vói ngưòi khỏL mạnh
Page 20 nt” 24
Pi Ìn/elcnce lÚUmg_2íllìmg_(`(`IJS !lìlun20U vl
Cảc thông số duọc dộng học của etravirin liều 200 mg, 2 lầnlngây trên những bệnh
nhân người lớn nhiễm 111V-1 (dữ lĩệu tổng hợp trong thử nghĩệm pha 3 ở tuần 48)*__
I`hông số Etravirin 201] mg, 2 lần/ngây
N= S75
AUC…1 (ng-h/mL)
Trung bình nhân 1 bộ lệch chuẩn 4522 :t 4710
'I`rung vị (khoảng) 4380 (458 — 59084)
Con (nghni..)
Trung bình nhân i Dộ lệch chuẩn 297 i 391
'l`rung vị (khoảng) 298 (2 — 4852)
* Iất cả bệnh nhân nhiễm 111V- 1 dược lựa chọn vảo các thử nghiệm 1âm sảng pha 3 dược
chỉ định darunavir/ritonavir 600/100 mg x 2 lần/ngây như một phần trong iiệu phảp dìểu trị
nến cùa họ. Vì vậy, các 1hông số dược dộng học thế hỉện trong bảng giải thich cho sư giả1n
các thông số duợc dộng học của ctravirin khi phối hợp lNTELENCE vói
darunavỉr/ritonavỉr.
Lưu ý: Trung vị nồng dộ diều chỉnh lỉên kềt protein huyết tương dạt 50% hiệu quả tối đa
dối vởi tế bảo M'1`4 nhiễm HIV- 1/11113 trong nghiên cứu in vitro lả 4 nglmL.
Ilâp thu
Không có dạng bảo chế ctravhin dùng lhco dường tĩnh mạch, do dó sinh khả dụng luyệt
đối của IN 1 FLENCE còn chưa duợc biết. Nồng dộ tối đa trong huyễt tương cùa clravĩrin
đạt dược lrong vòng 4 giờ sau khi uống cùng thức ăn. Ở các đối tượng khỏe mạnh, hắp thu
của ctravỉrin không bị ảnh hu~óng bới dùng phối hợp bằng dường uỏng vói ranitidin hoặc
omcprazol dược biếil ả các thuốc lảm tăng p1-1 dạ dảy.
Ảnh huởng của thửc an lên hẩp thu thuốc
Khả năng hấp lhu của ctravirin lá như nhau khi được uống sau bữa an chứa luợng caio tiêu
chuẩn binh thường (561 kcaI) hoặc bữa ăn gìảu năng lượng có chất béo cao (1160 kcai)
Khi so sảnh với cảch dùng sau bũa an chúa lưọng calo tỉêu chuẩn binh thuờng thì nồng độ
của ctravírin bị giảm khi dùng ctravirin trước bữa ăn có số calọ bình lhường (17%), sau khi
ăn bánh sừng bỏ (20%), hoặci 1'1c đói (51%). Do đó, để có nồng độ tối ưu, [NTELENCE
cằn phải dược uống ngay sau bũa ăn.
Phân bô
Etravirin gắn khoảng 99, 9% vảo protcin huyết tương, chủ yếu gắn với albumin (99,6%) vả
011 —acid glycoprotein (97, 66%- 99 ,02%) ỉn vitro. Việc phân bố của ctravirin vảo trong các
dịch lòng khảc huyết tương (như dịch nâo tùy, các dịch tiết đường sinh dục) chưa duợc
dảnh giá ở ngưòi.
Chuy ~ễn hỏa
Các thử nghiệm in vitro với các microsom gan người (HLM) ch1 ra rằng ctravirin chủ yếu
chuyến hóa qua phản ửng oxy hóa bằng hệ cytochrom P450 (CYP) 3A gan và bằng hệ
CYP2C ở phạm vi nhỏ hơn sau khi bị glucuronyl hóa.
Dản thải
Sau khi dùng 1 liồu gắn phóng xạ 14C- clravirín, có khoảng 93, 7% vả 1,2% cùa liều dùng
' C…ctravirỉn bị thải qua phân vả nước tiếu lương ứng. Lượng ctravirin không bị chuyển
hóa lả lù 81 1,2% dển 86,4% của liễu dùng theo phân. Không phảt hiện được ctravirin không
chuyền hóa trong nước tiều. '1hời gian bán thải cuỏi cùng cùa ctravỉrin lả khoảng
30— 40 giờ.
Page 21 of 24
Pi lnlelenfe 100771g 2Mng_CCDS 10.11m201 5_vi
Các đối tương dăc biêt
N~guơi giả
Phân tỉch dược dộng học trên những bệnh nhân nhỉễm HIV cho thấy dược dộng học cùa
ctravirỉn không khác biệt đảng kế ở khoảng tuốỉ (l 8- 77 tuốỉ) (xem ’lhỏng Iin lâm sảng —
Liều dùng vả cách dùng vò Cảnh báo vả thận lrọng).
Giới tính
Không thắy có sự khác biệt về dược dộng học gỉũa nam và nữ. Số lượng bệnh nhân nữ
Lham gĩa lrong nghìên cứu lả hạn chế.
Chủng Iõc
Phân tích dược dộng học quần thể cùa ctravirín lrẽn những bệnh nhân bị nhiễm HIV chỉ ra
rằng chùng tộc nguời không ảnh hưởng một cách rõ rảng dến nồng dộ ctravỉrỉn.
Suy Ilzận
Chưa tìến hảnh nghỉẽn cứu dược động học của ctravỉrịn ở những bệnh nhân suy lhận.
Những kết quả cùa thử nghiệm cân bằng khối lượng với MC-ctravỉrỉn phóng xạ chỉ ra rằng
<1,2% cùa liều dùng ctravirĩn dược đảo thải qua nước tỉểu Không phát hỉện đuợc thuốc
không chuyến hóa trong nuớc liều do dó ảnh huởng cùa tôn thương thận lên đảo thảí
clravỉrin coi như là tối thỉều. Như dã bỉềt ctravỉrỉn gắn chủ yếu vảo protein huyết tương,
nên không chắc rằng thuốc được loại trừ đáng kế bằng lọc mảu hoặc thẫm phân phúc mạc
(xem Thõng tin lâm sảng — Liều dùng vò cách dùng và Cânh báo và lhận Irọng).
Suy gan
I’ỉtravirỉn dược chuyển hóa vả đảo thải chú yểu qua gan Trong nghiên cứu so sảnh 8 bệnh
nhân suy gan nhẹ (Chìld- Pugh mức A) với 8 bệnh nhân dối chứng tương ứng và 8 bệnh
nhân suy gan Lrung bình vởỉ 8 dối chứng tương ứng (Child- -Pugh mức 8), đặc tính cùa
dược dộng học đa ĩỉễu của ctravỉrỉn lá không thay đổi ở những bệnh nhân suy gan nhẹ dễn
Lrung binh. Không yêu cầu dìều chinh liều o~ nhũng bệnh nhân suy gan nhẹ dến trung bình.
IN [ lỉLlỉNClỉ khỏng dược nghiên cứu ở nhũng bệnh nhân suy gan nặng. (Child- -Pugh mức
C) (xem ! `hóng Iz'n !âm .sảng L rêu dùng và cách dùng và Cảnh báo và lhận lrẹmg).
Dồng nkiễm virus vỉẽm gan B vă/hoặc virus viêm gan C
Phân tích dược dộng học quần thê cùa cảc thừ nghỉệm DUET- ] vả DUET-2 chỉ ra rằng
giảm dộ thanh thải cùa IN l` EU NCE ở cảc bệnh nhân bị nhỉễm HIV- ] có đổng nhỉễm vói
virus viêm gan B vả/hoặc vìrus viêm gan C. Dựa trên dữ liệu an toản (xem I'hông lin Iam
.sảng - I`ác dụng không mong muốn), không cần thỉổt diều chỉnh liều ở những bệnh nhân bị
dồng nhỉễm vói virus viêm gan B vả/h0ặc C.
I’hụ nữ có Ihm'
Phụ nữ có Ihar' và sau khi sính
Nồng dộ clravirỉn toản phần sau khi uống lN’I`ELENCE 200 mg x 2 lần/ngảy như một
phần của pháo dỗ đỉều lrị kháng virus nhìn chung cao hơn ở phụ nữ mang thai so với phụ
nữ sau khi sỉnh (xem Bảng bên dưới). Nồng dộ etravirỉn không gắn kết ít có sự khảo biệt
hơn.
ó những phụ nữ dùng INTELENCE 200 mg x 2 lẩn/ngảy, dã thấy các giá trị lrung bình
cao hơn cúa Cmax_ AUCIzh vả C…… ở phụ nữ mang thai so với sau khi sinh. Các gỉá trị trung
bình cùa các thông số nảy lả tương tự trong 3 tháng giữa vả 3 tháng cuối cùa thai kỳ.
Page 22 ul'Z4
Pl lnlelence IOUmg_ẽfflìmgg ("CDS lOJun20/í v)
Các kễt quả dược động học cũa etravirin toân phần sau khi dùng etravỉrin 200 mg x 2
Iầnlngây như một phẩn của phảc đồ điều trị kháng retruvirus, trong 3 tháng giữa của
thai kì, 3 thảng cuối của thai kì, và sau khi sinh.
Dược dộng học của ctraviẮn 200 mg ctravirin 200 mg ctravirin 200 mg x 2
ctravirin (trung bình x 2 lằn/ngây x 2 lầnlngây 1ần/ngùy
iSI), Lrung vị) sau sỉnh quí 2 thai kỳ quí 3 thai kỳ
N 10 13 10a
Cm-m, ng/m1. 269 i 182 383 i 210 349 d: 103
284 346 371
Cmax, ng/mL 569 L 261 774 i 300 785 :L: 238
528 828 694
AUCI2IL, h*ng/mL 5004 d: 2521 6617 1- 2766 6846 i 1482
5246 6836 6028
“ n=9 của AUCLzh
Mỗi cá Lhế dược sư dụng như một dối chứng cùa chính họ, và dưọc so sánh vởi chính
mình, các giả lrị Cmin, Cmax vả AUC…Ì loản phần của cưavirin Iẳn lượt cao hơn 1,2, 1,4 và
1,4 lần, , Lrong 3 Lhảng giũa cùa Lhai kì so với sau khi sỉnh và lần lưọ1 cao hơn 1,1, 1,4 vả
1,2 lằn, trong 3 lháng cuối của thai kì khi so với sau khi sinh.
THÔNG TIN TIỂN LÂM SÀNG
Cảo nghĩẽn cứu độc tính ở dộng vật được Liễn hảnh với ctravirin trẻn chuột nhắt, chuột
cống, Lhỏ vả chó O chuột nhắt, cơ quan đích duợc xác định lá gan và hệ thống dông mảu
Bệnh xuất huyết cơ tim chỉ quan sát thấy ở chuột nhắt dực và dược coi là Lhứ phát cùa bệnh
dõng mảu nặng gíán Liếp qua dường vitamin K. Diều nảy không tương Lhích với nguời. Ở
chuột cổng, cơ quan dích Lhcn chốt là gan, Luyển gỉáp và hệ Lhống dông ngảu. Phơi nhỉễm ở
chuột nhắt lả Lương dương với phoi nhiễm ở người, Lr0ng khi ở chuột cống phoi nhiễm là
Lhấp hơn mức phoi nhỉễm lâm sảng ở liều khuyến cáo. 0 chó, quan sải thẳy những Lhay dối
Lrong gan vả LL'Li mật ở múc Iphơi nhỉễm cao hon khoảng 8 lẫn so với mức phoi nhiễm ở
người Lhấy dược ở Iỉồu khuyến cảo (200 mg x 2 lẩn/ngảy).
Trong nghiên cứu Liễn hảnh Lrên chuột cống, không Lhấy có ảnh hưởng gì tởỉ sự gỉao hợp
vả sinh sản khi dùng 1N' [ ELENCIỉ diểu Lrị lên tới 500 mglkg/ngảy vả mửc dộ phơi nhiễm
Lương duơng vởi múc phơi nhỉễm trên người ở liều lâm sảng khuyến cáo. Không thấy có
dộc Linh sính quải Lhai do clravirin ở chuột công (1000 mg/kg) vả Lhó (375 mg/kg) tại mức
phơi nhiễm Lương duơng với múc phơi nhiễm quan sát Lhẩy 0 người khi dùng liểu lâm sảng
khưyến cáo 'l`rong dánh giá phát Lriền trưởo vả sau sinh ở chuột công, ctravỉrỉn không ảnh
hưòng dẻn sự phát Lriến của chuột con Lrong giai đoạn tạo sữa hoặc sau khi cai sủa khi
chuột mẹ dược dùng liêu dến 500 mg/kg vả ở mức phơi nhiễm lương dương vởi mức phơi
nhiễm quan sát dưọc ở liếư lâm sảng khuyến cáo.
Etravỉrin dược đảnh giá khả năng gây ung Lhư bằng cách đưa vảo đạ dảy của chuột nhắt và
chuột cống vòi thởi gian lên đến 104 Luẳn. Liều hảng ngảy là 50,200 và 400 mg/kg cho
chuột nhắt và 70 200 vả 600111g/kg cho chuột công Etravirin không gây ung Lhư cho
chuột cống và chuột nhắt dực. "Iỷ lệ u Luyến tế bảo gan và ung Lhu~ biểu mô Lăng ở chuột
nhắt cái. Dùng etravirỉn không lảm tăng tỷ lệ có ý nghĩa Lhống kê dối với bất kỳ khối u
lảnh hay ác Lính nảo ở chuột nhắt hoặc chuột cống Nhưng phát hiên trong tế bảo gan ở
chuột cải dược coi lả dặc trưng cho loải gặm nhấm, liên quan dến cảm ứng cùa mcn trong
gan và ít Lương Lhích với nguời. Ở lỉểu cao nhất, phơi nhiễm toản thân(dụa theo AUC) doi
Page 23 of 24
W Ắnlrlem~c iũl)mq 200mg f`(`DS HULJnJWJ`J/
a
1
/Í
với chavirin là 0, 6 lần (ở chuột nhắt) vả từ 0, 2 đển 0 7 lần (chuột cống), liên quan đến
phơi nhiễm quan sảL Lhấy ở người với liểu diều Lrị khuyến cáo (200 mg x 2 lầnlngảy).
Etravirin có kểt quả âm tính trong thử nghỉệm đột biến ngược Amcs in vilro, thử nghiệm
về sai lạc nhìễm sắc Lhể Lrong tế bảo lympho của người in vitro và thử nghiệm u lympho
Lrên chuột in vilro Lrong sự hiện diện hoặc không có hiến diện của hệ Lhống hoạt hóa
chuyền hóa. Etravirin không gây cảm ứng lâm hư hại Lhể nhỉễm sắc trong Lhử nghiệm vi
hạt nhân in vivo Lrên chuột nhắt.
HẠN DÙNG:
lntclcncc 200 mg: 2 năm kế từ ngảy sản xuất.
lntelcncc 100 mg: 2 năm kế từ ngây sản xuất.
DIẺU KIỆN BẤO QUẢN
Không bảo quản Lrên 300C.
Bảo quản Lrong lọ gốc. Dóng chặt nắp lọ để tránh ảm. Không vứt bỏ các tủi chống am.
Dễ xa tầm tay trẻ cm.
QUY CẢCII DÓNG GÓI
Intclcncc 200 mg: l-Iộp 1 lọ x 60 viên nén.
1ntclcncc 100 mg: llộp 1 lọ x 120 vỉên nén.
Sãn xuất Lại: JANSSEN CILAG S.P.A., Via C. Janssen (loc. Borgo S.Michelc) —
04100 Latina (LT), Ý. z
Phiên bản: CCDS 10 June 2015 v15. 0
I’I_Inlelence 100mg_ 200mg, CCIJS 10 June 2015
Ngảy sửa đồi: 21/08/2015
TUQ C_ỤC TRUỎNG
p TRUỒNG PHÒNG
-Ấfguyen JỔlgj Jfễềny
l’agc 24 01`24
P! Inlelem~e |lN'huỵ 200mg (`(`I)S IDJLJnZOI5 v]
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng