








"›.
Gemcitabina Actavis - Vial
_ ,, Gemcnsan
Ễ Mfsiịatlwẫ p A Gemcitabine Hydrochloride
z“ ActaVlsltalyy - ' ' ' eqv. to Gemcitabine 200mg
Lyophilisate powder for Solution for lnfusion
For intravenous infusion
LOT: XXXXX
EXP: DD/MMIYYYY
?
hss '4'7/ừ
\2ồ ' Ỹ\ễJ`\\ xẦ
Ắf/L/Ĩ ~ CT
Đọc kỹ hướn dẫn sư dụng Irươc khi dùng. Nếu cần thêm thông !in xỉn hỏi ý kíến bác sỹ. Để
thuốc ngoăỉ tam tay tre em. Thuốc nảy chỉ dùng theo đơn của bác sỹ.
GEMCISAN ,200 MG
Bộ! đông khô để pha tiêm truyền
Gemcitabine 200mg
Thânh phần:
Mỗi lọ có chứa:
- Hoạt chất: Gemcitabine Hydrochloride tương đương Gemcitabine 200mg
— Tá dược: Mannỉtol E421, Natri Aetate (t.đ. Natri Acetate trihydrate), Natri Hydroxide (t.đ dung dịch
IN).
Chỉ định đ'ều trị: ỢÌ/
GemcitabiỀầkẻt hợp với Cisplatin dược chỉ định điếu trị trong ung thư bảng quang giai đoạn tiển
triên tại ch oặc di căn. ' ' J ' _
Gemcitabine được chỉ định ở bệnh nhân ung thư carcinôm tuyên cùa tưyên tụy tiên triên tại chõ hay
di căn. /
Gemcitabine, kết hợp với Cisplatin, được chỉ định hảng đầu trong điếu trị ung thư phổi tế bảo không
nhỏ tiển triến tại chỗ hoặc di căn Đơn trị liệu Gemcitabine có thể dùng cho người cao tuổi /’
Gemcitabine được chỉ định kết hợp với carboplatin trong điếu trị carcinôm biều mô buồng trứng tiến
triến tại chỗ hoặc di cãn, ở bệnh nhân bị tải phảt ít nhất 6 thảng sau khi hóa trị liệu hảng đầu bằng /
platinum.
Gemcitabine, kêt hợp với paclitaxel, chỉ định cho bệnh nhân ung thư Vũ không thế phẫu thuật được,
tải phát tại chỗ hoặc di cản sau khi hóa trị liệu hỗ trợ/tân hô trợ. Nến hóa trị liệu trước đó băng
anthracycline trừ khi chống chỉ định. ,
Liều lượng và cách dùng:
Gemcitabine chi được kê toa do bảo sỹ ohuyên về hóa trị liệu ung thư.
Liều lượng khuyến cáo:
Ung thư bãng quang:
- Dùng kết họp: Liều khuyến cảo gemcitabine 1000 mg/mz, 2truyền 30 phút; truyền vảo ảy thứ 1, 8,
và 15 mỗi chu kỳ 28 ngảy, kểt hợp với cisplatin 70 mg/m2 truyền vảo Ngảy thứ 1 sạũjgemoitabine
hay Ngảy thứ 2 trong chu kỳ nảy. Sau đó lập lại chu kỳ 4 tuần nảy. Dựa trên mức độ độc tính trên
bệnh nhân, có thế giảm liều mỗi hay trong một ohu kỳ.
Ung thư tụy: Liều khuyến cảo gemcitabine 1000 mg/mz, tru ến 30 phút, 1 lần/1 tuần trong 7 tuần, rồi
ngưng ] tuan. Nhưng chu kỳ sau dó 1 lần/1 tuần trong 3 tuan liên tiếp nhau, ngưng ] tuân. Dựa trên
mức độ độc tính, có thế gỉảm liếu mỗi hay trong một ohu kỳ
Ung thưphỗỉ tế bâo không nhỏ:
- Đơn trị liệu: Liều khuyến cáo gemcitabine 1000 mglm², truyền 30 phút, 1 lầnll tuần trong 3 tuần,
rồi ngưng ] tuần. Lập lại chu kỳ sau đó. Dựa trên mức độ độc tính, có thể giảm liều mỗi hay trong
một chu kỳ.
~ Trị liệu kết họp. Liều khuyến cáo gemcitabine 1250 mg/m2, truyền . t’vạc`Ù thứ 2 và 8
cùa chu kỳ 21 ngảy. Dựa trên mức độ độc tính, có thế giảm liều mỗi h Ý ffliiỡtềhuắẵ\
Cìsplatin liếu từ 75— 100 mg/m2 3 tuần một lần. ' CO PHÁN
Ung thư vú Dược PHÂM ..
- T r: liệu kết họp Khuyến cảo kết hợp Gemcitabine với paclitaxelzz ifẩầiố Nffl5 Ìfinz) truyền
tĩnh mạch 3 giờ vảo ngảy thư ], tiếp đến là gemcitabine (1250 mg/m2 ) HỊp H-gịặchf'3O phủt vảo
1
_“ ỵ0300Ặ
ticihx
Ngảy thứ 1 vả 8 trong chu kỳ 21 ngả_y Dựa trên mức độ độc tinh, có thế giảm lỉếu mỗi hay trong một
ohu kỳ Lượng bạch cầu hạt tuyệt đối phải tối thiếu lả 1500 (x lOÓ/I) trước khi bắt đằu điếu trị phối
hợp nảy.
Ung lhư buõ_ng trứng:
- Trị Iiệu két họp: Khuyến cáo kết hợp Gemcitabine với carboplatin Gemcitabine 1000 mg/m²,
truyền 30 phủt vảo Ngảy thứ [ vả 8 của chu kỳ 21 ngảy Tiếp dển [ả carboplatìn vảo ngảy thứ 1 tương
ứng với Diện tích dưới đường cong (AUC) mục tiêu [ả 4, 0 mg/ml phủt Dựa trên mức dộ độc tính, có
thể giảm liếu mỗi hay trong một chu kỳ.
Theo dõi để phát hỉện độc tính vả đìều chĩnh liều:
- Điếu chmh liều do độc tmh khong phải huyết học: Nên khám lâm sảng định kỳ vả kiềm tra chức
nãng gan- thận để phảt hiện độc tinh không p_hải huyết học. Dụa trên mức độ độc tinh, có thế giảm
liều mỗi hay trong một chu kỳ. Nhin chưng, đối với độc tính nặng khõng phải huyết học (độ 3 hay 4),
ngoại trừ buồn nôn/ói, nên giảm hay ngưng gemcitabine tùy theo đánh giá cùa bảo sỹ điều trị, và
ngưng đến khi không còn độc tính.
Xin tham khảo mục Tóm tắt những đặc điếm oủa sản phẩm cùa císplatin, carboplatin, vả paclitaxel
khi điếu chinh [iếu trong điều trị kết hợp.
- Điều chinh Iiếu do độc tỉnh h_uyết hoc:
+ Khời đầu chu kỳ: Đối vởi tất cả ohỉ định, trước mỗi chu kỳ đếu phải theo dõi 1ượng tiếu cằn và
bạch cầu hạt. Lượng bạch cằn hạt tuyệt đối phải tối thiếu là 1.500 (x lOÓ/I) tiếu câu lả 100 000 (x
+ Trong 1 chu igy: Đỉếu chỉnh liếu gemcitabine trogmỗi chu kỳ nên dựa theo bảng dưới đâv:
106/1) trước khi bắt đầu mỗi chu kỳ.
fầiều chỉnh liễu gemcitabine trong 1 chu kỳ đổi với ung thư bảng quang, ung thư phổi
tế bảo không nhỏ, và ung thư tụy, đơn trị hay kết hợp với cỉsplatin
Lượng bạch cầu hạt tuyệt đối Lượng tiễu cầu Phần trăm liểu chuẩn
(x 10°J1) (x 1000 của gemcitabine (%)
› 1.000 vả › 100.000 100
500-1.000 hay 50.000100000 75
<…500 hay < 50.000 Bò liếu *
* Không đỉêu trị iại trong một chu kỳ trước khi lượng bạch cẳu hạt tuyệt đối đạt tối thiêu là 500
(xlOỐ/l) vả tiếu cầu là 50.000 (x106/1)
Điếu chỉnh liều gemcitabine trong 1 chu kỳ đối vởi ung thư vú, đỉều trị kết hợp với
cisplatin
Lượng bạch cầu hạt tuyệt đối Lượng tiễu cầu Phần trăm liều chuẩn
(x mỏm (x 10611) của gemcitabine (%)
z 1.200 và >7s.000 100
1.000- <1.200 hay 50.00075000 75
700- <1.000 và 2 50.000 so
<700 hay 1.500 và ì 100.000 100
1000-1.500 hay 75.000-100.000 50
<1000 hay < 75. 000 Bò liều*
* Không điều trị lại trong một chu kỳ Sẽ bắt đâu đỉếu trị vảo Ngảy ] của ohu kỳ kế tỉếp khi lượng
bạch câu hạt tuyệt đối đạt tỏi thiếu là 500 (xloóli) và tiến cằn là 50.000 (x106/ 1)
— Điều chmh Iíều do độc zinh huyết học lrong nhưng chu kỳ điều trị tiếp theo sau. đối với Iẩl cả chi
đinh:
Nên giảm ]iếu gemcitabinđ còn 75% so với liều dùng trong chu kỳ ban đầu. trong các trường hợp
độc tính huyết học sau dây:
- Lượng bạch cầu hạt tuyệt đối < 500 x 106/1 trên 5 ngảy.
Lượng bạch cầu hạt tuyệt đổi < 100 x 106/1 trên 3 ngảy.
Giảm bạch cầu có sốt. _
- Tiêu cằu < 25.000 x lO°fl.
Hoãn đợt điếu trị > 1 tuần do độc tinh
Cách dùng: Thuốc được dung nạp tốt trong lúc truyền và người bệnh có thế đi iạì Nếu có thoảt
mạch, phải ngưng truyền ngay và bắt đầu truy ến ở ] tĩnh mạch khảo. Nên theo dõi kỷ sau khi truyền.
Nhóm bệnh nhân đặc bỉệt:
- Bệnh nhán suy thận hay suy gan: Nên dùng Gemcitabine thận trọng Ở những bệnh nhân nảy do
không đủ thông tin từ nguyên cứu lâm sảng dể xác định rõ liều khuyến cáo.
- Người cao luối (>_65 Iuối). Gemcitabine được dung nạp tốt ở bệnh nhãn > 65 tuối Không cần điếu
chinh liếu ngoải liếu đã được khuyến cảo vì chưa có bằng chứng.
- Trẻ em (<181uố1'): Khỏng khuyến cảo dùng Gemcitabine cho trẻ em < 18 tuổi do khõng đủ dữ liệu
về mức độ an toản và hiệu quả.
Chống chỉ định: qì/
Quá mẫn với hoạt chẩt hay tả dược
Đang cho con bú (xem mục Thai kỳ vả giai doạn tạo sữa)
Cảnh báo đặc biệt và thận trọng khi dùng:
Kéo dải thời gia_n truyền và tẩn suât dùng _tăng đều lảm tãng độc tính.
- Độc tinh huyết học: Gemcitabine có thề ức chế chức năng tủy xương, được biền hỉện với sự giảm
bạch cầu, tiến câu vả thiếu mảu. Nên theo dõi lượng tiếu câu, bạch câu vả bạch cầu hạt trước mỗi liếu
dùng. Khi phát hiện suy tùy do thuốc, nên hoãn lại hay thay đồi iiếu. (xem mục Liều dùng vả Cảch
d_ùng) Tuy nhiên suy tùy chi trong thời gian ngắn vả thường không cẩn giảm hay ngưng lìếu Lượng
tế bảo mảu ngoại biên có thế tỉếp tục giảm sau khi ngưng gemcitabine. Thận trọng khi bắt đầu điều trị
ở bệnh nhân suy tùy Giống như cảc thuốc gây độc tế bảo khảo, phải cân nhắc nguy cơ suy tùy do tích
liếu khi điểu trị kết hợp
- Suy gan. Truyến gemcitabine ở bệnh nhân ung thư gan thứ phảt, hay tiến sử viêm gan, nghiện rượu,
hoặc xơ gan có thề lảm trâm trọng thêm tinh trạng suy gan săn có. Nên thực hiện định lý việc đảnh
giả cận Iảm sảng chức năng gan, thận (gốm test vi rút học). Nên dùng Gemcitabine thận trọng ở
những bệnh nhân nảy do không đủ thỏng tin từ nguyên cứu lâm sảng để xác định rõ liếu khuyến cảo.
(xem mục Liều dùng vả Cách dùng) i…eooị Ể\
— Xạ trị đồng thời: Xạ trị đồng thời (cùng lủc hay cảch 57 ngảy): lỉ)ặliif nhận -đỆC :,tính (xem mục
Tương tảo với cảc thuốc khảo và cảc dạng tương tảo). Wr CONG TY 4ễỵ\
- Tỉẻm chủng. Không khuyến cáo tiêm chủng sôi vản_g da vả cảc va_ elhe lfflằỡ’ờễaẸnii nhân được điều
trị với gemcitabine. _(xem mục Tương tảo với cảc thuốc khảo và cảci ng ỄWớiỸịtặềichảẻ')j
- Tim mạch. Phải rất thặn trọng khi dùng gemcitabine ở bệnh nhân c\ .hệRfflSừ ỀẾ1Ểi mặch do nguy oơ
gây rối loạn tim- -mạch \Ĩ\s 4146 Hồ ỡĩ
\ợ/ 3
- Phối: Đã ghi nhận những ảnh hưởng lên phối, đôi khi ở mức nghiêm trọng (như phù phối, viêm
phối mô kẽ, hay hội chứng suy hô hâp cấp người lớn). Chưa rõ nguyên nhân. Nên cân nhắc việc
ngưng thuốc khi có những ảnh hưởng trên. Áp dụng sớm biện phảp điều trị nâng đỡ gỉúp cải thiện
tình trạng _nảy.
- Thận. Rất ít ghi nhận biếu hiện lâm sảng tương ứng với hội chứng urea huyết tản huyết ở _bệnh nhân
dùng gemcitabine. Nên ngưng ngay khi có những dân hiệu đầu tiên cứa thiếu mảu tán huyết vi mạch,
như tăng bilirubin, creatinine huyết thanh, tăng BUN, hay LDH. Suy thận có thế không hồi phục khi
ngưng thuốc, và cần chạy thận nhân tạo.
- Kha năng sinh sán. Trong oảc nghiên cứu về khả năng sinh sản, gemcitabine đã gây giảm lượng
tinh trùng ở chuột đực. Vì thế, nam giới _đang điều trị với gemcitabine không nên lảm cha trong suốt
thời gian và 6 tháng sau điếu trị, và có thế cân hướng dẫn việc bảo quản lạnh tinh trùng trước khi đỉều
trị do có thế bị vô sinh
- Natri:
+ Óng gemcitabine 200 mg chứa 3,56 mg (<1 mmol) natri.
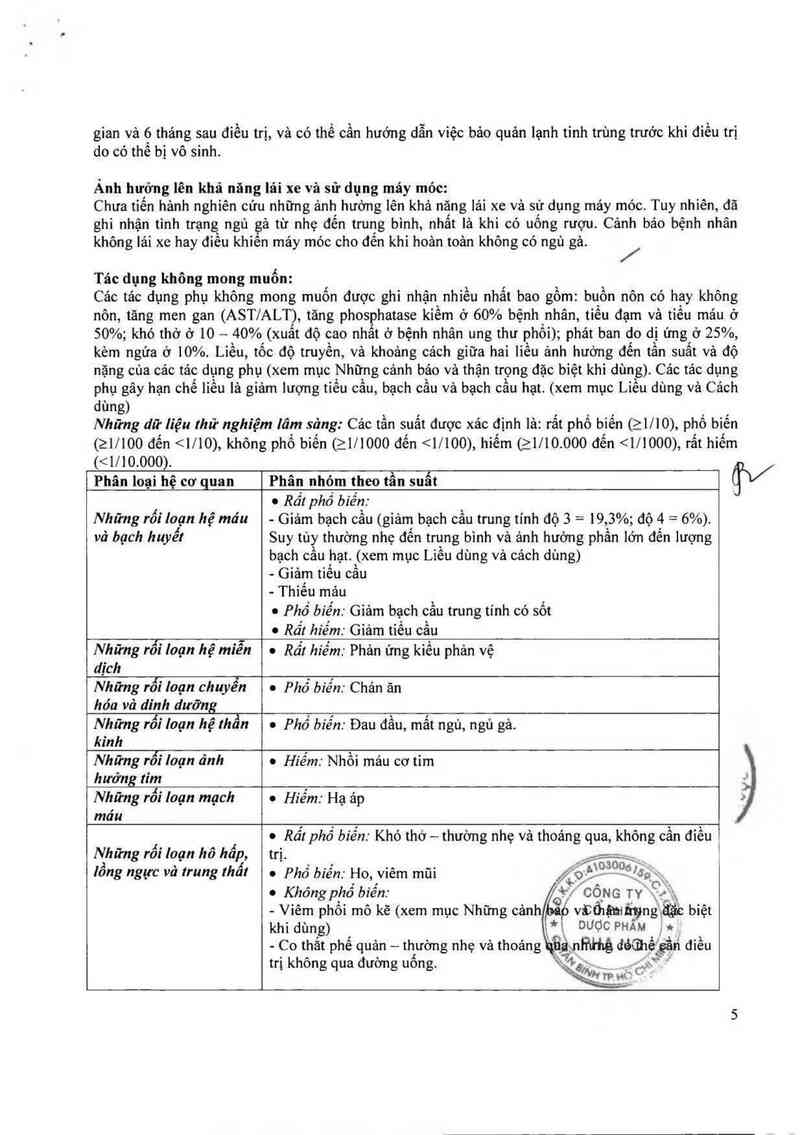
+ Óng gemcitabine lg chứa 17,81 mg (1/10) phổ biến
(21/100 đến <1/10), không phổ biến (21/1000 đến <1/100), hiếm (21/10. 000 đến <1/1000), rất hiếm
(<1/ 10 000)
Phân loại hệ cơ quan Phân nhỏm theo tần suất Ộ/
0 Rất phổ bìến:
Những rối 10an hệ máu - Giảm bạch cẳu (giảm bạch cầu trung tính dộ 3 = 19,3%; độ 4 = 6%).
vả bạch huyết Suy tủy thuờng nhẹ đến trung bình vả ảnh hướng phần lớn đến lượng
bạch cầu hạt. (xem mục Liều dùng và cảoh dùng)
~ Giảm tiều cầu
- Thiếu mảu
0 Phố biển: Giảm bạch cầu trung tính có sốt
. Rất hiếm: Giảm tiểu cầu
Những rôĩloạn hệ mỉễn . Rất hiếm: Phản ứng kiểu phản vệ
dịch
Những rốĨ !oạn chuyển 0 Phổ biến: Chản ăn
hóa và dinh dưỡng
Những rối loạn hệ thẩn o Phổ biển: Đau đầu, mất ngù, ngủ gả.
kỉnh
Những rẫloạn ănh o Hiếm: Nhồi mảu cơ tim
hưởng tim
Những rối loạn mạch o Hiếm: Hạ áp
máu
. Rất phố bíến: Khó thớ … thường nhẹ và thoảng qua, không cẩn đỉều
Những rối !oạn hô hấp, trị. '
, . /"
lồng ngực vả trung thất o Phó biên: Ho, viêm mũi Ẩọ M°~"°°O 13
o Khóng phố biển: 0* CÔNG TY-
- Viêm phôi mô kẽ (xom mục Những cảnh vả2Ổ:ậhtfiyng ủ biệt
khi dùng) * Dược PHẢM Jx
- Co thắt phế quản — thường nhẹ và thoảng Ềẩ .nffl'hậ dỏffl'iếgâfi điếu
trị không qua đường uống. ,
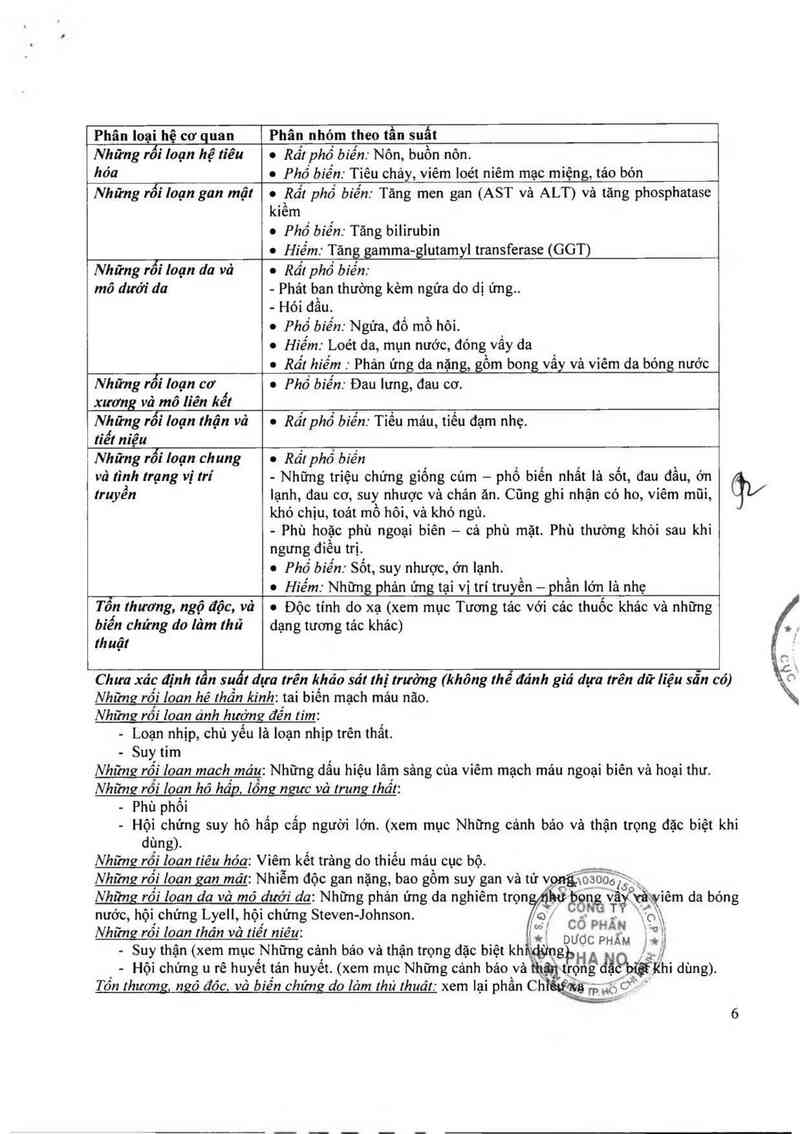
Phân Ioại hệ cơ quan
Phân nhỏm theo tần suất
Những rối !oạn hệ tỉêu
hóa
0 Râl phó biên: Nôn, buôn nôn.
0 Phó biên: Tiêu chảy, viêm Ioét niêm mạc mỉệng, tảo bón
Những rỗi loạn gan mật
0 Rất phổ biến: Tăng men gan (AST vả ALT) vả tãng phosphatase
kiềm
. Phổ biến: Tăng bỉlirubin
' Hiếm: Tảng gamma—glutamyl transferase (GGT)
Những rối loạn da vả
mô dưới da
0 Rất phổ biến:
— Phảt ban thường kèm ngứa do dị ứng..
- Hói đầu.
Phổ biến: Ngứa, đổ mồ hôi.
Hiếm: Loét da, mụn nước, đóng vấy da
Rất hiểm : Phản ứng da nặng, gồm bong_vẩy và viêm da bóng nước
Những rổỉ 10an cơ
xương vả mô Iỉên kết
Phổ biến: Đau lưng, đau cơ.
Những rỗi !oạn lhận vả
tiết niệu
o Rât phó biên: Tiêu máu, tỉêu đạm nhẹ.
Những rỗi loạn chung
và tình Irạng vị trí
truyền
0 Rất phổ biến
- Những triệu chửng giống cúm— phố bỉến nhất là sốt, đau đầu, ớn
lạnh, đau cơ, suy nhược vả chản ăn. Cũng ghi nhận có ho, viêm mũi,
khó chịu, toảt mồ hôi, vả khó ngù.
- Phù hoặc phủ ngoại biên — cả phù mặt. Phù thường khỏi sau khi
ngưng đỉều trị.
. Phổ biến: Sốt, suy nhược, ớn lạnh.
0 Hiếm: Nhữngphản ửng tại vị trí truyền —phần lớn lả nhẹ
ĩổn thương, ngộ độc, vả
biến chứng do Iảm thủ
Ih uậ!
o Độc tính do xạ (xem mục Tương tảo với cảc thuốc khác và những
dạng tương tảc khảo)
Chưa xác định tần suất dựa Irên khảo sát !hị trường (không 1hể đánh giá dựa Irên dữ liệu sẵn có)
Những rểí loan hé thần kinh: tai biến mạch máu não.
Những rỏi 10an ảnh hưởng đẻn tim:
- Loạn nhịp, chủ yêu là Ioạn nhịp trên thât.
- Suy tim
Những rối Ioan mach máu: Những dâu hiệu lâm sảng của viêm mạch mảu ngoại biên và hoại thư.
Những rỏi loan hô hảp. lỏng ngưc vả Irung thân
- Phù phổi
- Hội chứng suy hô hấp cấp người lớn. (xem mục Những cảnh báo vả thận trọng đặc biệt khi
dùng).
Những rót“ Ioan tíêu hóa: Viêm kểt trảng do thiếu mảu cục bộ.
Những rối loan gan mât: tNhiễm độc gan nặng, bao gổm suy gan và tử ỵoníosoool \ ,_
Những rổi Ioan da vả mỏ dưới da: Những phản ứng da nghiêm trọnĨìủễẵ'tìđỄVầẳ tầw\ìẻm da bóng
0
| I |
nước, hội chứng Lyell, hội chứng Steven-Johnson.
Những rỏí loan lhản vả tiết niẻu:
- Suy thận (xem mục Những cảnh bảo và thận trọng dặc bỉệt kh
- Hội chứng u rê huyết tản huyết. (xem mục Những cảnh bảo và
T on thương, ngỏ đóc. và biến chtmg do Iảm thu' Ihuât. xem lại phần Ch
có PHẨN `fỊ,`\
dằfg DƯÓCPHẢM n_l
n
` trọngAcịẳổỉầkhl dùng).
m_ ẸịịạỞ` '
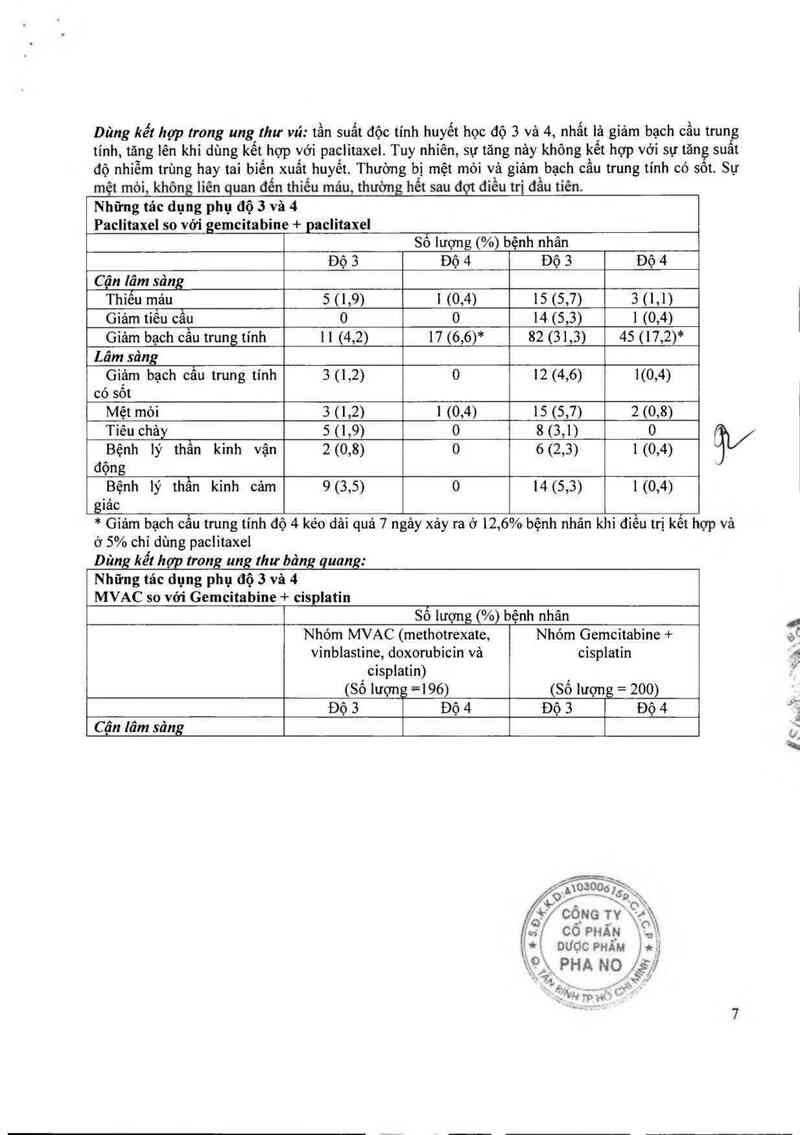
Dùng kết họp trong ung lhư vú: tần suất độc tính huyết học độ 3 và 4, nhất là gỉảm bạch cầu trung
tính, tăng lên khi dùng kết lhợp với paclitaxel. Tuy nhiên, sự tăng nảy không kết hợp với sự tăng suat
độ nhíễm trùng hay tai biến xuất huyết. Thường bị mệt mỏi và giảm bạch cầu trung tính có sôt. Sự
mệt mòi, không liên quan đến thiếu mảu, thường hết sau đợt diều trị đầu tiên.
Những tác dụng phụ độ 3 và 4
Paclitaxel so vởi gemcitabine + paclitaxel ,
Sô lượng (%) bệnh nhân
Độ 3 Độ 4 Độ 3 Độ 4
Cận lâm sâng
Thiểu máu 5 (1,9) 1 (0,4) 15 (5,7) 3 (1,1)
Gỉảm tiểu cầu 0 0 14 (5,3) 1 (0,4)
Giảm bạch cẫu trung tính 1 1 (4,2) 17 (6,6)* 82 (31,3) 45 ( 17,2)*
Lâm sảng
Giảm bạch cầu trung tính 3 (1,2) 0 12 (4,6) 1(0,4)
có sốt
Mệt mòỉ 3 (1,2) 1 (0,4) 15 (5,7) 2 (0,8)
Tiêu chảy 5 (1,9) 0 8 (3,1) 0
Bệnh lý thẫn kình vặn 2 (0,8) 0 6 (2,3) 1 (0,4)
động
Bệnh lý thần kính cảm 9 (3,5) 0 14 (5,3) 1 (0,4)
gnac
* Giảm bạch cầu trung tính độ 4 kéo dải quả 7 ngảy xảy ra ở 12,6% bệnh nhân khi diển trị kết hợp và
ở 5% chỉ dùng paclitaxel
Dùng kết họp trong ung thư bâng quang:
Những tác dụng phụ độ 3 và 4
MVAC so với Gemcitabine + cisplatin
sả lượng (%) bệnh nhân
Nhóm MVAC (methotrexate,
Nhóm Gemcitabine +
vỉnblastine, doxorubỉcin vả cỉsplatin
cisplatin)
(Số lượng =196) (Số lượng = 200)
Độ 3 Độ 4 Độ 3 Độ 4
Cận lâm sảng
;
/+ CÓNG TY~o
íS/ICOPHAN \2)
*( DƯỢCPHÂM ,
)DỊ PHA NO /ắÍ
; ,____ .
Ỉ~le'vw`b
®V
"cm
I.CÍL…I'Ĩ
Thiếu máu 30 (16) 4 (2) 47 (24) 7 (4)
Giảm tiểu cầu 15 (8) 25 (13) 57 (29) 57 (29)
Lâm sảng
Buổn nôn vả ói 37 (19) 3 (2) 44 (22) 0 (0)
Tiêu chảy 15 (8) 1 (1) 6 (3) o (0)
Nhiễm trùng 19 (10) 10 (5) 4 (2) 1 (1)
Viêm niêm mạc miệng 34 (18) 8 (4) 2 (1) 0 (O)
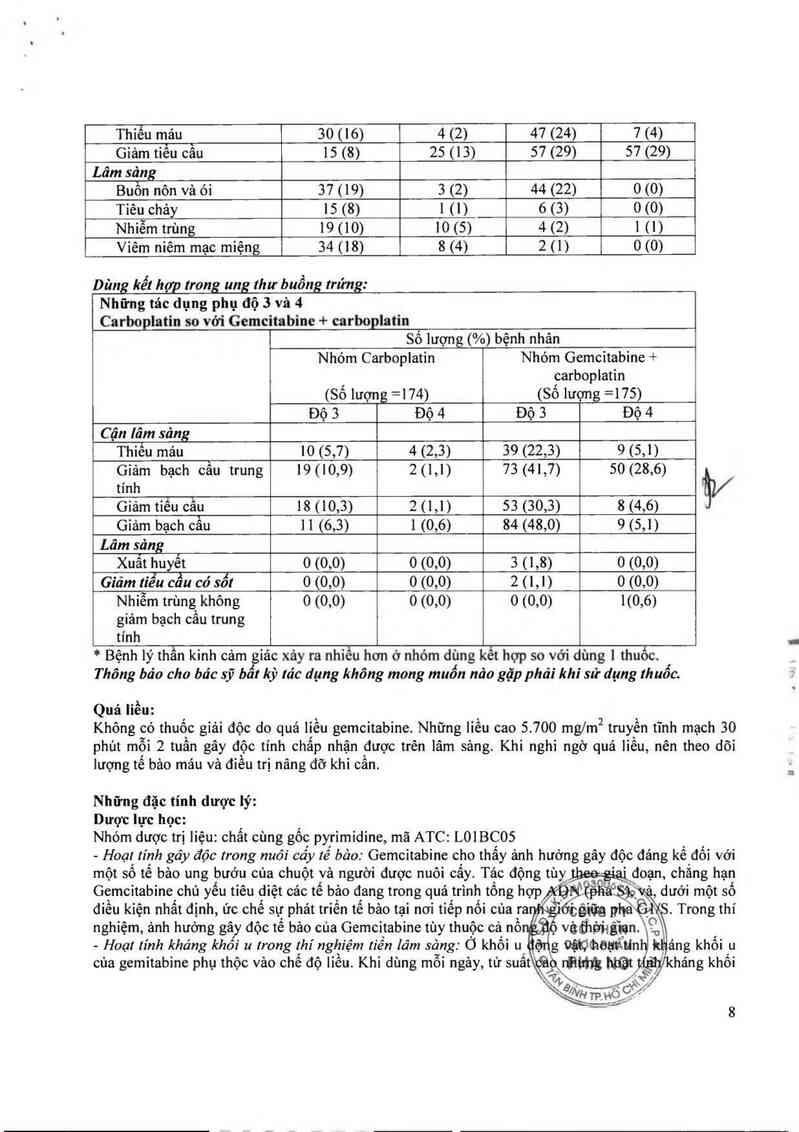
Dùng kết họp trong ung thư buồng trứng:
Những tác dụng phụ độ 3 và 4
Carboplatin so vởi Gemcitabine + carboplatin
Số lượng (%) bệnh nhân
Nhóm Carboplatin Nhóm Gemcitabine +
carboplatin
(Số lượng =174) (Số lượng =175)
Độ 3 Độ 4 Độ 3 Độ 4
Cận lâm sảng
ThĨêu mảu 10 (5,7) 4 (2,3) 39 (22,3) 9 (5,1)
Giảm bạch cầu trung 19 (10,9) 2 (1 ,1) 73 (41,7) 50 (28,6) qy
tính
Giảm tỉêu cầu 18 (10,3) 2 (1,1) 53 (30,3) 8 (4,6)
Giảm bạch cầu 11 (6,3) 1 (0,6) 84 (48,0) 9 (5,1)
Lâm sảng
Xuất huyết 0 (0,0) 0 (0,0) 3 (1,8) 0 (0,0)
Giảm tiểu cẩu có số! 0 (0,0) 0 (0,0) 2 (1,1) 0 (0,0)
Nhiễm trùng không 0 (0,0) 0 (0,0) 0 (0,0) 1(0,6)
giảm bạch cầu trung
tính
* Bệnh lý thẫn kình cảm giác xảy ra nhiều hơn ở nhóm dùng kểt hợp so vởi dùng 1 thuốc.
Thông bảo cho bác sỹ bất kỳ tác dụng không moug muốn nảo gặp phải khi sử dụng thuốc.
Quả liều: ` `
Không có thuôc giải độc do quá liếu gemcitabine Những liêu cao 5.700 mg/m2 truyền tĩnh mạch 30
phủt mỗi 2 tuần gây độc tính chấp nhận được trên lâm sảng. Khi nghi ngờ quá liều, nên theo dõi
lượng tế bảo máu và điều trị nâng đỡ khi cần.
Những đặc tính dược lý:
Dược lực học:
Nhóm dược trị liệu: chất cùng gốc pyrimidine, mã ATC: LO] BCOS
- Hoạt lính gảy độc trong nuôi căy lế bảo. Gemcitabine cho thấy ảnh hưởng gây độc đảng kể đối với
một số tế bảo ung bướu của chuột và người được nuôi cấy Tảc động tùy Mđoạn, chẳng hạn
Gemcitabine chủ yểu tiêu diệt các tế bảo đang trong quá trình tống hợp ` ,dưới một số
điểu kiện nhất định, ức chế sự phảt triển tế bảo tại nơi tìếp nối của ra .Trong thí
nghiệm, ảnh hưởng gây độc tế bảo của Gemcitabine tùy thuộc cả nổ
- Hoạt tính kháng khối u trong thí nghiệm riền lăm sảng: Ớ khối u ang khối u
của gemitabine phụ thộc vảo chế độ liếu. Khi dùng mỗi ngảy, từ suất khảng kh01
u thì rắt nhò. Tuy nhiên, nếu dùng liếu không gây từ vong cách 3 hay 4 ngảy, gemcitabine có hoạt
tính khảng đảng kể nhiều loại 11 ở chuột.
(` ơ chế tác dụng Chuyến hóa tế bảo và cơ chế tảo dụng: Gemcitabine (dFdC), một chắt chống
chuyển hóa pyrimidine, được chuyến hóa nội bảo bới nucleoside kinase thảnh các nucleosides hoạt
hóa là diphosphate (dFdCDP) vả triphosphate (dFdCTP). Ảnh hướng gây độc của gemcitabine lả do
sự ức chế tồng hợp ADN do hai cơ chế tảc dỤng cùa dFdCDP vả dFdCTP Đầu tiên, dFdCDP ức chế
ribonucleotỉdc reductase, men duy nhất xúc tảo cho phản ứng tạo ra
deoxynucleoside triphosphates (dCTP) cho sự tống hợp ADN Sự ức chế nảy lảm giảm nồng độ
deoxynucleosides nói chung, và dặc biệt là dCTP Thứ hai, dFdCTP cạnh tranh với dCTP vê sự kết
nhập với ADN. Tương tự, một lượng nhỏ gemcitabine cũng có thế kết nhập với ARN Vì thế nồng
độ dCTP nội bảo giảm tạo điều kiện cho dFdCTP kết nhập vảo ADN. ADN polymerase epsilon
không có khả năng thải Ioại gemcitabine vả chỉnh sừa mạch ADN dang kéo dải. Sau khi gemcitabine
kết nhập vảo ADN, có thêm ] nucleotide gắn vảo mạch ADN nảy. Sau đó, chủ yếu sẽ có sự ức chế
hoản toản trong việc tống hợp thêm ADN (kết mã chuỗi giả). Sau khi kết nhập vảo ADN,
gemcitabine có thể tạo ra sự chết tế bảo theo chương trình
Các dữ liệu [âm sảng:
- IUng thư bâng quang Một nghiến cứu Pha III ngẫu nhiên ở 405 bệnh nhân ung thư bỉếu mô đường
niệu tiến triên hay di căn không cho thẳy sự khảc biệt giưa hai nhỏm điếu trị: gemcitabine/cisplatìn so
với methotrexate/vỉnblastine/adriamycin/cisplatin (MVAC), về thời gian sổng trung bình (iần lượt là
12,8 và 14,8 thảng; p=0,547), thời gian đến khi bệnh tiến triến (lần lượt là 12,8 vả 14,8 thảng;
p=0,547), vả ti 1ệ đảp ứng (lần lượt lả 49,4% và 45,7%; p=0,512). Tuy nhiên, gemcitabine + cisplatin
gây độc tính thấp hơn MVAC.
- Ung thư tụy. Một nghiên cứu Pha 111 ngẫu nhiên ở 126 bệnh nhân ung thư tụy tiến triến hay di căn
cho thấy gemcitabine có đảp ứng thuận lợi lâm sảng cao hon dáng kế sọ với 5- fiuoroumcil (lẩn lư01
là 23,8% và 4,8%; p— —0 ,.0022) Cũng quan sảt thấy sự kéo dải đảng kể về mặt thống kê cùa thời gìan
đến khi bệnh tiến trỉến lả từ 0,9 đến 2,3 tháng (log- -rank p ụg/ml trong
vòng 30 hút sau khi kết thủc truyên, vả > 0,4 11ng trong 1 giờ sau đó.
Phân bốp Thể tich phân bố ở trung tâm là 12,4 l/m2 đối với nữ vả 17,5 l/m2 2đối với nam (độ biến
thiên giữa cảc cả nhân là 91 ,.9%) Thể tích phân bố ở ngoại biên lả 47, 4 I/m². Thể tích nảy không
nhạy với giới tinh. Gắn kểt với protein huyết tương được cho lá không đảng kề
Thời gian bản hủy: Thời gian nây dao động từ 42— 94 phủt tùy theo tuổi và giới tính. Đối với chế độ
liểu đã được khuyến cảo, thời gian bản hủy hấu như hoản tât trong 5 — 11 giờ khi bắt đầu truyền.
Gemcitabine không tích liều khi dùng 1 lẩn/ 1 tuần.
Chuyển hóa: Gemcitabine được chuyến hóa nhanh bới cytidine deaminase trong gan, thận, máu vả
các mô khác. Chuyến hóa ở nội bảo tạo ra mono, di vả triphosphate gemcitabine (dFdCMP, dFdCDP
vả dFdCTP), trong đó dFdCDP vả dFdCTP được cho là có hoạt tính. Không phát hiện các chắt
chuyền hóa nội bảo nảy trong huyết tương hạy nước tiều. Chất chuyền hóa chính lả 2' deoxy 2', 2'
difiuorouridine (dFdU) thi không có hoạt tính vả dược tim thắy trong huyết tươnzg và nước tiếu.
Thải trừ: độ thanh thải toản cơ thể biến thiên từ 29, 2 llgiờ/m2 đến 92, 2 /giờ/m2 tùy tuổi và giới tính
(độ biến thiên giữa cảc cả nhân là 52,2%). Độ thanh thải ở nữ khoảng 25%, thấp hơn ở nam. Dù
nhanh, nhưng độ thanh thải giảm theo tuổi ở cả hai giới. Với liếu khuyến cảo 1000 mglm2 truyền 30
phủt, khi giảm độ thanh thải thi không nhất thiết phải giảm liếu.
- Bải tỉết qua nước tìểu: < 10% dưới dạng không đối.
- Thanh thải ở thận 1ả 2 đến 7 I/giờ/m2
Suốt 1 tuần sau truyền, 92 đến 98% liều dùng được thải qua nước tiếu. 99% liếu dùng được bâi tiết
trong nước tiểu chủ yêu ở dạng dFdU và 1% trong phân.
— Dược động cúa dFdCTP: Chất chuyền hóa nảy có thể tim thấy trong bạch cầu đơn nhân ở mảu
ngoại biên như thông tin dưới đây: nông đó nội bảo tăng tỉ lệ với liếu từ 35 dến 350 mg/m²/3O phút,
tạo nông độ ỏn đinh là 0, 4- 5 ụg/ml. Ở nông độ gemcitabine huyết tương > 5 ụg/ml, nông độ dFdCTP
không tăng, cho thẩy mức bão hòa nội bảo.
- Dược động của dFdU. Nồng độ đinh huyết tương lả 28- 52 ụg/ml (3 — 15 phủt sau khi kết thúc
truyền 1000 mglm²/3O phút). Nồng độ đáy sau khi truyền 1 lần/1 tuần là 0,07 1,12 ụg/ml, không có
tích liều. Đường cong nồng độ huyết tương theo thời gian 3 pha, thời gian bản thải trung bình của pha
cuối là 65 giờ (trong khoảng từ 33 đến 84 I/m2 )
Tạo thảnh dFdU từ hợp chất mẹ: 91% -98%.
Thế tich phân bố trung bình ở ngăn trung tâm: 18 l/m2 (trong khoảng từ 1 1- ỮIũỄEUÓJỔ
Thế tich phận bố trung bình ở trạng thải on định (Vss): 150 l/m2 (trong kiẢẫgẵấ -22847mỉ ).
Sự phân phối ở mô: rộng khắp o 00 PHÂN ) .
Thanh thải biều kiến trung bình: 2, 5 l/giờ/m2 (trong khoảng từ 1-4 l/giờ/ Iaí. DƯOC PHẨM 1
Bải tiết qua nước tiếu: tất cả \_ọ \ ỆH OÍè
Điều trị Gemcitabine + paclitaxel. Điều trị kết hợp nảy không lảm t $Ĩ,đot ượcO cùa mỗi
thUốC ớiNHrpm" Ce
v
~k
I
10
W
Đỉều trị Gemcitabine + carboplatin: Dùng kết hợp không lâm thay đổi dược động của gemcitabine
Suy thận: Dược động của gemcitabine không bị ảnh hưởng đáng kể trong suy thận nhẹ đển trung
binh (GFR từ 30 ml/phủt đến 80 mI/phút)
Tương kỵ:
Không được hòa lẫn gemcitabine với cảc thuốc khác.
Bão quản:
Bảo quản dưới 30°C.
Dung dịch pha th uốc:
Tính ổn định hóa- lý trong lúc đang dùng được minh chứng trong 24 giờ ở nhiệt độ 25°C. Theo quan
điếm vi sinh học, nên dùng ngay sản phẫm. Nếu không dùng ngay, thời gian và điếu kiện lưu trữ
trước khi dùng là trách nhiệm ở phía người sử dụng. Không nên trữ lạnh dung dịch gemcitabine vi có
thẻ kêt tinh.
Những thận trọng đặc biệt cho việc loại bỏ và xử lý khác:
Xử lý: Phải theo dõi độ an toản đối với cảc thuốc kìm tế bảo trong khi chuẩn bị vả loại bỏ dung dịch
truyền. Nên tiến hảnh xử lý dịch truyền trong phòng an toản, dùng' ao choáng vả găng tay bảo vệ. Nếu
không có phòng an toản, nến nên mang mặt nạ vả kiếng mắt
Nếu dịch truyền chạm vảo mắt, có thế bị kích ứng nặng. Nên rửa mắt ngay và ký bằng nước. Nên
khám bảc sỹ nêu vẫn còn kích ứng Rửa thật kỹ bằng nước khi dung dịch nhỏ trên da.
Những hướng dẫn cho việc pha thuốc (vả pha !oãng thêm): Dung môi duy nhất được công nhận
cho việc hòa tan bột gemcitabine vô khuấn đế truyên lả chiorua natri 9 mg/ml (0, 9%) (không có chất
báo quản). Nồng dộ tôi đa của gemcitabine lủc hòa tan lả 40 mglml khi xem xét dộ hòa tan. Pha thuốc
ở nồng độ > 40 mglml có thể dẫn đển sự tan không hoản toản, và cân trảnh điều nảy.
Phải ảp dụng kỹ thuật vô khuẩn trong 1ủc pha thuốc và pha loãng gemcitabine dề truyền tĩnh mạch
1. Để pha thuốc, hãy cho thêm thể tích thích hợp của chlorua natri 9 mglml (0, 9%), không có chắt
bảo quản (như bảffl dưới đây) vả lắc để hòa tan:
Dạng đóng gói Thể tích chlorua natri Tổng thể tích sau khi Nồng độ sau cùng
0,9% (không có chất pha
bảo quản) dế thêm vảo
200 mg 5 ml 5,26 ml 38 mng
1 g 25 ml 26,3 ml 38 mglml
2 g 50 ml 52,6 ml 38 mglml
Có thể pha loãng thêm nữa với chlorua natri 9 mglml (0.9 %), không chât bảo quản. Dung dịch đã
pha lả ] dung dịch trong, không mảu hay mảu vảng nhạt.
2. Trước khi dùng, nên quan sảt kỹ những thuốc tiêm truyền để phảt hiện chất lạ hay sự đổi mảu.
Không sử dụng khi phảt hiện chất lạ. Thuốc không dùng hay chất thải, nên dược loại bỏ theo các qui
định tại địa phương.
Hạn dùng: 36 thảng kế từ ngảy sản xuất.
Tiêu chuẩn chẩt lượng: Nhà sản xuất %
Đóng gói: Hộp 1 lọ.
Sản xuất bởi: Actavis Italy S. P. A. 1 ' "Y“ '
Via L Pasteur, 10 20014 New1an(M.fgno) It—.
O
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng