









H ) ) ỹt’ó'Ìỷ
.,A
v,go g/tiM
A
I
.,
AN LÝ DƯỢC
ỘYTỂ
B
CỤP QỤ
ĐA`PHẺ DUY
ẸT
Lẩu Jáu:.ffl.J....Qỉ/……A*
\v
o—A
£6EừOO
í llllllllllllllllll
I 90% Actual Size
Store In the original container.
Dunu:As dìrectud by the physician.
NOT T0 EXGEED PRESCRIBED DOSAGE
KEEP OUT OF THE REAGH AND SIGHT
OF CHILDREN.
lndlutlons, Wlminus & Prucutlumz
Read tho packaoe leaflet betore use.
Chaque comprlmé pelliculé contlsnt:
Emlrìcuablna 200 mg
Fumarale de lènotuvir dlsopmxil 300 mg
À consawerả une tempénture ne
dépassant pas 30'C
À consemr dans !“ emballaqu d“ origine
Pmloulo: Cornme dirigé par votre
mủecin.
NE FA5 DẺPASSER LA DOSE PRESCRITE.
TENIR HORS DF. LA PORTÉE ET DE LA VUE
DES ENFANTs,
lllchlinu. MI… ou nardn It Priuutlons:
Lim la notice avant utillsation.
Emiricitabinefỉenoiovir
Disoproxil Fumarate
Tablets
200 mg/3OO mg
30 Tablets
Emtricitabine/Fumarate
de Ténolovir Disnproxil
Cumprimés
ẨẤ/LULU/pp :01eo 'dxg
MmeJpp IOIECI 'ỒJW . * . @—
I'ON 101 |ỰOỊEG , " Ặ'
; ĩ>
» ở '
'7 V
t 0
m 3”
RI- Thuộc ki m Nón hi
…
@ MYỈGIÌ www.mylan.com Each illm coaled iahlai contains: @ Mylan www.mylan.com Emtrlclubinnnnnd 'l'lnofẵvưbhopmxll
Emiriciiahine 201] mg Mum: Tnbht: 200 mg! mo mg
Tenofovir dlsnpronl Iumarale 300 mg ’ểẵưậẵằw 200 m
DO not store above 30°0. Ịgtơtovir Dilopmxl íummt 300 mg
cm dlnh. chóng chl đntl lìủ dùng vi dc
thông tin khlc mm 400 tù huớno dln nừ dung
00y cúch đóng uòi: Hdp 1 lọ 30 viOn
SỐ 16 SX NSX. HD. XIm "BMI Loi Nb.'. Mía
Dnto' vi Em Dlta' trln 000 bì
Blo quln duới 30°C. Giữ Ihuóc ưnnn blo hl
Sln xult bòi lylln leontorhl lettcd
F-4 & F- 12. moc. Mnlulon. TI. Stnnlr
Nuhik czz … Mchnrumn suu. An 00
ĐI ›… tìm uy trỏ om
Dục Itỹ hướng dln tù dụng trưởc ml dùng
200 mg/3UD mg
…—
edZule
30 Gomprimés
DNNN:
I 904093l 000054'
Mfg Lic. Noi Lic, Fnb.No.z
ffll
Mylan
ma by:! Fun plr
Mylnn Laboratorles Limited
F-4 & F-12. MIDC. Mcloqnm … Snnu
Nnnk cm 10. Mmmntu suu, hdil
\—
ỉ Ìf04933
/
@th %Mi WzịQw
\
u » … …… ut.u…nụ… Ệfl]llllhll q … WWE
EanHolJt-uư zM …; “ mylamum
m rer i› ự_ riMmum: JNJW_
Dn … su: uhm: acrr. M il … le cmmuu. Wg. Dlte: dde
Dnugu:An éuưud bylìu chlln
Nmmtm iusmưm msmr.
ưEF nưror n…s mưu mu Gnưtfruu mm
lndlowm. Wunlnulheamlms
n…“ n ;ukaụ …… bu… …
f>~~m…wwr-Mưw um
L …… ::……)
………… wu… i ẹf…~. t uli … .;
A :omemri umlzlnpullummủsanl
pn lửf› A m…uc &… lbmbuluqe dwulro.
hminlnxmm: dlflgl nlrntr: médecin … _, ah pc
NEPAS ưnssm A umrmwr Ê Schedute 2 pp UĨỊ] Ẹltm ……LW .
m
ủũlte:ddhnmtyy
Wu.lJr. NuLlc fib. No.- mam
7500439²
mua nms DE lel'Et ET DS IAWL DB IIMS.
Inmuzlnng Mlm In pldo ưnlnnllou: .
….l…………u… 30Tabletstompnmés
Thuốc nảỵ chỉ dùng theo đơn của thầv thuốc Ĩ( E 1
`“ỵzv ẢL lổ j
VIÊN NÉN BAO PHIM '. Ềsf…fĩịạp
EMTRICITABINE AND TENOFOVIR DISOPROXIL ' '
FUMARATE TABLETS 200 mg 300 mg
Thảnh phần:
Mỗi vìên nén bao phìm chứa:
Emtricitabin ..................................... 200mg
Tenofovir disoproxil fumarat ............ 300mg
Tá dươc: Cellulose vi tinh thê, Natri Croscarmellose, Lactose Monohydrat, Magnesỉum Stearat,
Opadry Blue.
ĐẶC TÍNH DƯỢC LỰC HỌC
Cơ chế iác dung vờ hiệu lực dược lực học. Emtricitabin là một đồng dẳng nucleoside thuộc
nhóm cytidin. Trong co thế, tenofovir disoproxil fumarat đuợc chuyển thảnh tenofovir, một đồng
đẳng nucleosid monophosphat (nucleotid) của adenosin monophosphat. Cả cmtricitabin vả
tenofovir đều có hoạt tính đặc hiện đối với virus gây suy giảm miễn dịch ở người (HiV-i vả
HlV-2) vả virus viêm gan B. Emtricitabin vả tenofovỉr dược phosphoryl hóa bới cảc enzym trong
tế bảo để tạo thảnh emtricitabìn triphosphat vả tenofovir diphosphat. Các nghỉên cứu in virro chi
ra rằng cả emtricitabin vả tenofovỉr đến có thể bị phosphoryl hóa hoản toản khi dùng kết họp với
nhau trong tế bảo. Emtricitabin triphosphat vả tenofovir diphosphat ức chế cạnh tranh men sao
chép ngược HlV-i, lảm kết thúc chuỗi DNA.
Cả cmtricitabin triphosphat vả tcnofovir diphosphat đều là chất ức chế yếu đối với polymerase
DNA của động vật có vú và không có dấu hỉệư độc tính đối với ty thế cả ín vilro và in vivo.
Iloạt tính kháng virus in vitro: Hoạt tính hiệp đồng kháng virus đã được thấy dối với viên kết
hợp emtrìcitabỉne vả tenofovìr in vìno. Đã thấy có hiệu 1ch cộng hoặc hiệp đồng trong các
nghiên cứu phối hợp thuốc vói các thuốc ức chế pLotease vả vói các thuốc ức chế men sao chép
ngược HIV nucleosid vả non- -nucleosiđ.
Kháng ihuốc: Tinh kháng thuốc đã được quan sát thấy in vilro vả trên một số bệnh nhân nhiễm
HIV-l do có sự xuất hiện đột bỉến Mi84V/l vói emtricỉtahin vả K65R với tenofovir. Không xác
định được nguyên nhân nảo khác gây kháng emtricitabin vả tenofovir. Các virus kháng
emtricítabine có mang đột biến Mi84V/i cũng đề kháng chéo vói lamivudine, nhưng vẫn duy tri
độ nhạy cảm với didanosin, stavudin, tenofovir, zalcitabin vả zidovudin. Đột biến K65R cũng có
thề dược chọn lọc vói abacavir didanosin hoặc zaicỉtabin vả lảm giảm nhạy cảm vói các thuốc
như lamivudin, emhicitabin vả tenofovir. Tránh dùng tenofovir disoproxil fumarat cho nhũng
bệnh nhân nhiễm chùng HIV- I có mang đột biến K65R.
Nhũng bệnh nhân bị nhiễm HlV- ] có ba đột biển liên quan đến các đồng đằng thymidin (IAMS)
hoặc nhiều hon bao gồm đột biến hoặc M4IL hoặc LZIOW tiên men sao chép ngược thế hiện
giảm nhạy cảm với tenofovir disoproxil fumarat.
Kinh nghìệm lá… sảng: Trong một nghiên cứu lâm sảng ngẫu nhiên mở (GS-Ol-O34), những
bệnh nhân nhiễm l-liV-l chưa sử dụng thuốc kháng retrovirus dùng hoặc chế dộ mỗi ngảy một
lẩn emtricitabin, tenofovir dis0proxil fumarate vả efavirenz (n=255) hoặc một sự kết hợp cố định
iamivudin vả zidovudin (Combivir) được dùng hai iần mỗi ngảy vả efavirenz mỗi ngảy một lần
(n=254). Những bệnh nhân trong nhóm emtricitabin vả tenofovir disoproxil fumarate được cho
dùng thuốc nén emtricitabin/tenofovir disoproxil fumarat vả efavirenz tù tuần 96 đến tuần l44
Tại đuờng chuân các nhóm ngẫu nhiên có HIV- ] RNA huyết tưon ng …th gian tưong đồng (5. Ọ2
và 5.00 log]O bản sao/ml) vả lLLợLig CD4 (233 và 241 tế bảo/mm) Đ.iếm cuôỉ hiệu quả so cấp
của nghiên cứu nảy lả đạt dược vả duy trì nông độ HIV- ] RNA < ›400 bản sao/ml nên 48 tuần.
Hiệu quả thứ cấp phân tich trên 144 tuần bao gồm tỷ lệ bệnh nhân có nồng độ HiV-I RNA < 400
hoặc < 50 bản sao/ml, và thay đối từ đường chuẩn ở lượng tế bảo CD4.
Dữ lỉệLL về điềm cuối sơ cấp 48 tuần cho thấy rằng sự kết hợp của cmtricitabin, tenofovir
disoproxil fumarat vả efavirenz có tác dụng kháng vỉrus cao hơn khi so sánh vởi sự kết hợp cố
Trang lllO
W
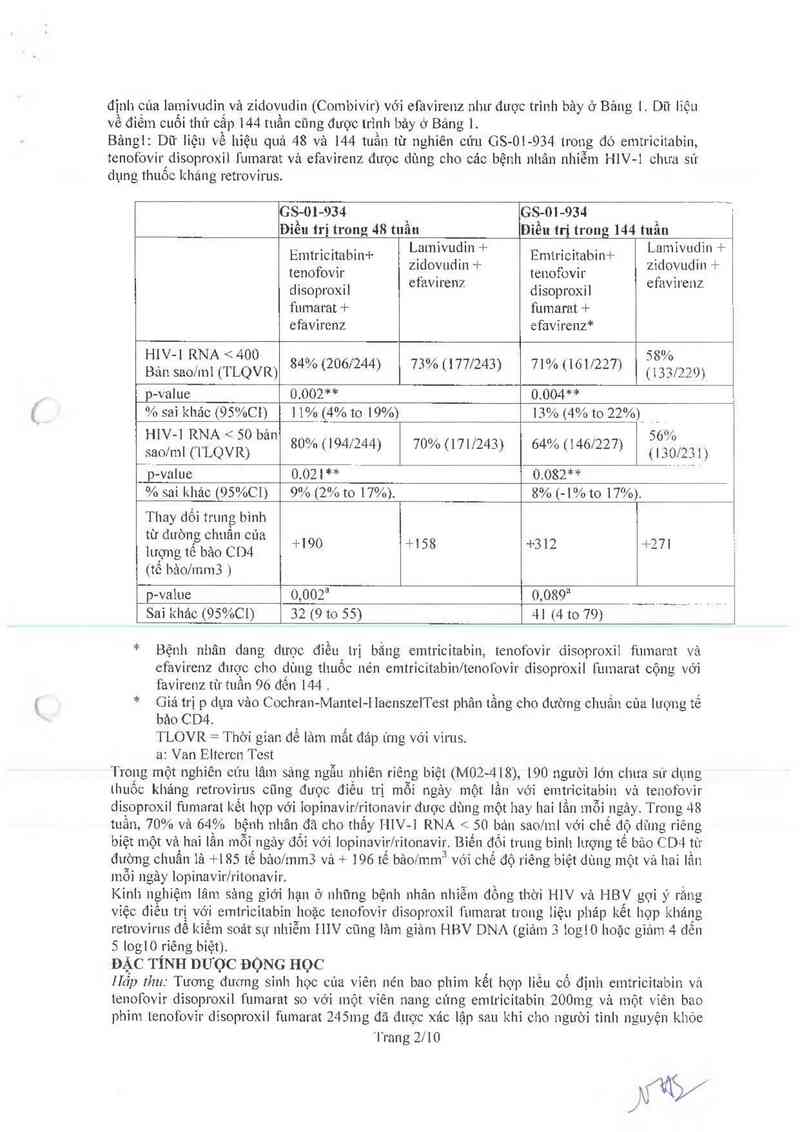
định cùa lamivudin vả zidovudin (Combivir) với efavhenz nhu đuọc trinh bảy ở Bảng 1 Dũ lìệLL
về điềm cuối thủ cấp 144 tLLầLL cũng đuợc trình bảy ớ Bảng 1.
Bảngl: Dữ liệu vê hiệu quả 48 và 144 tuần từ nghiên cún GS- 01- 934 tlong đỏ emUìcitabin,
tenofovh disoploxil fumzuat vả efavirenz đưọc dùng cho các bệnh nhân nhiễm HIV- 1 chua sủ
đung thuốc kháng LetLovilus.
GS-Oi-934 _ GS-Ol-934 _
Điều trị trong 48 tuân Điều trị trong 144 tuân
Emtricitabin+ L.amwqu + Emtrỉcitabin+ L_amwuc_hn +
. ZLdOVLLdLLL + . _ Zid0Vlidll] +
tenofovư . . tenofovn _ .
. _ . etavưenz . _ _. efavưenz
dlSOptOXll d]SOplOMÌ
fumarat + fumarat +
efavirenz cfavirenz*
HIV-l RNA < 400 0 o o 58%
Bản sao/mi (TLQVR) 84/o (206/244) 73 Ấ) (177/243) 71 /o (161/227) (133/220)
p-value 0.002** 0.004**
% sai khác (95%C1) ] 1%__(_4%10 19%) 13% (4% to 22°z_8 _ __
HIV-l RNA < 50 bản 0, 0. o . 56%
sao/ml (’l`LQVR) 80 /0 (194/244) 70 /0 (171/243) 64Á› (146/227) (|30/231)
p-value 0.02 1 ** . 0.082**
% sai khảo (95%C1) 9% (2% to 17%). 8% (-1% to 17%).
Thay dối trưng bình
từ đường chuân của
. ơ
1Lrợng tê bảo CD4 HỌO +158 +312 +—7l
(tê bảO/mmẵ )
p-vaiue 0,002a 0,089a __ __ __ _
Sai khác (95%C1) 32 (9 to 55) 41 (4 to 79)
* Bệnh nhân đang đuợc đỉềLL trị bằng emhicitabin tenofovir disoproxil fLLLnaLat vả
efavirenz được cho dùng thuốc nén emtricitabin/tenofovh disoproxil Í`LLLLLLLLLLt cộng với
favhenz tư tuần 96 đến 144
*
Giá trị p dựa vảo Cochran- ManteI—ilaenszeiTest phân tầng cho đường chuẩn của lượng tế
bảo CD4.
TLOVR = Thời gian để lảm mất đáp ửng vói vìrus.
a: Van Eltcmn Tcst
Trong một nghiên cửu lâm sảng ngẫu nhiên riêng biệt (M02-418), 190 người lớn chưa sư dụng
thuốc khảng LctLoviLus cưng đuọc điều trị môi ngảy một lần với em lC1tdblli vá tenofovh
disoproxil fumarat kết ILỌp với iopinavir/ritonavir được dùng một hay hai lần mỗi ngảy TLOLLg 48
tuần, 70% và 64% bệnh nhân đã cho thấy 111V- 1 RNA < 50 bản sao/ml vởi chế độ dùng LiêLLg
biệt một vả hai lằn mỗi ngảy đối với lopinavirhitonavh. Biến đoi trung binh lượng tế bảo CD— 1 tù
đường chuẩn là +185 tế bảolmm3 vả + 196 tế bảoz'3mm với chế độ Liêng biệt dùng môt và hai lằn
mỗi ngảy lopinavir/L' LLOLLaviL.
Kinh nghiệm lâm sảng giới hạn ỏ nhưng bệnh nhân nhiễm đồng thời HIV và HBV gợi ý Lằiig
vỉệc điều tLị vói emtricitabin hoặc tenoiovir disopxoxil fnmzuat trong 1iệu pháp kết họp kháng
rehovirus để kiếm soát sự nhiễm HIV cung Iảm gỉảm HBV DNA (giảmỆ 10g10 hoặc giảm 4 dến
5 log] O riêng biệt)
ĐẶC TÍNH DƯỢC ĐỌNG HỌC
lỉẩp thu: Tương đương sình học của vìên nén bao phim kểt hợp liều cố định emtricìtabin vả
tenofovir disoproxil fumamt so với một viên nang cứng emtric-itabin 200mg và một viên bao
phim tenofovir disoproxil fumarat 245mg đã được xác lập sau khi cho người tinh nguyện khóe
'l`rang 2/10
,WV
/
mạnh dùng liều duy nhất lúc đói. Sau khi cho người tinh nguyện khỏe mạnh uống viên kết hợp
liếu cố định emtricitabin vả tenofovỉr disoproxil fumarat, emtricitabin vả tenofovir disoproin
fumarat được hấp thu nhanh chóng và tenofovir disoproin fưmarat được chưyến thảnh tenofovir.
Nồng độ emtricitabin vả tenofovir tối đa đạt được trong huyết thanh từ 0,5 tới 3 giờ sau khi LLống
trong tình trạng đói. Uống viến kết hợp liếu cố định emtrìcitabin vả tenofovir disoproxil fưmarat
với thức ăn lảm chậm thời gian để đạt được nồng độ tối đa của tenofovir khoảng 45 phút vả lả…
tăng AUC vả CLnax cùa tenofovir _tLLOLLg ứng khoậng 35% và 15%, khi dùng kèm vói bũa ăn nhẹ
h_oặc nhỉều béo, so với uống thưốc IL'Lc dói. Đề tối LLLL hóa sự hẩp thu tenofovir, ngưòi ta khuyên
rằng nên Uống viên kểt hợp vói thức ăn.
Phân bố: Sau khi truyền tĩnh mạch, thể tích phân bố cùa emtricitabin vả tenofovir tương ửng lả
khoảng 1,4 l/kg và 800 mI/kg Sau khi uống emtricitabin hoặc tenofovir disoproxii fumarat
emtricitabin vả tenofovir được phân bố Lộng rãi trên khắp cơ thế. Trên ín vitr,o tỷ lệ emtricilabỉn
gắn kết với protein huyết tương người < 4% và độc lập với nồng độ tLong khoảng 0, 02 đến
2OOLLg/ml. Trên ín vilro, tỷ lệ tenofovir gắn kết với protein huyết tưong hoặc huyết thanh tương
ửng là dưới 0,7 và 7,2%, trong khoảng nồng độ tenofovir từ 0,01 — 25 LLg/ml.
Chuyến clạng sinh học: Hiền biết về quá trinh chưyến hoá của emtricitabin còn hạn chế. Chuyên
dạng sinh học của emtricitabin bao gồm quá trình oxy hoá nhóm Thiol tạo thảnh đồng phân lập
thể 3’-sulphoxid (khoảng 9% 1iều) và liên kết vởi acid glucuronìc để tạo thảnh 2’-O-glucuronid
(khoảng 4% liều). Cảo nghiến cứu in vina đã khẳng định rằng cả tenofovỉr disopmxil fumarnt
lẫn tenofovir đến không là cơ chắt của hệ enzym CYP4SO. Trong _quá tLình chuyến dạng sinh
học, cả emtricitabin vả tenofovir đều không ức chế quá trình chuyến hoá các thuốc tLLLLLg gian
qua bất kỳ đồng dạng nảo của CYP4SO người. Đồng thời emtricitabin cung không L'rc chế
Urìdỉne 5’-diphosphoglucuronyl transferase, lả enzym của quá trình Glucuronid hoá.
Thảí n~z`r.~ Emtricitabine được thải trừ chủ yếu qua thận, 86% trong nước tiếu, qua phân (khoảng
14%). 13% lìếu emtricìtabin trong nước tiếu là ba chất chưyến hoá. Dộ thanh thải của
emtricitabine trưng bình là 307…1/p11ủt. Sau khi uống, thời gian bán thải cúa emtricitabin khoảng
10 giờ. Tenofovir được thải trừ chủ yếu qua thận bằng cả con đường lọc ở cầu thận vả qua hệ
thống vận chuyển chủ động 0 ống thận, khoảng 70-80% liều truyền tĩnh mạch được bâi tiết qua
nước tiếu ciưới dạng không đổi. Độ thanh thải của tenofovir trung bình là 307ml/phút. Dộ t_hanh
thải của thận ước tính là khoảng 210 mi/phL'Lt, tốc độ thanh thải của tenofovir cao hơn nhiêu so
vởi tốc độ lọc ở cầu thận. Điều nảy chi ra rằng bâi tiết chủ động qua ống thận đóng vai trò quan
trọng trong quá trình thải trừ tenofovir. Thời gỉan bán thải của tenofovir sau khi uông lả khoáng
12 — 18 giờ.
Tuổi lác, giới tính vả chủng lộc: Dược động học của emtricitabin vả tenofovir là 11er nhau ở
nam, nữ. Nói chung, dược động học của emtricitabin ở trẻ sơ sinh, trẻ nhỏ và thỉếu nỉên (LLLỔi từ
4 tháng tới 18 tLLồi) là Lương đương với ở người lớn. Các nghiên cứu dược động học cưa
tenofovir chưa được thực hiện ở trẻ em và thiếu niên (dưới 18 Luổi). Các nghiên cứu dược động
học chưa được thực hiện vởi emtricitabin hoặc tenofovh ở người giả (trên 65 tLLồi)
Suy Lhận: Dược động học cua e_mtricitabin vả tcnofovir disochin fưmarat ở dạng bảo chế Liêng
rẽ hay dạng viên kết hỌp Iiếu cố định chưa được nghiên cứu trên bệnh nhân suy thận. Các chỉ sô
dược động học được xác định sau khi cho bệnh nhân không nhiễm HlV có các múc độ suy thận
khác nhau uống một 1iều đơn emtricitabin 200th hoặc tenofovir disoproin 24Smg. Mức độ sưy
thận được xác định dựa vảo độ thanh thải creatinin ban đầu (CLC!) (chức năng thận là bình
thường nếu chỉ số CLC] > 80mI/phủt; suy thận nhẹ nếu CLC! = 50-79 mllphủt; trung binh nếu
CLCI = 30-49 ml/phút và nặng nếu CLCI = 10-29 mI/phút).
Người ta khuyên rằng nến đìều chinh khoảng cách giữa các lần uống viên thuốc kết hợp liều cố
định emtrỉcitabin vả tenofovir disoproxil fumarat ở những bệnh nhân có độ thanh thải creatinin
từ 30 đến 49 mllphủt. Viên nén tenofovỉr vả Emtricitabin không thích hợp với những bệnh nhân
có độ thanh thải creatinin CrCl < 30 ml/phút hoặc nht_tng bệnh nhân cần thẩm tảch máu.
Suy gan: DLIỢC động học cùa thuôo kêt hợp liên có định emưỉcitabin vả tenofovh di_~sopmxỉl
fumarat chưa được nghiến cứu trên bện nhân suy gan. Tuy nhiên, hầu như không cần điều chinh
liều cho bệnh nhân suy gan.
Trang 3/10
W
Dược động học của cmtrìcitnhin chưa được nghiên cứu trên bệnh nhân không LLhiễm HBV nhưng
có tốn thương gan ở những mửc độ khác nhau. Nhìn chung, dược động học của cmtricitabin o~
bệnh nhân nhiễm HBV cũng tương tự như ở người khoẻ mạnh vả bệnh nhân nhiễm HIV.
Liều đơn tcnofovir dìsoproxỉi 245 mg được dùng cho các bệnh nhân không nhiễm H W có các
mức độ sưy gan khác nhau được xác định theo cảch phân loại Chỉld— Pưgh— 1` Lchoth (C PT). Duọc
động học của tenofovh thực chất không bị ảnh hưởng ở các đối tượng bị suy gan, điếu nảy gợi ý
Lăng không cần điếu chinh liếu ở các hệnh nhân nảy Các gỉá hị trung bình nông độ tenofovir
(%CV) szN và AUCụ.ao tương ủng 1ả 223 (34,8%) ng/mi và 2050 (50,8%) ng.giờlml ở nhưng
bệnh nhân chức nảng gan binh thường, so với 289 (46,0%) ng/ml và 2310 (43,5%) ng.giờ/mi 0
những bệnh nhân sưy gan mức độ trung bình và 305 (24,8%) LLg/LLLI và 2740 (44,0%) ng.gìờ/LLLI ở
những bệnh nhân suy gan nặng.
CHỈ ĐỊNH
Thưốc kết hợp iiếLL cố định cmtricitabin vả tcnofovir disoproxil fumarat dược chỉ định trong lỉệu
pháp kết hợp thuốc khảng rctrovirus cho người lớn bị nhiễm 1-11V-1 vả phối hợp vởỉ cảc thuốc
khảo theo hướng đẫn của Bộ Y Tế.
Sự khẳng định lợi ích của thuốc phối hợp emtricitabin vả tenofovir đisoproxil t`ưmamt trong điều
trị kháng Lctrovirus dựa chủ yếu vảo các nghiến cửu thực hiện tLếLL bệnh nhân chưa tùng điều trị
trước đó.
LIÊU LU ỢNG VÀ C_ÁCII DÙNG
Nên bắt đầu dùng thuốc theo chỉ định của bác sỹ có kinh nghìệm tL0ng điều uị nhiễm HIV.
Liền dùng.
Người lởn: Liếu_ khuyến các lá một viên, Uống ngây một lần. Dế tối ưu hóa sự hẩp thư của
tenofovir, nên uống viên kết hợp nảy cung với thưc ăn Thậm chí một lượng nhỏ thức ăn cũng
lảm tăng sự hấp thu cưa tcnofovir tư viến kết hợp.
Khi cân phải ngưng điều trị một trong hai thảnh phần của viên kết hợp hoặc khi cần điều chĩnh
liếư, nên sử dụng các chế phâm có chứa Liêng Lừng thảnh phần emtrỉcitabỉn vả tcnofovir
đisoproxil fumarat.
Nếu bệnh nhân quên một liều trong vòng 12 giờ, nên uống thưốc cùng với thức ăn cảng sớm
cảng tốt ngay khi nhớ ra và tiếp tục lịch trình LLống thuốc bình thường. Nếu bệnh nhân bỏ lỡ một
lỉều sau hơn 12 giờ và gần như tởí thời gian uống iiếư tìếp theo, không nên uống lỉều đã quên va)
chỉ cần tiếp tục lịch trình LLốLLg thưốc hình thường. Nếu bệnh nhân bị nôn trong vòng i gìò~ sau
khi uống thuốc, cần LLống thếm một liều khác.
T rẻ em vô vị Lhảnh niên: T ính an toản và hiệu quả của viên kểt hợp IiếLL cố định emtricìtahìn vả
tenofovir clisoproxii fưmarat chưa được khẳng định ở bệnh nhân đười 18 tLLồi. Do đó, không nên
dùn g viên kết hợp cho trẻ em Vả thiếu nìên.
Người giờ: Không có đủ dữ liệu để đưa ra khuyến cáo về liều dùng cho bệnh nhân trên 65 tLLồi.
Tuy nhiên, không cằn thiết phải điếu chinh liếu khưyến cáo cho người lớn trừ khi có bằng chưng
của tình trạng sưy thận.
Suy chức nãng thận: Các thông số hấp thu của cmtricitabin vả tcnofovir có thể tăng đáng kể khi
thuốc 6111Í1iffltabmfĩenof0VIl oỉsoproxil fummat được đùng cho các bệnh nhân bị suy thận vua
đến nghiếm _trọng do emt1ỉcitabin nnd tenofovir được loại hô chư yếu qua sự bải tiết ở thận.
DLL liệu giới hạn từ các nghiên cứu ủng hộ 1iếu dưng mỗi ngảy một lần tenot'ovir disoproxil
rllli1al'at với cmtricitabin ở cảc bệnh nhân bị suy thận nhẹ (thanh thải creatinin 50-80n11/phủt).
Cần điều chinh khoảng cách giữa các iiềư cùa thuốc cmtricitahinítcnofoviL~ disoproxil fưmnrat,
tuy nhỉẽn ở tất cả bệnh nhân bị sưy thận vừa phải (thanh thải creatinin giữa 30 vả 49LLLI/phút).
Các chỉ dẫn về điếu chỉnh khoảng cảch giữa các liếu cho nhóm nảy đưới đây được đựa vảo mô
hình cùa dữ liệu dộng dược học đơn liếư ở những đối tượng không bị nhiễm IIIV với các mức độ
suy thận khác nhau. Chưa có đũ' lìệư về tinh an toản và hiệu quả ò~ những bệnh nhân thải ìoạì
c-rcatinỉnc giữa 30 và 49ml/phủt được điều trị tenoi'ovir đisoproxíl fmnarat vói emtrỉcitabìn sư
dụng sự điều chỉnh khoảng cảch giữa liều nảy. Do đó, đáp L'Lng iâm sảng vởí việc diếư trị và chúc
năng thận nên được giảm sảt chặt chẽ ở những bệnh nhân nảy.
Trang 4/10
J(ỬỂÌ"V
Thanh thải Creatinin (mI/phút)*
50-80 30—49
Mỗi 24 giờ Mỗi 48 giờ
(không cần điếu chinh)
*Sử dụng thẻ Lrọng lý tưởng (gẫy) đã được ước lính
Không dùng viên kết hợp cho bệnh nhân suy thận rất nặng (có độ thanh thải creatinin < 30
mI/plnit) và ở những bệnh nhân phải thẩm tách máu vì không thế giảm liều viên kết họp cho phu
hợp với yêu cầu điều trị
Suy gan: Dưọc động học của viên kết hợp cũng như của emtricitabin cera được nghiên cứu ở
bệnh nhân suy gan. Dược động học cùa tenofovir đã được nghiên cứu ở những bệnh nhân suy
gan và không thẩy cần phải điếu chỉnh Iiếu cho những bệnh nhân nảy.
C ách dùng:
Nếu bệnh nhân khó nuốt, có thẻ phân tán viên kểt hợp trong khoảng 100 ml nước, nước cam
hoặc nước nho và uống ngay sau khi pha.
Khoảng cách giữa liều khuyên các
CHỐNG CHỈ ĐỊNH
Quá mẫn với emtricitabin, tenofovir, Lenofovir disoproxil fumarat hoặc bât cứ thảnh phân nảo
của thuôc.
NHỮNG KHUYẾN CÁO ĐẶC BIỆT VÀ THẬN TRỌNG KHI SỬ DỤNG
Không nên dùng viên kết hợp đồng thời với cảc thuốc khác có chứa emtricitabin, tenoiovh
disoproxil (dưới dạng fumarat) hoặc các đồng đẳng cytiđỉn khác, như lamivudin vả zalcitabin.
Líệu pháp kết hợp 3 nucleoside: Đã có bảo cáo về tỷ lệ thất bại cao trong đìều trị kháng virus và
xuất hiện chùng kháng thuốc vảo giai đoạn sóm khi tenofovir đisoproxii fumarat được kết hợp
với lamivudin vả abacavir cũng như vói Iamivudin vả didanosin trong phác đồ ngảy một lằn
Lamivudin vả emtricitabin có câu trúc Lất giống nhau vả hai chất nây cung có sư giông nhau về
dưọc động học và dược lực học. Do đó, có thể xuất hiện nhũng vấn đề giông nhau khi đưng viến
kểt hợp đồng thời với một thuốc tương tự nucleosid thứ ba.
Nhưng bệnh nhân đang diều tLi bằng viên kết hợp hoặc bất kỳ thuốc kháng L~~etroviLus nảo khác
vẫn có thể mắc nhiễm trùng cơ hội vả các biến chứng khác cùa nhiễm HIV. Vì vặy nhng bệnh
nhân nảy phải được theo đõi chặt chẽ bò1 các bác sỹ có kinh nghiệm trong điều trị bệnh nhân bị
bệnh có liên quan tới HIV.
Bệnh nhân phải được khuyên rằng, các liệu phảp kháng retrovirus kể cả viên kết hợp nảy, không
ngăn ngưa đuợc ngưy co lây trưyền HIV cho ngưới khác qua tiếp xúc tình duc hoặc trnyền máu.
Cân phải tiếp tục áp dụng các biện pháp phòng ngừa thích hợp.
Viên kết hợp có chứa iactose monohydrate. Vì vậy, những bệnh nhân bị cảc vấn để đi truyền
hiếm gặp như bất dung nạp galactose, thiếu men Lapp-iactase, hoặc kém hấp thu giuco-galactose
không nên dùng thuốc nảy.
Suy thận: Emtricitabin vả tenofovir dược thải trừ chủ yếu qua thận bằng cảch lọc ớ cầu thận kết
hợp vởi bải tiết chủ động qua ống thận. Các thông số hắp thu cùa emh icitabin vả tenofovir có thể
tăng đáng kể ở những bệnh nhân bị suy thận mức độ từ trung bình đến nặng. Do đó, cần phải
điểu chinh khoảng cách giữa cảc lần uống thuốc đối với nhưng bệnh nhân có độ thanh thải
meatinine tư 30 đến 49 mllphủt. Tính an toản và hiệu quả cùa tenofovir vả emtricitabin ò nhưng
bệnh nhân bị suy thận còn chưa được xác lập. Cần phải giám sát cấn thận các dấu hiện nhiễm
độc, ner sự suy giảm của chủ~c nãng thận, và các biến đổi của nồng độ vỉrus, đối với ca'c bệnh
nhân bị suy thận từ trưởc, khi bắt dầu dùng viên kết hợp, và kéo dải khoảng cách giữa các lẩn
Trang 5/I0
uống lhuốc. Không nên dùng viên kết hợp liều cố định emlricitabỉn vả lenofovir disoproxil
fumaral cho những bệnh nhân có độ thanh ìhảỉ creatinine < BOLLLVpILL'Lt hoặc những bệnh nhân cần
phải thấm tách mảu, vì không thế giảm lìền vỉên kết hợp cho phù hỌp với yêu cầu dìều nị.
Nếu phosphat huyết thanh < 1,5 mg/dl (0, 48 mmol/l) hoặc dộ thanh thải cmatinin hị giảm xuống
<50 mìlphút, chức nãng thận cần đưọc đánh gỉá lại tLong Vòng! tuần, bao gồm cả do nông độ
glucose máu, kaìi máu và glucose nước tiểu, và khoảng cách gỉũa các lần dùng thuốc cãn duợc
diếu chỉnh. Cũng nên cân nhắc ngừng diều trị vởĩ những bệnh nhân có độ thanh thải creatinin -=fí
50 mllphủt hoặc phosphat huyết thanh gỉảm xuống < 1,0 m gldi (0,32111n1011 l).
Nên tránh dùng viên kết hợp khi đang dùng hoặc mởi dùng trưởc đó không lâu một thuốc gây
dộc thận.
Nên trảnh dùng vìên kết hợp vởi các bệnh nhân đã đỉều trị kháng retrovirus Lrưởc đó mà nhỉễm
HIV- ] có mang đột biến K65R Trong một nghìên cứu lâm sảng có đối chúng kéo dải 144 tuần
so sảnh tenofovỉr disoproxil fLment vói stavudin trong công thúc kết họp với lamivudin vả
efavhenz trên các bệnh nhân dùng thuốc kháng Letrovirus lần đần, nguời ta thắy có sự gỉãLm nhẹ
mật dộ xương ở xuong hông vả cột sống tLOLLg cả hai nhóm đìễu nị Ở tnần l44, sự giảm mật dộ
xuơng ở cột sống và biến đối cảc chỉ sô sinh học của xương so với ]L'Lc bắt đầu nghỉên CÚll 0
nhóm diều t1ị hằng tenofovir dìsoptoxìl fumarat ìón hon đáng kể so vởi nhóm kỉa. Ở nhóm nảy,
sự gìảm mật độ xưong ở hông cũng lón hơn đáng kể so vởi nhóm kia cho tới tuần th'L 96. Tuy
nhìên, sau 144 tuần điều nị, không có nguy cơ gãy xương Lãng hoặc dấu hiện lâm sảng về bất
thuờng xuong Nên tham vấn bảo sĩ nếu nghi ngờ có bất thường xnơng.
Bệnh nhân nhiễm đồng thòi HJV vở virus viêm gan B hoặc viêm gan C: Bệnh nhân bị vỉêm gan B
hoặc C mạn tính, khi điều trị bằng phác đồ kháng Retrovirus phối hợp sẽ có nguy cơ cao bị bìền
chứng nặng ở gan và có thế tử vong.
Các bác sỹ lâm sảng nên tham khảo tải Liệu hướng dẫn điều trị HIV hiện tại để có biện pháp diều
trị tốt nhắt cho bệnh nhân dồng thời nhiễm cả HIV và HBV.
Độ an toản và hiệu quả của Thuốc kết hợp Iỉểu cố định mntricitabin vả tcnofovir disoproxil
fumarate chưa dược nghiên cửu trong điển trị nhiễm HBV mạn tính. Trong nghìên cứu dược lực
học cho thấy 6th ỉcitabin vả tenofovh khi sử dung Liêng rẽ hay kết họp đểu có khả nãng kháng
vi…s HBV. Vóì kinh nghìệm Lâm sảng còn hạn chế cho thấy emtrỉcỉlabìn vả tcnofovỉr disoptoxiL
fumarat có hoạt động kháng HBV khỉ đuợc su dung nong phác đồ kết hợp kháng chovhus đề
kiểm soát nhỉễm HIV
Bộc phát vỉêm gan đã xảy ra sau khi ngừng điều trị emtrỉc-ỉtabìn hoặc tenofovỉr đìsoproxỉl
lemafõÍ.
Bệnh nhân nhỉễm đồng thòi HIV vả HBV phải đuọc gìám sát chặt chẽ cả về lâm sảng vả xét
nghỉệm tmng thơi gìan ít nhất vải tháng sau khi ngùng diều tử bằng thuốc kết hợp.
Bệnh gan. Tính an toản vả hiệu quả của viên kết hợp lỉềLL có định cmtricitabìn vả tenoí`ovh
clisoptoxỉl fum:uat chưa đuọc xác định ở những bệnh nhân có các Lối loạn nặng ò gan. Dưọc
động rhọc của thuốc kết hợp và cùa emt1icỉtabín chua duợc nghìên CL'LLL ở những bệnh nhân bị suy
gan. Duọc động học cua tenofovh đã đuợc nghỉên cứu ở bệnh nhân suy gan vả không thấy cân
thiết phải đìểu chỉnh lỉều cho nhung bệnh nhân nảy Dưa t1ẽn vỉệc emhicỉtabỉn chỉ chuyến hóa
phần nhỏ ở gan và đuông [hải lLL`L chu yếu lả qua thận, duờng như không cằn phải đỉều chỉnh lỉều
cho nhưng bệnh nhân suy gan.
Những bệnh nhân có rối loạn chức năng gan từ truớc bao gồm cả viêm gan mãn tính thể hoạt
động có tần suất cao hơn bị cảc bất thuòng chức năng gan khi điêu trị bằng thuốc khảng
Renovỉrus kết họp và nên đuợc giám sảt theo thực hảnh tiêu chnẩn Nếu có các hằng chúng lả
bệnh gan nặng lên ở nhung bệnh nhân nảy, nên cân nhắc diều nị ngắt quãng hoặc ngùng việc
điều_trị.
Nhiêm acid lactic: Đã gặp các trường hợp nhiễm acid lactìc, thường kèm tth gan nhỉễm mỡ, khi
Sử dụng các chất tương tự nucleosid. Các dẩn hiệu sởm (tăng Iactat máu U`ỈỘII chứng} bao gồm
các tLỉệLL chúng tỉêu hóa nhẹ (buồn nôn, nôn và đau bụng), mệt mỏi không đặc hỉệu, ăn kém
ngon, gỉảm cân, các tliộLL chúng hô hấp (thò chậm vả/hoặc sâu) hoặc các tLiệu chúng thẩn kinh
(kể cả yên vặn động). Nhỉễm acid laclìc có tỷ lệ tử vong cao và thưòng kèm theo viêm tụy, suy
gan hoặc sny thận. Nhỉễm acid lactỉc thuờng xuất hỉện sau một vải hoặc nhiều tháng điều nị.
Trang 6/10
W/
Nên ngừng dìếu trị bằng các chất tuong tự nucleosid khi có các dấu hỉệu tảng Iactth máu vả
nhỉễm acid lacticfchuyến hóa, phi đại gan tìến tLìến, hoặc men gan tăng nhanh.
Cẩn thận trọng khi dùng oảc chắt tương tự nucleosid cho bắt kỳ bệnh nhân nảo (đặc biệt là phụ
nữ béo phì) bị phì đại gan, viêm gan hoặc có các yếu tố nguy co bị bệnh gan đã biết và gan
nhiễm mỡ (kể cả một số thuốc nhất định và cồn) Các bệnh nhân đồng thòi nhiễm viêm gan C vả
đuợc điều trị bằng aipha inteifelon vả1ibavhìn có thể có nguy cơ đặc biệt.
Cần theo dõi chặt chẽ các bệth nhân có nguy cơ cao.
Loạn dưỡng mõ“: Phảc đồ điều trị phối hợp thuốc chống Retrovirus thưởng gây ra tái phân bố mỡ
trong cơ thể ( loạn dLLõLLg mõ) ở bệnh nhân nhiễm HIV. Hậu quả lâu dải của những biến chứng
nảy hiện vẫn chua rõ. Hỉểu biết về co chế chnyển hoá hiện vẫn chưa đầy đủ Có giả thuyết cho
Lăng có mối liên quan giua tích mõ nội Lạng vói chắt L'Lc chế men PLoteztse (PIs) vả teo mô mõ
vởi chắt L'Lc chế men sao chép nthọc nucleoside (NRTIS). Nguy cơ cao của loạn duõng mở có
iiên quan tói nhưng yếu tố có tính chẫt cá nhân như tuốỉ cao, và những yếu tố iiên quan tói thuốc
như thòi gìan điều t] ị thuốc kháng Rel:ovirns kéo dải và Liên quan tói những rối loạn chnyến hoá.
Khám iâm sảng nên bao gồm cả việc đánh giá các LL~ỉệLL chứng thực thế cùa tải phân bố mỡ. Nên
cân nhắc lảm xét nghiệm Lipid huyết thanh vả Glucose máu. Rối loạn Lipid cung nên đuợc diều
trị một cách phù hợp theo lâm sảng. Tenofovir có tiên quan về cấu tLL'LC với cảc thuốc tnong tự
nncleosìd clo đó thế không loại trừ nguy cơ loạn dưỡng mỡ. Tuy nhiên, dữ liệu từ nghiên cứu lâm
sảng t44 tuần trên các bệnh nhân điều trị kháng retrovirth lần đầu chỉ ra rằng nguy cơ cùa loạn
dưỡng mở với tenofovỉr dỉsoproxỉl fumarat iả thấp hơn so vởỉ stavudine khi dùng kết hợp vói
lamivudin vả efavirenz.
Rối Ioạn chức năng ty lhế: Các chẳt Lương tự nucleosid vả nucleotid đã được chứng mỉnh in ví/ro
vả in vivo là gây huỷ hoại ty thể ở nhiều mức độ khảo nhau. Đã có những bảo cảo về rối loạn
cerc năng ty thế ở trẻ nhỏ HIV âm tính nhưng dã bị phơi nhiễm vói cảc chắt tương tự nucleoside
từ trong từ cung và sau khi sinh . Các tác dụng bắt iợi chính được bảo cảo lá các Lối loạn huyết
học (thiếu mảu, giảm bạch cẳu trung tính), các rối ioạn chuyển hoá (tăng lactat máu, tăng !ìpỉd
máu) Những tác dung có hại nảy thLLỜLLg lả nhất Lhởi Đã có báo cáo một số rối ioạn thần kinh
khởi phát muộn (Lăng tLLLơng lực, co giật lối ioạn hánh vì). liỉện vẫn chưa xác định đuợc lỉệu các
Lối loạn thần kinh lả tạm thời hay vĩnh viễn Bất cứ trẻ nảo dã có phoi nhiễm vởi cảc chắt tuơng
tự nucleoside vả nucleotid từ trong tu cnng, ngay cả vói trẻ HIV am tính, đễn phải duợc theo dỏi
về mặt iâm sảng vả xét nghiệm và nên thăm dò đầy đủ về khả năng Lối ioạn chức năng ty thế
trong trường hợp có các trỉệu chứng liên quan. Những phát hiện nảy không ảnh hLLởLLg dến các
khuyến cáo hỉện nay về sử dụng điều trị kháng Retrovirus ở phụ nữ mang thai đề phòng ngừa lây
truyền HIV theo chìều dọc.
Sử dụng đồng thòi tenofovìr disopmxỉl tumznat vả didanosin lảm tăng 40— 60% phơi nhiễm toản
thân cua didanosỉn dẫn đến tăng nguy cơ gặp cảc phán ung ngoại ý liên quan LỚỉ didanosin. Đã
có báo cáo về cảc trường hợp hiếm gặp viêm tụy và nhiễm acid lactic có cả một số ca LLL vong
Vìệc su dụng dồng thời tenotovh disoproxil fumarat vả dìdanosin vói lìền iưọng 400 mg mỗi
ngảy dã lảm giảm đảng kể một lượng tế bảo CD4, có thể ìả nhờ một Lương tác nội bảo iâm tăng
didanosỉn được phosphoryl hoá (hoạt động). Liều giảm 250 mg didanosỉn dược dùng đồng thời
vởi liệu pháp tenofovir disoproxil fumarat kèm theo cảc báo cảo về tỷ tệ cao của sự thắt bại virus
học trong nhiều sự phối hợp được thử nghiệm.
Phụ mì có thai:
Đối vói emt1icìtabỉn vả tenofovir clisopmxil funưưat, tác hại cua thuốc trên phụ LLLL mang thai
không đầy đu. Cảc nghìên cứu trên động vật không cho thấy tảo hại trục tiếp hoặc gián tìếp cua
emtricitabỉn hoặc tenofovir disopmxỉl fumamt vê khía cạnh thai nghén, sự phát tL iẻn của
phôỉ/bảo thai, quá trình sinh nở hoặc sự phảt triển sau khi ra đời.
Tuy nhiên, chỉ nên dùng viên kết hợp trong quá trình mang thai khi khỏng có iL_LtL chọn nâo khác
phù hợp hơn Khi dùng viên kết hợp phải đồng thời sử dụng một bìện phảp tránh thai hỉện quả.
Phụ nữ cho con bú:
Hìện oòn chua bìết liệu emtricìtabin hoặc tenofovir có được hải tỉết qua sua mẹ hay không.
Phụ nũ nhiễm HIV được khuyện Lằng không nên nuôi con bằng sua cùa mình tLong bat kỳ
tLLLò'LLg hợp nảo dề tránh lây truyôn HỈV cho con.
Trang 7/ 10
Anh lmởfng lẽn kim mĩng Mi xe vả vận ILL`mIL máy móc:
Không có nghiên cứu nảo về ảnh huởng cùa viến kết hợp liều cố định cmhicitabin vả tcnol`ovh
disopioxil futnarat.
Tuy nhiến, bệnh nhân cần được thông báo rằng đã có bảo cảo về tình trạng chóng mặt tLong quai
tLình đ iều trị bằng emtricitabin cũng như bằng tcnofovir disoproxil fLLmarat.
TƯỚNG TÁC THUỐC
Dược động học Ở trạng thái Ổn định của emtrỉcitabin vả tcnofovir không bị ảnh hưởng khi
emtricitabin vả tcnofovir disoproxil fumarat được dùng kết hợp vói nhau so vói khi dùng L~ỉếng
từng thuốc.
Các nghiên cứu tương tảc dược dộng học trên lâm sảng và in vilro đã cho thấy it có khả năng xây
ra cảc tương tác có trung gian lả CYP4SO liên quan tới cmtricitahin vả tcnofovir disoproxil
fumarat vởi cảc thuốc khác.
Cảo Lương Lác 1ìên quan đến emlricifabỉn:
Trên in vitro, etntricitabỉnc không ức chế sự chuyến hóa có trung gian iẺL bắt kỳ đồng đạng
CYP4SO nảo sau đây của người: 1A2, 2A6, 286, 2C19, 2D6 vả 3A4. ELLLtLiCỉtLLbÌLL không ức chế
cnzymc của quả trinh gìucuronid hóa. Không có tương tác clảng kế nảo vế lâm sảng khi
cmtrìcitabin được dùng cùng hic vói indinavir, zidovudin, stavudin hoặc famciclovir.
Emtricitabin được bải tỉết chủ yếu bằng cách lọc ở cầu thận và bảỉ tiết chủ động ở ống thận.
Ngoại trừ famcìciovir vả tenofovìr disoproxil l`umarat, hiệu lực của việc dùng kết hợp
emtricitabin với cảc thuốc được bải tiết qua thận, hoặc các thuốc được biết lá có ảnh hưởng tới
chức năng thận, còn cluta được đánh giả. Việc dùng kết hợp với các thuốc cũng dược bải tiết chủ
động ở ống thận có thể dẫn tới tăng nồng độ cùa cả mntricitabin vả thuốc kết hợp do sự cạnh
tranh đường thải trù nảy,
Không có kinh nghiệm iâm sảng về việc sử dụng kết hợp emtricỉtabin với các chất đồng đẳng
cytidinc. Do dó, không nên dùng kết hợp emtricitabin với lamivudin hoặc zaicitabin để điều trị
nhiễm HIV.
Các Lương lác liên quan Lới lenrjòvir:
Việc phối hợp Iamivudine, indinavir, efavirenz, nclfinavir hoặc saquinavir (có bổ sung Litonavir)
với tcnofovir disoproxil fumarat khỏng gây ra bắt kỳ tương tác nảo về iâm sảng. Khi tenoftwir
clisoproxil fnmarat được phối họp với topinavir/ritonavir, không có bìến đối nảo về dược động
học cùa lopinavir vả Lìtonavir. AUC của tenofovir tãng lên khoảng 30% khi tenofovir disoproin
futnarat được phối hợp vởi lopinavir/rỉtonavir.
Khi dùng didanosine dưới dạng viên nang Lan trong ruột 2 giờ trưởc khi dùng tenofovir
disoproxil fumarate hoặc cùng một lúc, AUC cùa dỉclanosine tăng tương ửng trưng bình lả 48%
và 60%. Mức tăng tLLLLLg bình gỉá trị AUC của didanosin lả 44% khi dùng viên nén có chắt đệm 1
giờ trước khi dùng tcnofovir. Trong cả hai trường hợp các chỉ số dược động học cùa lenol`ovir
được dùng kèm theo một bữa ăn nhẹ là không thay đôi. Không nên dùng phối hợp tenofovir
dìsoproxil fumarat với didanosin.
Khi tcnofovir đisoproxi] fumarat được dùng phối hợp với atanazavir, nồng độ atanazavir giâm
(mức giảm tuơng ửng cùa AUC vả Cmin là 25% và 40% so với atanazavir 400 mg). Khi dùng
thếm ritonavir với atanazavir, ảnh hưởng tiêu cực của tcnofovir lên C…… của atanazavir đã giảm
đi rõ rệt, trong khi mức giảm cùa AUC vẫn giữ nguyên (mức giảm tương ửng củ AUC vả C…… là
25% vả 26% so với atanazavirh itonavir 300/] OOmg).
Tenofovh đưọc bải tiết qua thận bằng cả hai cách iọc Ở cầu thận và bảỉ tiết chủ động qua con
đuờng vận chuyển anion hưu co 1 Ô người (ILOATI). Dung phối hợp tenofovh disomoxil
funmrate với cảc thưốc khác cũng đuợc bải tiết chủ động qua hệ thống vặn chuyến anion hũu cơ
(vi dư như cidofovh) có thế lảm tăng nồng độ của tenofovir hoặc của thuốc phối hợp.
Tenofovir disoproxil thnaLat chưa được đánh gỉá ở nhũng bệnh nhân đang dùng các thuốc gây
độc thận (chẳng hạn như cảc aminoglycosid, amphotericin B foscarnct, ganciclovir, pcntamiđin,
vancomycin, cidofovh hoặc intcrlcnkin-Z) Trảnh sử đụng tenofovir disoproxil fumznat khi đang
dùng hoặc mới ngung dung các thuốc gây độc thận Nếu bắt buộc phải kết hợp tenofovir
disoproxil fumarat với cảc thuốc gây độc thận, nên kiểm tra chửc năng thận hảng tuân
Trang 8110
ỰÙƯVÌ’Ề-Jớl
Vỉệc phối hợp tenofovìr dìsoproxil fumarat với methadon, rìbavỉrỉn, adefovìr dipỉvoxỉl hoặc các
thuôo tránh thai norgestimatlethìnyl oestradỉol không gây ra bâl kỳ tLL'ơtLg tác dược động học nảo.
TẤC DỤNG KHÔNG MONG MUÔN
Trong một nghìên cứu mở lâm sảng ngẫu nhiên trên những bệnh nhân chưa sử dụng thuốc tháng
Letrovirus (GS- 0] -934), bệnh nhân dùng emnìcỉtabĩn, tenofovh dìsoproxìl Fumarat vả efavireny
trong 144 tuần (dùng như công lhức kết họp lhuốc nén emtricitabìn/tenofovir dỉsoproxỉl fumarat,
cộng thêm etavhcnz tu tuằn 96). Dữ liệu về lính an toản cùa emtrìcìtabin vả tenoFovh dỉsoproxĩl
fuma1at phù hợp vói thí nghiệm hưởc đây vởỉ cảc tảc nhân năy khi một tLong chủng đuợc dùng
với các tác nhân khảng relrovirus khác. Các phản ửng có hại được báo cáo thường xuyên nhất
xem như có thế hay gần như có Iỉên quan với emtricỉtabin vả/hoặc tenofovỉr dỉsoproxil fumarat
lả huồn nôn (12%) và tìêu chảy (7%).
Nhĩmg phản L'mg ngoại ý nghi ngờ có liên quan tởi việc đỉều tLị (ít nhẩt lá có thế liên quan) bằng
cảc thảnh phần của viên kết hợp từ thứ nghìệm lâm sảng vả trong theo (.ỈỎỈ hậu mãi được liệt kê
dưới đây theo hệ thống các cơ quan [rong cơ thể vả tân suất gặp phải. Fần suất được xác định lả
rẩt hay gặp (2 lllO), hay gặp (2 1l100, < ì/IO), không hay gặp (2 1/1000, < IJ’IOO), hiếm gặp (2
Ill0.000, < l/1000) heặc rất hiếm gặp {< lÍI0.000) bao gồm cả những báo cáo rìêng lè.
Các rối loan về hệ máu vả bạch hzụ›ếf:
Hay gặp: giảm bạch cầu trung tính
C ác rôỉ Ioc_m ở hệ miễn dịch.
Hay gặp: phán L'LLLg dị ủng
Cch rói Ioạn về chuyển hóa vả dinh dương.
Rất hay gặp: hạ phosphat máu
Hay gặp: tăng triglycerỉd máu, tăng đường máu.
Hiểm gặp: nhìễm acid Iactic
Nhiễm acid Iactic thường kèm theo gan nhiễm mỡ, đã được bảo cáo trong quá trình SỬ dụng các-
thuốc tương tự nucleosid.
Các rối loạn rảm thần:
Thường gặp: gìấc mơ bất thưòng, mắt ngủ
Các rối loạn hệ Ihần kinh
Rấthaỵ gặp: chóngmặt, đau dằn
( ác ròi Ioạn hệ hô hấp ngục va nung lhốf.
Rắt hỉếm gặp: khó thỏ
Các rối loạn ở dạ dảy ruột:
Rắt hay gặp: tỉêu chảy, buồn nôn, nôn
Hay gặp: đằy hơi, khó tiêu, đau bụng, lipase huyết lhanh tăng, amylase tăng bao gồLLL amylase
của tuyến tụy.
I—Iỉếm gặp: vỉêm tụy
Các rối 10an ở gan mật:
Hay gặp: tăng bỉliL ubìn máu, tăng transamỉnase
Rất hìếm gặp: viêm gan
Các rrỂi loạn o’ da vả mô dtrói da
Hay gặp: nồi ban, ngứa, ban dát—sần mảy đay, ban Lộp, ban mú, vả bỉến mảu da (tãng sẳc tố)
Các rỏi loun cơ khớp và mô liên kếr.
Rất hay gặp: tăng CLeatỉn kỉnase
Các rói Ioc_m thận vờ tíết niệu
Hỉếm gặp: suy lhận (cắp và mãn), bệnh lý đầu ống thận hao gồm hội chứng Fanconỉ, protein
niệu, tăng creatinin.
Các rối loạn foòn thán vò tợi nơi dùng Jhuốc:
Hay gặp: đau, suy nhược
Ngoài ra, thỉếu máu lá hay gặp và biến mỉm da (tăng sắc tố) là rắt hay gặp khi dùng emtrỉcỉtabin
cho bệnh LLhâLL nhi.
'Frang 9/10
,_,LỉLPO/
Các ghi chép về phản ứng ngoại ý ở bệnh nhân bị nhiễm đồng thời HIV/HBV hoặc HIV/HCV
cũng tương tự như bệnh nhân chi nhiễm HIV. Tuy nhiên, đối với nhóm bệnh nhân nảy, sự tăng
AST vả ALT xuất hìện thường xuyên hơn so với nhóm bệnh nhân nhỉễm HIV nói chưng.
Liệu pháp kháng retrovirus kết hợp thường kèm theo các bất thường chuyến hóa như tăng
triglycerid mảu, tăng cholesterol mảu, đề kháng insulin, tăng đường máu vả tăng lactat máu.
Liệu pháp kháng retrovirus kết hợp cung kèm theo tái phân bố mõ trên cơ thể (Ioạn dLLõLLg mõ) Ò'
bệnh nhân HIV bao gồm mất mỡ ngoại vi và mỡ dưới da mật, tăng mỡ bụng và nội tạng, phì đại
ngưc và tích mỡ vùng có lưng (bướu trâu).
Những bệnh nhân nhỉễm bị sưy giảm miễn dịch nặng ở thời điếm bắt đầu lỉệư pháp kháng
retrovirus kết hợp (CART) có thể xảy ra phản ứng viêm với sự xâm nhiễm không có tL ỉệu chứng
hoặc cơ hội sót lại.
Nhũng truờng hợp hoại tử xuơng đã được báo cáo, đặc bỉệt ò nhũng bệnh nhân có nhũng nhân tố
nguy cơ đã đuợc nhận biết tổng quát, bệnh HIV cấp tiến hoặc diều trị lâu dải với lìệu pháp kháng
retrovirus kết hợp (CAR F) Tần số cùa trường hợp nảy vẫn chưa được biết.
Thông báo cho bác sĩ nhũng tác dụng không mong muốn gặp phải khi sư dụng rlzuốc.
QUÁ LIÊU
Nếu xảy ra quá liều, bệnh nhân phải được giám sát chặt chẽ về các dấu hiệu ngộ độc và được áp
dụng các biện pháp hỗ trợ tiêu chuẩn khi cân thỉết. 'Tôi 30% liều emtrỉcìtabìn và khoảng IO%
liêu tenofovir có thề Ioại bò bẳn cảch thầm tách máu. Hỉện còn chưa biểt có thế loại bo
emtricitabin hoặc tenotovh bằng thâm phân phúc mạc hay không.
ĐÓNG GÓI: Hộp | chai cera 30 viên nén bao phim.
THỜI HẠN SỬ DỤNG: 36 tháng kể tư ngảy sản xưất.
Không dùng thuốc quá hạn sủ dung.
BẢO QUÁN: Không quá 30°C Giữ thuốc trong bao bì gốc
Đọc kỹ llu'óng dẫn sữ dung rr u ơc khi dùng.
Nếu cần thêm thông rin, xin hỏi" y kìến bác sĩ.
Giữ rhuôc trúnh xa râm tay của tre.
Sãn xuất bởi:
MYLAN LABORATORIES LIMITED _
F-4 & F-l2, MIDC, Malegaon, Sinnar, Nashik — 422] I3, Maltrashtra State, An Độ
TUQ.CỤC TRUỜNG
P.TRLÚNG PHÒNG
%… ẵ'ấỉi “Va“m ấẩ_mắ
Trang 10l ] O
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng