














ẵMổ/e5'
nộ Y TẾ 1
cục QUẢN LÝ mr'ợc i
DÃ PHÊ DUYỆT i
F.án dẩu:..âẵ. . .....
: Efient 10…
“" … , rĩ/m- coated tablets
" 'Ể'" Drasugrel
`i ~……°zr… oi…
. " m…fizmw mmww
u… _
……ưẸ» Efient 10 mg ,
ỀẨỀ“NWM*MỪ flm- coated tablets
sDK ra re]
SlnubừE.hmĩomuu p SUg
ímeCat hùm: Mmu mua u… Wu uu
IMW W
mpmcmsJJvnn-u vdml, C…: actcu Scooúanaermtun-rưm
zlvukzbnsu.ưúd Yuu~dm lmunmmlnmnrcbẹnulchuuren
zymt` Ễtềominlheovlsẩglẩpỗcuqutunmmmnrmnustwe.
.… , nơ sloru I
ỂỂỦẸỂÊÝ '" “ lủhm Medcmu' pmđuoi mhed tn mooìcs prmnhun
1 …… 5 A Ava on .» lnmsve. 30
ao 0! Aocơbưdas (Mưdl Soon
MN Ụs:ikvn
; , | 6 n S 6 : ơ
xi NQEI pmer'i WB copuommpảu n) loánan B… 0;
6… 01 Jugug …… …. …,
mc… nmluncnmnhủnnưa
um… Mu
…n— …uu mun… VW… …lud: u…c
n iunus Z bn Emn …nu
_I ’ x-uun … mua…im IÍIIIm
mu :… u :
iủu—K unmm …… __
N…Juol …huui .x- J›… WA _
WA " nt ỰI….
lbdugn _.
… nu Illih):
mhụmn nncu- :
ismnm WA (
m \.A
u-nnum
u…umm
'" ……
@ ,.J ụ.J z.›
l
uu~ c.
huủIhM_ lntemal m MĐS 1no l.in diedt required)
"""nă "n'ii'fuẵn— MBS … Rel: mon
… Opera… Name: JL
6…0L iueụa = ieqel JGISỊIEI
Efient
Prasugrel
Thuốc nảy chỉ dùng theo đtm của bác sĩ.
Đọc kỹ hướng dẫn sử dạng Irước khi dùng. Nếu cần thêm thông tin, xin hỏi ý kiểu bảc sỹ
1. TÊN THUỐC
Vìên nén bao phim Efient 5 mg.
Viên nén bao phim Efient 10 mg.
2. THÀNH PHÀN ĐỊNH TÍNH VÀ ĐỊNH LƯỢNG
Efient 5 mg
Mỗi viên nén chứa 5 mg prasugrel (dạng hydrochlorid).
Efient 10 mg
Mỗi viên nén chứa 10 mg prasugrel (dạng hydrochlorìd).
Danh sách đầy đủ cảc tả dược, xem mục 6.1.
3. DẠNG BÀO CHẾ
Efient 5 mg
Viên nén bao phim.
Viên nén mảu vảng, hình mũi tên kép, dập chìm “5 mg" ở một mặt vả “4760” ở mặt còn lại.
Efient 10 mg
Viên nén bao phim.
Viên nén mâu be, hình mũi tên kép, dập chim “10 mg” ở một mặt và “4760“ ở mặt còn lại.
4. ĐẶC TỈNH LÃM SÀNG
4.1 Chỉ định điểu trị
Efient, sử dụng phối hợp với acid acetylsalicylic (ASA), được chỉ định trong dự phòng biến cổ,ết khối
trên bệnh nhân bị hội chứng mạch vảnh cấp (ví dụ đau thắt ngực không on định, nhồi máu e không
có đoạn ST chênh [UA/NSTEMI] hoặc nhổi máu cơ tim có đoạn ST chếnh [STEMID có chỉ định can
thiệp mạch vảnh qua da sớm hoặc trì hoãn (PCI)
Liệu phảp chống kết tập tiễu cầu sớm được khuyến cáo trong điều trị hội chứng mạch vảnh cấp (ACS) do
nhiều biến có tim mạch có thể xảy ra trong những gỉờ đẳu tiên. Cảc thử nghíệm lâm sảng đã chửng minh
hiệu quả cùa Efient, Efient và thuốc đối chứng không được sử dụng cho bệnh nhân nhổi mảu cơ tìm
không có đoạn ST chênh cho đến khi có kết quả chụp mạch vảnh. Với một số lượng nhỏ bệnh nhân cần
thực hiện phẫu thuật bắc cầu mạch vảnh (CABG) cẳp sau khi điều trị bằng Efient nguy cơ chảy máu
nghiêm trọng lả đáng kể [xem mục 4. 4 Cảc chú ý đặc biệt vả thặn trỌng khi sử dụng].
fl."
luf
Điều trị có thể được xem xét trước khi quyết định chụp mạch vảnh nếu đã cân nhắc không có khả năng
thực hiện phẫu thuật bắc cầu mạch vânh. Lợi ích cùa việc điểu trị sởm bằng Efient cần được cân bằng với
nguy cơ tăng tỷ lệ xuất huyết trên bệnh nhân có chỉ định thực hiện phẫu thuật bắc cầu mạch vảnh khẩn
câp.
Để biết thêm thông tin, xin tham khảo mục 5.1.
4.2 Liều dùng và đường dùng
Liều dùng
M@@@
Nên bắt đầu dùng Efient với liều đơn 60 mg, sau đó tiếp tục dùng liều IO mg một lần trong ngảy. Bệnh
nhân dùng Efient nên dùng cùng acid acetylsalicylic hâng ngảy (75 mg đến 325 mg).
ớ bệnh nhân có hội chứn mạch vânh cẳp (ACS) đã được xử lý can thiệp mạch vảnh qua dạ, việc dừng
sớm bất cứ thuốc chống ket tập tiểu cầu nảo, bao gồm cả Efient, có thẻ lảm tăng nguy cơ hụyêt khối, nhôi
mảu cơ tim hoặc tử vong do bệnh lý của bệnh nhân. Khuyên cảo sử dụng thuôo kéo dải đên 12 tháng trừ
khi có chỉ định lâm sảng ngừng dùng Efient (xem mục 4.4 và 5.1).
Bênh nhân > 75 tuồi
Do nguy cơ xuất huyết (kể cả xuất huyết gây từ vong) vả hiệu quả cùa thuốc không rõ rảng trên các bệnh
nhân > 75 tuổi, không khuyến cảo sử dụng Efient cho các bệnh nhân nảy, trừ trường hợp có nguy cơ cao
(bệnh nhân đải thảo đường hoặc có tiền sử nhồi mảu cơ tim) trong đó lợi ích của thuốc vượt trội hơn và
thuốc có thế được xem xét sử dụng. Sau khi đã cân nhắc cân thận lợi íchlnguy cơ trên từng bệnh nhân,
nếu cần thiết phải điều trị cho bệnh nhân > 75 tuổi, bảo sĩ điều trị nên kế đơn liều tấn công 60 mg, sau đó
dùng liếu duy tri giảm xuống còn 5 mg. Bệnh nhân > 75 tuối nhạy cảm hơn với tác dụng phụ xuất huyết
vả nồng độ chất chuyển hóa có hoạt tính của prasugrel trong tuần hoản cao hơn ở những bệnh nhân nảy
(xem mục 4. 4, 4.8, 5.1 và 5 2). Việc sử dụng liều 5 mg chỉ dựa trên cảc phân tích về dược lực học! dược
động học và hiện chưa có cảc dữ liệu lâm sảng về độ an toản của mức Iiếu nảy cho đối tượng bệnh nhân >
75 tuổi.
Bẻnh nhản cân nãne <60 ke
Nên dùng Efient với liều đơn tấn công ban đầu 1ả 60 mg, sau đó tiếp tục duy trì liều 5 mg m âìn trong
ngây.
Không khuyến cảo dùng liều duy trì 10 mg một lẩn trong ngảy do liếu nảy lảm tăng nồng độ các chất
chuyến hỏa có hoạt tinh cùa prasugrel, tăng nguy cơ xuất huyêt trên bệnh nhân có cân nặng < 60 kg so với
bệnh nhân cân nặng_ > 60 kg Hiệu quả và độ an toản ở mức liều 5 mg chưa được đánh giá tiển cứu (xem
mục4.4, 48vả5..2)
Su thân
Không cần hiệu chinh liếu cho bệnh nhân suy thận, bao gổm cả bệnh nhân bị bệnh thận giai đoạn cuối
(xem mục 5 2). Kinh nghiệm sử dụng thuốc cho bệnh nhân suy thận còn hạn chế (xem mục 4 4).
Su an
ỈMẺở'
Không cần hiệu chinh liếu cho bệnh nhân suy gan nhẹ đến trung binh (phân loại ChildPugh A vả B) (xem
mục 5. 2). Kinh nghíệm sữ dụng thuốc cho bệnh nhân rối loạn chức năng gan nhẹ và trung bình còn hạn
chế (xem mục 4. 4).
T rẻ em vả tre“ vi thảnh niên , Ả ›. _
Không khuyên cảo sử dụng Efient cho trẻ em dưới 18 tuôi do thieu cảc dữ liệu ve đọ an toan va hiẹu qua
của thuốc.
Cách dùng
Chỉ dùng đường uống. Efient có thể dùng cùng hoặc không cùng với thức ãn. Uống liều tấn công 60 mg
prasugrel lủc đỏi có thế tạo tảc dụng khới đầu nhanh nhất (xem mục 5.2). Không cắn h0ặc be` vỡ viên
thuốc
4.3 Chống chỉ đinh
Mẫn cảm với hoạt chắt hoặc bất cứ thảnh phần nảo của thuốc.
Đang có bệnh lý xuất huyết.
Cỏ tiễn sứ đột quỵ hoặc cơn thiếu máu não thoáng qua (transient ischaemic attack -TIA).
Suy gan nặng (phân loại Child Pugh C)
4.4 Các chủ ý đặc biệt và thận trọug khi sử dụng
Ngư cơ xuất huvết
Trong thử nghiệm lâm sảng pha 3, tiêu chuẩn loại trừ chính bao gổm bệnh nhân có tãng nguy cơ xuất
huyết; thiếu máu; giảm tiêu câu; tiền sử bệnh lý nội sọ. Bệnh nhân có hội chứng mạch vânh câp đã can
thiệp mạch vảnh qua da được điếu trị với Efient vả acid acetylsalicylic có tăng nguy cơ xuất hiện nghiêm
trọng và xuất huyết không nghiêm trọng theo hệ thống phân loại tiêu sợi huyết trong nhổi máu cơ tim
(TIMI). Do đó, chỉ nên xem xét sử dụng Efient trên bệnh nhân có nguy cơ xuất huyết khi lợi ích dự phòng
biến cố thiếu mảu hoại tử vượt trội hơn nguy cơ xuất huyết nghiêm trọng. Cần đặc biệt chủ ý trên các
bệnh nhân:
~ >75 tuối (xem dưới đây).
' có khả nãng xuất huyết (ví dụ mới bị chấn thương, vùa trải qua phẫu thuật, mới bị xuất huyết tiêu hóa
hoặc xuất huyết tiêu hóa tái phát hoặc loét dạ dảy tiến triền)
* cân nặng <60 kg (xem mục 4. 2 vả 4. 8). Trên những bệnh nhân nây, liều duy trì 10 mg kifớảđược
khuyến cảo. Nên sử dụng liều duy trì 5 mg.
' sứ đụng đổng thời với các thuốc lảm tăng nguy xuất huyết bao gổm các thuốc chống đông mảu đường
uống, clopidogrel, cảc thuốc khảng viêm phi steroid (NSAID) và các thuốc lảm tiêu fibrin.
Trên bệnh nhân đang có xuất huyết nếu cần đảo ngược tác dụng dược lý của Efient, có thể truyền tiếu cầu.
Do nguy cơ gây xuất huyết (bao gồm cá xuất huyết gây tử vong) và hiệu quả không rõ rảng trên bệnh
nhân > 75 tuối, nói chung không khuyến cảo sử dụng Efient cho các bệnh nhân nây, trừ trường hợp bệnh
nhân có nguy cơ cao (bệnh nhân dái thảo đường hoặc có tiến sứ nhồi mảu cơ tim) khi hiệu quả dự phòng
biến cố thiểu máu cục bộ của thuốc vượt trội hơn nguy cơ xuất huyết nghíêm trọng, việc dùng thuốc có
thế được xem xét và phải sử dụng thận trọng sau khi bác sĩ điều trị đã đánh gỉá cân thận lợi ích/nguy cơ
trên từng bệnh nhân. Trong nghiên cứu lâm sảng pha 3 các bệnh nhân nảy có nguy cơ xuất huyết cao, bao
gổm cả xuất huyết gây từ vong khi so sảnh với bệnh nhân < 75 tuổi Trong trường hợp kê dơn, nên dùng
mức liếu duy trì thấp 5 mg, không khuyến cáo sử dụng mức liều duy trì 10 mg (xem mục 4. 2 vả 4. 8).
LI
Hiện tại ít có kinh nghiệm điều trị prasugrel trên bệnh nhân suy thận (bao gổm cả bệnh thận giai đoạn
cuối) và trên bệnh nhân suy gan mức độ trung bình. Có thế có tăng nguy cơ xuất huyết trên cảc bệnh nhân
nảy. Do đó, nên thận trọng khi sử dụng prasugrel cho các bệnh nhân nảy.
Thông tin từỵ văn đối tượng bệnh nhân người Nhật và Trung Quốc có nguy cơ xuất huyết nội sọ cao hơn
so với cảc quân thể bệnh nhân tử các nước phương tây. Prasugrel không lảm tăng nguy cơ xuất huyết nội
sọ trên toản bộ quần thể bệnh nhân tham gia thử nghiệm lâm sảng (TRITON TlMl-38). Kinh nghiệm đíều
trị bằng prasugrel trên cảc bệnh nhân châu Á còn hạn chế Do đó, nên thận trọng khi sử dụng prasugrel
trên các bệnh nhân nảy.
Bệnh nhân cần được tư vấn rầng quá trình cằm mảu có thể kéo dải hơn binh thường khi sử dụng prasugrel
(kết hợp với acid acetylsalicylic) đồng thời bệnh nhân nên thông bảo với bác sĩ nêu xuất hiện chảy máu
bất thường (vị trí hoặc thời gian) trong quá trinh điếu trị..
Phău thuăt
Bệnh nhân cẩn được tư vẩn để họ thông báo với bác sĩ vả nha sĩ việc họ đang sử dụng prasugrel trưởc bẩt
cứ phẫu thuật nâo và trước khi dùng bât cứ thuốc mới nảo. Nếu bệnh nhân phải thực hiện cảc phẫu thụật
mổ phỉên theo chương trinh trong đó coi tác dụng chống kết tập tiểu cầu là tác dụng không mong muôn,
nên ngừng dùng Efient ít nhất 7 ngảy trưởc khi phẫu thuật. Tẩn xuất xuất huyết tăng lên (3 lần) và xuất
huyết nặng hơn có thế xuất hiện trên bệnh nhân có phẫu thuật bắc cẳu mạch vảnh trong vòng 7 ngảy
ngừng dùng prasugrel (xem mục 4. 8). Nên cân nhắc thận trọng lợi ich vả nguy cơ của prasugrel trên bệnh
nhân chua được chụp mạch vảnh và có thể cần phẫu thuật bắc câu mạch vảnh cấp.
Ouá mẫn bao Qồm Qhù mach
Phản ứng quá mẫn bao gổm phù,t mạch đã được ghi nhận trên bệnh nhân dùng prasugrel, bao gồm cả bệnh
nhân có tiến sứ phản' ưng quá mẫn với clopidogrel. Cẩn theo dõi cảc dấu hiệu quả mẫn trên cảc bệnh nhân
đã có tiền sử dị ứng với dẫn chất thienopyridin ( xem muc 4. 8)
Ban xuất hu ết Qiảm tiêu cấu hu ểt khối rombotic Thrombocvtonaeníc Pur ura- -TTP
Ban xuất huyết giảm tiểu cẩu huyết khổi đã được ghi nhận trên bệnh nhân dùng prasugrel. Đây lả một tinh
trạng nghiêm trọng và cần được điếu trị kịp thời.
lffl
Bệnh nhân có cảc bệnh di truyền hiếm gặp như không dung nạp galactosc, thiếu hụt men La
hoặc kém hấp thu glucose-galactose không nên dùng Efient.
4.5 Tương tác vởi các thuốc khác và các dạng khác của tương tác
Warfarín: Sử dụng đổng thời Efient với các dẫn chất coumarin khảc ngoải warfarin chưa được nghiên
cứu Do lảm tăng nguy cơ xuất huyết, nên thận trọng khi phối hợp warfarin (hoặc các dẫn chắt coumarin
khác) với prasugrel (xem mục 4. 4).
Các thuốc chống viêm phi steroid (NSAID): sử dụng đồng thời prasugrel và các thuốc NSAID thời gian
dải chưa được nghiên cứu Do lảm tăng nguy cơ xuất huyết, nên thận trọng khi phối hợp prasugrel với các
thuốc NSAID thời gian dải (bao gồm cả các thuốc ức chế COX-2) (xem mục 4. 4).
Efient có thế sử dụng được đồng thời với các thuốc chuyền hóa qua enzym cytochrom P450 (bao gổm các
statin), hoặc các thuôo gây cảm ứng hoặc ức chế enzym cytochrom P450. Efient có thế được dùng cùng
acid acetylsalicylic, heparin, digoxin và các thuốc lảm tăng H dịch vị, bao gồm cả cảc thuốc ức chế bơm
proton vả ức chế thụ thể Hz. Mặc dù chưa có nghiên cứu ve các tương tác chuyên biệt nảy, trong nghiên
cứu lâm sảng pha 3, Efient đã được dùng cùng với heparin trọng lượng phân tử thẩp, bivalirudin vả cảc
ỄỀỀỄI
\'.anf
thuốc ức chế GP IIb/llla (chưa có các thông tin về loại thuốc ức chế GP llblllla được sử dụng) vả chưa
ghi nhận được cảc dâu hiệu về tương tảc bât iợi có ý nghĩa lâm sảng.
Ánh hưởng của các thuốc khác rrẻn Efient:
Acid acetylsalicylíc: Efient được dùng đồng thời với acid acetylsalicylic (ASA)
Mặc dù có thế có tương tác dược lực học với acid acetylsaiicylic dẫn đến tăng nguy cơ xuất huyết, cảc
bằng chứng cho thấy hiệu quả vả độ an toản của prasugrel trên bệnh nhân được điếu trị đồng thời với
ASA.
Heparín:
Truyến tĩnh mạch nhanh liều đơn heparin không phân đoạn (liều 100 Ufkg) lảm thay đối không đảng kề
tảc dụng ức chế kết tập tiếu cầu cùa prasugrcl. Tương tự, prasugrel lảm thay đổi không có ý nghĩa tác
dụng chống đông của heparin. Do đó, có thể sử dụng đổng thời prasugrel vả heparin. Nguy cơ xuất huyết
có thế tãng khi dùng Efient cùng với heparin.
Statins: Atorvastatin (liều 80 mg/ngảy) không lảm thay đổi dược động học cùa prasugrel vả tác dụng ức
chế chống kết tập tiếu câu của thuôo Do đó, các statin, cơ chất cùa CYP3A, không ảnh hưởng đến dược
động học hoặc tác dụng chống kết tập tiếu cầu của prasugrel.
Các thuốc Iảm tăng pH dịch vị: đùng đồng thời ranitidỉn (thuốc ức chế thụ thể Hz) hoặc lansoprazol
(thuốc ức chế bơm proton) hảng ngảy không lảm thay đối diện tích dưới đượng cong AUC chắt chuyến
hớa có hoạt tính cùa prasugrel và T,… nhưng lảm giảm C,… tương ứng 14% và 29%. Trong iên cứu
lâm sảng pha 3, Efient được sử dụng mã không cẩn cân nhắc việc dùng cùng vói cảc thuốc ứẵếfỄơi
proton hoặc ức chế thụ thể Hz. Uống liều tân công 60 mg prasugrel không cùng với cảc thuốc ức c
proton có thế Iảm tảo dụng khời động cùa thuốc nhanh hơn.
Các thuốc ức chế CYP3A: Ketoconazol (liều 400 mg hảng ngây), thuốc ức chế mạnh và chọn lợc
CYP3A4 vả CYP3AS, không ảnh hưởng đến tác dụng’ ưc chế kết tập tiều cầu của prasugrel hoặc diện tich
dưới đường cong AUC của chất chuyến hóa có hoạt tính cùa Prasugrcl và T.… nhung lảm gỉảm C,…từ
34% đến 46%. Do đó, cảc thuốc ức chế CYP3A như các thuoc khảng nẩm azol, các thuốc ức chế HIV
protease, clarithromycỉn, telithromycin, verapamil, diltiazcm, indinavir, ciprofioxacin và nước ép bưới
đắng ảnh hưởng không có ý nghĩa đến dược động học cùa chẩt chuyến hóa có hoạt tính của prasugrel
Các thuốc gáy cảm ứng cytochrom P450. Rifampicin (600 mg/ngảy), thuốc gây cảm ứng mạnh CYP3A
vả CYPZBó, vả gây cảm ứng với CYP2C9, CYP2CI9 vả CYP2C8 không Iảm thay đối có ý nghĩa dược
động học cùa prasugrel. Do đỏ, cảc thuốc gây cảm ứng CYP3A đã được biết đến như rifampicin,
carbamazepin vả cảc thuốc cảm ứng cytochrom P450 khảo được dự kiến không có ảnh hưởng đáng kể đển
dược động học cùa chất chuyền hóa có hoạt tính cùa prasugrel.
Ảnh hưởng của Etzent trên căc thuốc khác:
Digoxin: Prasugrel không gây ảnh hưởng có ý nghĩa lâm sảng đến dược động học của digoxin.
Các thuốc chuyến hóa qua CYP2C9: Prasugrel không' ưc chế CYP2C9, do đó không ảnh hướng đến dược
động học cùa S—warfarin. Do lảm tăng nguy cơ xuất huyết, nên thận trọng khi sử dụng đồng thời warfarin
vả Efient (xem mục 4. 4).
Các thuốc chuyến hóa qua C YPZBỔ Prasugrcl có tảc dụng ức chế yếu CYP2B6. Trên người tình nguyện
khỏe mạnh, prasugrel lảm giảm 23% nông độ hydroxybupropion sau chuyến hóa trong tuần hoân, một
chẳt chuyền hỏa cùa bupropion qua trung gian CYPZBó. Tác dụng nảy có liên quan trên lâm sảng chỉ khi
\!
\ *ì.'An›.
prasugrel dùng cùng cảc thuốc chỉ chuyến hóa qua con đường CYPZBó và có khoảng điểu trị hẹp (ví dụ
oyclophosphamid, efavirenz).
4.6 Ành hưởng trên sinh sản, phụ nữ có thai và cho con bú
Chưa có các nghiên cứu lâm sảng được thực hiện trên phụ nữ có thai và cho con bú
Các nghiên cứu trên động vật không chỉ ra tác hại trưc tiếp của thuốc trên phụ nữ có thai, trên sự phảt
triển cùa bảo thai/ thai nhi, quá trình sinh sản hoặc phảt triên sau khi sinh (xem mục 5.3). Do cảc nghiên
cứu về khả năng sinh sản trên động vật không phải iuôn phản ánh đủng đáp ứng trên người, chỉ nên sử
dụng Efient cho phụ nữ có thai khi lợi ich của thuốc với người mẹ vượt trội nguy cơ gây hại cho thai nhi.
Chưa bỉết rõ prasug_rel có bải tiết qua sữa mẹ trên người hay không. Các nghiên cửu trên động vật cho
thây prasugrel bải tiêt qua sữa mẹ. Không khuyên cảo sử dụng prasugrel trong thời kỳ cho con bủ.
Prasugrel không ảnh hướng đến khả năng sỉnh sản trên cả chuột oống đực và cải ở liếu uống lên đến gấp
240 lần Iiếu duy trì được khuyến cảo sử dụng trên người (tính theo mg/m2 diện tích cơ thế)
4.7 Ảnh huởng trên khả năng lái xe vè vận hânh máy mớc
Chưa có oảc nghiên cứu được thực hiện trên khả năng lái xe vả vận hảnh máy móc. Prasugrel được dự
kiến là không có ảnh hướng hoặc ảnh hưởng không đảng kể trên khả năng lái xe vả vận hảnh máy móc.
4.8 Tác dụng không mong muốn
a. T óm Iắt các dữ liệu về đọ an toâncủa thuốc
Độ an toản cùa thuôo trên bệnh nhân hội chứng mạch vảnh cấp có chỉ định cạn thiệp mạch vảnh dưới da
đã được đảnh giá trên một nghiên cứu có đối chứng sư dụng clopidogrel (TRITON) trong đó 674,1bệnh
nhân đã được điếu trị bằng prasugrel (liếu tắn công 60 mg vả liêu duy trì 10 mg hảng ngảy) t thời
gian trung bình 14,5 tháng (5802 bệnh nhân được điếu trị trên 6 tháng, 4136 bệnh nhân điếu t lỆến 1
năm). Tỷ lệ ngùng điếu trị do cảc biến cố bất lợi của thuốc là 7,2% đối với prasugxel và 6, 3% doi với
clopidogrel. Trong số đó, xuất huyết 1ả phản ứng phụ thường gặp nhắt phải dưng điếu trị cùa cả hai thuốc
(2, 5% đối với prasugrel và 1,4% đối với clopidogrel).
X uẩt huvết
Biến cố xuất huyết khỏng liên quan đến hẫu thuật bắc cầu mạch vânh
Trong nghiên cứu lâm sảng TRITON, tân xuất bệnh nhân khộng phẫu thuật bắc cẩu mạch vảnh Iiến quan
đến biến cố xuất huyết được trinh bảy trong bảng 1. Tần suât xuât huyết nghiêm trọng không liên quan
đến liệu phảp tiêu huyết khối trong nhổi mảu cơ tim trên bệnh nhân phẫu thuật bắc cầu mạch vảnh, bao
gồm cả xuất huyết đe dọa tinh mạng và gây tử vong, cũng như xuất huyết không nghiếm trọng do 1iệu
pháp tiêu huyết khối trong nhổi mảu cơ tim trên bệnh nhân điều trị bằng prasugrel cao hơn có ý nghĩa
thống kê so với nhóm bệnh nhân dùng clopidogrel bệnh nhân đau ngực không on định/nhổi mảu oơ tim
đoạn ST không chênh (UA/NSTEMI) vả tât cả nhóm bệnh nhân bị hội chứng mạch vânh câp (ACS). Sự
khảo biệt không có ý nghĩa được ghi nhận trên nhỏm bệnh nhân nhồi máu cơ tim doạn ST ohênh (STEMI).
Cảo vị trí xuât huyết tự phát thường gặp là đường tiêu hóa (tỷ lệ 1, 7% với prasugrel vả 1 ,3% với
clopidogrel); vị trí gây nên xuât huyết thường gặp nhất lả thủng động mạch (tỷ lệ 1, 3% với prasugrci vả
1,2% với olopidogrel).
\”uh
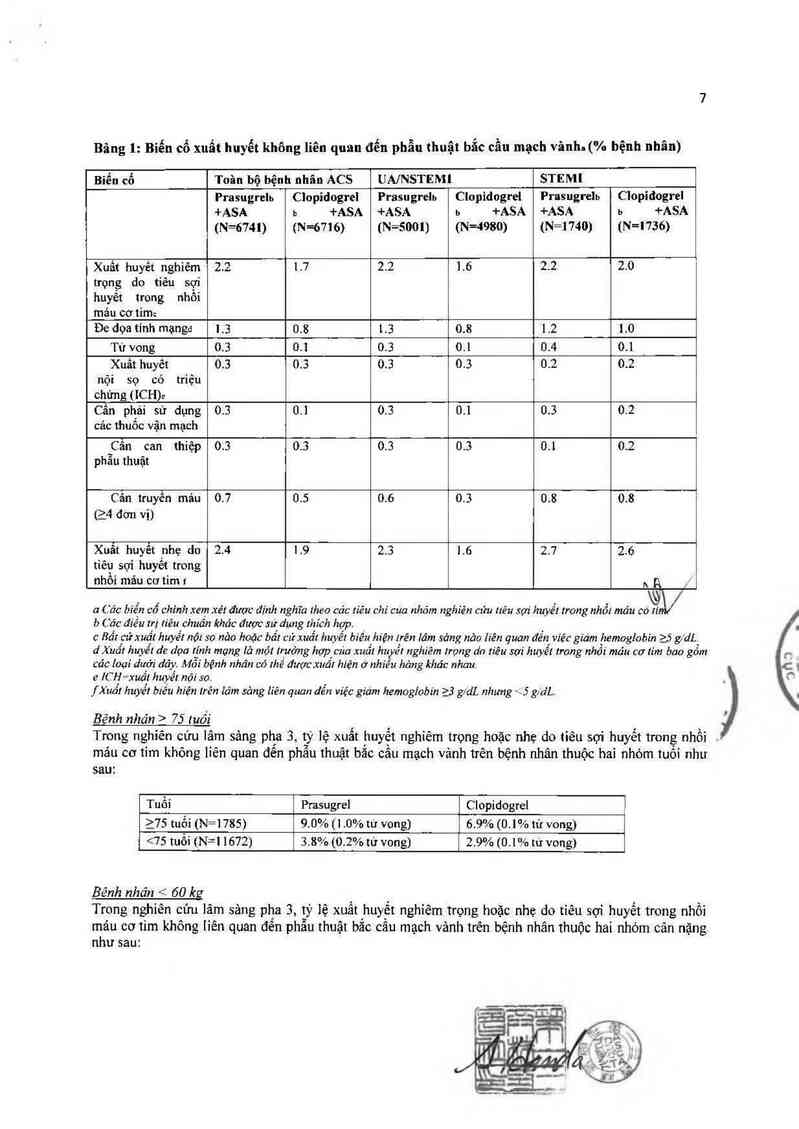
Bảng 1: Bỉến cổ xuất huyết không liên quan đến phẫu thuật bắc cầu mạch vânh. (% bệnh nhân)
Biển cổ Toản bộ bệnh nhân ACS UA/NSTEMI STEMI
Prasugreln Clopidogrel Prasugrelu Clopidogrel Prasugrelu Clopiđogrel
+ASA !: +ASA +ASA b +ASA +ASA h +ASA
(N=6741) (N=6716) (N=5001) (N=4980) (N=1740) (N=I736)
Xuất huyết nghiêm 2.2 1.7 2.2 1.6 2.2 2.0
trợng do tiêu sợi
huyết trong nhồi
mảu cơ tim
Đo dọa tỉnh mạnga 1.3 0.8 1.3 0.8 1.2 1.0
Tử vong 0.3 0.1 0.3 0.1 0.4 0.1
Xuất huyết 0.3 0.3 03 0.3 0.2 0.2
nội sọ có triệu
chứng (ICH)e
Cẩn phái sư dụng 0.3 0.1 0.3 0.1 0.3 0.2
cảc thuốc vận mạch
Cân can thiệp 0.3 0.3 0.3 0.3 0.1 0.2
phẵuthuật
Cân truyện mảu 0.7 0.5 0.6 0.3 0.8 0.8
(24 dơn vị)
Xuất huyễt nhẹ do 2.4 1.9 2.3 1.6 2.7 2.6
tiêu sợi huyết trong
nhồi mảu cơ tim f R R Ị.f
/
a (` ác biến có chính xem xét được định nghĩa rheo cảc riêu chi cua nhỏm nghiên cứu tiêu sợi huyết trong nhồi máu co It'lế/
b (` ác điều trị liêu chuẩn khúc được sư dụng ih1'ch hợp. .
c Rất cứxuốl huyết nôi sọ nòo hoặc bất cửxuốr huyết bíẽn hiện trên lâm sờng não Iiẽn quan đến việc giam hemoglobin 25 gde
d Xuất huyết de dọa n’nh mạng lẻ: một trường hợp của xuất huyết nghiêm trọng do tiêu SỢÍ hưyết trong nhối" mău cơ tim bao gốm r-
cđc loại dười dảy. Mỗi bệnh nhân có [hề được xuảt hiên ơ nhiêu hảng khớc nhau c |
19 IC H -xuat huyết nội sọ. . "
f X ua! huyết biên hiên trên iâm sảng iiên quan dển việc giam hemoglobin 23 gde nhưng a5 gidL. ,
Bẻnh nhán > 75 iuó'i
Trong nghiên cứu lâm sảng pha 3, tỷ lệ xuất huyết nghiêm trọng hoặc nhẹ do tiêu sợi huyết trong nhổi .
mảu cơ tim khỏng liẽn quan dến phẫu thuật bắc câu mạch vảnh trên bệnh nhân thuộc hai nhóm tuõi như
sau:
Tuổi Prasugrel C lopidogrel
ì75 tuổi (N=1785) 9.0%(1.0%tứ vong) 6.9%(0.1% tử vong)
<75 tuổi (N=l 1672) 3.8% (0.2% tử vong) 2.9%(0.1%111 vong)
Bênh nhân < 60 kg
Trong nghiên cứu lâm sâng pha 3, tỷ lệ xuất huyết nghiêm trọng hoặc nhẹ do tiêu sợi huyết trong nhổi
máu cơ tim không liên quan đến phẫu thuật bắc câu mạch vảnh trên bệnh nhân thuộc hai nhóm cân nặng
như sau:
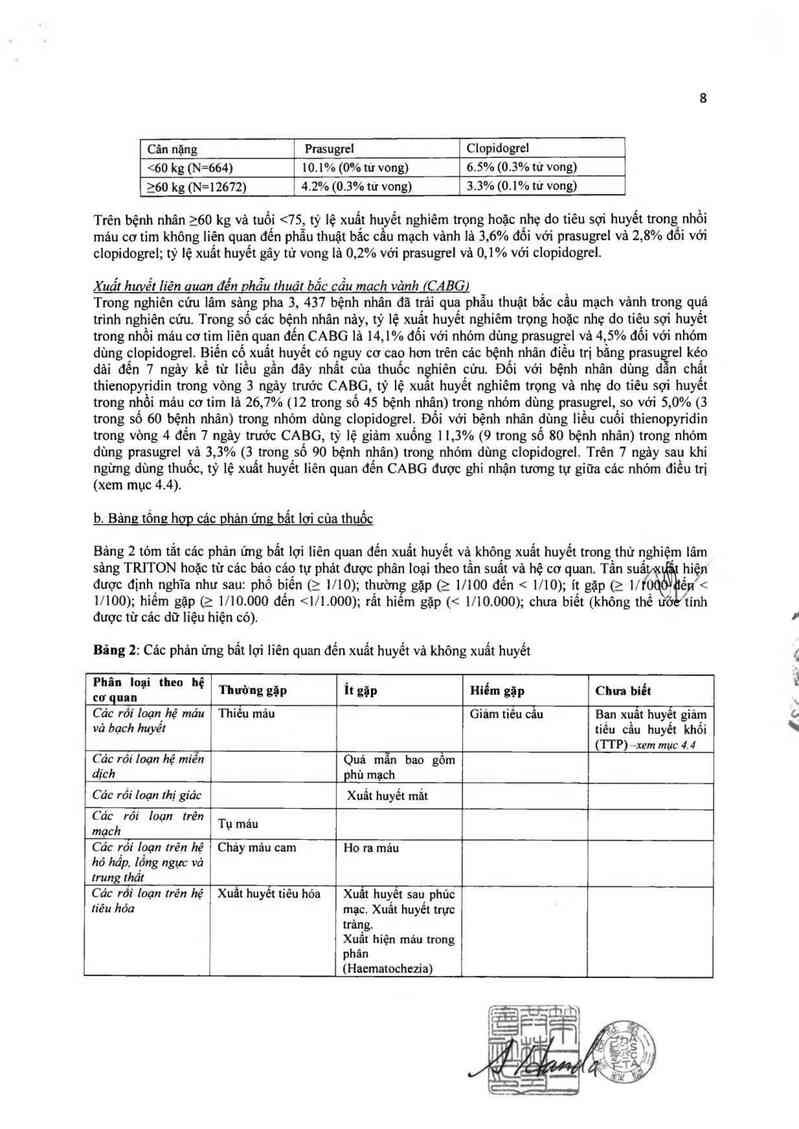
Cân nặng Prasugrel Clopidogrel
<60 kg (N=664) 10.1% (0% tư vong) 6.5% (0.3% tử vong)
_>_60 kg (N=12672) 4.2% (0.3% tử vong) 3.3% (0.1% tu vong)
Trên bệnh nhân >60 kg vả tuổi <75, tỷ lệ xuất huyết nghiêm trọng hoặc nhẹ do tiêu sợi huyết trong nhổi
mảu cơ tỉm không liên quan đến phẫu thuật bắc cẩu mạch vảnh là 3, 6% đối với prasugrel vả 2, 8% đối với
ciopidogrel; tỷ lệ xuất huyết gây tử vong lả 0,2% với prasugrcl và 0, 1% với clopidogrel.
Xuất huvết liên auan đến phẫu thuât bắc cầu mach vảnh (CABG)
Trong nghiên cứu lâm sảng pha 3, 437 bệnh nhân đã trải qua phẫu thuật bắc cầu mạch vảnh trong quá
trình nghiến cứu. Trong sô oáo bệnh nhân nảy, tỷ lệ xuất huyết nghiêm trỌng hoặc nhẹ do tiếu sợi huyết
trong nhổi mảu cơ tim liên quan đến CABG là 14,1% đối với nhóm dùng prasugrei vả 4, 5% đối với nhóm
dùng clopidogrel Biến cố xuất huyết có nguy cơ cao hơn trên cảc bệnh nhân điếu trị bằng prasu el kéo
dải đến 7 ngảy kế từ 1iếu gẳn đây nhất của thuốc nghiên cứu. Đối với bệnh nhân dùng dan chất
thienopyridin trong vòng 3 ngảy trước CABG, tỷ lệ xuât huyết nghiêm trọng và nhẹ do tiêu sợi huyết
trong nhồi mảu cơ tim iâ 26, 7% (12 trong số 45 bệnh nhân) trong nhóm dùng prasugrel, so với 5,0% (3
trong số 60 bệnh nhân) trong nhóm dùng clopidogrel Đối với bệnh nhân dùng liếu cuối thienopyridin
trong vòng 4 đến 7 ngảy trước CABG, tỷ lệ giảm xuống 11,3% (9 trong sô 80 bệnh nhân) trong nhóm
dùng prasugrel vả 3,3% (3 trong số 90 bệnh nhân) trong nhóm dùng clopidogrel. Trên 7 ngảy sau khi
ngừng dùng thuốc, tỷ lệ xuất huyết liên quan đến CABG được ghi nhận tương tư giữa các nhỏm điều trị
(xem mục 4.4).
b. Bảng tổng hợp các phản ứng bẩt lơi oùa thuốc
Bảng 2 tóm tắt cảc phản ứng bất lợi liên quan đến xuất huyết và không xuất huyết trong thử nghiệm lâm
sảng TRITON hoặc từ cảc bảo cảo tự phát được phân loại theo tần suât và hệ cơ quan Tần suấtqc hiẹn
được định nghĩa như sau: phổ biến (> 1/10); thường gặp (> 1/100 đến < 1/10); ít gặp (> 1/1'0ữ ênế<
1/100); hiếm gặp (> 1/ 10 000 đến <1/1 000); rât hỉêm gặp (< 1/ 10 000); chưa biết (không thế ư' tính
được từ cảc dữ liệu hiện có).
Bảng 2: Các phản ứng bất lợi liên quan đến xuất huyết và không xuất huyết
Phân loại theo hệ
cơ quan Thường gặp It gặp Hiếm gặp Chưa biết
Các rỏi Ioạn_hệ máu Thỉễu máu Giám tiêu cầu Ban xuât huyêt giảm
vả bạch huyêt tiếu cầu huyết khổi
` _ (TTP) --xem mục 4. 4
Các rỏi loạn hệ miên Quả mân bao gôm
dịch phù mạch
Các rồi !oạn thị giác Xuất huyết mắt
Cac ro: Ioạn tren Tụ máu
mạch
Các róí Ioạn trên hệ Chảy mảu cam Ho ra mảu
hô hẩp, lộng ngực vả
trung ihât
Các rỏi Ioạn trẻn hệ
!iẻu hóa
Xuất huyết tiêu hóa
Xuất huyết sau phủc
mạc. Xuất huyết trực
trảng.
Xuât hiện máu trong
phân
(Haematochezia)
L\
lcw
Chảy máu nướu
Các rồi Ioạn trẻn da Phát ban tụ máu
và mỏ duởi da
Các rỏi Ioạn trẽn Tiêu ra máu
thận và dường niệu
Các rối Ioạn chung Tụ mảu tại vị tự vỡ
vả tại vị trí đưa mạch. Xuât huyêt tại
thuôo vị trí vỡ mạch
Chản thương, ngộ Đụng dập Xuât huyết sau mô Tụ máu dưới da
độc và các biên (Contusion)
chứng kèm theo
Trên bệnh nhân có hoặc không có tiền sử cơn thiếu máu não thoáng qua (TIA) hoặc đột quỵ, biến cố đột
quy trong nghiên cứu lâm sâng pha 3 được trình bảy dưới đây (xem mục 4.4):
Tiến sứ TlA .
hoặc độ t quỵ Prasugrel Clop1dogrel
Có (N=518) 6.5% (2.3% lCH*) 1.2% (0% ICH")
Không (N=13090) 0.9% ( 0.2% ICH*) 1.0% (0.3% ICH*)
' [C H =xuấr huyết nội sọ
T hông bảo cho bác sĩ những tác dụng không mung muốn gặp phải khi sử dụng thuốc
4. 9 Quá liều
chưa có cảc dữ liệu về sự đảo ngược tảo dụng dược lý oủa prasugrel; tuy nhiến, nếu cân nhanh cho
chinh thời gian chảy máu kéo dải, có thể xem xét truyền tiêu câu vả/hoậc oảc chế phẩm mảu khảo
Quả liếu Efient có thể dẫn đến kéo dải thời gian chảy mảu và kéo theo các biến Iohứng xuất hun
1e
s. ĐẶC TÍNH DƯỢC LÝ
5.1 Đặc tính dược lực học
Nhóm dược lý điều trị : Chống kết tập tiều cầu không phải heparin
Mã ATC : BOlAC22
Dươc Iưc hoc
Prasugrel lá thuốc ức chế hoạt hóa và kết tập tiểu cẩu thông qua sự gắn không hồi phục chất chuyến hỏa
có hoạt tính của thuốc với nhóm P2Y12 cùa receptor ADP trên tiếu cầu. Do tiêu cẩu tham gia vảo quá trình
khởi động vả/hoặc tiến triến cùa các biến chứng huyết khối trong xơ vữa động mạch, ức chế chức năng
cùa tiêu câu có thể Iảm giảm các biến cố tim mạch như tử vong, nhồi mảu cơ tim hoặc đột quỵ.
Sau khi dùng liếu tấn công 60 mg prasugrel, tác dụng ức chế kết tập tiếu cầu thộng qua cảm ứng ADP
xuất hiện sau 15 phút với 5ụM ADP vả 30 phút với 20 ụM ADP. Tảo dụng ức chế kết tập tiếu cầu tối đa
thông qua cảm ứng ADP của prasugrei là 83% với 5 M ADP và 79% với 20 ụM ADP, trong cả hai
trường hợp 89% người khỏe mạnh và bệnh nhân xơ vữa động mạch ỏn định đạt được tỷ lệ ức chế kểt tập
tiêu câu ít nhất 50% trong 1 giờ. Tác dụng ức chế của prasugrel thông qua trung gian kểt tập tiếu cầu thế
hiện sự thay đối thẳp giữa cảc đối tượng (9%) vả trong từng đối tượng (12%) ở cả nổng độ 5 M và 20
ụM ADP. Tảc dụng ức chế kết tập tiêu câu trung binh ở trạng thải ổn định tương ứng lả 74% và 69% ở
nồng độ 5 M và 20 ụM ADP, đạt được sau 3 đến 5 ngảy dùng prasugrel liều duy trì 10 mg tiếp theo liều
10
tắn oông 60 mg. Hơn 98% người dùng thuốc đạt được tác dụng ức chế kết tập tiểu cầu 220% trong thời
gian dùng liều duy trì.
Quả trinh kết tập tiếu cầu dần trở về giá trị ban đầu trước điếu trị sau 7 đến 9 ngảy dùng prasugrel liếu tắn
công 60 mg vả sau 5 ngảy sau khi ngừng dùng liểu duy trì ở trạng thải òn định.
Clogidogelz Sau khi dùng liều 75 mg clopidogrel một lần trong ngảy trong 10 ngảy, 40 người khóc mạnh
được chuyến sang dùng prạsugrel 10 mg một lần trong ngảy có hoặc không dùng liều tấn công 60 mg
Tảo dụng ức chế kểt tập tiêu câu tương tự hoặc cao hơn đã được ghi nhận với prasugrel. Chuyền ngay
sang liếu tấn công prasugrel 60 mg cho phép khởi động nhanh nhất tác dụng” ưc ohế tiêu cầu cao hơn Sau
khi dùng liếu tấn công 900 mg clopidogrel (kết hợp acid acetylsalicylic), 56 bệnh nhân có hội chứng
mạch vảnh cẫp được điều trị trong 14 ngảy với prasugrel 10 mg một lần/ngảy hoặc clopidogrel 150 mg
một lần/ngảy, sau đó chuyển sang dùng oiopidogrel 150 mg hoặc prasugrel 10 mg trong 14 ngảy tiểp theo.
Tác dụng ức chế kết tập tiêu câu cao hơn đã được ghi nhận trên nhóm bệnh nhân chuyến sang dùng
prasu el 10 mg so với dùng clopidogrel 150 mg. Hiện ohưa cớ cảc dữ 1iệu vê việc chuyến đối trực tiếp từ
liều tân công ciopidogrel sang liêu tân công prasugrel.
Hiẻu gua` vả đo an toản trong hói chứng mach vảnh cấg [ACSỊ
Nghiên cứu lâm sảng pha 3 TRITON đã so sảnh Efient (prasugrel) với clopidogrel, cả 2 thuốc đếu dùng
kết hợp với acid aoetylsalicylio vả liệu pháp điếu trị chuẩn khảo. Nghiên cứu TRITON là một nghiên cửu
đa quốc gia, ngẫu nhiên, mù đôi, có nhóm song song bao gồm 13608 bệnh nhân. Bệnh nhân có hội ohứng
mạch vảnh câp với nguy cơ đau thắt ngực không on định (UA), nhồi mảu cơ tim không có đoạn ST enh /
(N STEMI) hoặc nhồi máu cơ tim oó đoạn ST chênh (STEMI) từ trung bình đến cao và đã được kiếiẵìo'
bằng can thiệp mạch vảnh qua da V
Bệnh nhân có UA/NSTEMI __trong vòng 72 giờ có triệu chứng hoặc STEMI từ 12 giờ đến 14 ngảy có triệu
chứng được phân nhớm ngẫu nhiên sau khi có kết quả giải phẫu mạch vảnh. Bệnh nhân STEMI trong
vòng 12 giờ có triệu chứng vả đã được 1ên lịch can thiệp m_ạoh vảnh qua da sớm có thế được _phân nhóm
n ẫu nhiên mà không cân kết quả giải phẫu mạch vảnh. Tất cả các bệnh nhân có thể dùng liểu tấn công
bat cứ lủc nảo trong quá trình phân nhóm và 1 giờ sau khi bệnh nhân rời khỏi phòng can thiệp mạch.
Bệnh nhân được phân nhỏm dùng prasugrel (liếu tấn công 60 mg, tiếp theo dùng liều 10 mg một
1ần/ngảy) hoặc ciopidogrel (1iều tấn công 300 mg, tiếp theo dùng liều 75 mg một lầnlngảy) được điếu trị
trong thời giẫm trung bình 14,5 tháng (tối đa 15 thảng với ít nhất 6 tháng theo dõi sau đó) Bệnh nhân
cũng được uổng acid acetylsalicylic (75 mg đến 325 mg một lần/ngảy) Bệnh nhân có sư dụng bất cứ dẫn
chất thienopyridin nảo t_rong vòng 5 ngảy trước khi tham gia đếu bị loại khỏi nghiên cứu. Các thuốc điều
trị khác, như heparin và các thuốc ức chế GPIIb/Illa được dùng theo chỉ định oùa bác sĩ. Khoảng 40%
bệnh nhân (trong mỗi nhóm điếu trị) được dùng c_ác thuốo' ưc chê GPllb/llla để hỗ trợ cho phẫu thuật can
thiệp mạch vảnh qua da (hiện chua có thông tin về loại thuốc ức chế GPHb/llla đã sử dụng). Khoảng 98%
bệnh nhân (trong mỗi nhóm điều trị) dùng thuốc chống đông (heparin, heparin trọng lượng phân từ thấp,
bivalirudin hoặc các thuốc khảo) trực tiếp để hỗ trợ phẫu thuật can thiệp mạch vảnh dưới da.
Cảo tiêu chí đánh giá chính trong thử nghiệm lâm sảng lả thời gian xuất hiện lẩn đầu một trong các biến
cố sau: tử vong do các bệnh tim mạch (CV), nhồi mảu cơ tim không gây tử vong (MI) hoặc đột qt_1y
không gây tử vong. Phân tích cảc ohi tiêu then chổt trên tất cả cảc bệnh nhân có hội chứng mạch vảnh cấp
(kết hợp cả nhóm UA/NSTEMI vả STEMI) dựa trên oảc số liệu thổng kế đã oho thấy hỉệu quả vượt trội
cùa prasugrel so với clopidogrel trên nhóm bệnh nhân UA/NSTEMI (p<0, 05).
11
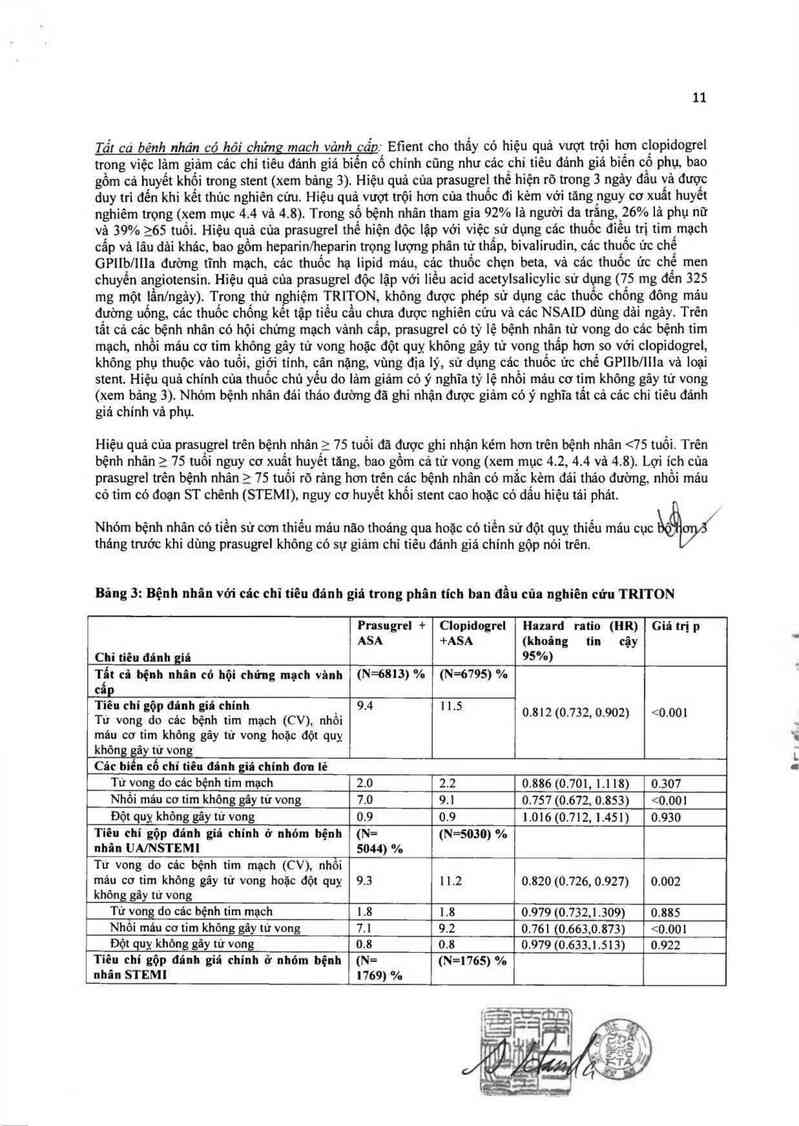
Tốt ca bênh nhăn có hôi chứng mach vảnh cấg:_ Efient cho thấy có hiệu quả vượt trội hơn ciopidogrel
trong việc lảm giảm các chỉ tiêu đánh giá biến cố chinh cũng như các chi tiếu đảnh giả biến có phụ, bao
gôm oả huyết khối trong stent (xem bảng 3). Hiệu quả của prasugrel_ thế hiện rõ trong 3 ngây đầu và được
duy trì đến khi kết thúc nghiên cứu. Hiệu quả vưọt trội hơn của thuốc đi kèm với tăng nguy oơ xuất huyết
nghiêm trọng (xem mục 4. 4 vả 4. 8) Trong số bệnh nhãn tham gia 92% lá người da trắng, 26% lá phụ nữ
và 39% >65 tuổi. Hiệu quả của prasugrel thể hiện độc lập với việc sử dụng các thuốc điếu trị tim mạch
cấp vả lâu dải khác, bao gôm heparinlheparin trọng lượng phân từ thấp, bivalirudin, cảc thuốc ức chế
GPllblllla đưòng tĩnh mạch, cảc thuốc hạ lipid mảu, cảc thuốc chẹn beta, vả cảc thuốc ức chế men
chuyển angiotensỉn Hiệu quả cùa prasugrel độc lập với liếu acid acetylsalicylic sư dụng (75 mg đến 325
mg một _iầnlngảy). Trong thử nghiệm TRITON, không được phép sử dụng cảc thuốc chống đông máu
đường uông, các thuốc chống kêt tập tiếu cầu chưa được nghiên cứu vả cảc NSAID dùng dải ngảy. Trên
tât cả các bệnh nhân có hội chưng mạch vảnh cấp, prasugrel có tỷ lệ bệnh nhân tử vong do cảo bệnh tim
mạch, nhồi máu cơ tim không gây tử vong hoặc đột quỵ không gây tử vong t_hấp hơn so với olopidogrel,
không phụ thuộc vảo tuôi, giới tinh, cân nặng, vùng địa Iỷ, sủ dụng các thuốc ức chế GPilbllila và loại
stem. Hiệu quả chính của thuốc chủ yếu do 1ảm giảm có ý nghĩa tỷ lệ nhồi mảu cơ tim không gây tử vong
(xem bâng 3). Nhóm bệnh nhân đái thảo đường đã ghi nhận được giảm oó ý nghĩa tắt cả các chi tiêu đánh
giá chính và phụ.
Hiệu quả cùa prasugrel trên bệnh nhân > 75 tuổi đã được ghi nhận kém hơn trên bệnh nhân <75 tuổi Trên
bệnh nhân > 75 tuồi nguy cơ xuất huyết tăng, bao gôm cả tử vong (xem mục 4 2, 4. 4 vả 4. 8). Lợi ich của
prasugrel trên bệnh nhân 2 75 tuổi rõ rảng hơn trên các bệnh nhân có mắc kèm đải thảo đường, nhổi mảu
cò tim có đoạn ST chênh (STEMI), nguy cơ huyết khối stem cao hoặc có dắu hiệu tải phát.
Nhớm bệnh nhân có tiểu sử cơn thiếu mảu não thoảng qua hoặc có tiền sử đột quỵ thiếu máu cục bợẳỹẮ
tháng trước khi dùng prasugrel không có sự giảm chi tiêu đánh giá chính gộp nói trên.
Bảng 3: Bệnh nhân vói các chỉ tiêu đânh giả trong phân tích ban đầu của nghiên cứu TRITON
Prasugrel + Clopidogrel Hazard ratio (HR) Giátrịp
ASA +ASA (khoảng tin cậy
Chỉ tiêu đảnh giá 95%)
Tất cả bệnh nhân có hội chưng mạch vânh (N=6813) % (N=6795) %
cấp
Tiêu chỉ gộp đảnh giả chính 9.4 1 1.5
Tư v0ng do cảc bệnh tim mạch (CV), nhồi 0'812(0'732’0902) 75 tuối) so với các bệnh nhân <]5 tuồi. Nên thận trọng khi sử dụng prasugrel
cho bệnh nhân > 75 tuổi do nguy cơ xuất huyết cao trên nhóm bệnh nhân nảy (xem mục 4. 2 và 4. 4).
Suỵ gan: Không cần hiệu chinh liều trên bệnh nhân suy gan nhẹ đến trung binh (phân loại Chiid Pugh A
và B). Dược động học cùa prasugrel và tác dụng ức chế kết tặp tiếu câu cúa thuốc lá tương đương trên
người suy gan nhẹ đên trung binh so với người khỏe mạnh. Dược động học và dược lực học của prasugrel
14
trên bệnh nhân suy gan nặng chưa được nghiên cứu. Không được sử dụng prasugrel cho bệnh nhân suy
gan nặng (xem mục 4.3).
Su_v__ thân. Không cần hiệu chinh liều cho bệnh nhân suy thận, bao gồm cả bệnh nhân bị bệnh thận giai
đoạn cuối. Dược động học cùa prasu_grel vả tảo dụng ửc chế tiếu câu của thuốc tương đương trên bệnh
nhân suy thận trung bình (sức lọc câu thặn 30-<50m1/phut/ 1 73m-) và người khỏe mạnh. Tác dụng của
prasugrel qua trung gian ức chế kết tập tiều câu cũng tương tự trên bệnh nhân bệnh thận giai đoạn cuối
cân thẩm tich mảu so với người khóc mạnh, mặc dù C.…vả AUC của chất chuyển hớn có hoạt tính giảm
tương ứng 51% và 42% trên bệnh nhân bệnh thận giai đoạn cuối.
Trong lương cơ Ihế: Nổng độ trung bình của chất ohuyền hóa có hoạt tinh trong tuấn hoản cao hơn
khoảng 30% đến 40% trên người khóe mạnh và bệnh nhân cân nặng <60 kg so với bệnh nhân oân nặng
260 kg. Nên thận trọng khi sử dụng prasugrel cho bệnh nhân có cân nặng <60 kg do tăng nguy cơ xuât
huyết trên nhóm bệnh nhân nảy (xem mục 4.4).
C hungt Trọng cảc nghiến cứu dược lý lâm sảng, sau khi đã hiện chinh theo trọng lượng oơ thế, AUC
của chất chuyển hỏa có hoạt tính cao hơn khoảng 19% t_rên bệnh nhân Trung Quôc, Nhật Bản và Hản
Quốc so với bệnh nhân da trắng, chủ yếu liên quan đến nồng độ chất chuyến hóa có hoạt tinh trong tuần
hoản cao hơn trên bệnh nhân châu Á <60 kg. Không có sự khác biệt về nồng độ c_hất chuyến hóa có hoạt
tinh trong tuần hoản giữa cảc bệnh nhận Trung Quôc, Nhật Bản vả Hản Quôc. _Nổng độ chất chuyến hóa
có hoạt tính trong tuần hoản giảm xuống trên cảc bệnh nhân châu Phi và người gôc Tây Ban Nha tương
đương với người da trắng. Không oần thiết hiệu chinh liều nếu chỉ dựa trên chùng tộc đơn thuần.
Giới: Trên người khỏe mạnh và bệnh nhân, dược động học của prasugrel trên cả nam và nữ ảậÌtỹg/I
đương nhau.
Trẻ em vả thiếu niên: Dược động học vả dược lực học của prasugrel chưa được đảnh giá trên quần thể nảy
(xem mục 4.2).
5.3 Dữ liệu an toân tiểu lâm sâng
Dữ liệu tiến lâm sảng cho thấy không thấy mối nguy hại đặc biệt nảo trên người dựa trên cảc nghiên cứu
thông thường về an toản dược học, độc tính liếu lặp lại, độc tính trên gen, khả _năng gây ung thư hoặc độc
tính trên s_inh sản. Cảo nghiên cứu tiến lâm sảng được thực hiện ở nổng độ thuốc trong tuần hoản vượt quá
nồng độ tổi đa trên người do đó it cớ’ y nghĩa trong việc ngoại suy trên lâm sảng.
Các nghiên cứu về độc tính trên sự phát triến cùa bảo thai-thai nhi trên chuột vả thỏ không cho thấy bằng
chứng gây dị _tật của prasugrel. Ở mức iiều rất cao (>_240 lần liều duy trì hảng ngảy trên người tính theo
mg/mz) có thể gây ảnh hưởng đến trọng lượng cơ thể mẹ vảlhoặc mức tiêu thụ thức ăn, có sự giảm nhẹ
tr_ọng lượng cùa con sau khi sinh (so với lô chửng). _Trong các nghiên cứu trước và sau sinh trên chuột,
việc điếu trị cho mẹ không có ảnh hưởng đến hảnh vi hoặc phảt triên sinh sản trên oon ở liều gấp 240 lẩn
Iiếu duy trì được khuyến cảo trên người (tính theo mg/mz).
Không xuất hiện cảo khối u liên quan đến thuốc trong vòng 2 năm nghiên cứu trên chuột cống với nồng
độ pra_sugrel trong tuần hoản lớn hơn 75 l_ần nồng độ điều trị được khuyến cáo trên người (dựa trên nổng
độ chẩt chuyến hóa có hoạt tính trong tuấn hoản). Có tỷ lệ gia t_ăng các khối u (u tuyến tế bảo gan) trên
chuột nhắt phơi nhiễm thuốc trong 2 nãm với liều oao (> 75 1ần nổng độ trong tuân hoản trên người)
nhưng kết quả nảy được xem như tảo dụng thứ cấp liên quan đến khả nãng cảm ứng enzym cùa prasugrel.
Các khối u ở gan liên quan đặc biệt đến ioải gặm nhấm và khả năng cảm ứng emzym do thuốc đã được
!
15
ghi nhận trong y văn. Việc gia tảng cảc khối u ở gan khi dùng prasugre] trên chuột nhắt trắng không dược
coi là có nguy cơ trên người.
6. ĐẶC TÍNH CÙA DƯỢC PHẨM
6.1 Danh mục cảc tả dược
Efient 5 me
Phần lõi viên:
Cellulose vi tinh thể
Mannitol (Ẹ42 1 )
Natri croscarmellose
Hypromellose (E464)
Magnesium stearate
Phẫu mảng bao: n
Hỗn dịch bao mầu vậng gổm có: Lactose monohydrat, Hypromellose (E464), Titanium dioxiầ 17,1’),
Triacetin (E1518), Săt oxid mảu vảng(El 72) /
Tale
Efient 10 mg
Phẫn lõi viến:
Cellulose vi tinh thể
Mannitol (E421)
Natric croscarmellose
Hypromellose (E464)
Magnesium stearat
Phần mảng bao:
Hỗn dịch bao mầu be gổm có: Lactose monohydrat, Hypromellose (E464), Titanium dìoxìde (Ei7l),
Triacetin (El518), Sắt oxyd đò (E172), Sắt oxyd vảng (El 72)
Tale
6.2 Không tương thỉch
Không áp dụng.
6.3 Hạn dùng
2 năm,
6.4 Các chú ý bảo quân đặc biệt
Thuốc không dòi hỏi các điều kiện bảo quản đặc biệt. Bảo quản thuốc trong bao bì tránh không khí vả độ
ấm. Không bảo quản thuốc ở nhiệt độ trên 30 ° c.
6.5 Nguồn gốc và thânh phần bao gỏi
ìư
Hộp carton có 2 ví nhôm, mỗi vi nhôm có 14 viê
6.6 Các chú ý Xử lý đặc biệt
Không có yêu cầu đặc biệt.
7.0 Ngây cập uhật
9 thảng 11 năm 201]
Sản xuất bời: Eli Lilly and Company
Lilly Technology Center, Indianapolis, Indiana 46285, USA
Đóng gói bời: Lilly, S.A.,
Avda. de la Industria 30, 28108 Alcobendas, Madrid, Spain
TUQ. cục TRUỞNG
P.TRUỜNG PHÒNG
J*fauyễn Jẳfff ẩẳW
16
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng