













1'1’1 ' ,r
* "-1'H'…HJ ~,
13Ộ )( TẾ
CLỉC Qt'AN LY mfọ'ơ
… PHÊ DUYỆT
;f"~1 Lm: ỮdllÁq/ỐIỤÁỊ/
W)…u
M)…ưi mưu Im
… :'cu qnug
:Iuđls
1mo uọqnmmu1mpu umd nommụduzon oc
sm1qn 1919 08 `
xnmo 50lede on
eulJ1nidlwwmnldm
soueịqnm sopị1uudmoo
steMm PGIIOO-UJIU
sẹmomsd mudmoo
_ cthanoaệ
JM lỡ£²
ÝEDURANT®
JỒIÌSSGÍÌỈ
Fubnquú pm | Mlnulaclumd byl
Flbvimdo port
Jnnlun-Ciing S.p A.. Vn c Joneun.
m 8. M…. ouoo utim. mwmn-
€EDURANT®
comprimés pelliculés
rilplvlrlne
Iu -Mhùiưwtuu
EDunAm'
Mnnmuohwv mmg1monnq … 25mg
›…
M 1
wnmmọm Wllcllìvlln
ui qm mu …. :hdnụ chi 1… n … nhu 1…
…::úvmmmrguklùdumlhntnc
g2c ỦW DẦNWDWG Yw Im DW
IATffl TAVTIỂ EU
nuẵmụnnamwmmm Bloqulouunglu
gủc nmómum
mc n- uu - u
cme Junưvữn; Lu TM la
la Iu. IQI: JANBSEN CIIAG lPA an D J-1-m
(18: W s…)-wno u… 1… )(
5610 !! NSx HDum hla
ỸEDURANT®
fiIm—ooated tablets
rilpivirine
30 oral tableto
Do not nlom nbovo 30'C.
810… 111 thu ortq1nal bam ln «dut
m pfotonl Im Ight.
Keep 1:1u1 of … ơ1 onllđmn.
For ulroctinm Im uu.
su oncloud pockeqe mun
Elch 111m-coetod mmol conlllns nchno
m…wmmmptmm,
ÝEDURANT®
comprỉmldos recubiertos
rllplvlrlna
ao comprlmldos para
administraclón oral
Cuuórvou : … mu do 30'C.
ConlOrvoso nn d cnvm odghll
mm pmuann de In 1111.
Mnnltngnu Iuou dll ntmnou dl Ion ninon
Pare mu htotrnưion mủ… d pfupeclo.
Coca comprlm1do mu… comieno
cigmtmm de tl1plvin’nl oqulvulents
- n 15 mg dl HpMnm
SP_Edurant_FCT 25mg_v1
16
3
\
comprtnldou mub1crtcn
Ỉ rtlplvlrlno/rllplvlrlnn
BAGK PANEL MAXIMUM 1 COLOR
////2 l
_, f _ _
W
Connrvot duns lo them d' o11qlnc
è1' abrl đc Il 1um
Gaudcl hoa do lo ponón m mlonts.
sẹ—
Llrl mmuvomem II notlon
/ Do not siotnbov eSO'C
Stcue In the ollqtnnl butt1a In order
to protoct trom Ilnn_t.
Kch out o! tuctt of children
For dirncllom lot uu. uu nncloud /
/ pucma 1mn.
Condmu : no máu ae we
conurveu en el cnvane orlglnu1
porn protouodod o la luz.
Mn…gmh1ndcl a…deluonủ
|, / Pnrn … 1nlhnnmán unrm'lm
| 'Jf9Jom |
—/ỈJ ///, '—
' BASE PANEL MAXIMUM 1 COLOR
EDURANT' 25 mg /
011un oomprlml pel1iculóa oontlent une
quintt 1… 0111 ameoe rlemm
ôquivdonto A? mg de lttplvirlno
Each 111… mud tnblol oonnim
rllptvtrtnn ttẩroehlorldq equivalent to
mg 111p111111m
Cedn compnmldo roouhlotto comiene /
clcrhidmo do r11 lvlrim oqu1vllonh /
n 25 mo 0) r1lplvldnc /
PP_Edurant_FCT 25mg_v1
, Ể²EỊấU RANT®
Thuốc năy chi dùng theo đơn của bác sỹ.
Đ c kỹ hướng dẫn trước khi dùng.
N 11 câu thêm thông tin xin hỏi ý kiến bác sỹ hoặc dược sỹ.
THÀNH PHẨN
Mỗi viên nén bao phim chứa rilpivirine hydrochloride tương đương với 25 mg rilpivirine.
Viên nén bao phim có mảu từ trắng đến trắng ngả, tròn, hai mặt lồi có đường kính 6. 4 mm,
dập chữ "TMC" ở một mặt và sô "25” ở mặt còn lại.
Các tả dược:
Lôi viên nén
Lactose monohydrate
Croscarmellose sodium
Povidonc K30
Polysorbate 20
Cellulose vi tinh thể silic dioxid hóa
Magnesium stearate
Vỏ bao viên
Lactose monohydrate
Hypromellose 2910 6 mPa.s %
Titanium dioxide
Polyethylenc glycol 3000
Triacetin
CHI ĐỊNH
EDURANT, phối hợp với các thuốc khảng retrovirus khác, được chỉ định để điếu trị nhiễm
virus gây suy giảm miễn dịch ở người typl (HIV-l) ở những bệnh nhân từ 12 tuổi trở lên,
chưa từng điều trị thuốc khảng retrovirus trước đó, có tải lưọng virus 5 100.000 HIV—l
RNA bản sao/ml.
Xét nghiệm để khảng kiểu gen nên định hướng sử dụng EDURANT (xem CẢNH BÁO
VÀ THẶN TRỌNG vả ĐẶC TÍNH DƯỢC LỰC HỌC).
Giới hạn sử dụng:
. Cảc bệnh nhân điều trị bằng EDURANT có HIV-l RNA lớn hơn 100.000 bản
saolml khi bắt đằu điếu trị, bị thất bại về virus học (HIV 1 RNA > 50 bản saolml)
nhiều hơn so với cảc bệnh nhân được điều trị bằng EDURANT có HIV- 1 RNA nhỏ
hơn hoặc bằng 100.000 bản sao/m] (xem ĐẶC TÍNH DƯỢC LỰC HỌC).
9 Bất kể HIV- ] RNA khi bắt đầu điều trị ở mức nảo, các bệnh nhân được điều trị
bằng EDURANT có số tế bảo CD4+ nhỏ hơn 200 tế bảo/mm3 ,gặp thất bại về virus
học nhiều hơn so với cảc bệnh nhân dược điều trị bằng EDURANT mã có số tế bảo
CD4+ lớn hơn hoặc bằng 200 tế bảo/mm (xem ĐẶC TỈNH DƯỢC LỰC HỌC).
. Tỷ lệ thất bại điều trị quan sảt được trên cảc bệnh nhân điểu trị bằng EDURANT đã
cho thấy, tỷ lệ kháng với điều trị nỏi chung và khảng chéo với cảc thuốc nhóm ức
chế men sao chép ngược không có cấu trúc nucleosid (NNRTI) cao hơn so với
efavirenz (xem ĐẶC TÍNH DƯỢC LỰC HỌC).
Page 1 of 23
l’l Iz’a’umnl L'K SPL`ZJJUI.ZOM D.›1l'requcxl ."00c12016 v]
o Cảc bệnh nhân điều trị với EDURANT đặ phát triển sự đề kháng có liên quan'đến
tenofovir vả lamỉvudinefemtrỉcỉtabìnc nhiêu hơn so với efavirenz (xem ĐẶC TINH
DƯỢC LỰC HỌC).
LIÊU pÙNG vÀ CÁCH DÙNG
Nên bắt đầu điều trị với EDURANT bới bảo sĩ có kinh nghiệm ttong việc quản lý bệnh
nhãn nhiễm HIV
Liều dùng
Liều dùng khuyến cáo của EDURANT là một viên 25 mg uống một lần mỗi ngảy
EDURANT phải được uổng cùng với bữa an (xemĐẬC TIN H DUỢC ĐỘNG HỌC).
Điểu chình liều
Đối với những bệnh nhân đang dùng rifabutin, liều EDURANT cằn tăng lên 50 mg (hai
viên nén 25 mg mỗi lần) dùng một lần mỗi ngảy Khi ngừng dùng rifabutin, nên giảm liều
EDURANT xuống 25 mg một lần mỗi ngảy (xem TƯỚNG TÁC VỚI CÁC THUỐC
KHẢC VÀ CÁC LOẠI TƯỚNG TÁC KHÁC).
Bỏ lỡ liêu
Nếu bệnh nhân bỏ 1ỡ một liều EDURANT trong vòng 12 giờ kế từ thời điếm thường dùng
thuốc, bệnh nhân phải dùng thuốc sớm nhắt có thể cùng vởi một bữa ăn và tiếp tục lại chế
độ líều bình thường. Nếu bệnh nhân bỏ lỡ liều EDURANT vởi thời gian lớn hơn 12 gíờ,
bệnh nhân không nên dùng liều bị lỡ, mà vẫn tiếp tục chế độ iiều binh thường.
Nếu bệnh nhân nôn trong vòng 4 gỉờ sau khi uông thuốc, cần uống một viên EDURANT
khảo cùng với bưa an. Nêu bệnh nhân nôn sau khi uống thuốc hơn 4 giờ, bệnh nhân không
cẳn phải uống thêm một lỉều EDURANT cho đến khi dùng líếu kế tiếp.
Các quần thể bệnh nhân đặc biệt ứ/
Người cao tuôi
cần điều chỉnh liều EDURANT ở những bệnh nhân cao tuối (xem ĐẶC TÍNH DƯỢC
ĐỘNG HỌC). Cần sử dụng thận trọng EDURANT cho những bệnh nhân nảy.
Bệnh nhân suy thận
EDURANT chủ yếu đuợc nghiên cứu ở những bệnh nhãn có chức năng thận bình thương
Không cần điều chinh liều rilpivirine ở nhũng bệnh nhân suy thận nhẹ hoặc trung binh. Ở
bệnh nhân suy thận nặng hoặc bệnh thận giai đoạn cuôi, cần thận trọng khi dùng
rilpivirine Ở bệnh nhân suy thận nặng hoặc bệnh thận gỉai đoạn cuối chỉ nên sử dỤng phối
họp rilpivirine vởi thuốc ức chế CYP3A mạnh (ví dụ, chẩt ức chế protease HIV được tăng
nông độ bởi ritonavir), nếu 1ợỉ ích vượt trội nguy cơ (xem ĐẶC TÍNH DƯỢC ĐỘNG
HỌC).
Điều trị bằng rỉlpìvìrine lảm tãng nhẹ nồng độ creatỉnỉne huyết thanh trung bình ở giai
đoạn đẩu, duy trì ốn định theo thời ian vả không được coi là có ý nghĩa lâm sảng (xem
TÁC DỤNG KHÔNG MONG MU N)
Bệnh nhân suy gan
Thông tin vê việc sử dụng thuốc EDURANT ở bệnh nhân suy gan nhẹ hoặc trung bình
(điếm Child- -Pugh A hoặc B) còn hạn chế. Không cần điều chỉnh liều của EDURANT ở
những bệnh nhân suy gan nhẹ hoặc trung bình Cần sủ dụng thận trọng EDURANT ở
những bệnh nhân suy gan trung binh. EDURANT chưa được nghiên cứu ở những bệnh
Page 2 nf 23
P] Edurrznf_l-’KSPC 33111! 2016 DAl’rcqwst ỆíJOCI.ỆÚIÓ vJ
Thông.tin.vằviệc sừdụng EDURANTỜ nhủng…bệnh nhânè 65 tuối còn hạn chế.…Không . …
nhân bị suy gan nặng (điểm Chỉld-Pugh C). Do’đó, không khuyến cáo dùng EDURANT ở
những bệnh nhân bị suy gan nặng (xem ĐẶC TINH DƯỢC ĐỌNG HỌC).
Bệnh nhân trẻ em ,
An toản và hiệu quả cùa EDURANT ở trẻ em dưới 12 tuôi vân chưa được xảc định.
Hiện vân chưa có dữ liệu.
Cách dùng
EDURANT phải được dùng đường uống, một 1ần mỗi ngảy cùng vởi bữa an (xem ĐẶC
TÍNH DƯỢC ĐON G HỌC) Khuyến cáo uống nguyên viên nén bao phim cùng với nước
vả không được nhai hoặc nghiền.
CHỐNG CHỈ ĐỊNH
Quá mẫn với hoạt chất hoặc vởi bẩt kỳ tả dược nảo được liệt kê trong mục THÀNH
PHẦN.
Không phối hợp EDURANT với các thuốc sau đây, do sự gỉảm đáng kể nổng độ rílpivirine
trong huyễt tương có thể xảy ra (do cảm ứng enzym CYP3A hoặc tăng pH dạ dảy), và có
thể iảm mất tảo dụng điều trị cúa EDURANT (xem TƯơNG TÁC VÓT CÁC THUỐC
KHÁC VÀ CÁC LOẠI TƯỢNG TÁC KHÁC):
- thuốc chồng co gìật carbamachine, oxcarbazepine, phenobarbital, phenytoin
- các thuốc khảng mycobactcria rifampicin, rifapentine
- các chất ức chế bom proton, chẳng hạn như omeprazole, esomeprazole, lansoprazole,
pantoprazole, rabcprazole
— glucocorticoid dexamethasone dùng đuờng toản thân, trừ khi điều trị một liều duy nhất
— chế phẩm từ cây ban di thực ( St J ohn’s wort -Hyperícum perforatum).
CÁNH BÁO VÀ THẬN TRỌNG
Mặc dù việc ức chế virus hiệu quả bằng liệu phảp kháng retrovirus đã được chứng minh là
lảm giảm đảng kể nguy cơ lây truyền qua đường tình dục, nhưng không thế loại trừ hoân
toản được nguy cơ. Các biện pháp phòng ngùa lây truyền nên được thực hiện theo các
hướng dẫn quốc gia.
Thẩt bại về vỉrus học và sự phảt triển để khảng thuốc
EDURANT chưa được đảnh giá ở những bệnh nhân đã có thất bại về virus học với bẩt kỳ
liệu phảp khảng retrovirus nảo khảc. Danh sảch các đột biến liên quan đến khảng
rỉlpìvỉrine được trình bảy ở phẩn ĐẶC TÍNH DƯỢC LỰC HỌC chỉ nên dùng để hướng
dẫn sử dụng EDURANT ơ nhũng bệnh nhân chua đuợc đìềư trị trước đó.
Trong một phân tích hỉệu quả tổng hợp tư các thử nghiệm pha 111 ở người 1ớn có thời gian
điều trị đến 96 tuần. bệnh nhân điều trị với rìlpivirinc với tải lượng virus HIV-l RNA trước
điều trị > 100 000 bản sao/ml có nguy cơ thẳt bại vê virus cao hơn (18,2% với rilpivirine
so với 7, 9% vởi efavirenz) so vởi bệnh nhân có tải lượng vỉrus HIV- ] RNA truớc điều trị 5
100.000 bản sao/ml (5,7% với rilpivirine so với 3,6% vởi efavirenz). Nguy cơ thắt bại về
virus học lớn hơn ở các bệnh nhân nhóm rỉìpivỉrine đã được quan sát trong 48 tuần đầu tiên
của nhũng thử nghiệm nảy (xem ĐẶC TÍNH DƯỢC LỰC HỌC). Bệnh nhân có tải
lượng virus HIV-l RNA trước điều trị> 100.000 bản sao/ml bị thất bại về mặt virus học, có
tỷ lệ kháng thuốc do điều trị cao hơn đối với nhóm thuốc ức chế sao chép ngược không có
cẳu trúc nucleoside (NNRTI). Bệnh nhân dùng ri1pivirinc bị thắt bại về virus học, đã phát
Page 3 of 23
P! Edumnt L'K SP1Ĩ 31m1 .“Dlrì DA 1’1-eqwsf 300c1. 2016__311
triển kháng 1iên quan đển lamivudinelemtricitabine nhiều hơn so với những bệnh nhân
dùng efavirenz bị thẳt bại về virus học (xem ĐẶC TỈNH DƯỢC LỰC HỌC)
Các phảt hiện ở thanh thỉếu niên (tù 12 đến dưới 18 tuồi) trong thử nghiệm C213, nhin
chung, phù hợp với những dữ liệu nảy (xem chi tiết ở phẩn ĐẶC TÍNH DƯỢC LỰC
HỌC).
Chỉ nến điều trị rilpivirine cho nhũng thanh thiểu niên đuợc cho là có khả năng tuân thủ
điều trị thuốc kháng retrovirus tốt, vì sự tuân thủ không tốt có thể dẫn đến phát triển đề
kháng và lảm mất cảc 1ựa chọn điểu trị trong tướng lai
Giống như cảc thuốc khảng retrovirus khác, xét nghiệm kháng thuốc nên định hướng sử
đụng rilpivirine (xem ĐẶC TÍNH DUỢC LỤC HỌC).
Tim mạch
Ở liều cao hơn so với liều điều trị (75 và 300 mg một lần mỗi ngảy), rilpivirine có liên
quan đến việc kéo dải khoảng QTc trên điện tâm đồ (ECG) (xem TƯO'NG TÁC VỚI
CÁC THUỐC KHÁC VÀ CÁC LOAI TƯỚNG TÁC KHÁC, TÁC DỤNG KHÔNG
MONG MUỐN, vả ĐẶC TÍNH DƯỢC ĐỘNG HỌC). EDURANT với liều khuyến cảo
25 mg một lần mỗi ngầy không gây ra những ảnh hưởng có ý nghĩa lâm sảng trên QTc.
Cần sử dụng EDURANT thận trọng khi dùng đỗng thời với cảc thuốc có nguy cơ gây ra
xoắn đính
Hội chứng phục hồi miễn dịch
Ở bệnh nhân nhiễm HTV bị suy giảm miễn dịch nặng ở thời điếm bắt đầu điếu trị CART,
phản ứng viêm đối với cảc tảc nhân gây bệnh cơ hội không có triệu chứng hoặc tồn dư, có
thế xuât hiện vả gây ra cảc tình trạng lâm sảng nghiêm trọng hoặc lảm trầm trọng thêm cảc
triệu chứng Thông thường, các phản ủng như vậy đã được quan sát thẩy trong nhũng tuần
hoặc nhũng tháng đầu tiên bắt đầu CART Cảc ví dụ liên quan lả viêm võng mạc do
cytomegalovirus, nhiễm trùng do mycobacteria khu trú vảÍhoặc toản thân và viêm phổi do
Pneumocystisjz'roveci. Bất kỳ triệu chứng viêm nảo cũng cần đuợc đảnh gỉá vả điếu trị khi
cân thiết
Các rối loạn tự miễn (như bệnh Basedow — hay bệnh Graves) cũng đã được bảo cảo là xảy
.,ra trongquá trinh phục hồi miễn dịch; tuy nhiên, thời gian khởi phảt được bảocáo lả dao
động hơn và những bìến cố nảy có thể xảy ra nhiều thảng sau khi bắt đầu điều trị (xem
TÁC DỤNG KHÔNG MONG MUÔN).
Thông tỉn quan trong về môt số thânh phần cũa EDURANT
EDURANT có chứa 1actose. Bệnh nhân bị các vắn để di truyền hiếm gặp về không dung
nạpg cralactose, thiếu hụt Lapp lactase hoặc rối loạn kém hấp thu glucose- gaiactose không
nên dùng thuốc nảy.
TƯỢNG TÁC VỚI cÁc THUỐC KHÁC VÀ CÁC LOẠI TƯơNG TÁC KHÁC
Các thuốc ảnh hưởng đểu mức độ tiếp xúc cũa rilpivirine
Rilpivirine được chuyến hóa chủ yểu bởi cytochrome P450 (CYP)3A. Cảc thuốc cảm úng
hoặc ức chế CYP3A có thề lảm ảnh hướng đến thanh thải rilpivirine (xem ĐẶC TỈNH
DƯỢC ĐỘNG HỌC). Sử dụng đồng thời rilpivirine vả cảc thuốc cảm ứng CYP3A đã cho
thấy 1ảm gỉảm nông độ rỉlpivirine trong huyết tương, có thế lảm giảm tảo dụng điếu trị của
rilpivirine
Sử dụng đồng thời rilpivirine và các thuốc ức chế CYP3A đã cho thấy lâm tăng nổng độ
rilpivirine trong huyết tương.
Sử dụng đồng thời rilpivirine với cảc lhuốc- lảm tăng pH dạ dảy có thể dẫn đển giảm nồng
độ rilpivirine trong huyết tương, có thế lảm giảm tảo dụng điếu trị cùa EDURANT.
Cảc thuốc bị ảnh hưởng bỡi việc sử dụng rilpivirine
Page 4 of 23
PJ Eđurcmt UK SPC 32.l1112016_ DJ! 1’ rưquexl 20061,20i ó_vl
Rilpivirine ở liều 25 mg một lần mỗi ngảy dường như không ảnh hưởng có ý nghĩa lâm
sảng đến nồng độ cứa các thuốc bị chuyển hóa bới các enzym CYP
Rilpivirine ức chế P-glycoprotein ín vỉtro (ICSU 1ả 9, 2 ụM). Trong một nghiên củu lâm
sảng, rilpivirine không ảnh hưởng đảng kế đến dược động học của digoxin Tuy nhiên,
không thế loại trừ hoản toản việc rilpivirine có thể lảm tãng múc độ tiếp xúc vởỉ các thuốc
khảo được vận chuyến bới P- g-lycoprotein mà những chất nảy nhạy cảm hơn Với sự ủc chế
P—gp trong ruột, ví dụ: dabỉgatran etexilate.
Rilpivirine là chất ức chế in vừro cùa chất vận chuyến MATE-ZK với ICso <2,7 nM. Hiện
vân chưa biết ý nghĩa lâm sảng
của phát hiện nảy
Các tương tảc vê lý thuyết vả cảc tương tảc đã biết rõ với một số thuốc khảng retrovirus vả
cảc thuốc không khảng retrovirus được lỉệt kê trong bảng 1
Bảng tương tảc
Cảo nghiên cứu về tương tác thuốc chỉ được thựchiện ở người lớn.
Tương tác giữa rilpivirine vả các thuôo dùng đông thời được liệt kê trong bảng 1 (tãng
được ký hiệu là "T", giảm lả "1", không thay đôi là "H". không áp dụng lá "NA". khoảng
tin cậy lả "CI") .
Bâng 1: CÁC TƯỚNG TẢC VÀ KHUYẾN CÁO LIÊU DÙNG VỚI CÁC THUỐC
KHAC
Các thuốc xếp theo nhóm
điều trị
Tương tảc
Thay đỗi trung bình (%)
Cảc khuyến cản liên quan
đểu việc sư dụng đồng thời
CÁC THUỐC CHỐNG NHIỄM TRÙNG
Cảc thuốc khảng retrovirus
Các thuốc điếu trị HJ V nhóm ức chế enzyme sao chép ngược NRTiĨ-W[IJRTI
ỉ903338133931ầ9 mễíngèy
DiđanosineM
dìdanosine AUC T 12%
_ _ didanosine Cmin NA
didanosihe Cma,ft—è
ri1pivirine AUC <—›
rilpivirine Cmm <—›
rilpivirine Cmax ,..,
Không cần điều chinh liều.
Didanosinc nên được dùng it
nhẫt hai giờ trưởc hỗẳễ i'Ỉ nhẫt
bốn giờ sau khi dùng
ri 1pivỉrine.
Tenofovir
fumarate*fi
300 mg một lản môi ngảy
disoproxil
tenofovir AUC T 23%
tenofovir Cmin) 24%
tcnofovir Cm,T 19%
rilpivirine AUC <—›
rilpivirine Cmin <—›-
rilpivirine Cmax <—+
Không cân điêu chinh liêu.
Các NRT1 khảo
(abacavir, emtricitabine,
lamivudine, stavudine vả
zidovudỉnc)
Chưa được nghỉến cúu. Dự
kiên không có tương tảc thuôo
- thuôo có ý nghĩa lâm sảng.
Không cân điêu chinh liêu.
Các thuốc điều lrị H] V NNRTJS
NNRTI
(delavirdỉne, efavirenz,
etravirỉne, ncvirapỉne)
Chưa nghiên cửu.
Không khuyến cảo phối hợp
rilpivirine với cảc NNRTI
khác.
Các lhuốc ức chếprotease HJ V (P!) — khi dùng cùng liều ĩhấp ritonavir
. , . );
Darunavưlntonavư* l
darunavir AUC <—›
Việc sử dụng đồng thời
P] Edumnt L-'KSPC ỈĨJuI.ỈỦỈỐ DA l’reque
s! I'OOCI.2ÚIÓ vi'
Page 5 of23
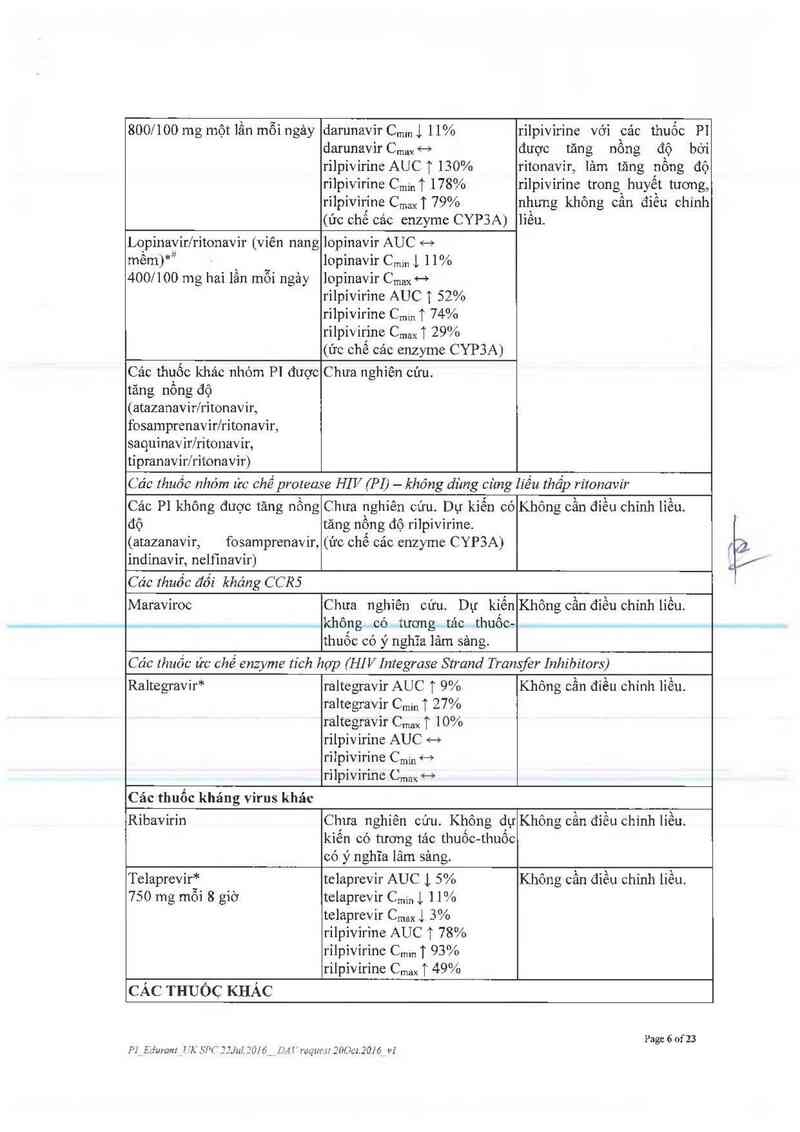
800/100 mg một lằn mỗi ngảy
darunavir Cmm J 11%
darunavir Cmax <—›
rilpivirine AUC T 130%
rilpivirine Cmin T 178%
rilpivirine CmaxT 79%
(ức chế cảc enzyme CYP3A)
rilpivirine với các thuốc PI
được tăng nồng độ bới
rỉtonavir, lảm tăng nồng độ
rilpivirine trong huyết tuơng,
nhung không cẩn điều chinh
liêu.
Lopỉnavirlritonavỉr (viên nang
mêm)*p
400/100 mg hai lân môi ngảy
lopỉnạvir AUC <—›
lopinavir Cmm 1 l 1%
lopinavir Cmax <—›
rỉlpivirine AUC T 52%
rilpivirine CmmT 74%
rilpivirine Cma,T 29%
(_ức chế cảc enzyme CYP3A)
Cảo thuốc khác nhóm Pi được
tăng nồng độ
(atazanavir/ritonavir,
fosamprenavir/ritonavir,
saquinavir/ritonavir,
tipranavirfritonavir)
Chưa nghiên cửu.
Cảc thuốc nhóm ức chế protease HI V (PI) — khóng dùng cùng lỉểu thấp ritonavir
Cảo P] không được tăng nồng
độ
(atazanavir, fosamprenavir,
indinavir, nelfinavir)
Chưa nghiên cứu. Dự kiến có
tăng nông độ rilpivirine.
(ức chẽ các cnzyme CYP3A)
Không cần điều chỉnh lỉều.
Các thuốc đối khảng CCR5
Maraviroc
Chưa nghiên cửu. Dự kiến
không có tướng-tác thuôo-
thuôc có ý nghĩa lâm sảng.
Không cần đìều chỉnh liếu.
Các thuốc ức chế enzyme tỉch họp (HI V [ntegrase Strand Transfer Inhibz'tors)
Raltegravir*
raltegravìr AUC T 9%
raltegravir CminT 27%
raltegravir C,… T 10%
rilpivirine AUC H
riipivirine Cmin 4—›
rilpivirine Cma, <—›
Không cân điếu chinh liếu.
Các thuốc kháng virus khác
Rỉbavirin Chưa nghiên cứu. Không dụ Khôngcẳn điếu chinh liếu.
kiên có tương tảo thuôc-thuôc
có ý nghĩa lâm sảng.
Telaprevir* telaprevir AUC ) 5% Không cần điều chinh liều.
750 mg mỗi 8 giờ
telaprcvir Cmm 1 1 1%
telaprevir Cmaxl 3%
rilpivirine AUC T 78%
rilpivirine C,… T 93%
rilpivirine Cmax T 49%
cÁc THUỐC KHÁC
P) Eđuram 1’Ă'Sỉ’i' JJJtiI.ÊỦJỔ_ DAt“rcqmuitJũOcl.20/ó W'
Page 6 of 23
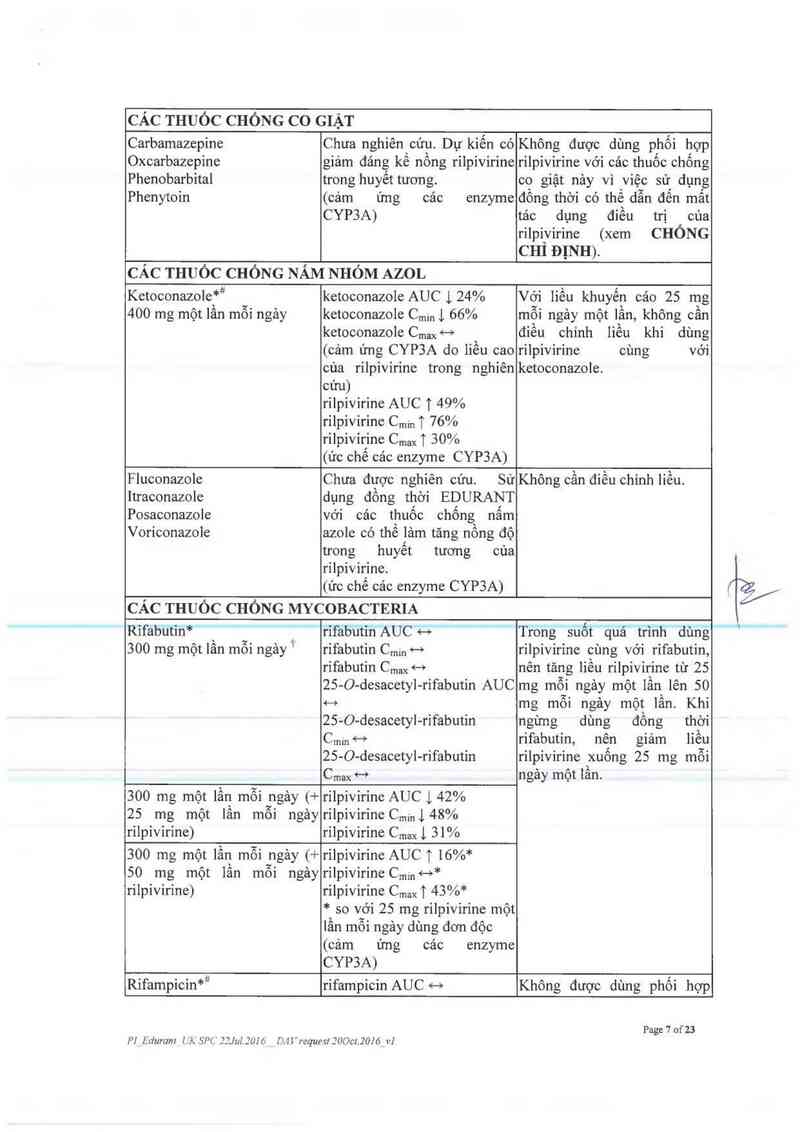
CÁC THUỐC CHỐNG co GIẬT
Carbamazepine
Oxcarbazepine
Phenobarbital
Phenytoin
Chưa nghiêncứu. Dự kiến có
giảm đáng kê nồng rỉlpỉvirine
trong huyêt tương.
(cảm ứng các enzyme
CYP3A)
Không được dùng phối hợp
rilpivirine với các thuốc chống
co giật nảy vì việc sử dụng
đồng thời có thể dẫn đến mất
tác dụng điếu trị của
rilpivirine (xem CHỐNG
CHỈ ĐỊNH).
CÁC THUỐC CHỐNG NĂM NHÓM AZOL
Kctoconazole’ỨJi
400 mg một lần môi ngảy
ketoconazole AUC 1 24%
ketoconazole Cmml 66%
ketoconazole Cmax .….
(cảm ứng CYP3A do liếu cao
của rilpivirine trong nghiên
cứu)
rilpivirine AUC T 49%
rilpivirine Cmin T 76%
rilpivirine Cmax T 30%
(ức chế cảc enzyme CYP3A)
Vởi liều khuyến cảo 25 mg
mỗi ngảy một lân, không cân
điêu chinh liều khi dùng
rilpivirine cùng với
ketoconazole.
Fluconazole
Itraconazole
Posaconazole
Voriconazole
Chưa được nghiên cứu. Sử
dụng đổng thời EDURANT
với các thuốc chống nấm
azole có thế 1ảm tăng nồng độ
trong huyết tương cứa
rilpivirine.
(ức chế cảc enzyme CYP3A)
Không cẩn đỉều chinh liều.
CÁC THUỐC CHỐNG MYCOBACTERIA
Rifabũti'ri* , _ ,
300 mg một lân môi ngảy 1
rifabứtĩii AUC +-›
rifabutin Cmin ~—›
rifabutin Cmax +->
25-0-desacetyl—rifabutin AUC
í—ở
25-0-desacetyl-rifabutin
Cmm ""
25-0-desacetyl-rifabutin
Cmax <—›
Trong suốt quá trinh dùng
rilpivirine cùng với rifabutin,
nên tãng liều rilpivirine từ 25
mg môi ngảy một lần lên 50
mg mỗi ngảy một lần. Khi
ngừng dùng đồng thời
rifabutin, nên giảm liều
rilpivirine xuống 25 mg mỗi
ngảy một 1ần.
300 mg một lần mỗi ngảy (+
25 mg một lần môi ngảy
rilpivirine)
rilpivirine AUC 1 42%
rilpivirine Cmínl 48%
rilpivirine Cmaxị 31%
300 mg một lần mỗi ngảy (+
50 mg một lần môi ngảy
rilpivirine)
rilpivirine AUC T 16%*
rilpivirine Cmm <—›*
rilpivirine CmaxT 43%*
* so với 25 mg rilpivirine một
lần mỗi ngảy dùng đơn độc
(cảm ứng các enzyme
CYP3A)
Rifampicìn**
rifampicin AUC «—›
Không được dùng phối hợp
P] Iídumm 1.'À SI’L 22J111.2016
DA !' request J(ìOcl.20]ó v]
Page 7 of 23
600 mg một lần mỗi ngảy
rifampicin Cmm NA
rifampicin Cmax <—-›
25-desacetyl-rifampicin AUC
,L 9%
25—desacetyl-rifampicỉn
Cmin NA
25-desacetyl-rifampicỉn
Cmax H
rilpivirine AUC l 80%
rilpivirine Cmin 1 89%
rỉlpivirỉne C,…) 69%
rilpivirine với rifampicin vì
việc sử dụng đồng thời có thể
dẫn đến mất tảo dụng điều trị
cúa rilpivirine (xem CHỐNG
CHỈ ĐỊNH).
(cảm ứng cảc enzyme
CYP3A)
Rỉfapentine Chưa được nghiến qcúzu. DựKhông được dùng phối hợp
kiên sẽ giảm đáng kê_nông độ rilpivirine với rifapentinc vi
rỉlpivirỉne trong huyêt tương. việc sử dụng dông thời cớ thê
(cảm ứng cảc enzyme dẫn đên mât tác dụng điếu trị
CYP3A) củaqrilpivirine (xem CHONG
CHI ĐỊNH).
CÁC KHÁNG SINH NHÓM MACROLID
Clarithromycin Chưa được nghiên cứu. Dự Khi có thế, cần xem )f(ét cảc
Erythromycin kỉên tăng phơi nhiêm lựa chọn thay thế như
rỉ1pivirinc. azithromycin.
(Ưc chê cnzyme CYP3A)
CÁC GLUCOCORTICOID
Dexamethasonc (dùng đường
toản thân, ngoại trừ sử dụng
đơn liếu)
Chưa được nghiên cứu. Dự
kìên có giảm nộng độ
rilpivirine trong huyêt tương
phụ thuộc vảo liêu dùng.
(cảm ứng cảc enzyme
CYP3A)
Không nên dùng phối hợp
rilpivirine với dexamethasonc
toản thân (ngoại trừ một liếu
duy nhất) vì việc sử dụng
đồng thời có thề lảm mắt tác
dụng điếu trị của rilpivirine
(xem CHỐNG CHỈ ĐỊNH).
Cần xem xẻt cảc biện phảp
thay thế, đặc biệt là khi sử
dụng lâu dải.
cAc THUỐC ỨC CHẾ Bơm PROTON
Omcprazole*ấ
20 mg một lân môt ngảy
omeprazolc AUC 1 14%
omeprazoie Cmin NA
omeprazole Cma,ị 14%
rilpivirine AUC 1 40%
rilpivirine Cmin], 33%
rìlpivirine Cmaxị 40%
(giảm hấp thu do tảng pH dạ
dảy)
Lansoprazole
Rabeprazole
Pantoprazole
Esomeprazole
Chưa được nghiên cún. Dự
kiên có gíảm đảng kế nông độ
rilpivirine trong huyêt tương.
(giảm hấp thu do tăng pH dạ
Không được dùng phối họp
rilpivirine với cảc thuốc ức
chế bơm proton vì việc sử
dụng đồng thời có thể lảm mẩt
tảc dụng điều trị của
rilpivirine (xem CHỐNG
CHi ĐỊNH)
ì’l Ỉ'Ĩd'LJP'G’HI i.:"À' SPC' 22Jtt1.2016_ DA 1 'request ."0ch.201 6 VI
Page 8 of 23
,\,)
dảy)
CÁC THUỐC KHÁNG THỤ THỂ H,
Famotidine*g
40 mg một liêu duy nhât, uông
rilpivirine AUC 1 9%
rilpivirine Cmin NA
Phối hợp giữa rilpivirine và
các thuôc đôi kháng thụ thế Họ
cân sủ“ dụng đặc bíệt thận
12 giờ trước khi uống rilpivirine Cmax 4—›
rilpivirine
F'amotidỉnớ"gi rilpivirine AUC 1 76%
40 mg một 1iều duy nhất, uộng
rilpivirine Cmm NA
trọng. Chỉ nên sử dụng cảc
thuốc đối kháng thụ thể H; có
thể dùng chế độ lỉếu 1 1%…
ngảy.
Chỉ nên sử dụng một chế độ
2 giờ trước khi uông rilpivirine Cmaxl 85%
rilpivirine (giảm hâp thu do tăng pH dạ
dảy)
Famotidine*a rilpivirine AUC T 13%
40 mg một liếư duy nhất uống
4 giờ sau khi uông rilpivirine
rilpivirine Cmin NA
rilpivirine CmaxT 21%
liều nghiêm ngặt, dùng thuốc
đối khảng thụ thể H2 ít nhẳt 12
giờ trước hoặc ít nhất 4 giờ
sau khi dùng rilpivirine.
Cỉmctidine Chưa được nghiên cứu.
Nizatidỉne (gỉảm hâp thu do tăng pH dạ
Ranitidine dảy)
CÁC ANTACID
Cảo antacid (ví dụ, aluminium
hoặc magnesium hydroxidc,
calcium carbonatc)
Chưa được nghiên cứu.
Dự kiến có giảm đáng kể nồng
dộ rilpivirine trong huyết
tương.
(gỉảm hấp thu do Lăng pH dạ
dảy)
Cần thận trọng đặc biệt khi sử
dụng phối hợp rilpivirine và
thuốc antacid. Thuốc antacid
chỉ nên được dùng it nhất 2
giờ trước hoặc ít nhắt 4 giờ
sau khi dùng rilpivirine.
CÁC THUỐC GIẢM ĐAU GÂY NGHIỆN
Methadone*
60-100 mg một lân mỗi ngảy,
1iêu cả thế hóa
R(-) methadone AUC 1 16%
R(-) methadonc Cmin 1 22%
R(-) methadone Cma,ị 14%
rilpivirine AUC <—›*
rilpivirine Cmin 4——›"'
rí1pivirỉne Cmax 4—› *
* dựa trên nhóm chúng lịch sử
Không cần điếu chỉnh liếu khi
bắt đầu sử dụng đồng thời
methadone với riipivirine. Tuy
nhiên, khuyến cáo theo dõi
lâm sảng vi có thế cần điếu
chỉnh điều trị duy trì bằng
mcthadonc ở một số bệnh
nhân.
CẢC THUỐC CHỐNG LOẠN NHỊP
Digoxin*
digoxin AUC <—›
digoxin Cmin NA
dígoxin Cma, <—›
Không cần điếu chinh liều.
CÁC THUỐC CHỐNG ĐÔNG
Dabigatran etexilate
Chưa được nghiên cứu. Không
thể loại trừ nguy cơ tăng nồng
độ dabigatran trong huyết
tương.
(ức chế P-gp đường ruột)
Nên thận trọng khi phối họp
thuôo rilpivirine vả dabigatran
etexiiate.
CÁC THUỐC ĐIỂU TRỊ ĐẢI THẢO ĐƯỜNG
Metformin*
lmctformin AUC <—›
iKhông cần điếu chinh liều.
P] En’ummj .v`C .S'18'11" ÊẺJnI. 31116
D11 ì’1-equesl JUOcJ.ZOIỐ v]
Page 9 01'23
Ỹ.
850 mg một liếu duy nhất
metformin Cmin NA
mctformin Cmax <—4
CÁC SẢN PHẢM TỪ DƯỢC LIỆU
Chế phẩm từ cây ban di thực
(St John's wort- Hypericum
peijòrtltum)
Chưa được nghỉên cứu. Dự
kỉến có giảm đáng kể nồng độ
rilpivirine trong huyết tương.
(cảm ứng các enzyme
CYP3A)
Không được sử dụng
rỉ1pivìrine kêt hợp với cảc sản
phâm có chứa dược liệu ban di
thực (St John's wort) do sử
dụng đồng thời có thế 1ảm mất
tảc dụng điếu trị _cùa
rilpivirine (xem CHỐNG
CHỈ ĐỊNH)
cÁc THUỐC GIÀM ĐAU
Paracetamol*g
500 mg một liêu duy nhât
paracctamol AUC <—›
paracetarnol Cmin NA
paracetamol Cmax 4—›
rilpivirine AUC <—+
rilpivirine Cmin T 26%
rỉlpivirine Cma, <—>-
Không cằn điếu chinh iiều.
CÁC THUỐC TRÁNH THAI ĐƯỜNG UỐNG
Ethinylestradiol*
0,035 mg một lằn mỗi ngảy
Norethỉndrone*
] mg một lần mỗi ngảy
ethinylestradioi AUC <—+
cthinylcstradioi Cmm <—›
cthinylcstradiol CmaxT 17%
norethindrone AUC <—›
norethindrone Cmm «—›
norethindrone Cmax H
rilpivirine AUC 4—›*
rilpivirine Cmin 4-›*
rilpivirine C,… +—›*
*dựa trên nhóm chúng lịch sư.
Không cần điều chinh liều.
CÁC THUỐC Ức CHẾ HMG CO-A REDUCTASE
Atorvastatin*“
40 mg một lân môi ngảy
atorvastatin AUC 4—›
atorvastatin Cmmị 15%
atorvastatin C.… T 35%
rilpivirine AUC <—›
rilpivirine Cmin <-*
rilpivirine C,…ị 9%
Không cãn điêu chinh 1iêu.
CÁC THUỐC Ức CHẾ PHOSPHODIESTERASE TYP 5
[PDE-S)
Sildenafil*“ ` ,
50 mg một liếu duy nhât
sildenatìl AUC H
sildenafil Cmm NA
sildenafil Cmax 4—›
rilpivirine AUC <—›
rilpivirine Cmin <—›
rilpivirine Cmax <—›
Không cân điêu chinh liêu.
Vardenafil
Tadalafil
Chưa được nghiên cứu.
Không cằn điều chinh liếu.
* Tương tác giữa rilpivirine vả cảc thuốc đã được đảnh giá trong một nghiên cứu lâm sảng,
Tât cả các tương tác thuôo - thuôo khảo được trinh bảy ìả được dự đoản.
P! Eđurum UK SPC` J.?Jitl 3016_ DẢ [’ request 200c1.20/6_ v]
Page 11] ot'23
ẩNghiên cứu tương tảc nảy đã được thực hiện với 1iều cao hơn liều khuyến cáo của
rỉipivirine đế đảnh giá tác dụng tối đa trên thuốc dùng đồng thời. Khuyến nghị về chế độ ]ỉếu
được áp dụng cho liếu được khuyến cáo lả rilpivirine 25 mg một lần mỗi ngảy.
'1' Nghiên cúu tương tảo nảy đã được thực hiện với một liều cao hơn liều khuyến cảo của
ri1pivirine.
Cảc thuốc kéo dải khoảng QT.
Có rất it thông tin về khả năng tuơng tác dược lục học giữa rilpivirine vả cảc thuốc lảrn
kéo dải khoảng QTc trên ECG. Trong một nghỉên cứu trên các đối tượng khỏe mạnh cảc
mức liều cao hơn liếu đỉếu trị cùa rilpivirine (75 mg một lần mỗi ngảy và 300 mg một lần
mỗi ngảy) cho thẩy có kéo dải khoảng QTc trên ECG (xem ĐẶC TỈNH DUỢC LỤC
HỌC). Cần sử dụng EDURANT thận trọng khi phối hợp với một thuốc đã biết là có nguy
cơ gây xoắn đỉnh.
PHỤ NỮ CÓ THAI, cnc con BÚ VÀ KHẢ NĂNG SINH SẨN
Phụ nữ có thai
Không có hoặc có it dữ liệu (ít hơn 300 kết cuộc thai kỳ) từ việc sử dụng rilpivirine ở phụ
nữ có thai.
Cảo nghiên cứu trên động vật không chỉ ra cảc tác dụng có hại trực tiếp hoặc giám tiếp về
độc tính sinh sản (xem THÔNG TIN TIỀN LÂM SÀNG).
Như một biện pháp phòng ngùa, nên tránh sử dụng thuốc EDURANT trong thai kỳ.
Cho con bú
Không rõ liệu rilpivirine có bải tiết vảo sữa mẹ hay không. Rilpivirine được bải tiểt vảo
sữa chuột cống. Do cả khả nãng lây truyền HIV và khả năng xáy ra phản ứng có hại ở trẻ
bú sữa, người mẹ nên được hướng dẫn không cho con bú nếu đang dùng rilpivirine.
Khả năng sinh sản
Không có dữ liệu trên người về tảc dụng cúa rilpivirine trên khả năng sinh sản. Không
quan sảt thấy tảo dụng có ý nghĩa lâm sảng liệu quan đến khả năng sinh sân trong các
nghiên cứu trên động vật (xem THÔNG TIN TIÊN LÂM SÀNG).
ẢNH HƯỞNG ĐỀN KHẢ NĂNG LÁI XE VÀ VẶN HÀNH MÁY MÓC
EDURANT không ảnh hưởng hơặc ảnh hưởng không đáng kể đến khả năng lái xe và vận
hảnh mảy móc. Tuy nhiên, một số bệnh nhân dùng EDURANT đã được bảo cáo về tinh
trạng mệt mỏi, chóng mặt vả buồn ngủ vả cần được xem xét khi đánh giá khả năng lải xe
hoặc vận hảnh máy móc của bệnh nhân.
TÁC DỤNG KHÔNG MONG MUỐN
Tóm tắt thông tin an toẳm
Trong chương trình phảt triến lâm sâng (1.368 bệnh nhân trong các thứ nghỉệm lâm sảng
phase 111 có đối chứng TMC27S- C209 (ECHO) vả TMC278- C215 (THRlVE)J, 55,7%
bệnh nhân có ít nhẩt một phản ứng có hại (xem ĐẶC TÍNH DƯỢC LỰC HỌC). Các
phản ung có hại đuợc bảo cảo nhiếu nhất (ADR) (> 2%) mã có cường độ ít nhất từ mức
trung bình trở lên là trầm cảm (4,1%), nhức đầu (3, 5%), mất ngủ (3, 5%), phảt ban (2,3%)
và đau bụng (2, 0%) Các ADR nghíêm trọng liên quan đển điếu trị thường gặp nhất được
bảo cáo ở 7 ( 1 0%) bệnh nhân dùng rilpivirine. Trung vị thời gian tiếp xức của bệnh nhân ở
Page 11 MB
P] Eư'umnl UK SPF 22.1'u1.201 6 j`1.~1VJ'equmtJỦÚCF.2ÚJ 0 ví
nhóm dùng rilpivirine và nhóm dùng efavirenz lần lượt là 104,3 vả 104,1 tuần. Hầu hết cảc
ADR xuất hiện trong 48 tuần điều trị đầu tiên.
Một số bất thường về xét nghiệm có liên quan đến điều trị được lựa chọn (độ 3 hoặc độ 4),
được coi là ADR, được bảo cảo ở các bệnh nhân được điều ni bằng EDURANT là tăng
amylase tụy (3,8%), tăng AST (2,3%), tăng ALT (1,6%), tăng LDL cholesterol (lúc đói,
1 ,,5%) giảm bạch cầu (1 ,2,%) tăng lipase (0, 9%), tăng bilirubin (0, 7%), tăng triglyceride
(lúc đói, 0 ,6%), giảm hemoglobin (0,1%), giảm tiếu câu (0,1%) vả tăng cholesterol toản
phần (lủc đói, 0,1%).
Bảng tóm tắt cảc phản ứng có hại
Các ADR được báo cảo ở các bệnh nhân người 1ớn điều trị bằng rilpivirine được tỏm tắt
trong Bảng 2. Cảc ADR được liệt kê theo phân loại hệ cơ quan (system organ class- SOC)
và tần suất. Cảc tần suất được định nghĩa là rất thường gặp (> 1/ 10) thường gặp (> 1/100
đến <1/10) và ít gặp (> 1/1. 000 đến <1/100). Trong môi nhóm tần suất, cảc ADR được
trình bảy theo thứ tự giảm dần về tần suất
Bảng 2: Cảc ADR được báo cáo ở những bệnh nhân ngưòi 1t'm nhiễm HIV—l chưa từng
điều trị kháng retrovirus trước đỏ, được điểu trị bằng Rilpivirine
(Dữ liệu tông hợp từ phân tích tuần 96 của các thử nghỉệm pha III ECHO vả THRIVE)
N= 686
Phân loại hệ cơ quan (SOC) Phân nhóm tần suất ADR
(Rilpivirine + BR)
Cảo rối loạn hệ mảu vả bạch huyết thường gặp giảm bạch cầu
giảm hemoglobin
giảm số lượng tìếu
câu
Cảo rối loạn hệ miễn dịch ít gặp hội chứng phục hồi
miễn dịch
Cảc rối loạn chuyền hóa và dinh rấtthường gặp tăng cholesterol toản
dưỡng phân (lúc đói)
(1úc đói)
tăng LDL cholesterol
thường gặp giảm thèm ăn
đói)
tãng triglyceride (lủc
Các rối loạn tâm thần rất thường gặp mắt ngủ
thường gặp giấc mơ bất thường
trầm cảm
rối loạn giấc ngủ
khí sẳc trầm
Các rối loạn hệ thần kinh trung ương rất thường gặp đau đằu
chóng mặt
thường gặp buồn ngủ
Cảc rối 1oạn hệ tiêu hóa rất thường gặp buồn nôn
tăng amylase tụy
thường gặp đau bụng
nôn
Page 12 of 23
P] bduram_ lfA 51²( ` JJJuI.JOIÓ DA1'reqưcslfflWc/JOIÓ vl
tăng lípase
khó chịu ở bụng
khô miệng
Cảo rối loạn hệ gan mật rất thường gặp tăng cảc transaminase
thường gặp tãng bilirubỉn
Các rối loạn da và mô dưới da thường gặp ban đỏ
Cảo rối loạn toản thân và cảc tinh thường gặp mệt mới
trạng tại vị trí đưa thuôo
BR=background regỉmen = Chế độ điều trị nền
N=sô lượng bệnh nhân
Các bắt thường về xét nghiệm
Trong nhóm dùng rilpivirine trong phận tich ớ tuần 96, các thủ nghiệm pha 111 ECHO vả
THRIVE, giá trị trung bình cùa thay đối so với trước điều trị của choiesterol toản phần (đo
lúc đói) lả 5 mg/d1, HDL cholesterol (lúc đói) là 4 mg/dl, LDL cholesterol lả ] mg/dl, vả
triglyceridcs (lủc đói) -7 mg/dl.
Mô tả một số phãn ứng có hại được lựa chọn
Hội chửng phục hồi míên dịch
Ở nhũng bệnh nhân nhiễm HIV bị suy giảm miễn dịch nặng ở thời điểm bắt đằu điếu trị
phối hợp kháng retrovirus (combination antiretroviral therapy- CART), có thể xảy ra phản
úng viêm đối với nhun g trường hợp nhiễm trùng cơ hội không có triệu chứng hoặc tồn dư
Các rối loạn tự miễn (như bệnh Basedow— bệnh Graves') cũng đã được báo Cảo; tuy nhỉên,
thời gian đến lúc khới phảt được báo cáo là dao động hơn và những biến cố nảy có thể xảy
ra nhiếu thảng sau khi bắt đẳu điếu trị (xem CẢNH BÁO VÀ THẶN TRỌNG)
Quần thể trẻ em (từ 12 đến dưới 18 tuổi)
Đảnh giá an toản dựa trên phân tích tuần thứ 48 cúa thử nghiệm pha 11, đơn nhóm, nhãn
mở TMC278- C213, trong đó 36 bệnh nhân thanh thiếu niên nhiễm HIV- ] chưa từng điều
trị thuốc khảng retrovirus có trọng luợng ít nhắt 32 kg đã được dùng rilpivirine (25 mg một
lần mỗi ngảy) kết hợp với cảc thuốc kháng retrovirus khác (xem ĐẶC TÍNH DƯ ỢC
LỰC HỌC). Trung vị thời gian đùng thuốc đối với bệnh nhân 1ả 63,5 tuần Không có bệnh
nhân ngùng điếu trị do ADR. Không có ADR mới được xảo định so với những ADR đã
quan sát thẩy ở người lớn
Hầu hết các ADR đều ở độ 1 hoặc 2. Cảc ADR thường gặp nhất (tất cả cảc độ, lớn hơn
hoặc bằng 10%) là đau đẩu (19, 4%), trầm cảm (19 4%), buồn ngủ (13,9%) và buổn nôn
(1 1,1%). Không có bẩt thường về xét nghìệm ở độ 3-4 đối với AST/ALT hoặc ADR độ 3- 4
của tăng transaminase được báo cảo.
Tinh an toản vả hiệu quả của rilpivirine ờ trẻ <12 tuổi chưa đuợc xảc lập. Hiện chưa có đủ
liếu.
Các quần thể bệnh nhân đặc hỉệt khác
Bệnh nhân đồng nhiễm vỉrus vỉêm gan B vả/hoặc virus viêm gan C
Ớo nhũng bệnh nhân đồng nhiễm virus vỉêm gan B hoặc C khi dùng rilpivirine, tầ suất
tăng cảc enzym gan gia tăng hon ơ nhũng bệnh nhân dùng rỉ1pivirine nhưng không @ ổng
nhiễm Hiện tượng nảy cũng giống nhóm dùng efavirenz. Phơi nhiễm dược động c của
I`llpl\ mm ở những bệnh nhân đồng nhiễm cũng tương đương với ở bệnh nhân k ng có
đồng nhiễm.
Page 13 of 23
Pẵ Ìídưrtml l-'KSPC JJJuI J()ló DÁi’rcợucsi JOOcLJÚIỔ _vl
T hông báo cho bác sĩ những tác dụng không mong muốn gặp phải khi dùng thuốc.
QUÁ LIÊU
Không có thuốc giải độc đặc hiệu để điều trị quá liếu với EDURANT. Kinh nghiệm quả
liếu với rilpivirine ở người còn hạn chế. Các triệu chứng quá liều có thế bao gồm nhức đầu,
buồn nôn, chóng mặt vả/hoặc có những giấc mơ bất thường. Điều trị quá liếu với
rilpivirine bao gôm các biện pháp hỗ trợ chung như giám sảt các dấu hỉệu sinh tồn và ECG
(khoảng QT) cũng như quan sảt tinh trạng lâm sảng của bệnh nhân. Than hoạt tính có thế
được sử dụng để giúp loại bỏ phần hoạt chất không bị hấp thu. Do rilpivirine liên kết nhiều
với protein huyết tương nên vỉệc thẩm phân có thể sẽ không loại bỏ hoạt chất đảng kề.
ĐẶC TÍNH DƯỢC LỰC HỌC
Nhóm dược trị liệu: Thuốc khảng virus để sử dụng toản thân, cảc chất ức chế phiên mã
ngược không có cấu trúc nucleoside, mã ATC: JOSAGOS.
Cơ chế tảc đụng
Rilpivirine là một NNRTI của HIV-l có cấu trúc diarylpyrimidine. Hoạt tính của
rilpivirine là qua trung gian ức chế không cạnh tranh enzyme sao chép ngược HIV-l
(reverse transcriptase - RT). Rilpivirine không ức chế DNA polymerasc 11, B và 'y của tế
bảo người.
Hoạt tính kháng virus in vitro
Rilpivirine thế hiện hoạt tính đối vói các dòng HIV— ] hoang dã nuôi cấy phòng thí nghiệm
trong một dòng tế bảo T bị nhiễm cấp tính vởi giá trị trung vị ECso đối với HIV- l/IIIB là
0,73 nM (0,27 ng/ml) Mặc dù rilpivirine có hoạt tính in vỉtro chống lại HIV- 2 với cảc giá
trị ECso dao động từ 2510 đến 10830 nM (920 đến 3970 ng/ml), không khuyến cảo điều trị
nhiễm HIV—2 với rilpivirine do không có dữ liệu lâm sảng.
Rilpivirine củng cho thắy có hoạt tinh khảng virus trên một dải rộng cảc chủng HIV- 1
nhóm M thuẫn (phân nhóm A, B, C, D, F, G, H) được phân lập từ bệnh nhân với cảc giá trị
ECso dao động từ 0, 07 đến 1,01 nM (0, 03 đến 0 ,37 ng/ml) và nhóm 0 chủng thuần được
phân lập từ bệnh nhân với các giá trị ECso dao động từ 2,88 đến 8,45 nM (1,06 đến 3,10
nglml).
Khảng thuốc
T rong nuôi cẩy tế bảo
Cảo chủng đề kháng rilpivirine được chọn lọc trong nuôi cẩy tế bảo bắt nguồn từ HIV- ]
hoang dã có nguồn gôc và phân typ khác nhau cũng như HIV- 1 khảng NNRT1. Cảo đột
biến liên quan đến kháng thuốc phô biến nhất xuât hiện bao gồm LlOOI, K101E, V1081,
E138K, V179F, Y181C, H221Y, F227C vả M2301.
sư kháng thuốc đối với rilpivirine được xảo định là một lần thay đổi giá trị ECso cao hơn
ngưỡng sinh học (biological cut-off -BCO) trong thử nghiệm.
T rên những bệnh nhân người lớn chưa đíều trị
Để phân tích kháng thuốc, sữ dụng một định nghĩa về thất bại virus học rộng hơn trong
phân tich hiệu quả chính. Ở tuần 48, phân tích sự đề khảng từ dữ liệu tổng hợp từ các thứ
nghiệm pha 111,62 (trong tống số 72) bệnh nhân thất bại vê virus học ở nhóm rilpivirine đã
có dữ liệu về mức độ khảng thuốc vảo thời điểm bắt đầu và thời điếm thẫt bại. Trong phân
tích nảy, các đột biến liên quan đến khảng thuốc (resistance— associated mutations -RAMs)
kháng với cảc thuốc NNRT] đã xuất hiện trong ít nhắt 2 trường hợp thất bại về virus học
của rilpivirine lả: V901, K101E, E138K, E138Q, V1791, Y181C, V1891, H221Y, vả
F227C. Trong cảc thử nghiệm, sự có mặt cứa cảc đột biến V901 vả V1891, ở thời diếm ban
đầu, không ảnh hưòng đến đảp ứng. Sự thay thế E138K xuất hiện thường xuyên nhất trong
Page 14 of23
Pl_lzduraní lÃKSPL'JZỈHIJOJÓ £l›11'requeslJ(IOcL2OIỔ vl
quá trình điếu trị bằng rilpivirine, thuờng kết hợp với sự thay thế M1841 Trong phân tích ở
tuần 48,31 trong số 62 trường hợp thẩt bại vê virus học khi dùng ri1pivirine, đă có đồng
thời RAMs khảng lại NNRTI vả NRTI; 17 trong số 31 bệnh nhân có sự kết hợp cùa
El38K vả M1841. Cảo dột biến phổ biến nhất là tuơng tư nhau trong các phân tich ở tuần
48 vả tuần 96
Phân tích kháng thuốc ở tuần 96, thẩy có tỷ lệ thắt bại về vỉrus thấp hơn trong 48 tuần thứ
hai so với trong 48 tuẫn đầu tiên của liệu trình điều trị. Tù tuần 48 đến tuần 96, có thêm 24
(3, 5%) và 14 (2,1%) bệnh nhân thất bại về virus học xảy ra tương ứng ở nhóm rilpivirine
vả efavircnz. Trong số những truờng hợp thất bại về virus học nảy, 9 trong số 24 và 4 trong
số 14 bệnh nhân có tải 1uợng virus truớc điểu trị <100. 000 bản sao/ml, tuong ứng.
Xem xét tẩt cả cảc dữ liệu in vier và in vivo đã có ở nhũng đối tuợng chưa đu ợc điều trị,
cảc đột biến liên quan đến kháng thuốc sau đây, nếu có mặt lủc bắt đầu điều trị, có thể ảnh
hướng đến hoạt tinh cùa rilpivirine: KlOlE, KlUlP, E138A, E1386, E138K, 13138R,
El38Q, V179L, Y181C, Y1811, Y181V, Y188L, H221Y, F227C, M2301 vả M23OL.
Những đột biến liên quan đến khảng riipivirine nảy chỉ nên hướng dẫn sử dụng thuốc
EDURANT ở nhũng người chưa đuợc điều trị Những đột biến liên quan đến kháng thuốc
nảy được rút ra từ dữ liệu in vivo chỉ 1iên quan đến những bệnh nhân ohưa được điếu trị
truớc đó vả do đó không thế sử dụng để dự đoán hoạt tính của rilpivirine ở những bệnh
nhân có thẳt bại về virus học với một phảo đồ điều trị kháng retrovirus
Giống như các thuốc khảng retrovirus khác, xét nghiệm kháng thưốc nến hướng dẫn sử
dụng thuốc EDURANT
Khảng chéo
Virus đột bỉến NNRTI tại một số vị trí
Trên một bộ gồm 67 chủng 1-11V- 1 tái tổ hợp trong phòng thí nghiệm những chùng có một
đột biên 1iên quan đến kháng thuốc ở cảc vị trí trên RT, liên quan đến khảng NNRTI bao
gồm cả cảc vị trí phổ bỉến nhẩt K103N vả Y181C, rilpivirine cho thấy hoạt tinh kháng
virus đối với 64 (96%) chứng trong số cảc chủng nảy. Cáo đột biến đơn lẻ liên quan đến
khảng thuốc, mả oó môi liên quan đến sụ mắt nhạy cảm cứa rilpivirine lả: K101P, Yi 811
và Y181V. Việc thay thế K103N không lảm giảm sự nhạy cảm với rilpivirine, nhưng sự
kết hợp của K103N vả 131001 đã lảm gỉảm 7 lẩn độ nhạy cảm với rilpivirine
Các chúng tái tổ hợp trên lâm sảng
Rilpivirine duy trì sự nhạy oảm (F_C < BCO) chống lại 62% trong số 4786 mẫu phân lập
HIV- 1 tải tổ hợp trên lâm sảng đề kháng với efavirenz vảlhoặc nevirapine
Những bệnh nhân người lởn nhỉễm HIV-l chưa được điều trị
Trong phân tích kháng thuốc tại tuần 96 kết hợp dữ liệu oủa cảc thử nghiệm pha III (ECHO
vả '1HRJVE), 42 trong số 86 bệnh nhân có thất bại về vìrus trên nhỏm dùng rílpivirine cho
thấy khả năng đề kháng rilpivirine 1iên quan đến điều trị (phân tích kỉếu gen) Ở những
bệnh nhân nảy, tính khảng chéo kỉếu hình đối với oảc thuốc NNRTI khảo được ghi nhận
như sau: etravirine 32/42, efavircnz 30/42 vả nevirapinc 16142. Ở những bệnh nhân có tải
luợng virus trước điếu trị < 100.000 bản saoÍml, 9 trong số 27 bệnh nhân có thất bại về
virus ở nhóm rìlpivirine cho thắy khả năng đề kháng rilpivirine 1íên quan đến điều trị (phân
tích kiếu gon) với tần suất kháng chéo theo kiểu hình như sau. etravirine 4/9, efavirenz 3(9
vả ncvỉrapino 11.9
Cảo tác dụng trên điện tâm đồ
Tảo dụng của riipivirino với liếu 25mg một lần mỗi ngảy trên khoảng QTcF được đánh giá
trong một nghiên cứu chéo ngâu nhiên, oó đối chưng giả đuợc và thuốc có hoạt tính
(moxỉfioxaoin 400 mg một lần môi ngảy) ở 60 người lớn khỏe mạnh, với 13 1ần đo trong
Page 15 of 23
1"! Iĩduranz_ IJ’K SPC 22Ju1 201] tỉ [J.11' request 3001.12016 v]
24 giờ ở trạng thái ổn định. EDURANT với liếu khuyến cáo 25 mg một lần mỗi ngảy
không gây ra tác dụng có ý nghĩa lâm sảng trên khoảng QTc.
Khỉ rilpivirine được nghiên cứu ở người lớn khỏe mạnh với các liều cao hơn liễu điều trị lả
75 mg một lần mỗi ngảy vả 300 mg một 1ẩn mỗi ngảy, sự khảo biệt trung binh lớn nhất
(giới hạn trên cùa khoảng tin cậy 95%) của khoảng QTcF so vởi giả dược sau khi hiện
chinh với giá trị trước điếu trị, lần lượt lả 10,7 (15,3) và 23,3 (28,4) ms. Dùng rilpivirine
75mg một lần mỗi ngảy và 300 mg một lần mỗi ngây dẫn đến Cmax trung bình ở trạng thái
ôn định lẫn 1ượt gập khoảng 2,6 lằn vả 6, 7 lần C,… trưng bình ở trạng thái ổn định được
quan sát thấy với liều khuyến cáo 25 mg mỗi ngảy một lần cúa rilpivirine
Hiệu quả và an toãn trên lâm sảng
Trên bệnh nhân người lớn nhiễm Hỉ V-1 chưa được đỉều trị
Bằng chứng về hiệu quả của rỉlpivirine dựa trên cảc phân tích dữ liệu ở tuần 96 tờ 2 thử
nghiệm pha 111 ngẫu nhiên, mù đôi, có đối chứng với thuốc có hoạt tính, 1âthứ nghíệm
TMC27S-CZO9 (ECHO) vả TMC278—C215 (THRIVE). Cảo thử nghiệm được thiết kế
giống hệt nhau, ngoại trừ phảo đồ nển (background regimen - BR). Trong phân tích hiệu
quả ở tuần 96, tỷ lệ đáp ứng virus (xác nhận tải lượng virus HIV—l RNA không phát hiện
đuợc (<50 bản sao/rnl)] đuợc đảnh gỉả ở nhũng bệnh nhân dùng rilpivirine 25mg môi ngây
một lần phối hợp với BR, so với bệnh nhân dùng cfavirenz 600 mg một lần môi ngảy phối
hợp với BR. Đã quan sát thắy hiệu quả tương tự đối với rilpivirine trong mỗi nghiên cứu,
chứng minh sự không thua kẻm so với efavirenz.
Các bệnh nhản nhiễm H1V chưa được diều trị thuộc khảng retrovirus trước đó, được thu
nhận vảo nghiên cứu, có HĨV-1 RNA huyết tương ì 5,000 bản sao/rnl và được sảng lọc độ
nhạy cảm đối với các thuốc N(t)RT1 vả sảng lọc không có đột biến liên quan đến khảng
cảc thuốc NNRTĨ Trong nghiên cứu ECHO, BR được cố định với các thuốc N(t)RT1,O gồm
tcnofovir disoproxil fumaratc cộng với emtricitabine Trong nghiên cứu THRIVE, BR bao
gổm 2 thuốc N(t)RT1 được nghiên cúu viên ohọn: tenofovir disoproxil fumarate cộng với
emtricitabine hoãc zidovudine cộng với Iamivudine @ abacavir cộng với lamivudine
Trong nghỉên cứu ECHO, việc phân ngẫu nhiên được phân tẩng theo kết quả sảng lọc tải
lượng virus. Trong nghiên cửu THRIVE, việc phân ngẫu nhiên được phân tầng theo kết
quả sảng lọc tái lượng virus và theo N(t)RT1 BR.
Phân tích nảy bao gồm 690 bệnh nhân ưong nghiên cửu ECHO và 678 bệnh nhân trong
nghiên cửu THRIVE đã hoản thảnh 96 tưần điều trị hoặc ngừng thuốc sớm hợn thời điếm
đó.
Trong phân tích tống hợp cả hai nghiên cứu ECHO vả THRlVE, cảc đặc điếm nhãn khẳu
học và đặc điếm trước khi điều trị là cân bằng giữa nhóm dùng rilpivirine và nhóm dùng
efavirenz. Bảng 3 mô tả một số đặc điếm ban đầu đã được 1ựa chọn của bệnh nhân trong
nhóm dùng rỉlpivirine vả efavirenz.
Bảng 3: Các đặc điếm bệnh ban đầu của các bệnh nhân người lởn nhiễm HIV- 1
chưa điếu trị thuốc kháng retrovirus trong cảc thử nghiệm ECHO vả THRIVE
(phân tích tổng hợp)
Dữ liệu tổng hợp từ các thử
nghiệm ECHO vả THRIVE
Rilpivirine + Efavirenz +
BR BR
N=686 N=682
Cảo đặc điếm bệnh lý trước đỉểu trị
Page 16 of 23
P] Iẩđurtml I.’A` ›S'I’C JJJ1d.ĨUỈtJ DA 1’reợucsi .“(10cL2016 v]
Trung vị của HIV-l RNA trong huyết tương 5,0 5,0
trưởc điêu trị (khoáng dao động), log… bản (2-7) (3-7)
saofml
Trưng vị cùa số lượng tế bâo QD4+ trưởc 249 260
điêu trị (khoảng dao động), x 106tê bảofl (1-888) (1-1137)
Tỷ lệ % bệnh nhân bị: đồng nhiễm virus
viếm gan B/C 7,3% 9,5%
Tỷ lệ % bệnh nhân dùng các phảc đồ nền sau
đây:
tenofovir disoproxil fumarate + emtricitabine 80,2% 80,1%
Zid0vudine + lamivudine
abacavir + lamivudine 14,7% 15,1 %
5,1% 4,8%
BR=background regimen = phảc đố nền
Báng 4 dưới đây oho thấy kết quả phân tich hiệu quả ở tuân 48 và tuần 96 đồi với cảc bệnh
nhân điều trị với rilpivirine và bệnh nhân điều trị với efavircnz từ dữ liệu tổng hợp từ các
thử nghiệm ECHO vả THRIVE Tỷ lệ đảp ứng (xác nhận tải lượng virus HIV- 1 RNA
không phảt hỉện được <50 bản sao/ml) ở tuần 96 lả tương đương giữa nhóm dùng
riìpivirine và nhóm dùng cfavircnz. Tỉ lệ thất bại về virus học cao Ồhơn ở nhóm dùng
rỉlpivirine so với nhỏm dùng efavirenz ở tuần 96; tuy nhiên, hầu hết các trương họp thất
bại vê virus học xảy ra trong vòng 48 tuần điều trị đầu tiên Cảo trường hợp ngừng thuốc
do cảc biến cố có hại cao hơn ở nhỏm dùng et'avirenz ở tuần 96 so với nhỏm dùng
rilpivirine. Phần lớn cảc trường hợp ngừng điếu trị nảy xãy ra trong 48 tuần điều trị đầu
tiên.
Bâng 4: Kết quả về virus học ở cảc bệnh nhân ngưòi 1611 trong cảc thử nghiệm ECHO
vả THRIVE
(Dữ liệu tổng hợp phân tich 0 tuần 48 (tiêu chí chính) và tuần 96,1TT-TLOVR *)
Kết quả trong phân tích ở íuẩn
Kểt quả trong phân tích ở tuần
48 96
Rilpivirin Efavirenz Sự khác Rilpivirin Efaviren Sự khác
e + BR + BR biệt quan e + BR z + BR biệt quan
N=686 N=682 sảt được N=686 N=682 sát được
(95% (95% C1) *
C1) *
Có đáp ứng (xảo nhận 84,3% 82,3% 2,0 77,6% 77,6% 0
1—11V-1 RNA < 50 bản (578/686) (561/682) (-2,0; 6,0) (S32/686) (5291682) (-4,4; 4,4)
sao/ml)ẵiị
Không đáp úng
Thất bại về virus học†
Tổng 9,0% 4,8% ND 11,5% 5,9% ND
(62/686) (33J682) (79/686) (40/682)
5 100,000 3,8% 3,3% ND 5,7% 3,6% ND
(141368) (11/330) (21/368) (_12/329)
> 100,000 15,1% 6,3% ND 18,2% 7,9% ND
(481’318) (22/352) (5 81318) (281353)
PÌ_ Eđumm lf.`iẨ Sf’l',"
Ĩ 1! 111 2121 (› DA V requesl .7 (16161 201² 6_ v]
Page 17 of 23
Tử vong 0,1% [),4% ND 0,1 % 0,9% ND
(11686) [37682) (11686) (67682)
Ngừng thuốc do biến 2,0% 6,7% ND 3,8% 7,6% ND
cô có hại (adverse (141686) [461682) (261682) (521682)
event - AE)
Ngừng thuốc không 4,5% 5,7% ND 7,0% 8,1% ND
do AE1 (311686) [391682) (481682) (557682)
Đáp ứng theo các phân nhóm
Theo phác đồ nền NRTI
Tenofovìr/emtrícitabi 83,5% 82,4% 1,0 76,9% 77,3% -0,4%
ne (4591550) [4501546) (-3,4; 5,5) (4231550) (4221546) (-5,4; 4,6)
Zidovudỉne1lamivudỉn 87.1% 80,6% 6,5 81,2% 76,7% 4,5%
e (881101) (831103) (-3,6; (821101) (791103) (~6,8; 15,7)
16,7)
Abacavir11amỉvudine 88,6% 84,8% 3,7 77,1% 84,8% -7,7%
(’317’35) [28133) (-12,7; (27135) (28133) (_-26,7;
20,1) 11,3)
Theo tải lượng virus ban đầu (bản sao/ml)
S 100,000 90,2% 83,6% 6,6 84,0% `79,9% 4,0
(332/368) (276/330 ('1,6; 11,5) (3091368 (2631329) ('-1,7; 9,7)
) )
> 100,000 77,4% 81,0% -3,6 70,1% 75,4% -5,2
(2461318) (2851352 (-9,8;2,5) (2231318 112667353) (-12,0;1,5)
) )
Theo số lượng CD4 ban đầu (x 106 tế bèoA)
<50 58,8% 80,6% -21,7 55,9% 69,4% -13,6
(20734) (29136) (-43,0; - (19734) (25736) (-36,4; 9,3)
0,5)
2 50-< 200 80,4% 81 ,7% -1,3 71,1% 74,9% -3.7
(1561194) (1431175 (-9,3; 6,7) (1381194 (1311175) (-12,8; 5,4)
) )
ì 200-< 350 86,9% 82,4% 4,5 80,5% 79,5% 1,0
(2721313) (2531307 (-1,2; (2521313 (2441307) (—5,3; 7,3)
) 10,²) )
2 350 90,3% 82,9% 7,4 85,4% 78,7% 6,8
(1301144) (1361164 (—0,3; (1231144 (1291164) (-1,9; 15,4)
) 1590) )
N = số bệnh nhân cho mỗi nhóm điều trị; ND = không xảo định.
* Phân tích theo dự định điêu trị: Thời gian đên khi mât đáp úng virus.
zb Dựa trên xâp xỉ phân phôi chuẩn.
@ Đối tượng đạt được đáp ủng virus (hai lần xét nghỉệm vírus liên tục có tải lượng <50 bản
sao/ml) và duy trì nó qua tuần 48196.
# Sự khác biệt về tỷ lệ đảp ửng được dự đoán (khoảng tin cậy 95%) trong phân tĩch 6 tuần
48: 1,6% (-2,2%, 5,3%) vả trong phân tĩch ở tuần 96: -0,4% (-4,6%, 3,8%); cá p—value
50 bản saoỉml sau khi đã đảp ứng) hoặc những nguời
chua bao gìờ bị ức chế virus (không xác nhận tải lượng Virus <50 bản sao1ml hoặc đang
tiếp tục hoặc đã ngửng thuốc do thiếu hoặc mất hỉệư quả).
1 Ví dụ, không theo dõi đuợc, không tuân thủ, không đồng y tỉếp tục nghiên cứu.
Ở tịuần 96, sự thay đôi trung bình so với trước điều trị của số lượng tổ bâo CD4+ lả +228 x
106 tể bảo/l ở nhóm dùng rilpivirine vả +219 x 10El tễ bảo/l ở nhóm dùng efavìrcnz trong
phân tích tổng hơp các thử nghiệm ECHO vả THRĨVE [ước lượng sự khảo biệt giữa cảc
nhóm điểu trị (khoảng tin cậy 95%):11 3 (… 68 ;29 4,).]
Phân tích đề kháng Itống hợp từ tuần 96, hậu quả khảng thuốc đối vởi các bệnh nhãn bị thất
bại về vỉrus học với tỉêu chí được định nghĩa trước trong để cuong, vả kíểu gen cặp (trước
điều trị và lúc thất bại) được trinh bảy trong bảng 5.
Bảng 5: Hậu quả của khảng thuốc theo phảc đồ NRTI nền đuọc sủ dụng
(dữ líệu tỗng họp tù cảc thử nghiệm ECHO vả THRIVE trong phân tích đề kháng tuần
96)
tenofovir/ zidovudỉne1 abacavir/ Tổng*
emtricitabine lamivudỉnc lamỉvudinc
Nhóm điều trị rỉlpivỉrine
Kháng“ với 6,9 (381550) 3,0 (31101) 8,6 (3135) 6,4 (441686)
emtricitabỉne1]amivưdine
% (n1N)
Khảng với rilpivirine 6,5 (361550) 3,0 (31101) 8,6 (3135) 6,1 (421686)
% (n1N)
Nhóm điều trị Efavirenz
Khảng với 1,1 (61546) 1,9 (21103) 3,0 (_1133) 1,3 (91682)
emtricitabine1lamivudỉne
% (n1N)
Kháng với efavirenz 2,4 (131546) 2,9 (31103) 3,0 (1133) 2,5 (171682)
% (n/N )
* Số bệnh nhân có thất bại về virus học và kỉếu gen cặp (trưởc điều trị và 1110 thất bại) lả 7],
11 và 4 cùa nhóm rilpivirine vả 30,10,vả 2 của nhóm efavircnz, lần lượt với các phảc đồ
tcnofovir/emtrỉcitabinc, zỉdovudine1lamivudínc vả abacav1r1lamw udme
# Khảng thuốc được định nghĩa là sự xuất hiện cùa bất kỳ đột bìến nảo lỉên quan đến khảng
thuốc khi thất bại.
Đôi vởi những bệnh nhân thất bại điều trị với rilpivirine vả những bệnh nhân phát triên
khảng thuốc với rilpivirine, thường thấy có sự kháng chéo vởí cảc thuốc NN'RTI khác đã
được phê duyệt (etravỉrine, efavirenz, nevirapine).
Nghiên cứu '1`MC278-C204 là một thử nghiệm Pha Ilb ngẫu nhiên, đối chứng với thuốc có
hoạt Lính, trên những bệnh nhân người lớn nhiễm HlV-l chưa đỉều trị thuốc kháng
retrovirus, bao gồm 2 phần: gỉai đoạn ban đầu dò liều mù một phẫn [mù liều (rilpivirine)]
đến 96 tuần, tỉếp theo là giai đoạn nhãn mở dải hạn Trong phần thử nghiệm nhãn mở, cảc
bệnh nhân ban đẩu được phân ngẫu nhiên vảo một trong ba mức liều cùa rilpivirine đều
được đíều trị với rìlpivirinc 25 mg mỗi ngảy một lằn phối hợp với BR, ngay khi liều cho
các nghỉên cứu Pha 111 đã được chọn. Bệnh nhân trong nhóm đối chứng được dùng
cfavircnz 600 mg một lần mỗi ngảy phối hợp vởi BR ở cả hai phần cùa nghiên cứu. BR
Page 19 of 23
P1 Eliumm ir'ẫ’Ị SP(` 211111.JOIfi__DÁVrequesf 30061,2016 _vl
bao gồm 2 N(t)RT1 được chọn bới nghỉên cứu vìên: zỉdovudine cộng với lamivudinc hoặc
tcnofovir disoproxil fumarate cộng vởi emtricitabinc.
Nghiên cứu TMC278— C204 đã thu nhận 368 bệnh nhân người lớn nhiễm HIV- ] chưa từng
điều trị, có tải lượng HIV ] RNA trong huyết tương_ > 5,000 bản sao/ml, trước đây đã được
đíều trị < 2 tuần bằng chất uc chế N(t)RT1 hoặc chất ức chế protease, chưa dùng NNRTI và
được sảng lọc tính nhạy cảm với N(t)RT1 vả sảng lọc không có đột biến đặc híệu lỉên quan
đến khảng NNRT1.
Ở tuẫn 96, tỷ lệ bệnh nhân có HIV-l RNA < 50 bản sao1ml đang dùng riipivirine 25 mg
(N = 93) so với bệnh nhân dùng efavirenz (N— - 89) lần 1ưọt là 76% và 71%. Mức tăng
trung bình so với ban đầu vê sô lượng CD4 + là 146 x 10Ô tể bảo1l ở bệnh nhân dùng
rilpivirine 25 mg vả 160 x 106 tế bảofl ở cảc bệnh nhân đang dùng efavirenz.
Trong Sô nhũng bệnh nhân đáp ung ở tuần 96,74% bệnh nhân dùng rilpivirine vẫn có duy
trì tải lượng virus không phảt hiện được (HIV- ] RNA < 50 bản saolml) ở tuân thứ 240 so
với 81% bệnh nhân đang dùng cfavirenz. Không có mối quan ngại nảo về an toản đuợc xác
định trong phân tích 67 tuần 240
Bệnh nhân trẻ em
Dược động học, tinh an toản, khả năng dung nạp và hiệu quả của rilpivirine 25 mg một lần
mỗi ngảy, kểt hợp với BR được nghiên cúu víên lựa chọn có chứa hai NRTl, đã được đánh
gíá trong thử nghiệm TMCZ7S- C213, một thủ nghiệm Pha 2 một nhóm, nhân mở, trên
bệnh nhân thanh thìếu niên nhiễm HIV-l chưa điều trị khảng retrovirus, có cân nặng ít
nhất 32 kg. Phân tích nảy bao gồm 36 bệnh nhân đã hoản thảnh ít nhất 48 tuần điều trị
hoặc đã ngừng thuốc sởm hơn. [
36 bệnh nhân có trung vị cùa tuổi là 14, 5 tuối (dao động từ 12 đến 17 tuối), vả 55,6% lả
nữ, 88, 9% lá người da đen và 11 1% người Châu Á. Trung vị H1V- 1 RNA trong huyễt
tương là 4,8 log… bản sao1ml, và trung vị sô lượng tế bảo CD4 + ban đẳu là 414 x 100 tế
bảo/l (khoảng dao động: 25 đến 983 x 106 tế bảo1l).
Tỷ lệ bệnh nhân có HIV—1 RNA < 50 bản saoÍml ở tuần 48 (TLOVR) là 72,2% (26136). Tỷ
lệ có đáp ứng cao hớn ở những bệnh nhân có tải lượng virus ban đầu 5 100.000 bản sao1ml
(78,6%, 22128) so với nhũng người có tải lượng virus ban đầu > 100.000 bản sao/ml
(50,0%, 418). Tỷ iẹ thẳt bại về virus học lả 22,2% (8136). Tỷ lệ thẩt bại về virus học thấp
hơn ở những người có tải lượng virus ban đầu < 100. 000 bản sao1ml (_,17 9%, 5128) khi so
với nhũng người có tải lượng virus ban đầu > 100.000 bản sao1ml (37, 5%, 318) Cảo đột
biến kháng rilpivirine đã được ghi nhận 157 62,5% (518) đối tượng có thất bại về vỉrus học. Ở
4 trong sô 5 đối tưọng nảy, cũng quan sảt thẩy có kháng NRTI Một bệnh nhân bị ngừng
thuốc do một biến có có hại vả ] bệnh nhân bị ngùng vi lý do không phải do biến cố có hại
hoặc thất bại về vìrus. Ô tuần 48, số luợng tế bảo CD4+ tăng trung bình so với trước đỉễu
ưị là 201,2 x 106 tế bảo/Ì.
Cơ quan Quản lý Duợc phẳm Châu Âu đã hoãn lại nghĩa vụ nộp kết quả nghiên cứu vởi
rilpivirine trên một hoặc nhiều phân nhỏm trẻ em trong điều trị nhiễm HIV- 1 (xem LIÊU
DÙNG VÀ CÁCH DÙNG đế bỉết thông tin về sử dụng thuốc trên trẻ cm)
ĐẶC TÍNH DƯỢC ĐỘNG HỌC
Đặc tính dược động học cúa r1lp1v1rmc đã được đánh giá ở người lớn khỏe mạnh và ở
nhưng bệnh nhân từ 12 tuối trở lên nhiễm HIV chua từng đỉều trị thuốc khảng retrovirus
trước đây. Nồng độ rilpivirine ở những bệnh nhân bị nhỉễm HIV- ] nhìn chung thấp hơn
những người khoẻ mạnh.
Hẩp thu
Page 20 of 23
PI 1Ĩdưram ›ĨÍA' 'J`Plỉ 23.11112016 DAI’reqzml 2001:1.2016 vỉ
Sau khi ưống, nồng độ tối đa trong huyết tuơng cùa rilpivirine thường đạt được trong vòng
4- 5 gíờ. Sinh khả dụng tuyệt đối của EDURAN T chua được biết
Ánh hưởng của thức an lên hẩp thu
Nồng độ rilpivirine thẩp hơn khoảng 40% khi EDURANT được dùng trong tình trạng đói
so với khi được dùng cùng bữa ăn bình thuờng (533 kcal) hoặc bũa an giản chất béo nhiều
calo (928 kcal). Khi EDURANT chi được uông với đồ uông dinh duõng giản protein, nồng
độ lhấp hơn 50% so với khi dùng chung vởi bũa ăn. EDURANT phải được dùng vói bũa
ăn để có được sự hấp thu tối ưu. Uống thuốc EDURANT trong tình trạng đói hoặc chỉ vởi
đồ uống dinh dưỡng có thể lảm giảm nồng độ rilpivirine trong huyết tương, điều nảy có thể
lảm giảm hiệu quả diều trị cùa EDURANT (xem LIÊU DÙNG VÀ CÁCH DÙNG).
Phân bố
Khoảng 99,7% rilpivirine gắn với protein huyết tuong in vilro, chủ yếu là albumin. Sự
phân bố rilpivirine VảO cảc khoang khác ngoải huyết tương (ví dụ như dịch năn tủy, dịch
tiết đuông sinh dục) chua được đảnh giá ở người.
Chuyến hóa ’ , ’
Cảo thí nghiệm in vitro cho thây rilpivirine chủ yêu trải qua quá trinh chuyên hóa oxy hóa
qua trung gian của hệ thông cytochrome P450 (CYP) 3A.
Thải trừ
Thời gỉan bản thải cuối cùng của rilpivirine là khoảng 45 giờ. Sau khi uống đơn liều 14C-
rilpivirine, trung bình 85% vả 6,1% hoạt tính phóng xạ có thế được thu hồi tù phân và
nước tiếu, tương ứng Trong phân, rỉlpivirine dạng không đổi chỉếm trưng bình 25% liếm
dùng Chỉ có vết cùa rilpivirine dạng không đổi (
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng