




'›I
sởvrẾrpuòc
CÓNG TY cỏ PHẦN DƯỢC PHAM MEDBOLIDE
Hỉ MINH
cục QUẢN LÝ mfợc
DÃ PHÊ gu › _
.J...QfJ.J…aẻơ A°°“
To“ d
Lân đâu:…Ổ
”W …… hí
Cộng Hòa Xô Hội Chủ Nghĩa Việt Nom
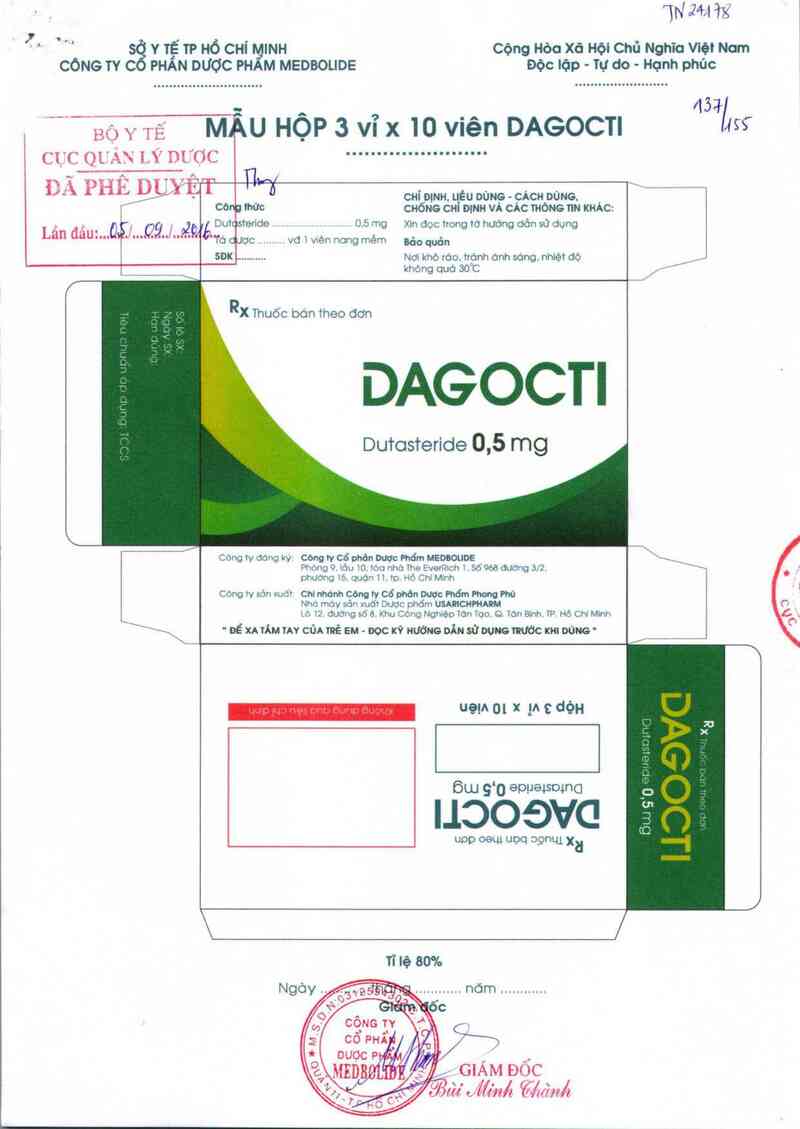
…; Y TẾ MẶU HỘP 3 vỉ x 10 viên DAGOCTI
n,
g thức
SDK
steride … . …
Uợc ...... . vd ] vcèn nong mẻm gò0 quón
cuỉ_ognu. ưèu oùnẹ - cÁcu DÙNG.
CHONG c… DINH VA CAC mòus nu KHÁC:
0.5 mg Xin đọc trong tờ huóng dỏn sủ dụng
Nơi khô róo. trộnh ónh sòng. nhìệt dó
khóng quở 30 C
RX Thuốc bón theo đơn
Cóng ry dóng ky Cóng w cố phỏn Duợc Pth MEDĐOLIDE
Cóng ty sớn …év cm nhónh cong ry cỏ phún Duợc Phdm Phong Phú
~ Dê XA TẢM TAY CỦA mè EM - ooc KỸ nuđue DÃN sử DUNG nước KHI DÙNG -
DAGOCTI
Dutcsteride 0,5 mg
Phòng 0. èỏu 10. too nhủ The EvefRuCh 1. Số % duong 3/2:
phuởng ìb. QuỘn H. tp` HỒ Chí Mtnh
th mơy sởn xuó'i Duợc phố… USARlCHPHARM
Lo 12 duõng sở 8. Khu Cóng Nghnép Tòn TỌO. @ Tón Binh. TP HỒ Chí Munh
_ …^… * z^fdèH
6… g'o epueịsoịno
llOOĐVG
UDD Oồbll UỌQ O_ỌnLLL Xa
Tỉ lệ 80%
, GIÁM ĐỐC
ảc'Jẩinắ ỂlưìnÁ
Độc Iộp - Tự do - Họnh phúc
43%LSỂ
\
CÓNG TY C PHẨN DƯỢC PHAM MEDBOLIDE
s Y TẾ TP HỒ cui MINH
............................
MẦU vỉ: … viên
Viên nong mềm DAGOCTI
Cộng Hòa Xõ Hội Chủ Nghĩa Việt Ncm
Độc Iộp - Tự do - Họnh phúc
Ỉ Dutostende 0,5 mg
Dutosteride 0,5 mg
ẻầ DAGOCTI DAGOCTI DAGOCTI
g Dutcs'reride 0,5 mg Dutosteride 0,5 mg Dutosteride 0,5 mg
'* DAGOCTI DAGOCTI ,…
Du'rosterìde 0,5 mg
CN CTY CPDP PHONG PHÚ - NM SX DƯỢC PHẨM USARICHPHARM
ổ DAGOCTI DAGOCTI DAGOCTI
Dutosteride 0,5 mg Dutosteride 0.5 mg Dutosteride 0,5 mg
DAGOCTI DAGOCTI
Dutosĩeride 0,5 mg
Tỉ lệ 100%
Ngòy ............ fhóng ............ ndm ............
X
-ẩ—~ị áh 7\
I I' ` . Izẵi
Ro
!
)
›
?
Đọc kỹ hướng dẫn sử dụng Irưởc khi dùng
Nếu cẩn thêm thông tin xỉn hỏi ý kiến thầy thuốc.
Chỉ dùng thuốc nảy theo sự kê đơn của thẩy thu» _
DAGOCTI
DAGOCTI
Thuốc bản theo đơn Ti (
TRÌNH BÀY.
DAGOCTI, vìên nang mềm hinh oblong, mảu `
dịch thuốc trong, không mảu, mùi thơm, đồng nhât. Mỗi viê ` = <
uông chứa 0, 5 mg dutasterid.
Tá dược: Ethanol tuyệt đối, Macrogolglyeerol hydroxystearat 20, Sorbitan
oleat, Polyetylen glycol 300_ Gelatin, Glycerin, Nước cất, Kali sorbat, Titan dioxyd,
ethanol 96%, Mảu' ưon oxide yellow.
CÁC ĐẶC TÍNH DƯỢC LÝ:
@
Dutasterid lả ức chế kép 5 alpha—reductase. Dutasterid ức chế isoenzyme 5
alpha-reductase cả type 1 và type 2 là những enzyme chìu trảch nhiệm biến
đôi testosterone thảnh 5 alpha-dihydrotestosterone (DHT). DHT lả androgen
đóng vai trò chinh trong sự tăng sản mô tuyến tiền liệt.
Hiệu quả trên DHT/Testosterone
Khi dùng dutasterìd hảng ngảy, tảc dụng tối đa lảm giảm DHT phụ thuộc
vảo liều dùng vả được quan sảt thấy trong 1 — 2 tuần dùng thuốc.
Điếu nảy là hệ quả được dự đoản trước của tác dụng ức chế 5 alpha-ređutase
và không gây ra bất kỳ tảo dụng không mong muốn đă bỉết nảo.
Dược động hgc
Hấp thu
Viên nang mềm gelatin dumsterid được dùng đường uống. Sau khi uống liều
đơn 0, 5 mg, nồng độ đinh trong huyết tương cùa dutasterid xuất hiện sau 1
đến 3 giờ.
Sinh khả dụng tuyệt đối ở người khoảng 60% sau 2 giờ truyền tĩnh mạch.
Sinh khả dụng của dutasterid không bị ảnh hưởng bời thủc ản.
Phân bố
Số liệu dược động học sau khi uống liều đơn và liều nhắc lại cho thấy
dutasterid có thể tích phân bố lởn (300 đến 500 L)
Dutasterid liên kết cao với protein huyết tương (> 99.5%).
Chuyển hỏa
Dutasterid được chuyền hỏa bời isoenzyme CYP3A4 của cytochrome P450
ở người thânh 2 chất chuyến hóa phụ dạng monohydroxylat, nhưng không bị
chuyến hóa bời CYPIA2, CYP2C9, CYP2CI9 hay CYP2D6.
Trong huyết thanh người, sau những liều đế dạt dược sự ốn dịnh, đảnh giả
bằng phương phảp khối phố dã phảt hiện được dutasterid dưới dạng không
bìến đổi, 3 chất chuyền hóa chinh (4’-hyđroxyduatsterỉde, 1,2-
dihydroxyduatsteride, 6—hydroxydutasterid) và 2 chẩt chuyến hóa phụ (6, 4’ -
dihydroxydutasterid và 15 hydroxydutasteriđ). Củng phảt hiện được 5 chất
chuyền hóa của dutasterid trong huyết thanh người ở huyết thanh của chuột
lớn, tuy nhiên vẫn chưa biết được hỏa học lập thể của nhóm hydroxyl gắn tại
vi trí 6 và 15 trong chất chuyển hóa 0 người và chuột
Thả! trừ
Dutasterid được chuyền hóa rộng răi. Sau khi uống dutasterid 0, 5 mg/ngảy
đề đạt được nồng độ ôn định ở người, 1,0% đến 15, 4% (trung bình 5,4%)
liều uống được bải tiết vảo phân dưới dạng dutasterid. Phần còn lại được
chuyến hỏa vảo phân dưới dạng 4 chất chuyền hóa chính (với tỷ lệ lần lượt là
39%, 21%, 7% vả 7%) và các chất chuyển hóa phụ (dưới 5% mỗi chất).
Chỉ một lượng rất nhỏ dutasterid không đổi (dưới 0,1% liều dùng) được tim
thấy trong nước tiểu người
Vtẵỉ1 nông độ đỉều trị, thời gian bản thải sau cùng của dutasterid là 3 đển 5
tu
Vẫn xác định được nồng độ dutasterid trong huyết thanh (lởn hơn 0,1
ng/mL) đến tận 4-6 tháng sau khi ngừng điều trị.
! terid dược chỉ định dễ điều trị và phòng ngừa sự tiến triến cùa bệnh
" Iảnh tính tuyến tiến liệt (BPH-Benign Prostatic Hyperpiasia) thông
lảm giảm triệu chứng, giảm kích thước (thề tich) tuyến tiền lỉệt, cải
thông nước tiều vả giảm nguy co bi tiếu cấp tính (AUR-Acute
, i etention) cũng như giảm nhu cẩu phẫu thuật liên quan đến BPH.
, dutasterid có thể dùng đơn trị 1iệu hoặc kểt hợp với thuốc chẹn
: o `} . gulosjn. `
fỂỉ`c'G VA CACH DUNG:
gườl lớn (gồm cả người cao tuổi)
Nên nuốt nguyên nang, không nên nhai hoặc mở nang ra vì tiếp xúc với chất
chứa trong nang có thẻ gây nên kích ứng niêm mạc mỉệng - hầu họng.
Dutasterid có thể uống trong hay ngoải bữa ản.
Liều đề nghị cùa dutasterid là một vỉên nang (0,5 mg) uống một lần mỗi
ngây.
Dù có thể thấy đảp ứng sớm nhưng có thể cần điều trị ít nhất 6 thảng dễ có
thể đảnh giá một cách khách quan liệu có thể dáp ứng điếu trị mong muốn
hay không.
Để điều trị bệnh tãng sản lảnh tinh tuyển tỉền liệt, dutasterid có thể dùng dơn
trị liệu hoặc kểt hợp với thuốc chẹn alpha tamsulosin (0,4 mg).
Suy thận
Chưa nghiên cứu ảnh hưởng của suy thận đến dược động học cùa dutasterid.
Tuy nhiên, không cần chinh lỉều dutasterid ở bệnh nhân suy thận
Suy gan
Chưa nghiên cứu ảnh hướng của suy gan đến dược động học của dutasterid.
CHỐNG cni ĐỊNH:
Chống chỉ định dùng dutasterid cho bệnh nhân dược biết quá mẫn với
dutasterid, với các chat ức chế 5-alpha—reduc1ase khác hay với bất cứ thảnh
phần nâo cùa thuốc '
Chống chỉ định dùng dutasterid cho phụ nữ và trẻ em. M
CÁNH BẢO vÀ THẬN TRỌNG:
Dutasterid được hấp thu qua da nên phụ nữ và trẻ em phải tránh tiếp xúc với
viên nang vỡ. Nếu tiếp xúc với viên nang vỡ, nên rửa vùng tiếp xúc với xả
phòng và nước ngay lập tức.
Chưa nghiến cứu ảnh hưởng cùa suy gan đến dược động học của dutasterid.
Nên sử dụng dutasterid thận trọng ở bệnh nhân mắc bệnh gan do dutasterid
được chuyển hóa rộng răi vả có thời gian bán thải từ 3 đến 5 tuần (xem phần
Liêu lượng vờ cách dùng và phần Dược động học).
Ắnh hưởng đển kháng nguyên đặc hiệu tuyến tiền liệt (PSA — Prostate
Specil'tc Atigen) và phát hiện ung thư tuyến tiểu liệt.
Nên thăm khảm trực trâng bắng ngón tay cũng như tiến hảnh các đảnh gỉá
khảc để phát hiện ung thư tuyến tỉền liệt trước khi sử dụng dutasterid và sau
đó nên kiềm tra định kỳ.
Nổng độ kháng nguyên đặc hiệu tuyến tiền liệt trong huyết thanh (PSA) là
một thảnh phần quan trọng trong quả trinh sảng lọc để phát hiện ung thư
tuyến tiền liệt.
Bệnh nhân dùng dutasterid nên có một giá trị PSA cơ bản mới, được thiết lập
sau 6 tháng điều trị với dutasterid. Khuyến cáo theo dõi thường xuyên giá trị
PSA sau đó. Bất kỳ sự Lãng PSA nảo cũng được xảc nhận từ sự tăng PSA
thấp nhất trong khi đang dùng dutasterid có thể là dẩu hỉệu sự hiện diện cùa
ung thư tuyến tiền liệt (đặc biệt ung thư mức độ cao) hoặc sự không tuân thủ
điều trị với dutasterid và nên được đảnh giá cấn thận, thậm chí cả khi cảc giá
trị nảy vẫn nằm trong giới hạn bình thường cùa nam giới không dùng chất ức
chế 5a-redutase. Đế đảnh giá giá trị PSA ở bệnh nhân dùng dutasterid, nên
tim cảc giá trị PSA trưởc đó để so sảnh.
Điều trị với dutasterid không gây ảnh hưởng đến việc sử dụng PSA như một
công cụ chuẩn đoán ung thư tuyến tỉền liệt sau khi giá trị cơ bản mới đã
được thiết lặp.
Tổng lượng PSA huyết thanh trở về giá trị cơ bản trong vòng 6 tháng sau khi
ngừng thuôc.
Tỷ lệ giữa lượng PSA tự do và PSA toản phẩn vẫn hằng định ngay cả dưới
tác động cùa dutasterid. Nếu bác sĩ muốn sử dụng phần trảm PSA tự do như
biện pháp bổ sung để phát hiện ung ư… tuyến tiền liệt ớ nam giới dang dùng
dutasterid thì không cần điều chinh giá trị của ti iệ nảy.
. I
Số 1iệu nghiên cứu giai đoạn 11 cho thấy giảm thanh thải đutasten'd k ` :: _ :
đồng thời với các chất ức chế CYP3A4 như verapamil (37%) và di '. — —. .
(44%). Ngược Iạỉ, không thấy giảm thanh thải khi đồng thời du , .. * :
amlodipin hay chất đối kháng kênh calcium khác. Gíảm thanh th'ẵi mQỆNG ỊY
tăng nồng độ toản thân với dutasterid khi có sự hiện diện cùa cáẩzĩc' ất ứGGIÉHAỤ
CYP3A4 thường không có ý nghĩa lâm sảng do phạm vi an toả1i-fộng (Uệũ PHẦN
nhân đã được sư dụng đến gấp 10 lần liều khuyên dùng trong 6 th'árỉgMfflWl—IDE
không cần điều chinh liều. - _.
In vitro, dumstcrid không được chuyến hóa bời các isoenzyme C * g/"
CYP2C9, CYP2CI9 vả CYP2D6 của cytochrome P450 ở người.
Dutasterid không ức chế các enzym chuyển hóa thuốc của cytochrome P450
ở người thử nghiệm in vitro, cũng như không gây cảm ứng các isoenzym
CYPIA, CYPZB vả CYP3A của cytochrome P450 ở chuột lớn và chó trên
thử nghiệm in vivo.
Cảc nghiên cứu in vitro cho thẩy rằn dutasterid không thế chổ warfarin,
diazepam hay phenytoin trong liên k t protein huyết tương, các loại hợp chẩt
nảy cũng không thay thế dutasteríd. Các hợp chất nảy được tiến hảnh thử
nghíệm về tương tác thuốc ở người bao gồm tamsulosin, temzosin, warfarin,
digoxin vả cholestaramin và không quan sát thấy những tương tác có ý nghĩa
lâm sảng.
Mặc dù chưa tiển hảnh nghiên cứu các tương tác đặc hiệu với cảc hợp chất
khác nhưng khoảng 90% đối tượng trong nghiên cứu lớn giai đoạn 11 đã
uống dumstedd đồng thời với các thuốc khảc. Không quan sát thấy các
tương tảc bất lợi có ý nghĩa về mặt lâm sảng trong các thử nghiệm lâm sảng
khi dutasten'd được dùng đồng thời với các thuốc giảm lipid mảu, cảc chắt
ức chế men chuyền angiotensỉn (ACE), cảc chất chẹn beta-adrenegrỉc, các
thuốc chẹn kênh calcium, các corticosteroid, các thuốc lợi tiểu, các thuốc
khảng viêm không steroid (NSAIDs), cảc thuốc ức chế phosphodiestease
type V vè các khảng sinh nhóm qưinolon.
Một nghiên cứu về tương tác khi dùng dumsterid đồng thời với tamsulosín
hay terazosin trong 2 tuẫn không thấy có bằng chứng về tương tác dược
độn học hay dược lực học.
PHỤ NỮ c THAI vÀ ĐANG CHO CON BÚ W
Không sử dụng cho phụ nữ có thai và đang cho con bú
ẨNH HƯỞNG LÊN KHẢ NĂNG LÁ] XE VÀ VẬN HÀNH MÁY MÓC:
Dựa vảo các đặc tính dược động học và dược 1ực học cùa dutasterid thì việc
điều trị bằng dutasterid không ánh hưởng đểu khả năng lái xe hay vận hảnh
mảy móc.
TÁC DỤNG KHÔNG MONG MUÔN:
Rối lo n hệ miễn dịch
Rất hi m: phản ứng dị ửng, bao gổm phảt ban, ngứa, mề đay, phù khu trú và
phủ mạch.
Rối Ioạn da vả mô dưới da
Hỉếm: rụng lông (chủ yếu rụng lông trên cơ thể), chứng rậm lông tóc
Thông báo cho bác sĩ những tác dụng không mong muốn gặp phải khi
dùng thuốc
QUÁ LIÊU
Tron những nghíên cứu trên người tinh nguyện, những đơn liều dutasterid
lên đen 40 mglngảy (cao gấp 80 1ần điều trị) trong 7 ngảy không thấy quan
ngại đảng kể nảo về tính an toản.
Trong các nghiên cứu lâm sảng, khi cho bệnh nhân dùng liều 5 mg mỗi ngảy
trong 6 tháng, không thẩy có thêm tác dụng không mong muốn nảo ngoải
những tác dụng không mong muốn đã gặp ở liều điều trị 0,5 mg.
Do không có thuốc giải độc đặc hiệu cho dutasterid nên trong trường hợp
nghi ngờ quá liều thì nên tiến hảnh đỉều trị triệu chửng và dùng các biện
phảp hỗ trợ thích hợp.
HƯỞNG DÂN sử DỤNG/XỬ LÝ
Dutasterid dược hấp thu qua da, do đó, phụ nữ và trẻ em phả'
với các viên nang vỡ. Nếu có tiếp xúc với viên nang vỡ, nê '
xúc với xả phòng và nước.
BẢO QUẢN : Bảo quản nơi khô mát, tránh ảnh sáng, nhiệt độ không quá 30°C.
HẠN DÙNG: 36 thảng kể từ ngăy sản xuất
TRÌNH BÀY : Hộp 03 vi, vi 10 vỉên nang mềm.
TIÊU CHUẨN : TCCS I J
ĐỀ XA TẦM m TRẺ EM._ _ `
ĐỌC KỸ HƯOZVG DẮz_v SƯDUNG THUỘC TRUUC_ KHI DUNG
NEU_ CẤN mEM THONG mv XIN Hòj Y KIẾN CUA ngà Y mu0c
KHONG DUNG muóc QUA HAN SƯDỤNG GHI TREN HỘP
Sản xuất tại nhà mảy:
Tên cơ sở sản xuất: Chi nhánh Công Ty Cổ phần Dược Phẩm Phong Phú —
Nhã mảy sx DP USARICHPHARM
Địa chỉ: Lô 12, Đường số 8, khu công nghiệp Tân Tạo, Quận Bình Tân, Thảnh
phố Hồ Chí Minh.
Điện thoại: 08. 37547998 … 08. 37547999 Fax: 08. 37547996
Phân phối bởi:
Tên cơ sở đăng ký: Công ty Cổ phần Dược phẩm Medbolide
Đia chi: Phòng 09, lẳu 10, tòa nhả Everrich l, sớ 968, Đường Ba Tháng Hai,
P.15, Q.11, TPHCM, Việt Nam
sớ điện thoại: 08.62622255 Fax: 08.62642568
TP.HCM,ngảy 12 tháng 04 năm 2014
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng