










' BỘ Y 1fỉ _
cục QUẢN LÝ DƯỢC 6Ở/gẫ
ĐÃ PHÊ DUYỆT
l
' Lản ơathẮỞJfflỄ l —
` 1
cg E Ế !
² ..U 3² ẵ
Ề°ềằầ ịỂãỄỆ
- gẵgễ ắ88« _
ơsgs* .Ễ n£Rã
Ẹgẵeẵa oẳAeã %
Ểẫ 8uẵ Ẻ ỉễ$ Ế
oỔ NA INHễằ
.«r ~ ,
“”mJ`cưmaóc
Illllllllll DS'IWTmHỒNG
ý ỉ
ủ0ỉ
uon"ẩifflq
dquo
" ., m… ..., mqu
Ú " Ê “ ….m 95 II.….M
mơn…
munosmưonnnc
Ễ …ũ. Ễ …!L ế …a. ẽ …n
E0dHủd ’ : .
pts;amtinvgm ' , / oxolỉplotin
m....w... ,\/
uuluiùn
su.…ao’c 50mg
. NhMDCNredby:
ÌVldl WEAIBỈNỂGPỈYW
1—5 7-²3 ond ²539
Mdưluliedhn LadeũoceMULfflVf
Fqu V1C3170Auslrolin
ơ!doởlửúsừolm:
PlemereudmdoMìeoũet
mumm
@ Cytotoxưc (ễ) Cytotoxic (ẫ) Cytotox1c
uaazn _ m_
nu … 50:- hw son
1—5 7—23 ond 25—39
Lada Ploce MUGRAVE
VIC 3170 Austmủ
PHÓ cục TRUỞNG
JVỵayểẵz AÍ/ỡn fflanắ
lfflfflfflh BOYTẸ
nu
CỤC QL'ẢN 1-1" moc
ĐÃ P DUYỆT
1²²/ h
uỵqdun Lân đẳU' 61 ỊẮÒ ! fflẫ
uoipelmni
uuuuuuuuuuuuuuuuuuuuuuuuuuuuuu
UỊIDIỦJWO .,190
=gw Ẹ ậ …Ẻiầ eỗẫ
g ,..a, ê …a. ẽ …e. ê …n.
%“…“ẵẳ DBL'“ Oxoliplulin
ẦÊủ f0l' Iniediffl
LỀỦUỞM oxaliplutin
d; mú … uq …
Sun Uow …
(Ễ1 Cvtotoxic
PHÓ cục TRUỞNG
JVMễn ”Vã/n W
; W_—
| lul' | I- cm…
lư…im
Dmogemduứviủluhut'
ủeteodmdosedleulel
nsumm
ffl Cyớotoxú
… …..mm
ưủ.
cmtuhn m chlơobicl
W
Modwod
mhunìnmi
1~5 7-23m25—30
MOMMULOM
WCSTTOMOrdG
M…IW
crcfflƯf—ìC
\ ĐÃ PHÊ DUYỆT
Lân đâu:M
@ỉÁQy Ặẵ... …
Nhãn phụ
Rx Thuốc kê đơn
DBL OXALIPLATIN
Mỗi lọ bột đông khô pha tiêm chứa Oxaljplatỉn 100 mg
Hộp ] lọ. Truyền tĩnh mạch. Chỉ định, liều dùng và cách dùng,
chông chí đinhdíiucmlùhưúnzdãnsíuìunathuâefflngụảnỷ…
nhìệt độ dưới 30°C.
SĐK:
Số lô SX, NSX, HD: Xem (B), DOM, EXP trên bao bì.
Nhà sản xuất: Hospỉra Australia Pty Ltd
1-5 7- 23 and 25- 39 Lexia Place MULGRAVE VIC 3170 Australia
Nhã nhập khẩu: 1
Để xa tầm tay trẻ em. Đọc kỹ hướng sử đụng trưởc khi
dùng. Các thông tin khác đề nghị xem tờ hướng dẫn sử
dạng kèm theo
Hospira Australia Pty Ltd
« -59 097 64 sao
Yoko Keng Teh
Director
%
DBL Oxaliplatin
Tên thuốc: Oxah'platin, bột đông khô để pha tiếm
Hoạt chẩt: Mỗi lọ chứa Oxaliplatin 100 mg.
Mô tâ: Tên hóa học của Oxah'platin lả [SP—4—2]—(lR,2R)—cyclohexane-l,2-diamine-k²N,N'
(oxalate(2)…kzol, O²]plaiinum (11).
Công thửc của Oxaliplatin lã CaHMNZOáPỈ. vả trọng lượng phân từ lá 397.3.
Sô'CAS: 61 825-94-3
Oxaliplatin dưới dạng hột kểt tinh trắng hoặc gẫn như trấng, tan ít trong nước, rất ít tan trong Methanol
vả gẩn như không tan trong ethanol.
Thìmh phẫn tá dươc : Oxaliplatin bột đông khô dể pha tiêm còn chứa lactose.
Dược lý học
Dược lực học:
Oxaliplatin lả thuôo chống ung thư thuộc văo nhóm mới các dẫn chất gốc Platin, trong đó phân tử
Platin đã phức hợp hóa với 1,2—diaminpcyclohexan (dach) và nhóm oxalate Ox_aliplatin lả đổng phận 7
đôi hình dơn độc Cis— [òxáláto (traús—l- 1,2-DACH) platinum] Oxaliplatin có họat pho rộng oầffl về đội:
tĩnh tê bão … vitro lẫn hoạt tính chống 11 in vivo trong nhiễu hệ thông mô hình 1.1 khác nhau,bao gồm
cãc mô hình ung thư đại trực trầng. Oxaliplatin cũng chứng tỏ có hoạt tĩnh in vitro vả in vivo ở nhiễu
mô hình ung thư khác nhau đã kháng cisplatin.
Đã nhận thấy có hoạt tĩnh hiệp đồng độc tế bảo khi phối hợp với fiuorouracil cảơ in vitro lẫn …
vivo.
Các nghiên cứu về cơ chế tãc động của Oxaliplatín tuy chưa được hòan tòan biết rõ, cho thấy rầng cảc
dẫn chất tan trong nước do sự sinh chuyển hóa của Oxaliplatin tương tác với DNA để tạo ra những
lìên kết cả giữa và trong các đọan mạch, từ đó gây ra sự gián đọan trong quá trình tổng hợp DNA dẫn
đến cãc hiệu lực độc tế băo vả chống u.
Dược dông học:
Dược động học của từng dẫn chất có họat tĩnh chưa dược xác dịnh. ược độ'hg học của Platin siêu lọc
được, đại diện cho hỗn hợp toãn bộ các lọai platin không liên kểừó 1__ at Énh vã không họat tĩnh, tiểp
theo lẫn tiêm truyền nhỏ gịot Oxalỉplatin trong 2 gìỡ với liếư 130 cứ 3 tuẩn một lẩn, cho từ ]
đển 5 đợt và liều 85mglm2 cứ 2 tuấn một lẩn, cho từ 1 đến 3 đợt, lả như sau:
Băng tóm tất đánh eiá các thông sốdươc đông hoc của Platinum rronz dich siêu Ioc tiếp sau các liều
bõi .cổOxalinlatin với liễu 85m2/m2. 2 !uần mô! lần hoãc 130m2/m2. 3 !uẩn môt lẩn.
Liều dùng C max AUC …, AUC ,… T ’/'2 T Va T Vz V ss CL
(uglml) íuglml.h) fuglml.h) a(h) Bihì v(h) (L) íLih)
85mg/m2
Trungbình 0.814 4.19 4.68 0.43 16.8 391 440 17.4
SD 0.193 0.647 1.40 0.35 5.74 406 199 6.35
130 mg/m2
Trung bình 1.21 8.20 119 0.28 16.3 273 582 10.1
SD 0.10 2.40 4.60 0.06 2.90 19.0 261 3.07
Các trị số trung bình AUCo.gg, C,… đã được xác định ở chu kỳ 3 (85mg/m2) hoặc chu kỳ 5
(lSOmg/m2)
Các trị sổtrung bình AUC o.… Vss và C1 đã được xãc định ở chu kỳ ]
KhiĨẵư'ạ ( ẹốtẳliaỹtỵạLtd
A . ’ ,, ầ01511 ?th1
Yoko Keng Teh
Director
Các mị số trung bình Cu,… AUC,AUC 0.4g, Vss vã Cl được xãc định qua phân tích không chia
ngăn.
T % a, T Vz B, T Vz y được xác định qua phân tích chia ngăn (các chu kỳ 1-3 phối hợp)
Khi chấm dứt lẩn tiêm truyền trong 2 giờ, 15% platin đã dùng có mặt ở hệ tuẩn hòan tòan cơ thể, phẩn
còn lại 85% được phân bố nhanh chóng văo các mô hoặc thãi qua nước tiểu. Liên kết không thuận
nghịch được với các tế bâo hổng cẩu vã huyết tương lã do các thời gian bán thải ở các mô đó đã ăn
khớp với chu trình tự nhiên cũa tể băo hồng cẩu vả albumin huyết tương. Chưa nhận thấy có tích lũy
trong dịch siêu lọc huyết tương tiểp theo liều 8Smg/m2 cứ 2 tuẫn một lẩn hoặc l30mg/m2 cứ 3 tuẩn
một lẩn vã trạng thái ổn định đã đạt được ở chu kỳ 1 trong cảc mô năy. Sự biến đổi giữa vã trong
từng đối tượng thường ở mức thấp.
Sinh chuyển hóa in vitro được coi như lã kết quả cũa sự giáng hóa không do enzyme và không có
chứng cô về sự chuyển hóa qua trung gian Cytochrom P 450 cũa vòng diaminocyclohexan (DACH).
Oxaiiplatin đã trăi qua sinh chuyển hóa rộng rãi ở các bệnh nhân và đã không phát hiện dược phẫn
thuốc còn nguyên vẹn trong dịch siêu lọc huyết tương sau khi kết thúc tiêm truyền trong 2 giờ. Văi
sân phẩm sinh chuyển hóa có độc tính tế bão bao gốm các lọai monochloro, dichloro vả diaquo DACH
~————platitrdã*đưỢơphát~hiệmởưuẩn-hòair'tờaưthể*cùng~với~một*số’Các~dẫn~chấtiiẻn"hợp'khôn'gcờhọat
tĩnh ở các thời điểm về cuối.
Platin chủ yếu thâi trừ văo nước tiểu, với độ thanh lọc phẫn lớn trong vòng 48h sau khi tiêm. Văo
ngả y thứ 5, khỏang 54% cũa tổng liễu được thấy lại trong nước tiểu và dưới 3% trong phân.
Đã nhận thấy có sự suy giảm rõ rệt về độ thanh lọc của platin siêu lọc được từ 17,6 1: 2,18 L/h đển
9,95 i 1,91 L/h trong trường hợp tổn thương thận (Độ thanh thải creatinin 12-57 ml/phút) cùng với sự
giãm sút rõ rệt về mặt thống kê ở thể tích phân bố từ 330 1 40,9 đến 241 1- 36,1 L. Tác động cũa sự
tổn thương nặng ở thận đến độ thanh lọc platin chưa được đánh giá.
Chỉ đinh
Oxaliplatin kết hợp với Flourouracil vã Acid Folinicđược chỉ định trong\c trường hợp:
0 Điểu trị hỗ trợ trong trường hợp ung thư đại trăng giai đọan 111 ổs C) sau khi phẫu thuật
cắt bỏ hòan tòan khối u tiên phát
0 Điều ttị ung thư đại trực trăng tiến triển
Chống chỉ định
Oxaliplatin chống chỉ định với các bệnh nhân sau:
- Có tiền sử quá mẫn đã biết với Oxaliplatin
— Có mang thai
- Cho con bú
~ Có hiện tượng suy tủy trước khi bắt đẩu liệu trình thứ nhẩt, trên 06 số số 1iệu được nên về
bạch cẩu trung tính < 1,5x10 % vâ/hoặc số đếm tiểu cẩu <75x10 %.
- Có bệnh về thẩn kinh cãm giác ngọai biên, có thể hiện rối lọan chức năng trước khi bất đẩu
liệu trình thứ nhất.
- Có suy thặn nặng (Độ thanh lọc Creatìnin < 30ml/phũt)
— Oxalỉglatin không đươc khuvến cáo dùng cho trẻ em_ịưới 15 tuổi vì tính an toăn vã hiêu
g_tẺ chưa đươc xãc đinh ở nhóm bênh nhân nầv
Thận trọng
Tổng quát Hospira Australia Pty Ltd
ABN 58 097 4 330
W.
Yoko Keng Teh
Direciof
Oxaliplatin phăi được bác sỹ chuyên về ung thư có kinh nghiệm trực tiếp cho bệnh nhân sử dụng hoặc
giám sát việc sử dụng.
Phản ứng dị ứng:
Đã có những báo cáo về những phản ứng kiểu phân vệ với Oxaliplatin và những phãn ứng nảy có thể
xuất hiện trong vòng mấy phút sau khi tiêm. Những bệnh nhân có tiểu sử có phân ứng dị ứng với các
hợp chất cũa Platin cẩn được theo dõi về các triệu chứng dị ứng. Trong trường hợp có phân ứng phản
vệ với Oxaliplatin, cẩn phãi ngững ngay việc tiêm truyền vã tiểu hănh ngay việc điều trị các triệu
chứng thích hợp. Chống chỉ định việc dùng lại Oxaliplatin.
Độc tỉnh với thần kinh:
Độc tính với thẩn kinh (xem phẩn phân ứng có hại) cũa Oxaliplatin cẩn được theo dõi cẩn thận, đặc
biệt trong trường hợp có phối hợp với các thuốc khác có độc tinh với thẩn kinh. Trước khi thực hiện,
mỗi iẩn dùng thuốc, cẩn được thăm khám về thẩn kinh vã sau khi sử dụng vẫn được định kỳ thăm
khám. Hiện nay chưa rõ lả có phải những bệnh nhân có tình trạng bệnh lý kéo theo những tổn thương
thẩn kinh ngọai biên thì ngưỡng liễu lượng Oxaliplatin dễ gây bệnh thẩn kinh ngọai biên sẽ hạ thẩp
hay không? Đối với những bệnh nhân có chứng lọan câm thanh quản —hẩu cấp tinh phát triển trong
thời gian tiêm truyền kéo dãi 2 giờ, trong vòng 48 giờ sau đó thì lẩn tiêm truyền Oxaliplatin tiếp theo
phâ—i—kéo—dăi—é—giờ.—Để—dự-phòng—hiện—tượng—dị—eâm…nây,…phãi-báo—eho—bệnh—nhân—tránh—bịJạ-nhựtránhr
ãn những thức ản lạnh, để uổng lạnh trong khi tiêm truyền Oxaliplatin hay trong vòng 48 giờ kể từ sau
khi tiêm.
Độc tính với dạ dây — ruột:
Độc tĩnh với dạ dăy — ruột, biểu hiện qua triệu chứng buồn nôn vả nôn. Để dự phòng độc tính nảy,
dùng các liệu pháp chống nôn, trong đó có các chất đối khãng với 5-HT3 vã các corticosteroid. Hiện
tượng nôn, ĩa chây nặng có thể gây ra mất nước, tẩc ruột, hạ Kali máu, nhiễm acid chuyển hóa, suy
thậ 11, đặc biệt hay thấy khi kết hợp Oxaliplatin với Flourouracil.
Độc tỉnh với máu:
Để theo dõi độc tính với máu, tiến hănh đếm máu tòan phẩn, dếm phân biệt các dạng bạch cẩu trước
khi tiểu hảnh liệu pháp và trước khi bắt đẫn một liệu trình tiếp theo. Có thể xuất hiện độc tính với
máu có tỉnh chất đặc ứng, đặc biệt đối với những bệnh nhân trước đó đã dùng những liệu pháp độc với
tủy.
Độc tính với phổi:
Oxalipiatin có thể liên quan đến hiện tượng xơ hóa phổi (0,7% số bệnh nhân nghiên cứu) vả hiện
tượng nây có thể gây tử vong. Trong trường hợp xuất hiện những triệu chứng đường hô hấp không giăi
thích được như ho khan, khó thở, thở có tiếng lép bép, có đãm thâm nhiều'fiẵịổi lua chụọ X quang,
phâi ngừng dùng Oxaliplatin ngay cho đến khi những nghiên cứu tiếp theoV oi lọai trừ bệnh phổi
kẽ hay xơ hóa phổi (Xem phẩn “tác dụng có hại”). \"
Độc tính với gan:
Đã có những báo cáo về các phãn ứng liên quan đến hội chứng tắc xoang gan, bao gổm hiện tượng
tăng sản thảnh cục (xem phẩn “tác dụng có hại”). Trong trường hợp có kết quả xét nghiệm chức năng
gan không bình thường hay trường hợp tăng huyết áp tình mạch cứa, không giâi thích được qua di căn
ở gan thì cẩn nghiên cứu đến hội chứng tắc xoang gan.
Suy thận:
Chưa có công từnh nghiên cứu việc dùng Oxaliplatin cho người suy thận nặng. Do đó chống chỉ định
dùng thuốc nãy cho những người suy thận nặng.
Có ít thông tin về tính an tòan cũa Thuốc cho những người suy thận mức vữa phâi và khi sử dụng
thuốc năy phãi cân nhắc đẩy dữ tương quan giữa lợi ích-nguy cơ cho bệnh nhân. Tuy nhiên có thể bắt
đẩu điếu trị với liều thường dùng. Trong trường hợp năy phãi theo dõi chặt chẽ chức năng thận vả
hiệu chỉnh liều dùng theo độc tinh đã thể hiện.
Hospira Australia Pty Ltd
ABN 58 097 064 3'30
Yoko eng Teh
Director
Không có nhu cẩu phãi hiệu chỉnh liễu với bệnh nhân rối lọan chức năng thận nhẹ.
Thiểu nãng gan:
Chưa có công trình nghiên cứu dùng Oxaliplatin cho những trường hợp suy gan nặng. Không thấy tãng
độc tính cấp của thuốc ở phân nhóm những bệnh nhân mà kết quả các xét nghiệm về chức nãng gan
lá không binh thường ở đường nền. Trong lâm sâng, khi nghiên cứu phát trìển, không để cập đến việc
hiệu chỉnh ].iểu cho những bệnh nhân 06 kểt quả xét nghiệm chức năng gan không bình thường.
Khả năng sinh ung thư gây biển dị và ãnh hưởng đến khả nãng sinh sản
Oxaliplatin thể hiện tính chất gây biến dị và lăm gẫy thể biển sắc ở động vật có vú in vitro cũng như
in vivo. Khả năng sinh ung thư cũa Oxaliplatin còn chưa nghiên cứu nhưng những hợp chất có cơ chế
tác dụng tương tự, có độc tính với gen tướng tự thường thể thiện có tính sinh ung thư. Oxaliplatin cẩn
được coi là có khả năng sinh ung thư.
Trên các con chó dùng Oxaliplatin có thấy giãm trọng lượng vả giãm sản tuyến tinh hòan, tiểu tới
ngừng sản khi liều lượng 2 lSmg/m2. Tuy nhiên không thấy ãnh hưởng đến chức năng sinh sân ở
chuột cống dùng thuốc với liếu vượt quá l²mglm2lngăy, mỗi liệu trình 5 ngăy ở chuột đực cũng như
chuột cái.
Sử dụng khi có thai :
Xếp~hnng—D-câe—nghiên—cứưtạo-hình-trở-lạiwềđộetínhđâ-choáhấykhông…hoạt-tính-sinhquãi…thaiở— __ ………
chuột cống hoặc thỏ với các liều tiêm tĩnh mạch 6 và 9 mg/m2lngăy tương ứng (nửa liều lâm sãng
khuyến cáo tối đa dựa văo diện tích da cơ thể ). Tuy nhiên để nhận thấy ở chuột cống tảng số tử vong
ở phôi, giâm trọng lượng ở bâo thai vả quá trình tạo xương bị chậm lại. Đã ghi nhận lã những dẫn chẩt
có liên quan với cơ chế tác dụng tương tự có tác dụng gây quái thai. Chưa có những nghiên cứu thích
hợp và được kiểm chứng đúng ở phụ nữ có thai. Nếu thuốc năy dùng trong khi mang thai hoặc nếu
bệnh nhân có thai trong khi dùng thuốc năy thì bệnh nhân đó phãi được nhận biết về nguy cơ tiểm ẩn
đến bão thai. Có thể là Oxaliplatin độc với băo thai người ở liều điều trị đã khuyến cáo và do đó có
chống chỉ định trong khi có thai.
Cũng như với các tãc nhân độc tế báo khác, cẩn tiến hănh các biện pháp tránh thai có hiệu quả ở
những bệnh nhân có tiễm ẩn khả nảng sinh sân trước khi băt đẩu hóa tnị liệu với Oxalipiatin
Sử dụng khi cho con bú :
Chưa có dữ liệu về sự tiểt Oxaliplatin vâo sữa ở súc vật hoặc người
Oxaliplatin có chống chỉ định ở phụ nữ đang nuôi con bú.
Trẻ em :
Oxaliplatin không đươc khuyến cáo dùngc_ho trẻ em vì tính an toăn vã hiêu uuả chưa đươc xác
đinh ỏ“ nhóm bênh nhân nèỵ.
Người cao tuổi: .
Chưa nhân thấy có gia tăng về độc tính nặng khi Oxaliplatin được dù` _n đội: hoặc phối hợp với
fluorouracil ở bệnh nhân trên 65 tuổi, do đó không cẩn điểu chỉnh liễu dù g ỷhg cho bệnh nhân cao
tuổi.
Những tương lác với các thuốc vả trị liệu khác :
Ở những bệnh nhân đã dùng liều đơn độc 85mglm2 Oxalipiatin ngay trước khi sử dụng fiuorouracil,
chưa nhận thấy có biển đổi nằm về mức nhận thấy phơi nhiễm với fiuorouracil . Tuy nhiên ở những
bệnh nhân dùng liều fluorouracil hăng tuẩn vả Oxaiipiatin cứ 3 tuẩn liều 130 mg/m2 đã nhận thấy có
gia tăng 20 % các nỗng độ fluorouracil ở huyết tương in vitro, chưa nhận thấy hoặc ở mức ít sự chuyển
dịch Oxaliplatin liên kết với các protein huyết tương với các tãc nhân sau đây: Erythromycin, các
salicylat, granisetron, paclitaxel, vã natri valproat, Oxaliplatin có tương kỵ với các dung dịch chứa
clorỉd vã các dung dịch base (kể cả fluorouracil ), do đó Oxaliplatin không dược trộn lẫn với câc dung
dịch nây hoặc đồng thời qua cùng một đường truyền tĩnh mạch. Với các thuốc khâc chưa có dữ liệu về
mặt tương kỵ.
Hospira Australia Pty Ltd
ABN 58 097 064 330
Yoko Keng Teh
Director
Sự vắng mặt cũa chuyển hóa qua trung gian Cytôchrôm P450 đã chỉ cho thấy lã Oxaliplatim không
có thể điểu biến chuyển hóa P450 của các trị liệu dống thời qua cơ chế cạnh tranh.
Thông báo cho bệnh nhán :
Bệnh nhân cẩn được thông báo thích hợp về nguy cơ tiêu chây, nôn vả giãm bạch cẩu trung tĩnh sau
trị liệu với Oxaliplatin | fluorouracil để cho họ có thể kịp thời tiểp xúc với bão sĩ điều trị nhẵm chữa trị
thỉch hợp.
Bệnh nhân vả người chăm sóc cẩn được thông báo về các tác dụng phụ xãy ra với Oxalipiatin vả đặc
biệt lâ, những người bệnh phải được biết truớc về:
-Tránh dùng các thực phẩm và đồ uống lạnh và tránh để da tiếp xúc trước khi phơi nhiễm với khí lạnh
bên ngoăi trong vòng 48h tiếp theo khi dùng Oxaliplatin vì có thể gây ra cãc biến cố thẩn kinh hoặc
lảm nặng thêm các tác dụng phụ do phơi nhiễm với lạnh.
-Tiếp xúc ngay với bác sĩ nếu thấy bệnh nhân bị sốt, nhất là khi kèm tiêu chảy kéo dăi hoặc có chứng
cớ nhiễm khuẩn, vì như vậy cho thấy công thức máu giãm đi.
-Tiếp xúc với bác sĩ nếu vẫn còn kéo dãi nôn mửa, tiêu chãy, triệu chứng mẩt nước, ho hoảc khó thở
hoặc có dấu hiện phân ứng do dị ứng xảy ra.
___.PhảnJ't'nglthônggmongmuốn—W _ __ ________ 2… ___ ______,_________ ___ _ _
Thần kinh
Các phản ứng có hại về thẩn kinh có độc tính phụ thuộc liều lượng. Bệnh thẩn kinh ngoại biên chủ
yểu về cãm giác gặp ở 80—95% số bệnh nhân có đặc điểm lả loạn cảm giác vă/hoặc dị cãm ở các chi
có kèm hoặc không kèm oo rũt cơ, thường xây ra do nhiễm lạnh hoặc thay đổi nhiệt độ. Có thể do hư
hại chức năng như khó thực hiện các động tác tế nhị. Thời gian gặp các triệu chứng đó tãng lên với số
lẩn các chu kỳ diển uị. Các triệu chứng thường xuyên giăm giữa các chu kỳ diều trị
Nếu các tn'ệu chứng tốn tại hoặc phát triển đau hoặc hư hại chức năng thì cẩn giâm liểu hoặc ngừng
điếu trị (Xem mục “liều lượng vả cách dùng”)
Trong sử dụng hỗ trợ với liều tích luỹ lả 850mg/m2 (10 đợt), thấy nguy cơ gặp nhiều triệu chứng tổn
tại dai dẳng n 10%, còn với liều tích luỹ in 1020ng m² <12 đợt) thì nguy cơ lã 20%.
Trong giai đoạn tiến triển, trong EFC 2962 có 16% số bệnh nhân dùng Oxaliplatin + FU/FA gặp dị
cảm vã hư hại chức năng thẩn kinh kéo dãi hơn 2 mẫn, sau khi dùng liễu tích luỹ trung binh 874mg/
m². Có 2% phãi ngừng điểu trị do tồn tại dị câm (như tốn tại giữa các đợt điều trị) sau khi dùng các
liễu tích luỹ Oxaiiplatin 759-1100mg/ ml. Trong EFC 2961, có 13% số bệnh nhân gặp dị cảm và hư
hại chức năng thẩn kinh, sau khi khớì đẫu điểu uị trung bình 6 tháng hoặc sau khi dùng liều
Oxalipiatin tích luỹ trung bình 111 1 100ng m².
Trong phẩn lớn các trường hợp, các dấu hiệu và triệu chứng thẩn kinh sẽ câi thiện khi ngừng điểu trị.
Phân tích cãc bệnh nhân dùng EFC2962 cho thấy Oó 34 bệnh nhân có độc thẩn kinh độ 3 (là mức tối
đa của nghiên cứu nãy), 25 người (73, 5%) có cải thiện tn`ệu chứng tpqng thời gian trung bình lã
13 ,;Ztuẩn 8/34 bệnh nhân (23%) khỏi hẳn triệu chững. Độc tĩnh thẫn kinh kềo đải tru g bình ở độ 3 là
13 6 tuấn, liều tích luỹ trung bình của Oxaliplatin vảo lúc bắt đẩu lã 913mg/ \ og khoảng 169,7 -
1713,15mg/ m²) thời gian theo dõi trung bình với 34 bệnh nhân năy iả 55,71 tua .
Hội chứng loạn cãm giác hạ hẩu cấp tính gặp ở 1% - 2% số bệnh nhân thường xăy ra khi nhiễm lạnh
và thay đổi nhiệt độ. Đặc điểm cứa hội chứng nây lá các cãm giác chủ quan về khó nuốt và khó thở
mã không có chứng cứ về rối Ioạn hô hấp (giảm ô xy — máu, co thất thanh quãn, co thắt phế quãn).
Các biểu hiện khác về độc tỉnh cấp, cảm giác thẩn kinh có thể phát triển trong hoặc sau khi truyền
Oxaliplatin, bao gốm các triệu chứng liệt thẩn kinh vận nhãn (xụp mí mẩt hoặc nhìn đôi), rối loạn
điểu hoả động tác (dáng đi khác thườnglthẩt điệu/ phối hợp động tác không bình thường), rối loạn
phát âm (mất tiếng/khó phát âmlkhản giọng) và nói khó.
Huyết học : Hospira Australia Pty Ltd
ABN 58 097 064 330
Yoko Keng Teh
Director
/""`x
- Rất hay gặp: chãy máu cam, thiếu máu, (mọi mức độ) giãm bạch cẩu trung tính (mọi mức độ) giâm
tiểu cẩu (mọi mức độ) (điều tnị bổ trơ), thiểu máu (mọi mức độ), giâm bạch cẩu trung tính (mọi mức
độ), giảm tiểu cẩu (mọi mức độ ) (giai đoạn tiển triển). Trong điểu trị ung thư cả bổ trợ và ung thư Liến
triển, dùng thêm Oxaliplatin văo fluorouracil vã acid Folinic:
- Tăng rõ rệt tỷ lệ giãm bạch cẩu trung tính và giãm bạch trung tính nghiêm trọng (bạch cẩu trung tỉnh
<1,0x10°l1ft )vă
- Tăng rõ rệt tỷ lệ giảm tiểu cẩu (bãng 8-9)
Gan -Mật:
— Rất hay gặp: Tăng hoạt tính transaminase vả phosphatase kiêm (tiến triển)
- Rất hiểm các phản ứng liên quan tới hội chứng tấc nghẽn xoang gan, bao gổm ban xuất huyết, tăng
sản hạch tái sinh, xơ hóa quanh xoang và tăng ãp lực tĩnh mạch cửa (bổ trợ và tiển triển)
Cơ —Xương:
Hay gặp : đau lưng, đau khớp
Quá mẫn căm :
Trong các nghiên cứu lâm săng eó gặp quá mẫn cảm với Oxaliplatin (<1% mức độ %) các phản ứng dị
ứng năy có thể gây tử vong, tương ứng về tỉnh chất vã độ nghiêm trọng với các chế phẩm khác cũng
chứa-Elatin.-nhtLphátban.…mây…đay,-ban-đỏ..ngứa.văihiếmigặp.-co…thắt-phêlquânthạ…huyết-ãp.
Những phản ứng nã y thường được kiểm chế bằng adrenalin chuẩn và thuốc kháng histamin (xem mục
“cãnh báo về Các phân ứng phản vệ |giâ phản vệ).
Các giác quan :
- Rất hay gặp: rối loạn vị giác
- Hay gặp: viêm kết mạc
- Ít gặp: độc tính với tai
— Hiếm: điếc | viêm thẩn kinh thị giác, mất thị lưc
Tỉêu hóa:
- Rất hay gặp: tiêu chãy, buổn nôn, nôn , viêm miệng, chán ăn, đau bụng, viêm niêm mạc, táo bón,
(bổ trợ), tiêu chây, buổn nôn, nôn, viêm miệng, chán ăn, đau bụng, viêm niêm mạc, mất nước, tắc
ruột, giâm Kali -máu, nhiễm acid chuyển hóa, táo bón (tiến triển)
- Hay gặp: Khó tiêu (bổ trợ)
- Hiểm: Viêm đại trảng, bao gổm tiêu chảy do clostridium difficile (tiển tn'ển). Bổ sung Oxaliplatin
văo fluorouracil vã acid Folinic sẽ lãm tăng tỷ lệ buồn nôn, nôn, tiêu chảy và viêm miệng nghiêm
trọng trong sử dụng bổ trợ (xem bãng 8) vã lăm tãng rõ rệt các tác dụng phụ đó trong sử dụng chữa
ung thư tỉến triển (xem bảng 9)
Da:
- Rất hay gặp: rụng tóc, phát ban
~ Có gặp rụng tóc vừa phãi ở 2% số bệnh nhân sử dụng Oxaliplatin lăm đơn chất,f;Ễộ'i hợựOxaliplatin
với fiuoroura_cil không lăm tăng tỷ lệ rụng tóc như khi chỉ dùng riêng fiourouracihb \\/
Chú ý tại chõ tiêm tĩnh mạch:
- Trãn dịch ra ngoăi mạch có thể gây đau và viêm tại chỗ, có thể nghiêm trọng và gây biến chứng,
bao gỗm hoại tử. Phản ứng nơi tiêm, bao gỗm đỏ, sứng tâ`y vã đau.
Thận:
- Hay gặp: Huỷ hoại chửc nảng thận (tiến triển)
- Rất hiếm: Hoại tử ống thận (tiến triển). Trong theo dõi lâm săng và hậu mãi: bệnh thận, ống thận
kẽ, kéo theo bệnh thận cấp tính (Rất hiếm).
Hô hấp: _ _
- Hay gặp: Viêm mũi, khó thở (bổ ượ> HOSWa AUStfahỄ PĨ>’ UC
— Hiểm gặp: Bệnh phổi kẽ cấp tính, xơ hoá phổi ABN 58 097 0134 330
/WỮJV __
Yoko Keng Teh
Dìrector
Hệ miễn dịch:
- Rất hay gặp: nhiễm khuẩn, sốt
- Hay gặp: Sổt do giãm bạch cẩu trung tĩnh
- Hiếm gặp: Thiếu máu tan máu tự miễn vả giãm tiểu cẩu, sốt do giảm bạch cẩu trung tính ở <2% số
bệnh nhân.
— Bảng sau dây cung cẩp các hiện tượng có hại trong nghiên cứu (xem mục “nghiên cứu lâm săng“)
với tẩn số theo thứ tự giãm dẫn khi dùng Oxaliplatin và truyền FUIFA
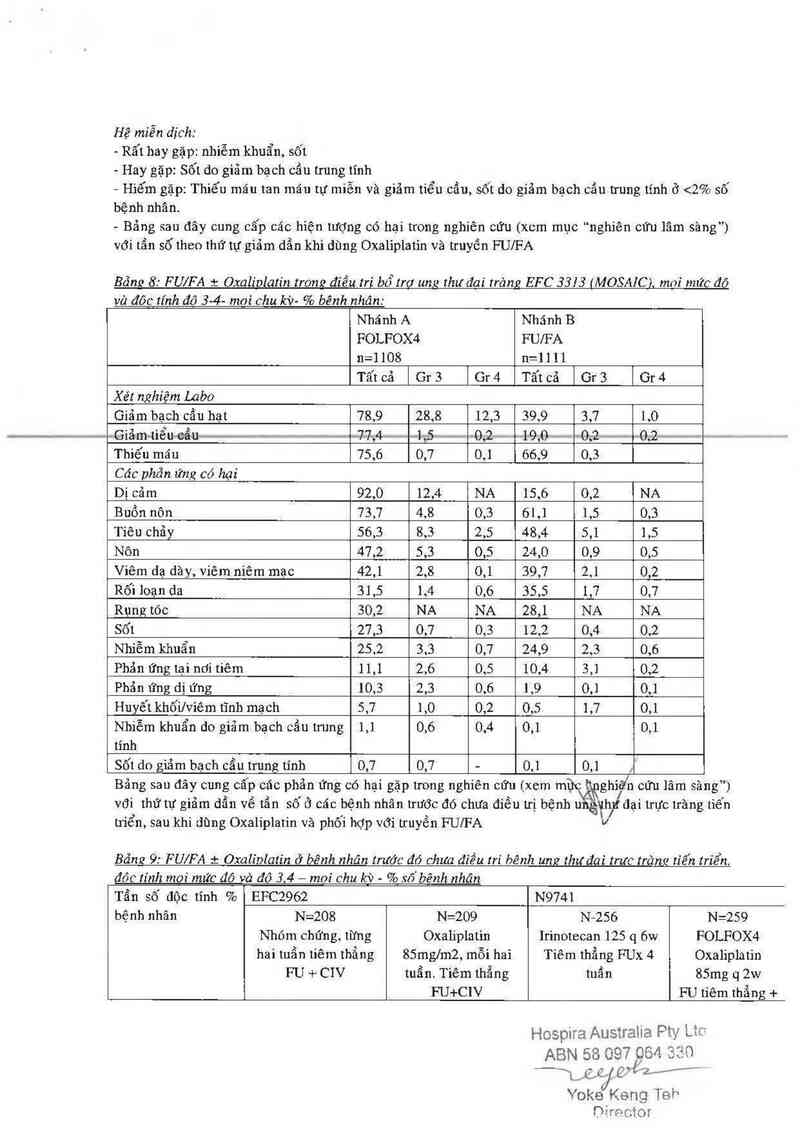
Bắnn 8: FU/FA t Oxaliolatin trom! đíểu trì bổtrơ ung thu' đai tròng EFC 3313 (MOSAICL moi mức đô
vả đôc tính đó 3-4- moi chu kx`J- % bênh nhân:
Nhấnh A Nhã nh B
FOLFOX4 FUJFA
n=1 108 n=l 1 l 1
Tấtcâ |Gr3 lGr4 Tấtcả lon 16…
Xét nghiệm Labo
Giảm bạch cẩu hạt 78,9 28,8 12,3 39,9 3,7 1,0
—Giả-m—tiểu—aẩu f —- 117,4 1,5—… …0,2… ~1~9,0… --o,aw —- -o,zwr
Thiểu mãn 75,6 0,7 0,1 66,9 0,3
Các phăn ứng có hại
Dị cảm 92,0 12,4 NA 15,6 0,2 NA
Buồn nôn 73,7 4,8 0,3 61,1 1,5 0,3
Tiêu chãy 56,3 8,3 2,5 48,4 5,1 1,5
Nôn 47,2 5,3 0,5 24,0 0,9 0,5
Viêm dạ dầy, viêm niêm mạc 42,1 2,8 0,1 39,7 2,1 0,2
Rối loạn da 31,5 1,4 0,6 35,5 1,7 0,7
Rụng tóc 30,2 NA NA 28,1 NA NA
Sốt 27,3 0,7 0,3 12,2 0,4 0,2
Nhiễm khuẩn 25,2 3,3 0,7 24,9 2,3 0,6
Phản ứng tại nơi tiêm 11,1 2,6 0,5 10,4 3,1 0,2
Phản ứng dị ứng 10,3 2,3 0,6 1,9 0,1 0,1
Huyết khối/viêm tĩnh mạch 5,7 1,0 0,2 0,5 1,7 0,1
Nhiễm khuẩn do giãm bạch cẩu tmng 1,1 0,6 0,4 0,1 0,1
tính
Sốt do gìảm bạch cẳu trung tinh 0, 7 0 ,7 - 0,1 0,1 ,
Bãng sau đây cung câp cảc phản ứng có hại gặp trong nghiên cứu (xem m
ùgẫẹghiên cứu lâm sâng”)
với thứtự giãm dẩn về tẩn sô ở các bệnh nhân trước đó chưa điểu trị bệnh ungầ\thjal đại trực trăng tìên
triển, sau khi dùng Oxaliplatin và phối hợp với truyền FU/FA
Bảmz 9: F U/FA i- Oxaliplatin ở bênh nhân trước đó chưa đỉểu m“ bênh une thư đai trưc trảnỵ tiển triển.
đỏc tính moi mức đô vả đó 3,4 — moi chu ki) - % sổ bẽnh nhân
Tẩn số độc tĩnh %
bệnh nhân
EFC2962 N9741
N=208 N=209 N-256 N=259
Nhóm chứng, từng Oxaliplatin Irinotecan 125 q 6w FOLFOX4
hai tuẩn tiêm thẳng 85mglm2, mỗi hai Tiêm thẳng FUx 4 Oxaliplatin
FU + CIV tuẩn. Tiêm thẵng tuần SSmg q 2w
FU+CIV
FU tiêm Ihẵng +
Hospira Austraiia Pty Lin
ABN 58 097 064 330
“lạc c ~ zf
Yoko Keng Teh
Dỉmcior
CIV
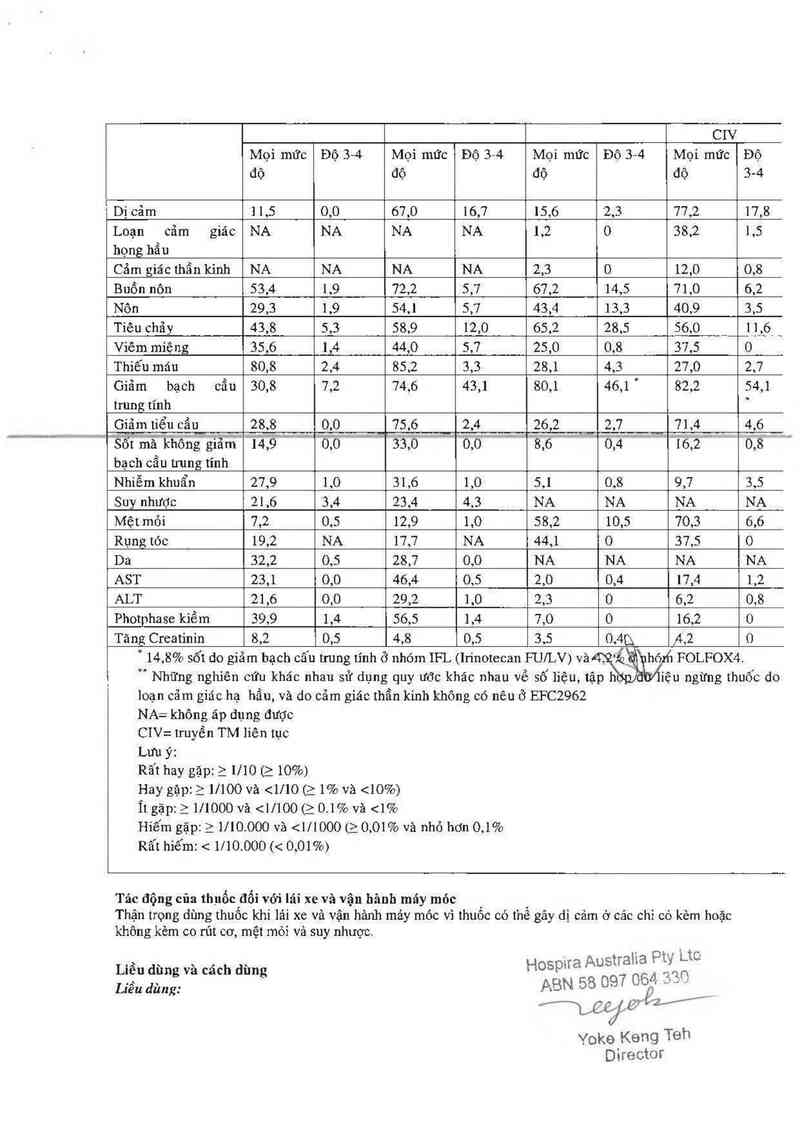
Mọi mức Độ 3-4 Mọi mức Độ 3-4 Mọi mức Độ 3-4 Mọi mức Độ
độ độ độ độ 34
Dị cãm ] 1,5 0,0 67,0 16,7 15,6 2,3 77,2 17,8
Loạn căm giác NA NA NA NA 1,2 0 38,2 1,5
họng hẩu
Cảm giác thẩn kinh NA NA NA NA 2,3 0 12,0 0,8
Buồn nôn 53,4 1,9 72,2 5,7 67,2 14,5 71,0 6,2
Nôn 29,3 1,9 54,1 5,7 43,4 13,3 40,9 3,5
Tiêu chãy 43,8 5,3 58,9 12,0 65,2 28,5 56,0 __ _1_1_,_6 _
Viêm miệng 35,6 1,4 44,0 5,7 25,0 0,8 37.5 0
Thiếu máu 80,8 2,4 85,2 3,3 28,1 4,3 27,0 2,7
Giâm bạch cẩu 30,8 7,2 74,6 43,1 80,1 46,1 ' 82,2 54,1
trung tính '
Giẳm tiểu cẩu 28,8 0,0 75,6 2,4 26,2 ' 2,7 71,4 4,6
Sốt mả khônguil'gỢiẵỉi— _14,9— _ ĨĨ) _ ___ "373,07- ' 70,0 7447778Ỉ6 _…….…. ẠOJ4'Ụ A 7" ỦÍỔỈZF _ ' 07,8
bạch cẩu trung tính
Nhiễm khuấn 27,9 1,0 31,6 1,0 5,1 0,8 9,7 3,5
Suy nhược 21,6 3,4 23,4 4,3 NA NA NA NA
Mệt mỏi 7,2 0.5 12,9 1,0 58,2 10,5 70,3 6,6
Rụng tóc 19,2 NA 17,7 NA 44,1 0 37,5 0
Da 32,2 0,5 28,7 0,0 NA NA NA NA
AST 23,1 0,0 46,4 0,5 2,0 0,4 l7,4 1,2
ALT 21,6 0,0 29,2 1,0 2,3 0 6,2 0,8
Photphase kìềm 39,9 1,4 56,5 1,4 7,0 0 16,2 0
Tăng Creatinin 8,2 0,5 4,8 [),5 3,5 0,4Q ,4,2 0
' 14.8% sốt do giảm bạch cấu trung tĩnh ở nhóm IFL (Irinotecan FU/LV) vả , 'Ấz ` hórh FOLFOX4.
" Những nghiên cứu khác nhau sử dụng quy ước khác nhau về số liệu, tậĨĨlỉpj iệu ngừng thuốc do
loạn cãm giác hạ hẩu, và do cảm giác thẫn kinh không có nêu ở EFC2962
NA= không áp dụng được
CIV= lruyến TM liên tục
Lưu ý:
Rất hay gặp:ặ 1/10(2 10%)
Hay gặp: 2 11100 vả <1/10 g>_1% vả <10%)
11 gặp: 2 111000 vả <1/1001z 0.1% vả <1%
Hiếm gặp: ì lIl0.000 vả <111000 (2 0,01% vả nhỏ hơn 0,1%
Rất hiếm: < 1/10.000 (< 0,01%)
Tác động cũa thuốcđối với lái xe và vận hânh máy móc _
Thận trọng dùng thuôo khi lải xe vả vận hảnh mảy móc vì thuôc có thẻ gây dị cảm ở cảc chi có kèm hoặc
không kèm co rút cơ, mệt mỏi vả suy nhuợc.
Hosọira Austraìia PW Ì-Ỉũ
ABN 58 007 064 330
fưcgff “V”
Yoke Keng Teh
Director
Liều dùng vả cách dùng
Liễu dùng:
Dùng kểt hợp với F1uorouracil vả acid Folinic, liều được khuyến cáo trong điểu trị ung thư đại trực
trảng tiển triển lả 85mglm², truyền tĩnh mạch trong 2—6 giờ, pha trong 250-500m1 dung dịch Glucose
5%, cử hai mẩn 1ễ truyền một lẩn.
Dùng kểt hợp với Fluorouracil vã acid Folinic, iiểu được khuyến cáo trong điểu tri bổ trợ 1ă 85mg/ m²,
truyền tĩnh mạch trong 2-6 giờ, pha trong 250-500m1 dung dịch Glucose 5%, cử hai tuẩn truyền một
lẩn, truyền 121ẩn (6 tháng).
Thay đổi liễu lượng
Trước mỗi lẩn tiêm truyền, bệnh nhân cẩn được đánh giá về độc tính của thuốc vã liều lượng của
Oxaliplatin sẽ được hiệu chỉnh tướng ứng.
Độc tính với thần kinh
Nếu xuất hiện những phân ứng cấp tĩnh về thẩn kinh, cụ thể là chứng loạn câm thanh quản-hẫu, thì
tăng thời gian tiêm truyền từ 2 giờ lên 8 giờ. Như vậy sẽ iăm giâm C.… được 30%, và 1ảm bớt đi độc
tính cấp.
Nếu hiện tượng mất cãm giác hay dị cãm vẫn tổn tại trên 7 ngảy, hoặc 1ăm rối loạn chức nãng (độc
tính cấp 2) thì giảm bớt 20% 1iểu dùng. Nếu hiện tượng mẩt cảm giác hay di cảm gây rối loạn cho
những hoạt động bình thường (độc tính cấp 3), thì ngừng dùng Oxaliplatin.
—Độcủwllthểưláư~ -———~ …— —~—~- ~——~—— — J—~—
Nêu có thể hiện độc tính với máu (bạch cẩu trung tính < 1 ,5x109/L hay tiểu cẩu < 75xl0glL) trước khi
bất đẩu điếu tn_ hoặc trước khi bắt đẩu một lẩn tiêm tiêp, thì:
- Hoãn điểu trị cho đển khi số đếm bạch cẩu trung tỉnh 21,5x109IL vả số đếm tiền cẩu 275x1091L vã
- Giảm liểu Oxaliplatin từ 85mgl m2 xuống còn 75mgl m2 hai tuần một lẩn vã liễu FU giâm 20%
(trong điều trị bổ trợ)
- Gỉãm liều Oxaliplatin từ 85mgl m2 xuống còn 65mg/ …2 hai tuẩn một lẩn vả liếư FU giãm 20%
(trong điều trị ung thư tiến triển)
Độc tính với dạ dảy — Ruột
Nếu xuất hiện những phân ứng về dạ dăy — ruột cẩp 3—4, đánh giá theo những tiêu chí của viện
ung thư quốc gia Mỹ:
- Hoãn điểu trị cho đến khi giải quyết xong những tăc dụng phụ vả
- Giâm liều Oxaliplatin m 85mgl m² xuống còn 75ng m² hai tuẩn một lẫn, vã liều FU giảm 20%
(trong điều trị ung thư tiển triển)
Độc tính liên quan đến F luorouracil:
Cẩn thực hiện hiệu chĩnh liểu theo những biểu hiện độc tinh của thuốc năy (xem “những thông tin
về loại thuốc nảy”)
Oxaliplatin cẩn được tiêm trước Fluorouracil
Oxah'platin được tiêm truyền tĩnh mạch trong 2 đển 6 giờ, pha trong 250 đến 500m1 dung dịch
glucose 5%
Cách pha chế vò cách tiêm
Một số điểu cẩn thận trọng khi tiêm:
— KHÔNG dùng bất kỳ dụng cụ tiêm nầo có bộ phận lảm bầng nhôm;
— KHÔNG dùng thuốc chưa pha loãng để tiêm;
— KHÔNG trộn lẫn, hoặc tiêm cùng với natri clorỉd, hoặc với bất kỳ một dung dịch năo chứa
clorỉd;
- KHÔNG trộn lẫn với một thuốc năo khác, hoặc tiêm đổng thời với thuốc khác theo cách đưa
thuốc đó văo cùng một dây truyền thuốc (đặc biệt với fiuorouracil vả acid Folinic). Có thể
dùng ống hình chữ Y (xem mục “tiêm truyền”); Hospira Australia Pty Ltd
ABN 58 097 064 330
”Ế
Yoke Keng Teh
Oỉrfacmr
(trong điểu trị bổ trợ) A /
- Giảm Iiềư Oxalìplatin từ 85mg/ m2 xuống còn 65mg/ …2 hai tuẩn một lẩn vã liểu cẦỷằỡiảm 20%
— CHỈ dùng những dung dịch pha loãng được đề nghị (xem đoạn dưới) những dung dịch sau khi
đã pha Ioãng có thể hiện rõ răng lả có kểt tủa thì không được dùng và phải đem huỷ bỏ.
Cách quăn lý
Như đối với những thuốc độc khác, cẩn phải cẩn thận khi thao tác và khi pha chế các dung dịch
Oxaliplatin
Công việc quản lý cãc thuốc độc với tế băo do các nhân viên y tế đòi hỏi phãi thực hiện nghiêm
chĩnh các điểu quy định, phải thận trọng để bảo vệ người quản lý trực tiếp và những người xung
quanh. Điều cẩn thiểt lã phải có quẩn áo bão vệ thích hợp, bao gổm kĩnh bão hộ, khẩu trang, găng
tay. Phụ nữ mang thai tránh không tiếp xúc với các chất độc với tế bảo. Nếu như dung dịch
Oxaliplatin đậm đặc chưa pha loãng, hoặc dung dịch đã pha loãng để tiêm truyền tiếp xúc vâo da,
vảo niêm mạc, vâo mắt, phãi rửa ngay và rửa kỹ với nước.
Cách pha chê'dung dich tiêm truyền
1) Tái tạo lại dung dịch:
Bột thuốc đông khô, được tái tạo thãnh dung dịch với một thể tích nước để tiêm hay dung dịch
glucose 5% để tiêm, cụ thể lả 4ml (đối với lọ 20mg) hay lOml (đối với lọ 50mg) hay 20m1 (đối với
lọ 100mg). Dung dịch tạo thảnh chứa 5mg Oxaliplatin cho 1 ml. Không tiêm dung dịch tái tạo nảy
mLchưa.phaJnăngạ.iệ A __ _ _ _______ _ủ Í ,
Về mặt hoá học vã vật lý học, dung dịch nây đã được chững minh lã on định vả dùng được trong
vòng 48 giờ, khi bão quân ở 2- 8"C vảơ ở30°C. Về mặt vi sinh vật học, thì dung dịch tái tạo phãi
được pha loãng ngay với dung dịch glucose 5% để Liêm. Nếu không pha loãng ngay, thì thời gian
bão quân và các điển kiện bảo quản trước khi sử dụng là trách nhiệm của người sử dụng, và bình
thường không để lâu quá 24 giờ ở nhiệt độ từ 2 đển 8“C
Việc tái tạo lại dung dịch phải được thực hiện trong những điều kiện vô khuẩn đã được kiểm tra
trước theo những tiêu chnẩn đã phê duyệt. Dung dịch cẩn được kiểm tra lại bằng mẩt thường trước
khi dùng. Chỉ những dung dịch trong suốt, không có các hạt lơ lững mới được dùng. Những lọ
thuốc Oxaliplatin để tiêm không chứa chất bão quãn, vả chi để dùng một lẩn. Dung dịch dùng còn
thừa phãi loại bỏ.
11) Việc pha loãng trứơc khi tiêm truyền:
Dung dịch tái tạo cẩn được pha loãng tiếp thânh 250-500m1 dung dịch để tiêm bầng dung dịch
glucose 5%. Trên quan điểm vi sinh học vã hóa học thì dung dịch để tiêm truyền cẩn được sử dụng
ngay và kiểm tra lại bẵng mẩt thường trước khi dùng. Chỉ đùng những dung dịch tron suốt, khộng
có các hoạt chất đục vẩn. Dung dịch chỉ để dùng một lẩn. Dung dịch còn thờa pỄ\ `›ỉi loại/bỏ.
KHÔNG bao giờ được dùng dung dịch natri clorỉd để tái tạo dung dịch, và để pha loăổun ldịch
đã tái tạo.
Việc tiêm truyền
Việc tiêm truyền Oxaliplatin không đòi hỏi phâi tiếp nước trước. Dung dịch Oxaliplatin pha loãng
trong 250 đến 500 ml dung dịch glucose 5% để tiêm có thể tiêm tryền vâo tĩnh mạch trung ương
hay tĩnh mạch ngoại vi trong thời gian 2 đển 6 giờ. Khi Oxaliplatin được điều trị cùng với
fluorouracil, thì phải tiêm truyền Oxaliplatin trước, tiêm truyền fluorouracil sau. Oxaliplatin có thể
tiêm đổng thời với acid Folinic, dùng một ống hình chữ Y (ống ba chạc), ống nảy đặt ngay trước
chỗ tiêm. Những thuốc nây không được trộn lẫn văo trong cùng một túi chứa. Acid Folinic phãi
được pha loãng bằng những dung dịch để tiêm truyền đẳng trương như dung dịch glucose 5%,
nhưng KHÔNG phải lã dung dịch natri clorỉd hay những dung dịch có tính kiểm. Sau khi tiêm xong
Oxaliplatin dội nước văo ống dẫn để rửa sạch.
Trong khi Oxaliplatin không có tính lăm rộp da, hay chi có tinh đó ở mức độ râ't ít thì hiện tượng
trăn dịch tiêm ở ngoãi tĩnh mạch có thể do đau và viêm tại chỗ. Điểu nầy lã nghiêm trọng và dẫn
đến nhiễu biến chứng, đặc biệt khi Oxaliplatin được tiêm truyền qua tĩnh mạch ngoại biên. Khi có
Hospira Austraiìa PW Ltd
ABN 58 097 064 330
Yoke Keng Teh
Direcior
hiện tượng thoát dịch tiêm ra ngoầi, phâi ngưng ngay việc tiêm truyền lại, vả tiến hânh ngay
những phép điểu trị tại chỗ thông thường đối với các triệu chứng.
Huỹ bỏ
Tất cả những vật liệu dùng vão việc tái tạo dung dịch, pha loãng dung dịch và tiêm dung dịch phãi
huỷ bỏ, đúng theo những quy định cũa địa phương.
Quá lỉễu
Không có thuốc giăi độc đặc biệt đối với Oxah'platin. Trong trường hợp dùng quá liểu, thì có thể
có hiện tượng các tác dụng không mong muốn nặng lên. Tiển hânh ngay việc theo dõi các thông
số về huyết học, và tiến hânh điểu trị các triệu chứng.
Trình bây
Oxaliplatin DBL® để tiêm trình bãy dưới dạng bột đông khô, để tiêm truyền, với liều 20mg, 50mg
vả 100mg một 1ọ.
Tiêu chuẩn: Nhã sản xuất
Bỏoquẻanổo-quẳa—đưới—âủ—
Hạn dùng : 36 tháng kể từ ngây sản xuất
Thuấc năy chỉ dzịmg theo đơn của thẩy thuốc
Đọc kỵ hướng dân sử dụng trước khi dùng. ` '
Nếu câu thêm thông tin xin hỏi ý kỉến của thây thuôc
/1
Để xa tẩm với của trẻ em - \ '
Thông bảo cho bác sĩ những tảc dụng không mong muốn gặp ph _i ùng thuôc.
Không dùng lhuổc quá hạn sử dụng. V
Tên và địa chỉ cơ sở chịu trách nhiệm
Hospira Australia Pty Ltd
1-5 7-23 and 25-39 Lexia Place MUL " ~ VE VIC 3170 Australia
pHÒ cục TRUỞNG
JKỹuấễn "ổn ỄễểanẨ
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng