














w…m —- *…
u….qe ợm:u
…
MỊ'buợ
smqez pazeoa ung
EGIZVIHLOUO1HJOHCIAH
/NV.LHVSEBUI
1audomv-OJ
… u nwlpu —caw
Co-ALVOPREL
IRBESARTAN/
HYDROCHLOROTHIAZIDE
film coated tablets
t'nch tablet contains
Actwe mg…dxent' lrnesanan 150 mg
Hyarochtmo:huarce 1? 5 mg
2 bllsterx1d latnats
Co-ALVOPREL
IRBESARTAN/
HYDROCHLOROTHIAZIDE
film coated tabtets
lnd caltcr ›;onlllưtdư'ìtllủr ›snga and umnr …1z ura1 un
sen nncme -oaM' nm: d~recled try nt'yszmm
Hoad nstructror Àeattet camtmly beỉcu'o Jso
Kuep o.Jl u'1huroach ot cMmsn
Stmu tzehrw JC*”
L›ag N \…
"`1ệw"Ullllly' QA ger
\ Meruleuumd Ly Gmmu~aưr -…— A
ta… từ ……r—m-u Mẹ…ư
1ấ'tU Pnll n ỉẫruu'
Inu…
“1xJỗuLl Luc un
ễ___
\ t
."
QJJ
28'ta'tlilfe’ts
J®
Rthnúc u am
Dụchýlmwơả›nìruụlnmhth
Ĩ ĩch CO~ALVOPREL
ì T…phb …venmnmưứndm
Im-un… '.SOthyúưbrdhhdd uan.
mu…umnnenheuưmdima
eủuwmócờmwtnoamao'c
E)Lulârnuỵntenu
su»…mu OnneptunnSA. …uọ
NMohhkhùt ..
sóon v…oootxx
~.nsx nom usx: ttĐmmfỵy uonơ«…w
cuamn. cm chi qm cm: n…g vi dc
thbngttnlhk ……msnmm
uỏnu
%…
J ặ__
\0 :
muẫ ;
10 _-~-
ogă 1 ' \
U zỉẵ *
`. 1 | PMS425C
lrbesarì-an HC“
erram1õíìmgj2 F~rm_1
28 TABS ()AR'U
134x69x27mm
RC 05/07/2012
dg 17/02/2014
1 2
\ ARTDBOO1SSGC
l PMS 116 C
PMS 158 C
PMS 165 C
Dle—Cut
ÍHERAPEUĨ
C—09 Base Cardìovascular
system
FCìRM ICON
J
004A - Oval biconvex tablet
BRAlLLEffv1€ìbergfv1ufflutĩl Cu…
NIA APAC
REGUI ATĨJRY APPROVAL
COPVRIGF 1TS «' CONTACT
ĩms avlwnll and 11; cantnnt Is ccpynghl ot Almgen
QAtvnqm 201? AI nghi: russmn.
Any Aruhmpơnen digilulty … hnvdcouy yeơnslntwllon
ntlemaz~zm … runmduchun ol uml 0: «I nl lhu umtov—ts M
my Ionn ís pmhlhutođ by onur IM… Amaan stntt IM
cempeny usnuu
Muln conllch
Dawn Garua. Art… Diectm
dum gmub@Almgun mm
quungen
Jó/ơfJ
.~ w .,
uu u.: ' 4 `
……“
,W
còus TY
mwwEW” …"
JUch PìịllỈ-«xìl
\VlcT PHẢP,N
V 'xè—
~ ìèạaz-qA.tẹgý
__ , : ,
lrbesartan HCTViatnam 150mg_125mg
28 T.ABS FOIL
126x64mm
DG 101111201²
13/0212014
02
ARTDBOOT9SBF
PRt NT COLOURS
SUPPORT COLOURS (NO PRINTJ
Die-Cut
REGULATORY APPROVAL
MOCK-IJP
COPYRIGHTS i CONTACT
Ĩhns lllWle nnd Ils conlanl is cupylqu of Alvogen
:zAtmgen 2012. All ragan reuơved
Any Anthmpmdst dignnllv or nardcopy redi:lnuulion.
lltvnlâlủùh nv leoraductiun oí uan … nll ní lhe eonLenls …
lny lot… Is pmnihnteơ by nther !hnn Alvugun statt Im
comna ny ucage.
Mlin contact:
n…… nam…. An…t Dlvu mm Q
davnd uarcta@Almgen com AỈVCIgEH
AỗG/9Lf
Thuốc bán theo đơn!
Đọc kỹ hưởng dân sử dụng trước khi dùng
Néu cân thêm lhông tin xỉn hói ý kiên bác sỹ
C O-ALVOPREL
Irbesartan 150 mg/ Hydroclorothỉazid 12,5 mg - Viên nén bao phỉm
THÀNH PHẦN:
Mỗi viên nén bao phim chứa:
Hoạt chất: 150 mg lrbesartan và 12,5 mg Hydroclorothiazid (HCT).
Tá dược:
T á dược lõi: 76 mg Microcrystailin cellulose, 10 mg Pregelatỉnized Starch, 26mg Lactose
monohydrat, 10 mg Poloxamer 188; 11 mg Natri Croscarmellose; 4,5 mg Magnesi stearat, Nước
tinh khiết vừa đủ.
Tá dược bao: 7,8 mg Hypromellose 6cP; 1,774 mg Titan dioxyd; 1,2 mg Stearic acid, 1,2 mg
Microcrystallỉn cellulose; 0,014mg Oxyd sắt đen; 0,012mg Oxyd sẳt đó; Nước tinh khiết vừa đù.
DƯỢC LỰC HỌC
Nhóm tác dụng duơc lý: Cảc thuốc đối kháng thụ thể angiotensin- l-I dạng kểt hợp.
lt'bCSãt'tũft/HCT là kết họp của một chất đối kháng của thụ thế angiotensin- -II, irbesaưan, và một
thuốc lọi tiếu thỉazìd, hydroclorothiazìd. Sự kết hợp cùa các hoạt chất nảy có tác dụng hạ huyết áp
cộng hợp, lảm giảm huyết ảp mạnh hơn so với từng thảnh phần đơn độc.
Irbesartan lả một chất đối kháng của thụ thể angỉotensỉn II chọn lọc mạnh, dùng đường uống.
lrbesartan được dự kiến chận tất cả các tác động qua trung gian angiotensìn 11 bởi thụ thể AT] bất
kể nguồn gốc hoặc con đưòng tống hợp của angỉotensin 11. Đối khảng chọn lọc thụ thể cùa
angìotensin- l-I (ATI) dẫn đến gia tăng nông độ renin và nông độ angiotensin II, và sự giảm nồng độ
aldosteron trong huyết thanh. Nồng độ kali huyết thanh không bị ảnh hưởng đáng kế bởi irbesartan
đơn độc ở mủc lỉếu khuyến cảo ở nhũng bệnh nhân không có nguy cơ mất cân bằng đỉện gìải.
Irbesartan không ức chế ACE (kinỉnase- -II), một enzym tạo ra angiotensin— —II và cũng giảng hóa
bradykinin thảnh chất chuyến hóa không hoạt động. Irbesartan không cân kích hoạt thảnh các chất
chuyến hóa cho hoạt động của nó
Hydroclorothỉazid tả một thuốc lợi tiếu thỉazid. Cơ chế chống tãng huyết áp cùa thuốc lợi tiếu
thiazid không được biết đầy đủ. Cảo thiazỉd ảnh hưởng đến cơ chế tái hấp thu các chất điện giải tại
ống thận, lảm gia tăng trực tiếp sự thải trừ natri và clorid vởì lượng gần tương đương. Tảo động của
hydroclorothỉazid Iảm giảm thể tích huyết tương, gỉa tăng hoạt hóa các renin huyết tuơng, tăng sự
bảì tiết aldosteron, với hậu quả là tăng kali nước tiếu và mất bicarbonat, Iảm giảm kali huyêt tương.
Thông qua sự phong tỏa hệ renin—angiotensin- -aldosteron, sử dụng đồng thời ỉrbesartan có xu hướng
dẫn tởỉ phuc hồi sự mất kali liên quan đến thuốc lợi tiếu hydroclorothỉazid Khi dùng
hydroclorothiazid, tảc dụng lợi tiếu xuất hiện sau 2 gìờ, vả tác dụng đạt đinh trong khoảng 4 gìờ,
tiong khi tảc dụng kéo dải trong khoảng 6- 12 giờ.
Sụ kết hợp hydroclorothỉazid vả irbesartan tăng thêm tác dụng lảm giảm huyết' ap liên quan đến liều
trong khoảng lìều điếu trị cùa chúng. Kết hợp 12, 5 mg hydroclorothỉazid vảo 300 mg irbesartan một
lẩn/ngảy cho nhũng bệnh nhân không được kỉểm soát đầy đủ với 300 mg ìrbesartan đơn độc lảm
giảm hơn nữa huyêt ảp tâm truơng đảy (24 giờ sau khi dùng thuốc) so với gìả duợc là 6,1 mmHg.
Sự kết hợp 300 mg irbesartan và 12, 5 mg hydroclorothỉazìd lảm gỉảm toản bộ huyết ảp tâm thu/tâm
nương tới 13, 6/11, 5 mmHg so vởỉ gìả dược.
Số lỉệu hạn chế (7 trong số 22 bệnh nhân) gợi ý rằng nhũng bệnh nhân không kiếm soát đuợc với kết
hỌp 300 mg/12, 5 mg có thể đáp ứng khi tăng liếu tới 300 mg/2S mg. Ở những bệnh nhân nảy, ảnh
W
hưởng hạ huyết ảp gỉa tăng đuợc quan sảt cá ở huyết ảp tâm thu (SBP) và huyết ảp tâm trương
(DBP) (tuơng úng 151 13, 3 và 8, 3 mmHg).
Liều dùng môi 1ầnfngảy với 150 mg irbesartan và 12, 5 mg hydrociorothiazid Iảm giảm huyết' ap tâm
thuftâm truơng trung binh ở mủc đảy (24 giờ sau khi dùng) 12 ,,91'6 9 mmi [g so với gỉả duợc ở bệnh
nhản tảng huyết ảp nhẹ và trung bình. 1-Iiệu quả nảy đạt đinh trong 3-6 giờ. Khi dảnh gìả hiệu quả
thông qua việc theo dõi huyết áp lỉên tục 24 giờ, vỉệ-c kết hợp 150 mg ỉrbesartan và ]2,5 mg
hydrociorothiazỉd một lần/ngảy duy trì tảo dụng giảm huyết áp suốt 24 gỉờ với việc giảm huyết ảp
tâm thu/tâm trương 24 giờ so với gỉả dược là 15,8/ 10,0 mmHg. Khi theo dõi huyết áp liên tục ngoại
trú, thì hiệu quả đảy/đinh của Irbesartan/HCT 150 ng12,5 mg là 100%. Hiệu suất đảy/đỉnh đo được
là 68% cho irbesartanx hydrociorothiazid 150 mg/l2, 5 mg và 76% cho IrbeseutaanCT 300 mg/12, 5
mg. Tảc dụng lên huyết’ ap trong 24 giờ nảy đuợc quan sảt lhấy mã không kèm theo sự hạ huyết ảp
dinh quả mủc, đồng thời hạ huyết ap một cảch an toản và hiệu quả ở khoảng nghỉ giũa cảc iiều
Ở nhũng bệnh nhân không kiếm soát đẩy đủ với liếu 25 mg hydroclorothiazid đơn độc, sủ đụng
thếm i1besartan lảm giảm thếm huyết ap tâm thultãm truơng so với giả dưọc lrung bình là 11,1/7,2
mmHg
Tảo dụng hạ huyết áp của irbesartan khi kết hợp với hydrơciorothiazid xuất hiện sau liếu đẩu tiến và
rõ rệt sau 1-2 tuần, với tác dung tối đa xuất hiện sau 6- 8 tuần Trong cảc nghỉến cứu dải hạn, tảc
dụng cùa Irbesartan/HCT đuợc duy trì trong hơn 1 năm Mặc dù không có nghiên cứu đặc biệt với
Irbesartan/HCT , hiện tượng huyết ảp dội ngược không được quan sát thấy ở irbesartan hoặc
hydroclorothiazìđ.
Ảnh hướng kết hợp cùa irbesartan vả hydrociorothiazid trên tỷ lệ thương tật và tử vong không được
nghiến cúu. Những nghiên cúu dịch tễ học chỉ ra rằng điều trị kéo dải với hydroclorothiazid lảm
gỉảm tỷ lệ măc cảc bệnh tim mạch Và tử vong
Không có sụ khảo bỉệt trong đảp ứng với lrbesa1tanli —,1CT về tuổi tảo vả giới tinh. Cũng như cảc sản
phẩm thuốc khảo ảnh huờng đến hệ renin- angiotensin, nhũng bộnh nhân lả. người da đen bị cao
huyết áp không có đảp úng đảng kể với điếu trị irbesartan đơn độc. Khi irbesartan đuợc dùng đồng
lhời với mộti iêu thấp hydroci orothỉazid (ví dụ 12, 5 mg mỗi ngảy), đáp ứng hạ huyết ảp ở nhũng
bệnh nhân lả nguời đa đen tu ơng tự như bệnh nhân không phải nguời da đen.
Tính hiệu quả và an toản của Irbesartan/l-ICT trong đ iếu trị khởi đầu cho tăng huyết ảp nghiêm trọng
[đuợc định nghĩa lả SeDBP > 110 mmlig) đuợc đánh gỉả trong một nghỉên cứu song song đa trung
tâm, ngẫu nhiên, mù đôi, có kiểm soát trong 8 tuần Tồng sô 697 bệnh nhân được chọn ngẫu nhiên
theo tỷ Iệ 2: 1 hoặc lả1rbesartaanCT 150 mg/l2, 5 mg hoặc itbesartan 150 mg và bắt buộc tăng ìiếu
có hệ thống (truớc khỉ đảnh giá dảp ủng với múc Iỉếu thắp hơn) Sau 1 tuần lương ủng iả
libesai'tan/HCT 300 mgi'2S mg hoặc ỉibesartan 300 mg
Nghiên cún tuyến chọn 585 là nam giới, trung bình là 52,5 tuổi, 13% trong số đó là tử 65 tuối tlở
lên, vả chỉ có 2% là từ 75 tuổi trở lên. Muời hai phần trăm ( 12%) lả bệnh nhân tiếu đường, 34% tăng
lipid máu và tình trạng tim mạch phố bỉến nhất là đau thắt ngục ổn định ở 3, 5% số nguời tham dự
Mục tiếu chủ yếu của nghiến cửu lả so sảnh tỷ 1ệ bệnh nhân có SeDBP được kiếm soát (SeDBP < 90
iang) ở tuần thủ 5 cúa đỉếu trị 47, 2% bệnh nhân cũa kết hợp đạt đuợc múc đảy SeDBP < 90
1111an so với 33, 2% bệnh nhân dùng ỉrbesartan (p= 0 ,0005). Huyết ảp cơ bản trung binh khoảng
172/1 13 mmllg trong mỗi nhóm điều tli_ và giảm SeSBP/SeDBP tại 5 tuần điều trị là 30, 8/24 ,0
mmlig cho lrbesartan/IICT vả 21,1119,3 mthg cho irbcsartan (p < 0,0001).
Cảc loại vả tỷ lệ của cảc tảo dụng không mong muốn cho bệnh nhân điếu trị vởi kết hợp là tương tự
về hồ sơ tảo dụng không mong muốn cho bệnh nhân khi đỉếu trị đơn độc. Trong khoảng thời gỉan 8
tuần điếu trị, không có trường hợp nảo bị ngất xiu đuợc bảo cảo ở cảc nhóm điếu trị Có 0 6% và 0%
bệnh nhân hạ huyết ảp vả 2, 8% vả 3,1% bệnh nhân chóng mặt lá cảc phản úng bất lợi đuợc báo oảo
tuơng ùng ở nhóm kết hợp và nhóm đơn trị liệu.
DƯỢC ĐỘNG HỌC
Kết hợp hydroclorothiazỉd vả ilbesartan khộng ảnh huớng đến duợc động học của cả hai thảnh phần
Irbesartan vả hydroclorothiazid lả cảc thuốc sử dụng đuờng uống và không yêu cẳu chuyến dạng
sinh học cho cảc hoạt dộng cùa chủng Sau khi sử dụng đuờng uông Irbesartan/HCT, sinh khả dụng
tuyệt đối đường uống cùa irbesartan là 60- 80% và 50- 80% hydroclorothiazid. Thúc ăn không ảnh
huởng đến sinh khả dụng cùa IRBESARTAN/HCT Nồng độ đinh trong huyết tuơng xuất hiện ở
1 ,-5 2 gỉờ sau khi uống cho irbesartan và 1- 2, 5 giờ cho hydroclorothiazid
Liên kết với protein huyết tương irbesattan khoảng 96%, liên kết không đáng kể với cảc thảnh phần
của tế bảo máu. Thể tích phân bố của irbesartan là 53-93 lít. Hydrociorothỉazid có 68% liên kết với
protein huyết tương, vả thể tích phân bố biếu kiến lả 0,83-1,14 l/kg.
Dược động học của Irbesattan tuyến tính và tỉ lệ với lỉếu trong khoảng từ 10 đến 600 mg. Sự hấp thu
thuốc đường uống tãng lên với tỉ lệ thấp hơn ở mửc iiều lớn hơn 600 mg đã được quan sảt; cơ chế
cho điếu nảy vẫn chưa được bỉết. Dò thanh thải toản phần vả thận tương ửng 1ả 157-176 vả 3,0-3,5
mlfphút. Thời gian bán thải cuối cùng cùa irbcsartan là 11-15 giờ. Nồng độ thuốc trong huyết tướng
ổn định đạt dược trong 3 ngảy sau khi bắt đẩu điểu trị một lẩnfngảy.
Tích 1ũy cùa irbcsartan (< 20%) được quan sát trong huyết tương khỉ lặp iại iiếu một lẩnfflgảy.
Trong một nghiến cứu, nồng độ hơi cao hơn của ìrbesatan được quan sảt ở bệnh nhân nữ cao huyết
ap.
Tuy nhiến, không có sự khảo biệt trong thời gian bản thải và sự tích lũy irbesartan. Không cẩn điếu
chinh iiếu ờ bệnh nhân nữ. Diện tich dưới đường cong cùa (AUC) irbesartan vả gỉả trị Cmax cũng hơi
tãng ở những đối tượng cao tuối (ì 65 tuồi) so với những đỗi tượng trẻ hơn (18-40 tuồỉ). Tuy nhiên
thời gỉan bán thải cuối cùng không biến đổi đảng kề. Không cần thiết phải điếu chỉnh liếm ở những
bệnh nhân cao tuối. Thời gian bản thải trong huyết thanh của hydroclorothiazỉd được báo cảo trong
khoảng 5- 15 gìờ
Sau khi uống hoặc tiêm tĩnh mạch 4C irbesattan, 80- 85% dạng phóng xạ luu hảnh trong huyết
tuong được là dạng không đối của hbesartan Irbesartan đuọc chuyển hóa qua,, Oan thông qua dạng
Iiên hợp với g1ucuronid vả dạng oxy hóa. Dạng chuyến hóa 1uu hảnh chinh lả ìrbesartan glucmonid
(khoảng 6%). Cảo nghiến cúu in vỉtro chi ra răng i1besartan đuợc oxy hóa chủ yếu bởi cytochrom
P450 enzym CYP2C9; isoenzym CYP3A4 có ảnh huởng không đảng kế
Irbesattan vả chất chuyến hóa cùa nó đuợc thải trừ theo cả con đuòng qua thận và mật Sau khi ưống
hoặc tỉếm tĩnh mạch 4C ỉrbesaztan, khoảng 20% dạng phóng xạ đuợc tìm thấy trong nuớc tiếu, vả
phần còn lại trong phân Duới 2% liều dùng đuợc bảỉ tiết duới dạng không đối ilbcsartan
Hydroclorothỉazid không được chuyến hóa nhưng thải trừ nhanh chóng bởi thận. Ít nhất 61% liều
dùng được bải tiết dưới dạng không đối trong vòng 24 gĩờ. Hydroclorothiazid qua nhau thai nhưng
không qua được hảng rảo máu - não, vả được bải tiết trong sữa mẹ.
Suy Ihận
Ở những bệnh nhân suy thận hoặc trải qua lọc máu, các thông số dược động học của irbesantan
không thay đồi đáng kế. 1rbesartan không đuợc loại bỏ bởi lọc máu. Ở nhũng bệnh nhân có độ thanh
thải cx cat1nm < 20 ml/phùt, thòi gian bản thải cùa hydroclorothiazĩd đuợc bảo Cảo tãng lên đến 21
giờ.
Suy gan
O nhũng bếnh nhân xơ gan nhẹ đến trung bình, cảc thông số duợc động học của ỉrbesartan không
biến đối một cảch có ý nghĩa Các nghiên cúu không đuợc thuc hiện trên nhũng bếnh nhân suy gan
nặng.
CHỈ ĐỊNH
Điếu tiỊ chúng tăng huyết ảp vô cănl tăng áp nguyên phảt ở nguời truởng thảnh mã không có đảp
ứng đầy đủ với irbesartan hoặc hydroclmothỉazid đơn độc.
Jìiì/f
CHỐNG CHỈ ĐỊNH
- Mẫn cảm với dược chất hoặc bất cứ tả dược nảo của thuốc, hoặc các dẫn chất của suifonamỉd khảo
(hydroclorothiazid là một dẫn chất của sulfonamỉd).
- Giai đoạn thứ hai vả thứ ba cùa thai kỳ vả phụ nữ đang cho con bủ.
- Suy thận nặng (độ thanh thải creatinin < 30 ml/phủt).
- Hạ kali huyết kéo dải, chứng tăng canxi huyết.
- Suy gan nặng, xơ gan mật, ứ mật.
- Chứng vô niệu.
- Sử dụng đồng thòi Co- -A1voprcl với cảc thuốc chúa aliskiren đuợc chống chỉ dịnh ở nhũng bệnh
nhân măc đái thảo đuờng hoặc suy thận (mức lọc cầu thận (GFR) < 60 ml/phut/ 1 ,73 m ².)
LIÊU LƯỢNG VÀ CÁCH DÙNG
Liều lượng:
[rbcsartan/HCT có thể dùng hảng ngảy kèm hoặc không kèm Vởi thức ăn.
Điếu chỉnh liều dối vởì từng thảnh phẩn của thuốc (Irbesartan hoặc HCT) có thế được khuyên dùng.
Việc thay đổi từ liệu pháp đơn trị lỉệư sang liệu pháp phối hợp có thế được cân nhắc khi thích hợp
trên lâm sảng:
- IrbesaztaanCT 150 mg/12, 5 mg đuợc dùng cho nhũng bệnh nhân khi huyết áp không được kỉếm
soát đấy đủ với hydroclotothiazid hoặc irbesattan 150 mg don độc.
Liều cao hơn 300 mg irbesartan/ZS mg hydroclorothiazid dùng một 1ần/ngảy không đuợc khuyến
cáo.
Khi cần thiết, Irbesartan/HCT có thế được dùng với các thuốc chống tăng ảp khác.
Nhũng bênh nhân đăc biêt:
Suy Ỉhật-L
Vì có thảnh phần hydtociorothiazid nên 11bcszutan/IICT không đuợc khuyến cảo cho nhũng bệnh
nhân suy thận nghiêm trọng (độ thanh thải creatinin < 30 mifphút). Thuốc lợi tiếu quai nên dùng hơn
lá là thìazid trong nhóm đối tuợng nảy Không cần thiết đỉếu chỉnh liồu ở bệnh nhân suy thận có độ
thanh thải creatinin thận ì 30 mlfphút.
Suy gan.
Irbesartan/HCT không đuợc chỉ định cho nhũng bệnh nhân suy gan nặng Các thiazid phải được sử
clung thận trọng ở nhũng bệnh nhân suy chúc năng gan. Không cân thiết điều chinh lỉều của
iibesaltan/HCT ở nhũng bộnh nhãn suy gan nhẹ tới trưng bình.
Nguờí cqo !uổi.
Khon g cần thiết diếu chỉnh ]iếu của Irbcsaưan/HCT ở bệnh nhân cao tuồi.
Nhóm bệnh nhi:
Irbesartan/l-ICT không được khuyến cáo sử dụng cho trẻ cm vả thanh thiếu niên bởi vi tinh an toản
và hiệu quả vẫn chưa được thiết lập. Không có sẵn dữ lìệu.
Cách dùng:
Dùng đường uống.
CÀNH BÁO VÀ THẬN TRỌNG
Bệnh nhân hạ huỵết áp- giám thể tích nội mạch
hbesmtan/HCT hiếm khi 1ìên quan đến hạ huyết ảp có triệu chúng ở nhũng bệnh nhân tăng huyết’ ap
mã không có cảc yếu tố nguy cơ khảo cùa hạ huyết áp. Hạ huyết ap có triệu chủng có thể đuợc dụ
đoản xuất hiện ở nhủng bệnh nhân giảm thế tich vả/hoặc natri bới điều t1ị thuốc lợi tiểu mạnh, chế
độ ăn kiếng muối, tiếu chảy hoặc nôn Nhũng tinh trạng nảy cần đuợc điếu chỉnh tlước khi bắt đầu
điều t1ị với hbcsattanli ICT.
/iỵ/ilièx
Hẹp động mạch thận — tãng huyết áp mạch thân.
Có sự gia tăng nguy cơ của hạ huyết ap nghỉõm trọng và suy thận khi những bệnh nhân bị hẹp động
mạch thận hai bên hoặc hẹp động mạch thận một bên duợc đỉều trị với thuốc uc chế cnzym chuyển
dạng angiotcnsỉn hoặc cảc chắt đối khảng thụ thể angioten5in 11. Trong khi đây không phải là tải liệu
dẫn chứng với Irbesartan/HCT, ảnh hưởng tương tự nến được dự đoán.
Suy thận và cấy ghép thận
Khi irbesartan/HCT được sử dụng ở những bệnh nhân suy thặn, khuyến cảo theo dõi định kỳ nồng
độ kali, creatinin vả acid uric huyết thanh.
Không có kinh nghiệm liến quan đến việc sử dụng IrbesartaanCT ở những bệnh nhân mới cẳy ghép
thận, Irbesartan/HCT không được sử dụng ở những bệnh nhân suy thận nặng (độ thanh thải creatinin
< 30mllphủt). Chứng nitơ huyết iiên quan đến thuốc lợi tiểu có thể xuất hiện ở những bệnh nhân suy
thận. Không cần thiết dỉều chĩnh liếu ở những bệnh nhân suy thận có độ thanh thải creatinin 2 30
mlfphút. Tuy nhiên, ở những bệnh nhân suy thận nhẹ tới trung bình [độ thanh thải creatinin 2 30
ml/phút nhưng < 60 mi/phút) kết hợp liếu cố dịnh nảy cần được sử dụng thận trỌng.
Ức chế kép hệ Renin-anigotensin—aldoslrone(RAAS) :
Có bằng chứng cho thấy sử dụng đồng thời các chất ức chế ACE, thuốc L'rc chế thụ thể angỉotcnsin LL
hoặc aliskircn lảm tăng nguy cơ hạ huyết ảp, tăng kaii mảu, và suy giảm chúc năng thận (bao gồm
suy thận cắp). Không khuyến cáo sử dụng kết hợp với thuốc L'Lc chế ACE thuốc ức chế thụ thể
angiotcnsin II hoặc aliskiren để gãy ức chế kép hệ RAAS. Nếu liệu phảp L'L~c chế phức hợp hệ RAAS
lả thưc su cần thiết thì phải được thục hìện bởi bảo sỹ chuyên khoa và phải theo dõi thuờng xuyến
chủc năng thận, điện giải và huyết ảp. Không nên sử dụng đỗng thời các chẳt uc chế ACE vả thuốc
L'LL: chế thu thế angiotensin II ở cảc bệnh nhân đải thảo dường.
SuyÒ oan
Thiazid cần được sử dụng thận trợng ở nhũng bộnh nhân suy gan hoặc bệnh gan tiến triến, từ nhũng
biển đối nhỏ cùa cân bằng đỉện giải và dịch thế có thể dẫn dến hôn mê gan` Không có kinh nghệm
lâm sảng với Irbesattan/HCT ờ bệnh nhân suy gan
Hẹp van hai lá và van động mạch chủ, bệnh cơ lim phì đại tắc nghẽn
Cũng như với các thuốc giãn mạch khảo, đặc biệt thận trọng đối với ra ở nhũng bệnh nhân bị hẹp
van hai lá hoặc van động mạch chù, hoặc bệnh cơ tim phì dại tắc nghẽn.
Chứng tăng nldosteron nguyên phát
Bệnh nhân bị tăng aiđostemn nguyên phảt thuờng không đáp úng với các thuốc chống tăng huyết ảp
hoạt động thông qua ức chế hệ renin — angiotensin Do đó, không khuyến cảo sủ dụng
ltbcsartaanCT
Ảnh Imõng trên chuyển hóa và nội tỉết
Điếu trị với thiazid có thế 1ảm giảm dưng nạp g1ucose. Ở bệnh nhãn tiếu đường điếu chinh liếư
ỉnsulìn hoặc cảc thuốc hạ đuờng huyết đuờng Uông có thế đuợc yếu cầu. Bệnh tiểu đuờng tiếm ẩn có
thế được biểu hiện trong khi điếu trị thuốc lợi tỉếLL thiazid. Su gỉa tãng nồng độ cholesterol vả
tLiglycerid có 1iên quan tới điếu trị thuốc lợi tỉếu thiazỉd; tuy nhỉến ở múc liếu 12, 5 mg tLong
Irbcsattan/HCT, ảnh huớng nhỏ hoặc không đảng kế được báo cáo. Tăng acid uric huyết có thể xuất
hiện hoặc bệnh gout có thế dược biểu hiện ở những bệnh nhân được điếu trị với thiazid.
Mất cân bằng điện giăi
Nhu bất cứ bệnh nhân điếu trị với thuốc 1ợi tiếu thíazid, xác định định kỳ điện giải trong hưyết thanh
phải được thục hiện ở cảc khoảng thời gian thich hợp. Cảc thiaziđ, bao gồm hydroclorothiazid, có
thể gây ra mất cân bằng điện giải hoặc dịch thế (hạ kali huyết, hạ natri huyết, vả hạ cio huyết, nhiễm
kiếm chưyến hóa) Dẫu hìệu cảnh bảo của mất cân bằng điện giải hoặc dịch thế lả khô miệng, khảt,
tinh trạng yêu đuối, hôn mê, uể oái, bỗn chồn, dau cơ hoặci chuột rút, mòi cơ bắp, hạ huyết ảp, thiếu
LLiệLL, mạch nhanh, và Lối loạn tiêu hóa như buồn nôn nôn.
Mặc du hạ kali mảu có thể tăng cùng vói sủ dụng thuốc lợi tiếu thiazid, điều trị đồng thời với
iL~besartan có thế giảm lợi tiếu gây ra hạ kaiỉ máu. Nguy cơ cùa hạ kali mảu là lớn nhất ở nhũng bệnh
nhân bị xơ gan, ở những bệnh nhân có kinh nghiệm lợi tiểu nhanh, ở những bệnh nhân không nhận
được đầy đủ cảc chẳt điện giải qua đường uống và ở những bệnh nhân được điếu trị đồng thời với
corticosteroid hoặc ACTH. Ngược lại, do irbcsartan lả thảnh phần của Irbesartan/HCT, tăng kali
huyết có thể xuất hiện, đặc biệt bệnh nhân bị sưy thận vả/hoặc suy tim, và tiếu đường.
Khuyến cáo giám sảt đẩy đủ kali huyết thanh ở những bệnh nhân có nguy cơ. Thuốc iợi tiếu giữ
kali, chẳt bổ sung kali hoặc muôi thay thế có chứa kali cần đuợc kết hợp thận trọng với
1rbcsaưaanCT.
Không có bằng chứng irbesartan sẽ lảm giâm hoặc ngăn ngừa thuốc lợi tỉễu gây ra hạ natri huyết.
Thiếu hụt clorid thường là nhẹ và không cần điếu trị.
Các thiazid có thế lảm giảm sự bải tiết calci niệu và gây ra sự tăng nhẹ vả giản đoạn của calci huyết
thanh trong trướng hợp không có các rối loạn của sự chuyến hóa calci được biết đến Dấu hiệu tăng
calci mảu có thể là bằng chúng của cường cận giáp tiếm ân. Cảo thiazid phải đuợc ngừng truớc khi
thuc hiện kiếm tin chúc năng tuyến cận giảp
Cảo thiazid đã chỉ ra sự tăng bảỉ tiết magnesi qua nuớc tiếu, có thể dẫn đến giảm magnesi huyết
Litlư'
Sự kết hợp của 1ithỉ vả Irbcsartan/HCT không được khuyến cảo.
Kỉểm ỉra chổng doping
Hydroclorothiazid có trong sản phầm thuốc nây có thế tạo ra phân tich dương tính trong kiếm tra
chống doping
Cảnh báo chung
Ó nhũng bệnh nhân trương lưc mạch mảu vả chúc năng thận phụ thuộc chủ yếu vảo hoạt động của
hế1enin-angiotcnsin aidosteron (ví dụ như suy tim sung huyết nghiếm tL~Ọng hoặc bệnh thận tiếm ắn,
bao gồm hẹp động mạch thận), điếu trị với cảc chất’ ưc chế enzym chuyến dạng angỉotensin hoặc các
chẩt đối kháng thụ thể angiotensin- -11 mà ảnh huớng cùa hê nảy lỉõn quan đến hạ huyết ảp cấp tính,
hội chúng nìtơ huyết, thiếu niệu, hoặc hỉếm khi suy thận cắp Như đối vởi bắt kỳ thuốc chống tăng
huyết ảp nảo, sự giảm huyết ảp quả muc ở nhũng bệnh nhân bị bệnh tim thiếu rnảu cục bộ có thể
dẫn đến nhồi mảu cơ tim hoặc đột quỵ.
Phản ứng quá mẫn với hydroclorothiazid có thể xuất hiện ở những bệnh nhân có hoặc không có tiến
sử dị ứng hoặc hen phế quản, nhưng có nhìều khả năng ở những bệnh nhân có tiến sử như vậy. Sự
trầm trọng hoặc kích hoạt của bệnh lupus ban đỏ toản thân đã được bảo cáo với việc sử dụng thuốc
lợi tiếu thiazid.
Nhung trường hợp phản úng nhạy cảm với ảnh sáng đã đuợc bảo cáo với các thuốc lợi tiếu thiazid.
Nếu các phản ưng nhạy cảm với ảnh sáng xuất hiện trong khi điều trị, khuyến cảo ngùng đỉếu trị.
Nếu tải sủ dụng thuốc lợi tiếu đuợc đảnh giả là cẩn thiết, nó đuợc khuyến cảo để bảo vệ khỏi tiểp
xúc vói vùng có ánh sảng hoặc với UVA nhân tạo.
Mang thai
Chất đối kháng thụ thể angiotensin II (AIIRAS) không được sư dụng trong khi mang thai. Trừ khi
điều trị với AIIRA được xem xét lả cần thiết, bệnh nhân có kế hoạch mang thai cần được thay dối
thuốc điếu trị tăng huyết ảp khảo mã đã được thiết lập hồ sơ an toản cho thai kỳ. Khi được chẩn
đoản mang thai, điếu trị với AIIRA phải được ngừng ngay lập tửc, và nếu thích hợp, thay đổi liệu
pháp khảc nên được bắt đẫu.
Lactose
Sản phẳm thuốc nảy chứa lactose. Bệnh nhân có cảc vấn đề dung nạp galactose di truyền hiếm gặp,
sụ thiếu hut laotase Lapp hoặc kém hắp thu glucosc-galactosc không nên sư dụng sản phẩm thuốc
nảy
Glõcôm góc đóng cấp lmh thủ cấp hoặc cận Ihị cấp tmh
Các thuốc sưlfonòamid hoặc các dẫn xuất của sullomamid có thể gây ra phản ủng đặc úng, dẫn đến
cận thị thoáng qua và glôcôm góc đóng cấp tính. Trong khi hydroclorothiazid 1ả một sulfornamid,
trường hợp chỉ dược phân lập cùa glôcôm góc đóng cẩp tinh được bảo cảo xa hơn với
m®
—/i
hydrochoirothiazid Cảc triệu chung baor gồm khới phảt cắp tĩnh cùa suy giảm độ nét của thị iục
hoặc đau măt vả đặc biệt xuất hiện trong vải giờ đến vải tuần sau khi bắt dầu sư dụng thuốc.
Không điếu trị glôcôm góc đóng câp tính có thể dẫn đến mù vĩnh viễn. Điếu trị chủ yếu là ngừng
dùng thuốc cảng nhanh cảng tốt. Điếu trị dùng thuốc hoặc phẫu thuật nhanh chóng có thế cần được
xem xét nếu nhãn ảp vẫn không kiếm soát được. Cảo yếu tố nguy cơ cho sự phảt triến cùa giôcôm
góc đóng có thế bao gồm tiến sử dị ứng với sulfonamid hoặc penicillin.
LÚC cớ THAI VÀ NUÔI CON BÚ
Lúc co' thai
Cảc chất đối kháng thụ thể angiotensin JJ (AJJRA).
Không khưyến cáo sử đụng cảc AHRA trong quý Icùa thai kỳ. Chống chỉ định sử dụng các AIIRA
trong quý II và 111 cùa thai kỳ.
Nhưng bằng chưng dịch tễ học về nguy cơ gây quải thai sau khi phơi nhiễm với cảc chẩt L'Lc chế
ACE trong quý I cùa thai kỳ không đuợc kểt luận; tuy nhiên một sự gia tăng nhỏ tLong ngưy co
không thế được ioại trù Trong khi không có dữ Iiệu dịch tễ kiểm soát nguy cơ cùa cảc chất đối
kháng angiotcnsin II (AIIRA), những nguy cơ Luong tự có thể tồn tại cho nhũng thuốc cũa nhóm
nảy Ngoại trừ tiếp tục điếu trị với A11RA đuợc coi là cần thiết, bệnh nhân có kế hoạch mang thai
cần được điều trị với thuốc chống tăng huyết’ ap khác mà đã đuợc thiết lập hồ sơ an toản cho sử
đụng trong thai kỳ Khi mang thai được chẩn đoán, dĩếu trị với AIIRA cần được ngừng ngay lặp tức,
vả, nếu thích hợp, liệu phảp thay đổi nên được bắt đằu.
Phơi nhiễm với điếu nị AIIRA trong quý II và 111 cùa thai kỳ được biết là gây quải thai ở người
Lgiảm chúc năng JthậLL, thiếu ối, chậm hỏa xuơng hộp sọ) và độc tính ở trẻ sơ sinh (sưy thận, hạ huyết
áp, tăng kali máu) Nếu phoi nhiễm với AIIRA xảy ra từ quý II của thai kỳ, khuyến cảo siêu âm
kiếm tra chúc năng ti 1ận và hộp sọ T rè sơ sinh có mẹ sủ dụng AIIRA cần đuợc theo dõi hạ huyết ap
chặt chẽ.
Hydroclorothiazz'd
Kinh nghiệm sử dụng hydroclorothiazid trong thai kỳ là hạn chế, đặc biệt trong quý I cùa thai kỳ.
Nhũng nghiên cúu ở động vật iả không dầy dù. Hydroclomthiazid đi qua nhau thai Dụa trên nhũng
cơ chế dược ly cua hoạt động của hydrociorothiazid việc sư dụng nó trong quý II và 111 cua thai kỳ
có thế iảm tốn thương thai nhi và trẻ sơ sinh nhưv vảng đa, rôi ioạn cân bằng điện giải vả giảm tỉếu
cầu. Hydrocimothiazid đuợc sư dụng khi bị phủ trong lhai kỳ, cao huyết áp nong thai k ỳ, và tiền
sản giật do giảm thể tích huyết tương và giảm tưới mảu qua nhau thai, không có ảnh hương có lợi
nảo trên tiến trinh của bệnh. Hydroclorothiazid không nên sử dụng cho tăng huyết ảp vô căn ở phụ
nữ mang thai ngoại trừ những tình hưống hiếm gặp, khi không thể điều trị với nảo thuốc khảo.
Vi lrbcsartan/HCT chứa hydrociorothiazid, không được khuyến cảo sử dụng trong quý I cúa thai kỳ.
Chuyến san g điếu trị một ioại thuốc phù hợp nến được thực hiện trước khi có kế hoạch man g thai.
Lúc cho con bú
Các thuốc đồi kháng ĩhụ Lhể angiotensz'n JJ (AJJRAS).
Chống chỉ định dùng IL~besartan trong thòi kỳ cho con bú. Thay đồi điếu trị với cảc thuốc dã được
thiết iập hồ sơ an toản trong khi cho con bú 1ả lưa chọn tốt hơn, đặc biệt trong khi cho trẻ sơ sinh
hoặc trẻ sinh non bL'L.
Không đuợc biết ỉrbesartan và các chất chuyến hóa cùa nó có đuợc bả] tiết qua sữa mẹ hay không
Nhũng đủ Iìệu sẵn có về duợc động học/độc tính ở chuột đã chỉ ra sụ bải tiết cùa irbesartan vả cảc
chẳt chuyến hóa cùa nó trong sua.
Hydrocloroihiazid
Hydroclorothiazid đuợc bải tiết trọng sữa mẹ ở một 1uợng nhỏ. Các thiazid ở mửc iiều cao gây ra sự
lợi tiến mạnh có thế' uc chế sự tiết sưa
Su dụng iLbesartaanCf trong thòi gian cho con bu không dược khuyến cáo Nếu phải dung
lrbcsartan/i ICT trong giai đoạn nảy, liếu dùng nên gỉũ ở mức thắp nhắt có thế
WỪ/
n/I
Khả nãng sinh sản
lrbcsartan không có ảnh hưởng đên khả năng sỉnh sản khi đĩêu trị trên chuột và thế hệ con cải cùa nó
vói mức lỉêu nhỏ hơn liêu gây ra những dâu hiệu đâu tiên của độc tính trên bô mẹ.
DỮ LIỆU AN TOÀN TIÊN LÂM SÀNG
eresartan/HCT
Khả năng gắy dộc tính cùa kết hợp Irbesartanli-ICT sau khi dùng đường uống đã dược dảnh giả trên
chnột và khi trong cảc nghiên cửu kéo dải đến 6 thảng. Không có nhũng phát hiện độc tính được
quan sảt liên quan đến việc sử dụng điếu trị ở người.
Sau khi thay đồi, quan sảt được ở chuột vả khi dùng tổ hợp lrbcsartan/HCT ờ ]0/10 và 90/90
mglkg/ngảy, cũng đã thấy L trong 2 thuốc dùng dơn độc và hoặc là thứ phát để gìảm huyết ảp
(không có tương tác gây độc có ý nghĩa đu ợc quan sảt thấy).
- Những thay đổi ở thận, đặc trưng như sự tăng nhẹ urc huyết thanh vả creatinin, và tăng sản/phỉ của
cơ quan cận quản cẩu, là kết quả trục tiếp cùa tương tác giưa irbesartan và hệ renin- angiotensin.
- Sự Lãng nhẹ cảc thông số cua hồng câu (hồng cãu hacmogiobin, hematocrít)
- Đổi mảu dạ dảy, loét vả hoại tư khu trú niêm mạc được quan sảt thấy ở một số chuột khi đùng
tLong 6 Lháng trong cảc nghiên cứu về độc t1nh cùa iL~bcsartan 90 LTLg/kg/ngảy, hydroclorothiazid 90
mg/kg/ngảy, vả Irbesartan/HCT 10/10 mg/kg/ngảy. Những thương tốn nảy không được quan sảL ở
khi.
- Giảm kali huyết thanh do hydroclorothỉazỉd vả chỉ giảm ít với hydroclorothìazid được kết hợp với
ỉrbesaưan.
Phần lởn các tác dụng được đồ cặp ở trên là do hoạt động được lý cùa ỉL~besartan (chẹn sự ức chế tư
angiotensỉn II do giải phóng Lenin, vởi sự kLch thích cùa các tế bảo sinh renin) và cũng thẳy xuất
hiện khi dùng cảc thuốc úc chế mcn chuyến dạng angiotcnsỉn. Nhưng phảt hỉện nảy xuất hiện không
lĩên quan đến Sư dụng liếu điếu tri cua Irbesartan/HCT ơ nguời.
Không có tảo động sinh quải thai ở chuột khi đùng iLbesartan vả hydroclorothiazỉd kết hợp với Iiếu
có thề sỉnh ra độc tinh ở mẹ. Những tảc động của kết hợp Irbcsartan/HCT trên khả năng sinh sản
không được đảnh giá trong những nghiên cứu ở động vật, do đó không có bằng chứng về tảo dụng
không mong muốn Lrên khả năng sinh sản ở động vật hoặc con người với irbcsaưan hoặc
hydmclorothỉazid khi dùng đơn độc.
Tuy nhỉên, ảnh hưởng cùa các chất đối khảng angiotensin khảo trên cảc thông số về khả năng sỉnh
sản tLong cảc nghỉên cúu ở động vật khi sử dụng đơn độc. Nhưng phảt hĩện nảy cũng đuợc quan sát
thất với mức iiều thẳp cùa cảc chẩt dối kháng thụ thể angiotcnsìn II khi sử dụng kết hợp vởi
hydroclorothỉazid.
Không có bằng chửng về sự đột biến gen hoặc sự tách nhiễm sẳc thế khi sử dụng kết hợp
Irbesartanl'HCT. Khả năng gây ung thư của ìrbesartan vả hydroclorothiazid kết hợp cũng không
được đánh gỉá Lrong các nghỉên cứu ở động vật.
Irbesarian ` _ `
Không có băng chứng cùa sự bât thường về độc tính hệ thống hoặc cơ quan đích vởi mức liều dùng
trẽn lâm sảng. Trong cảc nghiên cửu an toản tiến lâm sảng, liều cao của irbesartan (> 250
mg/kg/ngảy ở chuột và _>_ 100 mg/kg/ngảy ở khỉ) gây ra sự giảm các thông số tế bảo mảu (hồng cẩu,
haemoglobin, hacmatocrỉt). Ở mức iỉêu Lât cao (> 500 mg/kg/ngảy) gây ra các thoái biến ơ thận ( như
viêm thận kẽ, giãn ông thận, kỉếm hóa do óng thận, tăng nông độ Lch vả creatinin huyết) đuợc Lăng
cuờng bởi' LL~bcsartan ở chuột vả khỉ vả được xem như là thứ phảt từ tác dụng hạ huyết ảp của thuốc
lẳLLLL giảm sự tưởi mảu thặn.
Hơn nũa, iL~besartan còn gây ra sự tăng sản/phì đại cùa các tế bảo cận thận (ở chuột Với lỉếu > 90
mg/kg/ngay, ở khi với lỉếu > 10 mg/kg/ngảy). Tắt cả các thay đối nảy được xcrn như iả do Lác động
được lý của irbesartan. Vởi liếLL điều trị của iL~besartan ở người, sự tăng sản/phì dại ở các tế bảo cận
thận không xuất hiện với múc có líên quan nảo.
Lh)’
Không có bằng chứng về tinh sinh đột biến gen, khả năng tảch nhiễm sẳc thế hoặc khả nănggây ung
thu'.
Khả nặng sinh tinh và sinh sản không bị ảnh hưởng trong các nghìên cưu ở chuột đực vả chuột cải ở
liều LLông cua irbesartan gậy ra một sô độc tinh cùa cha mẹ (tư 50 đển 650 mglkgfngây),b ao gồm tỷ
lệ chết ở muc iiếu cao nhắt Không có tác dụng dảng kế trên số lượng thế vảng, cây ghép, hoặc thai
nhi đã được quan sảt. Irbcsartan không tác dụng đến khả năng sông sót, phảt trỉển, sinh sản cùa thế
hệ con cái.
Những nghỉên cứu trên động Vật chi ra các đồng vị dược đánh dắu cùa iL~bcsartan được phảt hỉện
Lrong phôi chuột vả thỏ.
h~besartan được bải tiết trong sữa cùa chuột.
Những nghiên cưu vởi irbesartan đã chi ra tác dụng độc tính thoản g qua (tăng sự tạo lỗ xương chậu
Lhận, l niệu quản Ú' nước, phù dưới da) ở bảo thai chuột, phục hồi sau khi sinh. Ớ thó, sự hẩp thu cùa
hoặc tái hấp thu sớm được chú ý ở liếu gây ra độc tính đảng kể ở mẹ, bao gồm cả tử vong. Không có
tảo dụng sinh quái thai được quan sảt ở chuột và thỏ.
Hydmcloroihìazz'đ
Mặc dù có cảc bằng chứng không chắc chắn về khả năng gây ra độc tính quái thai hoặc khả năng
gây ung thư được tan thấy trong một số cảc mô hình thử nghiệm, sự suy rộng ra ở người với
hydrociorothiazid lá không đúng khi chi ra sự liên quan giữa việc sử dụng hydroclorothiazỉd và sự
gỉa tăng cảc khối LL.
ẢNH HƯỞNG TRÊN KHẢ NĂNG LÁI XE vÀ VẶN HÀNH MÁY MÓC
Không có nghiên cứu ảnh hưỏng trên khả năng lảỉ xe và vận hảnh máy móc được thực hiện.
Dụa lL~ên nhũng đặc tính dược dộng học, IrbesartaanCl khó có ảnh huởng đễn khả năng nảy. Khỉ
iái xe hoặc vận hảnh mảy móc, có thể kể đến đôi khi chóng mặt hoặc mệt mòi có thể xuất hiện trong
khi đỉều trị chống tăng huyết ap.
TƯO'NG TÁC THUỐC
Các tlzuốc chỗng ỉăng huyết áp khác
Tảo dụng hạ huyết áp cùa lrbcsartan/HCT có thế được gia tăng với vỉệc sử dụng kết hợp của cảc
thưốc chống tăng hưyết ảp khác Irbesartan vả hyđroclorothiazỉd (ở mức liều lến đến 300 mg
ỉLbesaitan/ZS mg hydeoc]moLhiazỉd) đã được sư đụng an toản với các thuốc chống tăng huyết áp
khảo bao gồm thuốc chẹn kên calci và thuốc chẹn beta— adrenergic. Điều tLL truớc với thuốc ìợi tiêu
liều cao có thể dẫn đến mắt thế Lích nội mạch và nguy cơ hạ huyết áp khi bắt đầu điếu trị với
iL~besartan kèm hoặc không kèm các thuốc lợi tỉếu thiazid trừ khi tỉnh trạng mất thể tích được đìếu
chinh trước.
Các lhuốc chứa aliskiren hoặc các chất ức chế ACE
Cảo dũ iiệư lâm sảng cho thấy sụ ức chế kép hệ renin- angìotensỉn-aidosteron (RAAS) do sử dụng
kết hợp chắt uc chế ACE, thuốc’ ưc chế thụ thể angiotcnsin II hoặc alỉskiren Iiên quan đến việc tăng
tần suất gặp cảc tảo dụng phụ như tụt huyết ảp, tăng kali máu, suy gìảm chức năng thận (bao gôm
sưy thận cẳp) với tần suất cao hơn so với sử dụng đơn độc thuốc tảo dụng lên hệ RAAS.
Lithí
Sự gia tăng có phục hồi nồng độ lithi trong huyết thanh và độc tính được bảo các trong khi sư dụng
dồng thời lithi vởỉ cảc chất ức chế enzym chuyền dạng angiotensin II. Ảnh hưởng tương tư rất hiếm
khi dược bảo cảo vởỉ irbesartan cho đến nay Hơn nũ~,a độ thanh thải thận cùa lìthi giảm bởi các
Lhiazid vì vậy, nguy cơ của độc tính lithi có thể tăng với Irbcsartan/HCT. Do đó, kết hợp lỉthi vả
hbesartan/HC T không được khuyến cáo Nếu sự kết hợp chưng minh sự cần thiết, khuyến cảo theo
dõi cẩn thận nồng độ lỉthỉ trong huyết thanh.
)fLL’L/
Những săn pltấm thuốc ănh hưởng đến kali
Ảnh hưởng mắt kali cùa hydrociorothiazid bị suy giảm bởi tảo dụng giữ kali của irbesartan. Tuy
nhiên, ảnh hưởng nảy cùa hydroclorothiazid trên kali huyết thanh được dự đoán có khả năng bởi các
sản phấm thuốc khảo liên quan đến sự mất kali và giảm kali huyết (cảc thuốc lợi tiếu thải kali, thuốc
nhuận trảng, amphotericin, carbenoxolon, penicillin G natri). Nguợc lại, dựa trên kinh nghiệm sử
dụng cảc sản phấm thuốc khảo lảm suy yếu hệ renin — angiotensỉn, sử dụng đồng thời sử dụng cảc
thuốc lợi tỉếu giữ kali, bổ sung kali, muối thay thể chứa kaii hoặc các sản phẩm thuốc khảc có thể
dẫn đến tăng nông độ kali huyết thanh (ví dụ heparin natri) có thể dẫn đến Lãng kali huyết thanh. Sự
theo dõi đầy đủ cùa nồng độ kali huyết thanh ở những bệnh nhân có nguy cơ được khuyến cảo.
Những sản phẫm thuốc ãnh lzuỡng bởi sư rối loạn kali huyết thanh
Theo dõi định kỳ kali huyết thanh được khuyến cảo khi Irbesartan/HCT được sử dụng vởi những sản
phâm thuốc ảnh hưởng bởi sự rối loạn kali huyết thanh (ví dụ glycosid tim, thuốc chống loạn nhịp).
Thuốc chống viêm không sleroỉd
Khi sư dụng thuốc đối khảng angiotensin 11 đồng thời với cảc thuốc chống viêm không steroid (ví
dụ thuốc kim hãm chọn lọc COX- 2, acid acetylsalicyiic (> 3 g/ngảy) vả cảc NSAID không chọn
lọc), sự suy giảm tác dụng chống tăng huyết’ ap có thể xuất hiện
Với tảc dụng kìm hãm ACE, sử dụng đồng thời cảc thuốc đối khảng thụ thể angiotensin II vả cảc
NSAID có thể dẫn đến gia tăng nguy cơ sự xấu đi của chúc năng thận, có thế bao gồm suy thận cấp,
và sự gỉa tăng kali huyết thanh, đặc biệt ở những bệnh nhân bị yếu chức năng thận từ trước. Sự kết
hợp cân được sư dụng thận trọng, đặc biệt ở người cao tuổi. Bệnh nhân nên được bù nước đầy đủ và
cân nhắc theo dõi chức năng thận sau khi bắt đầu điều trị đồng thời, và đinh kỳ sau đó.
Thông tin bổ sung cho tương tác thuốc của irbesartan
Trong các thử nghiệm lâm sảng, dược lực học của irbesartan không bị ảnh hưởng bởi
hydroclorothiazid. Irbesartan được chuyến hóa chủ yếu bởi CYP2C9 và đến một mức dộ thấp hơn
gluconic. Không có tương tảo dược lực học hoặc dược động học có ý nghĩa quan sát được khi
irbesartan được sử dụng đồng thời với warfarin, một thuốc được chuyến hóa bời CYP2C9. Những
ảnh hưởng của thuốc gây cảm ửng như rifampicin trên dược lực học cùa irbesartan không được đảnh
giả. Dược lực học của digoxin không thay đổi bởi sủ dụng đồng thời vởi irbesartan.
Thông tin bổ sung cho tương tác của hydroclorothiazỉd
Khi sử dụng đồng thời, nhũng sản phẫm thuốc sau có thế tương tảc với thuốc lợi tiếu thiazid:
Alcohol
Khả năng hạ huyết ap tư thế có thể xuất hiện
Thuốc hạ đường huyết (thuốc đường uống và insulin)
Điều chinh liều của các thuốc hạ đường huyết có thế đuợc yêu cầu.
C holestyramin vả nhựa colestipol
Sự hấp thu của hydroclorothiazid bị suy yếu trong sự có mặt của nhựa trao đổi anion.
Irbesaưan/HCT cần được dùng ít nhất một giờ trước hoặc bốn giờ sau khi dùng cảc thuốc nảy.
Corticosteroids, A C TH
Mất cảc chất điện giải, đặc biệt là hạ kali có thế gỉa tăng.
Glycosid tím
Thiazid gây cảm ứng hạ kali huyết hoặc hạ magnesi huyết lảm Lãng sự khởi đầu sự Lối loạn nhịp tim
do glycosid tim gây ra.
Các lhuốc chống viêm khóng steroid
Sử dụng cảc thuốc chống viêm không steroid có thế lảm giảm sự lợi tỉếu, sự bâi tiết natri qua nuớc
tiếu và ảnh hưởng hạ huyết ap cúa các thuốc lợi tỉểu thìazỉd ở một vải bệnh nhân.
Các amin lảm tăng huyêt ảp (ví dụ: noradrenalin)
Ảnh hưởng cua các amin lảm tăng huyết’ ap có thể được lảm gỉảm, nhưng không đủ để loại bỏ tảo
dụng của chúng
W
Thuốc giãn cơ khóng khử cực ( ví dụ như tubocurarin)
Hydrociorothỉazid có thế 1ảm tăng tảc đụng cùa thuốc giãn cơ không khử cực.
Thuốc điều trị goth
Diều chỉnh liếu của cảc sản phấm thưốc đỉếu trị gcưt có thể cần thiết như hydrociorothiazid có thể
lảm tăng nồng độ cúa acid LLric huyết thanh. Sự gỉa tãng trong lỉếu dùng cùa probenecid hoặc
suli'mpyrazon có thế là cần thiết. Sử dụng đồng thời cảc thuốc lợi tiếu thiaziđ có thể dẫn đến tăng sự
tảc động của cảc phản ửng quá mẫn với ailopurinol.
Muối calci
Các thưốc lợi tiếu Lhiazid có thế gia tăng nồng độ calci huyết thanh do 1ảm giảm sự bải tiết. Nếu bổ
sung calci hoặc dùng cảc sản phẩm thuốc giữ calci (ví dụ điếu trị với vilamin D) phải được kê dơn,
nồng độ caici trong huyết thanh phải được theo dõi và điếu chỉnh Iiếu calci theo nó.
Carbamazepz'n
Sử dụng đồng thòi carbamachin vả hydrociorothiazid liên quan tới nguy cơ hạ natri có triệu chứng.
Cảo chẳt điện gỉải cần dược theo dõi trong quả trinh sử dụng kết hợp. Nếu có thế sử dụng thay thế
bằng cảc thuốc lợi tiếu khảo.
Các tưong tác khác
Ảnh huởng tăng đưòng huyết cua cảc thuốc chẹn bcta vả diazoxid có thế được tăng cuờng bởi
thiazỉd. Các thuốc đối khảng choiinergic (ví đụ atropin, bepriden) có thề lảm tăng sỉth khả dụng của
cảc thuốc lọi tiểu loại thiazid bởi sự giảm như động ruột và tỷ lệ rỗng của đạ dảy. Cảo thiazid có thể
gia Lăng nguy cơ cảc tảo dụng không mong muôn gây ra bởi amantadin. Các thiazid có thế 1ảm giảm
sụ bải tiết qua thận của các thuốc ung thu (ví dụ; cyciophosphamid, mcthotrexat) và tăng khả năng
L'Lc chế tuy của chúng.
TẢC DỤNG KLLÔNG MONG MUÔN
Sự kết lrọp Itbesartan/HC T
TLong sô 898 bệnh nhân cao huyết’ ap đã điếu trị vởi cảc liếu khác nhau cùa IrbesartaanCT (trcng
khoảng: 37,5 mg/6, 25 mg dến 300 mg/2S mg) trong cảc thử nhiệm đối chứng vởi giả dược, 29, 5%
sô bộnh nhận xưẳt hiện cảc phản ứng bất lợi. Cảo ADR được bảo cảo phổ biến nhất là chóng mặt
(5,6 Jo), một mòi (4,9%), buồn nôn/nôn (1,8%), và tiếu tỉện bất thường (1,4%). T hêrn vảo đó, sự gia
tăng nitro urc mảu (BUN) (2,3%), creatinin kinase (1,7%) và creatinin (1,1%) cũng được quan sát
trong cảc thử nghỉệm lâm sảng.
Bảng 1 đưa ra cảc phản ửng bắt 1ợi được quan sát từ bảo các phát sinh và trong cảc thử nghiệm với
giả dược có kiếm soát
Nhũng phản ửng bẩt lợi được lỉệt kê được định nghĩa bằng cách sử dụng cảc quy ước dưới đãy: Rất
phổ biến (2 1/10), Phổ biến (2 1f100 to < 1110), Không phố bỉến (ì 1/1.000 to < 1/100), Hĩễrn (2
]/10.000 to < lll .000), Rất hiếm (< 1710.000),K116ng rõ (không thể ước lượng tù' dữ liệu sẵn có).
Trong mỗi nhóm tẩn suất, những tảc dụng không mong muốn được iiệt kê theo trật tự giảm dần mức
dộ nghiêm trọng.
Bãng ]. Những phản ửng bất iợi trong các thử nghiệm với giả dược có kiểm soát và các bảo cảo
thường xuyến
Các hệ cơ quan ] Tần suất Tác dụng không mong muốn
Xót nghiệm Phò biên Gia tăng nitro urc (BUN), creatinin vả
creatinin kinasc huyêt
Không phô biên Giảm kaii và natri huyết
Rối loạn tim Không phổ biến Giảm kali và natri hưyết
Rối ioạn hệ thân kinh Phổ biến Chóng mặt
Không phổ bỉến Chóng mặt tư thế
Không rõ Đau đầu
W”
Rối loạn tai và mê dạo
Không rõ
Ù tai
Rối loạn hô hấp, ngực và trung
thât
Không rõ
Ho
Rôì loạn tìêu hóa
Phổ biến
Buôn nôn/Nôn
Không phố bỉến
Tỉêu chảy
Không rõ
Khó tiêu, loạn vị giảc
Rối loạn thận và tìết nỉệu
Phổ bỉến
Tỉểu tiện bẫt thường
Khôn g rõ
Suy thận, bao gồm cả cảo trường họp cá
biệt cùa suy thận ở những bệnh
nhân có nguy cơ.
Rôì loạn cơ xương và mô liên kêt
Không phổ biến
Sung cảc đắn chi
Không rõ
Đau khởp, Đau cơ
Rối loạn chuyến hóa và dinh
dưỡng
Khỏng rõ
Tăng ka1ỉ mảu
Rối loạn hệ mạch Không phổ biến Đò mặt
Rối loạn chun g Không rõ Mệt
Rối loạn hệ miễn dịch Không rõ Các trường hợp phản ứng quá mẫn
như phù, phảt ban, mảy đay
? Rối loạn gan mật Không phổ biến Bệnh vảng da
Không rõ
Viêm gan, bất thường chức năng gan
Rối 1oạn hệ sinh sản Vả tuyến vú
Không phố biễn
Mất khả năng sinh dục, thay dối ham
muôn tỉnh dục
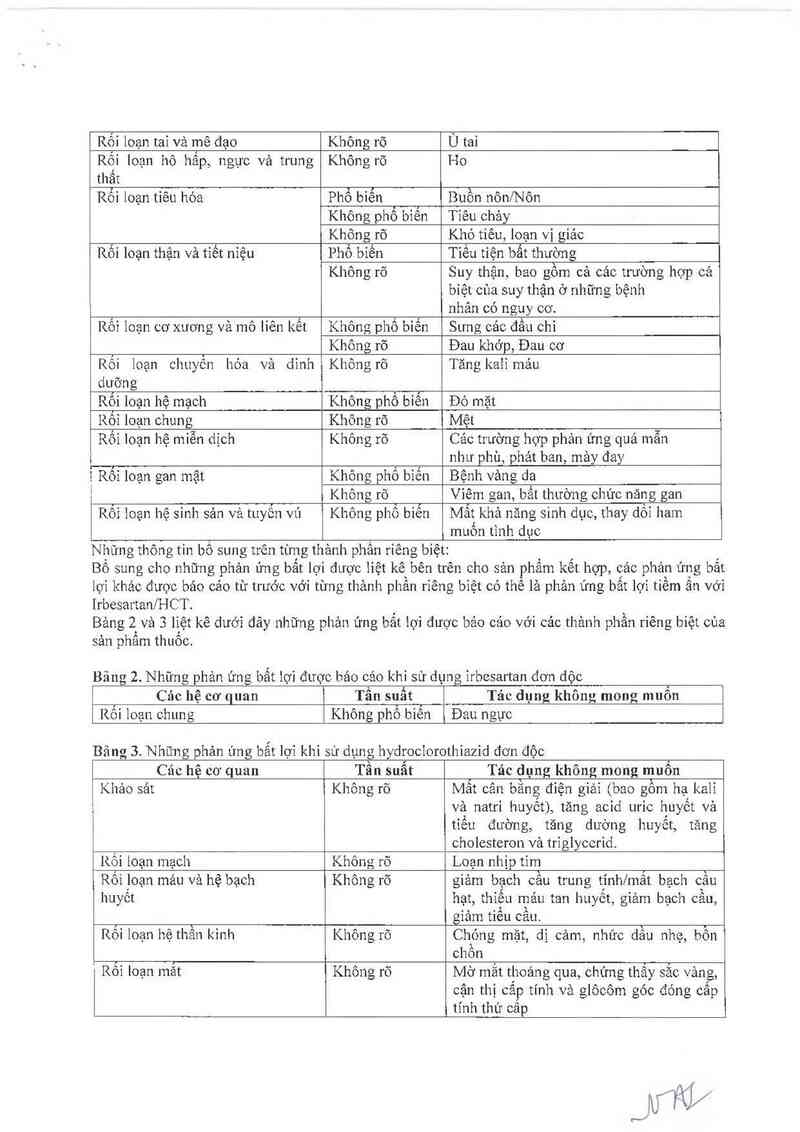
Nhung thông tin bô sung trên tùng thảnh phân riêng biệt:
Bổ sung cho nhũng phản úng bẳt lợi đuợc 1iệt kế bên trên cho sản phẩm kết hợp, cảc phản’ ưng bắt
lọi khảo được bảo cảo tù tLước vởi tùng thảnh phần rỉêng bỉệt có thể lả phản ứng bất lợi tiềm ân với
Irbesmtan/HCT.
Bảng 2 và 3 lỉệt kê dưới đây những phản ứng bắt lợi được báo cảo với các thảnh phần riêng biệt cùa
sản phẳm thuốc.
Bãng 2. Những phản ứng bất 1ợi được báo cảo khi sử dụng ỉrbesartan dơn dộc _
Các hệ cơ quan Tần suât Tác dụng không mong muôn
Rô] loạn chung Không phô biên Đau ngực
Băng 3. Những phản ửng bẫt lợi khi sử dụng hydrocĩorothỉazỉd đon độc
Các hệ cơ quan Tần suất Tảc dụng không mong muốn
Khảo sát Không rõ Mẩt cân bằng đỉện giải (bao gồm hạ kali
và natri huyết), tảng acid uric huyết và
tĩếu đường, tăng dường huyết, tăng
cholesteron vả trỉglyccnd.
Loạn nhịp tim
giảm bạch cầu trung tínhlmẳt bạch cầu
hạt, thỉếu mảu tan huyết, gìảm bạch cẩu,
gỉảm tiều cầu.
Chóng mặt, dị cảm, nhức dằn nhẹ, bồn
chồn
Mờ mắt thoan g qua, chứng thẩy sắc vảng,
cận thị cấp tính và glôcôm gỏc đóng câp
tĩnh thứ câp
Rồi 1oạn mạch
Rôì loạn mảu và hệ bạch
huyết
Không rõ
Không rõ
Rối loạn hệ thần kình Không rõ
Rối loạn mắt Không rõ
WÚ/
...)
Rối loạn hệ hô hấp, ngực vảtrung Khôngrõ Suy hô hẩp (bao gồm vỉêm thảnh phế
thất nangvả phù phồi)
Rối loạn hệtỉêu hóa Khôngrõ Viêm tụy, bỉếng ăn, tiếu chảy, tảo bón,
kích thích dạ dảy, vỉêm tuyến nước bọt,
mất cảm gìảc thèm ăn.
Rốì loạn thặn và tiết nỉộu Không rõ Viêm thận kẽ, rối loạn chức năng thận
Rối loạn da và mô dưới da Không rõ Phản úng phản vệ, hoại tử bỉếu bỉ nhiễm
độc, viêm mạch hoại tử (vỉêm mạch,
viêm mạch da), phản ứng giống như
lupus ban dò da, kích hoạt phản ứng ban
dò Iupưs da, phản ửng nhạy cảm với ánh
sáng, ban da, mảy đay
Rôi Ioạn mô cơ và mô lĩên kết Không rõ Yếu cơ, co thẳt cơ
Rối loạn mạch Không rõ Hạ huyết ảp tư thế
Rối loạn chung Không rõ Sõt
3 Rối loạn gan mật Không rõ vảng Jda (vảng da’ u mật trong gan)
1 Rôỉ loạn Lâm thần Không rõ Trầm cảm, rôỉ loạn giấc ngủ
Những tác dụng không mong muốn phụ thuộc lỉều của hydroclorothiazỉd (đặc bỉệt 1` rồi loạn đìện
giải) có thể tăng lên khi đìều chỉnh tăng ỉíều hydrocĩorothỉazỉd.
Bảo các phản ưng có hại đuợc nghi ngờ.
Cảo phản ứng có hại nghi ngờ được bảo các sau khi luu hảnh thuốc là rất quan Lrọng. Nó cho phép
tỉếp tục theo dõi sự cân bằng giữa lợi ích/nguy cơ của thuốc. Các chuyên gia chăm sóc súc khỏe
đuợc yêu cằn báo cảo bắt kỳ cảc phản’ ung bắt 1ợi nảo bị nghi ngờ thông qua hệ thống báo các quốc
tế
Thông báo cho bác sỹ, dược sỹ những iác dụng không mong muốn gặp _phái khi dùng thuốc.
QUÁ LIÊU
Không có thông tin đặc bìệt sẵn có cho đỉều trị quả lỉều Vởi lrbesartanlllCT. Bệnh nhân cẩn được
theo dõi chặt chẽ, vả đỉều LLị quá ìiều nên là đỉều trị Lrìệu chứng vả cẩn duợc hỗ tLợ. Điều trị phụ
thưộc VảO thời gìan uống thưốc và mức độ nghỉêm t1ọng cua trìệu chưng. Các biện pháp được đề
xuất bao gồm cảm ứng gây nôn vả rủa dạ dảy. Than hoạt có Lhể hữu dụng trcng đỉếu trị quá liều
Đỉộn giải trong huyết thanh vả creatinin có thế đuợc theo dõi thuởng xuyên. Nếu hạ huyết ảp xuất
hỉện, bệnh nhân cần đuợc dặt ttong tu thể nằm ngùa, và bổ sung muôỉ và dịch thay thể nhanh chóng
Cảc biếu hìện bất lợi nhất của quả lỉều ỉrbesartan dược mong dụ kỉến là cao huyết ảp vả tĩm đập
nhanh, nhịp Lỉm chậm cũng có thể xuất hiện.
Quá 1iều với hydroclorothiazìd có lỉên quan đến mất điện giải (giảm kali, clo, natri huyết) vả sự mất
nước lã kết quả từ sự1ợi tìếu quá mức. Các dấu hiệu phổ bỉến nhất và trỉệu chứng cùa quá liều lả
nôn và buồn ngủ. Hạ kali huyết có thể lả kết quả của sự co thắt cơ vả/hoặc loạn nhịp tim mạnh [Lên
quan tới việc sử dụng đồng thời các glycosỉd tim và cảc thuốc chốn g loạn nhịp.
Irbesartan không bị loại trừ bằng thẳm tảch mảu. Mức độ hydrociorothiazid bị loại bỏ bởi thẫm tách
máu không được thĩết lập.
TÍNH TƯỜNG KY \ ,
Không có sự tương kỵ gìũ~a cảc thảnh phân cùa Lhuôc.
ĐỎNG GÓI
Hộp 2 ví x 14 vỉên nén bao phìm.
LUỮAỀ
BẢO QUẢN:,
Bảp quản thuôc dưới 30°C.
Đê xa tâm tay trẻ em.
HẠN DÙNG: _
24 thảng kể từ ngảy sản xuât.
Khóng dùng thuôc đã quá hạn in trên bao bì.
TIÊU CHUẨN: Nhà sản xuất.
NHÀ SẢN XUẤT:
GENEPHARM S.A.
18th km. Marathonos Avenue - 15351, Pallinỉ - Hi Lạp.
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng