












2076149
BỘ Y TẾ
cục QUẢN LÝ DUỌC
ĐÃ PHÊ DUYỆT
Lãn dấu:.úffl…ẵszổi
231/2»
U NOVARTIS
Everolimus
/
Ư NOVARTIS
Everolimus
uôc tiin th cc đon
\, .s rng.SDK'XX-XXXX-XX
. ~ \ vủ1 nén Mói VIỒH nen dn“… 0.5 mg everolimus
Bhĩ ~)ỏ v
u 1 .
ừy hem
`4 0 Xem `LOT`, `MFD ', ”aF' lren bao bì
' ớy 01 của tháng rẻl Mn m lrđn beo ci
… ên :10'c, n1ũ trung hao hi, iránh ảm, vtnh ânn sáng
sĩ bới Noumc thn: Slein AG
z c 4332 Siein, Swnzerinnđ
( t-.X BÌNH DƯƠNG
ui nm. Đoc kỹ hướng đln lữ dung imớc khi đímg.
ôn-, khác zin nm lrcng từ hướng đẵn sứ đụng kẻm n…:
'0 CtieiicANi 0,5 mg
60 compnmés/tablets/cnmpnmdos
' CERTICANỄ'O,Smg
60 comprimés/tablets/compnmidos
\ đi'mg, chông chl đinh xln_ đọc trung 1ớ huởng đìn sử đụng
, 7’— 11, Đuông sớ 3, %… v.51 Nam-Smgaporc 2 Thi'. 061. 17151, tinh 81… m…:
))“
%
c
z
0
<
.c, ›
' W
… E
Ê m
_
ỂỀ ẳẵn
Ễẳ ãã>
99 nsz
SE °
ã
- _ - , ỉ `- ]
"Ú/Novn-rls
VIII! male o ỉehu 11015 116 18 11011: et da 18 171.5 des 57118an
| cnnmver ] une mme'uture ne dègasant 098 311 'C
A cnnunm đa i'embllllgt d'0ngim ả l'nn 11: In lumiére 91 051 humiđỉté
Fu au! use › Kem nui 51 thu 1660118111! sight d chìlđmn
Du nul 51010 lhme 30`C I Shi: … the nngmai nluiug in on)ei to pmth
170… m…… minh…
1118 mi! : Nahlmr 10… 1151 fcaucey de 1; …… u; lu n iios
Ne mnmvar a lnmuenmn lupenor | 30“C
Ccnưrvar en Il em…: nnciui uan nreseMrlo de li lui y 06 li humđad
CHW/lO1/dX]
HDmiìllfriélhhlet/mmurlmioucc 5muvacỉimns. L mglntns nmmnym…
74 ml ladcs. ziihyđr.. ủtyítiydmilniuen. (E 321161 constit. 41.5.
Vam.tacluieđ Dy/ hminm 501
1111qu11: Fharml 510111 AG, S…uulaun/Suiu
'01/ un N… ms Pimrn AG, SmizerhnđlSum
Ỉ (
om DIỆN
TẬI THÀNH P
Com Ricl &; 110.413115 ! :
Etuadui ZầEIE-ID-DI
[1 Salvaaơ W11112014
Guaianuln PF—17213
honduris M-llủũ
Nicaragua 017 5860101
Fanzmá 593l1
7160 1107111111th thim!
Vmuưlz RiF l-ùìũiaìẽĩồl
era ban receia médtu
LOUiS—GÉORGES ussomemr
C_hÍet Representative
The Ropresentative 011108 01
Novariís Pharma Sarvices AG in HCMC |
f NOVAR
39.0 mm Ỉ_`
Laưlrichlmg Folie ~. ,`
L0016-6EOR6E8 LASSONNERY
Chiet Representative
The Represemaiive Office of
Novarù’s Phanna Sarvices AG in HCMC
U) NOVARTIS
Rx - Thuốc bán theo đơn
Certican®
Thuốc ức chế miên dich chon ioc
THẦNH PHẢN
Certican 0.25 mg:
Hoat chát: Mỏi viên nén chừa 0.25 mg everolimus.
Corticon 0,5 mg:
Hoat chảt: Mõi vièn nén chứa 0.5 mg everolimus.
Certican 0,75 mg:
Hoat chảtị Mõi vièn nén chứa 0,75 mg everolimus.
Certican 1,0 mg:
Hoat chất: Mõi viên nén chừa 1,0 mg everolimus
Tá dược cho tất cả cảc hảm lượng: Hydroxytoluene butyl hóa, magnesi stearat, Iactose
monohydrat. hypromeilose. crospovidone, lactose khan.
DẠNG er c11E
Certican 0,25 mg: Viện nén máu trắng đèn hơi váng, có ván cảm thạch, tròn, dei với gờ xiên,
có khác chứ “C" trẻn một mật vả chữ 'NVR' trèn mặt kia.
Certican 0.5 mg: Viên nẻn máu trắng đẻn hơi váng, có ván cấm thach, tròn, dẹt với gờ xiên,
có khẳc chữ “CH" trén một mặt vả chữ "NVR' trẻn mãt kia.
Certicen 0,75 mg: Viên nén mảu trắng đẻn hơi vảng, có ván cảm thach. tròn, det với gờ xiên,
có khâc chữ “CL" trèn một mặt vá chữ "NVR' trèn mặt kia.
Certican 1,0 mg: Viên nén máu trăng đén hơi váng. cỏ vãn cảm thach, tròn, dẹt với gớ xiên.
có khác chữ 'CU' trèn một mật vá chữ "NVR' trẻn mặt kia.
cni ĐịNH
Cenican được chỉ định để dự phòng thái tang ghẻp ở bènh nhân ngưới iớn có nguy cơ về
miên dich từ thẩp đẻn trung bình đang được ghép thán hoặc tim cùng Ioải khác gen. Certican
nèn dùng phôi hợp với ciclosporin dang vi nhũ tương vả với corticosteroid
LIỂU LƯỢNG vA cAcu DÙNG
Việc đièu tri bãng Certican chi nèn khới đảo vá duy tri do cảc thầy thuóc có kinh nghiệm về
điều tri ức chế miễn dich sau ghép tang vá lả ngưới quyèt đinh việc theo dõi nòng đò
everolimus trong máu toán phán.
Người iớn
t.…M
Liều khởi đầu khuyên các lá 0,75 mg, 2 lầnlngảy đối với nhóm ghép thận vả ghép tim nói
chụng, lnên dùng cảng sớm cảng tồi sau khi ghép. Liều Certican hảng ngảy nẻn Iuôn chia lảm
2 iằn uổng (2 Iầnlngảy) Certican nèn được dùng một cách hằng định nghĩa lá hoặc iuôn cùng
thức ản hoặc iuôn không cùng với thức ăn (xem phần Dược động học) vả nên dùng đồng thời
với ciclosporin dạng vi nhủ tương (xem phần Theo dõi nồng độ thuốc điều trị).
Certican chi dùng đường uống.
Nên nuốt nguyên cả viên Ce_rtican vởi một ly nước vả khỏng nghi_èn trước khi dùng. Đối với
những bệnh nhân không t_hè nuôt nguỵẻn cả viên thi củng có săn Certican dạng viên nèn
phân tán (xem tớ hướng dán sữ dụng đôi với viên nẻn phản tán Certican).
Bệnh nhản đang dùng Certican có thể cần điều chỉnh lièu dựa trên nồng độ thuốc trong mảu,
sự dung nạp, đảp ứng của từng bệnh nhân, thay đối về thuốc dùng phội hợp vả tình trạng
lâm sảng. Việc điều chỉnh liều có thẻ thưc hiện cảch nhau 4-5 ngảy (xem phán Theo dõi thuôc
điêu trị).
Bệnh nhân da đen
Tần suất cùa cảc đợt thải ghép cắp được xác định bằng sinh thiêt cao hơn đảng kể ở bệnh
nhân da đen so với bệnh nhân không phải da đen Thỏng tin còn hạn chế cho thảy lả bệnh
nhản da đen có thế cần một liều Certican cao hơn để đạt đươc hiệu quả giống như hiệu quả
đạt được ở bệnh nhản không phải da đen khi dùng iiều khuyến cáo cho người lớn (xem phần
Dược động hoc). Hiện nay, dữ iiệu về hiệu quả và an toản còn rất han chế không cho phép
có khuyến cảo đặc biệt về việc dùng everolimus cho bệnh nhân da đen.
Sử dụng ở trẻ em vả thiếu niên
Chưa đủ dữ liệu về việc dùng Certican cho trẻ em và thiếu niên để hỗ trợ việc dùng thuốc cho
bệnh nhân trong các nhỏm tuồi nảy. Tuy nhiên có một it thòng tin ở bệnh nhi ghép thận (xem
phần Dược động học).
Bệnh nhãn cao tuổi (2 65 tuổi)
Chưa có nhiệu kinh nghiệm lâm sảng ở bệnh nhản 2 65 tuồi. Tuy nhiên, không thảy sự khác
biệt rõ rệt về dược động hoc của everolimus ở bệnh nhán z 65- 70 tuổi khi so với người
trưởng thảnh trẻ tuồi hơn (xem phần Dược động học).
Bệnh nhân suy thặn _ _ ệ
Không cân điêu chỉnh liêu (xem phân Dược động hoc). /
Bệnh nhân suy gan
Nống độ đảy (CO) của everolimus trong máu toản phần cần được theo dõi chặt chẽ ở bệnh
nhân bị suy chức nãng gan Đói với bệnh nhảm bị suy gan nhe (chỉ số Child- -Pugh nhóm A),
nẻn giám iiều đến khoảng 273 của liều thộng thường. Đôi với bệnh nhân bị suy gan vừa hoặc
nặng (chỉ số Child Pugh nhóm B hoặc C), nèn giảm liều đẻn khoảng ’/2 của liêu thòng thường
Việc chuẩn độ liều thẻm cần dựa trên sự theo dõi nồng độ thuốc điều trị (xem phần Dược
động học).
Theo dõi nồng độ thuốc điều trị
Khuyến cáo theo dõi thường xuyên nồng độ thuốc điều trị trong máu toản phần. Dưa trên
phản tích về nồng độ thuốc tồn lưu- hiệu quả vả nồng độ thuốc tồn lưu-độ an toán, đã ghi
nhặn những bệnh nhản đạt được nồng độ đảy (CO) của everolimus trong mảu toản phần 2
3, 0 ng/mL có tỷ lệ thấp hơn về thải ghép cắp được xa'c định bằng sinh thiét ở cả ghép thận vả
ghép tim so với bệnh nhân có nồng độ đáy (CO) dưới 3, O ng/mL Giới hạn trên của mức điều
trị được khuyên cảo 18 8 nglmL. Chưa có nghiện cứu về mức trên 12 ng/mL. Những mức
khuyên cáo nảy đối với everollimus được dựa trẻn phương pháp sắc ký.
Điều đăc biệt quan trong lá phải theo dõi nồng độ everolimus trong mảu ở bệnh nhân bị suy
gan, trong khi dùng đông thời với các chât gảy cảm ứng vả chắt ức chè mạnh CYP3A4, khi
2
chu èn sang thuóc khác vả/hoảc néu Iièu ciclosporin bị giảm rộ rệt (xem phản Tướng tác
thu ). Nòng độ everolimus có thế giảm nhẹ sau khi dùng dang vièn nén phán tán
Lý tướng lá nẻn điều chĩnh lièu Certican dựa trèn nòng độ đảy (CO) đat được > 4-5 ngảy seu
khi thay đỏi liều dùng trước đáy. Vi ciclosporin tương tác với everolimus, nòng độ everolimus
có thế giảm néu nòng độ ciclosporin tỏn lưu giám rõ rệt (tức lả nòng độ đảy (CO) < 50 nglmL).
Liều ciclosporin khuyến căo trong ghép thịn
Khộng nèn dùng Certican trong thới gian dải cùng với các Iièu ciclosporin đảy đù. Nòng độ
ciclosporin tòn lưu giám ớ benh nhân ghép thận được điều trị bấng Certican Iảm cải thiện
chừc nảng thặn Dưa trẻn kinh nghiệm đai được từ nghiên cứu A2309. giảm nồng độ
ciclosporin tòn iưu cản bắt đảu ngay sau khi ghép với nòng độ đáy khuyến cảo trong máu
như sau:
Ghép thận: nòrm độ đáy mục tiêu khuyên củo của ciclosporin trong máu
Nòng độ đáy moc tiéu ciclospotin C,, (nglmL) Tháng thứ 1 Tháng thư 2-3 Tháng thứ 4—5 Tháng thứ 6—12
Nhóm Certican 100-2 00 75—150 50—100 25-50
(Nỗng độ được tinh ở tren được trinh bảy trong phần Dược lưc)
Trước khi giám Iièu ciclosporin cản oha'i xác định lả nòng đó đảy (CO) của everolimus trong
mảu toản phản ở trang thái ỏn đinh bảng hoặc tren 3 nglmL.
Có các đữ iiệu hạn chế liên quan 11èu đùng Certican với các nòng độ đảy (CO) của ciciosporin
dưới 50 nglmL, hoảc nòng độ ciclosporin trong máu đo được 2 giờ sau khi dùng (02) dưới
350 nglmL. trong giai đoan duy tri. Néu bènh nhân khòng thể dung nap sự giảm nòng độ
ciclosporin tòn lưu, việc tiép tục dùng Cedican nèn được cản nhẳc iại.
Liều ciclosporin khuyỏn câo trong ghẻp tim
Benh nhán ghép tim trong giai đoan điều tri duy tri nèn bắt đảu giám iièu ciclosporin lủc 1
thảng sau khi ghép dù dung nep đề cải thiện chức năng thận. Nẻu suy chừc nảng thãn tién
triẻn hoặc néu hệ số thanh thải creatinine theo tinh toán < 60 mL/phút, cản điều chinh chế độ
điều tri. Ở bệnh nhán ghép tim. Iièu ciclosporin cấn dựa vảo kinh nghiêm đat được trong
nghiên cừu 2411 vả được xác nhận trong nghiện cứu 2310, trong đó Certican được dùng
cùng với ciclosporin với nòng độ đáy muc tiêu (CO) của ciclosporin trong mảu giảm như sau:
Ghep tlm: cửa số nồng độ đáy mục tiêu trong mảu được khuyến cáo cùa ciclosporin
Nòng dò đáy muc 1100 Ciclosporin CO Tháng thứ Tháng thứ Tháng thứ Thùng thử Tháng thứ
(ng/mL) 1 2 3—4 5—6 7—12
Nhóm Certican 200-350 150-250 100-200 75—150 50100
(Nồng độ được tinh ở trèn đươc trinh báy trong phấn oược LỰC)
Tn.rớc khi giảm Iièu ciclosporin cấn xác đinh lả nòng độ đáy (CO) của everolimus trong máu
toản phân ở trang thải háng đinh bằng hoặc tren 3 nglmL.
Ở bệnh nhán ghép tim. các dữ liệu liện quan đén Iièu Certican với các nòng độ đáy (CO) cùa
ciclosponn giảm xuỏn 50-100 nglmL sau 12 tháng còn han ché. Néu bènh nhản khộng thể
dung nap việc giảm n ng độ tòn lưu của ciclospn'n, việc tiẻp tuc dùng Certican cần được xem
xét lai.
cnóue CHI 911111
Chóng chi đinh dùng Certican ở bệnh nhãn đá biét quả mẫn cảm với everolimus. sirolimus
hoặc với bát kỷ thánh phần nảo của tá dược.
cAnu er vA THẬN TRỌNG ĐẠC BIỆT KHI sữ DỤNG
u-tJuf 4 `
Đọc kỹ hướng đỗn sử đụng trước khi dùng. Nón eân tth thòng tin. xin hới ý kiến bác
sĩ.
Thuốc nây chi dùng theo cư kê đơn của bic el.
Kiém soát ức chế miến địch
Trong ca'c thử nghiệm Iám sảng, Certican đã được dùng phói hợp với ciclosporin dang vi nhũ
tương, basiliximab vá corticosteroid Chưa có nghiên cứu đảy đủ về việc dùng phói hợp
Certican với các thuóc ức chế miến dich khác so với những chát náy.
Certican chưa được nghiẻ_n cứu đẩy_đủ trẽn bệnh nhán có nguy cơ cao về miễn dich.
Két hợp với liệu phâp đìn nhập báng thymoglobulin
Cản thận trong với việc sử dung thymoglobulin (globulin thỏ kháng thymocyte) như liệu pháp
dãn nháp vè chế độ điều trị Certican/ciclosporinlsteroid. Trong một nghiên cứu lảm sảng ở
ngưới được ghép tim (nghiên cứu A2310. xem phản DƯỢC LỰC HỌC). đã quan sát tháy ti iệ
mẩc các bẽnh nhiẻm trùng nghiệm trong tâng ièn trong ba tháng đáu tièn sau khi ghép ở phản
nhóm bệnh nhán đã dùng iiệu phá dẩn nhân với giobulin thỏ kháng thymocyte két hợp với
Certican, steroid vả ciciosponn ở n ng độ máu được khuyên 690 cho việc ghép tim (cao hớn
so với ghép thán). Điêu náy liẻn quan đén tỷ lệ tử vong cao hơn ở các bệnh nhản phái được
nhảp viện cùn với cằn đén thiết bi hỗ trợ tám thải tmớc khi ghẻp, cho thảy rằng cảc bệnh
nhán nảy có th đặc biệt nhạy cảm với ức chế miễn dịch táng cướng.
Nhiễm trùng nghiêm trọng vì nhiễm trùng cơ hội
Trén bệnh nhán đang được điều trị bảng thuóc ức chế miên địch, bao gòm Certican, có sự
gia tăng nguy cơ nhiễm trùng đặc biệt lả nhiễm trùng do các tảc nhán gả bệnh cơ hôi (vi
khuán, nảm, virus, động vải đơn bảo). Đã có báo cáo về nhiễm trùng huy 1 vé nhiễm trùng
gảy tử vong ở bệnh nhán được đỉèu trị bảng Certican (xem phân TÀC DỤNG KHÒNG MONG
MUON). Trong các nhiễm tn'1ng cơ hội mà bệnh nhán điều tri ức chế miễn dich dẽ bi nhiễm có
thề ké đén polyomavirus bao gòm bộnh thận Iién quan đẻn virus BK, có thẻ dăn đén mải thán
ghép vả bènh iỷ chát tráng nâo đa 15 tiến triẻn (PML) iiẻn quan đén virus JC có khá nảng gáy
tử vong. Những nhiẽm trùng nảy thường lièn quan với tóng lượng thuóc ừc chẻ miền dich sử
dụng, cần được chấn đoán phán biệt với bệnh nhân ức chế miễn dich có chức nảng thán
ghép suy giảm hoặc có cảc triệu chứng về thần kinh.
Trong các thử nghiệm iám sảng với Certican, kháng sinh dự phòng viêm phỏi do
Pneumocystic jiroveci (carinii) đã được dùng trong 12 tháng đảu sau héo tang. Điều trị dự
phộng nhiẽm Cytomegalovirus (CMV) được khuyên các trong 3 tháng đ 11 sau ghép tang. đặc
biệt đói với những bệnh nhán có gia tãng nguy cơ nhiễm Cytomegalovirus.
Suy gen
Khuyên cáo theo dội chăt chẽ nòng độ đáy (CO) của everolimus trong mảu toản phần vả điều
chinh Iièu everolimus ở bộnh nhân bi suy gan (xem phản LIÊU LƯỢNG VÀ CÁCH DUNG).
Tương tác với các thuốc ưc chẻ mạnh, chất gãy cám ứng CYP3A4
Không khuyên các dùng phói hợp với cảc chất ức chế manh CYP3A4 (vi dụ ketoconazoie.
itraconazole, von'conazole, clanthromycin, telithromycin, ritonevir) vả các chát gây cảm ứng
CYP3A4 (ví dụ rifampicin, nfabutin) trừ khi iợi ich vượt hản nguy cơ.
Khuyên cáo theo dội nồng độ đáy CO) của everolimus trong máu toán phản bát cứ khi náo
các chất gãy ợe'm ứng hoác các ch t ưc chẻ CYP3A4 được dùng phỏi hợp hoặc ngừng dùng
(xem phản Tương tác thuóc).
U lympho vi các bệnh ác tinh khác
Những bénh nhán đang dùng thuòc ức chế miên dich bao gòm cả Certican, có nguy cơ cao
về phát triền u Iymphò báo hoăc cảc bệnh ác tinh khác, đặc biệt lá ở da (xem phần Tác dụ
khòng mong muôn). Nguy cơ tuyệt đói dướng như lièn quan đén thới gian vá mớc độ ức cgẵ
miên dịch hớn lá với việc sử dung thuỏc đảc hiệu. Cân theo dỏi bẻnh nhản thướng xuyên về
4
ý
cảc u tân sinh ở da và nên trảnh đến mức thấp nhằt việc tiếp xúc với ảnh sáng từ ngoai của
mặt trời vả sữ dụng dẫn xuất chống nắng thich hợp
Tăng lipid máu
Ở bệnh nhán ghép tang, dùng đỏng thới Certican vả ciclosporin dạng vi nhũ tương có liên
quan với tãng cholesterol vả triglyceride huyết thanh, có thể cần phải điều trị. Bệnh nhân đang
sử dụng Certican cần được theo dõi tinh trạng tảng lipid máu vả, nếu cần điều trị bằng cảc
thuôc lảm giảm lipid máu vá điều chỉnh chế độ ăn kiêng thich hợp (xem phần TƯỞNG TÁC)
Cần xem xét nguy cơ/lợi ich ở những bệnh nhản đă được xác định tảng lipid máu trước khi
bắt đầu chế độ điều trị bằng thuốc ức chế miễn dịch bao gồm Certican Tương tự, cần đánh
giá nguy cơllợi ích cùa việc tiêp tục điều trị bầng Certican ở những bệnh nhản bị tăng lipid
huyết nặng không đáp ứng với thuốc
Bệnh nhán đang dùng thuốc ức chế HMG- CoA reductase vảlhoặc fibrate cần được theo dõi
về khả nảng xảy ra tiêu cơ vản vảlhoặc các tảc dụng phụ khác như đã được mô tả trong
thông tin kê đơn tương ưng cùa các thuốc nảy (xem phần TƯỚNG TÁC).
Phù mạch
Certican có liên quan với phù mạch. Trong đa số trường hợp, bệnh nhân được ghi nhận đang
dùng thuốc phối hợp lả chầt ữc chẻ men chuyền angiotensin (ACE)
Độc tinh trẽn thặn
Certican phối hợp với ciciosporin đủ liều Iám tăng nguy cơ rối loan chức nảng thận Cần giảm
liêu ciclosporin khi phỏi hợp với Certican để tránh rối ioạn chữc nãng thận Theo dõi thướng
xuyên chức nảng thận được khuyến cảo ở tắt cả bệnh nhân Điều chinh chế độ điều trị thuốc
ưc chế miễn dịch thich hợp, đặc biệt cần cân nhắc giảm liều ciclosporin ở bệnh nhản có nồng
độ creatinine huyết thanh tảng Cần thặn trọng khi dùng đỏng thời với các thuốc khác đã biết
có tác dụng có hại trên chức nảng thặn
Protein niệu Ễ/
Việc sử dụng Certican cùng với ciclosporin ớ_bệnh nhân mở] được ghép thận có liên quan với
tăng protein niệu. Nguy cơ nảy gia tăng với nòng độ everolimus cao hơn trong mảu.
Ở những bệnh nhản ghép thặn có protein niệu mức đó nhẹ trong khi điều trị duy tri thuốc ức
chế miên dịch bao gồm chắt ức chế caicineurin (CNI), đă được ghi nhận protein niệu nặng
thêm khi thay thế CNI bằng Cenican Đã quan sát thẳy khả năng có thể phục hồi được khi
ngưng sử dung Certican vả sử dụng [ại CNI. Độ an toản vả hiệu quả cùa việc chuyển đối từ
CN! sang Certican ở những bệnh nhân nảy chưa được xảc định.
Bệnh nhân đang sử dụng Cenican cần được theo dõi protein niệu.
Huyết khối trong thặn ghép
Gia tảng nguy cơ huyết khối động mạch vả tĩnh mạch thặn, dẫn đên mất mảnh ghép, đã được
ghi nhặn, hâu hẻt xảy ra trong vòng 30 ngảy đảu sau ghép.
Biến chững đối với khả nảng Iảnh vết thương
Cetiican, cũng giống như ca'c chắt ức chế mTOR khảo, có thể ảnh hướng đến quá trinh Iảnh
vết thương, tảng xuất hiện cảc biến chứng sau ghép t_ạng như nưt vết thương, tụ dịch vả
nhiễm trùng vẻt thương, có thể cần sự chăm sỏc thẻm bằng phẫu thuật U nang bạch huyềt lả
phản ưng phụ đã được ghi nhặn thường gặp nhẩt ở bệnh nhân ghép thận vả có xu hướng
5
thường gặp hơn ở bệnh nhân_có chỉ số khối cơ thể cao hơn. Tần suất của trản dich mảng
ngoải tim vả trản dịch mảng phỏi tăng Iẽn ở bệnh nhản ghép tim.
Bệnh vi_mạch huyết khối/Ban xuất huyết giảm tiều cầu huyết khổilHội chứng tảng urê
tán huyêt
Việc sử dụng đồng thời Certican với một chất ức chế calcineurin (CNI) có thế iảm tảng nguy
cơ hội chững tăng urê tán huyétlban xuất huyết giảm tiểu cầu huyết khối/bệnh vi mạch huyết
khối do CN!
Bệnh phổi mô kẽlviêm phồi không do nhiễm trùng
Cần xem xèt chẩn đoán bệnh phối mô kẽ (ILD) ở những bệnh nhân có các triệu chứng phù
hợp với viêm phồi do nhiễm trùng nhưng không đảp ứng với điều trị kháng sinh và ở những
bệnh nhân mà các nguyên nhân nhiễm trùng, khối u tân sinh vả những nguyên nhân không
do thuốc đã được ioai trữ qua các thăm dò thich hợp. Cảo trướng hợp bệnh phối mỏ kẽ với
Certican đă được ghi nhận, thường hồi phục khi ngưng thuốc, có hoặc không điều trị với
glucocoriicoid. Tuy nhiên, củng xảy ra các trường hợp tử vong (xem phần TÁC DỤNG
KHÒNG MONG MUÔN).
Đái tháo đường mới khời phát
Certican đã được ghi nhận lảm tăng nguy cơ đái tháo đường mởi khới phảt sau khi ghép
tạng. Cân theo dõi chặt chẽ nồng độ giucose máu ở bệnh nhân đươc điệu trị băng Ceriican.
Vô sinh ở nam giới
Có các bảo các trong y vản về tinh trạng không có tinh trùng vả ít tinh trùng có thể phục hồi
được ở những bệnh nhân được điêu trị bằng chắt ức chế mTOR. Các nghiên cứu về độc tính
tiền lâm sảng đã cho thắy everolimus có thề lảm giảm sự sinh tỉnh trùng, vô sinh ở nam giới
phải được xem lả một nguy cơ tiềm ấn cúa việc điêu trị bằng Certican kéo dải. Jệ
/
Nguy cơ không dung nạp vời cảc tặ dược
Bệnh nhản có các vân đè di truyẻn hiêm gặp về không dung nạp galactose, thiếu men Iactase
trâm trọng hoặc bất thường về hắp thu glucose—galactose không nèn dùng thuòc nảy.
TƯỜNG TÁC THUỐC
Everolimus được chuyền hóa chủ yếu ở gan vả ở một mức độ nảo đó ở thảnh ruột non nhờ
CYP3A4. Nó còn lả một cơ chầt đối với P-glycoprotein (PgP) lả chắt bơm cho sự thoát ra của
nhiều thuốc. Vì vậy, sự hấp thu vả thái trừ sau đó của everolimus đươc hấp thu toản thản có
thể bị ảnh hưởng bởi các thuốc ảnh hướng đên CYP3A4 vảlhoặc PgP. Không khuyên các
điều trị đỏng thời với cảc chắt ức chế vả/hoặc gây cảm ứng mạnh CYP3A4. Các chât ức chế
PgP có thề iảm giảm sự thoát ra cùa everolimus từ tế bảo ruột non vả lảm tăng nồng độ
everolimus trong máu, In vitro, everolimus lả một chắt ức chế cạnh tranh của CYP3A4 vả
CYP2D6, Iảm tăng mạnh nồng độ của các thuốc được thải trữ bởi cảc enzyme nảy. Vì vặy,
cần thận trong khi dùng phối hợp everolimus với các cơ chắt của CYP3A4 vả CYP2DB có chỉ
số điều trị hẹp, Tắt cả các nghiên cứu về tương tác thuốc in vivo đã được thực hiện mã không
dùng phối hơp với ciclosporin.
Ciclosporin (chẩt ức chế CYP3A4/PgP)
Sinh khả dụng của everolimus tăng đảng kể khi dùng phối hợp với ciclosporin. Trong một
nghiện cứu dùng iiều đơn ở những người khỏe mạnh, ciclosporin dạng vi nhũ tương (Neorai)
đả lảm tăng diện tich dưới đường cong nồng độ (AUC) cùa everolimus iả 168% (trong khoảng
46%-365%), vả nồng độ cao nhắt trong huyềt tương (C,…) iả 82% (trong khoang 25%-158%)
khi so với dùng everolimus đơn thuần. Có thể cân phải điều chỉnh iiều everolimus nếu thay
đổi liều ciclosporin (xem phần Liều lượng vả cách dùng). Certican chỉ có ảnh hưởng lâm sảng
6
nhẹ đối với dược động học của ciclosporin ở bệnh nhản ghép thặn vả ghép tim đang dùng
ciclosporin dạng vi nhủ tương.
Rifampicin (chắt gây cám ững CYP3A4)
Nhữn bệnh nhản khỏe mạnh được điều trị trước đó với nhiều liều rifampicin, sau đó dùng
một lieu đơn Certican đả táng hệ số thanh thải everolimus gần gắp 3 lần, giảm nồng độ cao
nhắt trong huyêt tương (C,…) lả 58% và giảm diện tích dưới đường cong nồng độ (AUC) lả
63% Không khuyến cảo dùng phối hợp với rifampicin (xem phần Cảnh báo vả thận trong dảc
biệt khi sử dụng)
Atorvastatin (cơ chẩt cùa CYP3A4) vả pravastatin (cơ chắt của PgP)
Dùng lièu đơn Cedican với atorvastatin hoặc pravastatin cho những người khỏe mạnh không
lảm ảnh hưởng đến dược động hoc của atorvastatin, pravastatin vả everolimus, củng như độ
phản ứng sinh học của HMG- CoA reductase toản phần trong huyệt tương đền một mức độ có
liẻn quan về lâm sảng Tuy nhiên những kết quả nảy không thể suy ra đối với các chắt ức
chế HMG- CoA reductase khảo
Bẻnh nhản phải được theo dõi về sự phát triển bệnh tiêu cơ vản và các phản ứng phụ khác
như đã mô tả trong Thông tin kê đơn vẽ các chât ức chế HMG-CoA reductase.
Midazolam (cơ chẩt của CYP3A4A)
Trong một nghiên cữu tương tác thuốc chéo hai giai đoạn, trinh tư cổ đinh, 25 người khỏe
mạnh nhận được liều đơn 4 mg midazolam đường uống trong giai đoạn 1, Trong giai đoạn 2,
họ uống 10 mg everolimus, 1 lần/ngảy trong 5 ngảy vả lièu đơn 4 mg midazolam vời iiều cuối
cùng cùa everolimus Cmax cúa midazolam tăng 1, 25 lần (90% Cl',1,14-1 37) và AUC… tăng
1,30 lần (1, 22- 1 ,39) Thời gian bán hủy của midazolam không thay đồi Nghiên cữu nảy chỉ ra
rằng everolimus là một chất ữc chê yếu của CYP3A4. ị
Các tượng tác khác có thể gặp
Các chầt ức chế trung binh của CYP3A4 vả PgP có thế iảm tăng nồng độ everolimus trong
máu (ví dụ cảc chẩt kháng nấm: fluconazole, các kháng sinh nhóm macrolide:
erythromycin; thuốc chẹn kênh calci verapamil, nicardipin diltiazem; thuốc ức chế
protease neifinavir, indinavir, amprenavir) Cảo chất gây cảm ứng CYP3A4 có thế Iảm tảng
sư chuyền hóa everolimus vá lảm giảm nông độ everolimus trong mảu (ví dụ: St John' s wort
(Hypericum perforatum) thuốc chổng co giặt carbamazepine, phenobarbital, phenytoin;
thuốc chống virus gây suy giảm miễn dịch mảc phải ở người (HIV): efavirenz,
nevirapine).
Quả bưới vả nước bưởi ảnh hưởng đẻn hoạt động của cytochrome P450 vả PgP, vi vặy nên
tránh sử dụng.
Sư tiêm chủng
Các thuốc ức chế miễn dịch có thể ảnh hưởng đến đáp ứng đối với sự tiêm chùng vả vi vậy
sự tiêm chủng trong khi điều trị băng Certican 11 có hiệu quả. Nên tránh sử dụng vacxin sông.
PHỤ NỮ có THAI vÀ CHO CON BÚ
Có thai
Chưa có dữ Iiệu đầy đủ về việc dùng Certican cho phụ nữ có thai. Các nghiên cữu trèn động
vật đã cho thắy các tác dung về đôc tinh sinh sản bao gồm độc tinh phôi vả độc tính đối với
thai (xem phần Các dữ Iiệu an toản tiền lâm sảng) Chưa rõ nguy cơ có thể có đối với người
Không nèn dùng Certican cho phụ nữ có thai trừ khí lợi ich dự tính vượt hẳn nguy cơ có thế
có đối với thai. Nên khuyên những phụ nữ có khả năng mang thai sữ dụng các phương pháp
ngữa thai có hiệu quả trong khi đang dùng Cenican vả dùng đến 8 tuần sau khi ngững điều trị
bằng Certican
Cho con bú
Chưa rõ có phải everolimus được bải tiết vảo sữa mẹ hay không, nhưng trong các nghiên
cứu ở động vật, everolimus vảlhoặc các chảt chuyến hóa của nó đi qua dễ dảng vảo sữa của
chuột cho con bú, Vì vậy những phụ nữ đang dùng Certican khỏng nên nuôi con bú.
TÁC ĐỌNG CÙA THUOC KHI 1.711 XE VÀ VẬN HÀNH MÁY MÓC
Chưa có nghiên cứu nảo được thưc hiện về ảnh hướng trèn khả năng iái xe vả sữ dụng mảy
móc.
TÁC DỤNG KHỎNG MONG MUỐN
Tần suất các phản ững phụ cùa thuốc được liệt kê dưới đây trinh bảy những biếu hiện quan
sải được ở những bệnh nhân dùng Certican kết hợp với ciciosporin vả các thuốc
corticosteroid ở thử nghiệm ở nhiều trung tâm, ngẫu nhiên, có kiềm chững. Chúng bao gồm 5
thử nghiệm ở tổng sô 2497 bệnh nhân mời ghép thận vả 3 thử nghiệm ở tông sô 1531 bệnh
nhân mời ghép tim (theo dân số có ý định điêu trị: 1TT, xem phần Dược lý). <ẳ/
Bảng 1 dười đảy gồm các phản ứng phụ có thế hoặc có iẽ iiẻn quan đén Certican đă được
ghi nhận trong các thử nghiệm iâm sảng giai đoạn III (ghép thặn vả ghép tim) Trừ khi có lưu
ý khác, những rối loạn nảy đă được xảc định bởi tỉ lệ tăng ở pha 111 trong cảc nghiên cữu so
sánh bệnh nhán đang điều trị với phác đồ Certican + ciclosporin với bệnh nhản theo phác đồ
ciclosporin mả khỏng điều trị với Certican Báng nảy được soan theo phân ioại cơ quan vời
tiêu chuẩn của Med DRA.
Cảo phản ửng phụ được liệt kê theo tắn suất dược xác đinh như sau: rẩt hay gặp. > 1/10, hay
gặp: > 1/100 va < 1/10, ít gặp > 171 000 vá < 1/100, hiểm gặp. > 1/10. 000 vả < 1/1. 000, rất
hiềm gặp < 1/10. 000.
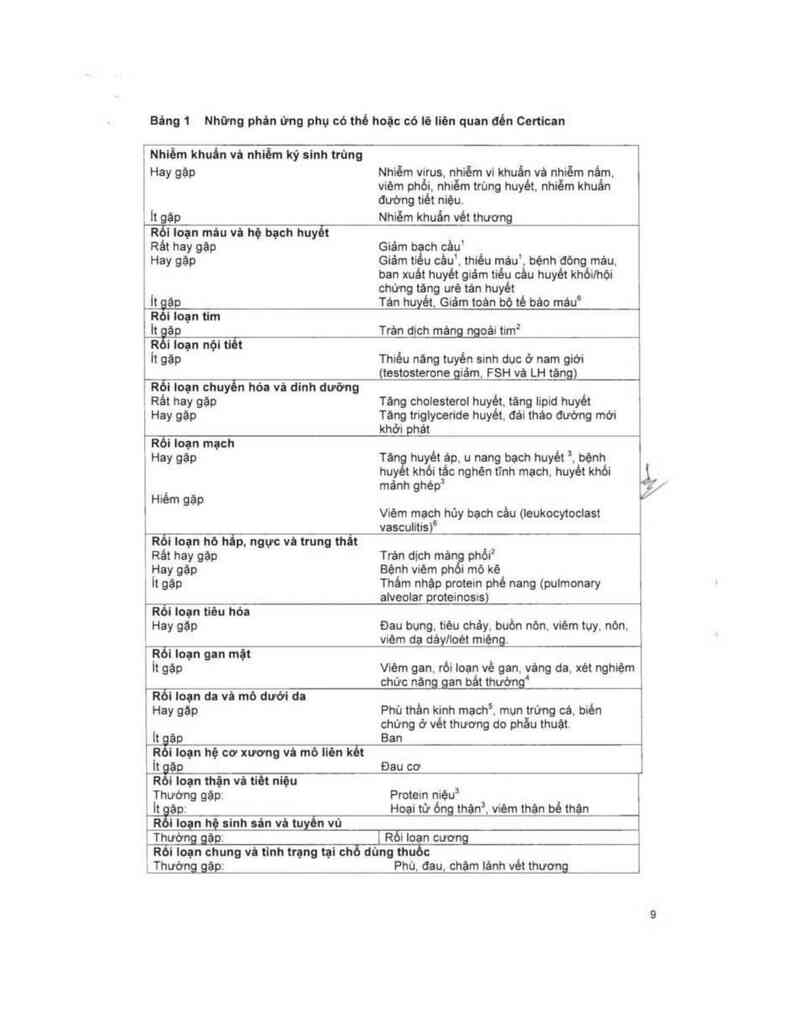
Bảng 1 Nhưng phân ưng phụ có thế hoặc có iõ Iiẻn quan đến Ceftican
Nhiễm khuẩn vả nhiễm kỷ slnh trùng
Hay gặp
ligặp
R Han tim
ịgặn
R iioạn nội tiất
ltgăp
Hay gặp Nhiễm virus, nhiẽm vi khuản vả nhiẻm nấm.
viêm phỏi, nhiễm trùng huyêt, nhiẽm khuấn
đường tiét niệu.
It gặp Nhiẽm khuấn vét thương
Rối Ioạn máu vả hộ bạch huyễt
Rảt hay gặp Giám b ch cầu'
Giảm ti u cảu`, thiêu mảu'. bệnh đông mảu,
ban xuất huyêt giám tiếu cãu huyêt khói/hội
chứng táng urê tản huyết
Tán huyêt, Giám toán bộ té báo máus
Trán dịch mánggggải iim²
Thiếu năng tuyến sinh dục ở nam giới
(testosterone giảm, FSH vè LH tăng)
Rối Ioạn chuyển hóa vù dinh đường
Rái hay gán
Hay 9ầP
Tãng choiesteroi huyêt, táng lipid huyêt
Tăng triglyceride huyêt, đái tháo đường mới
khới phát
Rõi Ioạn mạch
Hay 9áp
Hiém gập
Tả huyẻt ặp, u nang bach huyêt ’, bộnh
huy tkhói tảc nghẽn tĩnh mach, huyêt khỏi
mảnh ghẻpJ
Viêm mach hùy bach cảu (ieukocytoclast
vasculitis)’
Rối ioạn hô hấp, ngưc vi trung thất
Rét hay gặp
Hay 9ăp
it gảp
Trản dịch mán phỏi²
Bệnh vièm ph i mô kẽ
Thảm nhập protein phế nang (pulmonary
aiveolar proteinosis)
Rới Ioụn tiộu hỏa
Hay 9ã1›
Đau bụng, tieu cháy. buôn nộn, viêm tuy. nộn,
Vièm de dảy/Ioét miệng
Rỗi Ioạn gan một
it 9áp
Viêm gan, rói ioan vẻ gan, váng da. xét nghiệm
chớc năng_gan bảt thướng'_
Rối loạn do vi mô dưới da
Hay gặp Phù thần kinh mach’, mụn trừng cá, bién
chứng ớ vết thương do phẫu thuật.
_l_tgập Ban
Rói ioạn hệ cơ xương vá mò Iién kột
ãĐ
Đau cơ
It
PỂẵi loạn thận vá tiẻt niệu
Thướng gặp:
Ít ập:
R 1 logn hộ einh ein vá tuyỎn vù
Protein niệua
Hoại từ óng thịn’, viêm thặn bẻ thận
[ Thường_gặ_pz
Thướn ặp ị Ròi ioan cương
Rỗi Ioạn chung vi tinh tnng tại chỗ đủng thuỏc
Phù, đau, chám lánh vét thương
' Tảc dung phụ thuộc Iiẻu dùng đã được xác đinh hoặc tản suất cao hơn đảng ké dã dược ghi
nhận. ở những bệnh nhân dang dùng 3 mglngảy.
² trong ghép tim
’ trong ghép thặn
' tăng Y-GT. AST, ALT
’ Nỏi bát ở những benh nhán đang dùng dòng thời các chát ức chế men chuyền angiotensin
ACE)
5 các phát hiện sau khi đưa thuóc ra thi tmờng
Ở cảc thử nghiệm lám sáng có đói chứng trong dó tỏng số 2.781 bệnh nhán dang dùng
Certican (1.5 mg hoặc 3 mglngáy) phói hơp với các thuóc ức chế miên dich khác đã du
theo dõi trong it nhất '! nám. tỏng còn có 2.9% phát triẻn bệnh lý ảc tinh. vởi 1.2% phát triZẳ
bệnh iỷ ác tinh ở da vá 0.40% phát tri n u bach huyết hoặc bệnh tãng sinh mò bach huyẻt
Các phản ửng phụ xảy ra có thẻ tủy thuộc vảo mức dò vả thời gian diều trị bằng thuỏc ức chè
miễn dich. Trong các nghiên cứu then chòi. creatinine huyêt thanh tảng thường được tháy
hơn ở những bệnh nhán dùng Certican phòì hợp vởi ciclosperin dù Iièu dang vi nhũ tương so
với những bénh nhán ở nhòm chứng. Tần suất chung của các phản ứng phụ giám cùng với
việc giảm Iièu ciclosporin dang vi nhũ tương (xem phân DƯỢC LỰC HỌC-Các nghiên cừu
iám sảng)
Dữ liệu về độ an toản của Cenican trong các thử nghiệm trong đó thuóc dược dùng cùng với
ciclosporin ơi giảm iiều tương tự vởi các dữ liệu dã đươc mô tả trong 3 nghiên cứu then chót
sử dụng ciclosporin dù Iièu. n oai trừ tãng creatinine it gặp hơn, giá trị trung binh vá trung vị
của creatinine huyêt thanh th p hơn trong các nghiên cứu phase ill khác Đã ghi nhán tỷ iệ
nhiẽm vìrus thảp hơn. chủ yéu lá nhiẽm virus CMV ở bènh nhán ghép tim vả ghép thận vả
nhiếm BK ở benh nhân ghép thán. vởi chế độ ơuèu tri ừc chẻ miền dich dưa tren Ceưtican
được khuyên cảo hiên nay (xem phần DƯỢC ĐONG HOC-Các nghiện cứu Iám sáng).
Cảc trường hợp bènh phổi mỏ kẽ, Iảm nghĩ đẻn viêm trong nhu mô phỏi (viêm phỏi) vảlhoác
xơ hóa khỏng do nhiễm trùng. mòt sỏ trườ hơp đưa dẻn tử vong. đã xảy ra ở những bệnh
nhán đang dùng rapamycins vả các dẫn xu t cùa chúng. kể cả Certican. Thòng thường tinh
trang nảy qua di sau khi ngưng Certican válhoác khi sử dụng thèm glucocorticoid
Thỏng bủo cho bác sĩ những tác dụng khòng mong muôn gặp phải khi sử dụng thuốc.
QUÁ LIÊU
Trong các nghiên cứu ở đòng vật. everolimus cho tháy khả nảng gáy dộc cập tinh tháp Chưa
quan sát thảy dòc tinh gảy từ vong hoặc dòc tinh nghiêm trong ở chuột nhăt hoác chuột cóng
được cho uóng các iiẻu đơn 2000 mglkg (thử nghiệm giời han)i
Chưa có nhiều kinh nghiệm về uá liều ở người Có mot trường hợp rièng lè uóng nhâm
1.5 mg everolimus ở mòt trẻ 2 tuẵi. nhưng chưa tháy các phản ứng có hai nảo. Các Iièu đơn
Ièn đén 25 m đã dược dùng cho những bènh nhán ghép tang có khả náng dung nap cấp
tính có thẻ ch p nhận đươc.
Nẽn khởi đâu bâng cảc biện phảp điều tri hỗ trợ chung trong tải cá tmởng hơp quá lièu.
DƯỢC LỰC HỌC
Everolimus. mòt chát ức chế tin hiệu táng sinh. phòng ngừa thải mảnh ghép cùng loải trong
các mỏ hinh nghiên cứu ở Ioải gám nhám vả dòng vật linh tnrờng khỏng phải người vẽ ghép
cùng Ioải Nó có tác dung ừc chẻ miên dich báng cảch ức chế sự táng sinh té báo T hoat hóa
kháng nguyên. do dó mờ ròng thèm clon. được ơnèu khiến bởi các interieukin đặc hiệu dói với
tế bảo T. vi dụ interieukin—Z vả interieukin—iả Everolimus ức chế con dường dẫn truyền tin
hiệu nội báo vón thường dẫn đén tảng sinh té bảo khi được kich hoat do sự gân kẻt cùa các
yêu tỏ táng trường té bảo T vác các thu thé. Sự ngán chặn con dường dãn truyền nảy do
everolimus Iảm cho cảc tế bảo bi ngừng lai ở giai đoan G. của chu kỳ tế bảo.
10
Ở mức phân từ, everolimus tao thảnh môt phức hơp với protein FKBP-12 của bảo tương. Khi
có sự hiện diện của everolimus thì sự phosphoryl hóa p70 86 kinase vốn kích thích bởi yếu tố
tảng trưởng bị ưc chê Vì sự phosphoryl hóa p70 SB kinase chịu sự kiếm soát của FRAP (còn
được gọi là m—TOR) phát hiện nảy gợi ý lả phức hợp everolimus- KFBP- 12 gắn vảo và do đó
lảm cản trở chừc nảng cùa FRAP FRAP lả một protein điều hòa chinh kiềm soát sự chuyền
hóa tăng trưởng vả tãng sinh cùa tế bảo; vì vậy sự mắt chức năng cùa FRAP gìải thich cho
việc ngừng chu kỳ tế bảo gây ra do everolimus.
Như vặy everolimus có cách tảo dụng khảo so vởi ciclosporin. Trong các mô hình ghép cùng
loái tiẻn'lâm sảng, sự kèt hợp everolimus vả ciclosporin có hiệu quả hơn so với dùng riêng
từng chảt.
Tác dụng của everolimus không bị giới hạn ở tế bảo T Nói chung everolimus ức chế sự tăng
sinh kích thích bởi yếu tố tăng trưởng cúa tế bảo cơ quan tao huyết vả tế bảo không phải cơ
quan tạo huyết như tế bảo cơ trơn machmáu. Sự tăng sinh tế bảo cơ trơn mạch mảu kỉch
thich bời yếu tố tãng trưởng. vốn kich hoạt do sự tồn thương tế bảo nội mô vả dẫn đến hinh
thảnh tân nội mạc mạch đòng vai trò chủ yếu trong sinh bệnh học của thải ghép mạn tính
Cảo nghiên cứu tìền lâm sảng với everolimus đã cho thắy sư ức chế hình thảnh tân nội mạc
mạch trong một mô hình ghép cùng Ioải đòng mạch chủ ở chuột cống.
Cảc nghiên cứu lảm sảng %
Ghép thận
Certican ở liều cố định 1.5 mglngảy vả 3 mglngảy phối hợp với các Iièu chuẩn ciclosporin
dạng vi nhủ tương và corticosteroid đă được nghiên cứu trong 2 thử nghiệm giai đoạn III ở
bệnh nhân mới ghép thận (8201 vả B251), Mycofenolate mofetil (MMF) 1g. 2 lầnlngảy đã
được dùng lảm chắt so sảnh. Đồng tiêu chỉ đánh giá chỉnh lả thảt bại về hiệu quả điều trị (thải
ghép cầp đă được xác định bằng sình thiết. mắt mảnh ghép. chết hoảc không theo dõi được)
vảo lủc 6 thảng vả mắt mảnh ghép. chết hoặc không theo dõi được vảo lúc 12 thảng. Nói
chung Certican khỏng kém hơn so với MMF trong cảc thử nghiệm nảy. Trong nghiên cứu
8201. tỷ lệ thải ghép cấp được chứng minh bằng sinh thiết lúc 6 thảng đối vởi nhóm dùng
Certican 1.5 mglngảy lá 21.6%. nhòm dùng Certican 3 mglngảy là 18.2% và nhóm dùng MMF
iả 23,5%. Trong nghiên cứu 8251, tỷ lệ nảy đối với nhóm dùng Certican 1.5 mg/ngảy là
17,1%. nhóm dùng Certican 3 mg/ngảy iả 20,1% vả nhỏm dùng MMF iả 23,5%.
Suy giảm chức nảng mảnh ghép cùng loải kèm vơi creatinine huyết thanh tăng thường được
quan sát thầy hơn ở những bệnh nhán dùng Certican phối hợp vởi ciclosporin dang vi nhủ
tương lièu đầy đủ so với bệnh nhân dùng MMF. Tác dụng nảy cho thầy iả Certican lảm tăng
độc tinh thận do ciclosporin.
Phân tích nồng độ thuốc-dược lực học cho thắy chức năng thận có thế được cải thiện khi
giảm mức tiêp xúc ciclosporin mả vẫn bảo tỏn hìệu quả nếu nồng độ đảy cùa everoiìmus
trong máu vẫn duy tri cao hơn 3 nglmL. Quan niệm nảy đã được xảc nhận sau đó trong 2
nghiên cưu Phase ill (A2306 vả A2307 bao gồm 237 và 256 bẻnh nhân tương ứng) được
đảnh gìá về hiệu quả và độ an toản của Certican 1 5 mg vả Certican 3 mg môi ngảy (đảy iả
liều khởi đầu; các liều kế tiếp dựa trên nồng độ đáy mục tiêu (CO)Z 3 ng/mL) phối hợp với
giám nồng độ tồn lưu cùa ciclosporin Trong cả hai nghiên cứu chức nảng thận được cải thiện
mã không ảnh hưởng đền hiệu quả.Tuy nhiên trong những nghiên cứu nảy. không có nhóm
so sảnh khỏng dùng Certican.
Nghiên cứu A2309 phase ill đa trung tâm ngẫu nhiên biết rõ tên thuốc có đối chứng đã
được hoản tầt trong đó 833 bệnh nhân mới được ghép thận được lựa chọn ngẫu nhiên dùng
hoặc một trong hai chế độ điều trị bằng Cehican, phân biệt bởi lièu dùng, kềt hợp vởi giảm
liẻu ciclosporin hoặc một chế độ điều trị chuẩn bắng natri mycophenoiate (MPA) + ciciosporin
và điều trị trong 12 tháng. Tầt cả bệnh nhân đều được điêu trị dẫn nhặp vởi basilixumab trươc
khi ghép tạng vả vảo ngảy thứ 4 sau ghèp tạng. Steroid có thể được sử dụng theo nhu cầu
sau ghép iạng.
11
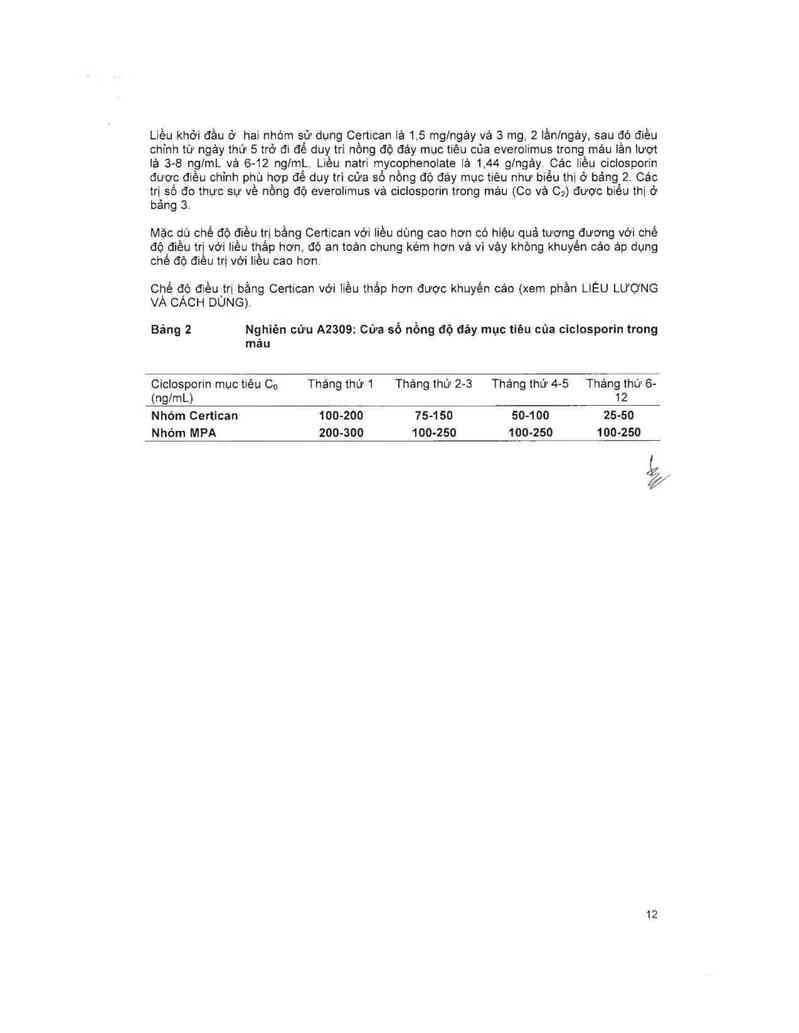
Liều khời đầu ở hai nhóm sử dụng Certican lả 1,5 mglngáy vả 3 mg. 2 iầnlngảy, sau đó điều
chỉnh từ ngảy thứ 5 trở đi để duy tri nồng độ đảy mục tiêu của everolimus trong mảu lần lượt
lả 3- 8 nglmL vả 6-12 ng/mL Liều natri mycophenolate iả 1 44 g/ngảy Các lièu ciclosporin
được điếu chỉnh phù hợp để duy trì cứa sô nông độ đáy mục tiêu như biều thi ở bảng 2 Các
trị số đo thực sự về nông độ everolimus vả ciclosporin trong mảu (Co vả C;) được biểu thị ở
bảng 3
Mặc dù chế độ điều t_rị bằng Certican vơi Iiều dùng cao hơn có hiệu quả tương đương với chế
độ điều trị với Iiêu thâp hơn. độ an toản chung kém hơn vả vì vậy không khuyên các ảp dụng
chế độ điều trị với iiều cao hơn.
Chế độ điếu tri bằng Certican với iiều thảp hơn được khuyên cáo (xem phần LIEU LƯỢNG
VÀ CÁCH DÙNG)
Bảng 2 Nghiên cứu A2309: Cứa số nồng độ đáy mục tiêu của ciclosporin trong
mảu
Ciclosporin mục tiêu Co Tháng thứ 1 Tháng thứ 2-3 Thảng thứ 4-5 Tháng thứ 6-
(nglmL) 12
Nhỏm Certican 100-200 75-150 50-1 00 25—50
Nhóm MPA 200-300 100-250 100-250 100-250
“\\ử“
12
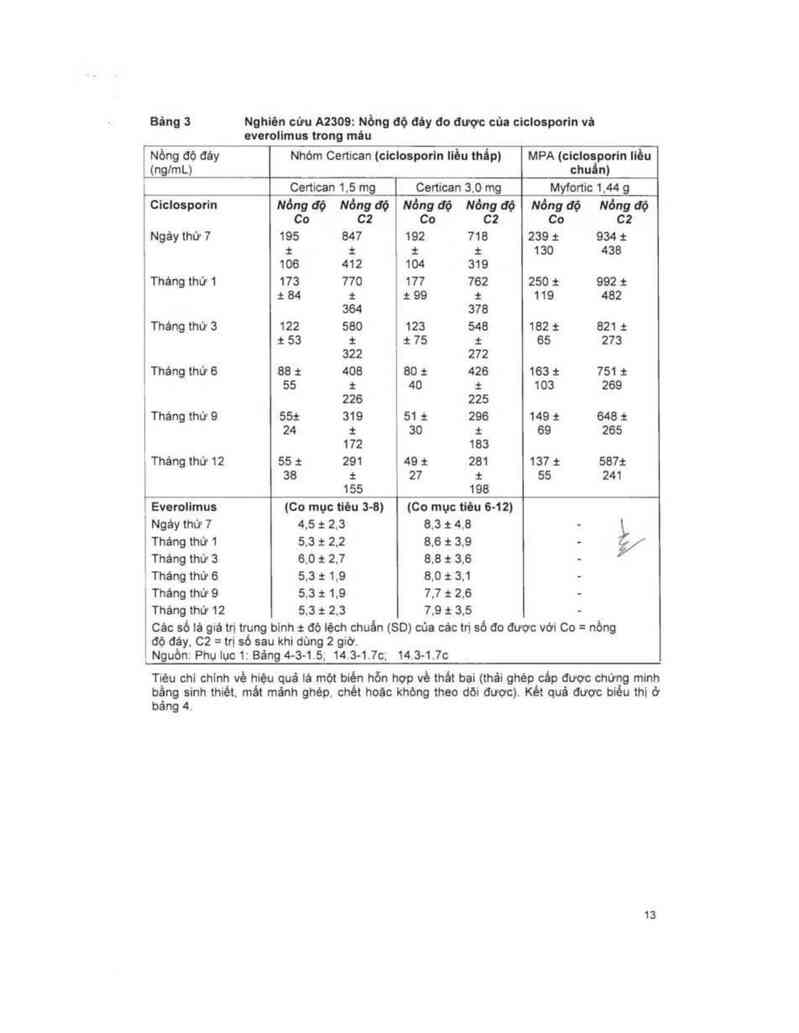
Bảng 3 Nghiên cữu A2309: Nồng dộ đủy đo được của ciclosporin vá
everolimus trong máu
Nòng đò đáy Nhóm Certican (clciosporln iièu thấp) MPA (ciclosporin ilều
(ngimL) chuẩn)
Certican 1,5 mg Certican 3.0 mg Myfortic 1.44 g
Ciclosporin Nông dộ Nông độ Nông độ Nóng độ Nông độ Nồng độ
Co 02 Cơ 02 Co 02
Ngảy thứ 7 195 847 192 718 239 :t 934 :
: t :: : 130 438
106 412 104 319
Tháng thứ 1 173 770 177 762 250 t 992 1
1 84 :t :t: 99 :|: 119 482
364 378
Thảng thứ 3 122 580 123 548 182 1 821 t
1 53 :t : 75 1 65 273
322 272
Tháng thứ 6 88 1 408 80 1: 426 163 1 751 t
55 t 40 1 103 269
226 225
Tháng thứ 9 55t 319 51 1 296 149 t 648 :1:
24 t 30 x 69 265
172 183
Tháng thứ 12 55 2 291 49 1 281 137 t 5871:
38 1 27 : 55 241
155 198
, Everolimus (Co mục tiẽu 3-8) (Co mục tiẽu 6-12)
Ngáy thứ 7 4.5 1 2.3 813 «x 4.8 -
Tháng thứ 1 513 1- 2.2 8.6 :t 3.9 . è
Tháng thứ 3 8.0 t 2.7 8.8 t 3,6 -
Thángthừô 5.3:t 1.9 8.0t 3.1 —
Tháng thứ 9 5.3 1: 1.9 7.7 : 2.6 -
Tháng thứ 12 5.3 : 2.3 7.9 :|: 3,5 -
Cảc sỏ lả giá trị trung binh : dó iệch chuẩn (80) của các tri só đo được với Co = nòng
ơo đáy, c2 = tri số sau khi dùng 2 giờ.
Ảuòn: Phụluc1:Bảng 4-3-15, 14.3…11c; 14.3-1.7c
Tièu chi chinh về hiệu quả lả một biên hõn hợp về thát bai (thải ghép cáp dược chừng minh
bảng sinh thiét, mảt mảnh ghép. chẻt hoãc khòng theo dỏi đươc). Kêt quả được biẻu thi ở
bảng 4.
13
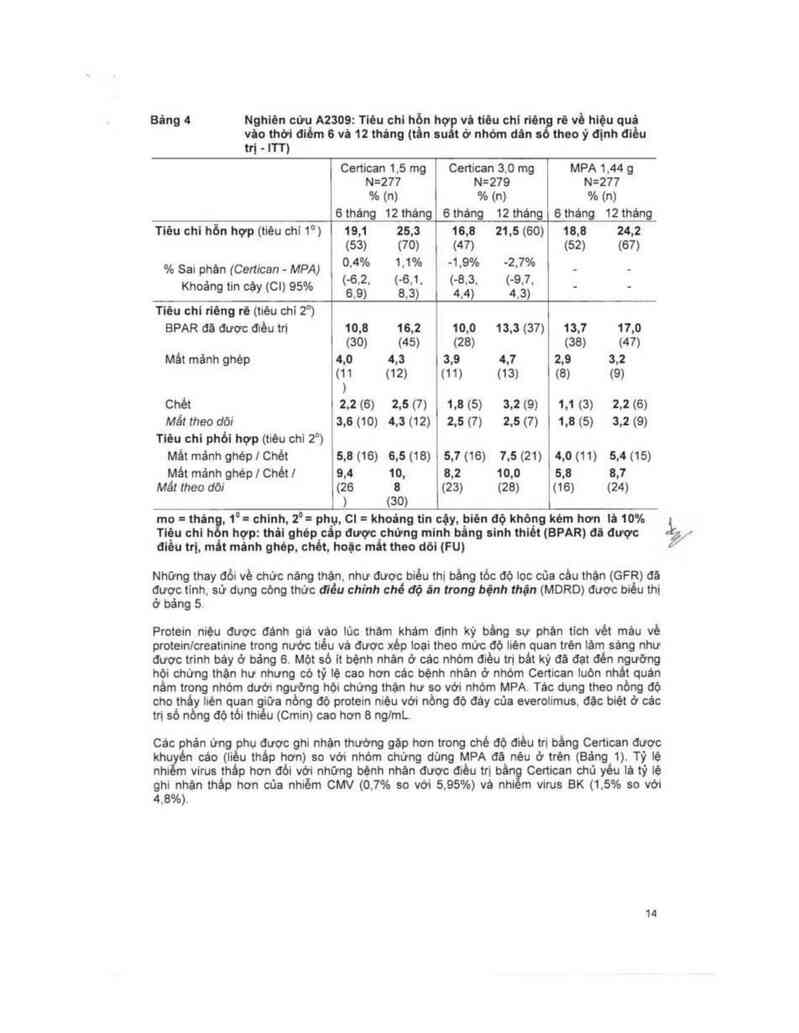
Bảng 4
Nghiđn cớu A2309: Tlèu chi hỗn hợf
vảo thớt điểm 6 vả 12 tháng itản ou t
vù tieu chi non rẽ vè hiệu quả
ở nhóm dân s theo ý định điều
tri - ITT)
Certican 1,5 mg Certican 3.0 mg MPA 1,44 g
N=277 N=279 N=277
% in) % tn) % (n)
6 tháng 12 tháng 6 thảng 12 tháng 6 tháng 12 thảng_
Tlẻu chi hỗn hợp (tiêu chỉ 1°) 19,1 25,3 16,8 21.5 (60) 18,8 24,2
(53) (70) (47) (52) (67)
% Sai phán (Certican - MPA) °_ểẳ° 1'6W" ’1'9% -2.m . .
Khoảng tin cáy (01) 95% (e.ẻ)' (8.ầ11' (Ểẵ' (Ỉàẫ' - -
Tiẻu chỉ riêng rẽ (tiêu chỉ 2°)
BPAR đã được điều tri 10,8 18.2 10.0 13.3 (37) 13,7 17,0
(30) (45) (28) (38) (47)
Mát mảnh ghép 4.0 4.3 3,9 4.7 2.9 3.2
(1)1 (1²) (11) (13) (8) (9)
Chét 2,2 (6) ²,5 (7) 1,8 (5) 3,2 (9) 1,1 (3) 2.2 (6)
Mải theo dói 3,8 (10) 4,3 (12) 2,5 (7) 2,5 (7) 1.8 (5) 3.2 (9)
Tièu chi phó! hợp (tiêu chỉ 2°)
Mát mảnh ghép ! Chét 5,8 (16) 6.5 (16) 5.1 (16) 1.5 (21) 4,0 (11) 5.4 (15)
Mất mảnh ghép I cnéu 9,4 10. 8,2 10,0 6,8 8,7
Mất theo dõi (26 8 (23) (28) (16) (24)
) (30)
mo = thán , 1° = chinh. 2°= phụ, C! = khoủng tin cịy. pièn độ khỏng kém hơn iâ 10%
Tièu chi h n hợp: thâi ghèp cấp được chứng minh bing oinh thiẻt (BPAR) đã được
điều trị, mất mânh ghẻp, chết. hoịc mẩt theo dõi (FU)
Những thay đòi về chức năng thận, như được biếu thi bẩng tỏc độ ioc của cảu thản (GFR) đã
được tinh, sử dụng còng thức đỉều chinh chế dộ in trong bệnh thận (MDRD) được biẻu thi
ở bảng 5
Protein niệu được đảnh giả váo Iủc thám khám đinh kỷ băng sự phân tich vét mảu vè
proteinlcreatinine trong nước tiếu vá được xép ioại theo mức độ liên quan trên iâm sảng như
được trinh bảy ở bảng 6. Mot sò it bènh nhán ở các nhớm điều tri bảt kỷ đã đai đẻn ngướng
hỏi ohứng thặn hư nhưng có tỷ lệ cao hơn cảc bènh nhản ở nhóm Certican luôn nhảt quán
nảm trong nhóm dưới ngướng hội chứng thân hư so với nhóm MPA. Tảc dụng theo nòng đó
cho thấy Iién quan giữa nồng đò protein nièu với nòng đò đáy cùa everolimus. đặc bièt ở các
tri sò nồng độ tói thiều (Cmin) cao hơn 8 ng/mL.
Các phản ửng phụ được ghi nhặn thướng gãp hơn trong chẻ đò fflèu tri bẳng Certican dược
khuyên các (iiều tháp hơn) so với nhóm chứng dùng MPA đã nẻu ớ tren (Báng 1). Tỷ lệ
nhiễm virus iháp hơn đói với những bệnh nhán được điều m bằn Certican chủ yếu iả tỷ lệ
ghi nhan tháp hơn của nhiễm CMV (0.7% so với 5,95%) vả nhi m virus BK (1.5% so với
4,8%).
14
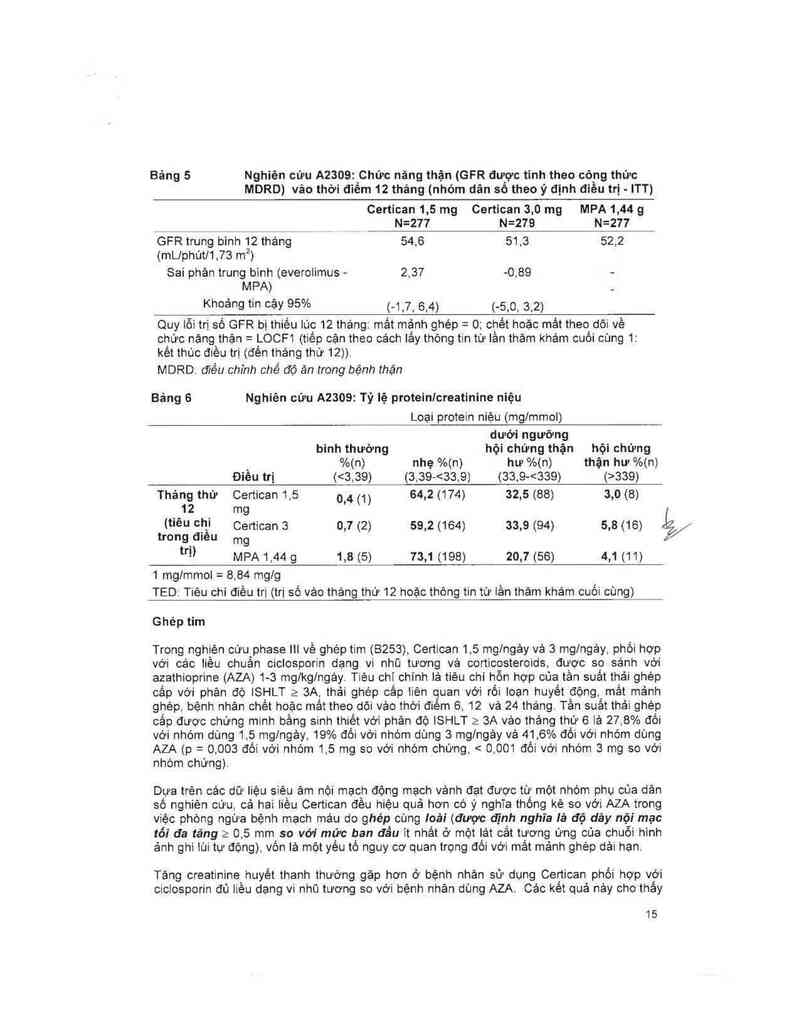
Bảng 5 Nghiên cứu A2309: Chức năng thận (GFR được tinh theo công thức
MDRD) vảo thời diềm 12 thảng (nhóm dân số theo ý định điều trị - ITT)
Certican 1,5 mg Certican 3.0 mg MPA1,44 g
N=277 N=279 N=277
GFR trung binh 12 tháng 54.6 51,3 52,2
(mL/phút/1,73 m²)
Sai phân trung bình (everolimus — 2,37 -0,89 -
MPA) -
Khoảng tin cậy 95% ("11.7 6 4) ( 5 o 3 2)
Quy lỗi trị số GFR bị thiếu lúc 12 tháng: mắt mảnh ghép= O; chêt hoặc mất theo dõi về
chức năng thặn - LOCF1 (tiềp cặn theo cách Iắy thỏng tin từ lần thăm khảm cuối cùng 1
kêt thúc điều trị( (đén thảng thứ 12))
MDRD. điều chỉnh chế độ ăn trong bệnh thận
Bảng 6 Nghiên cứu A2309: Tỷ lệ protein/creatinine niệu
Loại protein niệu (mg/mmol)
dưới ngưỡng
binh thường hội chứng thận hội chứng
` %(n) nhẹ %(n) hư %(n) thận hư %(n)
Điêu trị (<3,39) (3,39—<33,9) (33,9-<339) (›339)
Tháng thứ Certican 1,5 0,4 … 64,2 (174) 32,5 (88) 3,0 (8)
12 mg
(tiêu ==_h_i Certican 3 0,1 (2) 59,2 (164) sa,s (94) 5,8 (16) ệ/
trong điêu mg
"" MPA1,44 g 1,8 (5) 15,1 (198) 20,1 (56) 4,1 (11)
1 mg/mmol = 8,84 mg/g
TEDỊ Tiêu chỉ điều trị (trị số vảo tháng thứ 12 hoặc thông tin từ lần thám khám cuối cùng)
Ghép tim
Trong nghiên cứu phase III về ghép tim (8253), Certican 1,5 mg/ngảy và 3 mglngảy, phối hợp
với các iiều chuẩn ciclosporin dạng vi nhũ tương vá corticosteroids được so sánh với
azathioprine (AZA) 1 -3 mglkg/ngáy Tiêu chi chính lả tiêu chí hỗn hợp của tần suất thái ghép
cắp với phân độ iSHLT > 3A, thải ghép cắp Iièn quan với rối Ioạn huyết động, mất mảnh
ghép, bệnh nhân chêt hoặc mắt theo dõi vảo thời điếm 6,12 và 24 tháng Tần suất thải ghép
cắp được chứng minh bằng sinh thiẻt với phân độ ISHLT > 3A vảo thảng thứ 6 lá 27 8% đối
với nhóm dùng 1, 5 mglngảy 19% đối với nhóm dùng 3 mglngảy vả 41,6% đôi với nhóm dùng
AZA (p= 0,003 đối với nhóm 1,5 mg so vởi nhóm chứng, < 0,001 đối với nhóm 3 mg so với
nhòm chứng)
Dựa trèn các dữ liệu siêu âm nội mach động mạch vảnh đạt được từ một nhóm phụ cùa dân
số nghiên cứu, cả hai liều Certican đều hiệu quả hơn có ý nghĩa thống kê so với AZA trong
việc phòng ngừa bệnh mạch máu do ghép cùng Ioải (được dĩnh nghĩa la` độ dáy nội mạc
tối đa tăng 2 0, 5 mm so với mửc ban đầu 11 nhầt ở một lát cắt tương ứng của chuỗi hinh
ảnh ghi iùi tự động), vốn là một yếu tố nguy cơ quan trọng đối với mắt mảnh ghép dải han.
Tăng creatinine huyêt thanh thướng gặp hơn ở bệnh nhân sử dụng Certican phối hợp với
ciclosporin đú Iièu dạng vi nhũ tương so với bệnh nhản dùng AZA Các kêt quả nảy cho thảy
15
Certican lảm tãng độc tinh trẻn thặn do ciclosporin. Tuy nhiên, phân tich thêm cho thắy chức
nảng thận có thẻ được cải thiện vởi việc giảm liều ciclosporin mã không lảm mât hiệu quá
chừng nảo các trị số everolimus trong máu vẫn duy tri cao hơn ngướng đă nèu. Nghiên cứu
A2411 vả A2310 sau đó đã được tiến hảnh để điều tra điếm nảy.
Nghiên cứu A2411 là một nghiên cứu ngẫu nhiên trong 12 tháng, biết rõ tẻn thuốc, trong đó
Certican phối hợp với ciclosporin dạng vi nhũ tương giảm Iiẻu vả corticosteroid được so sánh
với mycophenolìc mofetil (MMF) vả ciclosporin dạng vi nhũ tương liều chuẩn vả
corticosteroids ở những bệnh nhân mới ghép tim. Nghiên cứu thu dung tồng số 174 bệnh
nhân Certican (N= 92) được khới đầu với liều 1, 5 mglngảy vả lièu nảy được điều chinh để
duy tri nồng độ đảy mục tiêu của everolimus trong máu giữa 3- 8 ng/mL Liêu MMF (N= 84)
khới đầu lả 1 500 mg, 2 lầnlngảy. Cảo Iièu ciclosporin dạng vi nhũ tương được điều chính đến
cảc nồng độ đảy mục tiêu sau đây (ng/mL):
Ciclosporin mục Tháng thứ Tháng Thảng thử Tháng thứ Tháng thứ
tiêu co 1 thứ 2 3-4 5-6 7-12
Nhóm Certican 200-350 150-250 100-200 75—150 50-100
Nhóm MMF 200-350 200-350 ( 200—300 150—250 100-250
Chức nảng thặn đã được cải thiện ở phác đồ giảm Iiều ciclosporin với độ thanh thải creatinin
trung binh (công thừc Cockcroft—Gault) lúc 6 thảng: Certican: 65,4 so với MMF: 72,2 mL/mn,
vả lúc 12 thảngt Certican: 68,7 so với MMF: 71,8 mL/mn. Hiệu quả, thể hiện iả tỷ lệ Thải ghép
cắp đã được chứng minh bằng sinh thiết với phân độ ISHLT z SA, đã được duy trị khi so
sánh hai nhóm lúc 12 tháng (Certican: 22,8% v MMF: 29 8%).
Nghiên cứu pha 3, đa trung tâm, ngẫu nhiên, nhãn mở A2310 so sánh về hiệu quả vả độ an
toản của hai chế độ điều trị: Iiệu trinh Certican/giảm liều ciclosporin so với liệu trinh tiêu chuẩn
mycophenoiat mofetil (MMF)]ciclosporin qua 24 thảng. Việc sử dụng iiệu phảp dằn nhập tùy
thuộc vảo từng trung tãm cụ thế, cảc Iưa chọn gồm có hay khỏng Iiệu pháp dẫn nhặp bằng
basiliximab hoặc thymoglobulin Tât cả cảc bệnh nhân đèu đã dùng corticosteroids.
Liều khởi đầu ở hai nhòm Certican lả 1, 5 mg/ngảy và 3 mglngảy, sau đó được thay đối từ
ngảy thứ 41rở đi để duy trì nồng độ đich everolimus trong máu ở mức lần lượt iả 3- 8 ng/ml và
6- 12 ng/ml Liều MMF lả 3 glngảy. Liều ciclosporin được điều chinh để duy trì cùng nồng độ
đich trong máu như trong nghiên cứu A2411. Nổng độ trong máu cùa everolimus vả
ciclosporin được trình bảy trong Bảng 7
Tuyến dụng cho thử nghiệm trên, nhóm điếu trị bằng Certican liều cao sớm kết thúc vì gia
tăng tỷ lệ tử vong trong nhóm điều trị nảy, do nhiễm trùng và các rối loạn tim mạch, xảy ra
trong vòng 90 ngảy đầu tiên sau nhóm phản ngẫu nhiên Nguyên nhân vả hình thái tử vong
trong nhóm liều nảy không cho thấy sự khác biệt có iiên quan đên sự có mặt cùa điều trị dẫn
nhặp.
So sánh thống kê được giới hạn để so sảnh giữa các nhỏm điều trị đã hoản thảnh. Mức nồng
độ cùa thuốc trong máu thực sự đat được được mô tả trong Bảng 7
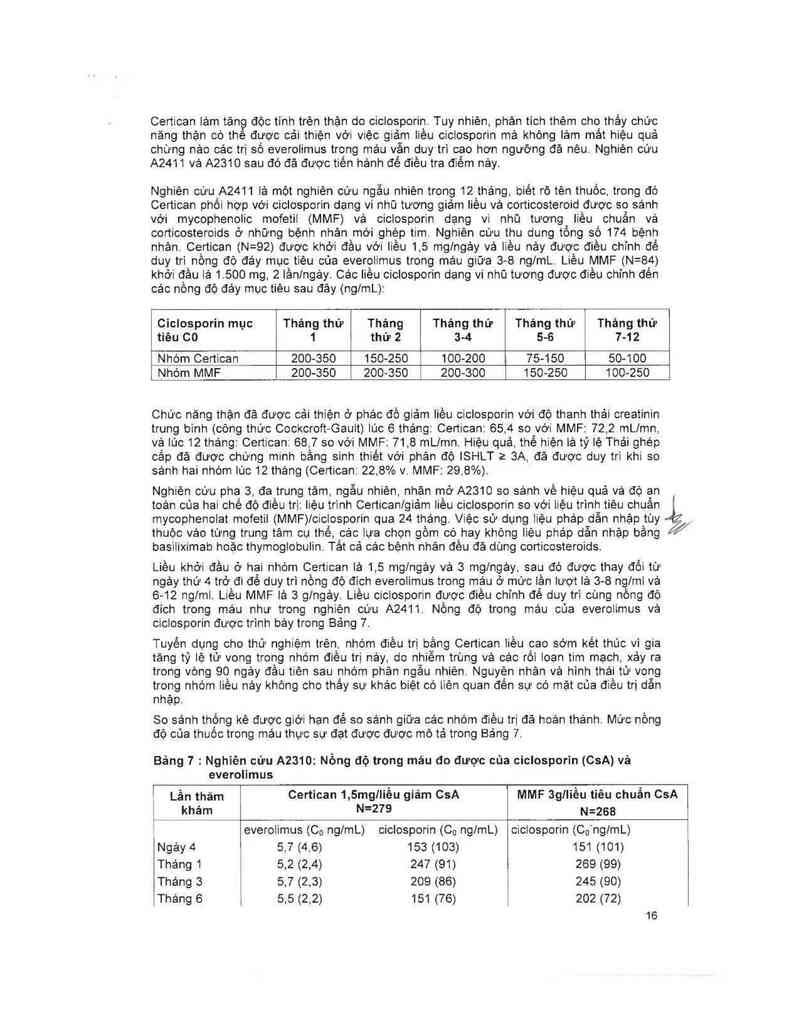
Bảng 7 : Nghiên cứu A2310: Nồng độ trong máu đo được của ciclosporin (CsA) vả
everolimus
' Lần thăm Certican 1,5mg/liều giảm CsA MMF 3glliều tiêu chuẩn CsA
khám N=279 N=268 :
everolimus (Co ng/mL) ciclosporin (Co ng/mL) ciclosporin (CựnglmL)
Ngảy4 5,7 (4,6) 153 (103) 151 (101)
Tháng 1 5,2 (2,4) 247 (91) 269 (99)
Thảng 3 5,7 (2,3) 209 (86) 245 (90)
Thảng 6 5,5 (2,2) 151 (76) 202 (72)
16
Lần thăm Certican 1,5mg/liều giảm CsA MMF 3glliểu tiêu chuẩn CsA
khám N=279 N=268
Tháng 9 5,4 (2,0) 117 (77) 176 (64)
Thảng 12 5,6 (2.5) 102 (48) 167 (66)
cảc số liêu nảy lá giá trị trung binh 4 SD cúa giả ưi đo dược cùa Cũ= nống độ dáy
Nguồn: PT-Bảng 14.3-1.5, PT- Bảng 146 — 17a
Tiêu chí đảnh giả tiên phát về hiệu quả lẻ một biến tổ hợp về thắt bai điều trị, bao hảm sự
xuất hiện của bầt kỳ những điều sau đây: đợt thải ghép câp được chứng mịnh bằng sinh thiết
(BPAR) với phản độ ISHLT >= 3A. đợt thải ghép cắp (AR) liên quan với rối loạn huyêt động
(HDC), mất mảnh ghéplghép iại, tử vong, hoặc mắt theo dõi. Hiệu quả lúc 12 thảng được thế
hiện trong Bảng 8
Bảng 8 Nghiên cứu A2310: Tỷ lệ kết cục về hiệu quả theo nhóm điều trị (Nhóm
dân sô nghiên cứu phân tich theo ý định điêu trị (ITT) - phán tich lúc 12
thảng)
Certican1,5mg MMF
N=279 N=271
Tiêu chỉ về hiệu quá 11 (%) n (%)
Tiên phátị Tổ hợp về thắt bại điêu trị 99 (35,1) 91 (33,6)
- Thái ghép cấp iiên quan với rối Ioạn huyết động 11 (3,9) 7 (2,6)
- Thải ghẻp cấp xảo định bằng sinh thiềt với phản độ 63 (22,3) 67 (24,7)
ISHLT >= 3A
… Tử vong 22 (7,8) 13 (4,8)
… Mắt mảnh ghéplghèp lai 4 (1,4) 5 (1,8)
— Mầt theo dõi ' 9 (3,2) 10 (3,7) <ề/
Thư phát:
- Mất mảnh ghép/ghèp lại, tử vong hoặc mất theo dõi " 33 (11,7) 24 (8,9)
Mầt theo dõi … 11 (3.9) 11 (4.1)
Thải ghép cấp được điều trị bằng khảng thể 13 (4 6) 9 (6,) 6)
Tổ hợp về thầi bại điều trị: cậc đợt thải ghép cẳp được xảo định bảng sinh thiêt với phản độ ISHLT >= 3A. thải
ghẻp câp (AR) Iiên quan với rối loạn huyết động (HDC), mắt mảnh ghèp/ghép lại tử vong, hoặc mầt theo dỏi.
“Mắt theo dõi về các tiêu chí liên quan (tiên phát hay thứ phát)
Nguồn: PT-Bảng 14.2-1 .1a
Tỷ lệ tử vong ở nhóm Certican tượng đối cao hơn nhóm MMF chủ yêu lả kềt quả của sự gia
tảng tỷ lệ tử vong do nhiễm trùng trong ba thảng đầu ở phân nhóm các bệnh nhân dùng
Certican được điều trị dẫn nhập bằng thymoglobulin. Tỷ iệ nhiễm khuẩn nặng trong 3 tháng
cao hơn một cách đảng chú ý ở bệnh nhản dùng Certican so với MMF trong phản nhóm dùng
thymoglobulin đã phản ánh hiệu lực ức chế miễn dịch cao hơn. Sự mất cản bằng về tử vong
trong nhóm thymoglobulin đặc biệt rõ rảng trong số cảc bệnh nh_ản nhập viện trước ghi ghép
tạng và có thièt bị hô trợ tảm thảt trải, cho thảy khả nảng bị tôn thương lớn hơn ở những
bệnh nhân như vậy với hậu quả của biến chứng nhiễm khuẩn
Nghiên cứu với siêu ảm nội mạch đã được thực hiện trèn một phân nhóm bệnh nhân để tìm
hiếu vệ sự thay đối độ dảy nội mạc bèn trong một đoạn của nhánh động mach vánh xuống
trước bên trái (LAO) (so sảnh thay đối tương đối cùa giá trị lúc 12 thảng với giá trị ban đầu
được thu thập trong 3 tháng đầu sau ghép).Cảc kết quả về sự thay đổi đo được về độ dảy nội
mạc tối đa cùng với tỉ_lệ bệnh nhản bị bệnh lý mạch mảu sau ghép tim cùng loải (xác định
bằng độ dảy nội mạc tôi đa tăng O,5mm hay hơn nữa) được mô tả trong Bảng 9.
17
Báng 9: Sự thay đồi về trị số trung binh của độ dảy nội mac tối đa (mm) từ ban đằu
cho đên sau 12 tháng vả tỉ lệ bị bệnh lý mạch máu sau ghép iim cùng ioải
(Cardiac Allograft Vasculopathy: CAV) theo bệnh lý của ngưới hiến tạng vá
theo điều trị- phản tich lúc 12 tháng
Certican 1,5mg MMF | Giá trị p của testt
N=88 N=101 ( (Certican so với
( MMF)
Thay đôi vê trung binh cùa độ dảy nội mạc tỏi da (mm) từ ban đẩu cho đển lủc 12 tháng
Trung binh (độ lệch chuẩn) 0,03 (0,05) 0.07 (0,11) <0,001
_ Trung vị (khoảng) 0,02 (-0,12, 0,19) 0,03 (-0,15, 0,56)
Bệnh lý mạch máu sau ghép tim cùng loải (CAV) theo bệnh lý của ngưới hiên tạng vả
theo điều trị
Bệnh lý của ngưới hiên [ nlM (%) nlM (%) nIM (%)
Tồng số 1 11788 (12.5) 277101 (26,7) o,o1a
Người hiển có bệnh , 10742 (23,8) 24754 (44,4) 0.052
Người hiến không có bẻnh 1l46 (2.2) 3147(6,4) 0,617
Giá irị ban dâu cùa síẽu âm nội mạc được được thực hiện cho đến ngảy 105
Giá trị p về thay đổi so với ban đằu được so sánh với mức độ có ý nghĩa 0, 025 ở cả hai phia.
N - số bệnh nhân với 1 biến cố cúa bệnh lý mạch máu sau ghép tim cùng loải có nguời hiến iạng có bệnh; M —
tông số bệnh nhân có người hiến tạng có bệnh.
Tinh trạng tăng độ dảy nội mạc mạch vảnh được giảm đi ở bệnh nhản dùng Certican tương
đối tốt hơn so với bệnh nhân dùng MMF rõ rảng lá không phụ thuộc vảo tuối, giới tinh, có đái
tháo đường hay khỏng vả nồng độ cholesterol huyềt thanh tồi đa quan sảt được ở tháng thứ
12.
Trong suốt quá trinh cùa nghiên cứu A2310, chức năng thận, được đánh giá bằng độ lọc cầu
thận (GFR) ước tỉnh theo công thức MDRD thâp hơn có ý nghĩa thống kê lả 5,5
mL/phút/1JSm2 (khoảng tin cặy 97, 5% lá -10, 9; -0 2) ở nhom everolimus 1 5mg vảo tháng
thứ 12 ả
Dữ iiệu gợi ý rằng sự khác biệt quan sát được chủ yếu Iiẻn quan với nống độ tồn lưu của
ciclosporin. Sự khác biệt được giảm xuống còn 3, 6 mL/phủi/1,7Sm² vả không có ý nghĩa thống
kê (khoảng tin cậy 97, 5% 16 -8,9; 1,8) ở những trung tâm mả nồng độ ciclosporin trung bình ở
nhóm bệnh nhân dùng Certican thảo hơn ở nhóm được phản ngẫu nhiên lám đối chứng, như
đã được khuyến cáo
Hơn nửa, sự khác biệt chủ yếu phát sinh trong tháng đầu iièn sau ghép khi mả tinh trạng
huyêt động của bệnh nhân vẫn còn chưa ốn định vốn có thể lả yếu tố gây nhiễu cho việc
phân tich chức năng thận. Sau đó, mức giảm cúa độ lọc cầu thận từ thảng thứ 1 đên thảng
12 ở nhóm everolimus nhỏ hơn đáng kể so với nhỏm chứng (6,4 so với -13 ,7mL/phút,
p= -0 ,.002)
Đạm niệu, biều thị bằng nồng độ creatinin niệu : protein niệu đo từ mẫu nước tiểu tại chỗ, có
khuynh hướng cao hơn ở bệnh nhân được điều trị bầng Certican. Giá trị dưới ngưỡng thặn
hư được quan sải thảy ở 22% các bệnh nhân dùng Certican so với 8,6% các bệnh nhân
MMF. Các mức độ thặn hư cũng được báo cáo (0,8%), tương ứng với 2 bệnh nhản ở mỗi
nhóm điều trị.
18
Cảo phản ứng bất iợi ở nhóm everolimus 1 5,mg trong nghiên cưu A2310 nhảt quán với các
phán ứng bất lợi của thuốc được trinh bảy ớ Bảng 1 Tỉ lệ nhiễm siêu vi thấp hơn ở các bệnh
nhân điều trị bằng Certican chủ yêu bắt nguôn từ tỉ lệ nhiễm trùng CMV được bảo các thắp
hơn MMF (7, 2% so với 19 ,.4%)
DƯỢC ĐỘNG HỌC
Hâp thu
Nồng độ đinh của everolimus đạt được 1-2 giờ sau khi dùng một liều uống. Nống độ
everolimus trong máu ở bệnh nhân ghép tỷ lệ theo iiều ở mức liều 0, 25- 15 mg Sinh khả dụng
tương đối của viên nén phân tán so với viên nén thông thường lả 0,90 (0, 76- 1,,07 khoảng tin
cặy 90%) dựa trẻn tỷ số dìện tich dưới đường cong nồng độ (AUC)
Tảo dụng của thức ăn: Nổng độ cao nhắt trong huyết tương giảm 60% vả diện tich dưới
đường cong nồng độ của everolimus giảm 16% khi thuốc được dùng với bữa ản giảu chắt
béo Đề lảm giảm thiều sự biến thiên, nên Iuòn dùng Certican với thức ăn hoặc luôn dùng
không có thức ản.
Phân bô
Tỷ số everoiimus trong mảu- -huyết tương phụ thuộc vảo nồng độ ở mức 5-5000 ng/nL là 17%-
73% Sư gắn kết với protein huyết tương khoảng 74% ở ngưới khỏe mạnh vả bệnh nhân suy
gan trung bình Thể tích phản bố Iiẻn quan với giai đoạn cuội (VZIF) ở bệnh nhản ghép thặn ở
giai đoan duy tri lả 342 : 107 L
Chuyên hóa
Everolimus iả một cơ chắt cúa CYP3A4 vả P- g-lycoprotein. Cảo đường chuyển hóa chinh
được nhận biết ở người lá mono- hydroxyl hòa và O—dealkyi hóa 2 chât chuyền hóa chỉnh
được hinh thảnh do sự thủy phân lactone vòng Everolimus lả một thảnh phần chinh lưu
thông trong máu Không có chải nảo trong hai chắt chuyến hóa chính có thể góp phần đáng
kể vảo hoạt động ức chế miễn dịch của everolimus. ị
Bải tiêt
Sau khi dùng một liều đơn everolimus có gắn phóng xạ trên những bệnh nhân ghép tạng
đang dùng ciclosporin, hầu hết phóng xa (8 0%) được phát hiện trong phân, và chỉ một lượng
nhỏ (5%) được bải tiết trong nước tiều Không phảt hiện được thuốc ban đằu trong nước tiểu
hoặc phản
Dược động học ở trạng thái ổn định
Dược động học giống nhau ở bệnh nhân ghép thặn và ghép tim dùng everolimus 2 Iầnlngảy
cùng với ciclosporin dạng vi nhũ tương. Trạng thái ồn định đạt được sau 4 ngảy, với sự tích
iủy nồng độ thuốc trong mảu gảp 2— 3 lần khi so với sự tồn lưu thuốc sau khi dùng liều đầu
tiên. Thới gian đạt được nồng độ cao nhất trong huyết tương (T……) xảy ra 1 -2 giờ sau khi
dùng thuốc Ở Iiều 0, 75 mg, 2 Iầnlngảy, nống độ cao nhắt trong huyết tương (Cmax) trung binh
là 11 1 1 4,6, ở liều 1 5 mg, 2 iần/ngảy, Cmax trung binh là 20,3 & 8 nglmL, vá diện tĩch
dưới đường cong nồng độ (AUC) trung binh lả 75 1 31 ngogiờ/mL ở iiều 0,75 mg 2 lần/ngảy
vả AUC trung bình lả 131+ 59 ngogiớlmL ớ lièu 1, 5 mg, 2 iầnlngảy. Ờ Iièu 0,75 mg, 2
iầnlngảy, nỏng độ đáy trong mảu trước khi dùng thuốc (C……) trung binh lả 4, 1 + 2 1 nglmL vả
ớlièụ 1 ,5 mg 2 iần/ngảy, Cmm trung binh là 7,1 i 4, 6 ng/mL Nồng độ everolimus tồn lưu vẫn
giữ ốn định theo thới gian trong năm đầu sau khi ghép. C…… có iiên quan đáng kể với AUC,
tao ra một hệ số tương quan giữa 0,86 và 0,94 Dưa trên phân tích dược động học ở nhóm
nghiên cưu, hệ sô thanh thải đường uống (CL/F) là 8,8 ngiớ (độ biên thiên giữa cảc bệnh
nhân lẻ 27%) vả thẻ tich phản bố chủ yêu (Vclf) lả 110 L (độ biên thiên giữa các bệnh nhảm lẻ
36%). Độ biến thiên còn lại về các nông độ trong mảu iả 31%. Thời gian bản thải là 28 + 7
giờ
Suy gan
19
So với điện tich dưới đường cong (AUC) của everolimus ở những ngưới cớ chừc nẽng gan
binh thướng, AUC trung binh của 7 bènh nhán suy gan nho (chỉ số Chiid-Pugh nhóm A) cao
hợn 1,6 Iản; diện tich dưới đường cong nòng độ (AUC) trung binh ở 2 nhòm gòm 8 bệnh
nhân suy gan tmng binh (chi sỏ ChiId—Pugh nhỏm B) được nghiên cữu độc lập cao gáp 2,1 vả
3,3 Iân;AUC trung binh ở 6 bẻhh nhan suy gan nặng (chi 66 Child-Pugh nhóm C) táng cao
hơn 3,6 lần Đói với bộnh nhân suy gan nhe (chỉ số Chlid-Pugh nhòm A) Iièu dùng nen giảm
còn 213 liều thỏng thướng. Đói với bệnh nhán suy gan vừa vả nặng (chi 66 ChiId-Pugh nhóm
6 hay C) iiều dùng nẻn giám còn một nữa iiều thòng thướng Các điều chinh Iièu hơn nữa
nèn dưa trèn theo dđi nòng độ thuỏc trong máu (xem phản Liều iượng vả cách dùng).
Suy thịn
Suy thận sau khi ghép (hệ số thanh thái Creatinine Cicm= 11—107 lephủt) khộng ánh hướng
đẻn được động hoc cùa everolimus.
Trẻ cm
Hệ số thanh thải đường uóng CL/F cùa everolimus tăng tuyên tinh với tuỏi cùa bènh nhản (1—
16 iuỏi), điện tich bề mệt cơ thẻ (0,49-1,52 m²) vả cán nặng (11—77 kg). cư ở trang thái ón
định lá 10.2 2 3 ngiớlm vả thới gian bán thải lả 30 2 11 giớ. 19 bệnh nhi (1—16tuỏi) mới ghép
thận đã dùng Certican dang viên nén phán tán với liều 0,8 mg7m² (tói đa 1.5 mg) 2 lânlngảy
với ciclosporin dang vi nhũ tương. Những bènh nhi nảy đai được AUC của everolimus lẻ 87 :
27 ngogiớ/mL giông với ngưới lớn dùng 0,75 mg, 2 Iảnlngảy. Nòng độ đáy (CO) ở trang thái
ỏn đinh lả 4.4 : 1.7 nglmL.
Người cco tuđi
Sư giảm giới han về hệ số thanh thải đường uống của everolimus lả 0.33% mõi nảm được
ước tinh ở ngưới lớn (mức tuỏi đã nghiên cứu 18 16-70 tuỏi). Khong cần xem xét điều chinh
liều.
Chủng tộc
Dưa trẻn phản tich về dược động hoc ở nhóm nghiên cừu, hệ 56 thanh thải đường uỏng
(CL/F) về trung binh cao hớn 20% ở bệnh nhán da đen ghép tạng (xem phấn Liều lượng và
cách dùng).
Mói Iiõn quan giữa nòng độ thuốc tòn iưu vá đủp ứng
Nòng đò đá (CO) trung binh cùa everolimus sau khi ghép 6 tháng đâu có iiện quan với tỷ iè
thải ghép c p đã được xảc định bấng sinh thiét vả với tỷ 16 giảm tiêu cầu ở bènh nhán ghép
thản vè ghẻp tim (xem Bảng 10)
Bảng 10
Ghép thận
Nòng độ đáy (CO) (ng/mL) s 3,4 3,5-4,5 4.6-5,7 5.8-7.7 7,615.0
_ Khỏng bị thải ghép 66% 61% 66% 81% 91%
Giám tiếu cảu (< 160 x 10% 9% 7% 14% 17%
10°7L)
Ghép tim
Nồng đò đáy (CO) tnglmL) s 3.5 3,6-5,3 5,4-7,3 7,4-1o,2 10.3—21,8
Khòng bi thải ghép 65% 69% 80% 65% 65%
Giám tiếu cầu (< 75 x 10°7L) 5% 5% 6% 8% 9%
cAc Dữ LIỆU AN TOẦN TIÊN LÂM SÀNG
Dữ liệu an toán tiền iám sáng cùa everolimus đã được đảnh giá ở chuột nhắt. chuột cóng, lợn
con, khi vả thỏ. Cảo cơ quan đich chinh lả hộ sinh sán ớ gióng đưc vá cái (thoái hóa tiểu
quăn tinh hoản, giảm lượng tinh trùng trong teo mảo tinh hoản vả teo tử cung) ở nhiều Ioâi, vá
20
/
\’ ( .'.1,
chí ở chuột cống lá ở phồi (tăng đại thưc bảo ở phế nang) vả mắt (đục đường khớp trước cúa
thủy tinh thế) Những thay đối nhỏ ở thận gặp ở chuột cống (tăng cao lipofuscin ờ biểu mộ
ông thặn liên quan đến tuồi giả vả lảm nặng thêm các tồn thương có sẵn ở chuột nhắt). Chưa
thầy độc tinh với thận khi hoặc lợn con
Everolimus dướng như lảm nặng thêm các bệnh có sẵn một cách tự phát (viêm cơ tim man
tinh ở chuột cống, nhiễm virus coxsackie ở huyêt tương và tim của khi, nhiễm ký sinh trùng
coccidium ở đường tiêu hóa của lợn con, tồn thương da ở chuột nhắt vả khỉ) Những phảt
hiện nảy thướng quan sảt thắy ở cảc nồng độ thuốc tồn lưu toản thân trong mức thuốc tồn
lưu khi điều trị hoặc cao hơn, ngoại trừ cảc phảt hiện ở chuột cống xảy ra dưới mức thuốc tồn
lưu khi điều trị do sự phân bộ cao vảo các mô
Ciclosporin phối hợp với everolimus đả iảm tăng nộng độ everolimus tồn lưu toản thân vả
tảng độc tính. Chưa có cơ quan đich mới ở chuột công. Trèn khi đã thấy xuất huyêt và viêm
động mạch ở một vải cơ quan.
Trong một nghiên cứu về sinh sản ở chuột cống đực. hinh thái học của tinh hoản bị ảnh
hưởng ở iiều o, 5 mglkg vá cao hơn, sự chuyến động cùa tinh trùng, số iượng tinh trùng vả
nòng độ testosterone trong huyêt tượng bị giảm ở liều 5 mg/kg trong mức cùa lượng thuốc
tồn lưu khi điều trị vả gây ra giảm khả nảng sinh sản ở giống đực. Có dắu hiệu vè tinh thuận
nghịch. Vô sinh ở giống cái không bị ảnh hướng, nhưng everolimus đi qua _nhau thai vả gặy
độc đối với thai. Ở chuột cống, everolimus gặy độc cho phôilthai ở mức nồng độ thuốc tồn
lưu toản thân dưới mức tồn lưu khi điều trị, biều hiện dưới dạng tử vong vả giảm trọng lượng
thai Tỷ iệ thay đồi ở bộ xương vả dị dạng tăng lèn ở iiều 0 ,3 vả 0,9 mglkg (ví dụ khe hở
xương ức). Ở thò, thầy rỏ độc tinh phòi do tăng tiêu phôi giai đoạn cuối.
Cảo nghiên cưu về độc tinh gen bao gồm các tiêu chí về độc tinh gen iièn quan cho thây
không có dấu hiệu gây đứt gãy nhiễm sắc thể hoặc gây đột biến. Sử dụng everolimus đên 2
năm khõng thầy bầt kỳ khả năng gây ung thư nảo ở chuột nhắt vả chuột cống cho đến cảc
Iièu cao nhầt tương ứng với 8,6 lần và 0,3 lần cùa nồng độ thuốc tồn lưu ước tinh trên lảm
sang.
TƯỞNG KY Ệg/
Chưa được ghi nhận.
HẬN DÙNG
36 thảng kể từ ngảy sản xuất.
BẢO QUÀN
Không b_ảo quản trên 30°_C. '
Giữ thuỏc trong bao bì gôc để tránh ánh sáng và tránh ảm.
Để thuốc xa tảm tay vả tầm nhin của trẻ em.
Không dùng Certican quá hạn sử dụng được ghi “EXP" trẻn bao bỉ.
QUY CÁCH ĐÓNG GÓI
Certican 0,25 mg: Hộp 6 ví x 10 viên nén.
Certican 0,5 mg: Hộp 6 vĩ x 10 viên nén.
Certican 0,75 mg: Hộp 6 vi x 10 viên nén.
Certican 1,0 mg: Hộp 6 vỉx 10 viên nẻn.
21
TIÊU CHUÃ_N
Nhã sản xuât
NHÀ SẢN quT
Novartis Pharma Stein AG
Schaffhauserstrasse
CH-4332 Stein,
Switzerland
Cho Novartis Pharma AG, Basel, Switzerland
Tờ hướng dẫn sử dụng cho quốc tế
Ngảy phát hảnh thông tin: 23 thảng 1 năm 2012
® = Nhản hiệu đã đăng ký
/M
77_u THÀNH …
om DIỆN
LOUIS—GEORGES LASSONNERY
Chiet Representative
The Hepresentative Office of
Novaíís Pharma Sanices AC in HCMC
22
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng