










BỘYTh
CỤC QUÁN u“ Di"ỢC
»
ẵ)ỉJ "’x Ẹ’i`
Lim điu/ÉZỔ
:,
`
1
J
ĐA PH1
ay
\,ểổb
ải Se c! ….ÉỂ Ế
.::oẫẫẵ :ub.
xnồ oc. % 3un: nẫ nnz % nãui?
na. n.…Mĩ :aư ẵể.
Dũnư oễ :Ễnẵ nơỂõ?
wỂn ơn.…ẵ uoeni
Do :u. :nnnn
m—Rn …: si E…mãb. unnưunn …: oai. ỉ uỗỉn. :oẵ ..03.
.:Ổ (ỉỉ 3l< ưa nỡẵA Ẻ.uìo .:n nẵn: #: :…. ỉ … nu :: N :uum
ỗumEEumổ
.EỀ. oS
,…cocE )
100% 50%
95% 5%
PROFILE
_927
12
20 ,
«w '.A
` “ n
² D Ì
RA8700 OS S10 REF10.0IJulyZO13
S-OS SmPC-MKSS1G-SOi-OTZO1B
THÔNG TIN SẢN PHẦM
sugammadex 100 mg/mL
Đọc kỹ hướng dẫn sử dụng !rước khi dùng.
Nếu cần rhêm thông n'n xin Iiẽn hệ vói bác sĩ hoặc dược sĩ.
Thông báo cho bác sĩ các tác dụng không mong muổn gặp phái khi sử dụng thuốc.
Đế !huốc xa tẩm vói của trẻ em.
1. TÊN THUỐC:
Bridion 100 mng dung dịch tiêm.
z. THÀNH PHÀN
] ml chứa sugammadex natri tương đương với 100 mg sugammadex.
2 ml chứa sugammadex natri tướng dương với 200 mg sugammadex.
5 ml chứa sugammadex natri tương đương với 500 mg sugammadex.
Danh mục tả dược đầy đù, xem mục 6.1 Danh mục tả dược
Mỗi ml chứa 9,7 mg natri (xem phần 4.4.Cảnh bảo và thận trọng đặc biệt khi sử dụng).
3. MÔ TẢ
Dung dịch tiêm.
Dung dịch trong suốt, không mảu đến mảu vảng nhạt.
pH từ 7-8 và dộ thầm thắu từ 300-500 mOsm/kg.
4. CÁC ĐẶC TÍNH LÂM SÀNG:
4.1.Chỉ định điều trị: ịfư
Hóa giải phong bể thẳn kinh cơ gây ra bởi rocuronium hoặc vecuronium.
Đối với nhóm bệnh nhi: chi khuyên dùng sugammadex dể hóa giải phong bế thần kinh cơ thông thường gây ra
bởi rocuronium ở trẻ em và thanh thiểu niên.
4.2.Liễu lượng vả cách dùng
Sugammadex chỉ nên được dùng bới hoặc dưới sự giảm sát oùa bảo sĩ chuyên khoa gãy mê. Nên sử dụng kỹ
thuật theo dõi thần kinh cơ thich hợp để theo dõi sự hối phục cùa phong bế thần kinh cơ. Như thực hảnh thông
thường sau gây mê sử dụng phong bế thần kinh cơ, cần theo dõi bệnh nhân ngay trong giai đoạn hậu phẫu đề
phát hiện cảo biền hiệu bất thường bao gồm tái xuất hiện phong bế (xem 4.4.Cảnh báo vả thận rrọng đặc biệt
khi sử dụng). Nên theo dõi cảc dấu hỉện tái phong bế ở những bệnh nhân được dùng đường tiêm một vải thuốc
trong vòng 6 giờ trước khi dùng sugammadex mã có thể gây tương tảo thay thể (xem 4.4.Ca'nh bảo và lhận
trọng đặc biệt khi sử dụng vả 4.5 T ương tác thuốc).
Liều đề nghị cùa sugammadex phụ thuộc vảo mức độ hóa giải phong bế thẳn kinh cơ.
Liều đề nghị nảy không phụ thuộc vảo phương pháp gây mê.
Có thể dùng sugammadex đề hóa giải cảc mức độ khảo nhau oùa phong bế thẳn kinh cơ gây ra bới rocuronium
hoặc vecuronium:
Người Iởn
Hóa giải thông thường: Nên dùng một liều sugammadex 4 mg/kg nếu sự hóa giải dạt được ít nhẩt 1-2 phản
ứng sau co cứng (post-tetanic count-PTC) sau sử dụng roouroninm hoặc vecuronium gây phong bế. Thời gian
trung bình để hồi phục tỷ lệ T4le đến 0,9 là khoảng 3 phút (xem 5.1. Dược động học)
› a
RA8700 08 510 REF10.0IJUIyZO1S
S-OS SmPC-MK8G1 6-SOi-07201 3
Nên dùng một liều sugammadex 2 mg/kg nếu hồi phục tự phảt xuất hiện cho dến khi ít nhất tải xuất hiện T2
sau sử dụng rocuronium hoặc vecuronium gây phong bế. Thới gian trung bình để hồi phục tỷ lệ T4/Tl đến 0,9
là khoảng 2 phùt (xem 5.1. Dược động học).
Sử dụng những liếu đề nghị như trên đề hóa giải thông thường sẽ gây tăng nhẹ thời gian tỷ lệ T4lTl dến 0,9
khi phong bế thẩn kinh cơ bằng roouronium so với vecuronium (xem 5.1. Dược động học).
Hóa eiải tức thì sư phong bể do rocuronium: Nếu về mặt lãm sảng cần hóa giải ngay tức thì sau khi dùng
rocuronium, nên dùng một liều sugammadex 16 mg/kg . Khi sugammadex 16 mg/kg được sử dụng 3 phủt sau
một liều tải rocuronium bromide 1,2 mg/kg, thời gian trung bình để đạt được hồi phục tỷ lệ T4lTl đến 0,9
khoảng 1,5 phủt (xem 5.1. Dược động học).
Chưa có dữ liệu để hướng dẫn sử dụng sugammadex để hóa giải tức thì phong bế thần kinh cơ sau khi dùng
vecuronium.
Tái sử dung sngammadex: Trong trường hợp ngoại lệ tải xuất hiện phong bế thằn kinh cơ sau phẫu thuật (xem
4.4.Cảnh báo vả thận trọng đặc biệt khi sử dụng) sau khi dùng liều khới đẳu sugammadex 2 mg/kg hoặc 4
mg/kg, nên dùng lại một liều sugammadex 4 mg/kg. Sau iiều sugammadex thứ hai, nên theo dõi bệnh nhân
ohặt chẽ dề dảm bảo duy trì sự hồi phục chức nãng thẳn kinh cơ.
Tải sử dung roouronium hoăc vecuronium saư khi dùng sueammadex: `Về thời gian chờ để tải sử dụng
rocuronium hoặc vccuronium sau khi hóa giải bãng sugammadex (xem phân 4. 4.Cánh bâo vả rhận trọng đặc
biệt khi sử dụng.) L/
Thỏng tin bổ sung cho nhóm bệnh nhân đặc biệt
Suy thân: Đối với suy thận nhẹ và trung bình ( độ thanh thải creatinine a 30 vả < 80 mL/phủt): liều đe nghị
tương tự như lỉều dùng cho người lớn.
Không nên dùng sugammadex cho những bệnh nhân suy thận nặng [kể cả những bệnh nhân cần thẩm phân
máu (độ thanh thải creatinine < 30 mL/phủt)] (xem 4. 4. Cánh báo vả thận trọng đặc biệt khi sử dụng).
Cảo nghiên cứu ở bệnh nhân suy thận nặng không cung cấp thông tin đầy đủ về tính an toản để hỗ trợ cho việc
sử dụng sugammadex ở những bệnh nhân nảy. Xem thêm phân 5.1. Dược lực học.
Bênh nhân cao tuổi: Sau khi dùng sugammadex tại thòi điểm tải xuất hiện T2 sau phong bế thần kinh cơ bằng
rocuronium, thời gian trung bình để hồi phục tỷ lệ Ti/Tị đển 0,9 ở người lởn (18-64 tuối) là 2,2 phủt, ở người
cao tuổi (ộs-74 tuồi) là 2,6 phút vả ở người rất cao tuối (z vs tuối) lả 3,6 phút. Mặc dù thời gian hồi phục ở
người cao tuổi có xu hưởng chậm hơn, nên sử dụng liều tương tự như người lớn (xem 4.4.Cảnh bảo và thận
Irọng đặc biệt khi sử dụng).
Bênh nhân béo phì: Ở những bệnh nhân béo phi, liều đề nghị sugammadex nên dựa vảo thể trọng thực của
bệnh nhân. Nên sư dụng liều tương tự như người 1ớn.
Suy gan: Đối với suy gan nhẹ đến trung bình: không cần điếu chỉnh liều do sugammadex được đảo thải chủ
yếu qua thặn.
Cảo nghiên cứu ở bệnh nhân suy gan chưa được tiến hảnh. Cần thặn trọng khi xem xét sư đụng sugammadex ở
bệnh nhân suy gan nặng hoặc khi suy gan di kèm với bệnh rôi loạn đông máu (xem phân 4.4.Cảnh báo vả
thận trọng đặc biệt khi sử dụng).
Bệnh nhi:
Dữ liệu từ nhóm bệnh nhi còn hạn chế (chỉ có 1 nghiên cứu về sự hóa giải phong bế do rocuronium khi tải
xuất hiện T,).
Trẻ em và thanh thiếu niên: Nên dùng sugammadex 2 mg/kg đế hóa giải thông thường phong bế do
rocuronium khi tái xuất hiện T2 ở trẻ cm và thanh thiếu nỉên (2-17 tuổi). c… tiến hảnh nghiên cứu các
trường hợp hóa giải thông thường khảo, do đó không nên dùng thuốc cho đến khi có thẻm dữ liệu.
Chưa nghiên cứu hóa giải tức thì ở trẻ em vả thanh thiếu niên do dó không nên dùng thuốc cho đến khi có
thêm dữ liệu.
AI
RA8700 OS S10 REF10.0IJUIyZO1S
S-OS SmPC-MKSG1 6-SOi-O72013
Có thể pha loãng Bridion 100 mg/mL thânh 10 mg/mL đế lảm tăng tinh chính xảo của iiều dùng cho hệnh nhi
(xem 6.6. Thận trọng đặc biệt khi Ioại bó vả các xử lý khác).
Trẻ mới sinh đủ thảng và trẻ nhò: Chi có kinh nghiệm giới hạn về việc sử dụng sugammadex cho trẻ nhỏ (30
ngảy đến 2 năm), chưa nghiên cứu ở trẻ mới sính đủ thảng (dưới 30 ngảy). Do đó khỏng nên dùng
sugammadex cho trẻ mới sinh đủ thảng vả trẻ nhỏ cho đến khi có thêm dữ liệu.
C ách dùng
Chỉ nên sử dụng sugammadex qua đướng tĩnh mạch với một liếu duy nhất tiêm trực tiếp. Liều trực tiếp nên
được tiêm nhanh, trong vòng 10 giây với tiêm trực tiếp vảo tĩnh mạch hoặc vảo một đường truyền tĩnh mạch.
Sugammadex chi được sử dụng dưới dạng tiêm trực tiếp một liều duy nhẩt trong các thử nghiệm lâm sảng.
4.3. Chống chỉ định
Quả mẫn vởi hoạt chắt hoặc với bẳt kỳ tả dược nảo (xem 6,1. Danh mục lả dược)
4.4. Cảnh báo và thận trọng đặc biệt khi sử dụng
Theo dõi ohức năng hò hẳp trong thời gian hối phuc:
Bắt buộc phải hỗ trợ thông khi cho bệnh nhân cho đến khi hô hẳp tự nhiên được phục hồi hoản toản sau khi
hóa giải phong bế thần kính cơ. Thậm chí khi hồi phục hoặn toản khỏi phong bế thần kinh cơ, cảc thưốc khảo
được sử dụng xung quanh và sau phân thuật có thẻ ức ohế chức năng hô hâp và do đó Có thế vân cân hô trợ
thõng khi.
/
Có thể tái xuât hiện phong bê thân kinh cơ sau khi rủt ông nội khí quản, nên cung Câp thông khi đây dù_ ỚỈJL
Ành hưởng đến sư cẩm máu:
Trong các thí nghiệm in virro, đã ghi nhận sự kéo dải thêm thời gian thrombopiastin từng phần hoạt hóa
(aPTT) và thời gian prothrombin (PT) đối vởi sugammadex phối hợp với các thuốc đối kháng vitamin K,
heparin không phân đoạn, heparinoid trọng lượng phân từ thấp, rivaroxaban vả dabigatran.
Trong một nghiên cứu ở những người tinh nguyện, cảc liều sugammadex 4 mg/kg và 16 mg/kg dẫn đến kéo
dải aPTT trung bình tối đa lả 17% với liều 4 mglkg vả 22% với liều 16 mg/kg và kéo dải PT (tỷ số chuẩn hóa
quốc tế, lNR) trung bình tối đa lả l 1% với liếu 4 mg/kg và 22% với iiều 16 mg/kg. Sự kéo dải aPTT vả PT
(INR) trung binh gỉởi hạn nảy oó thời gian ngắn (< 30 phút). Dựa trên cơ sở dữ liệu lâm sảng (n= 1738), khộng
có ảnh hướng nảo có ý nghĩa lâm sâng cùa sugammadex dùng đơn độc hoặc phối hợp với cảc thuốc chống
đông đối với tỷ lệ gặp biến chứng ohảy máu quanh phẫu thuật hoặc sau phẫu thuật.
Xem xét bản chất thoáng qua của sự kéo dải aPTT và PT giới hạn gây ra bởi sugammadex đơn độc hoặc cùng
với những thuốc chống đông nảy, không chẳc sugammadex có gây tăng nguy cơ chảy mảu. Vì không có thông
tin vê việc sử dụng sugammadex ở bệnh nhân đã biết có bệnh rôi loạn đông máu, cần theo dõi cân thận các
thông số đông mảu theo thực hảnh lâm sảng thường quy
Tải xuất hiên ghone bế:
Đ_ã ghi nhận tải xuất hiện phong bế trong cặc thử nghiệm lâm sảng chit yểu khi sử dgng\những líểu dưới liều
tôi ưu (trong những nghiên cứu xảo định liêu). Đê ngãn ngừa tái xuât hiện phong bê thân kinh cơ, nên dùng
những liều đề nghị hóa giải thông thướng hoặc tức thì (xem 4.2 Liều lượng và cách dùng).
Thời gian chờ để tải sử dung cảc thuốc bhong bế thần kinh cơ sau khi hóa giải bằng suaammadex:
Tái sử dụng rocuronium hoặc vecuronium sau khi hóa giải thông thường (sugammadex đến 4 mg/kg):
Thời gian chờ Thuốc phong bế thần kinh cơ (NMBA) và liều dùng
5 phút rocuronium 1,2 mg/kg
4 giờ rocuronium 0,6 mg/kg hoặc vecuronium 0,1 mg/kg
Dựa trên mô hình dược động học (PK), thời gian chờ được khuyến cảo ở bệnh nhân suy thận nhẹ hoặc trung
bình đề tải sử dụng rocuronium 0, 6 mg/kg hoặc vecuronium 0,1 mg/kg sau khi hóa giải thông thường bằng
sugammadex nên là 24 giờ Nếu cần thời gian chờ ngắn hơn, liều rocuronium cho sự phong bế thần kinh cơ
mới nên là 1,2 mg/kg
Tải sử dụng rocuronium hoặc vecuronium sau khi hóa giải tức thì (sugammadex 16 mg/kg):
-3-
1011
ỉẵ'Ềỉẻ
ii*i
RA8700 OS S10 REF10.0IJuIyZO1S
S-OS SmPC-MKSG1 6-SOi-O7ZO1 3
Đối với những trường hợp rất hiếm gặp mã có thề cằn điếu nảy, một thời gian ohớ 24 giờ được đề nghị.
Nếu cẩn phong bế thần kinh cơ trước khi thời gian chờ được khuyến cáo qua đi, nên sử dụng thuốc phong bể
thần kinh cơ không steroid. Sự khới phảt cùa thuốc phong bế thần kinh cơ khử cực có thế chậm hơn so với
dự kiến bới vi một phần dáng kề cảc thụ thể nicotinic sau chỗ nối vẫn còn có thể bị chiếm chỗ bới thuốc
phong bế thần kinh cơ
Suv thân:
Không khuyến cáo sử dụng sugammadex ở bệnh nhân suy thận nặng, bao gồm cả những ngưới cần thẩm phân
(xem phân 5.1. Dược lực học).
Tương tác do tảo dung kéo dải cùa rocuronium hoảc vecuronium:
Khi các thuốc có khả nảng phong bế thần kinh cơ được sử dụng trong giai đoạn hậu phẫu thì nên lưu ý đặc
biệt đến khả năng tải xuất hiện phong bế. Xin hãy tham khảo danh sáoh cảc thuốc cụ thể có khả năng gây
phong bể thẳn kinh cơ trong tờ thông tin kê toa cùa rocuronium hoặc vecuronium. Trong trường hợp tải xuất
hiện phong bế, bệnh nhân oó thể cẳn thông khí cơ học và sử dụng lại sugammadex (xem 4.2 Liều lượng vả
cách dùng).
Khả nảng tương tảo:
o Tương tác do chiếm giữ:
Do sử dụng sugammadex, một vải thuốc có thể trở nên kém hiệu quả do giảm nống độ của thuốc đó trong
huyết tương (dạng tự do) (xem 4. 5. Tương tác thuốc, tránh thai chứa hormon).
Nếu tinh trạng nảy xuất hiện, người thẩy thưốc được khuyên sử dụng lặp lại thuốc nảy, sử dụng thuốc có tảo
dụng điểu trị tương đương (tốt nhất là sư dụng nhóm thuốc khác) vả/hoặc những can thiệp không có tảo dụng
dược lý nếu thich hợp. J1V
, (A
0 Tương tác do thay thê: (
Do sữ dụng một vải thuốc sau khi dùng sugammadex, trên lý thuyết lả roouronium hoặc veouronium oó thế bị
thay thể ra khói sugammadcx. Kểt quả oó thể gây tải xuất hiện phong bế vả khi đó bệnh nhân phải được thông
khí. Nên ngừng sử dụng cảc thuốc có thể gây hiện tượng thay thế trong trường hợp truyền tĩnh mạoh. Trong
trường hợp tiên liệu có khả năng xuất hiện tương tác do thay thế, bệnh nhân nên được theo dõi chặt chẽ cảc
dấu hiện tải phong bể (khoảng 15 phút) sau khi sử dụng đường tíêm cảc thuốc khảo trong vòng 7,5 giờ sau khi
dùng sugammadex. Cho đến nay tương tảo do thay thế có thể xảy ra với một vải thuốc (toremifene, và axit
fusidic, xem 4.5 T zrcmg tảo thuốc).
Gâv mê nhe:
Trong cảc thử nghiệm lâm sáng khi phong bế thần kinh cơ đuợc hóa giải Chủ động giữa chững, dôi khi ghi
nhận cảc dấu hiệu cùa gây mê nhẹ (cử động, ho, nhản nhó, ngậm ống nội khí quản).
Nếu hối phục phong bế thần kinh cơ trong khi vẫn tiếp tục gây mê, nên dùng thêm những liều thuốc gảy m`
vả/hoặc opioỉd theo đòi hòi về mặt lâm sảng. .
Nhig tim châm đảng kể:
Trong một số hiếm trường hợp, nhịp tim chậm đảng kế đã được ghi nhận trong vòng vải phủt sau khi sử dụn
sugammadex dể hóa giải phong bế thần kinh cơ. Cả biệt có trường hợp nhịp tim chậm với ngùng tim đã được
bảo cáo (xem mục 4.8. Tác dụng bẩt lợi). Bệnh nhân nên dược theo dõi chặt chẽ những thay đồi về huyết
động học trong vả sau quá trinh hóa giải phong bế thần kinh cơ. Điều trị với cảc thuốc khảng cholinergic như
atropine nên được ảp dụng nểu có nhịp tim chậm trên lâm sảng.
Ẹtw_zạm
Sugammadex không được chuyến hóa hoặc thải trừ qua gan; do đó khỏng tiến hảnh nghiên cứu trên bệnh
nhân suy gan. Nên hết sức thận trọng khi điều trị cho những bệnh nhân suy gan nặng. Trong trường hợp suy
gan kèm theo bệnh rối loạn đông máu xem thông tin phần ảnh hưởng tới sự cầm máu.
Sử dung trong đơn vi chăm sóc đảo biêt (ICU):
~"l
l,_..l
\\ `\
RA8700 OS S10 REF10.0IJUIyZO1S
S-OS SmPC-MKSG1ô-SOi—O7201 3
Chưa nghiên cứu sugammadex ở những bệnh nhân dùng rocuronium hoặc vecuronium trong đơn vị chảm sóc
đặc biệt.
Sứ dung đề hóa giải cảc thuốc ghong bế thẩn kinh cơ khác không ghải rocuronium hoảc vecuronium: Không
nên sử dụng sugammadex đế hóa giải phong bế gây ra bởi các thuốc phong bế thần kinh cơ không steroid
như cảc hợp chẩt succinylcholine hoặc benzylisoquinolinium.
Không nên dùng sugammadex để hóa giải phong bế thần kinh cơ gây ra bới cảc thuốc phong bể thần kinh cơ
steroid khác ngoải rocuronium hoặc vecuronium do không có dữ liệu về tính hiệu quả và an toản đối với
những thuốc đó. Dữ liệu hiện có còn giới hạn về tác dụng hóa giải phong bế do pancuronium, do đó không
nên dùng sugammadex trong trường hợp nảy.
Tảo dung hóa giải châm:
Những bệnh kèm theo ứ trệ tuần hoản như bệnh tim mạch, tuồi cao (xem 4.2 Liều lượng vò cách dùng về thời
gian hóa giải ở bệnh nhân cao tuồi), hoặc tinh trạng phù thũng oỏ thề lảm cho thời gian hóa giải kéo dải hơn.
MẸ
Bảo sĩ nên chuẩn bị cho khả nảng xuất hiện cảo phản ứng dị ửng và có biện pháp phòng ngừa cần thiết (xem
4.8 T ảc dụng bất lợi).
Bênh nhân kiêng natri có kiềm soát:
Mỗi mL dung dịch chứa 9,7 mg natri. Một iiều chứa 23 mg natri được cho là " không chứa natri" (sodium
free). Nếu cẩn dùng nhiều hơn 2,4 mL dung dịch thì nên cãn nhắc đối với những bệnh nhân ăn kiêng muối có
kiếm soát. ft fL/'
4.5.Tương tác thuốc
Thông tin trong phần nảy dựa trên ái lực gắn kết giữa sugammadex vả cảc thuốc khác, oác thí nghiệm phi lâm
sảng, oảo nghỉên cứu lâm sảng và sự mô phỏng sử dụng mô hình, có tinh đến tác dụng dược lực học của thuốc
phong bể thần kinh cơ vả tướng tảc dược động học giữa thuốc phong bể thẳn kinh cơ và sugammadex. Dựa
trên những dữ liệu nảy, không có tương tảo dược lực học nảo với các thuốc khác có ý nghĩa lâm sảng được dự
kiến, ngoại trừ trường hợp sau:
Đối với toremifene vả acid fusidic, không thể loại trừ tương tảo do thay thế (không có tương tảo do chiếm giữ
nảo có ý nghĩa lâm sảng được dự kỉến).
Không loại trừ tương tác do chiếm giữ đối với cảc thuốc tránh thai chứa hormon (không có tương tác do thay
thê).
Tương tảo có khả nảng ảnh hướng` đến tảo dung của sugammadex (xem 4. 4.Cảnh bảo vả rhán rrone đăc biêl
khi sử dung):
Toremifene:
Đối với toremifene, chẳt có hằng số ải lực cao tương đối vả nồng độ huyết tương cao tương đối, có thể xuất
hiện một vải thay thế cùa vecuronium hoặc rocuronium từ phức hợp với sugammadex. Do đó có thẻ 1ảm chậm
quá trình phục hôi tỷ lệ th1`. đên 0,9 ở một số bệnh nhân dùng toremifene vảo cùng ngảy phẫu thuật.
Tỉêm tĩnh mạch acid fusidic:
Việc sử dụng acid fusidic trong giai đoạn trước phẫu thuật có thể lảm chậm một chút về sự phục hối tỷ lệ
T.JT. dến 0, 9. Tuy nhiên, khỏng dự kiến tái phát phong bế thần kinh cơ ở giai đoạn sau phẫu thuật, vì tốc độ
truyền acid fusidic trong khoảng thời gian vải giờ và nông độ trong máu tích lũy trong 2— 3 ngảy
Tướng tác có khả năng ảnh hưởng đến tảc dung của cảc thuốc khảc ( xem 4.4. Canh báo vả thân trong đăc biẻr
khi sử dung):
Thuốc trảnh thai ohứa hormon:
Tương tảo giữa sugammadex 4 mglkg vả một progestogen được tiên đoán gây giảm nồng độ progestogen (34
% đối với AUC) tương tự như sự suy giảm quan sát thẳy khi quên một liều hảng ngảy thuốc trảnh thai đường
uống được uống lại sau hơn 12 giờ, có thể gây giảm hiệu quả của thuốc. Đối với cảc estrogen, tảo dụng được
cho là giảm ít đi. Do đỏ, sử dụng một liều sugammadex tiêm tĩnh mạch trực tiểp được cho lả tương đương với
RA8700 08 810 REF10.0IJUIyZO1S
S-OS SmPC-MK861 6-SOi-O7201 3
quên một liếu hảng ngảy cùa steroid tránh thai đường uổng (hoặc kết hợp hoặc chỉ có progestogen). Nếu sử
dụng sugammadex vảo cùng một ngảy với thuốc trảnh thai đường uống thì tham khảo hưởng dẫn khi quên
thuốc trong tờ thông tin sản phẩm oủa thuốc trảnh thai dường uống. Đối với thuốc trảnh thai không phải
dường uống, bệnh nhân phải sử dụng thêm biện phảp tránh thai không ohức hormon trong 7 ngảy kế tiếp và
tham khảo thông tin sản phẩm.
Tương tảo với xét nehiẽm cân lâm sảng:
Nhin chung sugammadex không ảnh hưởng dến cảc xét nghiệm cận lâm sảng, ngoại trừ xét nghiệm
progesterone huyết thanh và một vải thông sộ động máu [thời gian thromboplastin hoạt hóa từng phằn, thời
gian prothrombin (tỷ lệ binh thường hóa quốc tế)]. Đã thấy những thay đối trong cảc mẫu huyết tương với
nồng độ sugammadex trong phạm vi tướng tự như đạt được với Cmax sau một liều 16 mg/kg Chưa rõ mối liên
quan lâm sảng cùa những phát hiện nảy do chưa được nghiên cứu trên bệnh nhân.
Bệnh nhi
Không tiến hảnh các nghiên cứu tương tảc chính thức. Nên xem xét những tương tác như nêu trên đối vởi
người lớn vả cảnh báo trong mục 4, 4. Cảnh báo vả thận lrọng đặc biệt khi sử dụng khi dùng cho trè.
4.6. Thai kỳ và cho con bú
Khỏng có sẵn dữ liệu lâm sảng về việc sử dụng sugammadex trong thai kỳ.
Những nghiên cứu trên động vật không cho thẳy tảo dụng gây hại trực tiếp hoặc gián tiếp liên quan đến mang
thai, phát triền phôi/thai, quá trình sinh đẻ hoặc phảt triến sau khi sinh.
Nên thận trọng khi dùng sugammadex cho phụ nữ mang thai.
Chưa biểt liệu sugammadex có được tiết vảo sữa mẹ hay không. Những nghiên cứu trên động vật cho thấy
sugammadex được tiêt vảo sữa. Nhin chung hâp thu cùa cảc cyciodextrin qua đường uống là thấp và tiên liệu
không ảnh hướng đến trẻ bú mẹ sau khi dùng liều duy nhất cho bả mẹ đang oho con bú.
4.7.Tảc động của thuốc khi lải xe và vận hânh máy móc
Không tìến hảnh nghiên cứu ảnh hưởng đến khả năng lái xe và vận hảnh mảy móc.
4.8.Tác dụng bất lợi
Độ an toản cùa sugammadex đã được đảnh giá dựa trên cơ sở dữ liệu an toản được tích hợp ở khoảng 1700
bệnh nhân và 120 người tinh nguyện. Phản ứng phụ được bảo cảo thường gặp nhất ở các bệnh nhân lả cảc
biến chứng do gãy mê (Thường gặp [> 1/100 đến < 1/10]).
Có thể dùng sugammadex trong thới gỉan cho con bú. ẩJ`/
Các tảc dụng không mong muốn sau đây được bảo các đối với những bệnh nhân được xem lả có liên quan với
việc sử dụng sugammadex:
Hệ cơ quan Tỷ lệ Phân ứng bẩt lợi
Rối loạn hệ miễn dịch Ít gặp (2 1/1000 đển < 1/100) Phận ứng quả mẫn do thuốc (xem
phân 4.4.Cảnh bảo và thận trọng
đậc biệt khi sử dụng)
Tốn thương, ngộ độc và biến Thường gặp (2 moo đến < mo> Biển chứng do gây mê (xem phẳn
chứng do thủ thuật 4.4.Cảnh bảo và thận trỌng đặc
biệt khi sử dụng)
Ỉt gặp (2 … 000 đến < moc» Thức tinh không mong muốn
trong khi gây mê
Biến ohứng gây mê:
Những biến chứng gây mê, biểu hiện cùa sự phục hồi chức năng thần kinh cơ, bao gổm cừ dộng chỉ hoặc cơ
thế hoặc ho trong thời gian gây mê hoặc thời gian phẫu thuật, biều hiện nhăn mặt hoặc mủt vảo ống nội khí
quản. Xem 4. 4. C ảnh báo vả thặn trọng đặc biệt khi sử dụng trong gây mê nhẹ.
Ọ\
fct?"
RA8700 OS S10 REF10.0IJUIy201S
S—OS SmPC-MK8õ1õ—SOi-O7ZO1S
Thức tinh:
Đã ghi nhận thức tinh ở một số người điều trị bằng sugammadex. Chưa chắc chắn mối 1iên quan với
sugammadex.
Tải xuất hiện phong bế:
Trong dữ liệu cơ bản của những nghiên cứu ohung giai đoạn 1-111 có so sảnh với nhóm placebo, tỷ lệ tái xuất
hiện phong bế như đánh giá bắng theo dõi thần kinh cơ là 2% sau khi dùng sugammadex và 0% trong nhóm
dùng placebo. Hằu hết những trường hợp nảy lả từ những nghiên cứu dò liều khi sử dụng liếu gần tối ưu (< 2
mg/kg) (xem 4. 4. Cảnh báo vả lhận trọng đặc biệt khi sử dụng).
Phản ứng quá mẫn do thuốc:
Phản ứng quả mẫn, bao gồm cả phản vệ đã xảy ra ở một số bệnh nhân vả người tinh nguyện (để biết thêm
thông tin vê người tình nguyện, xem Thông tin về người tinh nguyện khỏe mạnh dưới đây). Trong cảc thử
nghiệm lâm sảng về bệnh nhân phẫu thuật, những phản ứng nảy đã được bảo Cảo ít gặp và dối với cảc báo cảo
hậu mải thì tân suât chưa rõ.
Những phận ứng nảy thay đối từ cảc phản ửng da riêng lẻ đến cặc phản ứng toản thân nghiêm trọng (tức là
phản vệ, sôc phản vệ) vả đã xảy ra ở những bệnh nhân không có tiêp xúc trước đó với sugammadex.
Cảo triệu chứng liẽn quan với những phản ứng nảy có thể bao gồm: đỏ bừng mặt, nổi mề đay, ban đỏ, hạ
huyết ảp (nặng), nhịp tim nhanh, sưng phù lưỡi, sưng phù họng, co thắt phế quản vả biến cố tắc nghẽn phồi.
Phản ứng quả mẫn nặng có thể gây tử vong.
Thông tin về người tinh nguyện khóe mạnh:
Phản ứng quả mẫn, bao gồm cả phản vệ đã được quan sảt với sugammadex. Trong một nghỉên cứu ở những
ngưới tình nguyện tinh tảo khỏe mạnh (giá dược, n=150; 4 mg/kg, n=148 và 16 mg/kg, n=150), phản ứng quả
mân đã được bảo cáo thường gập với sugammadex liều 16 mg/kg vả it gặp với sugammadex liếu 4 mg/kg
hoặc giả dược
Trong nghiên oứu nảy, xu hướng phụ thuộc liều cũng đã được quan sảt thắy đối với ioạn vị giảc, buồn nôn và
đỏ bừng mặt.
Nhịp tim chậm đáng kể:
Sau khi lưu hảnh, các bảo cảo độc lặp về nhịp tim chậm đảng kế và nhịp tim chậm với ngừng tim đã được ghi
nhận trong vòng vải phủt sau khi tiêm sugammadex (xem mục 4.4. Cánh báo vả thận trọng đặc biệt khi“ sử
dụng)
Thông lin bổ sung trong nhóm đặc biệt
Bệnh nhân bị bệnh phối:
Dũ lỉệu hậu mãi trọng một nghiên cứu lâm sảng chuyên biệt ở những bệnh nhân có tiền sử biến chửng ở phổi,
đã ghi nhận co thẳt phế quản như một tác dụng bất lợi. Cũng như tẳt cả những bệnh nhân có tiền sử biến
chứng` ơ phồi, bảo sĩ nên lưu ý đến khả nãng xuất hiện co thắt phế quản.
Bệnh nhi
Cơ sở dữ lỉệu cơ bản còn hạn chế gợi ý rầng dữ liệu an toân của sugammadex (đến 4 mg/kg) ở bệnh nhi lả
tương tự như ở người lớn.
Thông bảo cho bảo sĩ những lác dụng phụ gặp phải khi dùng thuốc.
4.9. Quá liễu
Trong những nghiên cứu lâm sảng, đã ghi nhận 1 trường hợp tình cờ quá 1iều dùng 40 mg/kg mã không có bẩt
kỳ tác dụng bẩt lợi nảo. Trong một nghiên cứu về tính dung nạp ở người đã dùng sugammadex đến 96 mg/kg.
Không ghi nhận bỉều hiện bất lợi liên quan đển Iiểu dùng cũng như biểu hiện bắt lợi nghiêm trọng
Sugammadex có thế được Ioại bỏ bằng cách sử dụng thẩm phân máu vởi bộ 1ọc dòng cao (high- tìux), nhưng
không ảp dụng được vởi bộ lọc dòng thắp (low-flux). Dựa trên cảc nghiên cứu lâm sảng, nồng độ
sugammadex trong huyết tương giảm khoảng 70% với bộ lọc dòng cao sau một buối thẩm phân 3- 6 giờ.
\\
4`\"
//;.~`/-4- -
RA8700 08 810 REF10.0IJulyZO1S
S-OS SmPC—MKSG1G—SOi-O7ZO13
s. CẢC ĐẶC TÍNH DƯỢC LÝ
5.1. Dược lực học
Nhóm dược lý trị liệu: Tắt cả các sản phẩm điều trị khảo, mã ATC: VO3ABBS
Cơ chế tảo dung:
Sugammadex là một cyclodextrin gamma đã thay đồi lệ một Thuốc Gắn kết với Thuốc Giãn cơ Chọn lọc. Nộ
hình thảnh một phức hợp yới các thuộc phong bê thân kinh cơ rogouroniưm hoặc veouroniurn trong huyêt
tượng yả do đó Iảm giảm sô lượng t_huôc phong bê thân kinh cơ có sặn đê gãn kêt với các thụ thê nicotinic tại
chó nôi thân kinh cơ. Điêu nảy dân đên hóa giải sự phong bê thân kinh cơ gây ra bới rocuronium hoặc
vecuronium.
Tảo dung dưoc lưc hoc:
Sugammadex đã được dùng ở cảc liếu trong khoảng từ 0,5 mg/kg đến 16 mg/kg trong các nghiên cứu về sự
phong bê gây ra bới rocuronium đảp ưng vởi liêu dùng (rocuronium bromide 0, 6, 0,9, 1, 0 và 1 ,2 mg/kg, có vả
không oó liếu duy trì) và sự phong bể gây ra bời vecuronium (vecuronium bromide 0, 1 mg/kg, có hoặc không
có liếu duy trì) tại cảc thời điếm/độ sâu cùa sự phong bế khảo nhau. Trong các nghiên cứu nảy, đã quan sát
thẩy môi quan hệ rõ về liếu dùng—đảp ứng.
Hiêu quả vả đô an toản trên lâm sảng:
Có thể dùng sugammadex ở một số thời điềm sau khi sử dụng rocuronium hoặc vecuronium bromide:
Hóa giái thông thường sựphong bế thần kinh cơ sâu.
Trong một nghiên cứu then chốt, cảc bệnh nhân được phân bố ngẫu nhiên vảo nhóm rocuronium hoặc nhóm
vecuronium Sau Iiếu rocuronium hoặc vecuronium cuôi cùng, vảo lủc có 1-2 phản ứng sau co cứng,
sugammadex 4 mg/kg hoặc neostigmine 70 mcglkg dược sử dụng theo thứ tự ngẫu nhiên. Thời gian từ lúc bắt
đầu sử dụng sugammadex hoặc neostigmine đến khi phục hồi tỷ lệ T.;fT. đến 0, 9 lả:
Thời gian (phủt) từ lủc sử dụng sugammadex hoặc neostigmine lủc phong bế thần kinh cơ sâu (1-2 phản ứng
sau co cứng) sau khi dùng rocuronium hoặc vecuronium đẽn khi phục hồi tỷ lệ TilTi đến 0, 9
Thuốc phong bế thẳn Chế độ diều trị 1,
kinh cơ Sugammadex (4 mglkg) Neostigmine (70 mcngg) íẬV
Rocuronium
N 37 37
Trung vị (phủt) 2,7 49,0
Khoảng 1,2-16,1 13,3-145,7
Vecuronium
N 47 36
Trung vị (phủt) 3,3 49,9
Khoảng 1,4-68,4 46,0-312,7
Hóa giải !hóng Ihường sự phong bế !hần kinh cơ trung bình:
Trong một nghiên cứu then chốt khảo, cảc bệnh nhân được phân bổ ngẫu nhiên vảo nhóm rocuronium hoặc
vecuronium. Sau liêu rocuronium hoặc vecuronium cuôi cùng, vảo lủc tái xuât hiện T2, sugammadex 2 mg/kg
hoặc neostigmine 50 mcg/kg được sử dụng theo thứ tự n âu nhiên. Thời gian từ hic bảt đâu sủ dụng
sugammadex hoặc neostigmine đên khi phục hôi tỷ lệ T4lTi đên 0,9 lả:
\q-iK
Obt
II
RA8700 OS S10 REF10.0/July2013
S-OS SmPC-M K8616-80ỉ-07201 3
Thời gian (phủt) từ lủc sử dụng sugammạdex hoặc neostigmine vảo lủc tái xuất hiện T2 sau khi dùng
rocuronium hoặc vecuronium dên khi phục hôi tỷ lệ TJT; đển 0,9
Thuốc phong bế thần kinh cơ Chế độ điều trị
Sugammadex (2 mglkg) Neostigmine (50 mcg/kg)
Rocuronium
N 48 48
Trung vị (phủt) 1,4 17,6
Khoản g 0,9-5,4 3,7-106,9
Vecuronium
N 48 45
Trung vị (phủt) 2,1 18,9
Khoảng 1,2-64,2 2,9-76,2
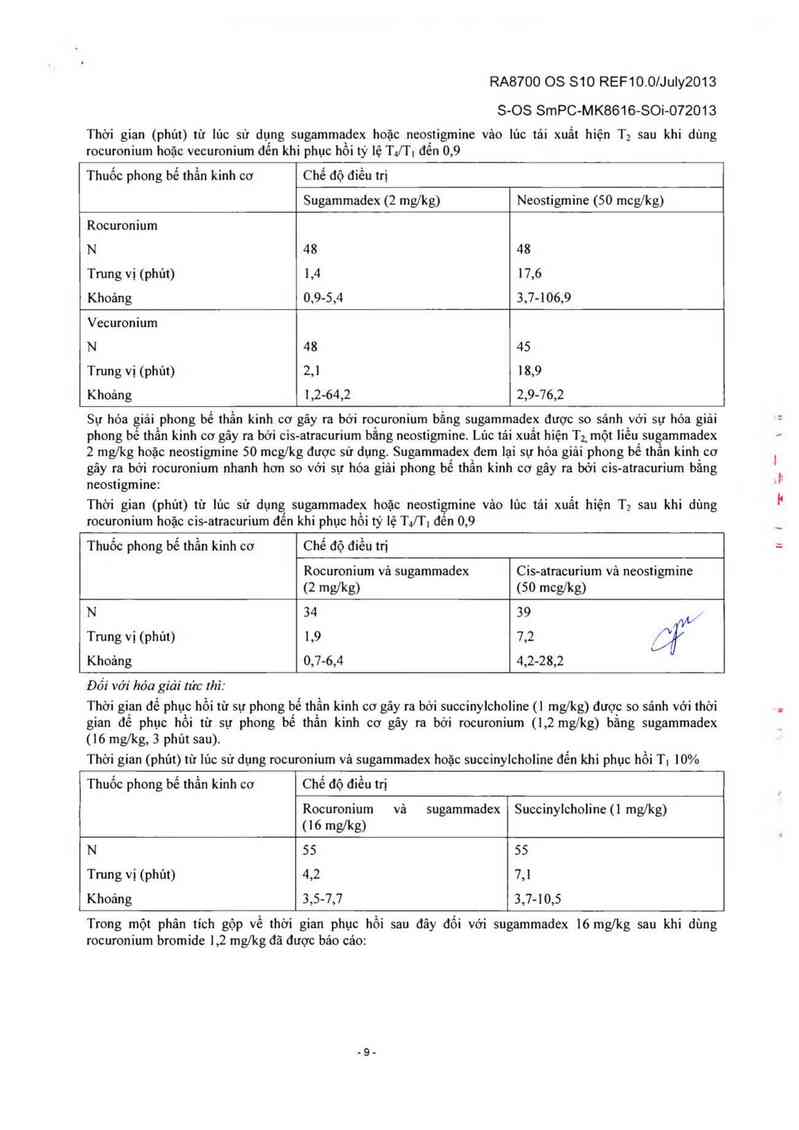
Sự hóa giải phong bế thẳn kinh cơ gây ra bới rocuronium bằng sugammadex được so sánh với sự hóa giải
phong bể thần kinh cơ gây ra bời cis-atracurium bằng neostigmine. Lúc tái xuất hiện T;_ một liểu su ammadex
2 mg/kg hoặc neostigmine 50 mcg/kg được sử dụng. Sugammadex đem lại sự hóa giải phong bể thân kinh cơ
gây ra bời rocuronium nhanh hơn so với sự hóa giâi phong bể thần kinh cơ gây ra bới cis-atracurium bằng
neostigmine:
Thời gian (phủt) từ lủc sư dụng sugammadqx hoặc neostigmine vảo lúc tái xuất hiện Tỵ sau khi dùng
rocuronium hoặc cis-atracurium đên khi phục hôi tỷ lệ T4ỈTỵ đên 0,9
Thuốc phong bế thần kinh cơ
Chế độ điều trị
Rocuronium vả sugammadex
(2 mg/kg)
Cis-atracurium vả neostigmine
(50 mcgfkg)
N
Trung vị (phút)
Khoảng
34
1,9
0,7-6,4
39
7,2 5fW
4,2-28,2
Đối với hóa giải Iức thì:
Thời gian để phục hồi từ sự phong hề thần kinh cơ gây ra bởi succinylcholine (1 mg/kg) được so sánh vởi thời
gian đê phục hôi từ sự phong bê thân kinh cơ gây ra bởi rocuronium (1,2 mg/kg) băng sugammadex
(16 mg/kg, 3 phút sau).
Thời gian (phủt) từ lủc sử dụng rocuronium vả sugammadex hoặc succinylcholine đển khi phục hồi T. 10%
Thuốc phong bế thẩn kinh cơ Chế độ điều trị
Rocuronium vả sugammadex Succinylcholine (] mg/kg)
(16 mg/kg)
N 55 55
Trung vị (phủt) 4,2 7,1
Khoảng 3,5—7,7 3,7-10,5
Trong một phân tích gộp về thời gian phục hồi sau đây đối với sugammadex lómg/kg sau khi dùng
rocuronium bromide 1,2 mglkg đă được báo cáo:
RA8700 OS S10 REF10.0IJUIy201S
S-OS SmPC-M K861 6-SOi-O7201 3
Thời giạn (phủt) từ lùc sứ đụng sugammadex vảo lúc 3 phủt sau khi dùng rocuronium đển khi phục hồi tỷ lệ
TưT. đên 0,9, 0,8 hoặc 0,7
T,,JTl đến 0,9 TưTl đến 0,8 T,m đến 0,7
N 65 65 65
Trung vị (phủt) 1,5 1,3 1,1
Khoảng 0,5-14,3 0,5-6,2 o,5-3,3
Suy Ihận:
Hai nghiên cứu nhãn mở so sảnh hiệu quả vả độ an toản của sugammadex ở những bệnh nhân phẫu thuật có
và không có suy thặn nặng. Trong một nghiên cửu, sugammadex được dùng sau phong bê thân kinh cơ gây ra
bới rocuronium vảo Iủc có 1—2 phản ứng sau co cứng (4 mglkg; N=68); trọng một nghiên `cứu khảc,
sugammadex được sư dụng vảo lủc tải xuât hiện T2 (2 mg/kg; N=30). Sự phục hôi từ phong bê thân kinh cơ
lâu hơn vừa`phải đôi vói bệnh nhân suy thậnnặng so với bệnh nhân không suy thận. Không có bảo cáo vê sự
phong bê thân kinh cơ tôn dư hoặc tái phảt đôi với bệnh nhân suy thận nặng trong những nghiên cứu nảy.
Ảnh hướng đến khoảng QTc:
Trong ba nghiên cứu lâm sảng chuyên biệt (N= 287) với sugammadex đơn độc, sugammadex phối hợp với
rocuronium hoặc vecuronium vả sugammadex phối hợp với propofol hoặc sevoflurane không liên quạn với
sự kéo dải khoảng QT/OTc có ý nghĩa lâm sảng Điện tâm dỗ tích hợp vả kết quả phản ứng phụ cùa các
nghiên cứu Phase 2— 3 hỗ trợ cho kết luặn nảy.
5.2. Dược động học
Cảc thông số dược động học của sugammadex được tính từ tồng toản phần nồng độ liên kết không phức hợp
và phức hợp cùa sugammadex. Các yếu tố dược động học như độ thanh thải và thể tích phân bố được cho lả
tương đương giữa sugammadex liên kểt không phức hợp vả phức hợp ở những người gây mê.
Phân bố:
Thể tích phân bố trong tinh trạng ốn định cùa sugammadcx khoảng 1 1 đển 14 lít. Sugammadex và phức hợp
của sugammadex với rocuronium không liên kểt với protein huyết thanh hoặc hồng cầu, như đã chứng minh
trong in vitro sư dụng huyết tương vả máu toản phẩn của nam giới. Sugammadex thể hiện động học tuyển tính
với liều tiêm tĩnh mạch trực tiểp … 1 đến 16 mglkg.
.’V
Chuvền hóa:
Trong những nghiên cứu tiền lâm sảng và lâm sảng không thấy sự chuyến hóa cùa sugammadex vả chi thắy
bải tiểt qua thận dưới dạng thuốc không biến đổi như con đường thải trừ.
ẸẶtieẸ
Nửa đời thải trứ (t )cùa sugammadex ở người lớn lả 1 ,8 giờ vả thanh thải huyết thanh ước Iưọng khoảng 88
mL/phủt Trong một nghiên cứu cân bằng tông thế (mass balance study) cho thấy > 90 % liểu dùng được bải
tỉết trong vòng 24 giờ 96 % liều dùng được bải tiễt qua nước tiêu, trong đó ít nhất 95 % dưới dạng
sugammadex không biển đổi. Thải trứ qua phân hoặc thở qua không khi chiếm < 0,02 % liếu dùng. Dùng
sugammadex cho những người tinh nguyện khóe mạnh gây tảng đảo thải rocuronium qua thận dưới dạng phức
hợp.
Nhóm bệnh nhăn đặc biệt:
Người cao tuối vả suv thân:
Trong 2 nghiên cứu về dược động học so sánh bệnh nhãn suy thặn nặng với bệnh nhân có chức nãng thận bình
thường, nông độ sugammadex trong huyết tương tương tự trong thời gian it nhắt là 20 phủt đầu tiên sau khi
dùng thuốc và sau đó nông độ giảm xuông nhanh hơn ở nhóm đối chứng Mức tiếp xủc toản bộ với với
sugammadex kéo dải, dẫn đển mức tiếp xúc cao hơn khoảng 15 lẳn ở bệnh nhân suy thận nặng Ở một số bệnh
nhân suy thận nặng, nồng độ sugammadex được phảt hiện ở mức tối thiều trong huyết tương sau khi dùng
thuốc 1 thảng.
-1o-
RA8700 OS S10 REF10.0IJUIy201S
S-OS SmPC-MK8G1 6-SOi-07201 3
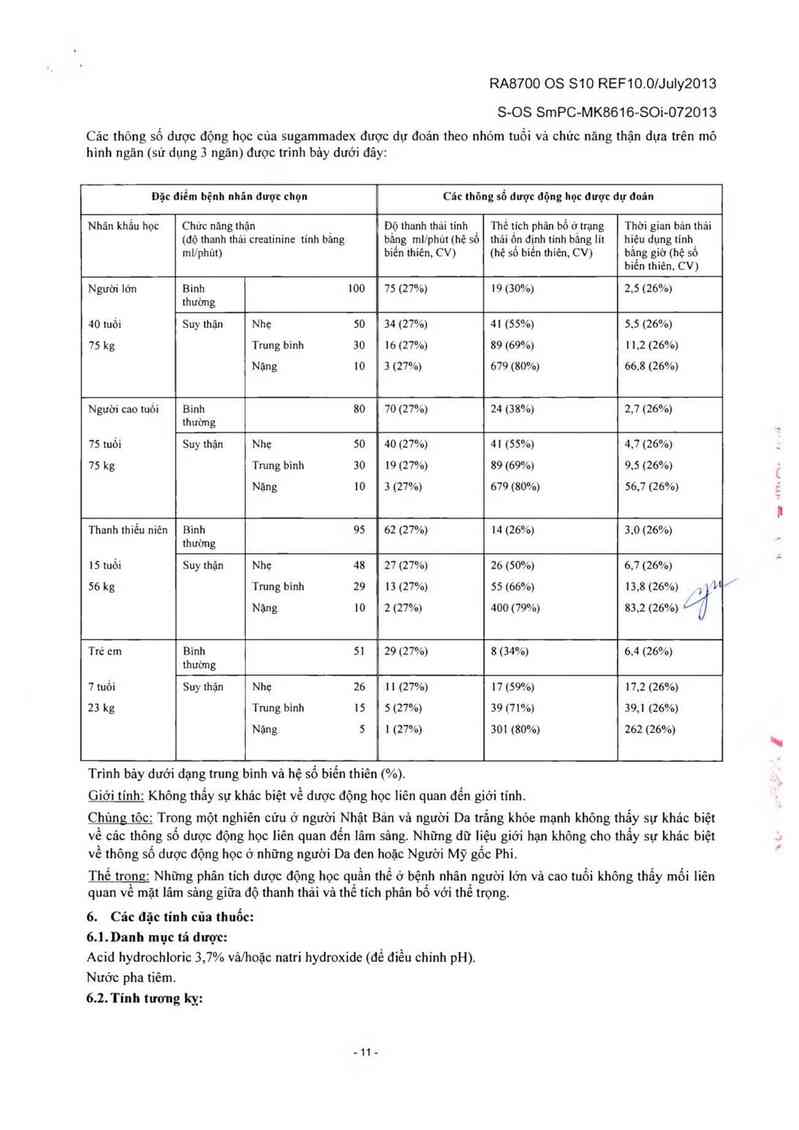
Cảc thỏng số dược động học của sugammadex được dự đoán theo nhóm tuổi vả chức năng thận dựa trên mô
hinh ngản (sủ dụng 3 ngăn) được trinh bảy dưới đãy:
Đặc điểm bệnh nhãn được chọn
Các thông số dược động học được dự đoán
Nhân khẳu học Chức năng thận _ Đ_ộ thanh thải tính . Thể tích phân bố ớ trạng Thời gian bán thái
(độ thanh thải creatinine tính bảng bapg mllphùt (hệ sô thải ớn đinh tính bảng lit hiệu dụng lính.
mllphùl) biên thiến. CV) (hệ sô biên thiẽn. CV) bảpg giờ (hệ sô
biến thiên. CV)
Người lớn Binh 100 75 (27%) 19 (30%) 2,5 (26%)
thường
40 tuõi Suy lhận Nhẹ 50 34 (27%) 41 (55%) 5,5 (26%)
75 kg Trung binh 30 16 (27%) 89 (69%) 1 1,2 (26%)
Nặng 10 3 (27%) 679 (80%) 66.8 (26%)
Người cao tuỏi Binh 80 70 (27%) 24 (38%) 2,7 (26%)
thường
75 tuối Suy thận Nhẹ 50 40 (27%) 41 (55%) 4.7 (26%)
75 kg Trung binh 30 19 (27%) 89 (69%) 9.5 (26%)
Nặng 10 3 (27%) 679 (80%) 56,7 (26%)
Thanh thiếu niên Bình 95 62 (27%) 14 (26%) 3.0 (26%)
thường
15 tuổi Suy thặn Nhẹ 48 27 (27%) 26 (50%) 6,7 (26%)
56 kg Trung binh 29 15 (27%) 55 (66%) 13,8 (26%) , M
Nặng 10 2 (27%) 400 (79%) 83,2 (26%) 4
Trẻ cm Bình 51 29 (27%) 8 (34%) 6.4 (26%)
thuờng
7 tuối Suy thận Nhẹ 26 | 1 (27%) 17 (59%) 17,2 (26%)
23 kg Trung binh 15 5 (27%) 39 (71%) 39,1 (26%)
Nặng 5 | (27%) 301 (80%) 262 (26%)
Trinh bảy dưới dạng trung bình và hệ số biến thiên (%).
Giới tính: Không thấy sự khác biệt về dược động học liên quan đển gìới tính.
Chùng tôc: Trong một nghiên cứu ở người Nhật Bản vả người Da trắng khỏe mạnh không thẳy sự khảc biệt
về cảc thông sô dược động học liên quan đến lâm sảng. Những dữ liệu giới hạn không cho thẩy sự khác biệt
về thông số dược động học ở những người Da đen hoặc Người Mỹ gốc Phi.
Thế trọng: Những phân tich dược động học qưần thế ở bệnh nhân _người lớn vả cao tuối không thẳy mối liên
quan vẻ mặt lâm sảng giữa độ thanh thải vả thê tích phân bộ với thẻ trọng.
6. Các đặc tỉnh của thuốc:
6.1.Danh mục tả dược:
Acid hydrochloric 3,7% vả/hoậc natri hydroxide (để điều chinh pH).
Nước pha tiêm.
6.2.Tính tương kỵ:
-11.
RA8700 OS S10 REF10.0IJUIy2013
S—OS SmPC-MK8õ1ô—SOi-O7201S
Không nên trộn lẵn thuốc nảy với cảc thuốc khác ngoại trừ những thuốc được nêu trong phần “6.6. Thận trọng
đặc biệt khi Ioạỉ bò vả xử lý khác". Dã ghi nhận tính tương kỵ vật lý với verapamil, ondansetron vả ranitidine.
6.3. Hạn dùng
3 năm kế từ ngảy sản xuất.
Sạn lần đằu tiên mở thuộc, đã chứng minh tính ổn định về mặt lý hoá trong thời gian sử dụng lá 48 giờ tại 2°C
đên 25°C.ịl`heo quan điêm vi sinh, nên sử dụng dung dịch đã pha ngay tức thì. Nêu không sử dụng ngạy, thời
gian và điêu kiện bảo quản trước khi sử dụng lá trảc\h nhiệm cùa người sử dụng và thườnnghông quả 24 giờ
tại 2°C đẽn 8°C, trừ khi dung dịch được pha trong điêu kiện vô khuân được thâm định vả kiêm tra.
6.4. Bảo quãn
Bảo quản dưới 30°C. Không đông đả.
Bảo quản trong bao bì gốc để trảnh ảnh sáng.
Có thể bảo quản lọ thuốc bên ngoải hộp carton trong 5 ngảy.
Điếu kiện bảo quản cho dung dịch đã pha, xem 6.3 Hạn dùng.
6.5 Bản chẩt và dung lượng của bao bì
Lọ thùy tinhloại 1 sử dụng một lẩn được đóng bằng nút cao su chlorobutyl mảu xám với nắp (crimp—cap) bằng
nhôm và miêng bịt bật (flỉp-oft).
Nút cao su cùa lọ không chứa Iatex.
M/
Hộp chứa 10 lo 2 ml hoặc 101ọ 5 ml. ,
Không phái tắt cả quy cảch đóng gói được lưu hảnh. “Ý
6.6. Thận trọng đặc biệt khi loại bỏ và xử lý khác \
Nếu sử dụng Bridion qua một đường truyền đã sử dụng với các thuốc khảc, điểu quan trọng là phải xả trôi '…,
đuờng truyên [như với natri cloride 9 mg/mL (dung dịch 0, 9 %)] giữa lần dùng Bridion và các thuốc khảc đã 113 J
biết tương kỵ với Bridion hoặc cảc thuốc chưa biết có tương thích với Bridion hay không , 1 `» 1
. J an
Có thế tiêm sugammadex vảo đường truyền đang sử dụng để truyền tĩnh mạch các dung dịch sau: nạtri'j /S/
chloride 9 mglmL (0, 9 %), glucose 50 mg/mL (5 %), natri chloride 4,5 mg/mL (0,45 %) vả glucose 25 mg/mL'JJ ậ/
(2, 5 %), dung dịch Ringers 1actate,dung dịch Ringers, glucose 50 mg/mL (5 %) trong natri chloride 9 mglmLịỵ
(0, 9 %).
Khi dùng cho bệnh nhi có thể pha loãng Bridion bằng dung dịch natri chloride 9 mg/mL (0,9 %) để tạo thảnh
nông độ 10 mg/mL (xem 6.3. Hạn dùng).
Nên loại bỏ phần thuốc không sử dụng hoặc chất thải tuân theo qui định của từng nơi.
SÁN XUẤT BỞI
N.V. Organon, Kloosterstraat 6, 5349 A
PHÓ cục TRUỞNG
-12.
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng