














——\
ạ.I.VNJHIOG
6mz uoựoaful 10) qụuozauog
Prescription Drug
lì
Bortezomib for
lnjection 2mg
CỤC QL'ẨN LÝ DƯỢC
ĐÃPHÊDUYỆT
Lân đẩu
BỘYTỂ
:..zé.z…ĩ……x…z.faư
^«HơW,
1090L891
"M 90! X8fIìfỢ9
Elch via! contains:
Bonemmib 2mg
Douge. As directod by
the thsicinn.
Remnstitution:
Rcoonsututc with Zml of 0. 9%
Scduum Chlondc Imecuun IP
Administration:
Rcfcr packagc mscn
Slorage: Sime al mom
tcmpetaturc not exceeding
Thuốc kê đơn
Bortezomib for
Injection 2mg
Mỗi lọ chưa:
Honemmxd .’.mg
Ch] dưth. chông chi dmh. hcu
lưcmg—cách dùng. tác dung
phu vá các thủng t… khac
Xem lơ hưởng dẫn sư dụng
Bâo quin:
Ó nhu}! dù phùng khỏng quu
10“(` Trung bt… hn gỂ›c vù
ưanh anh sang
Dế thuoc ngoa'u t_ảm lan tu: cm
DỌC kỹ hurmg daìn sư dung
* ~k : .
BORTENẨT wm………… BORTENÃT U………
package to prolect from light Trade mmk
- ~ ~ . : M !. 49AJAISC/P-thư»
ỊJJI’ỊỈ'ỊỄẸỆỆỆÍ’JMỀỆd Balch Nol Sở m sx
' ` ' MngleX
_ _ _ _ Keep uul of reach and l²vp DMD
Lyophulưod PWd'f f°r IIIJOCỈỈOII snght of chn]drcn BỘT ĐỒNG KHỎ DNNK
Please read cam“qu the PHÁ TIÊU TỈNH lIACH
puckuge mscn hcforc use` '
FOR BOLUS INTRAVENOUS INJECTION
FOR SINGLE USE ONLY
Manufacuued h_\ Sun xuat hm
.Q . . . . . . WẨỈÌÌNỈNBI ĨO be Sđldũby , ' . . . . . . Ẹẳỉfiẵ IATCO
ffltỀ ,, o o o o o . tetaN … the Dfescnpùon QưỀ o o o o . o c … No m. 1……… sam…
& g . . . . . ot an Oncologist only 0 0 0 0 0 0 O ịỄỄlịẵmỉxuẵịẫẵmm' Unamkhand.
W la,
l
« ầ
0 0
ở
3 v
~ ử’
WoEỸ~ ở
E M… mulm: R 2 mg/vial
' Bẵĩìemmitb 2mg . . . hú …
l g Bortezomlb ÍOI' ỈanỈIOÍÌ 2mg MI. wu,ụsc P-zuos
. lcnge:Slomaưoom tcmmnmmnol * Bu- _ v, _ _
ccd .lo'r Rgu , ] nh No bn!» bX.
ị Ĩ>ếễkigLnlẵ pI'DIDGK ImmnllilẫhỉmmI B 0 RT Ẹ N AT MÍg D'NSX
' - Lyophúzod n 1) H!)
1 Wưnlua:Tobexotdhy mlaulon me Fgf ủhs ỈfflĩVOUOUS |Wn “ P
’ prucn'pt'non of mOncologblonlp. For ungb use MN
Donge;m ủnzclndbylhephygieign \tanui'acmrcd b\_ ` 5… nút bởlĩ
Rudaccompanv'mg pxkngc: imun N ATC o
íordcmloddosage,dừuclions fofuu PHARMA LNITffl IẦĨCỦ O . . . . . .
mdprecauu'um. Pin! \'n 19. anrmacm Sclaqm. O . . O...
m……mm, l'nnuldmnđ o oợoooo
«___… . __ JE'ẵìếằ'ỉỗ’. - …- - _. -… -
Rx thuốc bán theo dơn
BORTENAT
(Bột đông khô pha tiêm tĩnh mạch Bortezomỉd)
MO TA
Bortenat (Bonezomib) là một thuốc chống ung thư chi được dùng tiêm tĩnh mạch (tiêm
mạch Ión nhanh).
Bortczomid là một acid boronic dipeptidyl đã được biển đổi, ở dạng ester boronic
mannitol, hình dạng đã được tái tạo, bao gồm ester mannitol cân bằng với cảc sản phẩm
thúy phân của nó, acid boronic monomeric.
Tên hóa học của bortezomib, acid boronic monometric, lả [(]R)-3—methyl-l-H(ZS)—l-
oxo-3-phenyl-2-[(pyrazinylcarbonyl)aminojpropyl} boronic acid.
Boxtczomib có câu trúc hóa học như sau;
Khối lượng phân từ lá 284.24. Công thức phân tử là CịọHỵsBNqu. Độ tan cùa
bortczomib giống như monomeric boronic acid, trong nước lá 3,3-3,8 mg/ml với khoáng
pH từ 2,0 tới (›,5.
THÀNH PHẨN
Mỗi lọ Bortenat 2mg chứa Bortezomib 2mg
Mỗi lọ Bortenat 3,5mg chửa Bortezomib 3,5 mg
DƯỢC LÝ LÂM SÀNG
Cơ chế hoạt động
Bohezomib là chất ức chế thuận nghịch hoạt tính giống chymotrypsin trên proteasomc
268 của tế bảo động vật có vú.
Bortezomib là một acid boronic dipeptide tổng hợp mới vởi tính đặc hỉệu cao đối với 268
proteasome và là một chất ức chế proteasome nhóm thứ nhất với hoạt tính chống ung thư.
Protcasome 268 là phức hợp protein lớn thoái bìến protein ubiquỉtin. Tồn tại trong cơ thể
con đường ubiquỉtin-proteasome đóng vai trò thiết yếu trong điều hòa nồng độ cảc
protein đặc hiệu nội bảo, do đó duy trì hằng định nội mô bên trong tế bảo. Ức chế
proteasome 268 ngăn chặn sự phân giải protein dích mã có thể ảnh hưởng dòng thảo tín
hiệu bên trong tế bảo. Sự cán trở cơ chế hằng định nội mô bình thường có thể dẫn đến
chết tế bảo. Thử nghiệm đã khẳng định rằng Bonezomib lá thuốc độc tính tế bảo đối với
nhiều loại tế bảo ung thư khảc nhau trên in vitro. Bortezomib gây trì hoãn sự phảt triến
khối u trên in vivo theo kiến khối u không lâm sảng, bao gồm u đa tủy.
Dược động học
Sau khi tiêm tĩnh mạch liều 1,3mg/mz, nồng độ bortezomib trong huyết tương đạt được
tối đa trung binh là 509ng/ml (từ l09-1300ng/mL) ớ bệnh nhân đa u tủy có độ thanh thải
creatinin từ 31 tới ]69ml/phút. Thời gian bán húy trưng bình của bortczomib sau liều đầu
tiên từ 9-15 giờ ở khoảng liều m- 1,4s tởi z,oo ngm² ở bệnh nhân có khối u ảc tinh tiến
triển. Dược động học cùa bortezomib khi dùng đơn thuần chưa được xác định hoản toản
ớ liều khưyến cảo trên bệnh nhân da u tủy.
Phân bố
Thể tích phân hố cùa bortczomib khi dùng dơn độc chưa được đánh giá ở lỉều khuyến cảo
trên bệnh nhân đa u tủy. Tỉ lệ gắn kết cùa bortezomìb với protein huyết tương người
trung bình khoảng 83% nồng độ từ lOO-lOOOng/ml.
C huyến hóa
Các nghiên cứu trên in vitro cho thấy rằng bortezomib được chuyến hóa chính bằng cảch
oxy hóa thỏng qua mcn cytochromc P450. Dường chuyến hóa chính thông qua khử gốc
boronate để tạo thảnh các chất chuyển hóa khử boronate và sau đó thủy phân thảnh một
số chắt chuyến hóa. Những chất chuyến hóa dcboronatc-boưezomib là chất không có
hoạt tính.
Thái trừ:
Dường thái trừ cưa bortezomib chưa được xảo định ở người.
cni ĐỊNH
BORTENAT (Bortezomib) dùng đường tiêm được chỉ định điều trị cho bệnh nhân đa u
tủy đã nhận ít nhất một đợt điều trị trước đỏ.
CHỐNG cni ĐỊNH
BORTENAT được chống chỉ định ở bệnh nhân mẫn cảm với bor’tezomìb, Boron hoặc
Mannitol.
CẢNH BÁO
uLf H
_ _?
' I
QR \' % ih ỉ'ãl
. J"
… _ 3
.M I
- - . L
… "Je ỔỎ -, T
ưưf, :. J. “w.l~J'
ug
o ›— , i'i lì .? 'UẺVt
ìì.- ư . › _
f“_iỤgli" f'l* .I I ".Ễlft E. ffl
iẻơử #—
lĨ-ub -ỄƯaẹúlẵúỹi "
gnsẹmt .l.›_—' n-
t….ẹr mẹ.. , mũ … .lr-w
… t…
…MJ "* ủ
z.sf—m= về-
I"I' 'ẩ`IỈỀ'LỄlỆ-eưẵqiỉh'vỉẹ-ủ'l Ề`i . hq'ã
’ ' ỉ .Ẹ"_F É' “v * * "
r 4.n`ỉ'
F Ỉ'FI-Mằẵl'ỉnỉ & ể.ililu -n.
- | 4
l
“ ']il
ư I'l`l n .. - …fn `... … "wễ
] l "
1
l
'=N It ẺW Ị:íừ all'lửõ .' lu IỈF *
' IIịíl aj
'Ivịiỉq Y:
I
-:'*_² -I_ ửnứổ?ỹfMẵũ ²
L I II“ 1
AI
| m 1_ Ở . ,.
’ & L! 'q' - lng 1: !ỈỮÍ_ ' ' .M t
s. … .. .Iaùlũffl - ỵn.i~ & .'m "
I | ẹi ủ“l ụ__ u.. F__uilhỆl_-
v.ắiả ,. J… n 1…
-… H fihiJ-hJIII _ w . ú,é . I…
9“ "|lf“ *iS-vfM n. 9 ° … ! “H ?
I
I . ,— n h lffl
~r ýl’ *J . A'Ể ' …o
_. ! .
I I !
.il li A
-I ` _
I
II
1
- k :.
I
BORTENAT nên dược chỉ định dưới sự gỉảm sát của bảo sỹ có kinh nghiệm trong điếu
trị ung thư.
THẬN TRỌNG
Bệnh thẩn kinh ngoại biên
Điều trị Bortezomib gây ra bệnh thần kinh ngoại bỉên mà nổi bặt là cảm giác ngoại biên,
mặc dầu một vải trường hợp bệnh lý thẳm kinh vận động cũng được bảo cảo. Bệnh nhân
có trước những triệu chứng (tê, đau hoặc cám giác nóng bòng tay hoặc chân) vả/hoặc cảc
dắu hiệu đau thần kỉnh ngoại bìên trước dó có thế sẽ bị nặng thêm (bao gồm—ìmức độ 3)
trong khi điều trị bằng bortcwmib.
Bệnh nhân nên dược giám sát cảc triệu chứng đau thần kinh, như là cảm giảc nóng bỏng,
tăng cảm, dị cảm, khó chịu hoặc đau thần kỉnh. Bệnh nhân mới bị đau lhần kỉnh ngoại
biên hoặc bị nặng lên có thế cần thay dối liều vả !ịch điếu trị bortczomìb (xem liều lượng
và cảch dùng).
Hạ huyết áp:
Thận trọng khi điều trị thuốc ở bệnh nhân có tiền sử hạ áp, ngắt và bệnh nhân bị mắt
nước. Kiếm soát hạ áp thế đímg có thể bao gồm điều chinh thuốc điều trị cao huyết ảp, bù
nước vả/hoặc dùng mineralcorticoids (xem tác dụng phụ).
Rôỉ loạn trên tim:
Bệnh nhân có yêu lô nguy cơ đôi với bệnh tim hoặc bệnh tim săn có nên được giám sát
chặt chẽ.
Xét nghiệm phòng thí nghìệm
Nên xét nghỉệm thường quỉ thông số huyết dỗ (dếm máu toản phần) trong suốt quá trình
diếu trị bortczomih.
Tác dụng phụ đường tiêu hóa
Diều trị với bortezomib có thể gây buồn nôn, tiêu cháy, tảo bón và nôn, nên thỉnh thoảng
bệnh nhân cẳn được cho dùng lhuốc kháng nôn và chống liêu chảy. Diều trị mất nước nên
dùng dịch thay thế và đung dịch điện gỉảỉ.
Giám tiếu cầu
Bortezomib được cho liên quan vởi giám tiêu câu, thường tiêu câu giảm thâp nhât ở ngảy
thứ 1 1 của mỗi chu kỳ và trớ vê mức ban đâu ở trước chu kỳ kế tiếp. Số lượng tiều cầu
giảm và phục hồi duy trì hằng định trong suốt quá trình điều trị và không có bằng chứng
cùa giám lìếư cầu tích lũy.
Trị lìệu hỗ trợ khi lượng tíếư cầu < zs,ooormcl vả tái điều lrị ở lìều được giảm hơn txcm
liều lượng cảch dùng vả tác dụng phụ).
Hội chứng ly giái khối u
Vì bodczomib lả thưốc độc tế bảo vả có thể tỉẽu diệt nhanh tế bảo ảc tính, biến chứng hội
chứng ly giải khối u có thể xáy ra. Bệnh nhân có nguy cơ bị hội chứng ly giải khổi u lả
những bệnh nhân có tống khối tế bảo ác tính lớn truớc đìều trị. Những bệnh nhân nảy nên
được gỉảm sảt chặt chẽ và cẩn thận trọng thich hợp.
Cảc biễn cổ trên gan:
Dã có bảo cảo vải trường hợp hiếm gặp suy gan cấp trên các bệnh nhân dùng nhiều thuốc
kết hợp và có tiền sử bệnh tiếm ắn trầm trọng. Cảo biến cố trên gan khảc đă được báo cảo
bao gồm sự gia tăng không triệu chừng về mcn gan, tăng bilurubỉn máu và viêm gan. Cảc
thay đổi nảy có thể hồi phục dựa vảo việc ngtmg điều trị bortczomỉb. Những thông tin
giói hạn ở các bệnh nhân kế trên.
Bệnh nhân suy gan
Bcrtezomib được chuyến hóa bời men gan và độ thanh thải bortezomib có thể giảm ở
bệnh nhân suy gan. Những bệnh nhân nảy nên được giám Sảt chặt chẽ về độc tính khi
đỉềư trị bortezomib.
Bệnh nhân suy thận
Chưa có sẵn thông tìn lâm sảng về sử tlụng bortczomỉb ở bệnh nhân có độ thanh thái
creatininc < 13 mL/phùt và bệnh nhân lọc máu. Những bệnh nhân nảy nến được giám sảt
chặt chẽ về độc tính khi điều trị với bortezomib.
Thông tin cho bệnh nhãn
Ánh hưởng tới khả năng lái xe và vận hảnh máy mỏc
Do Bortczomib có thể gây ra hạ huyết áp, mệt mói, choáng vảng, lả, nhìn mờ, bệnh nhân
nên thận trọng khi vận hảnh mảy mớc, lái xe.
Mẫt nước/hạ huyễt ảp
Bệnh nhân đang sử đụng trị liệu bortczomib cớ lhề bị nôn vả/hoặc tiếu chảy, bệnh nhân
nên được tư vắn về các biện pháp thich hợp để tránh mắt nước. Bệnh nhân nên được
hướng dẫn tìm đến tư vấn của y tế khi thấy cảc triệu chứng như chóng mặt, đau đẩu nhẹ
hoặc ngất xiu.
Tương tác th uốc
Các nghiên cứu trên in vitro cho thấy là Bortezomib là chất nến đối với cytochrome P450
3A4, 2C19, vả IA2. Bệnh nhân đang sử dụng đồng thời Bortezomib với cảc thuốc khảc
cũng ức chế hoặc cảm ứng cytochrome P450 nên được giám sát chặt chế đối với độc tính
cũng như nồng độ glucose trong máu và điều chỉnh liều thuốc đỉềư trị tiểu đường. Chưa
có các nghiên cứu tương tác thuốc chính thức được tiến hảnh với bortezomib.
Khả năng gây ung thư, đột biến gen, suy gỉảm khả năng sinh sản
Chưa có nghiên cứu nảo được bảo cáo về khả năng gây ung thư với bortczomib.
Bortezomib có thế có tảo dụng tiềm tảng trên khả năng sinh sản cùa cả nam và nữ
Thai kỳ nhóm D (xem phần Thận Trọng)
Phụ nữ có thai;
Bệnh nhân nên dược tư vấn về việc sử dụng cảc biện phảp trảnh thai hiệu quả để trảnh
mang thai.
Phụ nữ cho con bú
Chưa biết liệu bortezomib có được bải tiết vảo sữa mẹ hay không. Phụ nữ nên được tư
vấn là ngừng cho con bú khi sử dụng trị liệu Bortezomib.
Sứ tlụng trong nhi khoa
Tính an toản vả hiệu quả cúa Bontczomib ở trẻ em chưa được thiết lập
Sử dụng trong lão khoa
Không có sự khảc biệt tổng thể về sự an toản hoặc hiệu quả được quan sảt thấy giữa bệnh
nhân ì 65 tuối và bệnh nhân trẻ tuối hơn sử dụng Bortezomib; không thế loại trừ một số
người cao tuối nhạy cảm hơn với thuốc.
TÁC DỤNG PHỤ
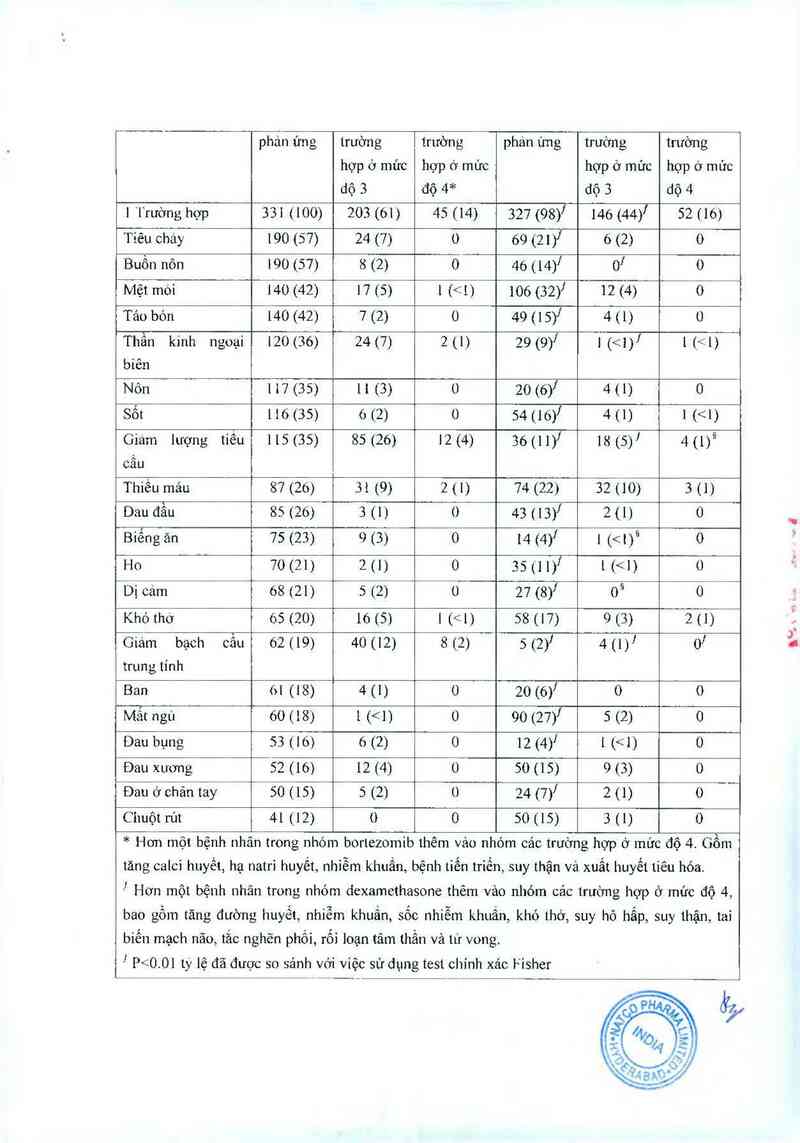
_Ễáng 3. Các tác dụng phụ được báo cảo trong quá trình điều trị là 15% hoặc hơn ở bệnh nhân sư
dụng bortezomib hoặc dexamethasone, gổm cả trường hợp ớ mức độ 3 và mức độ 4.
Trường hợp Bortezomib (N=331) [n(%)] Dexamcthasone (N=332) [n(%)]
Tât cả cảc Cảc Các Tât cả các Cảo Cảo
phán ứng trường trường phản ứng trường trường
hợp ở mức hợp ở mức hợp ở mức hợp ở mức
dộ 3 độ 4* dộ 3 dộ 4
1 1~…ờng hợp 331 (100) 20.3 (61) 45 (14) 327 (98)f 146 (44)f 52 (16)
Tiêu cháy 190 (57) 24 (7) o 69 (21)f 6 (2) (›
Buổn nôn 190 (57) 8 (2) 0 46 (14)f of 0
Mệt mòi 140 (42) 17 (5) 1 (<1) 106 (32)J 12 (4) o
Tảo bón 140 (42) 7 (2) 0 49 (15)f 4 (1) 0
Thần kinh ngoại 120 (36) 24 (7) 2 (1) 29 (9)f 1 (<1)f 1 (< 1)
biên
Nôn 117 (35) 11 (3) 0 20 (6)f 4 (1) 0
Sốt 116(35) 6 (2) 0 54 (16)f 4(1) 1(<1)
Giám lượng tiêu 115 (35) 85 (26) 12 (4) 36 (ml 18 (5)1 4 mã
cầu
Thiếu mảu 87 (26) 31 (9) 2 (1) 74 (22) 32 (10) 3 (1)
Dau đầu 85 (26) 3 (1) 0 43 (15)f 2(1) 0
Biếng ẩm 75 (2.3) 9 (3) 0 14 (4)f 1 (<1)5 ()
Ho 70(21) 2(1) 0 35(11)Ỉ 1(<1) o
Dị cảm 68 (21) 5 (2) o 27 (8)f 01 0
Khó thơ 65 (20) 16 (5) 1 (<1) 58 (17) 9 (3) 2 (1)
Giám bạch cầu 62 (19) 40 (12) 8 (2) 5 (2)! 4 (1 )J' 01
trung tính
Ban 61 (18) 4 (1) 0 20 (6)f 0 (›
Mẫt ngư 60 (18) 1 (<1) 0 90 (27)f 5 (2) 0
Dau bụng 53 (16) 6 (2) 0 12 (4)f 1 (<1) 0
Đau xương 52 (16) 12 (4) 0 50 (15) 9 (3) 0
Đau ở chãn tay 50 (15) 5 (2) 0 24 (7)f 2(1) () Ẹ
Chuột rút 41 (12) 0 0 50 (15) 3 (1) 0
* Hơn một bệnh nhân trong nhóm bortezomib thêm vảo nhóm các trường hợp ở mức độ 4. Gồm
tăng calci huyết, hạ natri huyết, nhiễm khuẩn, bệnh tiến trỉến, suy thận và xuất huyết tiêu hóa.
1 Hơn một bệnh nhân trong nhóm đcxamcthasone thêm vảo nhóm cảc 1rường hợp ở mức độ 4,
bao gồm tăng đường huyết, nhiễm khuẩn, sốc nhiễm khưấn, khó thở, suy hô hấp, suy thận, tai
biên mạch não, tăc nghẽn phối, rôì loạn tâm thân vảt1'r vong.
’ P
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng