













zOA- Luvoliz›io
’LoA-mvolexo- ABGS)IdH1H
I.IIBLIỊGỊA : ỊG)IJBW
mm |,a X oz :( gỳL - 01Ị8 LIOỤBO
S.oL 5qu. 6…oos annwxvs
>IOY\G SWe .
:› mc s…
3 592 SWd .
3 2130 SWd .
ỄO
10
Ẹln
1…
12
13
E
1ă
ịlIl
\
ợJỀ
ìWM K… IID u ; ui
~uu 1l1as nut vun um
'ưll5 … Dunm Buunu
uunu nq ums Mw: luuuu
;… …, 1Ẹ
f'ò ~ mm ủ
' ` _ ²TẢ ,
m
_ npumuibgm “’ ’ụ’ỳ’Ặ' “J
1: ;… ……mm ffl
. ĩ“ :
BAXMUNE 500
ẮXVHNVÌI
Each film coated tablet contains:
fểặ'ẳẫễ ; Mycophenolate Mofetil Ph.Eur ....... 500 mg
00 '
ỄỄỄ Dosage: As directed by
" the physician
Store below 30°C.
Keep in outer carton in order
to protect from light.
KEEP ALL MEDICINES OUT OF REACH
1
i
|
!
| protected trom moisture
|
|
|
|
1 OF CHILDREN
L
uxuuue sen Ju ~~MLJOC BÁN 'mED 01…
Mb: ler nin ban phưr ơiưa Mymnhemlm Mata…
vn [… SíDrrg uopv …~ mun snx- xxxxxx sò
» rasx uD~ um ~amm Nn um n; ' uAnbanhi
mb qu mn Jơ’c ›rinw .1~r ọt› Ilmq Mplhnỏr
d uu… u… xavg
\ Chỉdnn. caema’m crông cnimm cn lmogw
khác.- .… m mang năn sủ uung 11… in…
San uLâl nú1 R…ryuaomonut mm, An 00
mm… xxxxx
, ué1m.ee n ứr … us … Em: kỷ nm…g @… r…
ưu sủ qu
Visa No, XXXXX
Mfg. Lic. No MNBI061350
MADE IN INDIA
BANBAXY
LABORATORlES LJMITEDỔ
Village ~ Batamandi.
Paonta Sahib, Disựt. o1rrnour
Himachal Pradest — 173 025
uuẫvnuu/un mỉ"['ĩffl"mễp uẹ1
. /
J.ẸẮDỊI ẸIHd YG
aOna _Ă1 anò 3113
_ẹu A ỌH
Qj(fv1ỉỹ/Jỉãế
Clẵ.llel SHIHOlWOEVT
ẮXVENV'HỂ
ANBAXY
ABORATORIES LIMITED
BAXMUNE 500
Mycophenolate Mofetil Tablets
MADE IN INDIA
RANBAXY
LABORATORIES LIMITED
Village— Batamandi, Paonta Sahib,
Distt. Sirmour
Himachal Pradesh - 173 025
BAXMUNE 500
Mycophenolate Mofetil Tablets
MADE IN INDIA
RANBAXY
LABORATORIES LIMITED
Wlage- Batamandi, Paonta Sahib,
Distt. Sirmour
Himachal Pradesh — 173 025
Mfg Lic No. MNB/OS/3SO Mfg L1c. No MNBIDG/35E)
Balch No XXXXX
Exp ODMMIYY
Mycophenolate Mofetil Tablets
MADE IN INDIA
BANBAXY
LABORATORIES LlMITED
Village- Batamandi, Paonta Sahib,
Distt. Sirmour
Himachal Pradesh — 173 025
BAXMUNE 500
Mycophenolate Mofetil Tablets
MADE IN INDIA
RANBAXY
LA BORATORiES LIMITED
Wlage- Batamandi, Paonta Sahib,
Distt. Sirmour
Himachal Pradesh - 173 025
BAXMUNE 5DOmg Tabs. Foil
Strip size - 144 x 77mm
Ồ Foil width . 158 mm
Market : Vietnam
RLL/PKGDEV - CK21I04/11-V01
Mfg Lic. No MNB/OBIS5O Míg, Lic. No MNB/h
ọọc Kỹ HƯỔỊVG DẤN TR ựởc vKIịISỪDLOYG. ,
NỆU CẠN THẸM TJJONợ TIN, HAY HO! Y KIỆN CUA BAC sj.
THUỐC NA Y CHI DƯỢC SƯ DỤNG THEO SỰ KE ĐON CỦA BAC si
VIÊN NÉN BAXMUNE soo MG
(Vìên nén Mycophcnolatc Mofetil)
CẨNH BÁO
Ức chế miễn dịch có thể dẫn đểu tăng nhạy cảm với nhiễm khuẩn và có khả năng tiến
triễn đểu u bạch huyết. Chỉ những bác sĩ có kinh nghiệm trong trị liệu ức chế miễn
dịch và kiểm soát bệnh nhân được ghép thận, tim hoặc gan mới có thể sử dụng
Mycophenolate mofetil. Bệnh nhân đang dùng thuốc nên dược theo dõi trong cảc cơ
sở xét nghiệm thích hợp được trang bị tổt và được bố trí cản bộ nhân viên và có hỗ trợ
y tế thích hÃợp. Bác sĩ phụ trách việc trị liệu duy trì nên có thông tin hoản chỉnh cần
thiết cho việc theo dõi của bệnh nhân.
Người sử dụng thuốc là nữ giới trong độ tuõi sinh sản phải sử dụng biện pháp tránh
thai. Sử dụng Mycophenolate mofetil trong thai kỳ có liên quan đến tãng nguy cơ của
sự hư thai và ditjt bẫm sinh.
THÀNH PHẦN ỷ /
Mỗi viên nén bao phim có chứa: é/
Mycophcnolatc Mofetil Ph. Eur ......................................... 500 mg
Tá dược: .Microctystalline cellulose (Avicel Pll 102), Povidone (K-90), Croscarmellose
Sodium, Tale, Colloidal anhydrous silica, Magnesium stearate.
Thảnh phần bao phim: Opad1y Purple 20B50229, Hypromellose 3cp, Hydroxy Propyl
Cellulose, Titanium dioxide, Macrogol, Hypromellose 50cp, FD&C blue #2, Jron oxide red.
MÔ TẢ l ²
Viên nén Baxmune 500 mg chứa mycophcnolate mochil, 2- -mọrpholinocthyl ester cùa
mycophenolic acid (MPA), một chất ức chế miên dịch; chất ức chế mosine monophosphate
dchydrogenasc (IMPDH). Danh phảp hóa học cùa Mycophenolate mofetil 121 2-
morpholinoethyl (E)-6-( ] , 3-dihydro 4-hydroxy-ó—methoxy—7-methyl—3—oxo-S-
ísobenzofuranyl)-4-methy1-4-hexenoate.
Công thức phân từ lá CszleO'J,Và trọng lượng phân từ là 433,50. Công thức cấu tạo:
ẫ 0 0“ CM›
' O
; o `/`N
: ; OGH,
CH,
MYCOPHENOLATE MOFETIL
DƯỢC LÝ HỌC "²
0 Cơ chế tảc dụng
Mycophenolate mofetil 1ả ester 2- morphoiìnoethyl của MPA. MPA là một chẳt ức chế chọn
lọc, không cạnh tranh và có hồi phục cúa men inosine monophosphate dehydrogenase, vì vậy,
ức chế đường tồng hợp nucleotide guanosìnc trên de novo mã không sảt nhập vảo DNA. Vì sự
tăng sinh tế bảo iympho T và B phụ thuộc chặt chẽ vảo sự tống hợp purrincs trên de novo trong
1/13
khi cảc loại tế bảo khác có thể tận dụng cơ chế tải sử dụng nhân purinc, MPA có khả năng tảc
động kim tế bảo trên cảc tế bảo lympho đáng kể hơn hắn so với cảc tế bảo khác
0 Dược động học
Sau khi uông, mchphcno1ate mofetil được hẳp thu nhanh chóng và phần iớn ua chu ền hóa
iần đầu hoản toản thảnh chất chuyến hóa có hoạt tính, MPA Vì có chứng cứ cùa ức chế thải
gWau khi ghép thận, hoạt tính ức chế miễn dịch của Myc0phcnolate mofetil có liên
quan đến nông dộ MPA. Sinh khả dụng truạg—bình cùa mycophenolate mofetỉl dạng uống, dựa
vảo diện tích dưới dường cong cùa MPA, @ 94 96 tương dối với mycophenolate mofetil dạng
tiêm tĩnh mạch Thức ăn không ảnh hưởng đến mức độ hấp thu (MPA AUC) cùa
mycophenolate mofetil khi được dùng các liều 1 ,5g x 2 lần/ngảy cho bệnh nhân ghép thận
Tuy nhiên, Cmax cùa MPA giảm 40% khi có sự hiện diện cùa thức ặn. Mycophenolate mofetil
không được phát hiện trong huyết tương sau khi uống. MPA ớ nổng độ thich hợp trên lâm
sảng, 97% găn kết với protein albumỉn huyết tương.
Vì có chu kỳ gan ruột, đinh thứ hai cùa MPA thường được quan sảt sau 6— 12 giờ sau khi
dùng thuốc. Gìảm AUC của MPA khoảng 40% có iiên quan đến việc sử dụng đồng thời với
cholestyramỉne (4 g x 3 lần/ngảy), cho thẩy rằng có một lượng đảng kế cùa chu kỳ gan ruột.
MPA dược chuyền hỏa chủ yêu bới men glucuronyl transferase thảnh dạng phenolic
glucuronide cùa MPA (MPAG), chất khỏng có hoạt tính dược Iỷ.
Một iượng không đảng kế được bải tiết ở dạng MPA (< 1 % lỉều dung) trong nước tiếu. Dùng
dạng uõng mycc›phenolate mofetil dảnh dấu phóng xạ dẫn đến hồi phục hoản toản liếu đã
dùng với 93% liếu dùng được hồi phục trong nước tiêu và 6% liều đã dùng hồi phục trong
phân Hầu hết (khoảng 87 %) liếu đã dùng được bải tiểt trong nước tiều ở dạng MPAG.
Cảc nồng độ phát hiện được trên lâm sảng, MPA vả MPAG không được loại khói cơ thể bằng
thẩm phân mảu Tuy nhiến, tại nồng độ huyết tương cao cùa MPAG (> IOOụg/mi), một lượng
nhỏ MPAG được loại khỏi cơ thể.
Trong giai đoạn sớm sau khi ghép tạng (< 40 ngảy sau khi ghép), bệnh nhân được ghép thận,
tim và gan có AUCs trung binh cùa MPA lả thấp hơn khoảng 30% và có C,… thấp
khoảng 40 % so với khoảng thời gian muộn sau khi ghép (3— 6 tháng sau khi ghép).
Suy chức năng !hận
Trong một nghiên cứu dùng liều duy nhất (6 bệnh nhânlnhóm), AUC cùa MPA trung …
trong huyết tương quanl sát được ở cảc bệnh nhân suy chức Inăng thận nặng mãn tỉnh (ti lẹ ọc
câu thận < 25 mhphút" '1 ,73 m 2) cao hơn 28—75 % so với AUC trung binh quan sảt được ở
người bình thường khỏe mạnh hoặc so với cảc bệnh nhân suy chức nãng thận ở mức dộ nhẹ
hơn. Tuy nhiên, AUC cùa MPAG trung bình khi dùng Iỉếu duy nhất cao hơn 3— 6 1ần ở bệnh
nhân suy chức năng thận nặng so với người suy chức năng thận nhẹ hoặc người bình thường
khóe mạnh, phù hợp với dảo thải qua thận dã được biết cùa MPAG. Liều đa của
mycophcnolate mofetil khi dùng cho bệnh nhân suy chức năng thặn nặng măn tính chưa được
nghiên cứu. Không có dữ liệu thích hợp cho bệnh nhân ghép tim hoặc ghép gan bị suy chức
năng thận nặng măn tính.
Mãnh ghép lhận chậm hoạt dộng
Ở bệnh nhân có mảnh ghép chậm hoạt động sau khi ghép, AUC í;~)-~ 21, trung bìnhcị1a MPA có
thường. AUC 0~1211 cùa MPAG trung bình trong huyễt tương cao gắp 2— 3 lần so với cảc bệnh
nhân sau ghép cơ quan có tiến triến bình thường Tăng nhẹ phẩn tự do vả nồng độ huyết tương
cùa MPA ở bệnh nhân có mảnh ghép thận chậm hoạt động Điều chinh liều của
mycophenolate mofetil dường như không cân thiết.
Suy chức nãng gan
Ở người tinh nguyện bị xơ gan do rượu, quá trinh glucuronide hóa MPA ở gan không bị ảnh
hướng một cảch tương đối do bệnh như mô gan. Tảc dộng cùa bệnh gan trên quá trình nảy có
khả nảng phụ thuộc vảo bệnh riêng biệt. Tuy nhiến, bệnh gan kem tốn thương mặt, như xơ gan
mật tiên phát, có thể cho tác động khảo nhau
Trẻ em và Ihanh thiếu niên (tuốí từ 2 đến 18)
Cảo thông số dược động học được iượng giá ở 49 bệnh nhi ghép thận dùng 600 mg/m2
mycophcnolate mofetil bằng đường uống, ngảy 2 lần. Liều nảy cho AUC cùa MPA tương tự
như AUC quan sát được ở bệnh nhân là người trưởng thảnh được ghép thận dùng
Mycophenolatc mofetil với Iiếư lg, 2 lần/ngảy trong khoảng thời gian sớm và muộn sau khi
ghép Giá trị AUC cùa MPA trong cảc nhóm theo tuối tảc là tương tự trong khoảng thời gian
sớm vả muộn sau khi ghép.
Bệnh nhân cao mái (265 tuổi) 2
'l`ảc động dược động học cùa mycophenolate mofetil ở người cao tuôi chưa được lượng giá
một cảch chính thức.
Th uốc ngừa thai dùng đường uổng
Dược động học cùa thuốc ngừa thai dùng đường uống không bị ảnh hướng khi dùng đống thời
với mycophenolate mofctìl. Một nghiên cứu dùng đồng thời mycophenolate mofetil (lg,
21ần/ngảy) và thuốc ngửa thai dùng đường uống chứa ethinylestradiol (0 Ong đến 0 ,04mg)
vả Icvonorgestrel (0, 05mg đến 0,15mg), desogestrel (0,15mg) hoặc gestodene (0, 05mg đến
0,10mg) tiến hảnh ở 18 phụ nữ không ghép tạng (không dùng các thuốc ức chế miên dịch
khảc) trên 3 chu kỳ kinh nguyệt cho thấy khỏng có sự ảnh hưởng tương quan trên lâm sảng
cùa Mycophcnoiate mofetil trên sự ức chế rụng trứng cùa thuốc ngừa thai đường uống. Nồng
độ huyết thanh của LH, FSH vả progcstcrone không bị ảnh hướng đáng kể.
cui ĐỊNH ' ²
Mycophenolate mofctil được chỉ định phối hợp với ciclosporin vả corticosteroids trong phòng
ngừa thải ghép cấp tính ở bệnh nhân được ghép thặn, tim hoặc gan dị thân.
LỊÊU_LƯỢNG vÀ cÁcư nL`JNG'~²
Bãt đâu sử dụng và duy tri sử dụng mycophcnolatc mofetìl nên được quyết định bời cảc
chuyên gỉa ghép tạng đã được đảo tạo phù hợp.
Sử dụng trong ghép thận
Người trường thảth Dùng Mycophenolate mofctil dưìmg uống khới dấu trong vòng 72 giờ
sau khi ghép. Liều dùng khuyến cảo cho bệnh nhân ghép thận lả lg, 2 lẳn/ngây (liếu hằng
ngảy 1ả 2g).
Trẻ em và thanh thỉếu nien (2 đến 18 luối): Liều đùng khuyến cáo của mycophenoiate mofetil
là 600 mg/m2 dùng đường uống 2 lần/ngây (tối đa là 2g hắng ngảy). Viên n › ~ '
mofetìl chi được kê toa cho bệnh nhân có diện tích bề mặt cơ thể trên 1, 5 ' ' ọr `
2 Iằn/ngảy (iiều dùng 2_g hằng ngảy) Vì một số pháp ứng phụ xảy ra với tẫn suất cao hơn
trong độ tuối nảy so với người trương thảnh, giảm lỉều tạm thời hoặc dùng thuốc giản đoạn;
diếu nảy phải cân lưu ý đến cảc yêu tố tương quan trên [âm sảng gổm cả mức độ trầm trọng
của phản ú~.ng
Trẻ em (< 2 tuồi): Dữ liệu tinh an toản và hiệu quả bị giới hạn ở trẻ em dưới 2 tuổi. Cảo dữ
liệu nảy không t_hích hợp dế khuyến cảo 1iếu lượng thuốc và vì vậy không khuyến cảo sư dụng
thuốc cho độ tuồi nảy.
Sử dụng rrong ghép tim
Người trưởng thảnh: Dùng Mycophenolate mofetil đường uống khời đầu điều trị `trong vòng 5
ngây sau khi ghép. Liều lượng khuyến cảo cho bệnh nhân ghép tim 1ả 1 ,5g x 2 1ầnlngảy (liều
3g hằng ngảy).
Trẻ em: Không có dữ liệu thích hợp cho bệnh nhi dược ghẻp tỉm.
Sử dụng Irong ghép gan
Người lrưởng thânh: Dùng Mycophenolate mofetii dường tiêm tĩnh mạch trong vòng 4 ngảy
sau khi ghép gan, với Mycophenolate mofetil dùng dạng uống thì phải uống sớm ngay sau khi
ghép vì nó có thể bị dung nạp thuốc. Liều uống khuyến cảo ở bệnh nhân ghép gan ớ 1,5g x 2
lần/ngảy (liếu 3 g hằng ngảy).
Trẻ em: Không có dữ liệu thich hợp cho bệnh nhi được ghép gan.
Sử dung ở người cao luồi (> 65 tuối): Liều khuyến cảo lả lg x 2 iần/ngảy cho bệnh nhân ghép
thận vả 1,5g x 2 lầnlngảy cho bệnh nhân ghép tim hay bệnh nhân ghép gan.
Sư dụng thuốc khi suy chức nãng thận Ớ bệnh nhân ghép thận bị suy chức năng thận nặng
(tỉ lệ lọc cằu thận < 25 ml phút' —1, 73 m 2), ngoải khoảng thời gian ngay sau khi ghép, nên
tránh dùng Iiếu cao hơn 1 g x 2 lần/ngảy. Các bệnh nhân nảy nên được giảm sảt cân thận.
Không cân thiết chỉnh liều ớ cảc bệnh nhân có mảnh ghép thận chậm hoạt động sau phẫu
thuật Không có dữ iiệu thích hợp cho cảc bệnh nhân ghép tim hoặc ghép gan bị suy chức
năng thận nặng và mãn tính.
Sư dụng thuốc khi suy chưc năng gan nặng: Không cần chinh liều cho bệnh nhân ghép thận
bị bệnh như mô gan nặng. Không có dữ liệu thich hợp cho các bệnh nhân ghép tim có bệnh về
nhu mô gan nặng
Diều trị giữa các khoảng thời gìan Ihãi ghép: MPA (acid mycophcnolic) lả chẳt chuyến hóa
có hoạt tính của mycophenolatc mo_fetil. Thải mảnh ghép thận không dẫn đến thay đổi dược
động học cùa MPA; không yêu cầu giảm liều hoặc sử dụng cảch quãng Mycophenolate
mofetil. Không có cơ sơ cho sự điều chính liều dùng của Mycophenolate mofetil sau thải ghép
tim. Không có dữ liệu dược động học thích hợp trong thời gian thải ghép gan.
CẨNH BÁO VÀ THẬN TRỌNG ' ²
Bệnh nhân dùng phảc đổ ức chế miễn dịch trcng dó sử dung nhiều thuốc, gồm có cả
mycophenolatc mofctil, bị tăng nguy cơ tiến triên u bạch huyết vả cảc bệnh lý ảc tính khảo,
đặc biệt trên da Nguy cơ dường như có liên quan đến cường độ và thời gian ức chế miễn dịch
hơn là sư dụng bất kỳ thuốc chuyên biệt nảo Thông tin chung để hạn chế tối da nguy cơ ung
thư da, đó là hạn chế phơi nhiễm với ảnh nắng và tia UV bằng cách mậc ảo quần bảo vệ và sử
dụng sản phầm chống năng với yếu tố chống năng cao
Nên _hướng dẫn bệnh nhân dùng rpycophenolate rụof`etìi phải báq cảo ngay lập tức khi có bất
cứ bãng chứng nhiễm trùng, có vẽt thâm hoặc xuât huyêt hoặc bât cứ biên chứng của suy tùy
xương không rõ nguyên nhân.
Bệnh nhân được điều trị với ức chế miễn dịch, gồm mycophenolate mofetil, tăng nguy cơ
nhiễm trùng cơ hội (vì khuấn, nắm, virus vả nguyên bảo), nhìễm trùng và cảc nhiễm trùng gây
tử vong. Trong số các nhiễm trùng cơ hội là vỉrus BK liên quan đển bệnh thận và JC virus liên
quan đến bệnh lý chất trắng đaô tiến triến — progressỉve multifoca! leukoencephalopathỵ
(PML). Cảc nhiễm trùng nảy thường có liên quan dến cường độ ức chế miên dịch và có thể
dẫn đến các tinh trạng bệnh trầm trọng hoặc từ vong mả bác sĩ nên cân nhắc trong chấn đoản
phân biệt ở cảc bệnh nhân bị ức chế miễn dịch có chức năng thận bị suy giảm hoặc có cảc
triệu chứng về thần kinh.
Giảm bạch cầu trung tính nặng [số lượng bạch cầu trung tính tuyệt đối (ANC) 65 tuối): Bệnh nhân cao tuối (> 65 tuối) có thế thường tăng nguy cơ
phản ứng phụ do sự ức chế miễn dịch. Bệnh nhân cao tuổi dùng Mycophenolate mofetil là một
thảnh phần trong phảc đồ ức chế miễn dịch phối hợp, có thể tăng nguy cơ cùa một số nhiễm
trùng (gổm bệnh xâm lấn mô do cytomegalovirus) và có khả năng xảy ra xuất huyết dạ dảy
ruột vả phù phồi, so với các bệnh nhãn trẻ hơn.
Các phản ửng phụ khăc: Các phản ứng phụ, có thế hoặc có fkỵ/năng liên quan đến
mycophenolate mofetỉl, được báo cảo ờ >1l10 và ở >1/100 dến <1/10 sô bệnh nhân được điều
trị với mycophenolate mofetỉl trong cảc thử nghiệm lâm sảng có đối chứng ở bệnh nhân ghép
thận (dữ liệu 2 g), bệnh nhân ghép tim và gan được liệt kê trong bảng sau đây.
Các phản ửng phụ, có thế hoặc có khả năng liên quan đến Mycophenolate mofetỉl, được
bâo cáo ở các bệnh nhân được điều trị với Mycophenolate mofetỉl trong cảc thử nghiệm
lâm sảng trên thận, tim và gan khi sử dụng phối hợp với Ciclosporin vả Corticosteroids
Trong phân loại hệ cơ quan, tảc dụng không mong muốn được liệt kê theo tằn suất, sử dụng
phân loại sau đây: rất thường xuyên (>1/10); thường xuyên (>I/IOỌ đến <1/10), không thường
xuyên (>1/1 000 đến 1/10. 000 đến <1/1. 000); rất hiếm (<1/10. 000), không
biết (không thể đảnh giá từ dữ liệu sẵn có) Trong mỗi nhóm tằn suất, tảc dụng không mong
muốn được thế hiện theo thứ tự giảm tính trầm trọng.
Phâp loại hệ cơ quan Phân ứng phụ của thuốc
Nhiêm khuấn vả nhiêm ký sinh Rât thường Nhiêm trùng, nhiêm candida dạ dảy ruột, nhiêm
trùng xuyên trùng đường tiếu, nhiễm herpes sìmplex nhiễm
herpes zoster
Thường xuyên Viêm phối, củm, nhiêm trùng đường hô hâp,
nhiễm candida hô hấp, nhiễm trùng dạ dảy ruột,
nhiễm candida, viêm dạ dảy ruột, nhỉễm trùng,
viêm phế quản, viêm họng, vi nhìễm
trùng da do nẩm, nhiễm JEM ơihiễm
candida am đạo, viêm mũi (XM
Ữ\Ậ/l3
Phân loại hệ cơguan
Phản ứng phụ của thuốc
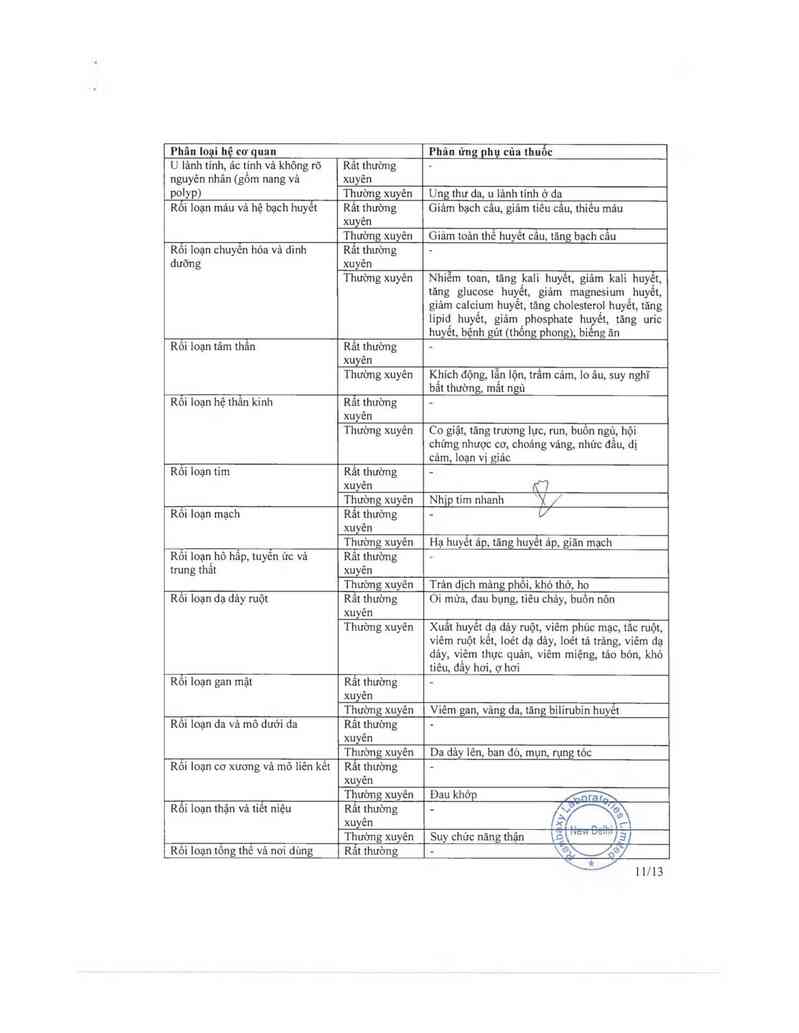
U lảnh tính, ảc tỉnh và không rõ Rỉthuờng -
nguyên nhân (gốm nang vả xuyên
polyp) Thường xuyên Ung thư da, u lảnh tính ở da
Rối loạn mảu và hệ bạch huyêt Rât thường Giảm bạch cẩu, giảm tiếu cẳu, thiếu mảu
xuyên
Thường xuyên Giảm toản thề huyết câu, tăng bạch Ệìu
Rôi loạn chuyên hóa và dinh Rât thường -
dưỡng xuyên
Thường xuyên
Nhiêm toan, tăng kali huyêt, giảm kali huyêt,
tăng glucose huyết, giảm magnesium huyết,
giảm calcium huyết, tăng cholesterol huyết, tãng
lipiđ huyết, giảm phosphate huyết, tảng uric
huyêt, bệnh gủt (thống phong), biêng ăn
Rôi loạn tâm thân
Rât thường
xuyên
Thường xuyên
Khich động, lẫn lộn, trầm cảm, lo âu, suy nghĩ
bât thường, mât ngủ
Rôi loạn hệ thân kinh
Rât thường
xuyên
Thuờng xuyên
Co giặt, tảng trương lực, run, buôn ngứ, hội
chứng nhược cơ, choáng vảng, nhức đâu, dị
cảm, loạn vị giác
Rối loạn tim Rât thường …
xuyên (f7
Thường xuyên Nhịp tim nhanh )(
Rỗi loạn mạch Rât thường — V
xuyên
Thường xuyên Hạ huyêt áp, tăng huyêt áp, giãn mạch
Rối loạn hô hẳp, tuyến ức vả Rẫt thường —
trung thất xuyên
Thường xuyên Trản dịch mảng phôi, khó thờ, ho
Rôi loạn dạ dảy ruột Rât thường Oi mứa, đau bụng, tiêu chây, buôn nôn
xuyen
Thường xuyên
Xuât huyết đạ dảy ruột, viêm phúc mạc, tăc ruột,
viêm ruột kẽt, Ioét dạ dảy, loét tá trảng, viêm dạ
dảy, viêm thực quản, viêm miệng, táo bón, khó
tiêu, đầy hơi, ợ hơi
Rôi loạn gan mật Rât thường ~
xuyên
Thường xuyên Viêm gan, vảng da, tăng bilirubin huyêt
Rôi loạn da vả mô dưới da Rât thường -
xuyên
Thường xuyên
Da dảy lên, ban đò, mụn, rụng tóc
Rối loạn cơ xương và mô liên kêt
Rẵt thường
xuyên
Thường xuyên Đau khớp
Rối loạn thận và tiễt niệu Rfflờng ~ Ẩạắ ’sẮ
xuyên fảƠỉ,
Thường gyên Suy chức năng thận ị…ố\"w W"")Ễx'i
Rôi loạn tông thê vả nơi dùng Rât thường - \'ỔMỄÍ
W
11/13
~ƠỄÍÍi'ìh—Ỉciại hệ cơ quan Phản ứngphụ của thuốc
thuỏc xuyên
Thường xuyên Phù, sôt, ởn lạnh, đau, mệt mòi, suy nhược
Các đìếu tra nghiên cứu Rất thường -
xuyên
Thườngxuyên Tăng mcn gan, tăng creatinine huyêt, tăng
1actate dehydrogenase huyết, tăng ure huyết,
tãng phosphate alkaline huyết, tăng cân
Lưu ý: 501 (2 g Mycophenolate mofetỉl hằng ngảy), 289 (3g mycophenolate mofetỉl hằng
ngảy) và 277 (hăng ngây dùng 2g tiêm tĩnh mạch | 3g dạng uõng, Mycophenolate mofetỉl)
bệnh nhân được điếu trị trong nghiên cứu pha 111 đề phòng ngừa thải ghép trong ghép thận,
tìm và gan.
Các tăc dụng khóng mong muốn sau đây gồm các phản ứng phụ từ kinh nghiệm sau khi đưa
lhuốc ra thị trường:
Các Ioại phản ứng phụ trong thời gian sau khi đưa thuốc ra thị trường cùa mycophenolate
moi`ctil là tương tự với cảc phản ứng phụ quan sảt được trong cảc nghiên cứu ghép thận, tim
và gan có đối chứng. Cảo phản ứng phụ bổ sung dược bảo cảo trong thời gian sau khi đưa
thuốc ra thị trường được mô tả dưới đây với tần suất được bảo cảo đặt trong dấu ngoặc đơn
nếu được biết W
Dạ dờy ruột: tăng sản lợi (>1/100 đến <1/10), viêm ruột kếỈzếỗm viêm ruột kết do
cytomegalovirus (>1/100 dến <1/10), viêm tụy (>1/100 đến <1/10) Va teo nhung mao ruột.
Các rồi Ioạn Iiẻn quan đến sự úc chế miễn dịch. Cảc nhiễm trùng nặng đe dọa tinh mạng gồm
viêm mảng não, viêm mảng trong tim, nhiễm lao vả nhiễm mycobacterium không điến hinh
Cảo trường hợp virus BK liên quan đến bệnh thận, cũng như các trường hợp virus JC liên
quan đển bệnh lý chất trắng đa 0 tiến triến, đã được bảo cáo ở cảc bệnh nhân dược điều trị với
các chất' ưc chế miễn dịch, gồm mycophenolate mofetỉl.
Mất bạch cầu hạt (2111000 đến <1/100) và giảm bạch cẩu trung tinh đã được báo cảo; vì vậy,
thường xuyên theo dõi bệnh nhân dùng mycophenolate mofetỉl. Có cảc báo cáo về thiếu mảu
bẩt sản và suy tùy xương ở những bệnh nhân dược điếu trị với mycophenolate mofetỉl, một số
trong số bệnh nhân nảy đã tử vong.
Rối Ioạn ma'u vả hệ bạch huyết Các trường hợp bất sản nguyên hồng cầu đã được bảo cảo ở
bệnh nhân được diếu trị với mycophenolate mofetỉl.
Cảc trường hợp được phân lập vẽ hình thải bạch cẩu trung tính bất thường, gồm bất thường
Pelger-Huet măc phải, đã được quan sát ở cảc bệnh nhân được điều trị với mycophenolate
mofetỉl Cảc thay dối nảy không 1iên quan đến giảm chúc năng bạch cầu. Cảo thay đối nảy có
thể gợi ý một tinh trạng tăng sô lượng bạch cầu chưa thảnh thục trong sự thảnh thục cùa bạch
cầu trong các diều tra nghiên cứu huyết học, diều mả có thế bị diễn giải sai lả dấu hiệu cùa
nhiễm trùng ở các bệnh nhân bị ưc chế miễn dịch dùng mycophenolate mofetỉl.
Quá mẫn: Cảo phán ứng quá mẫn gồm phù nề thần kinh mạch vả phản ủng
bảo cáo.
Rối“ loạp hô hấp, tuyến ức và lrungjhầt: Có các bảo cảo được phân lập yề bệnh phồi kẽ vả xơ
hóạ phôi ở cảc bệnh nhân được điêu trị với mycophenolate mofetỉl phôi hợp với các ức chế
miên dịch khác, một sô bệnh nhân dã tử vong.
QUÁ LIÊU '~²
Cảo báo cảo quả liếu xảy ra với mycophenolate mofetỉl từ cảc thử nghiệm lâm sảng và từ kinh
nghiệm sau khi đưa thuốc ra thị trưởng. Trong nhiều trường hợp nảy, không có tảc dụng phụ
nảo được báo cáo Trong cảc trường hợp quá liếu trong đó tác dụng phụ dã được bảo cảo, cảc
tảc dụng phụ nằm trong dữ liệu tính an toản đã được biểt của thuốc
Người ta cho rằng quá 1iều mycophenolate mofetỉl có khả năng ức chế quá mức hệ miễn dịch
và lảm tảng tinh nhạy cảm với nhiễm trùng vả suy tùy xương. Nếu giảm bạch cầu trung tính
tiến triến, nôn dùng Mycophenolate mofetỉl ngắt quãng hoặc giảm liều
Thẩm phân mảu không loại bỏ lượng thuốc đảng kể trên lâm sảng cùa MPA hoặc MPAG. Tác
nhân giữ acid mật, như cholestyraminc, có thể loại bỏ MPA bằng cảch lảm giảm chu kỳ gan
ruột cùa thuốc.
BẢO QỤẢN: Bảo quản đười 30°C, trảnh ậm. GIỮ THUỐC XA TÀM TAY TRẺ EM.
HẠPj DUNG: 36 tháng kế từ ngậy sản xuât. . _
KHONG DUNG THUOC QUA HẠN DUNG GHI TREN NHAN.
CUNG CẨP_: Hộp ] Vi 10 viên.
THAM KHAO
1. UK Summary of Product Characteristics ofCellcept 500 mg Tablcts, Roche
Registration Limited, October, 2009. _
2. US prescribìng information ofCellcept®, Hoffmann-La Rochc 1nc, February 2010.
Thóng tín được biên soạn văo lháng 3/201 ] .
Sản xuất tại Ản Độ
RANBAXY
Laboratories Limited
Village Batamandi, Paonta Sahib, District Sir our
Himachal Pradesh — 173 025
PHÒ" …tJ'C Tĩi ÍỜ\C
e/iẳh'ỉỷ'lJ’i Ị~£ểìồ «ÊLÝ'tỄỮỈỂÍỄ’
13/13
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng