



























77_VF/iiớo
1
59185094
M;utuupp TM
MIWWIPP Ì'WWW
'~WV9N`G
Tenoiovir Disoproxil
Fumarate/
Lamivudine/Eiavirenz
Tahlets
AVG NZA
3110111g3001110 400111q
--w
30 Tablets
_
Ủ]Mylan
Mylan.com
Í,
D E-1 ễ
34 ị—i
,… == ả ~i
1-Ĩ3 Q "Ề
>— Z @ :ỀỀ
ỂỄ Ế `Ồ.ễ attwotk-ioo%
ơ ấn ẳ
914
6 G ắ
Each 111… 1503151! 1311151 contains
Tenitiovtt đisopvoxil iumulte 31111 mg
Lamivuitint USP 31111mu
Fiutnmz USP 4011 mu
Do not store abovl 30'C.
St… in the oiiginll container.
Ptđlcl irom light. _
M: As dl… by … pnystctan.
NOT T0 EXCEED PRESCRIBED DOSAGE
KEEP OUT OF THE REACH AND SIBHT OF
CHtLDREN.
lnlatton. Wmlm ! …
Road thơ pactrage team Moto 1.150.
m: Fomưlttion contains Uctou.
Chaquc compnmó pellicule ocnhenti
iurnante đe lénciovư diloproul 1100 mg
Lamivutttne USP aoti mg
[iuimtz USP 406] mg
À conumt A une illl'lpíl’ittlfl ne đOpassam
pa 30'0.
Ầconwvordans l’cmtuihgn d'origine.
M 00 h Imnibn.
W: commo W w votn móđocin.
NE PAS otmssen u nose PRESCRITE.
TENIR HORS DE LA PORTÉE ET DE LA VUE
DES EMFANTS.
llttht. Ibn el nam 61 Mun:
Lm h notice mt utiiiutton.
lim n m: 00 thcment conthnt du
m.
1111
—
8l9 40!
16765
Fumarate de Ténoiovir
Disoproxil/
Lamivudine/Eiavirenz
Comprimés
AVONZA
“»
lx~Thnđchttthoobn
AVONIA
Mịù Mủvibubhopmeưự
Tudovtbmllỉmnù Mn;
mu
Ehv'lnz … ng
“Enp”lithobi
Bbqúiớmimmhhớiụqinso'c
Bbwbmhohigđe …như;
o;uuuủưmmmu
ƯIIIỤMỤ
sAnnủhới ưvuuunoumuuuum
PlaNo 11.12c13.…w…m
MmH—IIJmIILWGAWS.
ẵNũmMủybhủkẤubộ
K
30 Comprimós
iffllMylan
Wg. Llc. quUc. FỦ. Mo.z 2511/2014
NWIFlAPƯ.
"| Ithn …… Lhnitoớ
mm.n.tutamuumm
MMMI.MH.MWẸ
Mylm um.mm.nu
Myian.com
Unwinding Direction
GỈÌWOI`k _ 100% _
1ễẳ'
.ậịỉ a
_ iẳi
i
11
il
it
Ỉl
"i
li
111
iii
Eun mm cute! tu… cm…
iemf01.u06001011101111111120
75058162 llịI
IWI đtoJỗull …me Joo m
ti…"n'Ều'u ẾI'. L.… `'1111i111111113 E*fưirtìi1i
ẩiớ'f'n'ầ'i'ẩ'm’ẳẻiớwmmm F1111111'11i9i18161'101’211'0 D 1
mu…hymumm 1 a'11111101'W F1 ,
Ẹifâii'ớ'ẳfi’iềẳễfiềiì“ 2:% — . ~ ~
Mlllhnlhffllul: MW“ TwiiilfflỂ CỦNiỊNHTÌỔ` B.NolLot
mmm…mu
Muonựmnmuto enttm: ' MthFob.: ddlmmlyy
ễĩmwmutỉẽ=MImmu ẫẵ 3011…11.10111111411111110 ủ dd] m|
m .: m W
A…lmtmửmudipusat m.
Ammắuiwntẳhufẳahhniu suimb² "
htt…iâiớfớhớớtớibiư …… ““…… …ưii—r:…mu
_ Ithn u
m…undm m mm 11.121.131m5numu2ử
Lh Ilmtbuwtt utliatim.
ỰmugllezùmfflumcttccnhtllđuMnu. Mylan.com ủian W wtuTưiẵ'. um
THÔNG TIN CHO BỆNH NHÂN
AVONZA
Tenofovir Disoproxil Fumarate/ Lamivudine/ Efavirenz Tablets 300 m WO mg
Đọc kỹ hưởng dẫn sử dụng Irước khi dùng.
Đế xa tầm Jay má em.
T hóng báo ngay cho búc sỹ hoặc dược sĩ những lúc dụng khóng mong muốn gặp phải khi sử dụng
lhuốc.
T huốc nảy chi dùng Iheo đơn của bác sỹ.
THÀNH PHÀN
Mỗi viên nén bao phim chứa:
Tenofovir disporoxil fumarate 300 mg
Lamivudine 300 mg
Efavirenz 400 mg
Tá dược: cellulose vi tinh thề. croscarmellose natri. hydroxy propyl cellulose, natri lauryi sulfate. oxide
sắt vảng, lactose monohydrate. magnesi stearate, trắng Opadry 11 85F18422.
MÔ TẢ SẢN PHẨM
Viên nén bao phim mảu trắng đến trắng nhạt, hinh ovan có 2 mặt lồi, vát cạnh, được khắc chữ “’M` trên
một mặt vả “TLE” trên mặt còn lại.
QUY CÁCH ĐÓNG GÓI: Hộp 1 lọ HDPE x 30 viên nén bao phim.
THUỐC DÙNG CHO BỆNH GÌ
Tenofovir Disoproxil FumaratelLamivudine/Efavirenz 300 mg/300 mg/4OO mg lá thuốc điều trị nhiễm
virus HIV ở người lớn và thanh thiếu niên trên 12 tuồi.
NÊN DÙNG THUỐC NÀY NHƯ THẾ NÀO VÀ LIÊU LƯỢNG
Luôn luôn sử dụng Tenofovir Disoproxil FumaratelLamivudine/Efavirenz 300 mg/3OO mg/4OO mg theo
đúng Iỉều đã được kê đơn bời bảo sỹ. Điều nảy giúp đảm bảo rằng thuốc sẽ phát huy đẩy đủ tác dụng và
giảm nguy cơ phảt triền đề kháng thuốc. Bạn nên kiểm tra với bác sỹ, dược sĩ hoặc nhân viên y tế nếu
bạn cảm thấy không chắc chắn. Không được thay đổi liều trừ khi có chỉ định cùa bảo sỹ.
Liều thông thường là 1 viên mỗi ngảy. Nên uống Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/SOO mg/4OO mg lúc đói (1 giờ trước khi ăn hoặc 2 giờ sau khi
ăn). Uống nguyên viên Tenofovir Disoproxil FumaratelLamivudinelEfavirenz 300 mgl3OO mg/4OO mg
cùng với nước.
Việc uống Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg trước khi đi
ngủ có thề oỏ ích. Điếu đó giúp trảnh cảc rắc rối gây ra bời một số tảo dụng ngoại ý (như chóng mặt,
ngủ lơ mơ). Không được sử dụng thuốc nảy cho trẻ em (dưới 12 tuồi hoặc cân nặng dưới 40 kg).
Nếu bác sỹ cùa bạn quyết định ngừng 1 trong cảc thảnh phần cùa thuốc Tenofovir Disoproxil
Fumarate/LamỉvudinelEfavirenz 300 mgl3OO mg/4OO mg hoặc thay đổi liều cùa bất kỳ thảnh phần nảo
W
l"l Ắ'Ề ì-L
//JT\\
cùa thuốc, bạn có thế sẽ được kê đơn các chế phấm efavirenz, lamivudine vả/hoặc tenofovir riêng biệt
thay vì thuốc ớ dạng phối hợp hoặc cảc thuốc khảo để điều trị nhiễm 111v.
KHI NÀO KHÔNG NÊN DÙNG THUỐC NÀY
Không sử dụng Tenofovir Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/3OO mg/4OO mg:
> Nếu bạn dị ứng (quả mẫn) vởi efavirenz. lamivudine. tenofovir disoproxìl fumarate hoặc bất kỳ
thảnh phần nảo cùa thuốc. Khi đó, thông bảo ngay cho bảo sỹ và không được uống thuốc nảy.
`r Nếu bạn đang sử dụng St. John’s wort (H_1pericum pet_~forulum) ( một thuốc thảo dược điếu trị trầm
cảm và lo lắng) hoặc voriconazole (thuốc khảng nấm)
TẢC DỤNG KHÔNG MONG MUÔN
Giống như tất cả cảc thuốc khảo, Tenofovir Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/3OO
mg/4OO mg có thể gây ra cảo tác dụng không mong muốn nhưng không phải tất cả mọi người đều gặp
phải.
Thông báo cho bác sỹ nểu bạn gặp bất kỳ tác dụng nâo trong các tác dụng không mong muốn
dưới đây:
Các tảo dụng không muốn rất thường gặp
(Có thể ảnh hưởng nhiều hơn 1 người trong số 10 người)
> Chóng mặt
> Tiêu chảy, buồn nôn, nôn
> Phảt bạn ở da
> Thay đối chuyền hóa chắt béo biền hiện bời tãng nổng độ iipid trong mảu.
Các xét nghiệm có thể cho thấy:
> Nồng độ phosphate trong mảu thấp một cảch bất thường
Các tác dụng không mong muốn thường gặp
(Có thể ảnh hưởng 1 đến 10 người trong số 100 người)
> Đau bụng, đầy hơi
Cảm thấy yếu, sốt
Đau cơ vả khớp
Rối loạn chức năng gan biếu hiện bời tăng enzyme gan trong mảu
> Ho, cảc triệu chứng ở mũi
› Nhức đầu
> Giấc mơ bất thường, khó ngũ, buồn ngù, lo lắng, trầm cảm. rối loạn chú ý
> Mất tóc
> Ngứa
>
>
V
Câc tác đụng không mong muốn ít gặp
(Có thể ảnh hướng từ 1 đến 10 người trong số 1000 người)
› Thiếu máu (giảm hồng cầu có thề lảm bạn mệt và hụt hơi), giảm bạch Cầu (có thể lảm bạn dễ bị
nhiễm khuấn), giảm tiếu oầu (có thế lảm bạn dễ bị chảy máu).
W
i..i.u.
\“ \“ \J' \"
V \'
>
Thái độ giận dữ, ảnh hưởng đến tâm trạng, suy nghĩ bất thường, bồn chồn, trạng thải hưng phấn,
chứng cuồng (tình trạng đặc trưng bời cảc giai đoạn hoạt động quá mức. hứng khời hoặc dễ cảu
kinh). ảo giảc (hoang tường), hay quên. gặp cảc vấn đề về phối hợp. nhằm lẫn. có ý nghĩ và dự
định tự tứ. nhìn thấy hoặc nghe thấy những thứ không thực sự ở đó (áo giác).
Co gỉật
Hoa mắt, đầu óc quay cuồng (chóng mặt)
Nhìn mờ
Viếm gan vảng da hoặc vảng mắt, ngứa. hoặc đau bụng (viêm gan cấp)
Viêm tụy kèm đau bụng (vỉêm tụy oấp’)
Vú to ở đản ông
Phảt ban da nặng (hồng ban đa dạng, hội chứng Stevens-Johnson).
Cảo tác dụng không mong muốn hiếm gặp
(Có thể ảnh hưởng 1 đển 10 người trong 10.000 người)
\
7
>
Thừa acid lactic trong máu (nhiễm toan acid lactic — tảo dụng không mong muốn trầm trọng có thể
gây tử vong). Các tảo dụng không mong muốn sau có thế là dấu hiệu của nhiễm toan acid lactic:
o Thờ nhanh sâu
0 Ngủ lơ mơ
0 Buồn nôn, nôn và đau bụng
Cảo vấn đề về thận, bao gồm suy thận. Cảo triệu ohứng nảy có thế bao gồm buồn nỏn vả mệt mòi,
tiểu nhiếu vả khảt nước, cũng có thể dẫn đển mềm xương (kèm với đau xương và đối khi dẫn đến
gãy xương)
Các tác dụng không mong muốn rất hiếm gặp
(Có thể ảnh hưởng đến 1 người trong số 10.000 người)
`y/
V!
>
>
Thờ hụt hơi
Tồn thương thần kinh gây yếu và cảm giác đau nhói, châm chích hoặc tê, đặc biệt là ở bản chân và
tay (bệnh thần kinh ngoại vỉ)
Suy tủy xương sản xuất hồng cầu mới (suy tùy xương một dòng hồng oẩu)
Tốn thương tế bảo ống thận (hoại tử ống thận cấp)
Các tác dụng không mong muốn khác
v v
V
J
VVV
V
Tổn thương mô cơ
Rối loạn xương (như mềm xương (kèm đau xương và đôi khi dẫn đến gãy xương).
Nồng độ kali trong mảu thấp
Thay đổi hình dạng cơ thể do thay đối sự phân bố mỡ. Bao gồm mất mở ở chân, cảnh tay và mặt,
tăng mở ở bụng và cảc nội tạng, vú to và u mở ở sau cổ (gù trâu).
Sự xuất hiện cảc triệu chứng nhiễm khuấn lả một phần của hội chứng phục hồi miễn dịch.
Suy gan, gan nhỉễm mỡ
Viêm thận, tiểu nhiếu vả khải nước (đái tháo nhạt thận)
Tiếng huýt sáo, vang hoặc cảc âm thanh dai dắng ở tai (ù tai)
\ \\“ .'Ỉ
> Rung
> Bệnh tâm cản. tự tử thảnh công
> Ngứa phát ban gảy bời phản ứng với ảnh sảng (viếm da dị ứng ảnh sảng)
> Đó bừng mặt
Khi sử dụng Tenofovir Disoproxil Fumarate/Lamivudỉne/Efavirenz 300 mg/3OO mg/4OO mg cho thanh
thiếu niên. sự tãng trướng cùa xương có thế bị giảm.
Vui 1òng thòng bảo cho bác sỹ nếu có bất kỳ tảo dụng khỏng mong muốn nảo trở nên trầm trọng, hoặc
bạn để ý thắy có bắt kỳ tác dụng không mong muốn nảo không được lỉệt kê trong tờ hưởng dẫn sử dụng
nảy.
NÊN TRÁNI-I DÙNG NHỮNG THUỐC GÌ KHI ĐANG sử DỤNG THUỐC NÀY
Thông bảo cho bảo sỹ, dược sĩ hoặc nhân viên y tế nểu bạn đang sử dụng hoặc gần đây đã sử dụng bất
kỳ thuốc nảo, bao gồm cả cảc thuốc không kê đơn.
Không được sử dụng Tenofovir Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/3OO mg/4OO mg
với cảo chế phấm từ dược liệu oó chứa St. John’s wort (H_tpericum perforatum - được sử dụng đỉều trị
lo âu và trầm cảm) hoặc voriconazole (thuốc khảng nấm).
Ngoài ra, không nên sử dụng Tenofovir Disoproxil FumaratefLamivudine/Efavirenz 300 mgl300
mg/4OO mg cùng với cảc thuốc sau: `
> Astemizole hoặc terfenadine (thuốc điếu trị dị ứng theo mùa)
› Bepridil (thuốc điều trị bệnh tim)
> Cisapride (thuốc điều trị nóng rảt ngực)
> Cảo ergot alkaloid (ví dụ: ergotamine, dihydroergotamine, ergonovine vả meth_vlet
(thuốc điều trị migraine và đi… đầu từng chuỗi)
> Pimozide (thuốc điếu trị một số tình trạng tâm thần)
Không dùng Tenofovir Disoproxil Fumarate/Lamỉvudine/Efavirenz 300 mg/3OO mg/4OO mg nểu bạn đã
sử dụng oác thuốc khác có chứa emtricitabine, Iamivudine hoặc tenofovir disoproxil fumarate. Không
sử dụng Tenofovir Disoproxil FumaratelLamivudine/Efavirenz 300 mg/300 mg/4OO mg vả adefovir
dipivoxil cùng lúc.
Cần phải thông bảo cho bác sỹ nếu bạn sử dụng các thuốc khác có thể gây tốn thương thận bao gồm:
V
Aminoglycosides hoặc vancomycin (thuốc điếu trị nhiễm khuần)
Amphotericine B hoặc pentamidine (thuốc điều trị nhiễm nấm)
Foscamet, ganoiclovir hoặc cidofovir (thuốc điều trị nhiễm virus)
Adefovỉr dipivoxil (thuốc điếu trị nhiễm virus viêm gan B)
VVVV
Tacrolimus (thuốc điều trị suy giảm miễn dịch)
> 1nterleukin—2 (thuốc điều trị ung thư thận)
Cảo thuốc khảo có chứa didanosine (thuốc điều trị nhiễm HIV): Sử dụng Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg với các thuốc oó chứa didanosine có thề 1ảm
tăng nồng độ didanosine trong mảu. Hiếm khi, viêm tụy và nhiễm toan acid lactic (thừa acid lactic
trong mảu) đôi khi gây ohết đã được bảo cáo khi sử dụng các thuốc oó ohứa tenofovir disoproxil
W'
fumarate vả didanosine dồng thời. Phối hợp tenofovir với didanosine có thế lảm giảm tảo dụng của
thuốc khảng retrovirus.
Tenofovir Disoproxil F umarate/Lamivudine/Efavirenz 300 mg/3OO 111g/400 mg có thế tương tảo với các
thuốc sau và có thế lảm cảc tác dụng khỏng mong muốn xấu di hoặc có thể ảnh hướng đến hiệu quả cùa
thuốc:
> Amprenavir. atazanavir, darunavir. indinavir. lopinavir, maraviroc. nelfmavir. rỉtonavir. saquinavir
vả tipranavir (thuốc khảng virus).
Methadone, buprenorphine (thuốc điếu trị đau nặng hoặc lệ thuộc opioid)
C larithromycin. rifabutin hoặc rifampicin (thuốc khảng virus/thuốc trị lao)
\" \ '
Atorvastatin, pravastatin hoặc simvastatỉn (thuốc hạ lỉpid, oòn gọi lá các statin)
`Ị! ";
Thuốc tránh thai oó chứa hormon: dạng uống, tiêm hoặc que cấy tránh thai. Do đó, bạn nên thay
thế bằng cảc biện phảp trảnh thai như ngừa thai bằng vật chắn (như bao cao su) nếu bạn sử dụng
Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg.
Itraconazole, posaoonazole (thuốc khảng nấm)
Amodiaquine /artesunate, quinine, lumefantrine, halofantrine, artemisinines (thuốc khảng sốt rét)
Carbamazepine. phenytoin (thuốc chống co giật)
Diltiazem, verapamil, felodipine, nifedipine, nicardipine (thuốc chẹn kênh calci)
\›' V V V V
Tacrolimus. cyclosporine. sỉrolimus (thuôo ức chế miễn dịch)
Midazolam hoặc triazolam (thuôo ngù)
V
Warfarin (thuốc ngừa cục mảu đông)
CÀN LÀM GÌ KHI MỘT LẦN QUÊN KHÔNG DÙNG THUỐC:
Cố gắng tránh quên uống thuốc. Nếu bạn quên một liếu, sử dụng liều tiếp theo ngay khi có thế. Tuy
\l
nhiên, khi giờ uống liều kế tiếp sẽ đến trong vòng 12 giờ. hãy uống liều tiếp theo khi đến giờ uống
thuốc bình thường.
Nếu bạn bị nôn ngay sau khi uống thuốc, bạn nên uống một viên khảo. Đừng đợi cho đển khi đến gỉờ
uống liếu tiếp theo. _
CẦN BẢO QUẢN THUỐC NÀY THẾ NÀO:
Bảo quản ở nơi khô mảt, không quá 30 0C. Bảo quản trong bao bì gốc. Trảnh ảnh sảng.
Không sử dụng thuốc sau khi hết hạn ghi trên bao bì.
CÀN PHẢI LÀM GÌ KHI DÙNG THUỐC QUÁ LIÊU KHUYẾN cÁo
Nếu bạn uống quá nhiều viên Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mgl4OO mg, cần bảo ngay cho bảo sỹ hoặc trạm y tế gần nhất. Đem theo lọ thuốc bạn đã sử dụng để oó
thể mô tả những gì đã xảy ra.
NHỮNG ĐIỀU CÀN THẬN TRỌNG KHI SỬ DỤNG THUỐC NÀY
Thông bảo cho bảo sỹ nếu bạn bị bệnh thận hoặc cảc kết quả xét nghiệm oho thấy bạn có các vấn đề về
thận. Nếu có, có thể cần giảm liều cùa tenofovir vả lamivudine. Khi đó, nên dùng cảc chế phấm khác
có chứa efavirenz, lamivudine vả tenofovir thay vì Tenofovir Disoproxil
Fumarate/Lamỉvudine/Efavirenz 300 mg/3OO mg/4OO mg dạng phối hợp.
W
Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/300 mg/4OO mg có thể ảnh hưởng đến
thặn cùa bạn. Trước khi sử dụng thuốc nảy. có thế bạn cần phải thứ mảu để kiếm tra thận cùa bạn có
hoạt động tốt khòng. Cũng có thế cần phải thử máu trong suốt quá trinh điều trị để theo dõi chức nãng
thận.
Không sử dụng Tenofovir/Lamivudine/Efavirenz 300 mg/300 mg/4OO mg với oác thuốc Có thể gây tốn
thương thận. Nếu không thế trảnh khỏi việc sử đụng đồng thời, cằn kiềm tra định kỳ chức năng thận.
Không được dùng Tenofovir Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/3OO mg/4OO mg cho
trẻ em dưới 12 tuối hoặc cân nặng dưới 40 kg.
Trước khi sử dụng thuốc nảy, bạn nên thông bảo cho oảo bác sỹ về cảc vấn đề hiện tại hoặc tiền sử bao
gồm dị ứng, co giật, bệnh thần kinh, lạm dụng rượu hoặc oảo chất khảo.
Phát ban da nhẹ đến trung bình thường xuất hỉện trong 2 tuần đầu sử dụng Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg và luôn Iuôn phục hồi trong vòng 4 tuần sau
khi bắt đẩu điếu trị. Trong trường hợp phảt ban nặng, bạn cần thông bảo cho bảo sỹ ngay và có thế oần
phải ngừng Tenofovir Disoproxil FumaratelLamivudine/Efavirenz 300 mg/3OO mg/4OO mg.
Sau khi bắt đầu sử dụng Tenofovir Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/BOO mg/4OO
mg, cảc tác dụng không mong muốn rất thường gặp trên hệ thần kinh trung ương bao gồm chỏng mặt,
lẫn lộn, khó ngù. buồn ngủ, mất tập trung và giấc mơ bất thường và luôn luôn xuất hiện trong tuần điều
trị đầu tiên. Cảo tác dụng không mong muốn khác bao gồm mất trí nhớ, ảo giác. hưng phấn. trầm cảm,
có ý tường tự từ hoặc rối loạn tâm thẩn. Cảo tảo dụng không mong muốn nảy luôn luôn hồi phục trong
vòng 4 tuần điếu trị.
Thông bảo cho bảo sỹ và nhân viến y tế nểu bạn có tiến sư bị bệnh gan, bao gồm viêm gan. Các bệnh
nhân nhiễm HIV kèm bệnh gan bao gồm viêm gan B hoặc C mạn tính. người đã từng được điều trị
bằng thuốc khảng retrovirus có nguy cơ bị các biến chứng trên gan trầm trọng và có thể gây tử vong.
Nếu bạn bị nhiễm HIV và virus viêm gan B, bảo sỹ sẽ cân nhắc cấn thận về phảc đồ điếu trị tốt nhất
dảnh cho bạn. Nếu bạn có tiến sứ bị bệnh gan hoặc nhiễm virus viêm gan B mạn tính, bảo sỹ có thể
thực hiện thử máu để theo dõi ohức năng gan cùa bạn.
Cảnh giảc với các dấu hiệu nhiễm toan acid lactic (thừa acid lactic trong máu) một khi bạn bắt đầu
uống Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mgl3OO mg/4OO mg. Cảo dấu hiệu cùa
nhiễm toan acid lactic lả:
> Thờ nhanh. sâu
> Ngữ lơ mơ, buồn nôn và đau dạ dảy.
Tác dụng không mong muốn nảy hiếm nhưng nghiêm trọng, có thế lảm gan to và đôi khi gây tử vong.
Nhiễm toan aoid Iactic xuất hiện thường xuyến hơn ở phụ nữ và những bệnh nhân thừa cân. Nếu bạn bị
bệnh gan, nguy cơ bị nhiễm toan aoid Iactic của bạn sẽ oao hon. Trong khi điều trị bằng Tenofovir
Disoproxil Fumarate/LamivudinclEfavirenz 300 mgIBOO mgl4OO mg, bảo sỹ cùa bạn sẽ theo dõi chặt
chẽ bất kỳ dấu hiệu nảo của nhỉễm toan acid lactic. Nếu bạn nghĩ bạn oó thế bị nhiễm toan acid lactic,
hãy liên hệ ngay với bảo sỹ cùa bạn.
W
IC.
Cần cấn thận để tránh lây nhiễm cho người khảo. Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/BOO mg/4OO mg khỏng loại bỏ nguy oơ lây truyền HIV cho
người khảo thỏng qua quan hệ tình dục hoặc đường mảu. Bạn nến tiếp tục cắn trọng trảnh đế lây nhiễm.
Nếu bạn nhiễm HIV tiến triền (AIDS) và nhiễm khuấn cơ hội. bạn có thế có cảc triệu chứng nhiễm
khuấn và viêm hoặc lảm trầm trọng hơn cảc triệu chứng nhiễm khuấn khi bắt đầu điều trị bằng
Tenofovir Disoproxil FumaratelLamivudinelEfavirenz 300 mg/3OO mg/4OO mg. Nhũng triệu chứng nảy
có thế cho thấy hệ thống miễn dịch đang chiến đấu chống lại tinh trạng nhiễm khuấn. Cảnh giảc với oảo
dấu hiệu viêm hoặc nhiễm khuấn ngay sau khi bạn bắt đằu sử dụng Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/3OO mgl4OO mg. Nếu bạn chú ý thấy có cảc dấu hiệu viêm
hoặc nhiễm khuân, hãy thông báo với bảo sỹ hoặc nhân viên y tế.
Vải bệnh nhân sử dụng thuốc khảng retrovirus phối hợp oó thế phảt triền một bệnh trên xương gọi lả
hoại từ xương (chết mô xương gây ra bời mất nguồn cung cấp mảu cho xương). Thời gỉan diều trị bằng
thuốc retrovirus. sử dụng một corticosteroid như dexamethasone hoặc prednisolone, tiêu thụ rượu, suy
giảm miễn dịch nặng và thừa cân có thế là một số nguy oơ trong nhiều yếu tố nguy cơ phảt triến bệnh
nảy. Dấu hiệu hoại từ xương là cứng khớp. nhức và đau khớp (đặc biệt ớ hông, đầu gối vả vai) và khó
vận động. Nếu bạn thắy có cảo dấu hiệu nảy. hãy thông bảo cho bảo sỹ.
Cảo vấn đề về xương (đôi khi gây gây xương) có thể xuất hiện do tốn thương tế bảo thận. Sự tảng
trưởng của xương có thế bị ảnh hướng khi thảnh thiếu niên chưa phảt triến đầy đủ sử dụng Tenofovir
Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/3OO mgl4OO mg. Do đó. nếu bạn hoặc người được
điều trị là thảnh thiếu niên, bác sỹ sẽ cân nhắc cấn thận lợi ich và nguy cơ khi sử dụng Tenofovir
Disoproxil Fumarate/Lamivudỉne/Efavirenz 300 mg/3OO mg/4OO mg.
Bạn sẽ cần phải sử dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO
mg mỗi ngảy. Thuốc nảy giúp kiềm soát tinh trạng của bạn nhưng không phải là thuốc chữa khói tinh
trạng nhiễm HIV. Bạn có thề sẽ tỉếp tục tinh trạng nhiễm khuấn khác vả cảc bệnh khảo oó liên quan đến
HIV. Bạn nên khảm sức khỏe định kỳ. Không dược ngừng thuốc mà không thông bảo cho bảo sỹ.
PHỤ NỮ có THAI VÀ CHO CON BÚ
Không nên sử dụng Tenofovir Disoproxil Fumarate/Lamỉvudine/Efavirenz 300 mg/3OO mg/4OO mg
trong 3 thảng đầu của thai kỳ. Thông bảo cho bảo sỹ ngay nếu bạn đang có thai hoặc dự định có thai.
Nếu bạn có thải, bạn chỉ nên sử dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300
mg/3OO mgl4OO mg khi bạn và bảo sỹ đã thống nhất vỉệc dùng thuốc lá thật sự cằn thiết.
Cáo dị tật đã được ghi nhận ở bảo thai ở động vật vả trẻ sơ sinh từ người mẹ đã dược điều trị bằng
efavirenz trong thai kỳ. Do đó, nên trảnh có thai ở những phụ nữ sử dụng Tenofovir Disoproxil
Fumarate/Lamỉvudine/Efavirenz 300 mg/3OO mg|400 mg.
Nếu bạn lả phụ nữ đang sử dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mg/4OO mg, Iuôn luôn phải sử dụng các biện phảp ngừa thai bằng vật chẳn (ví dụ như bao cao su) cùng
với oảo biện phảp trảnh thai khảo bao gổm thuốc uống ngừa thải hoặc cảc biện phảp trảnh thải chứa
hormon khảo (que oấy, thuốc tiêm). Efavirenz 1ả một trong cảc thảnh phần có hoạt tính của Tenofovir
Disoproxil FumaratelLamivudine/Efavirenz 300 mg/3OO mg/4OO mg, có thế vẫn còn lưu lại trong mảu
W
› .
một thời gian sau khi đã ngừng. Do đó. bạn nên tiếp tục sử dụng cảc phương phảp trảnh thai như trên
trong 12 tuần sau khi bạn ngừng Tenofovir Disoproxil Fumarate/Lamivudinc/Efavirenz 300 mg/3OO
mg/4OO mg.
Nếu bạn muốn cho con bú. bạn nên thảo Iuận với bác sỹ về nguy cơ và lợi ích cùa việc cho con bú vởi
bảo sỹ cùa bạn.
LÁ] XE VÀ VẶN HÀNH MÁY MÓC
Chóng mặt. giảm tập trung. ngủ 1ơ mơ dã được báo cáo trong suốt quá trình điều trị bằng Tenofovir
Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg. Nếu bạn có cảc triệu chứng nảy.
bạn nến trảnh các hoạt động có thể gây nguy hiếm như lải xe hoặc vận hảnh mảy móc.
THÔNG TIN QUAN TRỌNG VỀ MỘT sò THÀNH PHẨN CÙA THUỐC
Nếu bạn đã được bảo sỹ thông bảo rằng bạn không thể dung nạp được một số loại đường. thông bảo
cho bảo sỹ trước khi sử dụng thuốc nảy.
Mỗi viên thuốc nảy có chứa 1,9 mmol (43 mg) natri. Bệnh nhân oần xem xét khi đang thực hiện chế độ
ãn kỉềm soát natri.
NÊU BẠN NGỪNG THUỐC
Khỏng được ngừng thuốc mà không thông báo cho bảo sỹ cùa bạn. Việc ngứng thuốc có thể ảnh hướng
nghiêm trọng đến sự đáp ứng cùa bạn đối vởi cảc thuốc diều trị trong tương lai. Nếu bạn ngừng
Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/SOO mg/4OO mg, thông bảo oho bảo sỹ
trước khi bắt đầu dùng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg.
Bảo sỹ có thế cân nhắc kê đơn cho bạn cảc thảnh phần cùa Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg một cảch riêng rẽ thay vì dạng phối hợp nểu
bạn gặp cảc vấn đề khi sử dụng thuốc hoặc cần điều ohinh liếu.
Khi thuốc Tenofovir Disoproin Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg sắp hết. cằn
lấy thếm thuốc từ bảo sỹ hoặc dược sỹ. Điều nảy rất quan trọng bời vì số 1ượng virus có thể bắt đầu gia
tảng nếu ngưng thuốc ngay cả trong một thời gian ngắn. Vìrus oó thể trở nến khó điếu trị hơn.
Nếu bạn bị nhiễm cả HIV và vỉrus viêm gan B, đặc biệt không dược ngừng thuốc mà không thông bảo
trước oho bảo sỹ. Vải bệnh nhân đã có kết quả xẻt nghiệm mảu hoặc triệu chứng cho thấy bệnh viêm
gan trở nên xấu đi sau khi ngừng lamivudine hoặc tenofovir disoproxil fumarate (2 trong 3 thảnh phần
của Tenofovir Disoproxi1 Fumarate/LamivudinelEfavirenz 300 mg/3OO mg/4OO mg). Nếu ngừng
Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 ng300 mg/4OO mg, bảo sỹ oó thế đề nghị
bạn quay trở lại điều trị viêm gan B. Bạn có thế cần phải thứ mảu để kiềm tra chức năng gan trong 4
thảng sau khi ngừng điếu trị. ớ vải bệnh nhân có bệnh gan tiến triến hoặc xơ gan, không khuyến cảo
ngừng điều trị vì điều nảy oó thể dẫn dến tinh trạng viêm gan xấu đi vả oó thể đe dọa tính mạng.
Thông bảo cho bảo sỹ ngay nếu oó triệu ohứng mới hoặc triệu chứng bất thường sau khi bạn ngừng
điếu trị, đặc biệt là oảo triệu chửng liên quan đến viêm gan B.
Nếu oần thêm thông tin xin hòi ý kiến bảo sỹ hoặc dược sĩ.
HẠN DÙNG: 24 thảng kể từ ngảy sản xuất
.IJ v'
"
Mylan
Sản xuất bời:
MYLAN LABORATORIES LIMITED
Plot No. 11. 12. & 13, Indore Special Economic Zone. Pharma Zone. Phảse—Il. Sector-Hl. Pithampur
454115. Dist. Dhar. Madhya Pradesh. Án Độ.
Ngăy xem xét sửa đổi, cập nhật:
'HƯỚNG DĂN SỬ DỤNG THUỐC CHO CÁN BỘ Y TẾ
AVONZA
Tenofovir Disoproxil Fumarate/ Lamivudine] Efavirenz Tạblets 300 mg/30 ~
THANH PHAN
Mỗi viên nén bao phim chứa:
Tenofovir disporoxil fumarate 300 mg
Lamivudine 300 mg
Efavirenz 400 mg
Tả dược: cellulose vi tinh thề, croscarmellose natri. hydroxy propyl oellulose. natri 1auryl sulfate.
oxide sắt vảng. lactose monohydrate. magnesi stearate. trắng Opadry II 85F18422.
DẠNG BÀO CHẾ
Viên nén bao phim.
DƯỢC LỰC HỌC
Phân nhóm dược lý điều trị: Thuốc khảng virus điều trị nhiễm HIV. dạng phối hợp, mã ATC:
JOSAR1 1.
Phân loại dược 1ỷ: 7.13 Thuốc khảng virus.
Cơ chế tác dụng:
Efạvirenz lá thuốc không nucleoside ức chế enzyme phiên mã ngược (reverse transcriptase) cùa HIV-
]. Efảvirenz gắn trực tiếp vảo enzyme vả chẹn các hoạt động của DNA polymerase phụ thuộc DNA
và phụ thuộc RNA bằng cách cảm ứng sự thay đổi cấu hinh không gian gây ra sự giản đoạn tại vị trí
xúc tảo cùa enzyme. Hoạt dộng cùa efavirenz không cạnh tranh với nucleoside triphosphates hoặc
chất tương tự nucleoside triphosphates. Enzym phiến mã ngược HIV-2 vả cảc DNA polymerase ở
eukaryote (như DNA polymerase 01. 13. y hoặc 8) không bị ức chế bởi efavirenz.
Lamivudine lả đồng phản tả truyền cùa 2`-deoxy—3`-lhiacytidỉne. có cẳu [1110 tương tự một
dideoxynucleoside.
Tenofovir disoproxil fumarate được biến đổi in vivo thảnh tenofovir, một nucleoside monophosphate
(nucleotide) tương tự adenosine monophosphate.
Lamivudine vả tenofovir được phosphoryl hóa bởi các enzyme nội bảo đế hinh thânh lamivudine
triphosphate vả tenofovir diphosphate. Lamivudine triphosphate vả tenofovir diphosphate ức chế oạnh
tranh với enzyme phiên mã ngược HIV—l, dẫn đến kết thúc chuỗi DNA. Cả hai chất nảy dều có hoạt
tinh kháng lại HIV-l vả HIV-2 cũng như khảng 1ại cảc virus viêm gan B.
Đề kháng:
Phần lớn bệnh nhân dã thất bại virus học trong khi sử dụng efavirenz sẽ đề khảng với efavirenz. Cảo
đột bỉến xuất hiện chủ yếu là K103N, Gl9OS/A/E vả Y188L, chỉ cần một trong những đột biến nảy là
đã đủ để gây đề kháng ở mức độ cao. Đế kháng chéo giữa efavirenz vả nevirapine hoặc delavirdine
rất rộng rãi; do đó bệnh nhân đã từng thất bại virus học với một trong số các thuốc nảy hẳn như có
chứa virus không nhạy cảm với efavirenz và ngược lại. Với sự tích lũy số lượng cảc đột biến NNRTI,
tính nhạy cảm với etravirine cũng sẽ bị ảnh hưởng.
W
'Do thời gian bản thải dải cùa efavirenz, sau khi ngừng một thuốc kháng retrovirus có hiệu quả có
chứa efavirenz. có thế có một thời kỳ giống như sử dụng efavirenz đơn trị. Điếu nảy có thể gây đế
khảng đáng kể và lảm giảm hiệu quả cùa efavirenz. nevirapỉne hoặc delavirdine trong tương Iải.
Trong nhiều trường hợp khi một phảc đồ điều trị có chứa lamivudine bị thất bại. đột biến M184V sẽ
được chọn lọc ở giai đoạn sớm. M184V gây đế khảng lamivudine ở mức độ cao ( giảm tinh nhạy cảm
> 300 lấn). Virus oó M184V tải bản kém hiệu quả hơn các chùng virus hoang dại.
Dữ liệu in vitro gợi ý rằng tiếp tục sử dụng lảmivudine trong phảo đồ kháng retrovirus mặc dù phảt
triến đột biến M184V Có thế cho hoạt tinh khảng retrovirus còn lại (hầu như thông quả giảm sự tương
thich virus). Sự phù hợp lâm sảng của cảc phải hiện nảy chưa được thiết lập.
Đề khảng ohẻo gây bới đột bỉến M184V bị giới hạn trong nhóm thuốc khảng retrovirus ức chế
nucleoside/nucleotide. M184V gây ra sự đề kháng ohẻo đầy đủ đối với emtricitabine. Zidovudine vả
stavudine duy trì oảo hoạt tinh khảng retrovirus đối vởi HIV-l đề kháng lamivudine.
Abaoav'ư duy trì hoạt tính kháng retrovirus đối với HIV-l dề kháng 1amivudine chi chứa đột biến
M184V. Đột biến M184V cho thấy giảm tính nhạy cảm với didanosine < 4 lần, ý nghĩa lâm sảng cùa
điều nảy vẫn chưa biết rõ.
Đột biến K65R được chọn lọc in vitro khi HIV-l dược nuôi cấy trong môi trường có tenofovir với
nồng độ tăng dằn. Nó cũng có xuất hiện trên in vivo khỉ thẳt bại vỉrus học với phảc đồ điều trị có chứa
tenofovir. K65R giảm tính nhạy cảm vởi tenofovir trên in vilro khoảng 2 iần vả có liên quan vởi sự
thiếu đáp ứng dối với phảc đồ chứa tenofovir.
Cảo nghiên cứu lâm sảng đảnh giá hoạt tính kháng HIV cùa tenofovir khảng lại cảc chùng HIV-l có
đột biến tương tự thymidine (TAMs) không được chọn lọc bởi tenofovir trên những bệnh nhân đã
từng điều trị. Bệnh nhân có HIV thể hiện ít nhất 3 đột biến TAMs có chứa hoặc M41 L hoặc L2IOW
cho thấy giảm đảp ứng vởi tenofovir.
Tính hiệu quả trên lâm sảng
Khi sử dụng tenofovir disoproxil fumarate vả lảmivudine phối hợp với efavirenz ờ nhĩmg bệnh nhân
nhiễm HIV-l chưa từng được điều trị, tỷ lệ bệnh nhân phân bố ngẫu nhiên ban đầu (1TT) có HIV-
RNA < 50 bản sao/rnl là 76,3% vả 67,8% ở tuần 48 và 144.
Không có nghiên cứu cụ thể sử dụng phối hợp tenofovir disoproxil fumarate, lamivudine vả efavirenz
trên thanh thỉếu niên.
DƯỢC ĐỌNG HỌC
Efavirenz:
Hấp thu vả sinh khả dụng:
Sinh khả dụng đạt 40% đển 45% khi không có thức ăn. Thức ăn lảm tăng hấp thư đảng kế. Thời gian
để đạt nổng độ đỉnh trong huyết tương (3 — 5 giờ) không thay đổi sau nhiếu liều vả nồng độ trong
huyết tương đạt trạng thải ổn định trong 6 — 7 ngảy.
Sảư khi uống liều đơn 1 viên Tenofovir Disoproxil FurnaratelLamivudine/Efavirenz 300 mg/3OO
mg/4OO mg ở những người tình nguyện khỏe mạnh, giá trị Cmax trung bình (iSD) oùa efavỉrenz là
2.689 (:t785) ng/ml và giá trị AUC o:th tương ứng là 64.850 (i21.728) ng.giờ/ml. Giá ttị tmax trung
bình của efavirenz lả 4,28 (i 1,61) giờ.
Phân bố
W
' Efavirenz gắn mạnh (hơn 99%) với protein huyết tương người, chủ yếu là ạlbumin. Cảo bệnh nhân
nhiễm HIV-l dã nhận efavirenz 200 đến 600 mg l lằn/ngảy trong it nhất 1 thảng. nồng độ trung bình
trong dịch não tùy là 0,69% so với nồng độ tương ứng trong huyết tương. Tỷ lệ nảy cao hơn khoảng 3
lằn so với phẩn không gắn với protein (dạng tự do) cùa efavirenz trong huyết tương.
Cluựến hóa
Efavirenz được chuyền hóa chủ yếu bới cytochrome P450 thảnh chất chuyến hóa hydroxylate hóa.
Những chất chuyến hóa nảy không có hoạt tính ohống HIV-l . C ảc nghiên cứu in vỉrro được hỗ trợ bởi
oảo ghi nhận trên in vivo gợi ý rằng C YP3A4 và C YP2B6 1ả cảc isoenzyme chịu trảch nhiệm chính
trong việc chuyến hóa efavirenz. Efavirenz cảm ứng cảc c;tochrome enzyme P450. kết quả lả gây
cảm ứng sự chuyến hóa cũa chính nó.
Đảo thải
Efavirenz Có thời gian bản thải pha cuối tương đối dải từ 11 dến 154 giờ sau khi dùng liều đơn và 40
— 55 giờ sau khi dùng nhiều liều. Ở những bệnh nhân có cảo kiều gen CYP2B6 đột biến (như kiến
gen T/T ở GSlóT), thời gian bản thải phả cuối có thế được kéo dải đáng kế và phơi nhiễm vởi thuốc
cao hơn. Những kiểu gen nảy đặc bỉệt phổ biến ở những người châu Phi vả người Mỹ gốc Phi. Ở
những bệnh nhân bị suy gan. độ thảnh thải efavirenz giảm và phơi nhiễm với thuốc cao hơn.
Khoảng 14 -34% cùa cảc liều efavirenz đảnh dấu phóng xạ được tìm thấy trong nước tỉếu và dưới 1%
liều được đảo thải trong nước tiều dưới dạng efavirenz không đối.
Lamivudine
Hấp !hu vả sinh khả dụng:
Lamivudine được hấp thu nhanh chóng sau khi uống. Sinh khả dụng dạt từ 80 đến 85%.
Sau khi uống lỉếu đơn 1 viên Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mg/4OO mg ở những người tình nguyện khỏe mạnh. C.,m trung binh (i SD) cùa lamivudine lả 2.483
(i706) ng/ml vả giá trị AUC tương ứng lả 13.457 (3: 3.717) ng.giờlml. Giá trị tmax trung bình (iSD)
của lamivudine lả 1,92 (:t0.93) giờ.
Sử dụng đồng thời lamivudine vởi thức ăn 1ảm trì hoãn tmax và giảm Cmỉm (giảm khoảng 47%). Tuy
nhiên, mức độ hấp thu lamivudine (dựa trên AUC) không bị ảnh hướng.
Phân bố
Cảo nghỉên cứu dùng lamivudine đường tĩnh mạch cho thấy thể tích phân bố biểu kiến trung bình là
1,3 l/kg. Lamivudine thể hiện dược động học tuyến tinh trong khoảng liều điều trị và thế hiện sự gắn
kết giởỉ hạn vảo protein albumin trong huyết tương (< 36% albumin huyết thanh in vitro).
Chuyến hóa
Chuyến hóa chi lả oon đường phụ trong sự đảo thải lảmivudine. Lamivudine ohù yếu được đảo thải
dưới dạng không đổi thông qua sự bải tỉết ớ thận. Khả năng tương tảo thuốc trong chuyến hóa với
lamivudine là rất thấp do chuyền hóa ở gan ở mức độ thấp (5 — 10%) và gắn với protein huyết tường
thấp.
Đảo thải
Thời gian bản thải cùa lamivudine được ghi nhận là 5 — 7 giờ. Thời gian bản thải cùa lamivudine
triphosphate nội bảo được xác định khoảng 22 giờ. Độ thanh thải toản thân trung binh của lamivudine
là khoảng 0,32 l/giờlkg, ohù yếu đảo thải ở thận (› 10%), bao gồm sự bải tiểt ờ ống thận qua hệ thổng
Jifi®
vận chuyên oatỉon hữu cơ.
' Đối lượng đặc biệt
Suy thận: Các nghiên cứu trên những bệnh nhản suy thận cho thấy sự đảo thải lamivudine bị ảnh
hướng bởi rối 1oạn chức năng thận. Giảm liều được khuyến oảo 6 những bệnh nhân có độ thanh thải
creatinine S 50 ml/phút.
Tenofovir disoproxil fumarate
Tenofovir disoproxil fumarate là một tiến chất ester có thể tan trong nước. được biến đổi nhanh chóng
trong in vivo thảnh tenofovir vả formaldehyde. Tenofovir được biến đổi nội bảo thảnh tenofovir
monophosphate vả thảnh phần có hoạt tính tenofovir diphosphate.
Hấp 1th
Sau khi uống tenofovir disoproxil fumarate bời những bệnh nhân nhiễm HIV . tenofovir disoproxil
fumarate được hấp thu nhanh chóng và biến đổi thảnh tenofovir. Sinh khả dụng đường uống của
tenofovir từ tenofovir disoproxil fumarate ở những bệnh nhân lúc đói là khoảng 25%.
Uống tenofovir disoproxil fumarate cùng với bữa ản giản chất béo lảm tăng sinh khả dụng đường
uống, tăng AUC của tenofovir khoảng 40% và Cmax khoảng 14%.
Sau khi uổng liều đơn 1 viên Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mg/4OO mg ở những người tinh nguyện khỏe mạnh. C,… của tenofovir trung bình (i SD) lả 277 (:1:
79) nglml vả AUC tương ứng lả 2.358 (i 627) ng.giờ/ml. T,… của tenofovir trung binh (:t SD) lả 1.17
(& 0,57) giờ.
Phân bố
Sau khi tiêm tĩnh mạch, thể tích phân bố của tenofovir ở trạng thái ổn định được xảo định khoảng 800
ml/kg. In vitro. sự gắn kết protein của tenofovir với protein huyết tương vả huyết thanh tương ứng
dưới 0,7 và 7.2% với nổng độ tenofovir trong khoảng 0.01 đến 25 ụg/ml.
Đảo thải
Tenofovir được đảo thải chủ yếu bởi thận thông qua sự lọc và hệ thống vận chuyến chủ động ở ống
thản, khoảng 70 — 80% liều được đảo thải dưới dạng không đồi trong nước tiều sau khi tiêm tĩnh
mạch. Thanh thải toản phần được xảo định khoảng 230 ml/giờlkg (khoảng 300 ml/phút). Độ thanh
thải thận được xảo định khoảng 160 ml/giờ/kg (khoảng 210 ml/phủt) vượt qua tỷ lệ 1ọc cầu thận. Điều
nảy thế hiện sự bải tiết chủ động ở ống thận đóng vai trò quan trọng trong sự bải tiết tenofovir. Sau
khi uống thời gian bản thải của tenofovir là khoảng 12 đến 18 giờ.
Cảo nghỉên cứu cho thấy con đường bải tiết chủ động ở ống thận cùa tenofovir lá được bơm vảo tế
bảo ống lượn gần bởi chất vận chuyền anion hữu cơ ở người (hOAT) 1 và 3 và đấy vảo nước tiểu bởi
protein khảng đa thuốc 4 (MRP 4). Các nghiên cứu in vitro đã xác định cả tenofovir disoproxil
fumarate vả tenofovir đều không phải là cơ chất oủa enzym CYP4SO.
Tuổi vả giởi tính
Dữ liệu dược động học oòn hạn chế oủa tenofovir ở phụ nữ cho thấy giới tính không có ảnh hưởng
lớn. Phơi nhiễm tenofovir đạt được ở những bệnh nhân thảnh thiếu niên sau khi uống tenofovir 300
mg ] lằn/ngảy tương tự với phơi nhiễm đạt được ở người lớn sử dụng tenofovir 300 mg dùng 1
lần/ngảy.
Cảo nghiên cứu dược động học chưa được thực hiện ở trẻ em hoặc ở người giả (trên 65 tuồi).
Chưa có oác nghiên cứu dược động học cụ thể được thực hiện trên những nhóm chùng tộc khảo nhau.
W
Suy thận
'Cảc thông số dược động học của tenofovir được xảo định sau khi sử dụng ] liều đơn tenofovir
disoproxil fumarate 300 mg trên 40 bệnh nhân nhiễm không HIV, không HBV có mức độ suy thận
khác nhau được xảo định theo độ thanh thải creatinine bản đầu (CrCl) (chức năng thận bình thường
khi CrC] > 80 ml/phút. suy thận nhẹ với C rCl = 50 — 79 ml/phút. suy thận trung bình với C rC1=30 —
49 ml/phút) vả su_v thận nặng với C rCl = 10 — 29 ml/phút. So với những bệnh nhảm có chức năng thận
bình thường. phơi nhiễm tenofovir trung bình (% C V) tãng từ 2.185 (12%) ng.giờ.fml ở những đối
tượng có CrC1 > 80 ml/phủt. tương ứng 3.064 (30%) ng.giờ/ml. 6.009 (42%) ng.giờ/ml và 15.985
(45%%) ng.giờ/ml ở những bệnh nhân suy thận nhẹ. trung binh. nặng. Liều khuyến cảo ở những bệnh
nhân suy thận. kèm theo tảng khoảng cảoh liếu. được mong đợi lả đem đển nồng độ đinh trong huyết
tương cao hờn vả nồng độ C … thắp hơn ở những bệnh nhân suy thận so với những bệnh nhân có
ohức năng thận bình thường. Ý nghĩa lâm sảng của điếu nảy vẫn chưa được biết rõ.
Ở những bệnh nhân bị bệnh thận giai đoạn cuối (ESRD) (ctc1 < 10 ml/phút) oần thấm phân mảu,
nồng độ của tenofovir tăng lên đảng kế trong 48 giờ đạt Cmax trung bình là 1.032 11ng vả AUConsh
trung bình là 42.857 ng.gỉờ/ml. Khuyến cảo điều chinh khoảng cảch liểu ot'1a tenofovir disoproxil
fumarate 300 mg ở những bệnh nhân có độ thanh thải creatinine < 50 ml/phút hoặc ở những bệnh
nhân đã bị bệnh thận giai đoạn cuối (ESRD) và cần thầm phân mảu.
Dược động học của tenofovir ở những bệnh nhân không thấm phân mảu có dộ thanh thải oreatinine <
10 ml/phút vả ở những bệnh nhân bị bệnh thận giai đoạn cuối được kiếm soát bằng thấm phân phúc
mạc hoặc cảc dạng thấm phân khác chưa được nghiên cứu.
Suy gan
Liều đơn 300 mg tenofovir disoproxil fumarate được sư dụng ở những bệnh nhân nhiễm không HIV,
không HBV có mức độ suy gan khảo nhau được xảo định theo phân loại Child-Pugh Turcotte (CPT).
C ảo thông số dược động học của tenofovir không bị thay đổi đảng kể ở những bệnh nhân suy gan gợi
ý rằng không oần điếu chỉnh liền ở nhĩmg đối tượng nảy. Cảo giá trị Cmax vả AUC… cùa tenofovir
trung bình (%CV) tương ứng lả 223 (34,8%) ng/ml và 2.050 (50,8%) ng.giờ/ml ở những đối tượng
bình thường so với 289 (46,0%) ng/ml và 2,31 (43.5%) ng.giờ/ml ở những đối tượng suy gan trung
binh và 305 (24,8%)ng/m1 và 2.740 (44,0%) ở những đối tượng suy gan nặng.
Dược động học nội bảo
Tenofovir dỉphosphate có thời gian bán thải nội bảo là 10 giờ trong oảo tế bảo đơn nhân trong máu
ngoại vi ở trạng thải hoạt động và 50 giờ trong cảc tế bảo đơn nhân trong mảu ngoại vi ở trạng thái
nghi.
DỮ LIỆU TIÊN LÂM SÀNG
Efavirenz
Dữ liệu tiến lâm sảng cho thấy không có nguy hiềm nảo đặc biệt trên người ngoải những gì đã được
ghi nhận trong cảc nghiên cứu lâm sảng nghiên cứu tính an toản, dược lý, độc tinh lìều lặp lại vả độc
tính di truyền. Trong cảc nghiên cứu độc tính sinh sản, dị tật được ghi nhận ở 3 đến 20 bảo thai/ khi
cynomolgus sơ sinh được điếu trị bằng efavirenz với cảc lỉểu oho nổng độ efavirenz trong huyết
tương tương tự với nồng độ trong huyết tương ở người. Các nghiên cứu tính sinh ung thư cho thấy oó
sự gia tăng biến oố trên gan và khối 11 ở phối ở chuột nhắt cải nhưng không thấy ở chuột nhắt đực.
Lamivudine
Trong oảo nghiên oứu độc tính trên động vật, việc sử dụng lamivudine ở liếu cao không có liên quan
đến bất kỳ độc tính trên tạng lớn nảo. Lamivudine không gây đột bỉến trong thí nghiệm trên vi khuấn
W
'nhưng cho thấy có hoạt tính trong một thử nghiệm độc tính tế bảo in vitro và thử nghiệm lymphoma ở
chuột nhắt. Lamivudine không gây độc tính di truyền in vitro ở cảc liếu cho nồng độ trong huyết
tương cao hơn khoảng 40 — 50 lần so với nồng độ phơi nhiễm trên lâm sảng. Do không thể chứng
thực hoạt tính đột biến trên in vilro cùa lamivudine trong thứ nghỉệm in vivo. lamivudine không nên
thế hiện độc tinh di truyền ờ những bệnh nhân đảng được điều trị. Kết quả nghiên cứu độc tinh dải
hạn ở chuột nhắt vả chuột cống không thế hiện bất kỳ nguy cơ độc tinh sinh ung thư ở người.
Tenofovir
Các nghiên cứu tiền lâm sảng được thực hiện trên chuột cống. chó và khi hé lộ cơ quan đích tác động
ở đường tiêu hóa. thận. xương và tãng nồng độ phosphate huyết thảnh. Độc tinh trên xương được
chấn đoản lả nhuyễn xương (ở khi) và giảm mật độ khoảng ở xương (ở chuột oống vả chó). Phảt hỉện
từ các nghiên cứu trên chuột oống và khi chỉ ra rằng có một sự giảm hấp thu phosphate ở ruột do
thuốc có khả nảng lảm gỉảm thứ oấp mật độ khoảng ờ xương. Tuy nhiên, không thể rủt ra được kết
luận về cơ chế đằng sau những độc tính nảy.
Các nghiên cứu trên hệ sinh sản đã được thực hiện trên ohuột cống và thó. Không có ảnh hưởng nảo
trên sự kết đôi, các chỉ số khả năng sinh sản hoặc bất kỳ ohi số mang thai và thai nảo. Không có sự
thay đổi nảo trên mô mềm và mô xương. Tenofovir disoproxil fumarate 1ảm giảm chỉ số sinh tồn và
cân nặng cùa con non trong nghỉên cứu độc tính chu sinh — sau sinh.
Cảo nghiên cứu độc tính di truyền cho thấy tenofovir disproxil fumarate âm tính trong thử nghiệm vì
nhân tủy xương ờ ohuột nhắt in vivo nhưng dương tính trong cảm ứng đột bỉến tiến trong thử nghiệm
tế bảo lymphoma ở chuột nhắt L5178Y ín vitro khi có mặt hoặc vẳng mặt sự hoạt hóa chuyển hóa 89.
Tenofovir disoproxil fumarate dương tính ở hai trong ba nghiên cứu thử nghiệm Ames (chủng TA
1535). một khi có mặt S9 (tảng 6,2 đến 6.8 lần) và một khi không có 89. Tenofovir dìsoproxil
fumarate cũng dướng tính nhưng yếu trong in vivo/ in virro trên tế bảo gan chuột cống nguyên thủy.
Tenofovir disoproxil fumarate không thế hỉện bất kỳ khả năng gây ung thư trong nghiên cứu tính sinh
ung thư ở chuột cống được cho uống thuốc trong thời gian dải. Nghiên cứu về tính sinh ung thư bằng
đường uống trong thời gỉan dải ở chuột nhắt cho thấy tỷ lệ khối u tả trảng thấp. hầu như oó liên quan
đến nồng độ tenofovir disoproxil fumarate tại chỗ cao trong đường tiêu hóa ở liếu 600 mg/kg/ngảy.
Trong khi cơ chế hình thảnh khối u ohưa rõ, phát hiện nảy hầu như không tương thích ở người.
QUY CÁCH ĐỎNG GÓI: Hộp 1 lọ HDPE x 30 vỉên nén bao phim
CHỈ ĐỊNH
Viên nén Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg là viên nén
kết hợp cố định liều của tenofovir disoproxil fumarate, lamivudine vả efavirenz.
Thuốc được chỉ định để điếu trị nhiễm virus HIV-l ở người lớn và thanh thiếu niên (từ 12 tuồi trở lên
và cân nặng 2 40 kg) có khả nãng ức chế virus đến nồng độ RNA HIV-l < 50 bản sao/ml khi đang
điều trị bằng phối hợp khảng retrovirus hơn 3 thảng. Bệnh nhân phải chưa từng thất bại virus học
trong bất kỳ phác đồ khảng retrovirus nảo trước đó.
Việc lựa ohọn Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg đề đỉều
trị cho những bệnh nhân nhiễm HIV -1 đã từng điều trị bằng thuốc khảng retrovirus nên dựa trên kết
quả xẻt nghiệm sự đề khảng oùa virus cùa từng bệnh nhân vả/hoặc tiền sử điếu trị cùa bệnh nhân.
Nên tham khảo hướng dẫn chính thức cho điều trị nhiễm HIV-l (như hướng dẫn từ WHO)
LIÊU DÙNG & CÁCH DÙNG
..
`-LJUJ
' Việc điều trị nên được khời đầu bởi thầy thuốc có kinh nghiệm trong việc kiếm soát nhiễm HIV-l.
Liều dùng
Người Iởn vả thanh lhiểu niên:
Liều khuyến cảo của Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg
lả 1 viên uống 1 lần/ngảy.
Cảch dùng: Nên uống nguyên viên Tenofovir/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg với
nước.
Khưyến cảo uống Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg khỉ
dói do thức ản có thề lảm tăng phơi nhiễm efavirenz và dẫn đến tăng tần suất tảo dụng không mong
muốn.
Để cải thiện khả năng dung nạp efavirenz liên quan đến các tảo dụng không mong muốn trên hệ thần
kinh, khuyến cảo sữ dụng thuốc trước khi đi ngù.
Phơi nhiễm tenofovir sẽ thấp hơn khoảng 35% sau khi uống Tenofovir Disoproxil
FurnaratelLamivudine/Efavirenz 300 mg/300 mg/4OO mg lủc đói so vởi khi sử dụng thuốc cùng với
thức ăn. Ở những bệnh nhân giảm virus, sự phù hợp lâm sảng cùa sự suy giảm nảy oòn hạn chế.
Trẻ em
Không khuyến cảo sữ dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mgl4OO mg ở những trẻ em dưới 12 tuối do thiếu dữ liệu về tính an toản vả hìệu quả.
Nguới lớn Iuốỉ
Nên sử dụng cẩn trọng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO
mg ở người lớn tuổi.
Đíều chinh liều:
Khi được chỉ định ngừng sử dụng 1 trong cảc thảnh phần cùa Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mgl3OO mg/4OO mg hoặc khi cần điều ohinh liếu. nên sử dụng
cảc chế phầm riêng biệt cùa tenofovir disoproxil fumarate. lamivudỉne vả efavirenz. Vui lòng thảm
khảo tờ Tóm tắt đặc tinh sản phẩm của cảc thuốc nảy.
Nếu Tenofovir Disoproxil Fumarate/Lamỉvudine/Efavirenz 300 mg/300 mg/4OO mg được sử dụng
dổng thời với rifampicin, oó thế cân nhắc bổ sung thêm efavirenz 200 mglngảy (tổng cộng 800 mg).
Suy thận
Không khuyến cáo sử dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mg/4OO mg ở những bệnh nhân suy thận trung bình hoặc nặng (độ thanh thải creatinine (CrCl) < 50
ml/phút). Việc sử dụng viên nén dạng phối hợp cố định liều không phù hợp cho những bệnh nhân suy
thặn trung bình hoặc suy thận nặng cần được điếu chinh khoảng cảoh liếu của lamivudine vả
tenofovir disoproxil fumarate.
Suy gan
Dược động học của Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mgl4OO mg
chưa được nghiên cứu ở những bệnh nhân suy gan. Bệnh nhân cần dược theo dõi cấn thận oác tảo
dụng không mong muốn, đặc biệt là cảc triệu chứng trên hệ thống thần kinh có liên quan đến
efavirenz.
W
'Nếu ngừng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/300 mg/4OO mg ở những
bệnh nhân đổng nhiễm HIV vả HBV, những bệnh nhân nảy nên được theo dõi chặt chế bằng chứng
cùa bùng phát viêm gam.
Nếu ngừng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mgl3OO mg/4OO mg, nên xem
xét thời gian bản thải dải của efavirenz và thời gian bán thải nội bảo dải cùa tenofovir vả iamivudine.
Do sự thay đối các thông số nảy giữa cảc bệnh nhân vả cảc quan ngại liến quan đến sự phảt triến đề
khảng, nên thạm khảo hưởng dẫn điều trị HIV và xem xét lý do ngừng thuốc.
CHỐNG CHỈ ĐỊNH
Tenofovir Disoproxil FumaratelLamỉvudine/Efavirenz 300 mg/BOO mg/4OO mg bị chống chỉ định ở
những bệnh nhân bị quá mẫn với tenofovir. lamivudine. efavirenz hoặc cảc thảnh phần khảo cùa
thuốc.
Không được sử dụng cảc chế phẩm dược liệu có chứa St. John’s wort (Hypericzim perforamm) trong
khi đang sử dụng Tenofovir Disoproxil Fumarate/LamivudinelEfavirenz 300 mg/3OO mg/4OO mg do
nguy cơ giảm nồng độ trong huyết tương và giảm tảo dụng lâm sảng của efavirenz.
Efavirenz lảm giảm đảng kế nồng độ của voriconazole trong huyết tương trong khi voriconazole cũng
lảm tảng đảng kế nồng độ efavirenz trong huyết tương. Do Tenofovir Disoproxil
F umarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg lả viến nén kết hợp cố định liếu, không thể
thảy đồi liếu của efavirenz, do đó không được sư dụng đồng thời voriconazole vả Tenofovir
Disoproxil Fumarate/Lamỉvudine/Efavirenz 300 mg/3OO mg/4OO mg.
THẬN TRỌNG KHI SỬ DỤNG THUỐC
Chang
Không nên sử dụng viên nén kết hợp cố định liều Tenofovir Disoproxil
Fumarate/Lamiwdine/Efavirenz 300 mg/3OO mg/4OO mg đồng thời với cảc thuốc khảo có chứa cùng
thảnh phần hoạt chất, efavirenz, lảmivudine hoặc tenofovir disoproxil fumarate. Không nên sử dụng
đồng thời Tenofovir Disoproxil Fumarate"Efavirenzfflamivudine 300 mg/3OO mg/4OO mg với các chất
tương tự cytidine khác như emtricitabine. Không nên sử dụng đồng thời
Tenofovir/Lamivudinc/Efavirenz 300 mg/300 mg/4OO mg với ảdefovir dipivoxil.
Sự lây nhiễm HIV
Điều ưị bằng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg không
chấm dửt được nguy cơ lây nhiễm HIV qua đường tình dục hoặc truyền mảu, mặc dù nguy cơ có thể
giảm đi. Bệnh nhân nên tiếp tục sử dụng các biện phảp ngăn ngừa lây nhiễm HIV.
Didanosíne
Không khuyến cáo sử dụng đồng thời Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300
mg/3OO mg/4OO mg vả didanosine do phơi nhiễm với didanosine tăng đáng kể sau khi sử dụng đồng
thời vởi tenofovir disoproxil fumarate.
Bệnh gan
Tỉnh ản toản và dược động học của efavirenz chưa được nghiên cứu ở những bệnh nhân bị bệnh gan
trầm trọng. Do đó, Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg chỉ
được sử dụng ở những nhóm bệnh nhân nảy nếu lợi ích vượt qua nguy cơ và được theo dõi tính an
toản một cách chặt chẽ.
Độc tính trên gan
W
`ol.`x 'hhư’ơ’ 'ÌJ
' Nồng độ transaminase tăng có thể xuất hiện vải thảng sau khi bắt đấu efavirenz vả có thể xuất hiện
thường xuyên hơn ở những bệnh nhân đồng nhiễm HBV vả/hoặc HCV. Khuyến oác ngừng thuốc nếu
oó triệu chứng cùa độc tinh trên gan hoặc nếu nồng độ transaminase > 10 lần giới hạn bình thường
trên.
Suy gan xuất hiện ở những bệnh nhân khỏng có bệnh gan từ trưởc hoặc cảc yếu tố nguy cơ có thế xảo
định được khảo. Nên cân nhắc theo dõi enzyme gan ở những bệnh nhân khỏng bị suy gan từ trước
hoặc cảc yếu tố nguy cơ khảo.
Bệnh nhán đồng nhiễm virus H] V vả vỉrus víêm gun B (HB V ) hoặc virus viêm gan C' (HCV)
Bệnh nhân viêm gan B hoặc C mạn tính vả được điều trị bằng phảc đồ khảng retrovirus kểt hợp có
nguy oơ tăng cảc tảo dụng không mong muốn trên gan vả có thể gây tử vong.
Bác sỹ nên tham khảo cảc hướng dẫn điều trị HIV hiện hảnh để kiềm soát một cách tối ưu tinh trạng
nhiễm HIV 6 những bệnh nhân đồng nhiễm vởi HBV.
Lamivudine vả tenofovir disoproin fumarate cũng có hoạt tính kháng lại HBV. Do đó, ngừng sử
dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg ở những bệnh
nhân đồng nhiễm HIV vả HBV oó thế liên quan đến bùng phát viêm gan cấp trầm trọng. Bệnh nhân
đồng nhiễm HIV vả HBV ngừng sử dụng Tenofovir/LamivudinclEfavirenz 300 mg/3OO mg/4OO mg
phải được theo dõi chật chẽ cả trên lâm sảng vả cảc xét nghiệm trong ít nhất 4 thảng sau khi ngừng
điếu trị bằng Tenofovir Disoproxil Fumarate/I.amivudine/Efavirenz 300 mg/3OO mg/4OO mg. Nếu
phù hợp, có thể tải điều trị với phảc đổ khảng viêm gan B đặc hiệu. Ở những bệnh nhân bị bệnh gan
tiến triến hoặc xơ gan, không khuyến cảo ngừng điều trị do bùng phảt viêm gan sau điếu trị có thể
dẫn đến hiện tượng gan mắt bù.
Phát ban
Phảt ban nhẹ đến trung bình rất thường gặp trong vòng 2 tuần đầu sau khi bắt đầu điều trị bÀng 6
efavirenz vả không cần phải ngừng diều trị. Phảt ban thường hồi phục trong vòng 2 tuần. Phịt ban '
hoặc hồng ban nặng, bao gổm hội chứng Stevens-Johnson. oần ngưng điếu trị ngay lập tức.
Ảnh hưởng lên tâm thẩn vù hệ thẩn kinh trung ương
Tác dụng không mong muốn lến tâm thần và hệ thần kinh trung ương rất phố biển sau khi sử dụng
efavirenz. Những triệu chứng nảy xuất hiện trong vòng tuần đầu điều trị và luôn luôn phục hồi trong
vòng 4 tuần điểu trị. Có thế có tảo dụng cộng hợp với rượu vả các thuốc có tác động lên tâm thần
khảo. Bệnh nhân nên được khuyên rằng nếu họ có cảc triệu chứng như trầm cảm nặng, loạn tâm thần
hoặc có ý nghĩ tự tử, họ cần liên hệ với bảo sỹ hoặc trung tâm chăm sóc sức khóe ngay dế xảo định lợi
ích/nguy cơ cùa việc tiếp tục điều t1ị.
Chức năng thận , _
Tenofovir ohù yếu được bải tiết bởi thận thông qua sự bhốỉ hợp cùa lọc ở cầu thận vả bải tíết chủ
động ở ống thận. Do đó, sự thanh thải giảm ở những bệnh nhân bị suy chức năng thận. Có những dữ
1iệu oòn giới hạn về tính an toản và hiệu quả cùa tenofovir disoproxil futnarate ở những bệnh nhân
suy chức năng thận (<80 m1/phút). Ở những bệnh nhân nảy, Tenofovir Disoproxil
Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg chỉ được sử dụng nếu lợi ích cùa vỉệc điều
trị vượt qua nguy cơ oó thể xảy ra.
Ở những bệnh nhân suy thận trung bình đến nặng, thời gian bán thải của lamivudine trong huyết
tương tăng lên do gỉảm dộ thanh thải. Khuyến cáo giảm liều cho những bệnh nhân oó dộ thanh thải
creatinine < 50 ml/phủt.
' Không khuyến cảo sử dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mg/4OO mg 6 những bệnh nhân có độ thanh thải creatinine < 50 ml/phút. do không thể giảm liếu phù
hợp khi sử dụng viên nén kết hợp cố định liếu.
Suy thận. tổn thương thận. gỉa tăng creatinine. phosphate mảu thấp vả bệnh ống lượn gần (bao gổm
hội chứng Fanconi) đă được báo cảo khi sử dụng tenofovir disoproxil fumarate trên lâm sảng.
Khuyến các tính toán độ thanh thải creatinine ở tất cả bệnh nhân trước khi bắt đầu điều trị vả khi phù
hợp trên lâm sảng trong quá trình điều trị bằng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz
300 mg/3OO mg/4OO mg. Định kỳ theo dõi độ thanh thái creatinin vả phosphate huyết thanh ở những
bệnh nhân có nguy cơ tốn thương thận.
Ở những bệnh nhân nhận tenofovir disoproxil fumarate, nên đảnh giả lại chức năng thận trong vòng 1
tuần, bạo gồm đo glucose máu. kali mảu vả nồng độ glucose niệu. nếu phosphate huyết thanh < 1.5
mg/dl (0,48 mmol/l) hoặc độ thanh thải creatinin giảm đưới 50 ml/phút.
Cân nhắc vỉệc tạm ngưng điều trị bằng Tenofovir Disoproxil Fumarate/LmnivudinelEfavirenz 300
mg/3OO mg/4OO mg ở những bệnh nhân có độ thanh thải creatinine dưới 50 ml/phủt hoặc có
phosphate huyết thanh giảm dưới 1,0 mg/dl (0,32 mmol/l)
Nên tránh sử đụng đồng thời Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO
mgj4OO mg với các thuốc độc thận (như ảminoglycosides. ảmphotericin B. foscarnet, ganciclovir,
pentamidine. vancomycin. cidofovir hoặc interleukin-Z). Nếu không thế trảnh khỏi việc sử dụng đồng
thời tenofovir disoproxil fumarate vả oảo thuốc gây độc thận. nên theo dõi chức năng thận mỗi tuần.
Ảnh hưởng Iên xương
Trong một nghiên cứu lâm sảng được kiếm soát. Sự suy giảm mật độ xương ở cột sống và thay đối
cảc ohi dấu sinh học của xương so với ban đầu được ghi nhận ở cả hai nhóm điều trị. nhưng lớn hơn
đảng kế ở nhóm điếu trị bằng tenofovir disoproxil fumarate so với nhóm đối chứng được điều trị bằng
stavudine (cả hai được kết hợp với lamivudine vả efavirenz) trong 144 tuần. Giảm mật độ xương ở
hông lớn hơn đảng kế ở nhóm nảy cho tới tuần 96 tuần. Tuy nhiến. không gia tăng nguy cơ gãy hoặc
bằng chứng cùa các bất thường xương trong 144 tuần.
Tenofovir được nghiên cứu ở những trẻ em từ 12 tuổi trở lên nhiễm HIV-l. Trong điều kiện bình
thường, mật độ xương tăng nhanh chóng trong nhóm tuối nảy. Trong nghiên oứu nảy, tốc độ tích lũy
xương trung bình ít hơn ở nhóm được điều trị bằng tenofovir so vởi nhóm giả dược. Tăng trường
chiều cao không bị ảnh hưởng. Chỉ dấu chu chuyến xương ở nhóm trẻ em từ 12 tuổi trở lên được điếu
trị bằng tenofovir gợi ý oó tăng chu chuyển xương, phù hợp với những tảo dụng được ghi nhận ở
người lớn. Do tenofovir oó thể ảnh hưởng trên sự chuyền hóa xương, ohi sử dụng Tenofovir
Disoproxil FumaratelLamivudine/Efavirenz 300 mg/3OO mg/4OO mg ở trẻ vị thảnh niên dưới 18 tuổi
nếu lợi ích đạt được vượt qua nguy cơ.
Các bất thường trên xương (hiếm khi góp phần vảo gãy xương) oó thể liên quan đến bệnh ống lượn
gần. Nếu nghi ngờ oó cảc bất thường trên xương, cần phải hội chấn.
Nhiễm toan acid Iactic
Nhiễm toan ảoid lactic lả một biến chứng tuy hiếm nhưng nghiêm trọng, có thể đe dọa tính mạng có
lỉên quan đến việc sử dụng các thuốc ức chế enzyme phiên mã ngược nucleoside (NRTI). Nhiếu
thuốc khảo trong nhóm nảy đã biết là gây nhiễm toan acid lactic. Cảo dữ liệu tiến lâm sảng và lâm
sảng gợi ý rằng nguy cơ xuất hiện nhiễm toan acid lactic. thường được cho là ảnh hưởng của cảc
thuốc tương tự nucleoside, lả rất thấp đối với tenofovir disoproxil fumarate vả lảmivudine. Tuy nhiên,
W
I.u ,
' không thế loại trừ nguy cơ nảy. Nhiễm toan ảcid lactic có thể xuất hiện sau một vải đến nhiếu thảng
điều trị bằng NRTI. Những bệnh nhân tảng 1ảctate mảu có thế không có triệu chứng hoặc trầm trọng,
hoặc có thế oó cảc triệu chứng không đặc hiệu như khó thờ. mệt mòi. buồn nôn. nôn. tiêu chảy và đau
bụng. Cảo yếu tố nguy cơ cùa nhiễm toan aoid lactic do NRTI bao gồm phụ nữ vả béo phì. C ằn phải
theo dõi chặt chẽ oác bệnh nhân có nguy cơ cao. Rả soát tăng lactate mảu ở những bệnh nhân không
triệu chứng được điều trị bằng NRTI. tuy nhiên không khuyến cáo sử dụng. Bệnh nhân có triệu chứng
luôn luôn có nồng độ > 5 mmol/l vả cần ngừng tất cả NRTI. Nồng độ ảcid lảctic > 1011111101/1 luôn
1uôn cần được cấp cứu.
Loạn dưỡng mỡ và rối Ioạn chuyển hóa
Thuốc khảng retrovirus dạng phối hợp có liên quan đến sự tải phân bố mở cùa cơ thể (loạn dưỡng
mỡ) ở những bệnh nhân nhiễm HIV. Trong khi có những bằng ohứng đảng kể của tảo dụng phụ nảy
đối với thuốc khảng retrovirus khảo, bằng chứng về mối quan hệ nhân quả đối với tenofovir,
lảmivudine vả efavirenz lại yếu, việc chuyền từ một chất tương tự thymidine (như stavudine) sang
tenofovir lảm tăng mở ở chân tay ở những bệnh nhân bị teo mô mỡ. Nguy cơ teo mô mỡ tảng có liên
quan đến tuổi cao, thời gian điếu tnf khảng retrovirus dải hơn và rối loạn chuyền hóa có liên quan.
Kiếm tra1âm sảng bao gồm đảnh giả oác dấu hiệu thực thế của tải phân bố mỡ. Cân cân nhắc đo lipìd
huyết thanh vả glucose huyết lủc đói oũng như kiềm soát rối loạn lipid.
Rối Ioạn chức năng ty thể
C ác thuốc tương tự nucleoside vả nucleotide đã dược xảo định ưên in vilro vả ín vivo gây tồn thương
ty thế ở cảc mức độ khảo nhau. Có cảc bảo cảo rối loạn chức năng ty thế ở trẻ sơ sinh âm tính với
HIV phơi nhiễm với thuốc tương tự nucleoside trong từ cung vả/hoặc sau sinh. Tảo dụng không mong
muốn chính được báo cảo là rối loạn huyết học (thiếu mảu, giảm bạch oần trung tinh) và cảc rối loạn
chuyến hóa (tãng lactate máu. tảng lipase mảu). Nhĩmg biến cố nảy thường thoáng qua. Một vải rối
loạn thần kinh khời phát muộn đã được bảo oảo (tăng trương lực cơ. co giật. hảnh vì bệnh 1ỷ). Hiện
vẫn chưa biết rối ioạn thằn kinh thoảng qua hay vĩnh viễn. Bắt kỳ trẻ nảo phơi nhiễm với thuốc tương
tự nucleoside vả nucleotide trong tử oung. ngay cả trẻ âm tính với HIV, cần được theo dõi bằng thăm
khám lâm sảng vả xét nghiệm và cần được đảnh giả đầy đủ khả năng rối loạn chức nãng ty thế trong
trường hợp có cảc dấu hiệu hoặc triệu chứng phù hợp. Những phải hiện nảy không ảnh hướng đến cảc
khuyến cảo quốc gia hiện hảnh trong việc sử dụng thuốc khảng retrovirus ở phụ nữ có thai để ngăn
ngừa lây truyền dọc HIV.
Viêm tụy
Nên ngừng ngay lập tức Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/300 mg/4OO
mg nếu oác dấu hiệu, triệu ohứng lâm sảng vả cảc kết quả xẻt nghiệm bất thường gợi ý xuất hiện viếm
tụy.
Nhiễm khuẩn cơ hội
Bệnh nhân sử dụng oảo phảc đồ khảng retrovirus có thể tiếp tục nhiễm khuản cơ hội và oảo biển
chứng khảo cùa HIV. Do đó, nên duy tri theo dõi chặt chẽ bệnh nhân bởi bảo sỹ có kinh nghiệm điều
trị HIV.
Hội chứng phục hồi mìễn dịch
Ở những bệnh nhân nhiễm HIV bị suy giảm miễn dịch trầm trọng từ trước, trong vải tuần hoặc thảng
đầu tiên sau khi bắt đấu điều trị bằng phối hợp ART. một phản ứng viêm đối vởi những bệnh cơ hội
không triệu chứng hoặc bệnh cơ hội còn lại (như viêm võng mạc do CMV, nhiễm mycobacteria. viêm
W—
.ả’ A....“f ,
'phối do pneumooystis) có thề nảy sinh và gây các tình trạng lâm sảng nghiêm trọng hoặc lảm trầm
trọng hơn triệu chứng bệnh. Điều trị khi cần thiết.
Hoại tửxương
Mậc dù nguyên nhân được cho là do nhiếu yếu tố (bao gổm sữ dụng corticosteroid. tiêu thụ rượu. suy
giảm miễn dịch trầm trọng. chí số khối cưa cơ thế cao hơn). cảc trường hợp hoại từ xương đã được
bảo cảo. đặc biệt ở những bệnh nhân mắc HIV tiến triến vảJhoặc phơi nhiễm trong thời gian dải vời
phối hợp thuốc khảng retrovirus. Bệnh nhân nên được khuyến tham vấn y khoa nếu họ bị nhức vả đau
khớp, cứng khớp hoặc cử động khó khản.
Bệnh nhân cao tuổi
Hầu hết bệnh nhân cao tuối có ohức năng thận bị suy giảm. do đó nên cắn trọng trong khi điếu trị cho
bệnh nhân cao tuổi bằng tenofovir disoproxil fumarate.
Ca'c tả dược
Bệnh nhân có cảc bệnh di truyền hiếm gặp như không dung nạp galactosc, thiếu hụt Lapp lactase
hoặc kém hấp thu glucose-galactose không nên sử dụng thuốc nảy.
Mỗi viên thuốc nảy có chứa 1,9 mmol (43 mg) natri. Bệnh nhân đảng trong chế độ kiếm soát natri cần
thận trọng khi sử dụng thuốc nảy.
Cảnh báo: Thuốc có chứa Lactose.
TƯỢNG TÁC THUỐC VÀ CÁC LOẠI TƯONG TẢC KHÁC
T ương tác với Iamivudine
Sử dụng đồng thời với trimethoprim/sulfamethoxazole dẫn đến tăng 40% diện tich dưới đường cong
cùa lamivudine. Không cần điều chinh liều cùa Tenofovir Disoproxil
Fumarate/LamivudinelEfavirenz 300 mg/3OO mg/4OO mg. Lamivudine không có ảnh hướng trên dược
động học cùa trimethoprim hoặc sulfamethoxazole.
T ương tác vởi tenofovir
Didanosine
Không khuyến cảo sữ dụng đồng thời tenofovir disoproxil fumarate vả didnnosine.
T huốc thái irừ bởi thận
Do tenofovir được đảo thải chủ yểu bời thận, sử dụng đồng thời tenofovir disoproxil fumarate vởi cảc
thuốc lảm giảm chức năng thận hoặc cạnh tranh đảo thải chủ động ở ống thận thông qua oảo protein
vận chuyền hOAT l, hOAT 3 hoặc MRP 4 (như cidofovir) có thế lảm tảng nồng độ trong huyết thanh
oùa tenofovir vả/hoặc các thuốc sử dụng đồng thời.
Nến trảnh sữ dụng tenofovir disoproxil fumarate đồng thời với cảc thuốc gây độc cho thận, như
minoglycoside, ảmphotericin B, foscamet, ganciclovir, pentamidine, vanoomycin, oidofov'ư hoặc
interleukin—2.
Tacrolimus có thể ảnh hưởng chức năng thận, khuyến cảo theo đõi chặt chẽ khi sử dụng thuốc nảy
đồng thời với tenofovir disoproxil fumarate.
T ương tác vởi efavirenz
Efavirenz được đảo thải qua chuyến hóa ở gan, chủ yếu được xúc tảo bời cytochrome da hình di
truyền cvp4so isoform CYP2B6, nhưng cũng được xúc tảo bới CYP3A. Do đó. những chất lảm thay
đồi hoạt động cùa CYP2B6 hoặc CYP3A có thể thay đổi nồng độ của efavirenz.
Ir1 JJ“! .
' Efavỉrenz là một chất cảm ứng cảc enzyme cytochrome P450 như CYP3A4 quan trọng trên lâm sảng,
do đó có thể có cảc tương tác với cảc thuốc được chuyến hóa bởi oon đường nảy. ln vitro, efavirenz
cũng ức chế UDP-glucuronosyl transferases. CYP3A4. C YP2C9 và C YP2CI9. Trong phần lớn
trường hợp mả efavirenz tương tác in vivo với oảo cơ chất đã biết cùa CYP3A. kết quả cuối oùng sau
khi dùng nhiếu iiếu lả gỉảm phơi nhiễm toản thân với thuốc tương tảo với efavirenz. Mặc dù efavirenz
có thể hoạt dộng in vivo như một chất ức chế CYP3A4 sau liều đầu tiên nhưng không chẳc rằng sẽ
xảy ra một khi có sự cảm ứng C YP3A4.
Không nên sử dụng efavirenz đồng thời với terfenadỉne. astemizole. cisapride pỉmozide, bepridil hoặc
cảo dẫn chất ergot (nấm cựa gả). do nó có thể dẫn đến thay dối nồng độ trong huyết tương oủa những
thuốc nảy. '
Bảng 1 : T ương tác thuốc của T enofovir Disoproxil F umarate/Lamivudine/Efavirenz 300 mg/300
mg/400 mg
Dảnh sảch tương tảo thuốc sau đây không được xem là hoản toản đầy đủ nhưng mang tính chất đại
diện cho các nhóm thuốc cần cấn trọng khi sử dụng (tăng phơi nhiễm được biếu thị là “T”, gỉảm phơi
nhiễm được biếu thị là “’1, không thay đổi 1ạ …<-›, 3 lần/ngảy 13 “t.i.d.”, 2 lần/ngảy 1ạ “b.i.d.”, và 1
lần/ngảy lả “q.d.”)
Khu ến cảo liên uan đến
Các thuốc điều trị Tưong tác thuốc __y _ ,q ` _
v1ẹc sư dụng đong thơi
THUỐC KHÁNG KHUẨN
Thuốc kháng retrovirus
Các thuốc tương tự nucleoside Không có tương tảo
Zidovudine
Stavudine
Abacavir
Abacavir/tenofovir Không nên sử dụng đồng thời
abacavir vả Tenofovir
Disoproxil
Fumarate/Lamivudine/Efavir
enz 300 mgl3OO mg/4OO mg,
do tảo dụng hiệp dồng cộng
của abacavir bị gỉởi hạn hoặc
bị mất.
Emtricỉtabine/lamivudine Không nên sử dụng đồng thời
emtn'cỉtabine vả Tenofovir
Disoproxil
FumaratelLamivudine/Efavir
enz 300 mgl300 mgl4OO mg,
do sự tương tự giữa
emtricitabine vả lamivudine
và hậu quả là mất tảo dụng
W
» buì“n.
hiệp đồng cộng.
Didanosine (400 mg q.d.)/
tenofovir
Didanosine
AUC T 40—60%
Nguy cơ tác dụng không
mong muốn do didanosine
(như tăng viêm tụy, nhiễm
toan acid lactic, và có thế
giảm đáng kể tế bảo CD4) khi
sử dụng đồng thời.
Didanosine 250 mg dùng
đồng thời với tenofovir trong
nhiều phối hợp kháng virus
khác nhau có liên quan đến tỷ
lệ thất bại virus học cao.
Không khưyến cáo sử dụng
đồng thời Tenofovir
Disoproxil
F umarate/Lamivudine/Efavir
enz 300 mg/3OO mg/4OO mg
vả didanosine.
Thuỏc ức chê enzyme phiên mã
ngược không nucleoside
Nevirapine
Etravirine
Không khuyến cáo sử dụng
dồng thời Tenofovir
Disoproxil
Fưmarate/LamivudinelEfavir
enz 300 mg/3OO mg/4OO mg
do bổ sung độc tính và không
có lợi ich về hiệu quả.
T huốc ức chếprotease
Fosamprenavir/ritonavir
(700/100 mg b.i.d.)/efavirenz
Amprenavir
Cdáy 1 17%
Không có tương tảc với phác
đồ dùng 2 Iần/ngảy ở trạng thái
ốn định.
Không cân thiêt điều chinh
liêu.
Fosamprenavir/ritonavir
(1400l200 mg q.d.)lefavirenz
Amprenavir
c……: 1 36% ở trạng thải ổn
định.
Trảnh sử dụng đồng thời
Tenofovir Disoproxil
Fumarate/LamivudinefEfavire
nz 300 mg/3OO mg/4OO mg vả
W
hi.c … ..
phác đồ fosamprenavir 1
lần/ngảy
Saquinavir HCGlritonavir
(l OOO/l OOmg b.i.d.)]efavirenz
Không có tương tảc có ý
nghĩa lâm sảng được ghi
nhận.
Cảc dữ liệu có sẵn không đủ
để khuyến cảo liếu cho
saquinavir kèm hoặc không
kèm ritonavir, khi sử dụng
đồng thời vởi Tenofovir
Disoproxil
Fumarate/Lamivudine/Efavir
enz 300 mg/3OO mg/4OO mg.
Không khuyến cáo sử dụng
đồng thời với saquinavir kèm
hoặc không kèm ritonavir.
Indinavir (800 mg t.i.d.) |
efavirenz
Indỉnavir
AUC 1 31%,
Cdáyl 40%
Không khuyến cảo sử dụng
đồng thời Tenofovir
Disoproxil
Fumarate/Lamivudine/Efavir
enz 300 mg/3OO mgl4OO mg
với indinavir một mình
(không được hỗ trợ bởi
ritonavir).
Indinavir/ritonavir (800/100 Indinavỉr Chi sử dụng Tenofovir
mg t.i.d) | efavirenz AUCss 1 25%_ Disoproxil
Cdáy 1, 50%
F ưmarate/Lamiwdine/Efavir
enz 300 mgl3OO mgl4OO mg
với indinavir được hỗ trợ bởi
ritonavir khi có thể theo dõi
nổng độ cùa indinavir trong
huyết tương.
Ritonavir (500 mg b.i.d.) / Cảc nghiên cứu tương tảc cho Trảnh sử dụng đồng thời
efavirenz thấy tăng AUC cùa Cả Tenofovir Disoproxil
ritonavir vả efavirenz ở mức
độ trung bình.
FumarateỉLamivudine/Efavir
enz 300 mg/3OO mg/4OO mg
với liều đẳy đủ cùa ritonavir
do khả nãng dung nạp thấp.
Nelfmavir (nhiêu liêu khác
nhau) | efavirenz
Các nghiên cứu tương tảc đưa
ra cảc kết quả biến thiên, bao
gồm tãng 20% trong AUC vả
Cmin của nelfinavir. cũng như
gỉảm 25% AUC và 45% Cmm.
Chỉ khuyến cáo sử dụng đồng
thời Tenofovir Disoproxil
F umarate/Lamivudine/Efavir
enz 300 mg/3OO mg/4OO mg
khi có thế theo dõi nồng độ
của nelfinavir trong huyết
W
tương.
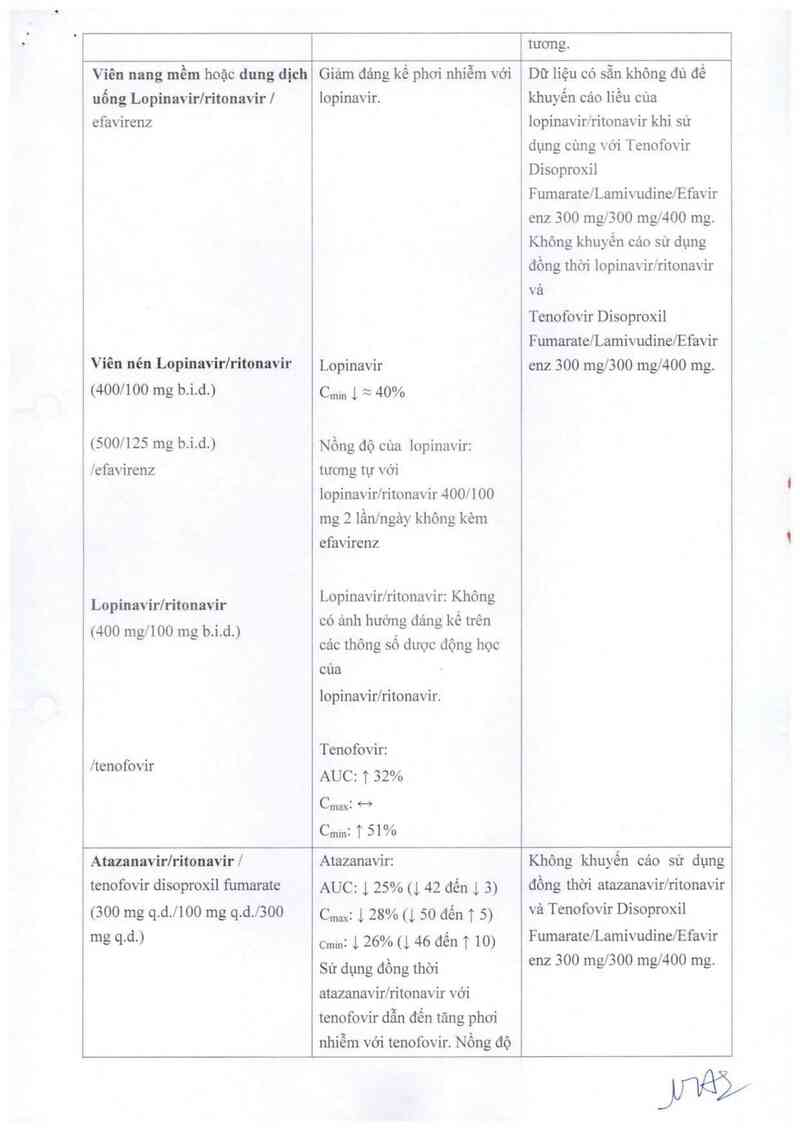
Viên nang mềm hoặc dung dịch
uống Lopinavir/ritonavir |
efavirenz
Giảm đáng kể phơi nhiễm với
lopinavir.
Dữ liệu có sẵn không đủ để
khuyến cảo liều của
lopinavir/ritonavir khi sử
dụng cùng vởi Tenofovir
Disoproxil
FưmaratelLamivưdỉne/Efavir
enz 300 mg/3OO mg/4OO mg.
Không khuyến cảo sử dụng
đồng thời Iopinavir/ritonavir
vả
Tenofovir Disoproxil
Fumarate/LamivudinelEfavir
Viên nén Lopinavir/ritonavir Lopinavir enz 300 mg/300 mg/4OO mg.
(400/100 mg b.i.d.) Cmm 1 = 40%
(500/125 mg b-Ỉ-d-) Nồng độ cùa lopinavir:
/efavirenz tương tự với
lopinavir/ritonavir 400/100
mg 2 lần/ngảy không kèm
efavirenz
Lopinavir/ritonavír L'oninavưỉntonalvư: iĨhôẠng
(400 mg/IOO mg b.i.d.) “’ anh hqu đang ke tren
các thông sô dược động học
của
lopinavir/ritonavir.
. Tenofovir:
ltenofovxr AUC: T 32%
Cmaxễ H
Cmm: T 51%
Atazanavirlritonavir/ Atazanavir: Không khuyến cảo sử dụng
tenofovir disoproxil fumarate
(300 mg q.d.l 100 mg q.d./300
mg q.d.)
AUC: l 25% (l 42 đến 1 3)
c…: & 28% (l 50 đến T 5)
C…: 1 26% a 46 đến 1 10)
Sử dụng đồng thời
atazanavir/ritonavir với
tenofovir dẫn đển tăng phơi
nhiễm với tenofovir. Nồng độ
đồng thời atazanavir/ritonavir
vả Tenofovir Disoproxil
Fumarate/LamivudinefEfavir
enz 300 mgl3OO mg/4OO mg.
W
tenofovir cao hơn có thể lảm
nặng hơn cảc tác dụng không
mong muốn do tenofovir. bao
gôm cảc rôi loạn về thận.
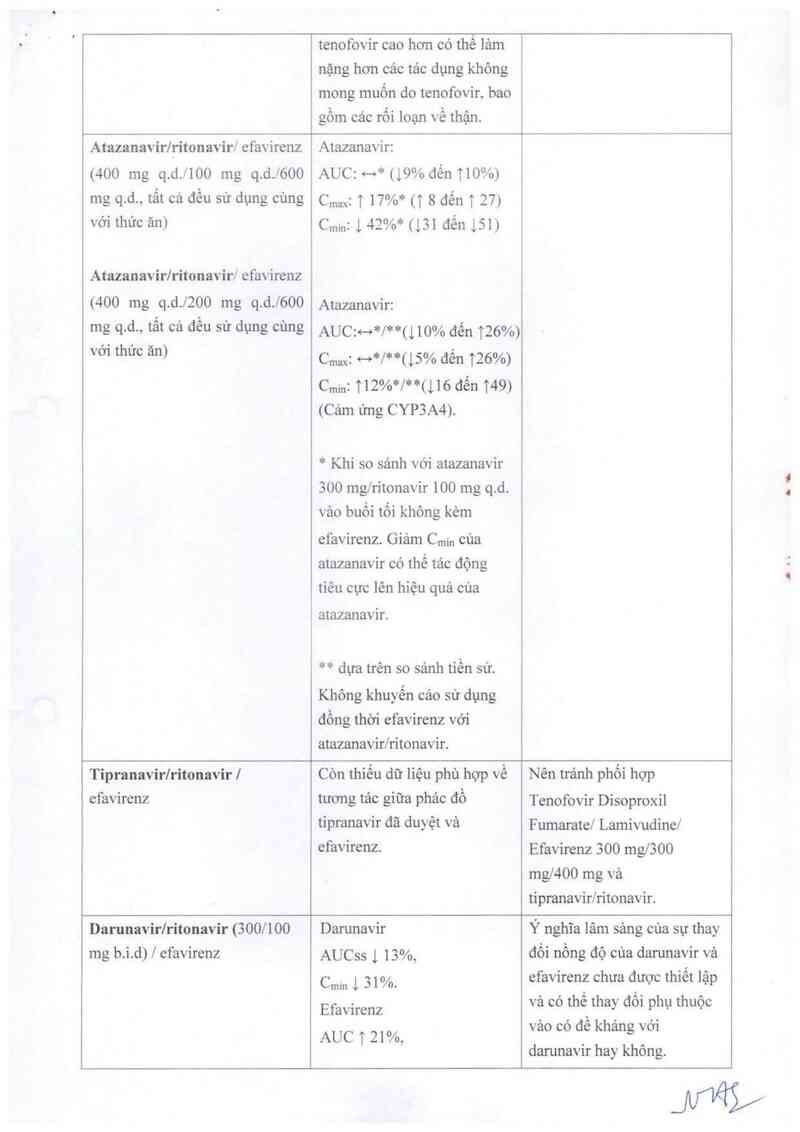
Atazanavir/ritonavir/ efavirenz
(400 mg q.d.!lOO mg q.d.JỔOO
mg q.d., tất cả đều sử dụng cùng
với thức ăn)
Atazanavir/ritonavir/ efavirenz
(400 mg q.dJZOO mg q.d.l60O
mg q.d., tất cả đều sử dụng cùng
với thức ăn)
Atazanavir:
AUC: <-›* (19% đến TIO%)
c…: T 17%* (1 8 đến 1 27)
C……: 142%* (131 đến isn
Atazanavir:
AUC:H*/**(l 10% đến T26%)
c…: <—›*/**(l5% đến T26%)
c…: 112%*/**(116 đển T49)
(Cảm ứng CYP3A4).
* Khi so sánh với atazanavir
300 mg/ritonavir 100 mg q.d.
vảo buổi tối không kèm
efavirenz. Giảm Cmin của
atazanavir có thề tảc động
tiêu cực lên hiệu quả cùa
atazanavir.
** dựa trên so sảnh tiền sử.
Không khưyến cáo sử dụng
đồng thời efavirenz với
atazanavir/ritonavir.
Tipranavir/ritonavir |
efavirenz
Còn thiếu dữ liệu phù hợp về
tương tảc giữa phác dỗ
tipranavir đã duyệt và
Nên trảnh phối hợp
Tenofovir Disoproxil
Fumaratel Lamivudine/
efavirenz. Efavirenz 300 mg/3OO
mg/4OO mg vả
tipranavir/ritonavir.
Darunavir/ritonavir (300/100 Darunavir Ý nghĩa lâm sảng của sự thay
mg b.i.d) / efavirenz AUCss l 13%, đối nồng độ của darưnavir vả
Cmm l 31%. efavirenz chưa được thiết lập
Efavirenz vả có thẻ thay đôi phụ thuộc
AUCTZI%, vảocóđêkhảngvới
darunavỉr hay không.
W
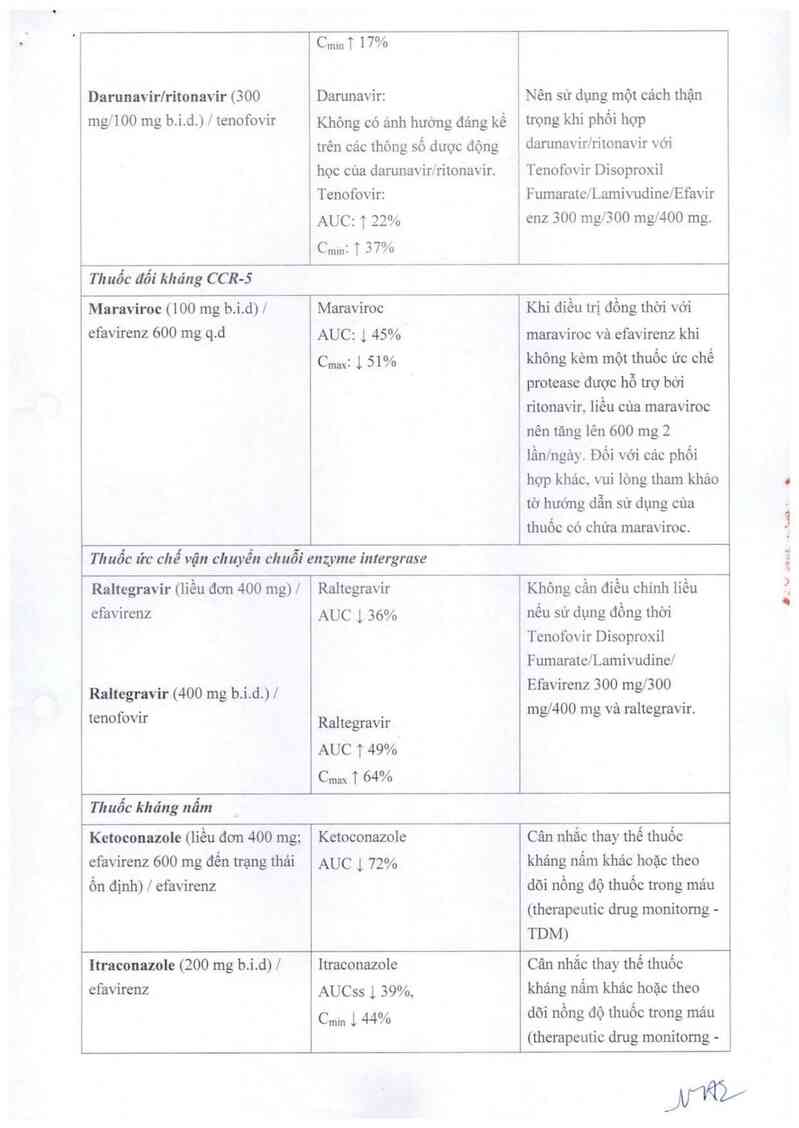
Damnavir/ritonavir (300
mg/lOO mg b.i.d.) | tenofovir
Cmin T 17%
Darunavir:
Không có ảnh hưởng đáng kể
trên các thông số dược động
học cùa darunavir/ritonavir.
Nên sử dụng một cảch thận
trọng khi phối hợp
damnavir/ritonavir với
Tenofovir Disoproxil
Tenofovir: F umarate/ Lamivudine/Efavir
AUCỵ T 22% enz 300 mg/3OO mg/4OO mg.
Cmin: T 37%
Thuốc đối kháng CCR-5
Maravỉroc (100 mg b.i.d) / Maraviroc Khi điều trị dồng thời với
efavirenz 600 mg q.d AUC: 1 45% maraviroc vả efavirenz khi
Cmaxĩ l 51% không kèm một thuôc ửc chê
protease được hỗ trợ bởi
ritonavir. liều của maraviroc
nên tâng lên 600 mg 2
lần/ngảy. Đối với cảc phối
hợp khảo. vui lòng tham khảo
tờ hướng dẫn sử dụng cùa
thuôo có chứa maraviroc.
! › [ Z :. .
T huoc ưc che vận ch uyen chuoz enzyme mtergrase
Raltegravir (liều đơn 400 mg) | Raltegravir Không cần diều chinh liều
efavirenz AUC 1 36% nếu sử dụng đồng thời
Tenofovir Disoproxil
FumaratefLamivudine/
Raltegravir (400 mg b.i.d.) | Efavirenz 300 mg/3OO _
t en ofo vir Raltegravir mg/4OO mg va raltegravư.
AUC T 49%
Cmax T 64%
T huốc kháng nấm
Ketoconazole (liều đơn 400 mg; Ketoconazole Cân nhắc thay thế thuốc
efavirenz 600 mg đến trạng thái AUC l 72% khảng nấm khảc hoặc theo
ổn định) | efavirenz dõi nồng độ thuốc trong máu
(therapeutic drug monitorng —
TDM)
Itraconazole (200 mg b.i.d) | Itraconazole Cân nhắc thay thế thuốc
efavirenz AUCss 1 39%, kháng nấm khác hoặc theo
Cmin 1 44% dõi nồng độ thuốc trong máu
(therapeutic drug monitomg -
W
I; V .….L
TDM)
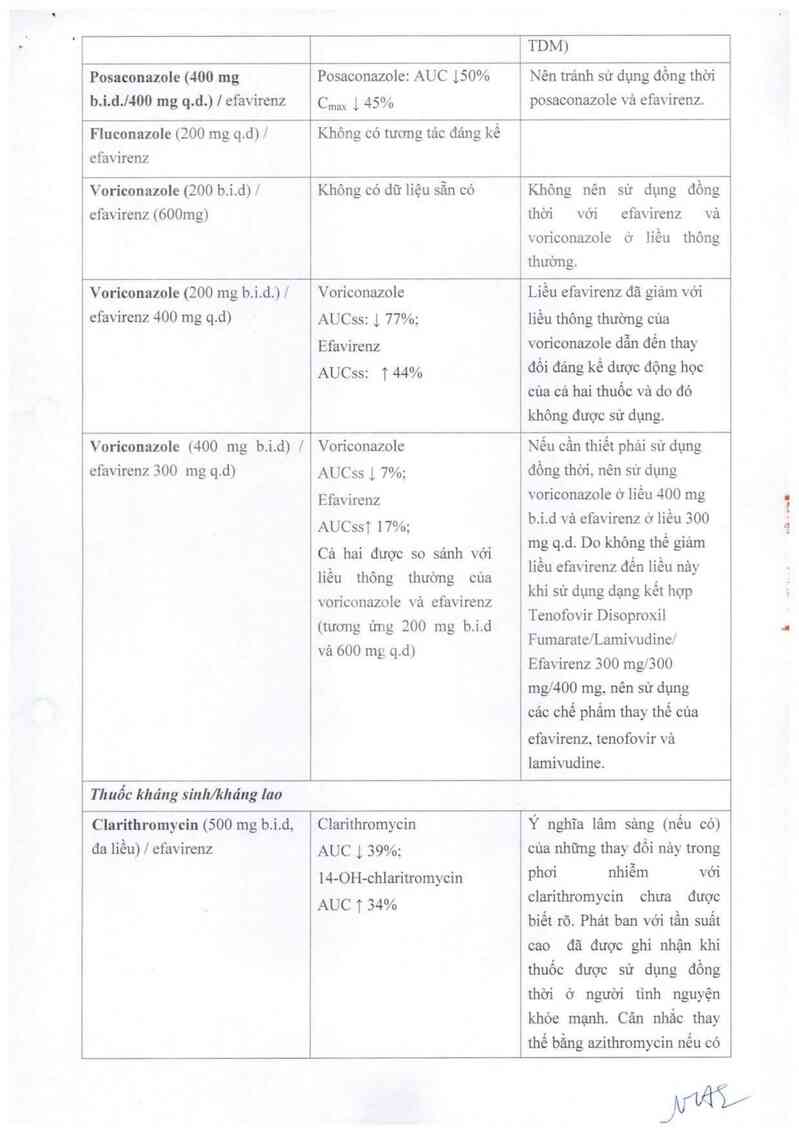
Posaconazole (400 mg
b.i.dJ400 mg q.d.) | efavirenz
Posaconazole: AUC 150%
Cmax J, 45%
Nên tránh sử dụng đống thời
posaconazole vả efavirenz.
Fluconazole (200 mg q.d) /
efavirenz
Không có tương tác đáng kể
Voriconazole (200 b.i.d) /
efavirenz (600mg)
Không có dữ liệu sẵn có
Không nên sử dụng đồng
thời vởi efavirenz vả
voriconazole ở liều thông
thường.
Vorỉconazole (200 mg b.i.d.) /
efavirenz 400 mg q.d)
Voriconazole
AUCss: l 77%;
Efavirenz
AUCss: T 44%
Liều efavirenz đã giảm với
liều thông thường cùa
voriconazole dẫn đến thay
đồi đáng kể dược động học
của cả hai thuốc và do đó
không được sử dụng.
Voriconazole (400 mg b.i.d) /
efavirenz 300 mg q.d)
Voriconazole
AUCss l 7%;
Efavírenz
AUCssT 17%;
Cả hai được so sánh với
liều thông thường cùa
voriconazole vả efavirenz
(tương ứng 200 mg b.i.d
và 600 mg q.d)
Nếu cần thiết phải sử dụng
đồng thời, nên sử dụng
voriconazole ở liều 400 mg
b.i.d vả efavirenz ở liều 300
mg q.d. Do không thế giảm
liều efavirenz đến liều nảy
khi sử dụng dạng kết hợp
Tenofovir Disoproxil
Fumarate/Lamivudine/
Efavirenz 300 mg/3OO
mg/4OO mg, nên sử dụng
các chế phẩm thay thế cùa
efavirenz, tenofovir vả
lamivudine.
T h uốc kháng sinh/kháng Iao
Clarithromycin (500 mg b.i.d,
đa liều) / efavirenz
Clarithromycin
AUC 1 39%;
l4-OH—chlaritromycin
AUC T 34%
Ý nghĩa lâm sảng (nếu có)
của những thay đổi nảy trong
phơi nhiễm với
clarithromycin chưa được
biết rõ. Phảt ban vởi tần suất
cao đã được ghi nhận khi
thuốc được sử dụng đồng
thời ở người tình nguyện
khỏe mạnh. Cân nhắc thay
thế bằng azithromycin nếu có
W
thế.
Azithromycin (liều đơn 600
mg) / efavirenz (400 mg 1
Không có tương tác dược
động học có ý nghĩa trên lâm
Không cân điêu chinh liêu.
lẩn/ngảy) sảng.
Rifampicin (600 mg q.d. đa Efavirenz Khi điều trị đồng thời. nên
liều)/ efavirenz AUC 1 26%. cân nhắc tăng liều efavirenz
C…… 1 32% từ 600 mg đến 800 mg q.d.
Rifabutin (300 mg q.d) / Rifabutin Tăng liều rifabutin khoảng
efavirenz AUCss l 38% 50% nểu sư dụng đồng thời
T huốc kháng sốt rét
Atovaquone Chưa có nghiên cứu tương
Chloroquine tảC chính thức. CảC tương ỈảC
Mefloquine thuốc và tính an toản khi sử
Proguanil, dụng đong thơ] với efavnrenz
đ 'nh ' ' ^t h
Sulfadoxine chưa dược a gia mọ các
Pyrimethamine / efavirenz
hệ thống. theo lý thưyểt hầu
như không có tương tác
thưốc đảng kể với efavirenz.
Amodiaquine/artesunate
(600/250 mg q.d.) / efavirenz
Một nghiên cứu tương tảc
(efavirenz ở trạng thái ổn
định) kết thúc sau khi 2 đối
tượng đầu tiên gia tăng
enzyme gan đảng kể nhưng
không có triệu chứng sau một
chu kỳ 3 ngảy sử dụng
amodiaquine.
AUC của amodiaquine T
tương ứng 114 và 302%
Có thể tăng độc tính trên gan.
Tránh phối hợp.
Quínine | efavirenz
Chưa có nghiên cứu chỉnh
thức về tương tác. Quinine
được chuyền hóa rộng rãi bởi
Nếu có thề, nên thay thế
quinine bằng thuốc khảc khi
sử dụng phối hợp vởi
CYP3A. Sử dụng đồng thời efavirenz .
với efavirenz có thể lảm giảm
phơi nhiễm quinine và giảm
tảc dụng kháng sốt rét.
Lumefantrine, halofantrine/ Không có nghiên cứu tương Không khuyến cảo sử dụng
efavirenz tảc thuốc chính thức được đổng thời.
thực hiện. Những thuốc nảy
được chưyển hóa bời CYP3A,
do đó, sử dụng đồng thời với
W
efavirenz có thế lảm giảm
phơi nhiễm.
: o . Â …
Artemtsmm và dẫn chat cua
nỏ/ efavirenz
Cảc nghiên cứu tương tảc
thuốc chinh thức chưa được
thực hiện. Artemisinin và dẫn
chất cùa nó được biến đối
thảnh chất chuyền hóa có
hoạt tính bởi C YP3A. Phơi
nhiễm có thế giảm bời
efavirenz. Thiếu số liệu thực
nghiệm và chưa biết hậu quả
[âm sảng có thể xảy ra.
THUỐC KHẤNG WR US HB V
Adefovir dipivoxil | tenofovir AUC: <—› Không nên sử dụng đồng thời
cnm; H Tenofovir Disoproxil
FưmaratelLamivudine/
Efavirenz 300 mg/300
mg/4OO mg với adefovir
dipivoxil do mất tảc dụng
hiệp đổng cộng.
Entecavir (] mg q.d.) AUC: <—› Không có tương tác dược
CmaxỈ i-+ động học đáng kể trên lâm
sảng khi sử dụng đồng thời
Tenofovir Disoproxil
FurnaratelLamivưdine/
Efavirenz 300 mgl300
mgl4OO mg với entecavir.
THUỐC CHỐNG co GIẶT
Carbamazepine (400 mg q.d)/ Carbamazepine Nên trảnh sử dụng đồng thời
efavirenz AUCss: l 27%, trừ khi có thế theo dõi nồng
Cmin l 35%; độ trong huyết tương của
Efavirenz carbamazepine vả efavirenz.
AUCss: J, 36%,
C… 147%
Phenytoin | efavirenz
Chưa có nghiên cứu tương tảc
được thực hiện. Có thể tăng
Trảnh sử dụng đồng thời trừ
khi có thế theo dõi nồng độ
độ thanh thải phenytoin và của phenytoin vả efavirenz
efavirenz. trong huyết tương.
Valproic acid (250 mg b.i.d)/ Hầu như không có tương tảc
efavirenz đáng kế.
W
no.
' Vigabatrin
Hầu như không có tương tác
đảng kế.
Có thể sử dụng đồng thời
Tenofovir Disoproxil
Fưmarate/Lamỉvudỉne/Efavir
enz 300 mg/3OO mgl4OO mg
vả vigabatrin mà không cần
điều chinh lỉều.
l
THUỐC TIM MẠCH
Thuốc chẹn kênh calci
Diltiazem (240 mg q.d.) /
efavirenz
Diltiazem:
AUC : 1 69%
Desacetyl diltiazem:
AUC: 175%
N—monodesmethyl diltiazem:
AUC: 137%
Theo dõi ảnh hướng trên lâm
sảng cùa diltiazem và tăng
liêu nêu cân thiêt.
Verapamil, felodipine,
nifedipine, uicardipine |
Chưa nghiên cứu tương tác
thuốc. Phơi nhiễm với thuốc
Theo dõi ảnh hưởng trên lâm
sảng và tăng liêu thuôc chẹn
efavirenz chẹn kênh calci hầu như bị kênh calci nếu cần thiết.
giảm khi sử dụng đồng thời
với efavirenz.
Các thuốc hạ !ỉpỉd
Atorvastatin (10 mg q.d)l Atorvastatin: Nên định kỳ theo dõi nồng độ
efavirenz AUC: l 43% cùa cholesterol và tăng li Ă
Tổng phần có hoat tính: cùa atorvastatin trong trư`
AUC_ 1 34% hợp hiệu quả không đầy đủ
Pravastatin (40 mg q.d.) | Pravastatin: Nên định kỳ theo dõi n độ
efavirenz AUC: 1 40% của choiesterol và tăng liều
cùa pravastatin trong trường
hợp hiệu quả không đẩy đù.
Simvastatin 40 mg q.d.) | Simvastatin: Nên định kỳ theo dõi nồng độ
efavirenz AUC: l 69% của cholesterol và tăng liều
Tổng phần có hoạt tính: của simvastatin trong trường
AUC' 1 60% hợp hỉệu quả không đẫy đù.
Rosuvastatin l efavirenz
Tương tảc chưa rõ.
Rosuvastatin được đảo thải
phần lởn dưới dạng không đổi
trong phân, do đó, không có
tương tảc thuốc trong chuyến
hóa với efavirenz.
THUỐC TRẢNH mm có CHỬA HORMON
Ethinylestradiol/norgestimate
(0,035 mg + 0.25 mg q.d)/
efavirenz
Không thay đối phơi nhiễm
ethinylestradiol.
Levonorgestrel
AUC 1 83%,
Norelgestromin
AUC 1 64% (chất chuyền
hóa có hoạt tính).
Nên sử dụng biện pháp tránh
thai đảng tin cậy cùng với
thuốc trảnh thai đường uống.
DMPA (tỉêm bắp liều đơn 150
mg) | efavirenz
Dược động học vả hiệu quả
của DMPA không bị thay đối
do điều trị dồng thời với
Do thông tin còn hạn chế,
phải sử dụng biện phảp trảnh
thai đáng tin cậy cùng với
efavirenz. thuốc trảnh thai có chứa
hormon.
Etonogestrel (que cấy) | Tương tác thuốc chưa được Phải sử dụng biện phảp tránh
efavirenz
nghỉên cứu. Có thế giảm phơi
nhiễm etonogestrel do sự
cảm ứng C YP3A của
efavirenz. Đôi khi có những
bảo các hậu mại về việc mất
hiệu quả tránh thai cùa
etonogestrel ở những bệnh
nhân phơi nhiễm vởỉ
efavirenze.
thai đáng tin cậy cùng với
thuốc trảnh thai đường uống.
THUỐC ức CHẾ MIỀN DỊCH
Tacrolimus, cyclosporine,
sirolimus | efavirenz
Tương tảc thuốc chưa được
nghiên cứu chính thức. Giảm
phơi nhiễm với các thuốc lảm
suy giảm miễn dịch có thể
được mong đợi khi sử dụng
đồng thời với efavirenz.
Có thể cần điều chinh liều
cùa thuốc ức chế miễn dịch.
Khuyến cáo theo dõi chặt chẽ
nồng độ thuốc ức chế miễn
dịch trong it nhất 2 tuần (cho
tới khi đạt nồng độ ở trạng
thái ồn định) khi bắt đầu hoặc
ngừng điều trị bằng
Tenofovir Disoproxil
Fumarate/Lamivudine/Efavir
enz 300 mgl3OO mg/4OO mg.
CÁC THUỐC KHÁC
Methadone | efavirenz Methadone Theo dõi cảc triệu chứng cai
AUC l 52% thuôc và tăng liêu methadone
nêu cân thiêt.
Buprenorphine | efavirenz Buprenorphine Theo dõi cảc triệu chứng cai
W
AUC 1 50%; thuốc và tăng liễu
Norbuprenorphine buprenorphine nếu cần thiết.
AUC l 71%
(chất chuyền hóa có hoạt 1
tính) 1
Mặc dù, giảm phơi nhiễm với
cảc thưốc nảy. không có bệnh
nhân nảo trong nghiên cứu
thế hiện cảc triệu chứng cai
thưốc.
Warfarin | efavirenz Không có sẵn nghiên cứu Theo dõi INR. Có thể cần
tương tảc thuốc. Sử dụng thiết điều chinh liều warfarin.
đổng thời có thề lảm giảm (vả
ít khả nảng tăng) phơi nhiễm
warfarin.
Lorazepam (lỉều đơn 2mg) | Lorazepam: Không cằn thiết điều chinh
efavirenz AUC: T 7% (T 1 đến T 14) liều.
Midazolam, Triazolam | Cảc nghiên cứu về tương tảc Cảc thuốc benzodiazepine
efavirenz thuốc không có sẵn. được chưyến hóa bời
CYP3A. Trong khi efavirenz
là một thuốc cảm ứng
CYP3A trên in vivo. nó tác
động như một chất ức chế
trên in vítro. Hiện chưa bỉết
ảnh hưởng cùa việc sử dụng
thuốc đồng thời trên dược
động học của midazolam vả
triazolam. Nên thận trọng khi
sử dụng đồng thời.
St. John’s Wort (Hypericum Các nghiên cứu về tương tảc Chống chỉ định điều trị đồng
perforatum ) thuốc không có sẵn. thời. Sử dụng đồng thời hầu
/ efavirenz như lảm giảm nồng độ
efavirenz vả gây thất bại
virus học.
PHỤ NỮ có THAI VÀ CHO CON BỦ
Phụ nữ có khả năng mang thai
Dựa trên dữ liệu trên động vật, khưyến cảo trảnh có thai ở những phụ nữ đang được điều trị bằng
efavirenz, một trong cảc thảnh phần cùa Tenofovir Disoproxil FumaratelLamivudine/Efavirenz 300
mg/3OO mg/4OO mg. Luôn luôn ngừa thai bằng vật chắn cùng với cảc biện pháp ngừa thai khảc (ví dụ
như cảc thuốc trảnh thai có chứa hormon dùng đường uống và cảc biện phảp khác) . Do thời gian bán
W
Ithải cùa efavirenz kéo dải, khuyến cảo sư dụng các biện pháp tránh thai đầy đủ trong 12 tuần sau khi
ngừng efavirenz. Phụ nữ có khả năng mang thai nên thử thai trước khi bắt đằư sử dụng Tenofovir
Disoproxil Fumarate/Lamivudine/Efavỉrenz 300 mg/3OO mg/4OO mg.
Phụ nữ có thai:
Cảc nghỉên cứu efavirenz ở động vật cho thấy độc lính trẻn hệ sinh sản. bao gồm anh hướng gây quái
thai rõ rệt. Các trường hợp dị tật ống thần kinh ở trẻ sơ sinh dược sinh bời người mẹ phơi nhiễm
thuốc trong 3 thảng đầu cùa thai kỳ đã được bảo cảo. Cảc dữ liệu hậu mại có sẵn
(
liệu ban đầu. không chứng to gia tảng sô lượng dị dạng ớ người mẹ phơi nhiễm với efavirenz cũng
u wax _:i 'ìl`ợịi~~iĩ"
cum) bao gồm số lượng phụ nữ có thai đủ để loại trừ việc tăng gấp 2 lần so với dữ
như không có kiếu dị dạng đặc trtmg nảo. Không nẻn sư dụng efavirenz trong suốt 3 tháng đằư cùa
thai kỳ.
Cảc nghiên cứu trên động vật không chỉ ra ảnh hưởng có hại trực tiếp hoặc giản tiếp của tenofovir
disoproxil fumarate đối với thai kỳ, phát ưiến cùa thai nhi, quá trình sinh hoặc sự phảt triền sau sinh.
Ở người, tính an toản của tenofovir trong thai kỳ chưa được thiết lập đầy đù. Số lượng đầy đủ của
phơi nhiễm trong 3 tháng đầu thai kỳ đã được theo dõi, tuy nhỉên, dế phải hiện tăng ít nhất 2 lần trong
cưistrxxmn).
nguy cơ dị tật bẩm sinh toản bộ. Không phải hiện gia tăng dị tật thai.(mmựu r
Không có gia tăng nguy cơ dị tật bẩm sinh được bảo các đối với lamivudine (xxxxw.zmrceầstrx .com).
Tuy nhiên, nguy cơ trên thai không thế được loại trừ.
Do efavirenz có thể gây quải thai. không nên sử dụng Tenofovir Disoproxil
FumaratelLamivudine/Efavirenz 300 ng300 mg/4OO mg trong suốt 3 tháng đầu thai kỳ vả chỉ sử
dụng trong những tháng tìếp theo nếu lợi ích đem lại vượt qua nguy cơ có thể xảy ra.
C ho con bú:
Cảc nghiên cứu trên động vật cho thắy tenofovir được bải tiết vảo sữa. Chưa biết tenofovir có được
đảo thải trong sữa mẹ hay không. Lamivudine được bải tiết vảo sữa mẹ của phụ nữ cho con bú, không
chắc efavirenz có được bải tiết vảo sữa mẹ hay không.
Tham khảo cảc khuyến cáo về HIV vả việc cho con bú sữa mẹ (ví dụ từ WHO) trước khi cho lời
khuyên cho bệnh nhân về vấn đề nảy. Lựa chọn có thể thay đổi tùy theo hoản cảnh tại địa phương.
ẢNH HƯỞNG LÊN KHẢ NĂNG LÁI XE VÀ VẶN HÀNH MÁY MÓC
Chưa có nghiên cứu về ảnh hướng trên khả năng lái xe và vận hảnh mảy móc. Tuy nhiên, choáng
vảng có thế được bảo cáo trong suốt quá trình điều trị bằng efavirenz vả tenofovir disoproxil
fumarate. Efavirenz có thể cũng gây rối loạn tập trung vả/hoặc rối loạn giấc ngù. Các bệnh nhân nên
được khuyên nếu họ gặp cảc triệu chứng nảy nên trảnh cảc hoạt dộng nguy hiểm như lải xe và vận
hảnh mảy móc.
TÁC DỤNG KHÔNG MONG MUÔN
Các tảc dụng không mong mưốn sau đã được bảo cáo trong cảc nghiên cứu lâm sảng cỏ kiếm soát
trong suốt quá trình điều trị nhiễm HIV bằng efavirenz, lamivudine vả/hoặc tenofovir disoproxil
fumarate.
Các tảc dụng không mong muốn được xem là có khả năng liên quan đển thuốc điều trị được liệt kê
bên dưới theo hệ thống cơ thề, lớp cơ quan và tần suất tuyệt đối. Tần sưất được xảc định là rất thường
gặp (ì1110), thường gặp (21/100, <1/10). ít gặp (ầl/IOOO, <1/100), hỉếm gặp (21/10000. <1/1000),
rất hiểm gặp (<1/ 10000). Ngoài ra còn có cảc tảc dụng không mong muốn được xác định trong sưốt
W
' quá trình sư dụng sau khi được thuốc dược phê duyệt (phân loại tằn suất: không biết). Do cảc tác
dụng không mong muốn nảy được báo cảo một cách tự nguyện từ một dân số không thế xảc định
được kích cỡ nên không thế xảo định được tần suất. Cảc tảc dụng không mong muốn nảy được đưa
vảo do có khả năng có mối quan hệ nhân quả với các thảnh phần hoạt tính trong Tenofovir Disoproxil
F umarate/Lamivudine/Efavirenz 300 mg/300 mg’400 mg. theo mức độ nghiêm trọng vả số lượng bảo
cáo.
Rối Ioạn ch uyển hóa vả dinh dưỡng
Rất thzrỏng gặp: tảng triglycerid lủc đói. cholesterol toản phần. HDL vả LDL. giảm phosphat máu.
Hiếm gặp: nhiễm toan acid lactic.
Khóng biết: loạn dưỡng mỡ, hạ kali máu.
Rối Ioạn máu vả hệ bạch huyết
Í! gặp: giảm bạch cầu trưng tính, thiếu mảu, giảm tiều cầu
Rất hiếm gặp: suy tủy xương một dòng hồng cẩu
Rối Ioạn hô hấp, ngực và trung thất
T hưởng gặp: ho, cảc triệu chứng ở mũi
Rất hiếm gặp: khó thở
Rối Ioạn hệ thẩn kính trung ương
Rất thưòng gặp: chóng mặt
Thường gặp: giấc mơ bất thường, rối loạn sự chú ỷ, đau đầu. mất ngủ, buồn ngù.
Ít gặp: kích động, quên, thất điều, phổi hợp bất thường, lù lẫn, co gỉật, tư duy bất thường.
Rất hiếm gặp: bệnh thần kinh ngoại vi (tê dại)
Khỏng biểt: run
Các rổi !oạn tãm thần
Thường gặp: lo âu và trầm cảm
Ỉt gặp: cảm xúc không ốn định, gây hấn, hưng phấn, ảo tưởng, hưng cảm, hoang tướng paranoia, dự
định tư từ, ý nghĩ tự tứ.
Khóng biết: tâm căn,
Rối Ioạn gan mật
I71ưỏng gặp: tăng enzym gan
Ít gặp: viêm gan cấp
Không biết: suy gan, gan nhiễm mỡ
Rối Ioạn thận và tiết niệu
Hiếm găp: suy thận cấp, suy thận, bệnh ống lượn gần (bao gồm hội chứng Fanconi), tãng creatinin
hưyết thanh
Rất híếm gặp: hoại tử ống thận cấp
Không biết: viêm thận (bao gồm víêm thận kẽ cấp), đái thảo nhạt do thận
Rối Ioạn da và mô dưới da
Rất Ihưòng gặp: phát ban
Ĩ7mờng gặp: ngứa. mất tóc
Ít gặp: hồng ban đa dạng, hội chứng Stevens-Johnson.
Không biết: viêm da dị ứng ảnh sảng
Rối Ioạn cơ xương và mô liên kết
T hưởng gặp: đau khớp. đau cơ
Khỏng biết: ly giải cơ vân. nhuyễn xương (biền hỉện đau ở xương vả hiếm khi góp phần vảo gãy nứt
xương). yếu cơ. bệnh cơ. hoại từ xương.
Rối Ioạn vú vả hệ sinh sản
ỈI gặp: wi to ở nam giới
Rối !oạn mắt
Ít gặp: nhin mờ
Rối Ioạn lai vả mê nhĩ
Ỉt gặp: chóng mặt
Không biển ù tai
Rối Ioạn tiêu hóa
Rất thường gặp: tiêu chảy, buồn nôn. nôn
T hưởng gặp: đau bụng, đầy hơi,
Ít gặp: viêm tụy cắp
Rối Ioạn chung và rối loạn tại chỗ
Thường gặp: mệt mòi, khó ở, sốt
Không biết: hội chứng tải tạo miễn dịch, đỏ bừng mặt.
Mô tả một số tác dụng không mong muốn
Bệnh ổng thận
Các tác dụng không mong muốn sau đã được liệt kê theo hệ thống cơ thể ở trên, có thể xuất hiện như
hậu quả cùa bệnh ống lượn gần do tenofovir disoproxil fumarate: tiêu cơ vân, nhuyễn xương (biền
hiện đau xương và hiếm khi gây găy xương), hạ kali máu, yếu cơ, bệnh cơ và hạ phosphat mảu.
Những biến cố nảy không được xem là do Tenofovir Disoproxil Fumarate/Lamiwdine/Efavirenz 300
mg/3OO mg/4OO mg nếu không xưất hiện bệnh ống lượn gần.
Các rriệu chửng trên hệ thần kinh
Cảc triệu chứng trên hệ thần kinh thường gặp đối với efavirenz, một trong các thảnh phần của
Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg. Trong các nghiên
cứu lâm sảng có kiểm soát cùa efavirenz, cảc triệu chứng trên hệ thần kinh với cường độ trung bình
đến nặng xuất hiện ờ 19% bệnh nhân (trường hợp nặng chiếm 2%) và 2% bệnh nhân ngừng điều trị
do cảc triệu chứng nảy. Các triệu chứng nảy thường bắt đầu trong 1 đến 2 ngảy đầu điều trị bằng
efavirenz và thường hồi phục trong 2 đến 4 tuần đầu. Triệu chứng có thể xuất hiện thường xưyên hơn
khi sử dụng Tenofovir Disoproxil Fumarate/Lamivudine/Efavirenz 300 mg/3OO mg/4OO mg trong bữa
ãn, có thể do tăng nồng độ efavirenz trong huyết tương. Sử dụng thuốc trước khi đi ngủ giúp cải thiện
khả năng dung nạp những triệu chứng nảy.
Ảnh hưóng trên xương của renofovir ở thanh thiếu niên
W
' Ành hướng của tenofovir trên khối lượng xương ở những người chưa phát triền hoản chinh là một
quan ngại về tính an toản cụ thể theo lý thuyết. Đảnh giá các tảc dụng không mong muốn dựa trên
một thử nghỉệm ngẫu nhiên trên 87 trẻ em nhiễm HIV ( 12 đến <18 tưổi) được điều trị bằng tenofovir
(N=45) hoặc giả dược (N=42) phối hợp vởi cảc thuốc kháng retrovirus khảc trong 48 tuần. Ành
hưởng trên xương được ghi nhận ở những trẻ từ 12 tuổi trở lên như tảng chu chuyền xương. phù hợp
với những gì được ghi nhận ở các nghiên cứu lâm sảng ở người lớn.
QUÁ LIÊU
Nếu xảy ra quá liều. cần theo dõi các bằng chứng của độc tính và thực hiện các biện pháp điều trị hỗ
trợ chuẩn nếu cần thiết.
Một vải bệnh nhân dùng efavirenz 600 mg ?. lần/ngảy một cảch tình cờ đã được bảo cảo là tăng cảc
triệu chứng trên hệ thần kinh. Một bệnh nhân đã bị co cơ vô ý. Có thể sử dụng than hoạt để loại bỏ
cfavirenz chưa được hấp thu. Không có chất giải độc đặc hiệu khi quá liều efavirenz. Do efavirenz
gắn kết mạnh với protein trong huyết tương, thẩm phân mảu hầu như không thể loại bỏ được
efavirenz khỏi máu.
Tenofovir có thể được loại bỏ bới thấm phân mảu, hệ số thanh thải bằng thấm phân mảu trung bình
cùa tenofovir là 134 ml/phút. Sự đảo thải tenofovir bằng thẩm phân phúc mạc chưa được thực hiện.
Do lamivudine được loại bỏ không đáng kể qua thầm phân máu (4 giờ), thấm phân phủc mạc liên tục,
và thấm phân phủc mạc tự động, không biết rõ thẩm phân mảu liên tục có đem lại lợi ích lâm sảng
nảo khi quá liều lamivudine hay không.
BÁO QUẢN
Bảo quản ở nơi khô mảt, không quá 30 0C . Bảo quản trong bao bì gốc. Tránh ánh sáng.
HẠN DÙNG: 24 tháng kể từ ngảy sản xuất.
Mylan
Sản xuất bời: MYLAN LABORATORIES LIMITED.
Piot No. 11,12 & 13, Indore Special Economic Zone, Phanna Zone, Phase-II, Sector—III, Pỉthampur —
454775, Dist. Dhar, Madhya Pradesh, Ẩn Độ.
Ngảy xem xét sửa đổi, cập nhật:
Tâi liệu tham khảo:
Tải liệu tham khảo chung:
European SmPC, Sustiva:
http:l/www.ema.europa.eu/docs/en_GB/document_library/EPAR_Product_
Information/human/OOOZ49/WCS000583 1 1 .pdf
European SmPC, Vìread:
http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Product_
Infonnation/human/OOO4I9/WC50005173 7.pdf
Viread, US prescribing information, available at: xvmv.nilead.com `pdtĩ“`viread pi.nđt`
E uropean SmPC, Epivir:
W
' him: xvxnv.cnm.cnronacư docs en GBđoctnncni liinnrx EP.-\R —
Product Informutionfhumau UUUNỮ \K'C5íltl0375710d1`
WHO: Antiretroviral therapyfor HIVinfection in adults and adolescents.
htlD: \\1hịlihthit'.~txiiu.íht D'tii2iiCtìiitìiìở' ÌUẺU ỌĩờhC—i ] Ể^fCỂ(²4__ciiư.iìtit'
Các tâi liệu tham khảo khác bao gồm:
Mục tương tác thuốc
van Leth et al Lancet. 20041363:1253-63 European SmPC Telzir.
http:J/vxwwzemaeumDa.eu/docs/
en GB/document librarv/EPAR Product Informationlhuman/OOOSB4/WCSOOO35345.Ddf
European SmPC Crixivan.
ht_tp:/lwww.ema.europa.eufdocslen GB/document libfflg/EPAR Product
Information/human/OOO128/WC500035730.0đf
Smith et al. Antimicrob Agents Chemother, 2005. 49(8): 3558-3561 Kaletra, Scientific Discussion.
httnz//www.ema.eurona.euldocs/en GB/document librarv/EPAR Scientific Discussionlhuman/OOO
368/WC500039040fflf
European SmPC Aptivus.
http://www.ema.europa.euldocs/en GB/document librarv/EPAR Product
Information/hưmanlOOOó3 l/WCSOOO2S93ó.Qdf
European SmPC Prezỉsta.
http://ww.ema.europa.eu/docslen GB/document libraW/EPAR -
Product Information/human/OOO707/WC500041756.pdf
Sriwiriyajan et al. Eur J Clin Pharmacol 2007;63:479-83 European SmPC ernd:
http://www.ema.europa.euldocs/en GB/document librarv/EPAR Product Information/human/OOO3
87/WC500049756.pdf
German P, et al. 14th CROI, Los Angeles, February 2007, abstract 577 DiCenzo et al. Antimicrob
Agents Chemothet
2004; 48: 4328-4331 SE Cohn et al. Clin Pharm Ther 2007; 81:222-7
Clarke et al. Br J Clin Pharmacol 2001; 51:213—17.
Wire et al. AIDS 2004;18:897-907
Aamoutse et al. C lin Pharmacol Ther 2002;71:57-67 European SmPC Invirase.
httn:l/www.ema.eurona.euldocs/en GB/document librarv/EPAR -
Product Information/human/OOOI l3/WCSOOOBSO84.Ddf
Reyataz, US prescribing information: packageinserts.bms.comlpiJni revataz.ndf
Muc phg nữ có thai và chg con bủ.
Antiretroviral Pregnancy Registry: www.apregistg.com
WHO: Antiretroviral drugs for treating pregnant women and preventing HIV infection in infants:
httpzl/whqlibdoc.who.intlpublications/20l0/9789241599818 enngf
Mgc dược Iưc hgc
W
' Gallant et al, JAMA 2004 ;292 :191-201
The Stanford HIV drug resistance database: httpz/lhivdbstanfordcdu
Mục đgzc động hgc
Haas et al. AIDS 2004 ;18z2391-400
Klein et al. Pharrnacogenet Genomics 2005; ] 5:861-73
Batreiro et al. J Infect Dis 2007;195:973-9
TUQ.CỤC mưmo
nmưme mom
%… % %… Jf’M
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng