













BANBAXY
LABORATORIES LIMITED
Ì BỘ Y TẾ
\ cuc QUAN LÝ DUỢC
f ĐÀ PHÊ DUYỆT
Lân dauO'i/ẮJOJẢ}
uu ipmn; mun
u uu mu… ll.Jis Sul
«
…
…
…
nau.unuumnzu
WIIIMWHHDWII
mm un lum… luu
ma au «… ủ… nm
\
ò/VR (iỏ C-FU
“N'S
umwmơ I'dxa
wwwmo : '…
xxxxxx ĩ'ON uJiee
er19
6… ooo suuu
…zuuuw
AVIRMIZ'"
TABLETS 600 mg
_ __ ụ
TM
muư“ ẨVlRMZ mmz'"
mms … mg TABLETS 600 mg mms … mg
EFAVIRENZ TABLETS Í EAÊI lllll\~Cũlllũ tam onmms
Ỉlm
Vusa No.1 xxxxxx
Mig. Lic. No; MNB/95/2
MADE IN INDIA
ĩ BANBAXY
LABOR ATORIES LIMITED
Village Ganguwda
Paonta Samb, District Sưmour
Himachal Pradesh ~ 173 025
MUlChD num.u
nlgu,
…nmm. … …
num
nnlh
…
ManntnhumnsemnEmnxm
SGIỊSITESI … Inn
Nt' MI! Bp` IM III BI Uilq.ỉn 00 m, IInl hu
cum…` cm cm. cum w mm` cu hnrg … .…
du nm … `
wudcun m “« nu… :d… ::
ninh nnằxfủuễlĩufflmm
<©
30 Tablels
ệ ị Ẹ ỂỄ umnz'"
ễ ĩ _s ~ị TIILFI'S 600mg
', _
ỉ ẵ Ễ Ễ EFAVIHENZTABLETS
ẵ Ễ Ẹ ỉ
z—ẫ, Ể Ê
ỉ : Ễ Ễ Ể O
ã Ễ 2 Ý ẫ
ẫ ' ; Ĩ mam -~ Ê =
5 ~“ 2 _ .
Ễ m~ Ể ải
_ uu C AVIRANZ Tab! 600 mg 30'0 CT
- … I: Label llze: 90x37 mm
Market:Viotuam
_ Mlu Blue Cv 60%
- 431 D & 10% 5men
Eiavirenl 600 mg
Dong: : As duecled uy the uhystcmn
Si… mm… aưc. ~n lhe uigìnal
cmtainsr.
-0320
-IIZIC
_ 431 c & JII% Suun
RLUPKGDE\A CK23105111- V01
Vu No; xxxxx
EFAVIRENZ TABLETS
RANẺAXY
JO Tablets
AVIRANZ Tabs 600 mg 30's CT
Carton size: 58x52x80 mm
_ WuWC "mm… Market: Vietnam
RLLIPKGDEV: CK23105111- VM
>t ẵẳ
Ể NỄ ễ2I
Ễ (ỂỂ-Ẻs’
n- ẽmẵẵỉẵ
ÉảZỄẵấì
;— ỄỔỄỄỀỄ
s Ểíẵnz'
_ ọọc K_Ỹ HU’ớgVG DẨN TR ƯỚC _Kfợ SỨDỤNG. ,
NỆU ch N THẸM THONG TIN, HÃ Y HO] Y KIỆN CUA ẸAC sg”.
THUỐC NA Y CHI ĐƯỢC SƯDỤNG THEO SỰKE ĐUN C UA BA c sỉ
VIÊN NÉN AVIRANZ 600 mg
(Viên nén Efavirenz)
THÀNH PHÀN
Mỗi viên nén bao phim chứa: Efavirenz ..................................... 600 mg
Tá dược: Microcrystalline cellulose, Croscarmellose natri (hoặc Croscarmellose sodium),
Hydroxypropyl cellulose-L, Natri lauryl sulphate (hoặc Sodium Iauryl sulphate), Lactose
monohydrate, Magnesium stearate vả Mảu vảng Opadry 03B5 28 74.
MÔ TẢ '
Viên nẻn Aviranz 600 mg chứa efavirenz, là một chất ức chế men phiên mã ngược không phải
nucleoside, chuyên biệt trên HIV-l (NNRTI). Tên hóa học cùa efavirenz lả (S)-ó-chloro—4-
(cyclopropylcthynyl)—i,4—dihydro-4-(trifiuoromethyl)—ZH—3, [ -benzoxazin-2-onc. Công thức phân
tử cùa efavirenz lả C;4iiọCiFgNOỵ và công thức câu tạo như sau:
CẤU TRÚC CỦA EFAVIRENZ
CHỈ ĐỊNH'
Efavirenz khi phối hợp với cảc thuốc kháng retrovirus khác dược chỉ định điều trị nhiễm virus
týp 1 gây suy giảm miễn dịch ở người (HIV-l). Chỉ định nảy dựa vảo hai thử nghiệm lâm sảng
trong thời gian ít nhắt một năm đã chứng minh sự ức chế lâu dải HIV RNA.
LIẺU LƯỌNG VÀ CẢCH DÙNG '~²
Trị liệu chỉ nên dược bắt đầu sử dụng khi dượơ chuyên gia có kinh nghiệm trong kiếm soát
nhiễm HIV.
VIÊN NÉN AVIRANZ 600 mg không có tất cả ở cảc phảc đồ được phê duyệt; cảc dạng bảo
chế và hảm lượng khảc cùa efavirenz nên được sử dụng trong cảc trường hợp nảy.
Người trưởng thânh
Liều lượng khuyến cáo cùa efavirenz là 600 mg, dùng đường uống, ngảy 1 lần, phối hợp với cảc
thuốc ức chế protease vả/hoặc với cảc thuốc ức chế men phiên mã ngược thuộc dổng dắng
nucleoside (NRTIS) Chi khuyến cáo sử dụng VIÊN NÉN AVIRANZ 600 MG khi dói, thích
hợp nhắt lả trước khi ngủ. Nỗng độ efavirenz tăng được quan sảt sau khi dùng Viên nén
Efavircnz kòm với thức ăn có thể dẫn đển tăng tần suất phản ửng phụ (xem ĐẶC TỈNH DƯỢC
ĐỘNG HỌC VÀ DƯỢC LỰC HỌC). Dùng thuốc trước giờ ngủ có thể cải thiên sự dung nạp
các triệu chứng trên hệ thằn kình (xem CÁNH BÁO VÀ THẬN TRỌN
và Thông tin cho bệnh nhân). 7 Ấm
(ỄỊJ New Deih ẫ
\ \_jwar
\ũ-l
1/30
VIÊN NÉN AVIRANZ 600 mg phải được sử dụng phối hợp với cảc thuốc khảng retrovirus
khảo (xem CHỈ ĐỊNH CẢNH BÁO VÀ THẬN TRỌNG, vả TL ONG TÁC THUỐC. vả
DẶC TỈNH DƯỢC ĐỌNG HỌC VÀ DƯỢC LỰC HỌC).
Chỉnh liễu
Nếu VIÊN N ẾN AVIRANZ 600 mg dược dùng đồng thời với voriconazole, liều duy trì của
voriconazole nến tăng dến 400 mg môi 12 giờ vả liếu dùng cùa efavìrenz phải giảm 50%, tức
300 mg, uống ngảy ] lần. Khi dừng điểu trị vởi voriconazolc, 1iều dùng cùa efavirenz trở về như
lủc khời đầu. Không được bè vỉên nén Efavirenz (xcm TD ƠNG TÁC THUỐC vả ĐẶC TÍNH
DƯỢC ĐỘNG HỌC VÀ DƯỢC LỰC HỌC).
Nếu VIÊN NÉN AVIRANZ 600 mg dược dùng đồng thời với rifampicin, có thể cân nhắc tăng
1iều cùa efavirenz lên 800 mg/ngảy (xem TƯỚNG TÁC THUỐC).
Bệnh nhỉ
Khuyến cáo sử dụng VIÊN NÊN AVIRANZ 600 mg khi đói, tốt nhất là trước khi ngủ Bảng
bên dưới mô tả liều dùng khuyến cảo cùa efavircnz cho bệnh nhi từ 3 tuổi trở lên và cân nặng
giữa 10 và 40 kg (xem SỬ DỤNG Ở CẢC ĐÓ] TƯỢNG ĐẶC BIỆT). Liều lượng khuyến cảo
cùa efavirenz cho bệnh nhi trên 40 kg là 600 mg ngảy [ lần.
Bảng: Liều dùng cho bệnh nhi, ngăy ] iẩn
Cân nặng Liễu Efavirenz (mg)
kg lbs
10 dến dưới 15 22 đễn dưới 33 200
15 đên dưới 20 33 dển dưới 44 250
20 đên dưới 25 44 đên dưới 55 300
25 đến dưới 32,5 55 đên dưới 71,5 350
32,5 đến dưới 40 71.5 đến dưới 88 400
11 nhât 40 Ỉt nhất 88 600
SỬ DỤNG ở cÁc Đói TƯỢNG ĐẶC BIỆT ' (Ỹ/
o Thai kỳ
Thai kỳ Nhóm D: Xem CẨNH BÁO VÀ THẬN TRỌNG.
0 Cho con bú
Khuyến cáo các bả mẹ nhiễm HIV-l không được nuôi Ẩcon bằng sữa mẹ để tránh nguy cơ truyền
HIV sau sinh. Mặc dù không biết là efavirenz có bải tiêt vảo sữa người hay không, efavirenz bải
tiết vảo sữa chuột cống Vì khả năng truyền HIV và khả năng xảy ra tảc dụng phụ nặng ở trẻ bú
mẹ, cảc bả mẹ phải dược hướng dẫn là không nuôi con bằng sữa mẹ nểu đang dùng efavirenz
0 Trẻ em
Trong một nghiên cứu đang tiến hảnh, mớ nhăn ở 57 bệnh nhi đã được điều trị bằng NRTI đế
xảc định tinh an toản, dược động học vả hoạt tính kháng virus cùa efavirenz khi phối hợp với
nelfmavir (20- 30 mg/kg, 3 lần/ngảy) vả NRTIS. Tuổi trung bình lả 8 tuoi [thay đối từ 3-16).
Efavirenz không được nghiên cứu ở bệnh nhi dưới 3 tuôi hoặc người có .eW ưới 13 kg. Ở
48 tuần, loại và tần suất phản ứng phụ thông thường giống nhau vẽ ở rig`ứơi trườẳg' hảnh ngoại
trừ tỉ lệ cao hơn về ban đò, được bảo cáo ở 46% (26/57) bệnh nhi soi 5% ở mỗi nhỏm điếu trị với cfaVircnz) với mức
độ trầm trọn ít nhẳt lả ưung binh trong số các bệnh nhãn trong nghiên cửu được điếu trị với
cfavircnz phoi hợp với zidovudinellamivudinc hoặc indinavir lá ban đỏ, choáng vảng, buổn nôn.
nhức đẩu, mệt mòi, mất ngủ vả ói mừa.
K inh nghiệm trên lhữ nghiệm lãm sảng ở nguời trướng tluìnll g'
v1 cảc nghiên cửu lâm sảng được tiển hânh ở các điều kiện thay đổi khảo nhau, ti 1ẹ phán ứng
phụ được báo cáo khỏng thế so sảnh trực tiếp với tỉ lệ trong các nghiên cửu iám sảng khác vá có
thế khõng phản ánh tỉ lệ quan sát được trong thực tế. Các phản ứng phụ trên lãm sảng được chọn
lọc về tính ưầm ưọng từ trung binh đến nặng quan sát được ở 22% bệnh nhân được điều trị với
cfavircnz trong hai thử nghiệm lâm sảng có đối chứng được thể hiện trong bâng dưới đây.
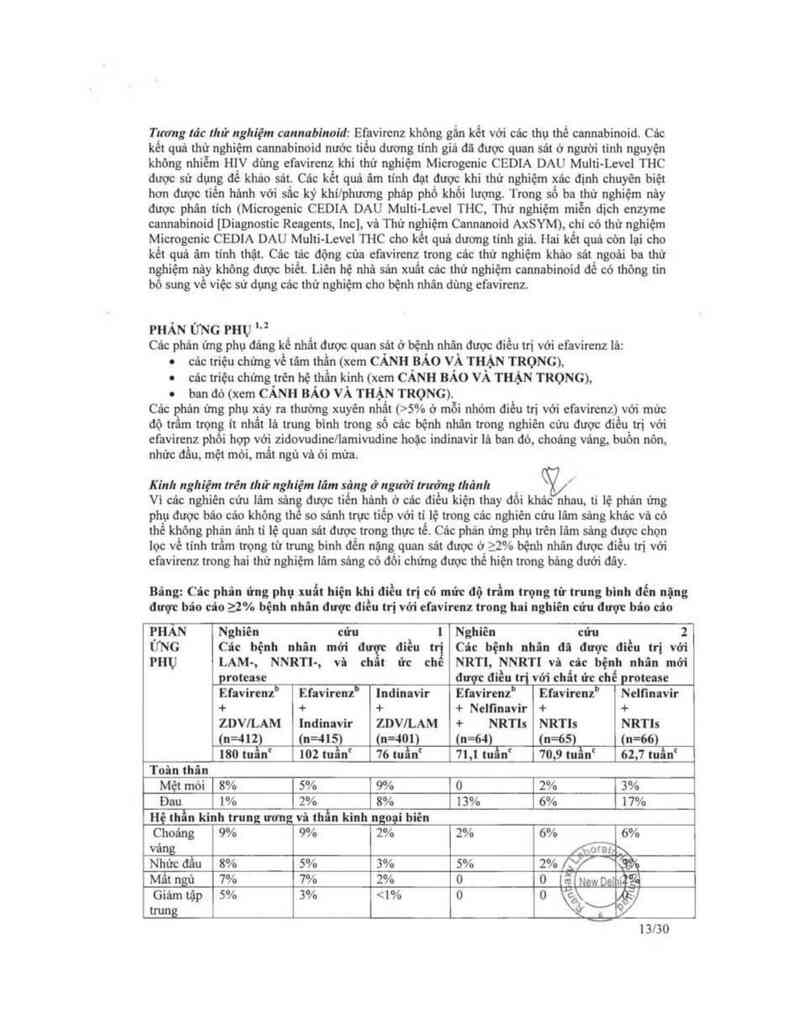
Bing: Cic phân ứng phụ xuất hiện khi đỉều trị có mức độ trẩm trọng từ trung bình đểu nặng
được bâo câo 22% bệnh nhân được đỉều trị với efavirenz trong hni nghiên cứu được báo cảo
PHAN Nghiên cứu | Nghiên cửu 2
ỦNG Các bệnh nhin mới đuỵc ớièti Các bệnh llllẩn ttii được điều trị với
PHỤ LAM-, NNRTl—, vù ch t ửc che NRTI, NNRT! vi câc bệnh nhân tnởi
protease được điều trị với chất ức chế protease
Efavircnz" Efavircnz' lnđinavir Efavircnz' Efnvirenzb Nelfinavir
+ + + + Nclftnnvir + +
ZDWLAM lndinavir ZDV/LAM + NRTI: NRTIs NRTIs
(n=412) (n=415) (n=401) (n=64) (n=65) (n=66)
l80 tuẫnt 102 tuẵnc 76 tnẫnc 7l,l tuẩn' 70,9 tnổnc 62,7 tuẫn'
Toản thin
Mệt mói 8% 5% 9% 0 2% 3%
Đau 1% 2% 8% 1 3% 6% 1 7%
Hệ thầu kỉnh trung ương vi thẩn kinh n oại biên
Choáng 9% 9% 2% 2% 6% 6%
váng ,,iiorar Ầ
Nhức đẫu 8% 5% 3% 5% 2% /;7 {%
Mâtngủ 7% 7% 2% o o (.’ảiNgwgeiiizg
on… tập 5% 3% <1% o o Ề,\ ,QỂ
… ở-Vọ“
B_ \ ứ
13l30
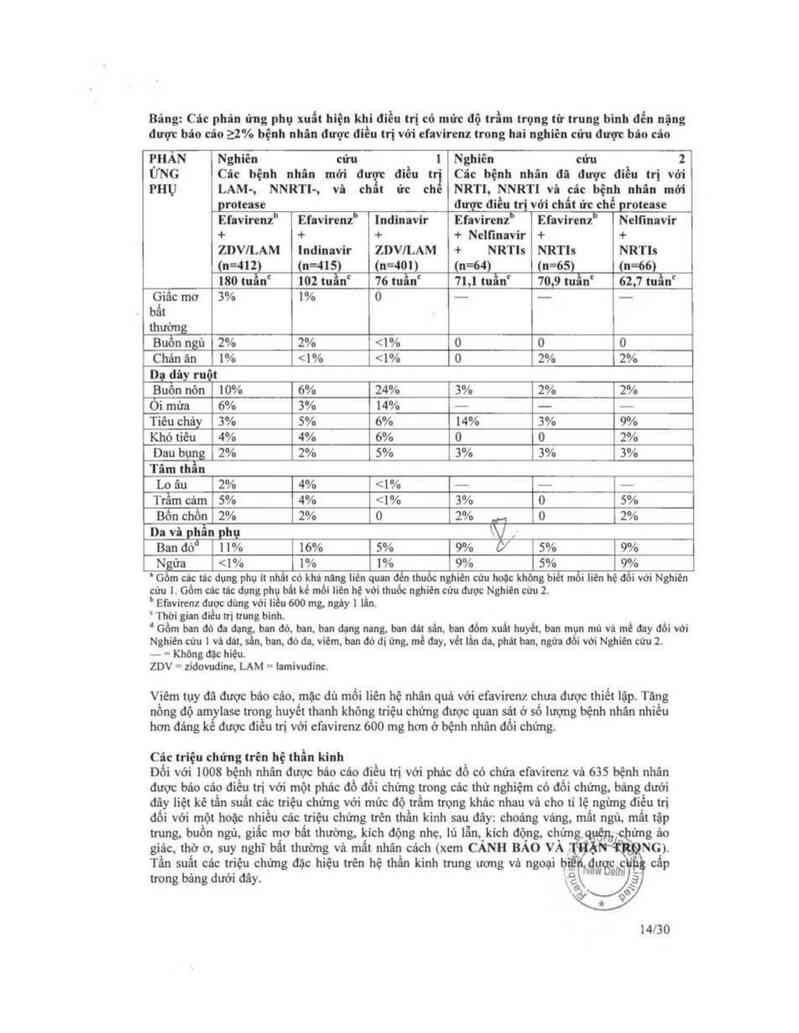
Bâng: Cđc phia ứng phụ xuất hiện khi điều tri có mức độ trếm trọng từ trung hình đến nịng
được bủo cảo 22% bệnh nhân được điều trị với efavircnz trong hni nghiên cứu được bío câo
PHẢN Nghiên cửu 1 Nghiên cửu 2
ỨNG ca 601… nhân mới đ điều t ciic bệnh nhân đã được điếu trị với
mụ LAM-, NNRTI—, vì ch t ửc ch mm, NNRTI vì cớc bệnh nhân mới
protease đuỵc điếu trị với chất ức chế protease
Efnvirenz" Efnvirenz' lnđinnvir lỉf1wircuzh Efavirenz' Nelftnavir
+ + + + Nclftnnvir + +
ZDV/LAM lndinnvir ZDVILAM + NRTIs NRTIs NRTIs
(n=412) (n=415) (n=401) (n=64) (n=65) (n=66)
100 mi…e 102 tuằn= 76 tninf 71,1 t…“…c 70,9 tuèn° 62,7 tuổn'
Giấc mơ 3% 1% o — — -
bất
thường
Buôn ngủ 2% 2% <1% 0 0 O
Chánăn 1% <1% <1% 0 2% 2%
D; dây ruột
Buồn nôn 10% 6% 24% 3% 2% 2%
ói mủa 6% 3% 14% — — —
Tiêu chảy 3% 5% 6% 14% 3% 9%
Khótiêu 4% 4% 6% o o 2%
Dau bụng 2% 2% 5% 3% 3% 3%
Tấm thẩn
Loãu 2% 4% <1% — — —
Trẫm cảm 5% 4% <1% 3% o 5%
Bôn chồn 2% 2% o 2% o 2%
Da vi phẫn phụ iỮ ,
Ban 66“ 11% 16% 5% 9% V 5% 9%
N ùa <1% 1% 1% 9% 5% 0%
' Gôm các tác đụng phụ It nhũ có khả nđng liẻn quan đến thoớc nghiến cừu hoặc khớng hỉết mới liến hệ đới với Nghiên
cửu I. Gồm dc ttc dung phụ bết kế mỏi lien hệ với thuốc nghiến cửu được Nghiên cúu 2.
’ Efnvitcnz được đùng với iièu 600 mg. ngùy 1 1Àn.
° Thời gian điếu tri ưung binh.
“còmbanớớớadạn ,banđớ.ban,bunđạngnangbnnđảtsẩn,banđđmxuấthuyết.banmụn múvâmếđayđớivới
Nghiên cứu 1 vớ đít. Ẩn ban, đỏ đn, viem, ban đó di ủng. mè đay. vết iin đa, pi… ban, ngứa đới với Nghiến cửu 2.
—— = Khđng đỌc hiẹu.
ZDV = zidovudine, LAM = [amivuđinc
Viêm tụy đã được báo cáo, mặc dù mới Iiẽn hệ nhân quả với cfavircnz chưa được thiết lập. Tđng
nông độ am lasc trong huyết thanh khõng triệu chứng được quan sát ở sô lượng bệnh nhân nhiếu
hơn đáng k được điều trị vởi efavirenz 600 mg hơn ở bệnh nhân đổi chửng.
Câc triệu chửng trên hệ thần kinh
Dối với 1008 bệnh nhân được báo cáo ttiètt trị với phác đồ có chứa efavirenz vá 635 bệnh nhân
đuợc báo cáo đỉếu trị với một phảc đồ đối chửng trong các thử nghiệm có đối chứng, bảng dười
đây liệt kê tẫn suất các triệu chứng với mức độ mi… trọng khác nhau vả cho ti 1ẹ ngỉmg điều trị
đối với một hoặc nhiễu cảc triệu chứng trên thẩn kinh sau đây: choáng váng, mất ngủ, mất tập
trung, buồn ngủ, giấc mơ bất thường, kích động nhẹ, tú lẫn, kich động. chứn qụgiị, '
giác, thờ 0, suy nghĩ bất thường và mất nhân cách (xem CẨNH BÁO VÀ ( Ặ
Tần suất các triệu chửng đặc hiệu trên hệ thần kinh trung ương vá ngoại b
trong bảng dưới đây. '
14/30
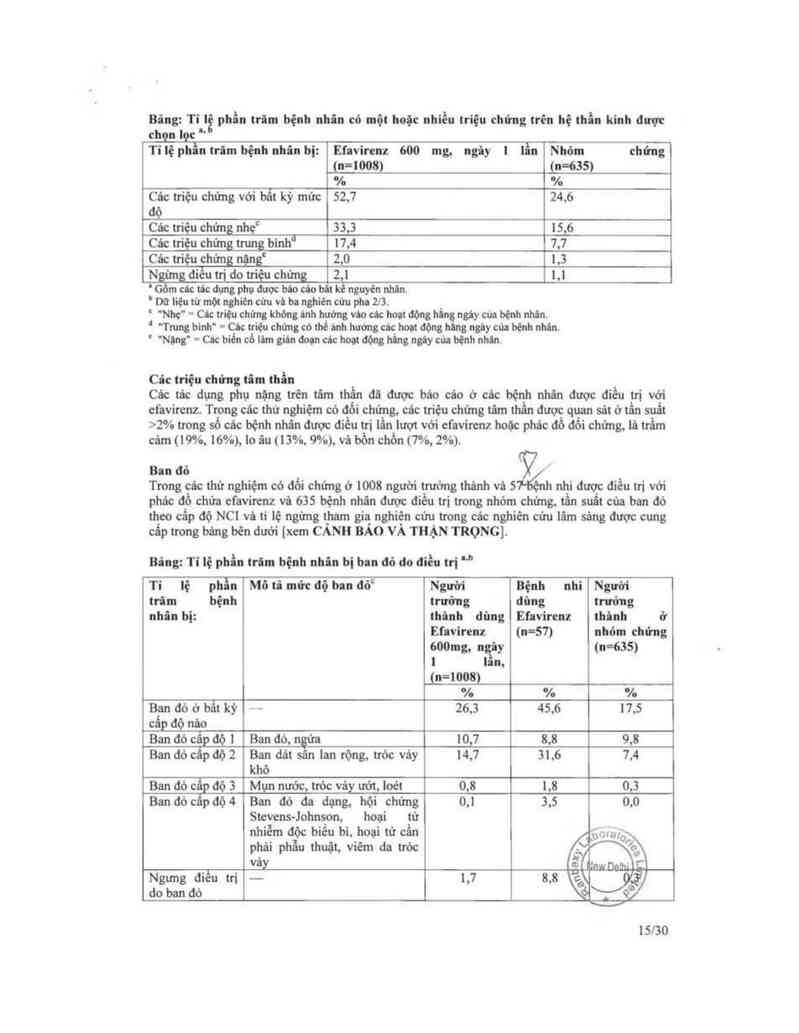
Bâng: Ti lẺ phẩn trăm bệnh nhân có một hoặc nhiếu triệu chứng trên hệ thẫn kinh được
chọn lọc "
Tỉ lệ phần trim bệnh nhin bi: Efavirenz 600 mg, ngùy I lÌn Nhỏm chứng
(n=1008) (n=635)
% %
Cảc triệu chứng với bã kỳ mức 527 24,6
độ
Các triệu chứng nhẹc 33,3 15,6
Các triệu chứng trung blnh“ 17,4 7,7
Các triệu chứng nggc 2.0 1,3
Nẵimg điêu ttị do triệu chửigÙ 2,1 1,1
' … dc tic đụng phụ được bđo cớo bãi kì nguyen nhin.
“ Dit iiẹu tử một nghiên cửu vi ba nghỉến cứu pha 273.
° "Nhẹ“ ~ Cđc ưiẹtt chửng khớng inh huởng via cớc hoạt động hằng ngùy của bệnh nhin.
“ "Trung binh" — ca: triệu chửng có thế inh hướng các hoợt động hlng ngớy cin bệnh nhin.
° ”Nặng“ = ca: biến cớ … gián đoạn cỏc hoạt ttộng itâng ngây của bếnh llhấll.
Cđc triệu chứng tâm thẩn
Cáctácdụngphụnặngtrêntâmthẫnđãđượcbáocảoờcảcbệnhnhânđượcđiếutti với
efavircnz. Trong các thử nghiệm có đổi chủng, các triệu chứng tâm thần được quan sát ở tẩu suất
>2% trong số cảc bệnh nhân được điếu trị 1ấn lượt với cfavircnz hoặc phác độ đối chửng, lả trầm
câm (19%. 16%). lo âu (13%. 9%). vâ bồn chổn (7%, 2%).
Ban đó
Trong cảc thử nghiệm có đối chứng ở 1008 người trường thảnh vá ST'áh nhi được điểu trị với
phác đồ chứa cfavirenz vè 635 bệnh nhân được điếu trị tmng nhỏm chứng, tần suất của ban đó
theo cẩp độ NC! vả tỉ lệ ngừng tham gia nghiên cửu trong các nghiên cứu iâm sâng được cung
cắp trong bảng bẽn dưới [xem CANH BẢO vA THẬN TRỌNG].
Bâng: Tỉ 1ẹ phân triim bệnh nhân bị bnn đô đo ttièu tri …
Tỉ lệ phổn Mô tả mức độ ban đỏc Người Bệnh nhi Người
trùn bệnh trướng đùng trướng
nhân bi: thình đùng Efavircnz thùnh ở
Efavirenz (n=57) nhớm chứng
600mg. n iy (n=635)
| | n,
(n=1008)
% % %
Ban đỏ ở bẩt kỳ … 26,3 45,6 17.5
cảp độ mio
Ban đó cấp độ 1 Ban đò, n ửa 10.7 8,8 9,8
Ban dò câp độ 2 Ban dát lan rộng, tróc vây 14,7 31.6 7,4
khô
Ban đò cẩp độ 3 Mụn nước, trỏc vảy ớớt, loét 0,8 1,8 0,3
Ban đò cẩp độ 4 Ban đó đa dạng, hội chứng 0,1 3.5 0.0
Stevens—Johnson, hoại tử
nhỉễnì độc bièu bì, hoại tử cằn g,ớru,g,
phâì phẫu thuật, viêm đa trỏc Ể ’fcì,
váy ãl r
Ngưng điếu trị — 1,7 8,8 cổ .
do ban đỏ , Q}
15/30
' Gồm các biến cố được bớo do khỏng liẻn quan đến nguyên nhin.
’ Dữ iiộu tù Nghiến cửu 1 va 3 nghiến cứu pha 273.
* He phia chia cip độ NCI.
Cũng ttược quan sát ở báng trên, ban đó 15 phổ biến hơn 6 bệnh nhi vả thường 6 cấp độ cao hơn
(ví đu nặng hơn) (xem THẬN TRỌNG: Cânh bảo).
Kinh nghiệm vời cfavircnz ở các bệnh nhân ngừng cảc thuốc kháng rctrovirus khảc của nhóm
NNR'I1 bị giới hạn. Mười chín bệnh nhãn ngừng sử dụng nevirapine vi ban đỏ đã được điếu trị
với efavircnz. Chin trong số cảc bệnh nhân nảy tiến triến ban đỏ nhẹ đến trung binh khi trị liệu
với cfavircnz, vả hai trong số các bệnh nhân nây ngừng điếu trị đo ban đò.
Bất ttiimg xét nghiệm _
Cảo bât thường xẻt nghiệm cấp độ 34 được báo cáo ở 22% bệnh nhân được điêu trị với
efavirenz trong hai thử nghiệm lâm sảng được thế hiện ương Báng đưới đây.
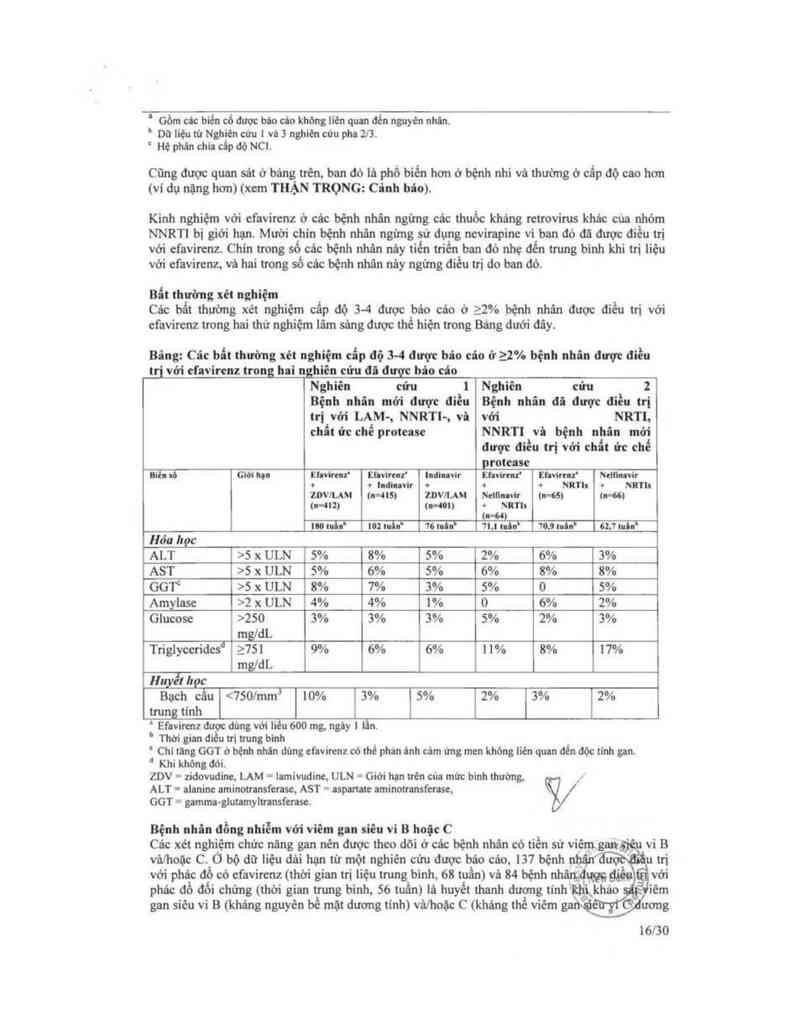
Bing: ciic bổt ti…timg xẻt nghiệm cấp độ 34 được bio cáo ở 22% bệnh mm được điếu
trị với cl'nvircnz trong hai nghiến cứu đi được báo câo
Nghiên cứu ! Nghiên cứu 2
Bệnh nhin mới được điều Bệnh nhin đi được điều trị
trị với LAM-, NNRTl-, vì với NRTI,
chấtủcchế protease NNRTI vì bệnh nhân mới
được điếu trị với chất ức chế
protease
aaha cm … Ellvircn' ctmm lnđỉuvir Eínvimz' Ellvtmz' Nellinnvir
+ + lcđinvtr + 0 + NRTI: › NIITB
znwuu ÍI²ỐỈSÌ znwum Nclũunvir (pm (o-661
in-4I2) 1puli + mưu
tI-ut
llOtnh' lum]? 7610h' 71,1th 70,90d0’ 61.710h’
Hỏa học
ALT >5 x ULN 5% 8% 5% 2% 6% 3%
AST >5 x ULN 5% 6% 5% 6% 8% 8%
GGT“ >5 x ULN 8% 7% 3% 5% 0 5%
Amylasc >2 x ULN 4% 4% 1% 0 6% 2%
Glucose >250 3% 3% 3% 5% 2% 3%
mg/đL
Trigiytzcridesd 2751 9% 6% 6% 11% 8% 17%
mgldL
Huyết học
Bạch cầu <7501mmT 10% 3% 5% 2% 3% 2%
ưunjtính
' Efavirenz được đimg với liếư 600 mg, ngùy 1 lấn.
“ Thời ginn điếu tri ưung bình
“ Chỉ tang GGT ở bệnh nhác dùng cfavirenz có thế phia inh cim ứng mcn không Iiẽn quan đến độc tinh gan.
' khi không đo1.
ZDV = zidovudinc, LAM = lunivuđinc, ULN = Giới hợn ưến của mửc binh thường,
ALT ' alcninc cmỉnotnnsfensc, AST = nspamtc aminotnnsfcmsc,
GGT = gnmma-gluumyltnnsfcnse.
Bệnh nhân đồng nhiễm với viếm gnn siêu vi B hoặc C
Các xét nghiệm chức nãng gnn nến được theo đòi ở các bệnh nhân có tiến sử việ
vảlhoặc C.`Ỏ bộ dữ liệu đâi hạn từ một nghiên cứu được báo cáo, 137 bệnh __ ư
với phác đô có cfavirenz (thời gian tri liệu trung binh, 68 tuân) vả 84 bệnh nhân,,đmg gân
phác để đối cht'mg (thời gian trung binh, 56 tuần) lả hưyết thanh dương tính`lthi,khảo
gan siếu vi B (kháng nguyên bề mặt dương tinh) vả/hoặc C (khảng thế viêm g 0 c
77
`gtiiiitsj_ệiivitì
@
u ưi
vởi
iếm
ươnB
16l30
tính). Trong số cảc bệnh nhân đồng nhiễm nảy, tăng AST gấp năm lẩn giới hạn trên cùa mức
binh thường tiến triến ở 13% bệnh nhân trong phác đồ dùng efavirenz và 7% trong nhóm đối
chứng, và tăng ALT gắp nảm lần giới hạn trên của mức binh thường tiến triến ở 20% bệnh nhân
trong phảc dỗ có efavirenz và 7% bệnh nhân trong nhóm đối chứng. Trong số cảc bệnh nhân
đồng nhiễm, 3% số bệnh nhân nảy dược điếu trị với phác đồ có efavirenz vả 2% trong nhóm đối
chứng ngừng tham gia nghiên cứu vì rối loạn trên hệ gan hoặc mật (xem CẢNH BÁO VÀ
THẬN TRỌNG).
Lipids
Tăng mức cơ bân về cholesterol toản phần ở 10-20% đã được quan sảt ở một số người tình
nguyện không nhiễm dùng efavirenz. Ở cảc bệnh nhân được điều trị với cfavirenz + zidovudine
1 lamivudine, tãng mức cơ bản về cholesterol toản phần và HDL- -c khi không đói được quan sảt
lần lượt ở khoảng 20% và 25% Ô cảc bệnh nhân, được điếu trị với efavircnz + indinavir, tặng
mức cơ bản vẽ cholesterol vả HDL-c khi không đói được quan sảt lần lượt ở 40% và 35%. Nồng
độ cholesterol toản phần khi không đói 2240 mg/dL và 2300 mg/dL được quan sải lần lượt ở
34% và 9% bệnh nhân được điếu trị vởi efavircnz + zidovudine + lamivudine; lần lượt 54% và
20% ở bộnh nhân được điếu trị với cfavircnz + indinavir; vả lần lượt 28% vả 4% bệnh nhân được
điều trị với indinavir + zidovudine + lamivudine. Tảc động cùa efavirenz trên triglyceridcs vả
LDL trong nghiên cứu nảy không được mô tả tổng thể vì mâu được lấy từ cảc bệnh nhân không
đói. Ý nghĩa lâm sảng cùa cảc phát hiện nảy không biết (xem CẨNH BÁO VÀ THẬN
TRỌNG).
Kinh nghiệm thử nglư'ệm lâm sảng ở bệnh nhi
Tảo dụng phụ trên lâm sảng được quan sải ở 210% của 57 bệnh nhi tuổi từ 3 đến 16 dùng viên
nang efavirenz, neliinavir, và một hoặc nhiếu NRTIs trong một nghiên cứu (xem SỬ DỤNG Ó
NHÓM ĐÔI TƯỢNG ĐẶC BIỆT) là ban đó (46%), tiêu chảy/phân lòng (39%), sốt (21%), ho
(16%), choáng vảng/chóng mặt/ngất (16%), đaulnhứclkhó chịu (14%), buồn nôn/ói mừa (12%),
vả nhức dầu (1 1%). Tỉ lệ có triệu chứng trên hệ thần kinh là 18% (10/57). Một bệnh nhân có ban
đó cấp độ 3, hai bệnh nhân có ban đó cấp độ 4 và nãm bệnh nhân ngừng điếu trị do ban đó (xem
CẢNH BẢO VÀ THẬN TRỌNG vả PHẢN úNG PHỤ).
Kinh nghiệm sau khi đưa Iliuổc ra thị trường
Các phản ứng phụ sau đây đã đuợc nhận biết sau khi efavirenz được phê duyệt. Vì các phản ứng
nảy được bảo cảo tự phảt từ một nhóm dân số không rõ cỡ mẫu, không phải luôn 1uôn đánh giá
một cảch tin cậy tẩn suất của chứng hoặc thiểt lập một mối liên hệ nhân quả dối với phơi nhiễm
thuôc.
Toản thân: phản ứng dị ứng, suy nhược, tái phân bố/tích iũy mỡ của cơ thể (xem CÃNH BÁO
VÀ THẬN TRỌNG).
Hệ thần kinh tr ung ương vả ngoại bỉên: phối hợp bất thường, mất điếu hòa, rối ioạn phối hợp và
cân bằng tiếu não, chứng co giật, giảm cảm giảc, dị cảm, bệnh thần kinh, rung, chóng mặt.
Nội tiên chứng to vú ờ đản ong
Dạ dảy ruột: tảo bón, hấp thu kém
Tím mạch: nóng bừng, ngất
Ilệ gan vả mật: tăng men gan, suy chức năng gan, viêm gan. Một vải báo cảo sau khi đưa thuốc
ra thị trường về suy chức năng gan, gồm cảc trường hợp ờ những bệnh nhân trước đây không có
bệnh gan hoặc các yếu tố xác định bệnh gan, được mô tả bằng các dợt kịch phát tiến triền ở một
số trường hợp phải ghẻp gan hoặc tử vong.
Chuyến hóa và dinh dưỡng: tăng cholesterol huyết, tăng triglyceride huyết Ji GJA\
C 0 xương: đau khởp, đau cơ, bệnh cơ iy\° ’?Ầ
Tâm thần: gây hấn, kich động, ảo tướng tâm trạng hay dao động, thao cuồng, Jchứngdm ẹiĩthấn
kinh chức năng, chứng hoang tường, chứng loạn thân, tự từ Iẵ/
’/
Hô hấp: khó thở `ự
Da vả phân phụ: ban đó đa dạng, viêm da do dị ứng với ánh sảng, hội chứng Stevens- ohnson
17/30
Cảm giác đặc biệt: thị giảc bắt thường, ù tai. ' ,
Các tảc dụng phụ không mong muôn khảo được báo cảo lá có găng tự từ, ý nghĩ tự từ, đã tự tứ,
nhin mờ.
TẸÔNG BÁO cụo BÁC sĩ CÁC TÁC DỤNG KHÔNG MONG MUÔN GẶP PHẨI KHI
SƯ DỤNG THUOC.
QUÁ LIÊU '
Một số bệnh nhân tinh cờ dùng 600 mg, ngảy 2 lấn đã được bảo cáo tăng cảc triệu chứng trên hệ
thần kinh. Một bệnh nhân bị co cơ không chủ động.
Điếu trị quá liều cfavirenz nên thực hiện cảc biện phảp hỗ trợ toản thân, gồm theo dõi dấu hiện
sinh tồn và quan sát tình trạng lâm sâng cùa bệnh nhân. Dùng than hoạt có thể giúp loại bỏ phần
thuốc không hấp thu. Không có chất giải độc chuyên biệt khi quá liều efavircnz Vì cfavirenz găn
kết cao với protein, thẩm phân dường như không loại bộ đảng kế thuốc ra khói mảu
ĐẶC TÍNH DƯỢC ĐỌNG nọc VÀ DƯỢC LỰC nọc“²
0 Tác động dược lực học
Cơ chế tác dụng
Efavirenz lả một chắt khảng virus. Efavirenz (EFV) là một chẩt ức chế men phiên mã ngược
không phải nucleoside (NNRTI) của HIV- 1. Hoạt tính cùa EFV chủ yếu qua trung gian bằng sự
ức chế không cạnh tranh trên mcn phiên mã ngược (RT) cùa HIV- 1. HIV 2 RT vả DNA
polymerases 01, B, ) và ô tế bảo không bị ức chế bởi EFV
Họạt tính kháng virug ở lễ bảo nuôi cẩy
Nông độ EFV ức chế sự sao chép Cảc chùng hoang dại đã được thích nghi trong phòng thí
nghiệm vả các chùng phân lập trên lâm sảng ở tế bảo nuôi cấy từ 9095% (Ecgoộs) thay đổi từ
1,7 đến 25 nM ở các dòng tế bảo nguyên bảo lympho, các tế bảo đơn nhân máu ngơại biên
(PBMCS), vả cảc tế bảo đơn bảoldại thực bảo. EFV đã chứng minh là có hoạt tính khảng virus
chùng B và cảc chùng phân lập không thuộc chùng B (phân týp A, AE, AG, C, D, F, G, J, N),
nhưng 1ảm giảm hoạt tinh khảng virus đối với cảc virus nhóm 0. EFV đã chứng minh hoạt tinh
kháng virus bổ sung không kòm dộc tinh tế bảo đối với HIV-1 ở tế bảo nuôi cây khi phối hợp với
NNRT is delavirdine (DLV) vả nevirapinc (NVP), NRTIs (abacavir, didanosine, emtricitabine,
lamivudine [LAM], stavudine, tenofovir, zalcitabine, zidovudine [ZDVD, Cảo thuốc ức chế
protease (amprcnavir, indinavir [IDV], Iopinavir, neifinavir, ritonavir, saquinavir), và chất ức chế
hợp nhất enfuvirtidc. EFV đã chứng minh bổ sung hoạt tinh kháng virus đối kháng ở tế bảo nuôi
cẳy vởi atazanavir. EFV không đối kháng với adefovir, được dùng cho đìều trị nhiễm virus gây
viêm gan B, hoặc ribavirin, được sử dụng phối hợp với interferon cho điếu trị nhiễm virus gây
viêm gan C.
Để khăng %
Ở tê bảo nuôi cây `
Trong nuôi cẳy tế bảo, cảc chùng phân lập HIV-l giảm nhạy cảm với EFV (> tăng 380 1ẳn vé giá
trị ECớo) bùng phát nhanh chóng khi có sự hiện điện của thuốc. Đặc điếm kiếu gen cùa cảc virus
nảy được mô tả bới cảc gốc thề amino acid đơn LlOOI hoặc V179D, các gốc thế đôi
LlOOI/VIOSI, và các gốc thế ba LlOOl/Vl79D/YI8IC trong RT.
Căc nghiên cứu lâm sâng
Đã ihu dược cảc chủng phân lập trên lâm sảng giảm tính nhạy cảm trong nuôi cắy tế bảo đối với
EFV. Một hoặc nhiều gôc thế RT tại cảc vị trí amino acid 98,100,101,103,106,108,188,190,
225, vả 227 đã được quan sát ở cảc bệnh nhân thất bại diếu trị với EFV khi phối hợp với IDV,
hoặc với ZDV + LAM. Sự đột biển K103N thường được quan sát nhất. Khảo sải đề kháng dải
hạn (trung bình 52 tuần, thay đối 4- 106 tuần) phân tích 28 chùng phân lập thẫt bại về mặt virus
học và so với mức nên. Sáu mươi mốt phần trăm (17/28) cảc chùng phân lập thất bại nảy giảm
nhạy cảm với EFV trong nuôi cấy tế bảo với sự thay đối tính nhạy cảm với EFV trung bình 88
lẳn (giá trị ECso) từ tham khảo. Gốc thế NNRTI phổ biến nhất phảt triền ớ cảc chùng phân lập
bệnh nhân là KIO3N (54%). Cảc gốc thế NNRTI khác phải triến gồm LIOOI (7%), KlOlE/Q/R
(14%), V1081 (11%), Gl9OS/T/A (7%), P225H (18%), và M2301/L (11%).
Đề kháng chéo
Đế khảng chéo giữa các NNRTIs dã được quan sải Cảo chứng phân lập trên lâm sảng trước đây
dược mô tả là dễ khảng EFV cũng đề khảng kiều hình trong nuôi cây tế bảo đối với DLV vả
NVP so với mức nên. Cảc chủng virus phân lập trên lâm sảng đề kháng với DLV— vả/hoặc NVP
với các gốc thế liên quan đến đề kháng NNRTI (A98G, L1001, KlOlE/P, KlO3N/S, V106A,
Y181X, Y188X, Gl9OX, P22511, F227L, hoặc M230L) cho thấy giảm nhạy cảm với EFV trong
nuôi cấy tế bảo. Hơn 90% cảc chùng phân lập trên lâm sảng đề kháng NRTI được kiếm tra trong
nuôi cấy tế bảo vẫn nhạy cảm với EFV.
o Dược động học
Hấp thu
Nồng độ đỉnh trong huyết tương cùa efavirenz lả 1,6-9,1 ụM đạt được sau 5 giờ sau khi dùng cảc
liều uống duy nhẩt 100 mg đến 1600 mg ở người tình nguyện không bị nhiễm. Tăng c…, và
AUC liên quan đển liều dùng được quan sải đối với các liếu dùng lên đến 1600 mg; sự gia tăng
không theo 11 lệ cho thấy độ hắp thu giảm ở cảc liếu dùng cao hơn.
Ở cảc bệnh nhân nhiễm HIV- ] khi ở tình trạng cân bằng, Cmax trung bình, Cmm trung bình, và
AUC trung bình lả tỉ lệ với liếu dùng sau các liếu hẳng ngảy 200-mg, 400- -mg, và 600- -mg Thời
gian để đạt nồng độ đinh trong huyết tương là khoảng 3- 5 giờ vả nông độ huyết tương ở tình
trạng cân bằng dạt được trong 6- 10 ngảy. Trong 35 bệnh nhân dùng efavirenz 600 mg, ngảy [
lần, C,… ở tinh trạng cân bằng là 12,9 :): 3,7 111% (trung bình 3: độ lệch chuấn), C…… ở tinh trạng
cân bằng là 5,6 x 3,2 ụM, vả AUC là 184 i 73 ụM—h.
Tác động của thức ăn trên sự hẩp thu qua đường uống: Dùng liếu duy nhất viên nén 600-mg
efavirenz với bữa ăn giản chất béo/giảu năng lượng (khoảng 1000 kcal, 500-600 kcal từ chắt
béo) liên quan đến tãng 28% về AUC,, trung bình cùa efavirenz vả tăng 79% về c,… trung binh
cùa cfavirenz 1iên quan đến phơi nhiễm đạt được ở tinh trạng khi dói (xem LIÊU LƯỢNG VÀ
CÁCH DÙNG, Thông tin cho bệnh nhân).
Phân phối Cỹ/
Efavircnz gắn kết cao với protein huyết tương người (khoảng 99,5-99,75%), chủ yếu là albumin.
ớ cảc bệnh nhân nhiễm HIV-l (n=9) dùng cfavircnz 200 đến 600 mg ngảy 1 lần trong it nhất
một thảng, nồng độ trong dịch não tủy thay đổi từ 0,26 đến 1,19% (trung binh 0,69%) nồng độ
tương ứng trong huyết tương. Tỉ lệ nảy là cao khoáng gâp 3 lần với phần efavirenz (tự do) không
gắn với protein trong huyết tương. ớ -
O"o
m
; , N81“ Delhi
Chuyen hoa ~Ỉ². léẵý
Các nghiến cứu đã được báo cảo ở người và cảc nghiên cứu trên in vitro ầẺị-e’ỂĨI thể gan
người đã chứng minh rằng efavirenz được chuyến hóa chủ yếu bời hệ cytochr 450 thảnh
chất chuyến hóa được thùy phân sau đó glucuronide hóa cảc chất chuyển hóa được thủy phân
19/30
nảy. Cảo chất ohuyến hóa nảy thực chất không có hoạt tính khảng 111V 1 Các nghiên oứu in
vítro gợi ý rằng CYP3A4 vả CYP2B6 lả oảo isoenzyme chủ yêu chịu trảch nhiệm chuyển hóa
ofavircnz
Efavirenz đã được chứng minh lả cảm ứng oảo mcn CYP, dẫn đến cảm ứng chuyển hóa chính nó.
Dùng đa liều 200- 400 mg cho một ngảy trong 10 ngảy dẫn đến mức độ tích lũy thẩp hơn (thấp
hơn 22— 42%) và thời gian bản thải giai đoạn ouối ngăn hơn 40- 55 giờ (thới gian bản thải liều duy
nhất 52- 76 giờ).
Đâo thâi
Efavirenz có thời gian bản thải gìai đoạn cuối lả 52- 76 giờ sau khi dùng oảo liều duy nhất và 40-
55 giờ sau khi dùng đa liếu Một nghiến oứu khối lượng/bải tiết được thực hiện trong 1 thảng sử
dụng 400 mg/ngảy với liều dược đánh dấu phỏng xạ lC vảo ngảy 8. Khoảng 14— 34% liều đảnh
dấu phóng xạ được hồi phục trong nước tiếu và 16- 61 % dược hồi phục trong phân. Gần như tất
oả sự bải tiết qua thặn cùa thuốc đánh dấu phóng xạ là dạng ohất ohuyền hóa. Efavirenz oho phần
iớn hoạt tính phóng xạ toản phần oó trong phân.
Các đổi tượng đặc biệt
Giới tỉnh và chủng tộc: Dược động học cùa cfavirenz ở bệnh nhân dường như tương tự nhau giữa
nam giới và nữ giới vả giữa cảc nhóm chùng tộc.
Suy chức năng thận: Dược dộng học oùa efavirenz không dược nghiên cứu ở bệnh nhân suy chức
năng thận; tuy nhiên, dưới 1% efavirenz được bải tiêt ở dạng nguyên vẹn trong nuớc tiêu, vì vậy
tác động cùa suy ohứo năng thận trên sự đảo thải efavirenz lả tôi thiêu.
Suy chức năng gan. Một nghiến cứu dùng đa Iiếu oho thấy không có tác động đáng kể trên dược
động học của cfavircnz 0 bệnh nhân suy chức năng gan nhẹ (Child- -Pugh Nhóm A) so với nhóm
chứng. Không đủ dữ liệu để xảo định rằng suy ohức năng gan từ trung binh đến nặng (Child-
Pugh Nhóm B hoặc C) ảnh hưởng đến dược động học oùa efavircnz.
Các nghiên cửu tương tác thuốc
Efavircnz đă được chứng minh trên in vivo gây cảm ứng men gan, vì vậy lảm tăng chuyển dạng
sinh học oùa r_nột số thuốc được ohuyến hóa bời CYP3A4 vả CYP2B6. Cảo nghiên oứu in vitro
chứng minh răng efavircnz ức ohể cảc isocnzymc CYP 2C9, 2C19, vả 3A4 với giá trị Ki (8,5-17
ụM) trong khoảng nổng độ huyết tương oùa efavirenz được quan sảt Trong các nghiên cứu trên
in vitro, efavirenz không ức chế CYP2EI vả ức ohế CYP2Dó vả CYPIA2 (giá trị Ki 82-160 ụM)
Chỉ ở các nồng độ ở trên nổng độ đạt dược trên lâm sảng. Tảo động ức ohế trên CYP3A4 dược
cho lả tương tự nhau giữa oảo liều 200—mg, 400—mg, và 600— —mg efavìrenz. Dùng đổng thời
efavirenz với oảo thuốc được chuyền hóa chủ yêu bởi isoenzyme 2C9, 2C19, vả 3A oó thể dẫn
đến nồng độ huyết tương thay đổi oùa thuốc dùng đống thời. Cảo thuốc gây oảm ứng hoạt tinh
CYP3A4 được cho lả Iảm tãng dộ thanh thải cfavircnz dẫn đến nống độ huyết tương bị giảm.
Cảo nghiên cứu tương tảo thuốc được tiến hảnh với efavirenz vả oác thuốc khác được dùng đồng
thời hoặc oác thuốc thường được sử dụng để thảm dò tương tác dược động học. Cảo tảo động của
việc sử dụng đổng thời ofavirenz trên Cmax, AUC, và C… được tóm tắt trong Bảng bến dưới (tảo
động cùa efavircnz trên cảc thuốc khảo) và Bảng (tảo động cùa các thuốc khảo trên efavirenz).
Dối với thông tin liến quan đến khuyến cáo trên lâm sảng; xem CHỐNG CHỈ ĐINH vả
TU ỚNG TÁC THUỐC
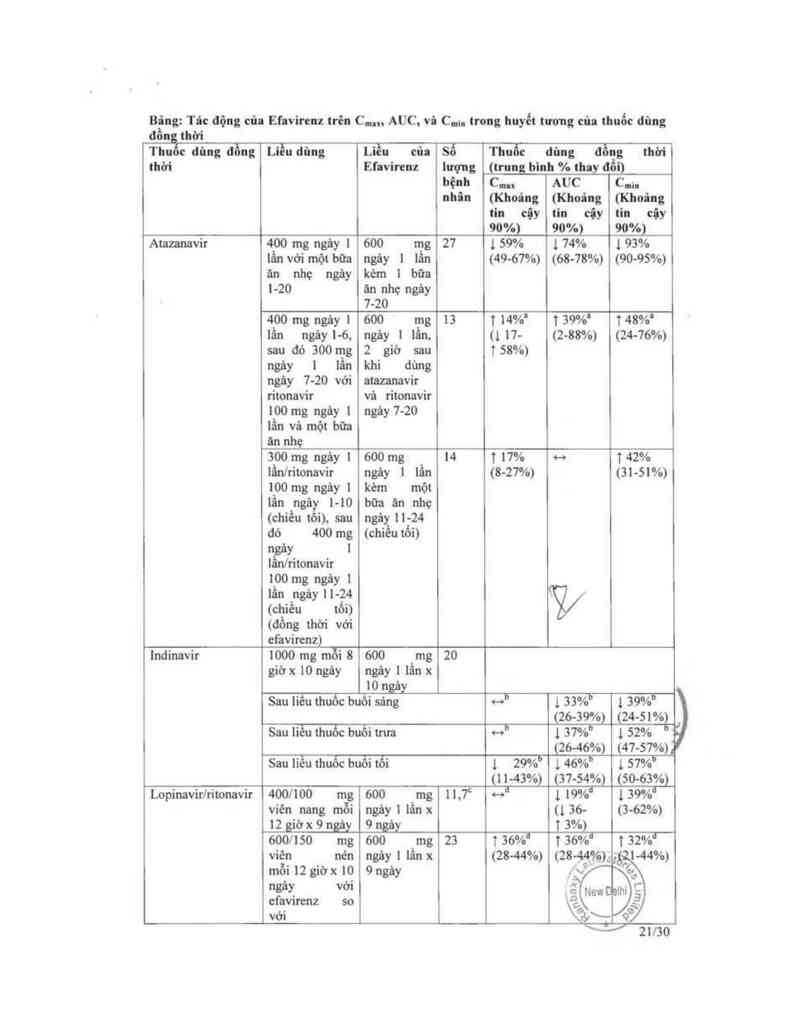
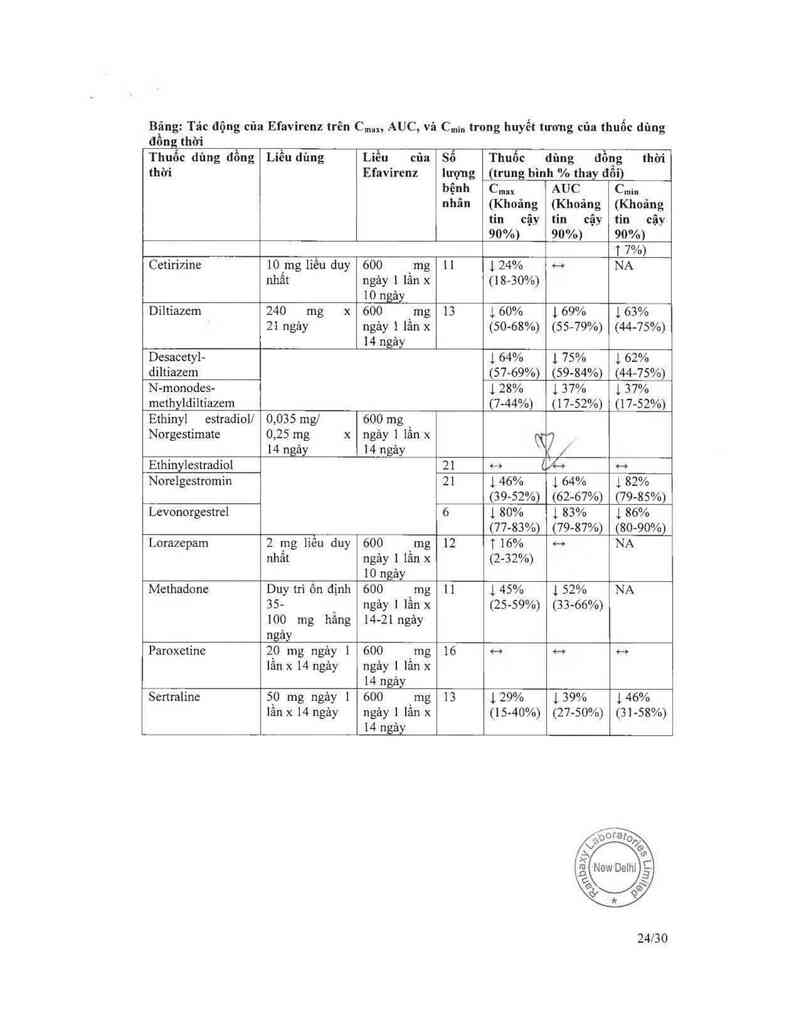
Bing: Tđc động cùa Efavircnz trên C.,m AUC, vù C.h tr0ng huyết twng của thưốc đũng
đồn thời
Thu đùng đỗng Liễu đùng Liền của sá Thuốc dũng đỗllg thời
thời Efnvircnz lượng (trung binh % tth đỗi)
bệnh C.… AUC C.,i.
nhủ (Khoing (Khođng (Khoing
tin cậy tỉn cộy tin cậy
90%) 90%) 90%)
Ataznnavir 400 mg ngây 1 600 mg 27 1 59% 1 74% 193%
lần với một bữa ngiy 1 lẩn (49-67%) (68-78%) (90-95%)
ăn nhẹ ngây kèm 1 bữa
1—20 ãn nhẹ ngảy
7—20
400 mg ngity 1 600 mg 13 114%' 139%’ T48%'
lần ngèy 145, ngảy 1 1ấn, (117— (2—88%) (24-76%)
sau đó 300 mg 2 giờ sau 158%)
ngảy 1 1ần khi dùng
ngủy 7—20 với atazanavir
ritonavir vả ritonavir
100 mg ngáy 1 ngây 7-20
lần vả một bữa
ãnnhẹ
300 mg ngảy 1 600 mg 14 1 17% … T42%
lần/ritonavir ngảy 1 lần (8-27%) (3151%)
100 mg ngảy1 kèm một
lẩn ngảy 1-10 bữa ăn nhẹ
(chiếu tôi), sau ngảy 11—24
đó 400mg (chiềutổi)
ngây |
lẩnlritonavir
100 mg ngảy 1
lần ngảy 11-24 -
(chiếu tối)
(đồng thời với
efavirenz)
lndinavir 1000 mg mỗi 8 600 _mg 20
giờx 10 ngây ngảy 1 lân x
10 ngỀ_y
Saưliều thuộc buổisáng …“ 133%” 139%“
(26-39%) (24—51%)
Sau liều thuốc buôi ưưa c-oĨ 1 37%b 1 52% "
j26—46%) (4757%)
Sau liếu thuốc buỏitỏi ) 29%“ 146%” 157%”
(11-43%) (37-54%) (50-63%)
Lopinavir/ritonavir 400/100 mg 600 mg 11,7c <-o° 1 19%1 139%“
viến nang mỗi ngảy 1 lầnx (136- (3-62%)
12giờx9ngây 91_1gáy ĩ3%)
600l150 mg 600 mg 23 T36%' T36%'l
viên nẻn ngây 1 Iầnx (28—44%) (28-44%)J
mỗi 12 giờx 10 9 ngảy /Ự`
- …x
"W … ; NewCe
efavirenz so ị
kt…
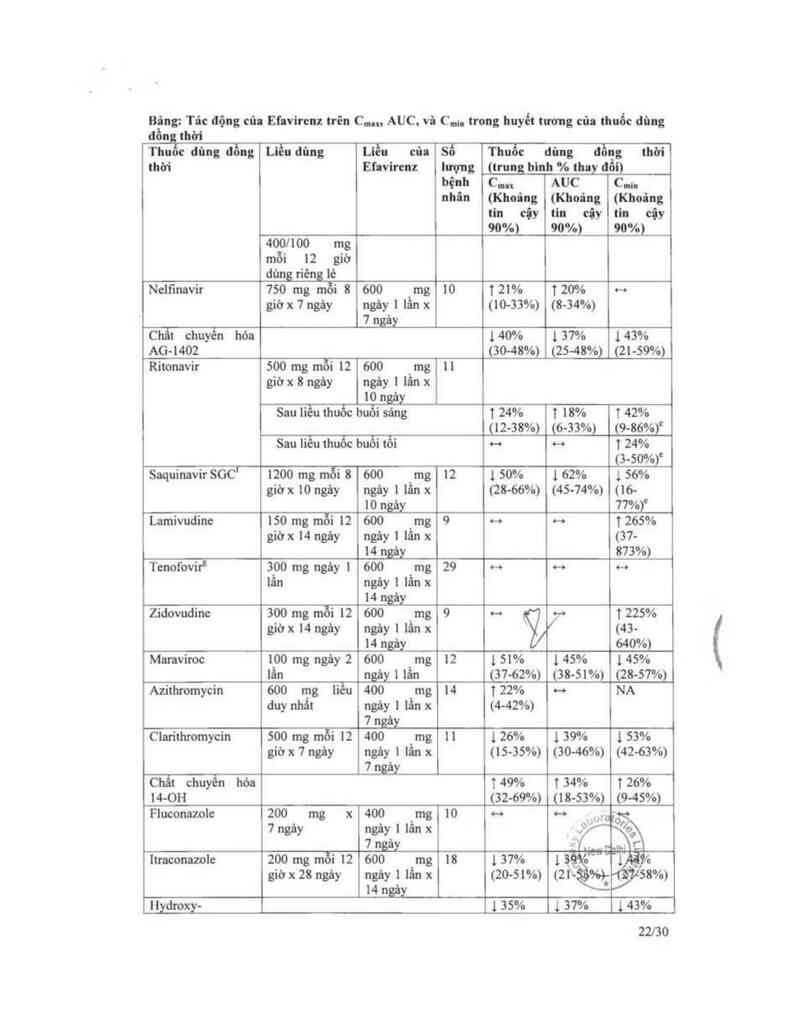
Bâng: Tảc động cũa Efnvircnz trên C,…, AUC, vi C.… trong huyết tương của thuốc đùng
đồn thời
ThưỄc đùng đồng
Liễu đùng Liễn cũa SỈ Thước đímg đồng thời
thời Eanil'cnz lượng (trung binh % thay đổi)
bệllh C.“ AUC Cuin
nhân (Khoing (Khoing (Khoảng
tin ciy tin cậy tin cậy
90%) 90%) 90%)
400/100 mg
mỗi 12 giờ
dùng riêng 1é
Nelfinavir 750 mg mỗi 8 600 mg 10 121% 120% -o
giờ x 7 ngảy ngùy 1 lằn x (10-33%) (8-34%)
7 ngảy
th cituyẻn hóa 140% 137% 143%
AG—1402 (30-48%) (25-48%) (21—59%)
Ritonavir 500 mg mỗi 12 600 mg 11
giờx 8 ngảy ngây 1 lần x
10 ngảy
Sau liều thuốc buổi sáng 1 24% 1 18% 1 42%
(12-38%) (6-33%) (9—8690)e
Sau liếu thuốc buồi tối … o—› 1 24%
(3—50%)°
Saquinavir SGCr 1200 mg mỗi 8 600 mg 12 1 50% 1 62% 1 56%
giờx 10 ngây ngảy 1 1ẳn 74 (28-66%) (45-74%) (16-
10 ngảy 77%)°
Lamỉvudine 150 mg mỗi 12 600 mg 9 o—› … 1265%
giờ x 14 ngây ngảy 1 1ẩn x (37-
14 ngảy 873%)
Tenofovir' 300 mg ngùy 1 600 mg 29 -o ~ ~
lần ngảy 1 lần x
14 ngậy
Zidovuđinc 300 mg mỗi 12 600 mg 9 … j» 1 225%
giờ x 14 ngây ngảy 1 lẩn x % (43—
14 ngảy 640%)
Maraviroc 100 mg ngảy 2 600 mg 12 1 51% 1 45% 1 45%
lằn ngáy 1 lẩn (37-62%) (38-51%) (28-57%)
Azithromycin 600 mg liếc 400 mg 14 122% ~ NA
đuy nhẩt ngảy 1 lẩn x (4-42%)
7 ngây
Clarithromycin 500 mg mỗi 12 400 mg 11 126% 1 39% 1 53%
giờ x 7 ngây ngảy 1 lẩn it (15-35%) (30—46%) (42-63%)
7 nstìy
Chât chuyến hỏa 149% 134% 126%
14-0H (32-69%) (18-53%) (9-45%)
Fluconazolc 200 mg x 400 mg 10 ~
7 ngảy ngảy 1 lần x
7 fflẻv
ltmconazole 200 mg mỗi 12 600 mg 18 137%
giờ x 28 ngảy ngảy 1 lẩn x (20—51%)
14 ngáy
Ilydroxy- 1 35%
Bâng: Tảc động cũa Efnvircnz trên C..., AUC, vù C.,g. trong hưyết tung cũa thuốc đùng
đồn thờ1
ThIỄC đùng đỗng
ời
Liễu đủng Liều cũa SỈ Thuốc đùng đồng thời
tii Efnvircnz lượng , trun bình % thay đồi)
hệnh CInu AUC C...
nhân (Khoâng (Khoảng (Khoâng
tin cặv tin cậy tiu civ
90%) 90%) 90%)
iưaconazole (12-52%) (14-55%) (18-60%)
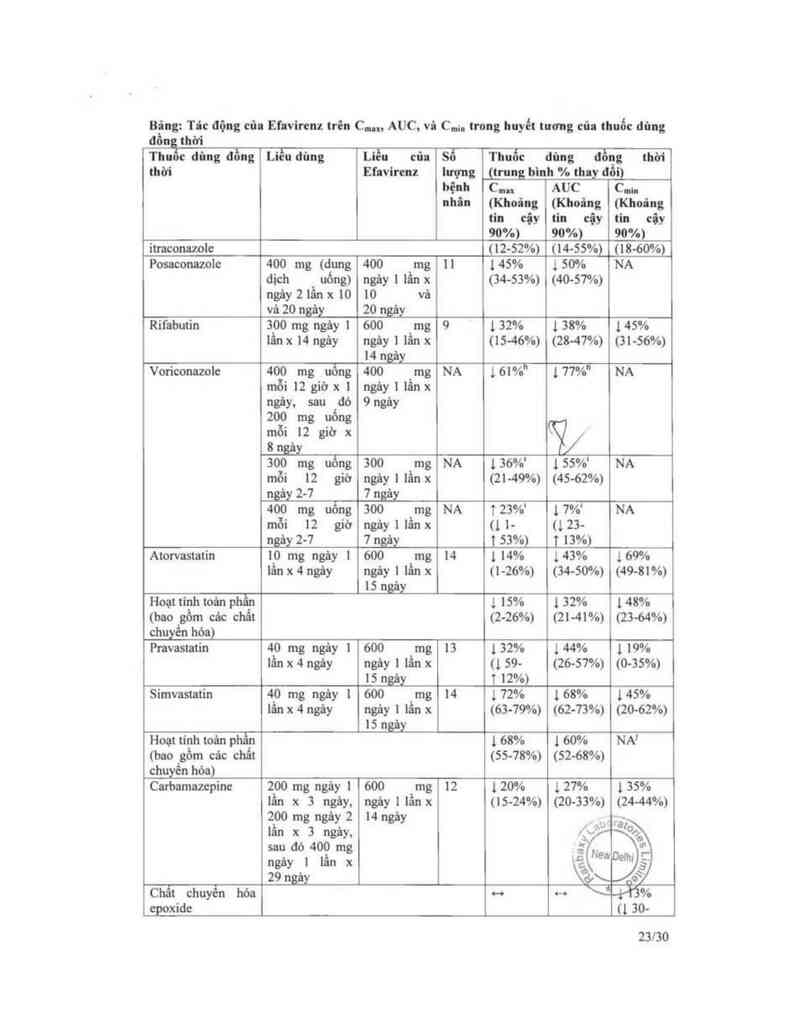
Posaconazolc 400 mg (dưng 400 mg 11 145% 150% NA
đich uống) ngity ] lẩn x (34-53%) (4057%)
ngảy 2 lằn x 10 10 vi
vả 20 ngáy 20 ngây
Rifabutin 300 mg ngảy 1 600 mg 9 1 32% 1 38% 145%
lầnx 14 ngảy ngảy 1 lấn x (15-46%) (28-47%) (31—56%)
14 ngảy
Voriconazolc 400 mg uổng 400 mg NA 161%" 177%“ NA
mỗi 12 giờx 1 ngảy 1 1ẩnx
ngảy. sau đó 9 ngảy
20ẳ'1 mg uống
m i 12 giờ x ~
8 nsây fỸ/
300 mg uống 300 mg NA 136%' 155%' NA
mỗi 12 giờ ngảy ! lẳn x (21-49%) (45-62%)
.nzẻy ²—7 7 nsảy
400 mg uỏng 300 mg NA 123%' 17%I NA
mỗi 12 giờ ngây 1 lần x (11- (123-
ngảy 2—7 Dgảy 1 53%) 1 13%)
Atorvastatin 10 mg ngảy 1 600 mg 14 1 14% 143% 169%
lẳn x 4 ngáy ngây 1 lần x (1-26%) (34-50%) (49-81%)
15 ngi_iy
Hoạt tinh toân phân 1 15% 1 32% 1 48%
(bao gồm các chất (2-26%) (2141%) (23-64%)
chuyền hớa)
Pravastatin 40 mg ngây ] 600 _mg 13 132% 144% 1 19%
lẫn x 4 ngảy ngảy 1 lân x (1 59- (26-57%) (0-35%)
15 ngảy 1 12%)
Simvastntin 40 mg ngảy 1 600 mg 14 172% 1 68% 145%
lần x 4 ngảy ngảy 1 lẩn x (63—79%) (62—73%) (20-62%)
15 ngảy
Hoạt tính toán phân 1 68% 1 60% NAJ
(bao gồm các chẳt (55-78%) (52-68%)
chuyển hớn)
Carbamachinc 200 mg ngảy 1 600 mg 12 1 20% 1 27% 1 35%
lần x 3 ngây, ngáy 1 lẩn x (15-24%1 (20-33%) (2444%)
200 mg ngây 2 14 ngảy
lân x 3 ngảy,
sau đó 400 mg
ngáy ] lấn x
29 ngịiy
Chất chuyến hớa ~
epoxiđe
Bảng: Tác động của Efavircnz trên C…… AUC, và C…… trong huyết tương của thuốc dùng
đồng thời
Thuốc dùng dồng Liều dùng Liều của sớ Thuốc dùng đồng thời
thời Efavirenz lượng (trung bình % thay đổi)
bệnh c.… ' AUC cm,,
nhân (Khoảng (Khoảng (Khoảng
tin cậy tin cậy tin cậy
90%) 90%) 90%)
1 7%)
Cetirizinc 10 mg Iiếu duy 600 mg 11 1 24% H NA
nhất ngảy 1 lần x (18—30%)
10 ngảy
Diltiazem 240 mg x 600 mg 13 1 60% 1 69% 1 63%
21 ngảy ngảy 1 lần x (50—68%) (55—79%) (44-75%)
14 ngảy
Desacctyl— 1 64% 1 75% 1 62%
diltiazem (57—69%) (59-84%) (44—75%)
N—monodes- 1 28% 1 37% 1 37%
methyldiltiazcm (7—44%) (17-52%) (17-52%)
Ethinyl estradiol/ 0,035 mgl 600 mg
Norgestimate 0,25 mg x ngảy ] lần x N7
14 ngảy 14 ngảy ` , /`
Ethinylestradiol 2] 4-› (_X-v …
Norelgestromin 21 1 46% 1 64% 1 82%
(39-52%) (62-67%) (79-85%) _
Levonorgestrel 6 1 80% 1 83% 1 86% )
(77-83%) (79-87%) (80-90%) ị
Lorazepam 2 mg liều duy 600 mg 12 1 16% … NA *
nhất ngảy 1 lần x (2-32%)
10 ngảy
Methadone Duy trì Ổn định 600 mg 11 1 45% 1 52% NA
35- ngảy 1 lần x (2559%) (33-66%)
100 mg hẳng 14-21 ngảy
ngảy
Paroxetine 20 mg ngảy ] 600 mg 16 4-› 4—~ <—›
lấn x 14 ngảy ngảy l 1ần x
14 ngảy
Sertraline 50 mg ngảy 1 600 mg 13 129% 139% 146%
lẳn x 14 ngảy ngây 1 lần x (15-40%) (27-50%) (31-58%)
lịngảy
Bãng: Tủc động cũa Efnvircnz trên Cu,, AUC, vả C… trong hưyết tương của thuốc dùng
đ n thờ1
Ti…Ễe đủng đồng Liếu đùng t.ièu của ỉỗ Thuốc đủng đồng thời
thời Efnvircnz lượng (trung blnh % thay đồi)
bệnh C.u AUC C….
nhin (Khoâng (Khoing (Khoâng
tin cộy tin cậy tin cộy
90%) 90%) 90%)
1 tăng 1 giảm H không thay đới hoặc tãng trưng binh hoặc giảm trung binh <10%.
' So với atazanavir 400 mg ngáy 1 lần, đơn độc
Liều dùng so sánh cùa inđinavir lẻ 800 mg mỗi 8 giờ 14 10 ngây.
° Thiết kế nhóm song song; n cho efavirenz + lopinavir/ritonavir, n cho lopinavirlritonavir riêng
lé.
“ Cảo giá trị cho lopinavir; dược động học của ritonavir trong nghiến cứu nảy không bị ảnh
hướng bới sử dụng đong thời efavircnz.
° rKhoáng tin cộy 95%
Viến nnng Gelatin mếm
' Tcnofovir disoproxil fưmnratc.
Khoảng tin cậy 90% khỏng có.
' Liên quan đến khi dùng ổn đinh voriconazolc (400 mg trong 1 ngảy, sau đó 200 mg, uống, mỗi
12 giờ trong 2 ngây).
’ Không có vi thiếu dữ liệu
NA= khõng có
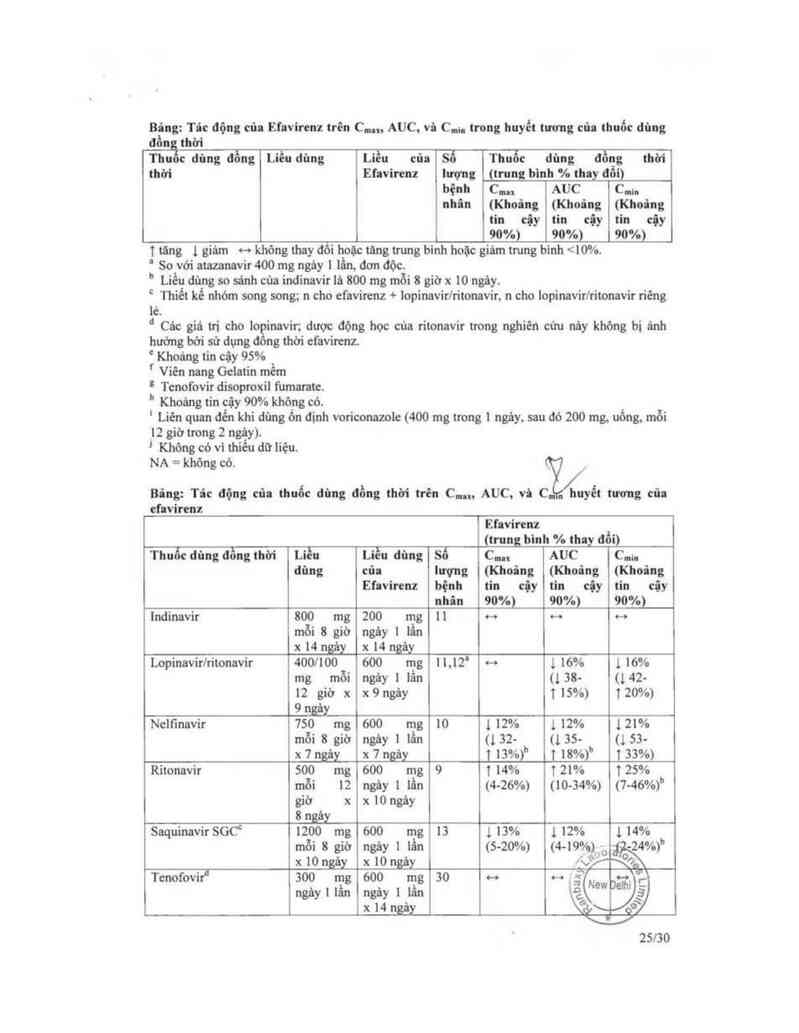
Bing: Tít: động của thuốc đủng đồng thời trên C..., AUC, vi CỆ41yết tương cũa
efavỉrcnz
Efnvircnz
(trung bình % tth đổi)
Thuốc đùng đồg thời Liều Lièu đùng sỏ c.,., AUC c,.i.
đũng cũa lượng (Khoing (Khoing (Khoing
Efnvircnz hộnh tin cộy tin cộy tin cộy
nhin 90%) 90%) 90%)
Inđinavir 800 mg 200 mg 11 ~ ~ …
mỗi 8 giờ ngây 1 lần
x 14 ngảy_ x 14 ng`y
Lopinavirlritonavir 400/100 600 mg 11,12I -o 1 16% 1 16%
mg mỗi ngảy 1 lằn (138- (142—
12 giờ x x9ngảy 1 15%) 120%)
9 ngầy
Nclfmnvir 750 mg 600 mg 10 1 12% 1 12% 121%
mỗi 8 giờ ngity 1 lần (132- (135- (153—
x 7 ngáỵ x 7 ngảy ( 13%)b 1 18%)" 1 33%)
Ritonavir 500 mg 600 mg 9 1 14% 121% 125%
mỗi 12 ngảy 1 iần (4—26%) (10-34%) (7415%)"
giờ x x10 ngảy
8fflây
Saquinavir SGCc 1200 mg 600 mg 13 1 13% 1 12% 1 14%
mỗi 8 giờ ngảy 1 1ần (5-20%) (4 19%),u -24%)
d x 10 ngảy ›: 10 ngảy fảfủ_
Tcnofovir 300 mg 600 mg 30 ~ … o-v
ngảy 1 lần ngảy 1 1ần ỄỄew Delh'ĩ ẵ
x 14 ngảy " g°`
25/30
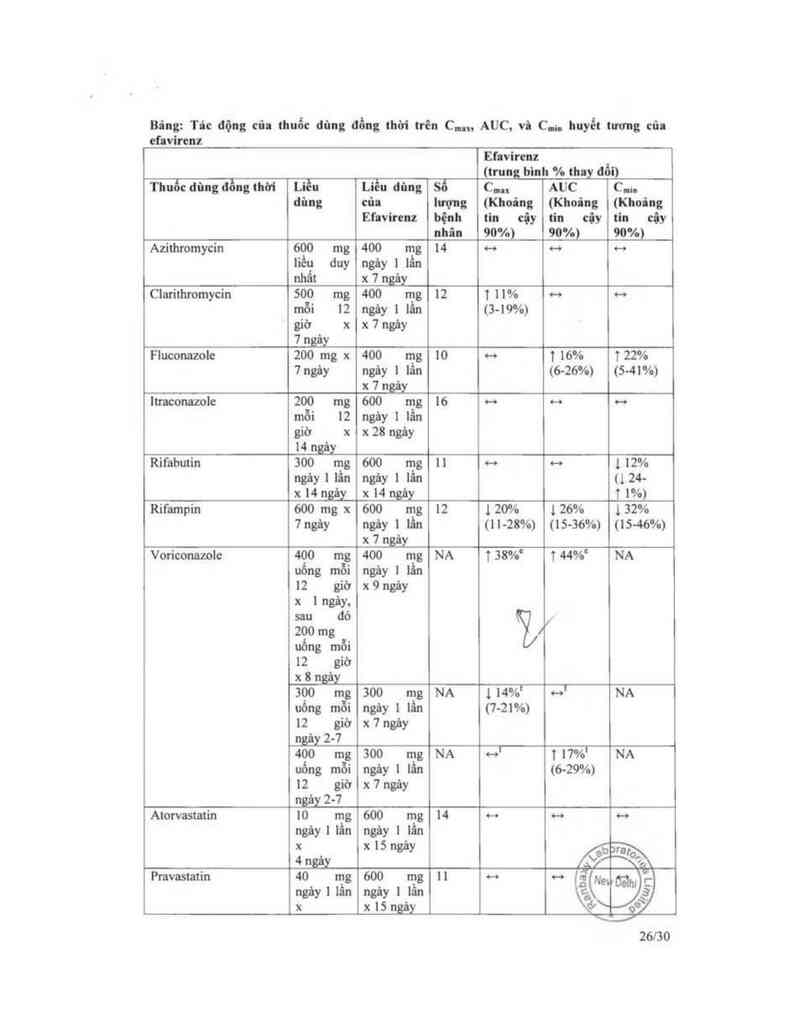
Bâng: Tâc động cũa thuốc đùng đồng thời trên C..., AUC, vì C... huyết tương cũa
efavircnz
Efnvircnz
(trung blnh % thay đỗi)
Thuốc đũng tiồng thời Liền Liễu đùng s8 c.... AUC c...
đùng cũ: lượng (Khoing (Khoing (Khoảng
Efnvirenz bệnh tin cậy tin ciy tin cây
nhân 90%) 90%) 90%)
Azithromycin 600 mg 400 mg 14 H H H
liếu duy ngây 1 lẩn
nhất x7ngây
Clan'thromycin 500 mg 400 mg 12 1 11% H H
mỗi 12 ngây 1 lần (349%)
giờ x x 7ngảy
7ngảy
Fluconazole 200 mg x 400 mg 10 H 1 16% 122%
7ngảy ngảy 1 lẩn (6-26%) (5-41%1
x 7 ngây
[ưaconnzo1c 200 mg 600 mg 16 H H H
mỗi 12 ngiy 1 1811
giờ x x28 ngảy
14 ngảy
Rifabutin 300 mg 600 mg 11 H H 112%
ngảy 1 lần ngảy 1 1ấn (124—
x 14Ẹgảy x 14 ngảy 1%)
Rifampin 600 mg x 600 mg 12 120% 126% 132%
7ngảy ngảy 1 lẩn (11-28%) (15-36%) (15-46%)
74 7 ngậy
Voriconazolc 400 mg 400 mg NA 138%e 144%e NA
uổng mỗi ngảy 1 lần
12 giờ x9ngảy
x lngây,
sau đó /
200 mg |
uống mỗi
12 giờ
74 8 ngây
300 mg 300 mg NA 114%' HT NA
uống mỗi ngáy 1 lẩn (7-21%)
12 giờ x7ngảy
_naâyz-v
400 mg 300 mg NA H' 1 17%l NA
uống mỗi ngảy 1 lẩn (6-29%)
12 giờ x7ngảy
ngùy 2—7
Atorvastatin 10 mg 600 mg 14 H H H
ngây 1 lần ngây 1 lẳn
x x 15 ngây /6fbị
4nẸày A"
Pravastatin 40 mg 600 mg 11 H H ổ
ngảy 1 11… ngây 1 lần lằiNe`
x x 15 ngảy ởN
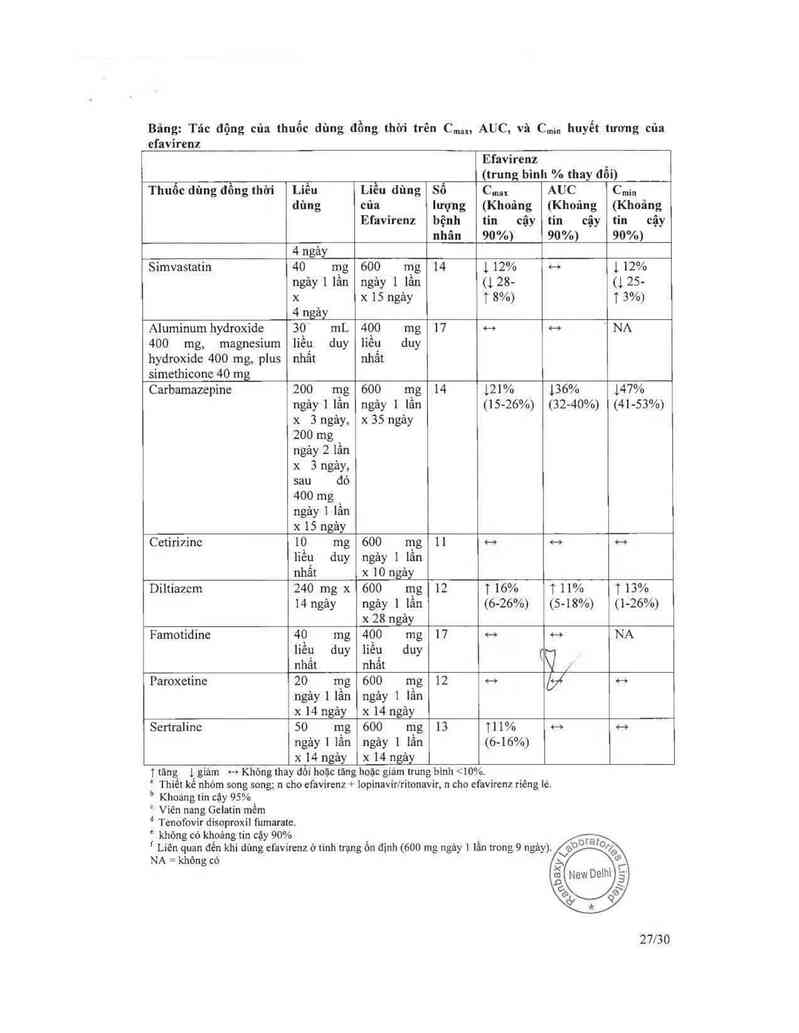
Bãng: Tác động của thuốc dùng đồng thời trên C…… AUC, và C…;,, huyết tương của
cfavirenz
Efavirenz
(trung bình % thay đổi)
Thuốc dùng đồng thời Liễu Liều dùng số cm,, AUC C……
dùng của lượng (Khoảng (Khoảng (Khoảng
Efavirenz bệnh tin cậy tin cặy tin cậy
nhân 90%) 90%) 90%)
4 ngảy
Simvastatin 40 mg 600 mg 14 1 12% H 1 12%
ngảy 1 lần ngảy 1 lần (128- (125-
x x 15 ngảy 1 8%) 1 3%)
4 ngảy
Aluminum hydroxide 30 mL 400 mg 17 H H ` NA
400 mg, magnesium liều duy liều duy
hydroxide 400 mg, plus nhất nhẩt
simethiconc 40 mg
Carbamazepine 200 mg 600 mg 14 121% 136% 147%
ngảy 1 lẩn ngây 1 lần (15-26%) (32-40%) (41-53%)
x 3 ngây, x 35 ngảy
200 mg
ngảy 2 lần
x 3 ngảy,
sau đó
400 mg
ngảy 1 lần
x 15 ngảy
Cetirizỉnc 10 mg 600 mg 11 H H H
liểu duy ngây ] lẩn
nhắt x 10 ngảy
Diltiazcm 240 mg x 600 mg 12 1 16% 1 11% 1 13%
14 ngảy ngảy 1 1ằn (6-26%) (5-18%) (1-26%)
x 28 ngảy ,
Famotidine 40 mg 400 mg 17 H H 1NA
liếu duy liếu duy (
nhất nhất Ụ «
Paroxetine 20 mg 600 mg 12 H bố H
ngảy 1 lần ngảy 1 lần
x 14 ngảy x 14 ngảy
Sertralinc 50 mg 600 mg 13 111% H H
ngảy 1 lẩn ngảy 1 lần (6-16%)
x 14 ngảy x 14 ngảy
1 tăng 1 giảm H Khỏng thay dối hoặc tăng hoac giám trung bình <10%.
' Thiết kế nhỏ… song song; n cho cfavirenz + lopinavirlritonavir, n cho efavirenz riêng le’.
b Khoáng tin cậy 95%
° Viên nang Gelatin mếm
" Tenofovir disoproxil fumarate.
' không có khoảng tin cặy 90%
{ Liên quan dển khi dùng et`avirenz ở tình trạng ổn định (600 mg ngảy 1 lần trong 9 ngảy).
NA = không có
27/30
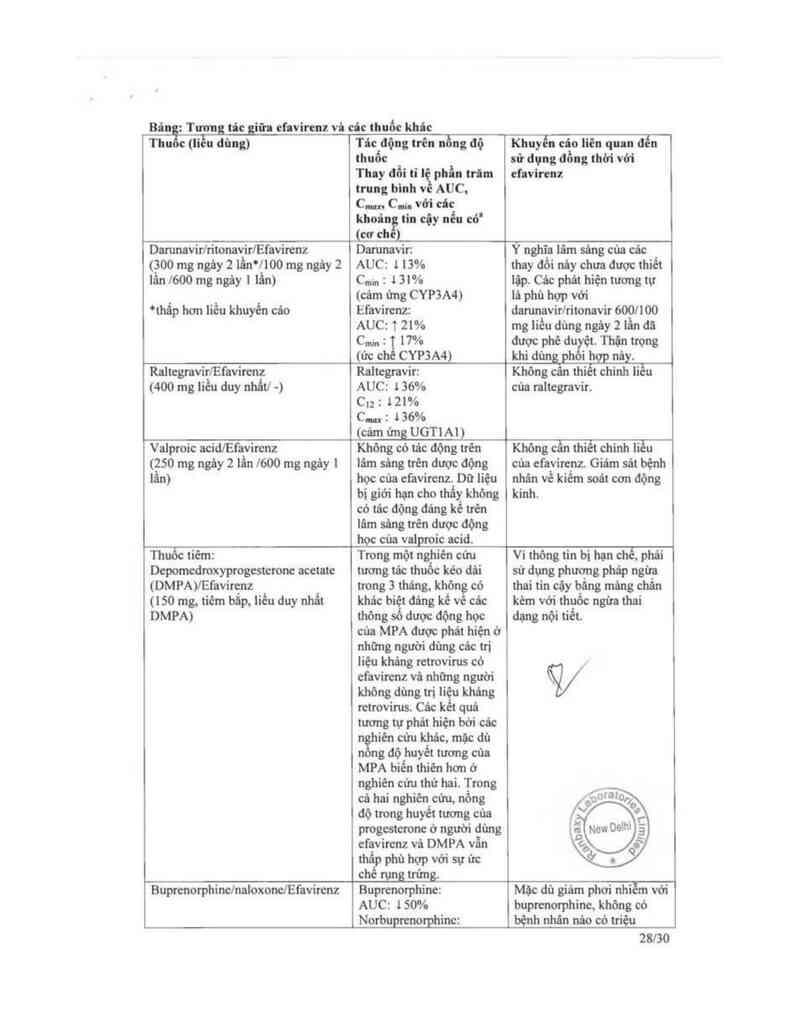
Bân : Tươn tic iữn cl'nvircnz vi cđc thuốc khâc
Thuẵc (liẵ đùng) Tâc động trên nồng độ
không dùng trị liệu kháng
rctrovirus. Cảo kểt quả
tương tự phát hiện bới các
nghiến cứu khác. mặc dù
nỏng độ huyết tương của
MPA biển thiếu hơn 6
nghiên cứu thứ hai. Trong
cả hai nghiên cửu, nổng
độ trong huyết tương của
progcstcronc ờ người dùng
efavircnz vả DMPA vẫn
thế)) phù hợp với sư ửc
che rụngtn'mg.
Khuyến cđo liên quan đến
thuốc sử đụng đồng thời với
Tiny đối tỉ lệ phia trint cfnvircnz
trung binh về AUC,
C… C… vởi cđc
khoân tin cộy nếu có'
(cơ ch )
DarunavirlritonavirlEĩavircnz Damnavir: Y nghia iâm sâng cùa cáo
(300 mg ngiiy 2 1ản~7100 mg ngảy 2 AUC: 1 13% thay đổi nây chưa được thiết
lẩn l600 mg ngiy 1 lần) c.….. : 1 31% lập. Các phát hiện tương tự
(cảm ứng CYP3A4) 11) phủ hợp với
*thẫp hơn iiếu khuyến cáo Efavircnz: đarunavirlritonavir 600/100
AUC: 1 21% mg 1iều dùng ngảy 2 lần đã
C… : 1 17% được phê du ệt. Thộn trọng
(ửc chế CYP3A4) khi di… phoi hợp nảy.
RnltcgravirlEfavircnz Raltegrnvir: Không thiết chinh liếu
(400 mg liều duy nhất! -) AUC: 1 36% của raltegravir.
C); 2 12l%
C…: 136%
(cámỆg UGTI A1)
Valproic aciđfEfavirenz Khỏng cỏ tảo động ưên Không cần thiết chinh iiếu
(250 mg ngảy 2 iần l600 mg ngảy 1 1âm sâng ưên dược động của cfavircnz. Giám sát bệnh
11…) học của et'avircnz Dữ liệu nhân về kiểm soát cợn động
bị gỉới hạn cho thấy không kinh.
có tác động đáng kể trên
lâm sâng ưên được động
học cùa valproic acid.
ThuỀc tiếm: Trong một nghiến cửu Vì thông tin bị hạn chế, phải
Depomcdmxyprogcsteronc acetate tương tác thuốc kẻo đải sư dụng phương pháp ngừa
(DMPAVEi'avircnz trong 3 thảng, khôn có thai tin cộy bảng mãng chắn
(150 mg, tiêm bắp, liếu dưy nhẳt khác biết đâng kế vẵ các kèm với thuốc ngừa thai
DMPA) thỏng số dược động học dạng nội tiết.
của MPA được phát hiện ở
những người dùng các trị
iiệu kháng reưovints cỏ
ct`avirenz vả những người
BuprenorphinelnaloxonclEfavircnz
Buprcnorphine:
AUC: 1 50%
Norbuprcnorphinc:
Mặc dù giám phơi nhiễm với
buprcnorphinc, không có
bệnh nhân nảo có triệu
28130
Bảng: Tương tác giữa efavirenz vit các thuốc khảo
Thuốc (liều dùng) Tảo động trên nồng độ Khuyến cáo liên quan dển
thuốc sử dụng đồng thời với
Thay đổi tỉ lệ phần trăm efavirenz
trung bình về AUC,
Cmaxy Cmin Với CáÊ
khoảng tin cậy nêu cóil
_ _ __ (cơ chế)__ ,
` AUC: 1 71% chứng cại thuộc. Có thế
Efavirenz: không cân thiêt chinh liêu
Không có tương tảo dược oùa buprenorphino hoặc`
động học đảng kê trên lâm efavircnz khi sử dụng dông
sảng thời.
“ Cảo khoảng tin cậy 90% trừ khi có lưu ý khác.
” Các khoảng tin cặy 95%.
ĐỌC TÍNH KHÔNG THUỘC TRÊN LÂM SÀNG '
o Khả nãng gây ung thư, Đột biến gen, Giảm khả năng thụ tinh
Cảo nghiến cứu về khả nãng gây ung thư dải hạn ở chuột nhắt và chuột cống được tiến hảnh với
efavỉrcnz. Chuột nhắt được dùng với liều 0, 25, 75, 150, hoặc 300 mg/kglngảy trong 2 năm. Tỉ lệ
mắc u vả caroinoma tế bảo gan và u tủi phối/phể quản tăng ở trên mức nên ở con cái. Không tăng
tỉ 1ệ mắc khối u 01 trên mức nến ở con đực Trong cảc nghiên oứu mả chuột cống được dùng
efavirenz với liều 0, 25, 50, hoặc 100 mg/kglngảy trong 2 năm, không tăng tỉ lệ mắc khối 11 ở
trên mức nền. Phơi nhiễm toản thân (dựa vảo AUCs) ở chuột nhắt lả khoảng 1,7 lần ờ người
dùng liều 600-mg/ngảy. Phơi nhìễm ở chuột cống thấp hơn ở người. Cơ chế oủa khả năng gây
ung thư là không được biết. Tuy nhiên, trong các thử nghiệm độc tính trên gen, efavirenz không
cho bằng chứng cùa đột biến gon hoặc hoạt tính đứt gãy nhiễm sắc thể trong bộ nghiên cứu in
vitro và in vivo. C ao thử nghiệm nảy gồm thử nghiệm đột biến vi khuẩn ờ S. typhimurium và E
coli, thử nghiệm đột biến ờ động vật có vú ở tế bảo buồng trứng chuột hamster Trung Quốc, thử
nghiệm gây đột biến nhiễm săo thế ở tế bảo bạch huyết máu ngoại vi ở người hoặc ở tế bảo
buồng trứng chuột hamstcr Trung Quốc, và thứ nghiệm vi nhân tùy xương chuột nhắt trên in
vỉvo. Thiếu hoạt tính gây độc gen cùa efavirenz, không biết tính tương quan với ung thư ơ người
ở chuột nhắt được điếu trị với efavirenz.
Efavirenz không lảm giảm sự động dục hoặc thụ tinh oủa chuột cống dực mgặo cải, và không ảnh
hưởng tới tinh trùng ở ohuột công đực được điếu trị. Khả nãng sinh sản ếtia động vật oon được
sinh ra từ con vật mẹ dùng efavirenz không bị ánh hướng. Vì lý do sự thanh thải nhanh chóng
oùa efavirenz ở chuột cống, sự phơi nhiễm thuốc toản thân trong oảo nghiên cứu nảy là tương
đương hoặc thấp hơn sự phơi nhiễm thuốc toản thân ở người dùng liếu điếu trị cùa efavirenz.
' Cảo nghiên cứu khảo
Chứng co giật ngắn được quan sảt ớ 6 trong số 20 con khi dùng efavirenz ở oảo liều oho giá trị
AUC cao hơn 4 dến 13 lần AUC ở người dùng liểu khuyến cảo [xem CẢNH BÁO VÀ THẬN
TRỌNG]
BẢO QUẢN _
Bảo quản trong bao bì_gôo ở nhiệt độ không quá 30°C.
GIỮ THUỐC XA TAM TAY TRE EM.
29/30
CUNG CẤP , _
Chai HDPE với nãp được siêt kín. Hộp 1 chai 30 viên nén bao phim.
HẠN DÙN(1: 36 tháng kể từ ngậy sản xuất. _ _
KHONG DUNG THUỐC QUA HẠN DUNG GHI TREN NHAN.
THAM KHẢO
1.
Prescribing Information of SUSTIVA® (efavircnz) capsules and tablets, Bristol-Myers
Squibb Company USA. November 2010 accesscd online f rom
httn:llwww.accessdatafda.govldrugsatfđa docs/labeUZO10l02136050241b1pdf on February
2, 2011
Summary of Product Characterỉstics of Sustiva 600 mg film coatcd tablets, Bristol-Mycrs
Squibb Pharmaceuticals Ltd. November 201 0 accessed online from
httpz/lwwwmedicincs.org.uk/EMClmedicinel1 l284/SPCISustiva+600+m12+Fi1m—
Coated+Tabletsl on February 2, 2011
SUSTIVẨỉ lả thmmg ln'ệu cua Bri'stol-Myers Squibb, không phát thương hiệu cua Ranbaxy. Người mo !huơng híẽu nảy khõng
phái lá có đõng vò khỏng đại diện cho Ranbaxy hoặc các sản phân: cua Ranbaxy.
Thông tỉn được biên soạn vảo tháng 2/ 2011.
SÀN xuẨr TẠI ÁN ĐỘ
RANBAXY LABORATORIES LIMITED
PAONTA SAHIB, DISTRICT SIRMOUR,
IIIMACHAL PRADESH — 173 025.
PHÓ cục TRUỞNG
Ấ ft … Cì°
e/iỷõíỷửál lễm xUẨGN &
30/30
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng