











BỘ Y TẾ '236/ Ềẳ,
› , ..
i
ửPGMASCOLIPICFNOPUÀNT CỤC Ql \N Lì .`_l_._DLƠC 423150101/Ph01 MENHIR
AẢS AROMASIN 25MG 30CPR VN ĐA PHÊ… DUYỆ Ề231501 … 27.01.2015 006
ẨS'Ì'UCCIO » = . … .. … , ' tna n Helvetica 7
s"TA"sfozm (87,00 x 54.00 x 30.00)
.ev-oụ; ỈẺ'Ểv; rưe ' c; …; Ềnn*J c.…a ỉ,JimS fnlu;E ;..th NO VARMSHAREASI
2009M-CX … NERO PANT.S41 PANT. 241 PANT.Z727 PANT.32SS FiiẵiiằoLoA MEỄẺỂ ;ặRN'GỈ'OTỆAM “CN'CHE
anmllulni ——
Aggiornamenti Documel'lt0l ':nM1nr 1 ;… n…c:w 2 =a an.;nm 3 n muom 4 In
Document Updatings
copvmsuwwzowrm Pfỉzer Italia S.r.l. DO xo; ;AMpm - anti… M'TIR mm…mwmm;
_____ \
Prescription only medicine
KEEP OUT OF REACH OF CHILDREN
READ THE PACKAGE INSERT
CAREFULLY BEFORE USE
Indicatìons. contraindications. dosaga.
administration and other information:
Please refer to the package insert.
O
XXXXXXX
DDIMMIYY
DD/MMÍYY
Store below 30°C. Protect from moisture
_ g_ . ;;uuul;unuunu : , , >Ầi
SĐK: XX-XXXX—XX
PRINTED/STAMPA:
Batch no./Sõ lò SX:
Mtg date/NSX
Exp date/HDz
ả Sản xuất bời :
g Pfìzer Italia S.R.L.
g Locallta Marino del Tronto,l
-; 63100 Ascoli Piceno (AP). Y ;
DNNK: xxxxx /i
._z
@ Thuỏc bán theo don
ARÒMASINỔ
25mg EXEMESTANE
Box of 2 blisters x 15 sugar coated
tablets
Hộp 2 ví x 15 viên nén bao đường
eÉ XA _TÁM TAY TRẺ EM_
ĐỌC ; Jul 20!5
Tý iệ ngưng thuốc do cảc tảo đụng không mong muốn là 2, 8% trên tông số bệnh nhân ung
thư vú tiên triến Cảo tảc dụng không mong muôn thường gặp nhắt là nóng bùng (14%) và
buồn nôn (12%)
[lầu hết cảc tảc dụng không mong muốn iả do tác dụng thông lhường vẻ mặt dược iý cùa
việc giám ocstrogen (ví đụ: nóng bừng).
Cảo báo cáo về tảc dụng khỏng mong muốn tù nghiên cúu lâm sảng vả thục tế sau khi luụ
hảnh thuốc đuợc lỉệt kê dưới đây, phân loại theo hệ thống cơ quan vả theo tần suất. Tần suất
đuợc quy ước như sau: Rất thuòng gặp (>1/10), Thuờng gặp _(>1in0 đến <1/10), _Không
thường gặp (>1/1 0.00 đến <11100), Hiếm gặp (_21/10000 đến <1/1.000); Rẩ; hiếm gặp
(<1 ; '10.000); Chưa biết (không thể ước tính từ dữ liệu có sẫn).
Rối loạn máu và hệ bạch huyết:
Rál Ilnrởng gặ
Giảm bạch cẳu'**J
Tlmờng gặp Giảm tiếu cấul**i
C hưu biêt Giản; số lượng tế bảo lympho'WJ
Rối loạn hệ miễn địch:
Kỉ;óng thuờng gặp | Quả mẩn
Rối“ Io_an chựvên hóa vả dinh duõng:
T hương gặp
[ Chán ăn
Rôi Ioạn tâm thân:
Rất thường gặp
[ Trẩm cảm, mất ngủ
Rôì Ioạn hệ thần kinh:
Rầl lhương gặp
Đau đẩu, chóng mặt
T hương gặp Hội chứng ông cổ tay. dị cảm `
Hiếm gặp Lo mơ `Ềì \ `\
Rối loạn mạch: "N
Rầt thường gặp [ Nóng bừng v
Rối“ Ioạn tỉẽu hóa:
Rầl 1hưòng gặp ị Đau bụng, buôn nôn '
T hưởng gặp , Nôn, tiêu chảy, táo bón, khó tiêu
Rối loạn gan mật:
Rár thường gặp Tặng mcn_ gan, tăn g bilirubin huyết, tăng phosphatase
kiêm huyêt
Hiểm gặp Viêm gan m_ víêm gan ứ mật …
Rối Ioạn da vả mô dưới da:
Rất rhường gặp Tăng tiết mồ hôi
Thường gập Rụn g tóc, phải ban, mề đay, ngứa
Hiểm gặp Ngoại ban mụn mù toản thân câp tính…
Rối loạn cơ xương và xương:
Rât thường gặp
| Đau khởp và cơ xương "’
Page 4 of12
LPD Title: Exemesmn mbleis
|.PD Dam; lJ`eb 15. 2016
Count;le I’íenmm
Reference 5PCĨ UK SPC quẻzrence SP(` dme.’ .1111 2015
T hướng gặp | Găy xuong, loãng xươn g
Các rối loạn chung vả tại vị m'điều trị:
Rất thường gặp Đau, mệt mòỉ
Thường gặp Phù ;; goại biên, suy nhược
(*) Bao gốm: đau khóp, và đau với mật độ it hơn ở các chi, viêm xương khởp, đau lưng, viêm khớp,
dau cơ vả cứng khởp
“** ’ Gìảm bạch cầu và giảm tiểu cầu hiếm khi đuợc bảo cáo ở bệnh nhân mắc ung thư vú tiến t;iền
Đã quan sát thẳy dôi khi giảm tế bảo lympho 0 khoảng 20% bệnh nhân đuợc cho dùng Aromasin,
đặc biệt lá ở bệnh nhân bị gỉảm tế bảo iympho tù tnlớc; tuy nhiên, số lượng tế bảo iympho trung
binh ở cảc bệnh nhân nảy kh_ông thav đối rõ rệt thco thời gian vả không thẳy mức tảng nhiễu; vi rus
tưong úng. Chưa quan sải thấy cảc tác dụng nảy ở cảc bệnh nhân được điều t;ị trong nghiên cứu ung
thư vú giai đoạn sớm
mTần suất được tính theo quy tắc 31X.
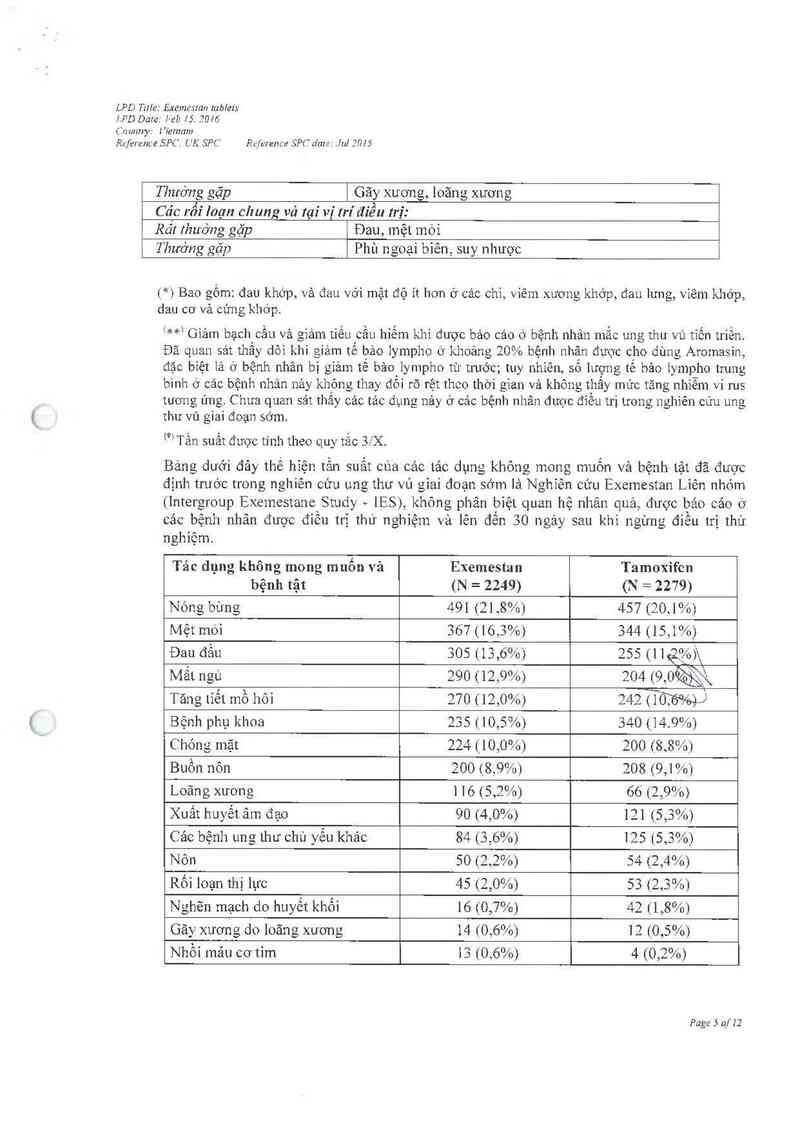
Bảng dưới đây thế hiện tần suất của cảc tảc dụng không mong muốn và bệnh tật đã được
định trưởc trong nghiên cứu ung lhư vú gỉai đoạn sớm là Nghiên cứu Exemestan Liên nhóm
(Intergroup Exemestane_Study ~ IES), không phân biệt quan hệ nhân quả, được bảo các ờ
cảc bệnh nhân được điêu trị thử nghiệm vả lên đến 30 ngảy sau khi ngừng điêu trị thứ
nghiệm.
Tác dụng không mong muốn vả Exemestan Tamoxifcn
bệnh tật (N = 2249) (N = 2279)
Nóng bùng 491 (21,8%) 457 (20.1%)
Mệt mói 367 (16,3%) 344 (15,1%)
Đau đầu 305 (13,6%) 255 (11,2%);
Mất ngủ 290 (12,9%) 204 (_9. 042ạg\
Tăng tiết mồ hôi 270 (12,0%) 242 (W
Bệnh phụ khoa 235 (10,5%) 340 ('14.9%)
Chóng mặt 224 (10,0%) 200 (8.8%)
Buồn nôn 200 (8,9%) 208 (9,1 %)
Loãng xương 1 16 (5,2%) 66 (2,9%)
Xuất huyết ân; đ ạo 90 (4,0%) 121 (5,3%)
Cảc bệnh ung thư chủ yếu khảo 84 (3,6%) 125 (,5 3%)
Nôn 50 (2,2%) 54 (2,4%)
Rối loạn thị lực 45 (2,0%) 53 (2,3%)
Nghẽn mạch do huyết khối 16 {0,7%) 42 (1,8%)
Găy xương do loãng xương 14 ( 0.6%) 12 (0,5%)
Nhổi mảu cơ tim 13 (0,6%) 4 (0,2%)
Page 5 of 12
LPD 1'111E: Exemex/an mbỉets
LPD Dnle. Fei; 15. 2016
Coun/ij
1 ’;e lnam
Reference SPFJ UA' S'ỉ’C Reference SPC' dale: Jul 2015
4.9.
T_rong nghiến cún IES, tần suất của cảc biến cố thiếu mảu cục bộ tim trong nhóm điều trị
bằng exemcstan 1ả 4,5% so vởi nhóm điếu trị bằng tamoxỉfe_n 12) 4, 2% Không thẳy chẻnh
lệnh rõ rệt đối với bất kỳ biến cố tim mạch riêng lẻ nảo bao gồm tăng huyết' ap (9, 9% so với
8,4%) nhồi máu; cơ tim (0,6% so với 0 ,2%) và suy tim (1,1% so với 0 ,.7%)
Trong nghiên cứu IES, exemestan liên quan đến tỷ lệ tăng choiesterol trong mảu cao hơn so
với tamoxifen (3,7% so vởi 2,1%).
Trong một nghiên cúu ngẫu nhiến, mù đôi riêng biệt về phụ nữ sau mãn kinh mắc ung thư
vú giai đoạn sóm có nguy cơ thấp đuợc điều trị với cxemestan (N=73) hoặc giả dược (N— 73)
trong 24 thảng, excmestan liên quan đến mức giảm trung bình 7- 9% cholesterol HDL trong
huyêt tương, so với mức tãng 1% ơ gỉả dược. Cũng giảm 5-6% apolipoprotein A1 trong
nhóm exemestan so với 0-2% ở giá dược. Tảo dụng lến các thông số chắt béo khác được
phân tích (tồng cholesterol, cholesterol LDL, triglycerid, apolipoprotein-B vả lipoprotein-a)
tương đưong nhau ở hai nhóm điều trị. Ý nghỉa iâm sảng của các kết quả nảy lả khỏng rõ
rang.
Trong nghiên củu lES, quan sảt thấy loét dạ dảy ở tần suất cao hơn nong nhóm exemestan
so với nhón; tamoxifen (0, 7% so Với <0 1%) Phần lớn bệnh nhân dùng exemestan bị ioét dạ
dảy đã được đìều trị đồng thời với cảc chắt chống viêm không phái loại steroìd vảJhoặc có
tiến su bệnh.
Bảo cảo các tảc dụng không mong muôn nghi ngờ
Báo cáo cảc tác dụng không mong muốn nghi ngờ sau khi iuu hảnh thuốc 12) rất quan trọng.
Điếu nảv cho phép tiễp tục theo dõi tỷ lệ lợi ichJ’ nguy cơ khi sử dụng thuốc.
Quá liều
Cảo nghiên CỦU lâm sảng dã được tiến hảnh với Aromasin với liêu đơn lên tới 800mg cho
nguời tình nguyện là phụ nữ khóe mạnh và liều 600mg/ngảy vói phụ nữ sathhiửềq kỉnh bị
ung thư vú giai đoạn tiên tiiềi;; nhủngl ìều nảy được dung nạp tổt. Liều dơi; Arồrrỉcsền có thể
dẫn dến cảc triệu chủng đe dọa tỉnh mạng chua được biết đến Trên chuột công vả chó, con
vật bị chết sau khi dùng Iỉếu đơn tương đuong tuơng úng với 2000 vả 4000 1ần lìều đuợc
khuyến cản ở nguời tính theo mglm Không có thuốc giải độc đặc hiệu khi dùng quá liếu
mà phải điều t1ị triệu chủng. Chăm sóc hỗ trợ chung, bao gồm theo dõi thường xuyên cảc
dấu hiệu sinh tồn vả quan sả; chặt chế bệnh nhân, được chỉ định
CÁC ĐẶC TÍNH DƯỢC LÝ HỌC
Cảc đặc tính dược lực học _ _
Nhóm dược lý điêu trị: chât ức chê aromatase dạng steroìd, chông tản sinh.
ATC: LOZBGOG
Cơ chế tảc dung
Exemestan_ lả chẳt ưc chế không thuận nghịch aromatase dạng steroìd, có cẳư t;úc liên quan
đến chất nền tụ nhiến lả androstenedion. Ở phụ nữ sau khi mãn kinh, các oestrogen được tạo
thảnh chu yếu từ sụ chuvến đổi androgen thảnh oe_strogen nhờ enzym aromatase trong các
mô ngoại vi. Sự giảm tạo thảnh oestrogen do úc chế aromatase lẻ; một phuong phảp điều lrị
Page 6 of 12
LPD Tnle: E.vemesIan Jabiexs
!.PD Dale' Feb 15. 2016
Co ;mrrj' : Ĩ 'ie rnam
Reference SI’CĨ' IJK SPL" Reference SPfỈ' dam: Jul 2015
chọn lọc vả hiệu quả cho trường hợp ung thư vú phụ thuộc hormon ở phụ nữ sau khi mãn
kỉnh. Ó phụ nữ sau khi mãn kinh, Aromasin p.o. (dùng đường uống) lảm giảm dáng kế
nồng độ oeslrogen trong huyết thanh, bắt dầu từ liều 5mg, sự giảm nồng dộ oestrogen đạt
được tối đa (> 90%; với liều 10 — 25mg. Ó bệnh nhân ung ư… vú giai đoạn sau măn kinh,
điều trị với iiều 25mg/ngảy, quá trình tạo oestrogen nhờ aromatase trong toản bộ cơ lhể
giảm 98%.
Excmestan không có bắt kỳ hoạt tính progestogen hay ocstrogen nảo. Hoạt Lính androgen
nhẹ có thế do dẫn c-hẩt l7-hydro, đã được quan sảt thắy chủ yếu ở liều cao. Trong các thử
nghiệm đa liều dùng hảng ngảy, không xảo định được ảnh hưởng nảo cùa Aromasin tới sự
sinh tống hợp co;tisol hay aldosteron cúa tuyến thượng thận, đo trước và sau khi tiến hảnl;
lhử nghiệm ACTH, điểu đó chứng, tỏ tính chọn lọc cùa exemestan đối với các enzym khác
liên quan đến con đường lồng họp các ho rmon nhản steroìd.
Do đó sự lhay lhế các glucocorticoid hoặc mineralocorticoỉd lá không cần thiết, Đã quan sảt
thắy có sự gia tãng nhẹ, không phụ thuộc iiếu của nồng độ LH vả FSH trong huyết thanh,
thậm chí ở các liều thấp. Tuy nhiên, tác dụng nảy, dự kiến sẽ xảy ra với nhóm dược chẳt nảy
vả có thế lả do kết quả của quá trình điều hòa ngược (feedback) cùa tuyển yên, do thuốc lản;
giảm oestrogen nên sẽ kỉch thích tuyến yên liết gonadotropin (ở cả những phụ nữ sau khi
mãn kỉl;h).
Hiệu quả vả an toản lâm sâng
Điêu tri hô lrơ unLy lhu' vú Qiai đoan sớm
Trong thử nghiệm đa trung tâm, ngẫu nhiên, mù đôi (Nghỉên cửu lntcrgroup Exemestan
[IES]), được lhực hiện trên 4724 bệnh nhản ớ giai đoạn sau mãn kinh có thụ thể ocstrogen
dương tính hoặc ung thư vú giai đoạn dằn chưa phát hiện, nhũng bệiiiỊ;;l;ẵij›ki;ôlịig còn bộnh
sau khi dùng liệu phảp hỗ lrợ lamoxifen trong 2 - 3 nãm được chọn nẳẫu"nh\ệịầđỆ được diều
trị bằng Aromasin (25tng/ngảy) hoặc tamoxifen (20 hoặc 30mg/ngảy) đế ổầr'Ễthảnh hết 5
năm điều trị bằng lìệu phảp honnon.
T heo dõi trung binh trong 52 rháng nghiên cứu 1158
Sau khoảng thời gian điều trị trung binh khoáng 30 thảng vả theo dõi lrung bình khoảng 52
tháng, các kết quả cho thắy diều trị lỉên tục Với Aromasin sau khi dã điều trị 2 đến 3 năm với
iiệu phảp tamoxifen cho sự tỉến triển rõ rệt có ý nghĩa lâm sảng và thống kê về khoảng thời
gian sống không mang bệnh (disease — free survival - DFS) so với việc dùng liếp tục
lamoxifen. Cảo phân tích cho thắy trong thời gian tiến hảnh nghiên cứu, Aromasỉn lảm gìảm
nguy cơ tải phảt ung thư vú tới 24% so với tamoxỉfcn (tỷ số nguy cơ 0,76; p=0,00015). Lợi
ích của exemestan đối với khoảng thời gian sống khỏng mang bệnh so với tamoxifen lả rõ
rảng, dù iả trong tỉnh trạng có hạch hay dùi; g hóa trị liệu lrước đó.
Aromasin cũng iảm gỉảm rõ rệt nguy cơ bị ung thư vú đối bên (tỷ số nguy cơ 0,57; p =
0,04158).
Trong loản bộ quằn thể nghiến cứu, quan sát thắy có xu hưởng tăng tỷ lệ sống còn toản bộ ở
nhóm dùng exemestan (222 người chết) so với nhóm dùng tamoxỉfen (262 người chết) với
tỷ số nguy cơ 0,85 (log—rank test: p = 0,07362), thế hiện ở việc gìảm 15% nguy cơ tử vong
với nhóm dùng exemestan. Quan sảt thắy giảm rõ rệt về mặt thống kế 23% nguy cơ tử vong
Page ? o] ].?
LPD ĩưie Ẹxemesran mblem
LPD Dam Feb 15. 2016
Counlr_v T'ielnam
Reference SP(" ( ;g SPC
(tỷ số nguy cơ cho tỷ 1ệ còn sổng còntoản bộ 0,77; kiểm định Wald: p
Reference Sl’t“ date. Jul 2015
= 0,0069) ở nhóm
exemestan so với nhóm tamoxifcn khi điều chinh cho cảc yếu tổ tiên lượng đã được định
trước (ví dụ như tinh trạng ER, tình trạng có hạch, hóa trị trước đó, sử dụng HRT vả sử dụng
bisphosphonat).
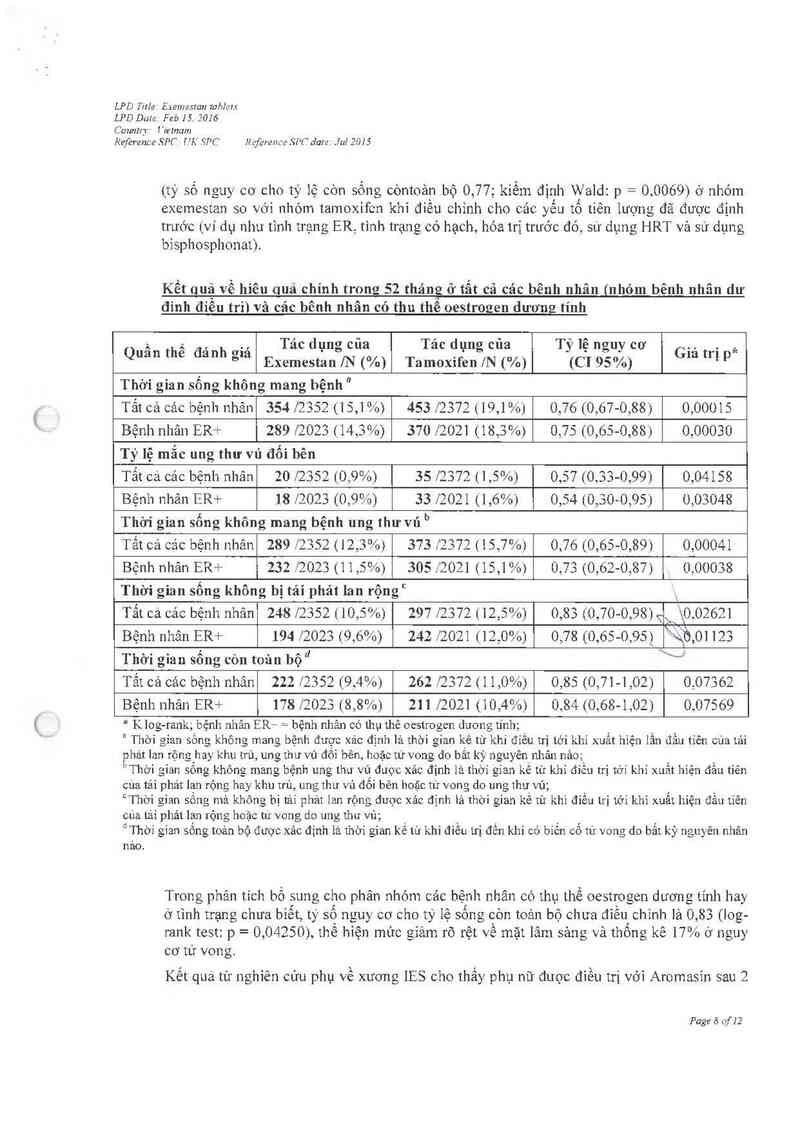
Kểt quả về hiêu quả chính trong 52 tháng ở tẫt cả các bênh nhân _fflhóm bênh nhân dư
đinh điều tri) và cảc bênh nhân có thu thể oestroaen dương tính
Quần thể đánh giá ExỉỉiiceỆtỉliigfỄIUỄ/n) Taririlẵxcilfỉiligiiĩiuễxo) Tầiớẹlrểgsliỉ)cơ Giá trị pà
Thời gian sống không mang bệnh "
Tất cả các bệnh nhảm 354 /2352 (15,1 %) 453 12372 (19,1%) 0,76 (0,67-0,88) 0,00015
Bệnh nhân ER+ 289 /2023 (14,3%) 370 l202] (18,3%) 0,75 (0,65-0,88) 0,00030
Tỷ lệ mắc ung thư vú đối bên
Tất cá cảc bệnh nhân 20 /2352 (0,9%) 35 /2372 (1 ,5%) 0,57 (0,33-0,99) 0,04158
Bệnh nhân ER+ 18 12023 (0,9%) 331202; (1,6%) 0,54 (0,300,95) 0,03048
Thời gian sổng không mang bệnh ung thưvủ "’
Tất cả các bệnh nhân 289 12352 (12,3%) 373 ;'2372 (15,7%) 0,76 (0,65-0,89) 0,00041
Bệnh nhân ER+ 232 f2023 (11,5%) 305 7202] (15,1%) 0,73 (0,62-0,87) 0,00038
Thời gỉan sống không bị tái phảt lan rộngc -,
Tât cá cảc bệnh nhản 248 /2352 (10,5%) 297 /2372( 12. 5%) 0,83 (0,70-0,98) %, \0,02621
Bệnh nhân ER+ 194 .72023 (9,6%) 242 0.021 12 ,00 xo) 0,78 (0,65-095.) \ìặò,o; ;23
Thời gian sổng còn toản bộ“P \“
Tất cả cảc bệnh nhân 222 /2352 (9.4%) 262 !2372 (’11,0%) 0,85 (0,71 -1 ,02) 0,07362
Bệnh nhân ER+ 178 J’2023 (8,8%) 211 Í2021 ('10,4%) 0,84 (0,68-1,02) 0,07569
* K log-rank; bệnh nhân ER— = bệnh nhân có lhụ thê oeslrogcn dương tính;
a Thời gian sống không mang bệnh được xác định là thời gian kê từ khi điều ưị lới khi xuất hiện lẳn đầu tiên cúa tải
hát lan rộng hay khu trú, ung thư vú đối bên hoặc tử vong do bất kỷ nguyên nhân nảo;
`Thời gian sông không mang bệnh ung thu vú đuợc xảo định là thời gian kế từ khi điêu trị tới khi xuất hiện đầu tiên
cùa tải phát lan rộng hay khu trú, ung thư vú đối bên hoặc từ vong do ung thư vú;
cThời gian sổng mã không bị lái phảtl an rộng đuợc xảc định ìả thời gian kề lù khi điều trị tởi khi xuất hiện đầu tiên
cúa tái phát lan lộng hoặc
từ vong do ung thư vú;
dThời gian sống toản bộ được xảo định lả. thời gia;; kế từ khi điều 1.rị đến khi có biến cố tủ vong do bất kỳ ngu;v ên nhân
nảo.
Trong phân tich bổ sung cho phân nhóm cảc bệnh nhân có thụ thể oestrogen dương tinh hay
ở tình trạng chua biết, tỷ số nguy cơ cho tỷ lệ sống còn toản bộ chưa điều chinh lả 0,83 (log-
rank test: p— 0 ,,04250) thể hìện mức giảm rõ rệt về mặt lâm sảng và thống kê 17% ở nguy
cơ tử vong.
Kết quả từ nghiến cứu phụ về xương IES cho thấy phụ nữ được điếu trị với Aromasỉn sau 2
Fage 5 of12
LPD Tille: Eưmesmn lablels
LPD Daie: Feb l5. Jriiú
Coumry:
i ;enmm
Refirence SPCJ L'K SPC Rejerence SPC date. Jul 2015
đến 3 năm điều trị bằng lamoxifen bị giản; với mức độ trưng bình về tỷ trọng khoảng chẳt
cưa xương. Trong nghiên cứu lổng lhể, tỷ lệ gãy xương phát sinh trong diều trị được đảnh
giả trong thời gian điều trị 30 tháng cao hơn ớ bệnh nhân được điều trị với Aromasin so với
tan;oxifcn (tương ứng là 4,5% và 3,3%, p = 0,038).
Cảc kểt quả từ một nghiên cứu phụ về nội mạc tử cung IES cho thấy sau 2 năm điều trị, ở
bệnh nhân dùng Aromasin trung bình giảm 33% độ dảy nội mạc tử cung trong khi ở nhóm
điều trị bằng tamoxifen không có sự thay đối đảng kể ;;ảo. Dộ dảy cùa nội mạc tử cung,
được bảo cảo khi bắt đầu điều ui, trở lại bình thường ;
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng