















…… Tề ỀỀ. Ềr. …ằỀỦ
› womĩỉmmm
ề=_ …:mm…ưm…z…
mo…ỂểG. _:mozẫz. Ể…Eẵozì n…3ơI
EnỉỂ-l r.
&? .:ỡẳẵe: a ễa.
.ẵỉẵìư 3ìlẳâ s: a.:i
!: …ễ. ẫẫ. 4 1 N… 1 W… i
#:…ỂIỀa 8. l :.
LỄ…WF. !ỉ . \ v :. #…
......ĩẵ lễ. w…… ịiulizịề Ĩ…Ễ. ! :…
l.Eli L _, _1 |Ll i 1i LLL
:: :. El …ỉ… …ẵzẵ: ! .!
Ỉillaỉ. L5.n sềẵẵ Ề:: :… .i sẳ— e …M...ĩơa ..
ẸỀ ỉ-oẵẵlna, !… … lì i
…èuẵỉ . L L ..…Lnuủđcẵ .1 i
… the.ẵỀă %: htẩồữauEneẫ 1 L
ẫỈ. ị
u..:sẵẵ
Ĩz.Ễ_ ……aẵnẵ.zzẫ
ãlÍl-Ỉlenẫẩ ĩ: ỄaỄ.›
Illlll .ầhĨltỈlI-Ổẵẵ.to ln.lỄễẫẵ
22. .Lumaỉtsẵẵẫ L
::…-3 2… i.... .ẵtl xã .ẵỉíỂ: ..….7. 5… RE.
1…1
Glue
/
Pllp
Ễ EE uu ẵzìễ
Enẳ .oxtă
R… 2 Ểỉm
……ẵn. u…ảỀ-vẫẫễn c…
«x .oẫEễ>
……3 31² 8ễẳ ›8 3-
n: sn$ỉì:n …»… m:ễnỉ:m…
mẫuỂẫ… .:nỂ-R .ằỡÊ
OỆ :…n
xnne o£ Z En 3nns
oẵ …Ể: % ẵỂẵ.
mẵũ ơn.oả Ế .n
0sz…
"99 "3.²1
~
G
C)le
a
<…ỂỄỄ. xa
uc vồ.ẵnằảoỡẵn ỉưỂu
mOI…
. nzsă. ẫã s. .…Ể a; ầ3 sẵ… _ . Ế
… Ìễ.aẫnầẵ aễẵ e.ã … O:nm uEể 1ẵnẵ: a.. :. ỄỂ
%ảbẫ Ễ wo _ ni _ ' … ao
… … vồ O:Mn ổ n……o … ỉỂỀỄẾ. 0:51
_ . …Nưĩ—u lĨEỄ² m…ỉ…ồ 5…
… … nunĩ…ẵ. … muuễ :.nnỉaấ. !: zso…s
..P 1.F ỉn….ĩ.ẫ . 0nẵỉẳ
Ọa
v
nvnò
.A …ốxmzo
L… P…ẫẵ mỉ…
3… ổSSỂu»
ÍlCI EIHd V
LĩịẮ
ot'mo XI
<…Bẵẵo. xa
u…Ể … FLL ..Ể
. %… uẽ.ẵwẵ.ỉỉuầ ỉưỂạ
… <…nmẳẵmộ xx
..
. :nễẵỉo …
Iỉnẵ Amx…
>ỉm
ỉ ! rdN M
Lửụmmi III
Wfflmu.ffl ...itẵỂă ……
F lrl | W.…
.. a. .. "
Ềs ……rtt …m
nẮ—wưW
. uf
41
. H…fflẵẵ .:
Lmư ỂẹẫnỂ: .: :....ỉ
r.i s.t oẵs …Ềmẵẵ. u 1: I…
!: ….e. .: :…
..ĩceẵỉ .: .:
.:.: :....ẵl... : .: .: Ễ… e e.… a...
. u
…...Jsẩ ›..ẵ ljễẫ. Jẵ-Ỉ 1... .! ỉ…… … ..… ......
… _ … _ … Ế… n. .... ......
..... :. 2…» ….L...1 .ẵẵẵ. .: .!
….3Ì
.3Ễ. ::.....Ể.
ẫl uỉẵỉ. 5 .. ..:.ỄỄ... c...... : .... .z.i .. .ẵỉ ..… iẵ.ìu
Ếiẵ ...ỉẳẵẵ
. ...ỉ $ % EJỂ
… . f....Ểầdn! . .. .1ỀỄẵỂỂ:
Ễỉỉ. 1
...Ễỉỉ...Ễ jiĩ :: _ _ …i
_ _ .
l
›ỄỄSL. P :ỂỂ3u & F .. m:o
Ỉll! ..… 2… a... . …rẫ ......
.uỂỄ. u:..ỂIẽ! u..……. ..3
. , 4 . I f.u.…ẵỀẫ s..….
!.ìổỉani. Sn.› tềôỉ... n.f …..ỉỉẳ … 33.3. «8 ỂỈ .. KS
LfflM ỈẳnlỂ. … …. ......
xỄể » ĩỉ ỉBỔ
%x
Ý/T Mot'
VIRAMUNE XR® j6'
Thânh ghần
Mỗi viên nén giải phóng chậm chứa 400 mg hoặc] 00 mg nevirapine khan.
Tá dược: Lactose monohydrate, hypromellose, oxit săt, magnesium stearate.
Chỉ đinh
VIRAMUNE XR được chỉ định đề kết hợp với các thuốc khảng retrovirus khảo điều trị nhiễm
HIV-l. Thông tin quan trọng liến quan đển việc sử dụng VIRAMUNE XR trong diều trị nhìễm
HIV-iz
0 Không nên khời đầu điều trị nevirapine trên phụ nữ trưởng thảnh có số lượng CD4+
cao hơn 250 bản/mm3 do đã ghi nhận được độc tính gan nghiêm trọng vả đe dọa tính
mạng trong cảc thử nghiệm có và không có đối chứng (xem mục Cảnh bảo đặc biệt và
thận trọng),
. Cần tuân thủ chặt chẽ giai đoạn dẫn đầu 14 ngảy với VIRAMUNE gìải phỏng nhanh
dùng hảng ngảy; điều nảy đã được chứng minh lảm giảm tần suất phát ban (xem mục
Liều lượng và cách dùng vả Cảnh báo đặc bìệt vả thận trọng).
. Không bắt đầu diễu trị với VIRAMUNE XR nếu phảt ban kéo dải sau giai đoạn dẫn
đầu 14 ngảy sử dụng VIRAMUNE giải phóng nhanh. Không nên tiểp tục dùng liếu dẫn
dầu VIRAMUNE giải phóng nhanh 200 mg một lẩn mỗi ngảy quả 28 ngảy mả nến
thay mộ bằng chế độ điếu trị khảc.
Liều lương và cách dùng
Người lớn
Đối với bệnh nhân hiện lại khỏng điều Irị bằng VIRAMUNE giải phóng nhanh
Bệnh nhân nên được bẳt đầu điều trị với VIRAMUNE giải phóng nhanh hảng ngảy phối hợp
với các thuốc kháng retrovirus khác trong 14 ngảy đầu tiên (nên áp dụng giai đoạn dẫn đầu nây
do đã được chứng minh 1ảm giảm tần suất phát ban), tiếp nôi bởi một viên VIRAMUNE giải
phóng chậm 400 mg một lần mỗi ngảy. Bệnh nhân phải nuốt trọn vẹn viên nén VIRAMUNE
XR. Không đựoc nhai, nghiền hay chia nhỏ viên. Khi diếu trị kết hợp, nên tuân thủ liều dùng
vả theo dõi như khuyến cảo cùa nhà sản xuất. VIRAMUNE XR có thể dùng cùng hoặc không
cùng với thức ăn.
Đối với bệnh nhân chuyền íừ VIRAMUNE giải phóng nhanh sang VIRAMUNE XR
Những bệnh nhân hiện dang theo phác đồ VIRAMUNE giải phóng nhanh hai lần mỗi ngảy kết
hợp với cảc thuốc khảng retrovirus khác có thể chuyền sang dùng VIRAMUNE XR một lần
mỗi ngây kết hợp với các thuốc khảng retrovirus khác mà không cần giai đoạn dẫn dầu với
viên VIRAMUNE giải phóng nhanh.
Không bao giờ được sử dụng cùng lủc nhiều dạng bảo chế cùa nevirapine.
Bệnh nhân nhi từ3 tuối trở lên
Tính an toản vả hiệu quả cùa viên nén VIRAMUNE XR trên trẻ nhỏ dưới 3 tuối chưa được
thiềt lập.
Đfz
®
Tổng liếu mỗi ngảy trong suốt thời gian điều trị không nên quá 400 mg cho bất kỳ bệnh nhân
nảo. Có thế tính liêu viên nén VIRAMUNE XR dựa trên thẻ trọng hoặc diện tích bề mặt cơ thể
(BSA) cùa bệnh nhân.
Liều trong giai đoạn dẫn đầu với VIRAMUNE viến giải phóng nhanh hoặc hỗn dịch uống (14
ngảy đầu): Tẩt cả bệnh nhi nên bắt đầu diều trị với liều 150 mg/m2 (sử dụng công thức
Mosteller) hoặc 4 mg/kg thể trọng dùng một lần mỗi ngảy Lrong 14 ngảy đầu tiên. Nên ap dụng
giai đoạn dẫn đầu nảy do đã được chứng minh lảm giảm tần suất phảt ban Không cần ảp dụng
giai đoạn dẫn đầu nảy nếu bệnh nhân đã dùng kéo dải VIRAMUNE hỗn dịch uổng hoặc
VIRAMUNE viên giải phóng nhanh 200 mg hai lần mỗi ngảy.
Liều duy trì với viên nén VIRAMUNE XR (sau giai đoạn dẫn đầu): Liều uống khuyến cáo cho
bệnh nhi dựa trên BSA của bệnh nhi được nêu trong bảng dưới dây:
Liều uống khuyến cảo cho bệnh nhi dựa trên BSA sau giai đoạn dẫn đầu:
Phạm vi BSA (mĩ) Liêu VIRAMUNE viến giải phóng chậm (mg)
0,58 - 0,83 200 (2 x 100 mg hoặc 4 x 50 mg)
0,84— 1,16 300 (3x 100 mghoặcóxSO mg)
21,17 400(1x400 mg)
3600
Công thức Mosteller: BSA (ml) = \
Liều uống khuyến cáo cho bệnh nhi dựa trên thể trọng được mô tả trong bảng dưới đây. Liều
khuyên Cảo cho bệnh nhi dựa trên thế trọng phụ thuộc tuôi của bệnh nhi, với liếu khuyên cảo
khảc biệt cho trẻ từ 3 đẽn dưới 8 tuôi và trẻ 8 tuôi trờ iên.
Phạm vi thể trọng (kg)
cho bệnh nhi dưới 8 tuối
Phạm vi thể trọng (kg)
cho bệnh nhỉ 8 tuổi hoặc
lón hơn
Liều VIRAMUNE viên gìải phóng
chậm(mg)
12,5-17,8 17,9-31,2 200 (2x 100 mghoặc4xSO mg)
17,9 - 24,9 31,3 — 43,7 300 (3 x100 mg hoặc 6 x 50 mg)
25 trở lên 43,8 trở lên 400 (1 x 400 mg)
Theo dõi bệnh nhân
Theo dõi lâm sảng vả xẻt nghiệm chặt chẽ bao gồm cảc xét nghiệm men gan nên được tiến
hảnh khi bắt đầu và trong suốt 18 tuần điều trị với nevirapine. Tần suất theo đõi tối ưu trong
giai đoạn nảy chưa được thìết lập. Một số chuyến gia khuyến cáo nên theo dõi lâm sảng và xét
nghiệm hơn 1 lần mỗi thảng, và đặc biệt bao gổm theo dõi xét nghiệm men gan trước khi bắt
đầu giai doạn dẫn đầu 14 ngảy với VIRAMUNE giải phóng nhanh, trước khi bắt đầu điều trị
vởi VIRAMUNE XR vả 1ủc 2 tuần sau khi điều trị vởi VIRAMUNE XR. Sau giai đoạn khởi
dằu 18 tuần. nên tiếp tục theo dõi lâm sảng và xét nghiệm thường xuyên trong suốt quá trình
điều trị với VIRAMUNE XR [xem Cảnh bảo dặc biệt và thận trọng] Trong một số trường hợp,
tổn thương gan vẫn tiến triền ngay cả khi ngừng thuốc.
`ố11
Bệnh nhân đang theo phảc đồ điều trị với VIRAMUNE giải phóng nhanh hai lần mỗi ngảy
chuyên sang VIRAMUNE XR một lân mỗi ngây nên dược tiêp tục theo dõi lâm sảng vả xét
nghiệm.
Chỉnh liều
Bệnh nhân bị phát ban: Ngừng sử dụng nevirapine nếu bị phát ban nặng hoặc phát ban đi
kèm với các dấu hiệu toăn thân [xem phần Cánh báo đặc biệt vã thận trọng]. Không bắt
đầu điều trị với VIRAMUNE xa nếu bệnh nhân bị phảt ban mức độ nhẹ tới trung bình
và không đi kèm các triệu chứng toăn thân trong giai đoạn dẫn đầu 14 ngảy điều trị với
VIRAMUNE giải phỏng nhanh (200 mg một lần mỗi ngãy) cho đểu khi hết phát ban [xem
Cánh báo đặc bíệr vả Ihặn trọng]. Tổng thời gỉan điều trị với chế độ liều dẫn đầu 1 lần mỗi
ngãy không nên vượt quá 28 ngảy, khi đó nên thay thế bầng chế độ điều trị khác.
Bệnh nhân có biển cổ ở gan: Ngừng hẩn nevirapine nếu có biến cố lâm sảng (triệu chứng)
ở gan xăy ra. Không bãt đầu điều trị lại với nevirapine sau khi hồi phục [xem Cảnh báo
đặc biệt và thặn Irọng].
Bệnh nhân sử dụng lhuốc gián đoạn
Với bệnh nhân ngừng VIRAMUNE XR quả 7 ngây, khuyến cảo nến bắt đầu lại liều dẫn đầu
với viến nén VIRAMUNE giải phóng nhanh 200 mg mỗi ngảy trong 14 ngảy đâu tiên.
Bệnh nhân bị suy thận
Bệnh nhân có CrCL từ 20 mL/phủt trở lên và khõng cẩn lọc mảu thì không cần chỉnh liều. Với
bệnh nhân cần lọc máu, 1iểu bổ sung 200 mg VIRAMUNE giải phỏng nhanh được chỉ định sau
khi lọc máu. Các chất chuyền hóa cùa nevirapine có thể tích lũy ở bệnh nhân lọc mảu; tuy
nhiến, chưa rõ ý nghĩa lâm sảng cùa sự tích lũy nảy [Xem Đặc tính dược lý học]. VIRAMUNE
XR chưa được nghiên cứu trên bệnh nhân rối loạn chức nãng thận.
Chống chỉ đỉnh
Suy gan
Chống chỉ định VIRAMUNE XR trên bệnh nhân suy gan vừa hoặc nặng (Chiid-Pugh phân ioại
B hoặc c> hoặc chỉ số ASAT hoặc ALAT trước khi điều trị › s iần giới hạn trên cùa mức binh
thường (ULN) cho đến khi chỉ số ASAT/ALAT giảm xuống < 5 lần ULN [Xem phần Cănh
báo đặc biệt vả thận Lrọng].
Phòng bệnh sau phơi nhíễm
Chông chỉ định sử dụng VIRAMUNE XR như là một phần cùa biện phảp phòng bệnh sau phơi
nhiễm do nghê nghiệp hay không do nghê nghiệp [Xem phản Cảnh báo dặc biệt và thận
trọng].
Cảnh bảo đăc biêt và thân trong
Các phản ứng có hại nghiêm trọng nhất liên quan đển nevirapine lả viếm gan/suy gan, hội
trứng Stevens-Johnson, hoại từ biểu bì nhiễm dộc vả phản ứng quả mẫn.
Viêm gan/suy gan có thế liên quan đến cảc dấu hiệu quả mẫn bạo gồm phảt ban nặng, phát ban
đi kèm với sốt, khó chịu, mệt mòi, nhủc cơ hoặc khớp, rộp da, tồn thương miệng, viêm kết
mạc, phù mặt, tăng bạch cầu ải toan, giảm bạch cầu hạt, nổi hạch hoặc rối loạn chức năng
thân.
“LOỂ
mĩ
co=1
l8 tuần điều trị đẩu tiên với ncvinpiuc lù gini đoạn quan trọng cẩn theo dõi bệnh nhân
chặt chẽ để phit hiện các khả ning xuất hiện bìển cổ ở gui vi phủ ứng trên đa đe dọa
tính mạng. Tẩn suất theo dõi tối ưu trong giai đoạn náy chưa được thiết lập. Một số chuyên
gia khuyến cảo nến theo dõi lãm sâng vả xêt nghiệm hơn L lẩn mỗi tháng vả đặc biệt bao gổm
theo dõi xét nghiệm men gan trước khi bắt dẩn giai đoạn dẫn đầu 14 ngảy vởi VIRAMUNE
gìải phóng nhanh, truớc khi bắt đẩu điều ưi với VIRAMUNE xa (trong giai đoạn dẫn đầu) vả
2 tuần sau khi điều ui với VIRAMUNE xa. Sau giai đoạn khởi đẩu 18 tuần. nên tiếp tục theo
dõi lâm sảng vả xét nghiệm thường xuyến trong suốt quá ưth điều trì với VIRAMUNE XR.
Hơn nữa, giai đoạn đẫn đẳu 14 ngảy vởi VIRAMUNE 200 mg mỗi ngảy đã được chứng minh
1ảm giảm lẩn suất phát ban [xem Liễu lượng võ cách dùng]
Những bệnh nhân đang điều trì với VIRAMUNE giải phóng nhanh hai Li… mỗi ngảy chuyến
sang VIRAMUNE XR cần tiếp tục theo dõi lâm sâng vả xét nghiệm
Độc tính gan vì suy gnn
Độc tinh nặng đe dọa tinh mạng và dẫn tới tử vong trong một số trường hợp. bao gổm viêm
gan tối cẩp vả ứ mật. hoại tử gan vả suy gan. trến bệnh nhân điếu trị với nevirapine đã được
báo câo.
Nguy cơ xuất hiện biển cố gan triệu chứng bất kế độ nặng cao nhẩt trong 6 tuần đầu tiên của trị
liệu. Trong cảc thử nghiệm lâm sảng, nguy cơ tiểp tục tăng lẽn ờ nhỏm sủ dụng nevirapine
trong 18 tuẳn điều tn'.
Tuy nhiên. biển cổ ở gan có thế xáy ra bất kì thời điểm náo trong quá trinh điểu tri. Trong một
số trường hợp, bệnh nhân biểu hiện các triệu chứng không đìển hinh, báo trước như mệt mới,
khó chiu, chản ăn, buồn nỏn. vảng da, đau vùng gan hoặc gan to, đi kèm hoặc không kèm với
nồng độ transaminasc trong huyết thanh ban đẳu bẩt thường. Đã ghi nhận phải ban trong
khoảng một nứa bệnh nhân có biến cố bất lợi trên gan có ttiệu chứng. sội vả các triệu chủng
giả củm đi kèm với các biến cố trén gan nây. Một số biến cố. đặc biệt lả những biến cố đi kèm
với phát ban vá cảc triệu chứng khác, tiểu triển thảnh suy gan vởi transaminase tăng lên có
hoặc không Lãng bilirubin mảu, bệnh não gan, kẻo dải thời gian thromboplastin tửng phần hoặc
tăng bạch cẩu ải toan, Hùy cơ vân đã được ghi nhận trên một số bệnh nhân gặp phái phản ủng
trên da vả/hoặc trên gan liên quan đến việc sử dụng nevirapine. Bệnh nhãn có dấu hiệu hoặc
triệu chửng viêm gan phải ngứng sử đụng ncvirnpine vè đi khám bệnh ngay, có thể bao gổm cả
xét nghiệm men gan.
Nên kiềm tra cảc transnminnse ngay nểu bệnh nhin gặp phâi những dẩn hiệu hoặc triệu
chứng gợi ý vỉêm gnn vèlhoịc phân ứng quả mẫn. Nên kiếm tra transnminnse ngay lập
tức cho tẫt cả bệnh nhin tiến Lriẽn phât ban trong is tuẫn đẩu tiên. Bảc sĩ vì bệnh nhin
cần cânh giác với sự xuất hiện của cic dấu hiệu hoặc triệu trứng viếm gan chẵng hạn mệt
mỏi, khó chiu, chản in, buồn nôn, vâng dn, bilirubin niệu, phân nhạt lnâu , gan to hoặc
đau. Nên xem xét chẩn đoán độc tính gan trong trường hợp nây, ngay cả khi
tnnsaminase ban đẩu binh thường hoặc có thể li câc chẫn đoản khảc. [xem Liều lượng vè
cách dùng].
Nếu viêm gan trên lâm sảng hoặc tảng transaminase đi kèm với phát ban hoặc các triệu chứng
toản thán khác xuãt hiện, cấn ngùng nevirapine vĩnh vìễn. Không dùng lại ncvirapine sau khi
hổi phục. Trong một số truờng hợp, tôn thương gan vẫn tiến triền ngay cả khi dã ngứng điêu
tri.
Những bệnh nhân có nguy cơ cao gặp phải biến cố trên gan. bao gổm cả các biển cổ oó nguy
cơ gây tử vong, lả phụ nữ có số lượng CD4+ cao. Trong một phân tích gộp hồi cứu các thử
nghiệm Lim sảng sử dụng VIRAMUNE giâi phỏng nhanh. trong suốt 6 tuần đìễu trị đầu tiên
phụ nữ có nguy cơ gặp phải biến cố trên gan có tn'ệu chứng, thường kèm phát ban. cao gấp 3
iần so với nam giới (6% so với 2%). Bệnh nhân có số lượng tế bảo CD4+ cao hơn lủc khới dầu
điều tn' với nevirapine có nguy cơ cao gặp phải cảc biến cố trèn gan có triệu chứng. Phụ nữ có
số lượng tể bâo CD4+ trên 250 LnLn/mm3 có nguy ớớ gặp phái biển cổ bất lợi trến gnn có triệu
chứng cao gấp 12 lần so với phụ nữ có số lượng tổ bâo CD4+ dưới 250 tế ij (] 1% so
với ivi). Nguy cơ tăng 1ẽn dã được ghi nhận nến nam giới có số lượng ié bớo CD4+ cao hơn
400 binlmm’ Lớvi so với m ở nam giới cớ số lượng tế bảo coa+ dưới 400 bánJmm’). Tuy
nhiến, tất cả bệnh nhin, bẩt kề giới tính. số lượng tế bâo con hay iièn sứ điều trị với thuốc
kháng retrovirus, nến được theo dõi độc tinh gan do biến cố bẩt lợi trên gan có triệu chứng đã
được báo cáo với tất cả các mức số lượng tể báo CD4+. Đồng nhìễm viêm gan B vả C vâlhoặc
Lãng transaminasc lúc bắt đầu điều trị với ncvirapine liên quan đến nguy cơ cao gặp phải các
biến oố muộn có triệu chứng (6 tuần hoặc muộn hơn sau khi bắt đầu sử dụng nevirapine) vả
tăng AST hoặc ALT không triệu chứng.
Ngoài ra. độc tính gan nặng (ví dụ suy gan cần ghẻp gan trong 1 trướng hợp) xảy ra trên bệnh
nhân không nhiễm HIV-l sử dụng nhiễu liều VIRAMUNE giới phóng nhanh để phòng bệnh
sau phơi nhiễm (post-exposure prophylnxis (PEF)) - một chi đinh chưa được phê duyệt. Chống
chi đinh sử dụng VIRAMUNE XR trong phòng bệnh sau phơi nhiễm (PEF) [Xem Chống chỉ
định].
Dã ghi nhận nồng độ dảy của nevirapine tăng lên ở bệnh nhân xơ gnn hoặc chai gan. Vi vậy.
cẳn theo dõi cẩn thặn bệnh nhân bị xơ gan hoặc chai gan dể phới hiện dấu hiệu độc tính do
thuốc. Không sử dụng nevirapine cho bệnh nhân suy gan trung binh hoịc nặng (Chiid-Pugh
phân loại B hoặc C) [Xem Chống chi đinh. Đđc diếm dược lý]. VIRAMUNE XR chưa được
đánh giá trên bệnh nhân suy gan.
Phin ứng trên đa
Cảc phân ửng trên da nặng vù đe dọa tính mạng, kể cả tử vong, đã xuất hiện ở những bệnh
nhân điểu trì với ncvirapine. Các phân ứng nảy xây ra thường xuyên trong 6 tuấn đầu điều tn“.
Phán ứng bao gồm hòi chứng Stevens Johnson, hoại từ biểu bì nhiễm độc (TEN) vả phản ửng
quá mẫn mẻ hiện bời phảt ban, các triệu chứng toản thân vả tổn thương nội tạng bao gồm cá
suy gan. Đã ghi nhận hùy cơ vân ở những bệnh nhân có phán ửng trên đa válhoặc trên gan liên
quan đến sử dụng ncvirapine.
Phái ngứng nevirapine vĩnh viễn vả đảnh giá y khoa ngay ở những bệnh nhân xuất hiện các
đẩu hiệu hoặc triệu chứng phán ứng trến da nặng hoặc phán ứng quá mẫn (bao gồm nhưng
không giới hạn ở : phát ban nặng hoặc phát ban đi kèm với sốt. khói chiu. mệt mỏi, nhửc cơ
hoặc khởp, rộp da. sang thưong ở miệng, viêm kểt mạc, phù mặt vảlhoặc viêm gan, tăng bạch
cầu ải toan. giảm bạch cầu hạt, hạch to vả rối loạn chức nâng thận). Không tái sử dụng
ncvirapine sau khi phát ban nặng, phát ban đi kèm với tâng transaminasc hoán các triệu chứng
khác hoặc phản ứng quá mẫn.
Nếu bệnh nhãn xuất hiện phảt ban nghi ngờ liên quan đển nevirapine cẩn đinh lượng
transaminasc ngay. Ngừng sử dụng nevirapine vĩnh viễn ở những bệnh nhân có tăng
transaminasc đi kèm với phát ban [Xem Độc lỉnh gan vù suy gan].
Ặẫ/
Li
,\t
Bệnh nhãn cẩn khới đẳu ớiẻu ui với VIRAMUNE gìải phóng nhanh, dùng Lning ngảy trong 14
ngảy đẩu. Giai đoạn dẫn đầu nớy đã được chửng minh 1ảm giảm tằn suất phát ban. Ngừng sử
dụng nevirapine nếu bệnh nhân bị phả! ban nặng hoặc phát ban đi kèm với các triệu chửng toân
thân. Không bắt đẩu điều ưi với VIRAMUNE xa nếu bệnh nhãn bi phảt ban mức nhẹ tới
trung binh vả không đi kèm các triệu chứng toản thân trong giai đoạn dẫn đầu 14 ngây điểu trị
với VIRAMUNE giải phỏng nhanh 200 mglngảy) cho đến khi hễt phát ban. Tồng thời ginn
điều ui với chế độ Lièu dẫn đầu của VIRAMƯNE giải phóng nhanh không nen vượt qua' 28
ngảy mả khi đó nến thay thế bằng chế độ điều trị khác [xem Liễu lượng vù cảch dùng]. Bệnh
nhân cần được theo dõi chặt chẽ nểu xuất hiện phát ban đơn độc ở mọi mửc độ nghiêm trọng.
Tri hoãn việc ngưng điều trì với nevirapine sau khi khới phát ban có thể dẫn đến phản ứng
nghiêm trọng hơn.
Nữ giới có nguy cơ cao xuất hiện phảt ban hơn nam giới.
Trong một thử nghiệm lâm sảng sử dụng VIRAMUNE giải phỏng nhanh, sử dụng đồng thời
prednisone (40 mglngảy trong 14 ngây đẩu điều trị với ncvirapine) Iiẽn quan đến sự gia tang tỳ
1ệ vả mửc độ nghiêm trọug của ban trong suốt 6 tuần đầu điều trị với ncvirapine. Vi vậy. không
khuyến cáo sử dụng prednisone đề phòng ngừa phát ban liên quan đển nevirapine.
KLning thuốc
Không đuợc sử dụng VIRAMUNE XR đơn độc trong điều tri HlV-i hay bổ sung đơn độc vâo
một chế độ điều ưi thẩl bại. Vims kháng thuốc nhanh chỏng khi ncvirapine được sử dụng đơn
trị Iiệu. Nên cân nhắc nguy cơ kháng chẻo khi 1ựa chọn thuốc kháng retrovirus mới phổi hợp
với nevirapine. Nên xem xẻt đển thời gian bán thải dải của nevirapine khi ngững sử dụng một
chế độ điều trị kháng retrovirus chứa VIRAMUNE XR; nếu ngửng đổng thời các thuốc khảng
retrovirus cỏ thới gian bản thải ngắn hơn nevirapine, nổng độ nevirapine đơn độc trong huyết
tương thấp có thể kéo đải trong 1 tuần hoặc lâu hơn vá do vậy tinh trạng virus kháng thuốc có
thể xuất hiện sau đó [xem Đặc điểm dược 1ỷ]
Tương tâc thuốc
Bảng 1 iiệt kê các phản ứng tiềm tảng và đã được thiềt 1ập [Xem mục Tương tác thuốc]. Không
khuyến cáo sử dụng đồng thời với có St. John's (Hypericum perforatum) hoặc các chế phẩm
chửa cỏ St. John's với nevirapine. sn dụng đổng thời có 81. John's với các chẩt ức chế men sao
chẻp ngược không nucleoside (NNRTI). bao gồm cả nevirapine. được cho 1ả iảm giâm nồng độ
NNRT] LLiảp đưới mức hiệu quả vả dẫn đến giảm đảp ứng với virus. có mẻ dẫn đến kháng
nevirapine hoặc nhóm thuốc NNRTI.
Không khuyến cáo sử đụng đồng thời nevirapine vả ct'avirenz do phối hợp nây liến quan đểu
sự gia tảng phản ứng có hại vả khòng câi thiện hiệu quả.
uới chứng hồi phục miễn dich
Hội chửng hồi phục miễn dich đã được ghi nhặn ở những bệnh nhân điếu tn' bằng phác đồ phối
hợp thuốc khảng retrovirus bao gổm nevirapine. Trong giai đoạn đẳu của trị liệu phổi hợp
thuốc kháng retrovirus, nhũng bệnh nhãn có hệ míễn dich đảp ứng có thể xuất hiện đáp ứng
viếm với các nhiễm trùng cơ hội âm ỉ hoặc tồn lưu (chảng hạn nhiễm Mycobacterium avium,
cytomegalovims. viêm phối do Pnctunocystis jiroveci ( PCP) hoặc lao) mã có thể cần đảuh giá
hoặc điều ni me….
Rối loạn phân bố mỡ
Rối loạn phân bố/tích lũy mỡ bao gồm béo phì trung tâm, tãng mỡ sau cổ (gù trâu), teo ngoại
biên, teo mặt, tuyến vú lớn, vả “hình dạng kìền cushing” đã được ghi nhận 0 bệnh nhân điều trị
với cảc thuốc khảng retrovirus Hiện chưa rõ cơ chế và hậu quả lâu dải của những biển cố nảy.
Chưa thiết lặp mổi quan hệ nhân — quả.
Tương tác thuốc
Nevirapine được chuyển hóa chủ yếu bởi gan thông qua isoenzyme cytochrom P450, 3A và
2136. Nevirapine được biểt là một chất gây cảm ứng các enzym nảy. Kết quả là khi sử dụng
đồng thời với nevirapine, cảc thuốc chuyển hỏa bởi hệ thống enzym nảy có thể có nổng độ
trong huyết tương giảm đi.
Kết quả cùa cảc nghiên cứu về tương tảc thuốc với VIRAMUNE giải phóng nhanh được cho 1ả
cũng áp dụng đối với VIRAMUNE XR. Nhận định lâm sảng về hiệu chỉnh liều dựa trên cảc
tương tác đã thiết lập được liệt kê trong bảng 1. Dữ liệu trong bảng 1 dựa trên kết quả cùa các
nghiên cứu về tương tảc thuốc tiến hảnh trên bệnh nhân dương tính với HIV-l trừ khi nếu khảo
đi. Ngoài các tưong tảc đã được thiết lập, có thể có tương tảo dược dộng học tiềm năng giữa
nevirapine vởi cảc nhóm thuốc khác chuyến hóa bời hệ cytochrom P450. Những tương tác
thuốc tiểm năng nảy cũng được liệt kê trong bảng 1. Mặc dù cảc nghíên cứu về tương tảc thuốc
chuyên biệt trên bệnh nhân dương tính với HIV-l chưa được tiển hảnh trên một số nhóm thuốc
liệt kê trong bảng 1, cần tiển hảnh theo dõi lâm sảng khi phổi hợp với cảc thuốc nảy.
Có tương tảc phức tạp in vitro gíữa nevirapine vả chất chống huyết khối warfarin. Vì vậy, khi
sử dụng đồng thời cảc thuốc nảy, nồng độ warfarin trong huyết tương có thể thay đối cùng với
nguy cơ kéo dải thời gian dông máu, Khi phối hợp warfarin vởi nevirapine, nên theo dõi
thường xuyên mức độ kháng đông
Tến thuốc Ành hưởng trên nổng Nhận định về lâm sảng
độ Nevirapine hoặc
thuốc dùng đồng thời
Atazanavir/Ritonavir lAtazanavir Không sử dụng đồng thời nevirapine với
TNevirapine atazanavir do nevirapine iảm giảm nổng độ
atazanavir
Clarithromycin lClarithromycin Nevirapine lảm giảm đáng kể nông độ
T 14-0H clarithromycin; tuy nhiên, nồng độ chất
clarithromycin chuyến hỏa l4-OH tăng lên. Do chất chuyển
hỏa còn hoạt tính cùa clarithromycin có hoạt
tính khảng Mycobacterium avium—
intracellulare complex giảm, vì vậy hoạt tỉnh
kháng chùng bệnh nảy có thế bị ảnh hưởng.
Nên cân nhắc sử dụng azithromycin thay thế
cho clarithromycin.
Efavirenz l Efavirenz Chưa xác định được liếu an toản vả hiệu quả.
phù hợp cho dạng phối hợp nảy [Xem Mục
Cảnh bảo đặc biệt vả thận trọng]
[ Ethinyl estradiol vả l Ethinyl estradiol Phụ nữ đang điều trị với nevirapine không nên
, Norethindrone ], Norethindrone sử dụng các thuôo tránh thai đường uống và
Ỉ1
'
LI'
Lgc`
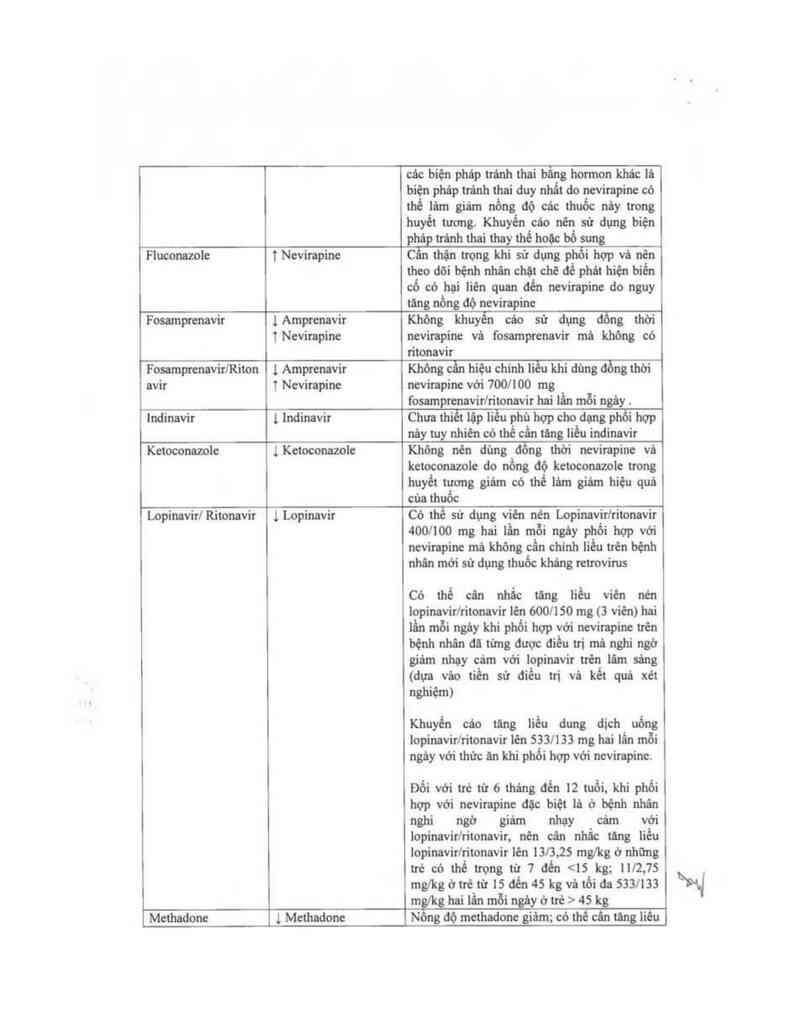
cảc biện pháp tránh thai bẵng hormon khác lả
biện phảp tránh thai duy nhẩt đo nevirapine có
thế lâm giảm nổng độ các thuốc nảy trong
huyết tượng. Khuyến cáo nên sử dụng biện
pháp tránh thai thay thế hoặc bổ sung
Fluconazole
T Nevirapine
Cẩn thặn trọng khi sử dụng phối hợp vá nên
theo dõi bệnh nhân chặt chẽ aẻ phới hiện bỉến
cổ có hại 1ièn quan đến nevirapine đo nguy
tăng nồng độ nevirapine
Fosamprenavir
1 Amprenavir
T Nevirapine
Không khuyến cảo sử dụng đồng thời
nevirapine vả fosamprenavir mả khỏng cỏ
ritonavir
FosamprenavirlRiton
avir
l Amprenavir
T Nevirapine
Khỏng cán hiệu chinh liều khi dùng đồng thời
nevirapine với 700/100 mg
fosamprenavirlritonavir hai lẩn mỗi ngảy.
lndinnvir
1 1ndinavir
Chưa thiết lập liều phu hợp cho đạng phôi hợp
nảy tulnhiẽn có thể cần Lãng Iiều indinavir
Ketoconazole
ị Ketoconazole
Khỏng nên dùng đồng thời ncvirapinc vả
ketoconazoie do nồng độ ketoconazole trong
huyểt tượng giám cớ mẻ Liim giớm hỉệu quá
của thuốc
Lopinavirl Ritonavir
l Lopinavir
Có thể sử dụng viẽn nén Lopinavir/ritonavir
400/100 mg hai lần mỗi ngáy phối hợp với
nevirapine mã không cần chinh liều trến bệnh
nhân mới sử dụng thuốc kháng retrovirus
Có mẻ cân nhác tãng liều viên nén
iopinavirlritonavir lến 600/150 mg (3 viến) hai
lần mỗi ngảy khi phối hợp với ncvirapinc trên
bệnh nhân đã từng được điều in mã nghi ngờ
giảm nhạy cảm với Iopinavir trên lâm sâng
(đựa vâo tìền sủ điều ưi vả kểt quá xẻt
nshiệm)
Khuyến cảo tãng liều đung dich uổng
lopinavirlritonavir lèn 533l133 mg hai 1ẩn mỗi
ngây với thửc ân khi phôi hợp với nevirapine.
Đối với ue từ 6 tháng đển 12 tuổi, khi phổi
hợp với nevirapine đặc biệt lá ở bệnh nhân
nghi ngờ giảm nhạy cám với
lopinavirlritonavir. nến cân nhắc tãng iiều
lopinavirlritonavir iẽn 1313,25 mglkg ở những
ni cô mẻ trọng từ 1 đến <15 kg; 11l2,75
mglkgởtrètừ 15đến45 kgvảtốiđaSJ3/i33
Methadonc
t Methađonc
mẵkĩgdhai lẫnmỗingèyờttè>ctS kg
N dộ mcthađone giảm; có thế cồn tâng iiều
methadonc đề phòng ngừa triệu chứng cai
thuốc opiatc. Bệnh nhân đang sử dụng
methadone nến theo đõi dấu hiệu cai LL…ớc vù
chỉnh liều tương ửng khi bắt đầu điều ui với
nevirapine.
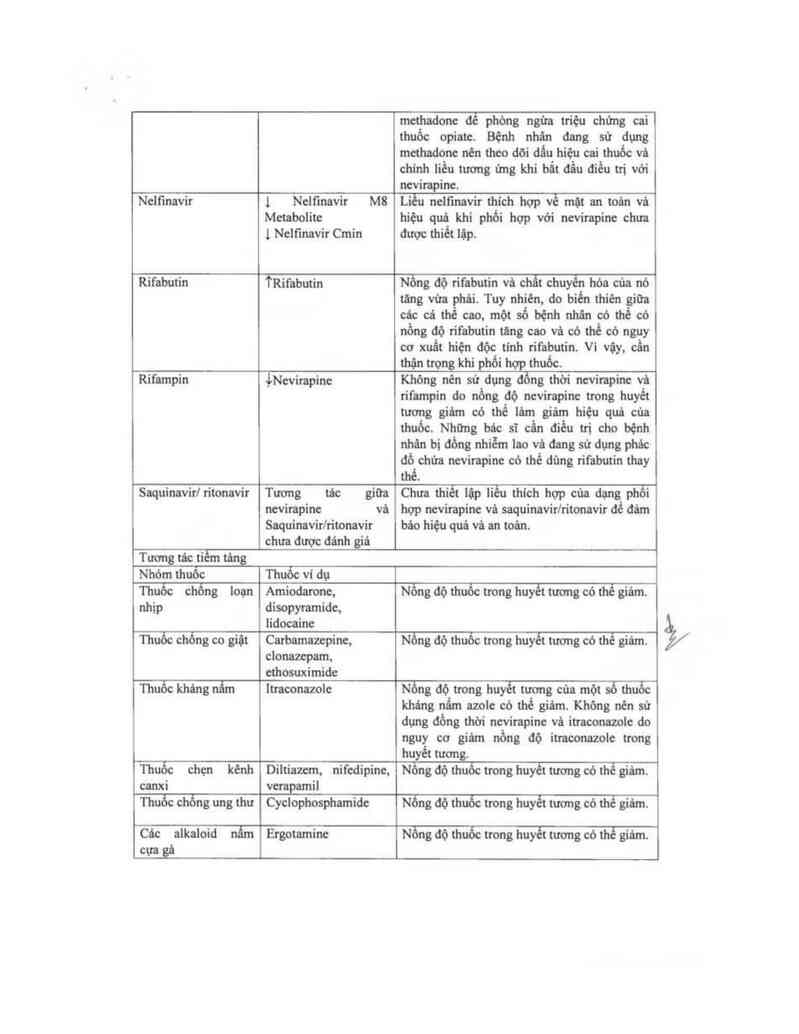
Nclt'mavir l Nelftnavir M8 Liêu nelfinavir thich hợp về mặt an toản vá
Metabolite hiệu quả khi phổi hợp với nevirapine chưa
t Nelt'mavir Cmin được thiết lập.
Rifabutin TRit'abutin Nồng độ rifabutin vả chất chuyến hỏa của nó
LLng vừa phải. Tuy nhien, do biến thiếu giữa
cớc cá iLiẻ cao. một số bệnh nhân có mẻ có
nồng độ rifabutin tãng cao và có thế có nguy
cơ xuất hiện độc tinh rifabutin. Vi vậy. cần
thận trọng khi phối hợp thuốc.
Rifampin Ịchimpinẹ Không nên sử dụng đổng thời nevirapine vù
rifampin do nồng dộ ncvirapine trong huyết
tuong giâm cỏ ihè lám giảm hiệu quả của
thuốc. Những bác sĩ cần điều tri cho bệnh
nhân bị đồng nhiễm iao vả đang sử dụng phác
ớớLớiiớa nevirapine có mẻ dùng rifabutin thay
the.
Saquinavirl ritonavir Tương tảc giữa Chưa thiễt lặp liều thich hợp của dạng phồi
nevirapine vù hợp nevirapine vả saquinavirlritonavir để đám
Saquinavirlritonavir bảo hiệu quả vả an toản.
chưa được đánh giá
Tường tảc tiềm tùn
Nhóm thuốc Thuốc ví dụ
Thuốc chỏng loạn Amiodarone, Nồng độ thuốc trong huyết tường có thế giám.
nhip disopyramiđc.
1idocaine
Thuốc chống co giặt Carbamachinc. Nỗng độ thuôc ttong huyết tuơng có thẻ giâm.
clonazepam,
cthosuximide
Thuốc khảng nấm Iưaoonnzole Nồng độ trong huyểt tương của một số thuốc
kháng nấm azoic có thể giám. Không nẻn sử
đụng đồng thời ncvirapinc vá itraconazole do
nguy cơ giảm nồng độ itraconazole trong
huyết tương.
Thuốc chẹn kênh
canxi
Diltiazcm, nifedipine,
vcrapamil
Nồng độ thuốc trong huyết tương có thế giảm.
Thuốc chỏng ung thư
Cyclophosphamiđc
Nồng độ thuốc trong huyết tương có thể giám.
Các alkaloid nấm
cvìẽả
Ergotamine
Nông độ thuốc trong huyết tương có thế giảm.
Thuốc ức chế miễn Cyclosporin. Nỗng độ thuốc trong huyết tương có thế giảm.
dich tncrolimus. sirolimus
Thuốc kích thich nhu Cisapride Nòng độ thuốc trong huyết tương có thể giảm.
động
Thỉỗc chủ vận Fentanyl Nồng dộ thuốc trong huyẩ tương có thế giảm.
opiatc
Thuốc chống huyết Warfarin Nồng độ thuốc trong huyẵ tương có thẻ tãng.
khối Cỏ Liié có tảc động trên tinh Lmng kháng đông.
Khuyển cáo thoo dõi mức kháng đông.
Thời g' mang thai vi cho con bị
Thời ki mang thai
Dộc Linh gãy quải lhai. Phản Ioại Lrong Ihai kỳ nhỏm B
Chưa ghi nhặn độc tính gây quái thai trong các nghiến cứu về sinh sản tiển hảnh uc… chuột vè
Lhò mang thai. Mức 1iều khỏng gây tảc dụng lên mẹ vả sự phát triền của thai kỳ tạo ra nổng độ
toản thãn chuột vả thò tường đương hoặc cao hơn khoảng 50% so với nồng độ thuốc ở 1iều
khuyến cáo hảng ngảy cho người (dựa trên AUC). Đã ghi nhặn sự giám khồi lượng bảo thai do
sử dụng liểu gây độc cho mẹ ờ chuột (nồng độ cao hơn khoáng 50% nồng độ ở liều khuyến cáo
cho người). Chưa tiến hảnh nghiên cửu đầy đủ vả có đối chứng về việc sử dụng nevirapine cho
phụ nữ mang thai.
Dữ liệu khảo sát phụ nữ có thai tử Đang ký Thai sán Dùng thuốc kháng retrovirus triển khai từ
tháng 111989. khỏng cho thấy nguy cơ tâng đi tật khi sinh sau khi dùng nevirapine trong 3
thảng đầu của thai kỳ. Tỷ lệ đi tật khi sinh sau khi dùng thuốc ttong bất kỳ tam cả nguyệt nùo
tương đương với tỷ lệ ghi nhặn được ở dán số chung.
Biển cổ gan nặng bao gồm cả tử vong đã được bâo câo ở phụ nữ có thai sử dụng ncvirapine dải
ngây như là một phẫn cùa ưi 1iệu phối hợp điều ưi nhiễm HIV-l. Phụ nữ có CD4+ cao hơn 250
bản/mmẵ bất kể tinh trạng thai sản. khỏng nên bắt đầu sử dụng nevirapine trừ khi lợi ich vượt
trội nguy co. Chưa rõ iiệu thai sản có lảm tãng nguy cơ được ghi nhận ở phụ nữ không có thai
hay không.
Chỉ sử dụng VIRAMUNE XR trong thai kỳ nếu iợi ích cao hơn nguy cơ đổi với thai nhi.
Đủng hỷ lhai sán dùng Lhuốc kháng retrovirus
Dáng ký thai sân dùng thuốc kháng retrovirus đã được thỉết 1ập nhằm theo dõi ảnh hướng trên
mẹ vả thai nhì ở phụ nữ mang thai sủ dụng VIRAMUNE giải phóng nhanh vả VIRAMUNE
XR. Bác sĩ được khuyến khích đâng kí cho bệnh nhân qua điện thoại tới số (800) 258-4263
Phụ nữ cho con bú
Trung tâm Kiềm soât vi Phòng ngừa Bệnh (CDC) khuyến cảo bệnh nhân nhiễm HIV-l
không choconbú đễ trảnh n y cơ liy nhiễm HIV- ! an sinh. Nevirapine bii tiết qua
x-L iL`1ĩ ~i ,i'i Li: `41Ạ'; '~J_v1i " _i’ni'
Ảnh 11 trẻ i nin 1ii e vi vân hânh má
Chưa có các nghiên cứu riêng biệt về khả năng 1ái xe và vặn hảnh máy. Tuy nhiên, nên lưu ý
bệnh nhân về các tác dụng phụ có thể gặp phải khi điều trị với VIRAMUNE. chắng hạn mệt
mỏi. Vi vậy, cần thận trọng khi lái xe hoặc vặn hânh máy. Nếu cảm thấy mệt mòi, bệnh nhân
cần tránh các oông việc có khả năng găy nguy hiếm như lái xe hoặc vặn hảnh máy.
Ịảc dung ghu
Kinh nghiệm từ thử nghiệm lâm sing
Do các thử nghiệm lãm sảng được tiến hảnh ttong điều kiện khác nhau, ti lệ phân ủng có hại
ghi nhận trong un: nghiệm lâm sâng của một thuốc không mẻ được so sánh trực tiếp với tỉ lệ
trong thử nghiệm Iám sáng của một thuốc khác và có thể không pth ánh đủng tỉ lệ ghi nhận
trong thực hùnh lãm sảng.
Phản ửng ngoại ỷ nghiêm trọng nhất liến quan đển nevirapine lá viếm gan. suy gan, hội chứng
Stevens-Johnson, hoại tử biền bi nhiễm độc vớ phán ứng quá mẫn.
Viêm ganlsuy gan có thể ríêng lẻ hoặc đi kèm với các đấu hiệu của quá mẫn bao gồm phảt ban
nặng hoặc phát ban đi kèm với sốt, khó chiu, mệt mỏi. nhức cơ hoặc khớp. rộp da, tổn thương
miệng, viêm kết mạc, phù mặt, tãng hạch cẩu ái toan, giảm bạch cẩu hạt, hạch to hoặc rối lọan
chức nãng thận [xem Cánh bảo dậc biêl vả !hăn Irọng].
Độc tính lâm sảng phổ biến nhất của nevirapine lả phảt ban, có thể nặng h0ặc đe dọa tỉnh mạng
[xem Cảnh bảo đặc biẽt vả Lhăn trọng]. Phát ban xuất hiện thường xuyên nhất trong vòng 6
tuần đầu điều tri. Phát ban thường ở mủc độ nhẹ tới trung binh, dạng dát sần có hoặc khỏng
ngửa, xuất hiện tại thân. mặt vù các chi.
cơ sở dữ liệu về độ an Loi… trong thử nghiệm lãm sảng của VIRAMUNE xa bao gồm dữ liệu
tử 800 đối tượng điều ni với VIRAMUNE XR vả 654 đối tượng điều trị với VIRAMUNE giải
phóng nhanh,
Thử nghiệm 1100.1486 (VERx VE)
Trong thử nghiệm 1 100.1486 (VERxVE). bệnh nhân trước đó chưa được điều trị được sử dựng
liều dẫn đầu VIRAMUNE giâi phỏng nhanh 200 mg một lấn mỗi ngèy trong 14 ngảy (n=1068)
và được phân nhỏm ngẫu nhiên sử dụng VIRAMUNE giải phóng nhanh 200 mg hai lần mỗi
ngảy (n=506) Lioạc VIRAMUNE xa 400 mg một lẩn mỗi ngáy (n=505). Tẩt cả các đối tượng
đều được điều trị nền bằng tenofovir + cmtricitabínc. Các đổi tượng tham gia có sổ luợng tể
bâo CD4+ dưới 250 bâ:ưmm² ớ nữ giới vả dưới aoo bớnlmm² ớ nam giới [xem Chổng chỉ
định]. Trong Lhứ nghiệm náy,đữ liệu về triệu chứng tiểm tảng của các biến cố gan đuợc thu
thặp tiển cứu. Dữ liệu về an toản bao gồm tất cả cảc iần khám bệnh tính đến thời điềm hoân tất
của dỏi tượng cuối cùng đối với tiếu chi chinh 48 tuấn trong thử nghiệm (thới gian ghi nhận
ưung binh là 61 tuần).
Sau giai đoạn dẫn đầu, tỉ lệ xuất hiện biến cố gan bất kỳ lẻ 9% ở nhóm sử dụng VIRAMUNE
giải phóng nhanh vả 6% ớ nhỏm sữ dựng VIRAMUNE xa; tỷ lệ xuái hiện các biển cố triệu
chửng ở gan (chán ãn, vảng da, nôn) tượng ủng là 3% vả 2%, Tỷ lệ có ALTIAST tăng mửc độ
3 hoặc 4 Là 1% ở nhóm sử dụng VIRAMUNE giâi phỏng nhanh vả 6% ớ nhỏm VIRAMUNE
xa. xa tổng thế, tỷ lệ xuải hiện biến cố triệu gan chửng cùa nam giới và nữ giởi tham gia thứ
nghỉệm VERxVE lả tương đương.
Phát ban nặng hoặc đe dọa tinh mạng được cho lả liên quan đến việc sử dụng nevirapine xảy ra
ớ w… đối tượng trong giai đoạn dẫn đằu với VIRAMUNE giLi phóng nhanh vả ớ … đổi tượng
cùa mỗi nhỏm điều trị trong giai đoạn chia ngẫu nhiên. Ngoùi ra, 5 trường hợp bị hội chứng
Stevens-Johnson đã được ghi nhận trong thử nghiệm vả đểu xáy ra trong vòng 30 ngây điều ui
đẫu tiên với ncvirapim.
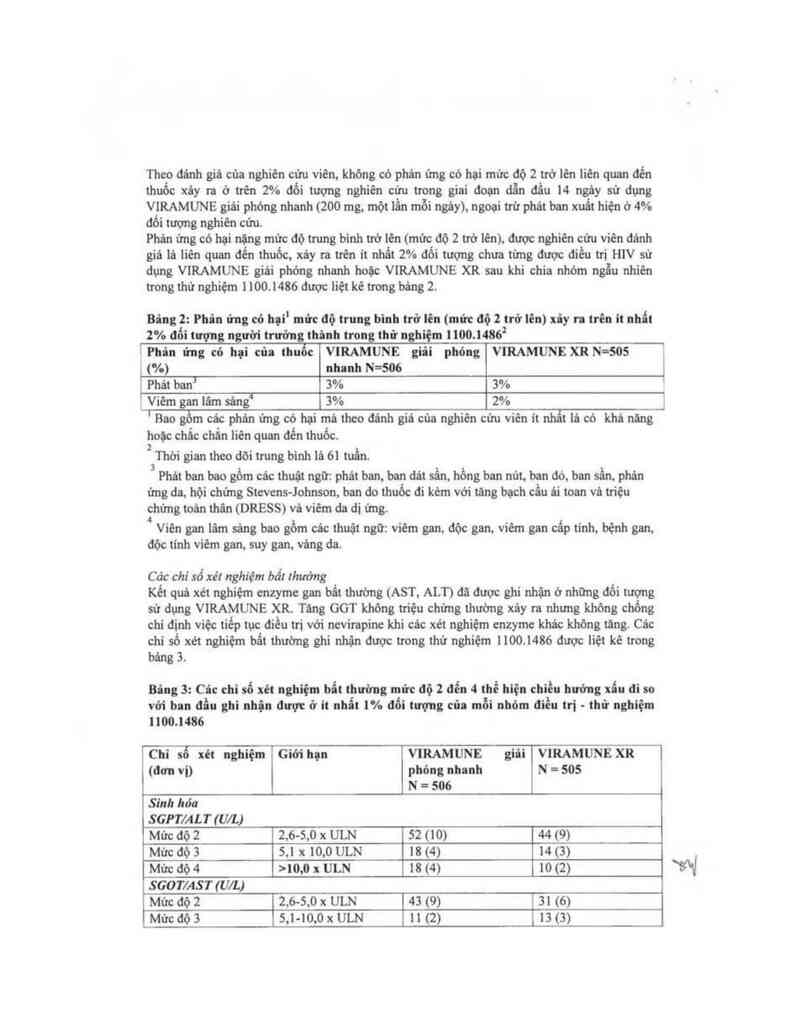
Then đảnh giá cùa nghiên cứu viên. không có phân ủng có hại mức độ 2 trở lên liên quan đển
thuỏc xảy ra ở trên 2% đối tượng nghiến cứu trong giai đoạn dẫn đẩu 14 ngây sữ dụng
VIRAMUNE giâi phóng nhanh (200 mg, một lần mỗi ngáy). ngoại trừ phát ban xuất hiện ớ 4%
đối Lượng nghiên cứu.
Phản ửng có hại nặng mức độ trung binh trở lên (mức độ 2 trở lên), được nghiên cứu viến đánh
giá iả liên quan đển thuốc, xảy ra trên it nhẩt 2% đổi tượng chưa tùng được điểu tri HIV sử
dụng VIRAMUNE giải phóng nhanh hoặc VIRAMUNE XR sau khi chia nhóm ngẫu nhiên
trong thử nghiệm 1 100.1486 đuợc iiệt kế trong bảng 2.
Bâng 2: Phản ứng có hạiI mửc độ trung binh trở lên (mức độ 2 trở 1ẽn) xiy ra trên it nhất
2% đối tượng_n_gười trưởn
thânll trong thử nghiệm LLoo.Lớsớ²
1 Phân ửng có hại cùa thẫốc
("lo)
VIRAMUNE gũi phỏng
nhanh N=506
VIRAMUNE XR N=505
i
Phát me
3%
3%
Viêm gan lâm sângI
3%
2%
' Bao gồm các phản ứng có hại mả theo đánh giá cùa nghiên cứu viên ít nhẩt lá có khả nảngg
hoặc chẳc chắn liên quan đến thuốc.
² Thời gian theo dỏi trung binh lả 61 tuấn.
3 Phát ban bao gồm các thuật ngữ: phát ban, ban dảt sấn, hồng ban nút, ban đò. ban sẩn. phán
ửng da, hội chứng Stevens—Johnson, ban đo thuốc đi kèm vởi tăng bạch cằu ải toan vả triệu
chứng toản thân (DRESS) vá viếm dn đi ửng.
. Viên gan lâm sảng bao gồm các thuật ngữ: viêm gan, độc gan, viêm gan cấp tinh. bệnh gan,
độc tinh viêm gan, suy gan. vảng da.
Cảc chí số xét nghiệm bất Lhướng
Kểt quả xét nghiệm cnzyme gan bẩt thường (AST, ALT) dã được ghi nhặn ở những đổi tượng
sử dựng VIRAMUNE XR. Tăng GGT không triệu chứng thường xáy ra nhưng khòng chổng
chi đinh việc tiếp tuc điều trị với nevirapine khi các xét nghiệm cnzyme khác khỏng tăng. Các
chỉ số xét nghiệm bẩt thường ghi nhận được trong thử nghiệm 1100.1486 được liệt kê trong
bảng 3.
Bâng s: Câc chỉ số xét nghiệm bất thường mức aớ 2 đến 4 thể hiện chiều hướng xin đi lo
vởi L…. đẫn ghi nhận được ở it nLifii … đối tượng của mỗi nhỏm diều tri . thử nghiệm
1100.1486
Chỉ số xét nghiệm Giới hạn VIRAMUNE giâi VIRAMUNE XR
(dơn vi) phỏng nhanh N = 505
N = 506
SInIL hóa
SGPT/ALT (U/L)
Mức độ 2 2.6-5.0 x ULN 52 (10) 44 (9)
Mức độ3 5,1 x 10,0 ULN 18(4) 14 (3)
Mức độ 4 >10,0 x ULN 18 (4) 10 (2)
SGOT/AST (U/L)
Mức độ 2 2.6—5,0 x ULN 43 (9) 31 (6)
Mức độ 3 5.1-10,0 x ULN 11 (2) 13 (3)
Mức độ4 [›L0,0xULN [10(2) Ỉ7U)
BíIírubin Ioăn phẫn (mg/dL)
Mửcđộ2 l.6-2,5xULN 2(<1) 4(1)
Mức độ 3 2.6-5,0 x ULN 3(1) 3(1)
Mức độ4 >S.Ox ULN 1(<1) 5(1)
Alkaline Phosphatau (U/L)
Mức độ 2 2.6—5,0 x ULN 18 (4) 11 (2)
Mức độ3 5.1-10,0xULN 1(<1) 4(1)
Mức độ 4 >10.0 x ULN 0 0
Huyết học
Bạch cẩu trung tỉnh
Mức độ 2 750-999/mm3 33 (7) 22 (4)
Mức độ 3 500-749lmm3 13 (3) 8 (2)
Mức độ 4 <5001mm3 3 (l) 2 (<1)
Lipid
LDL (mgẻdL)
Mức độ2 160—190mịdL 66(13) 66(13)
Mức độ 3 >190_mgldL 21 (4) 20 (4)
Cholesterol (mg/dl.)
Mức độ 2 240—300 mgldL 81 (16) 83(16)
Mửc độ 3 >300 mgldL 14 (4) 9 (2)
Triglycerỉde (mg/dL)
Mức độ 2 500-750 mgldL 10 (2) 15 (3)
Mứcđộ3 751-1,200 mg/dL 9(2) 4(1)
Mức độ4 >1,200 mg/dL 1 (<1) 2(<1)
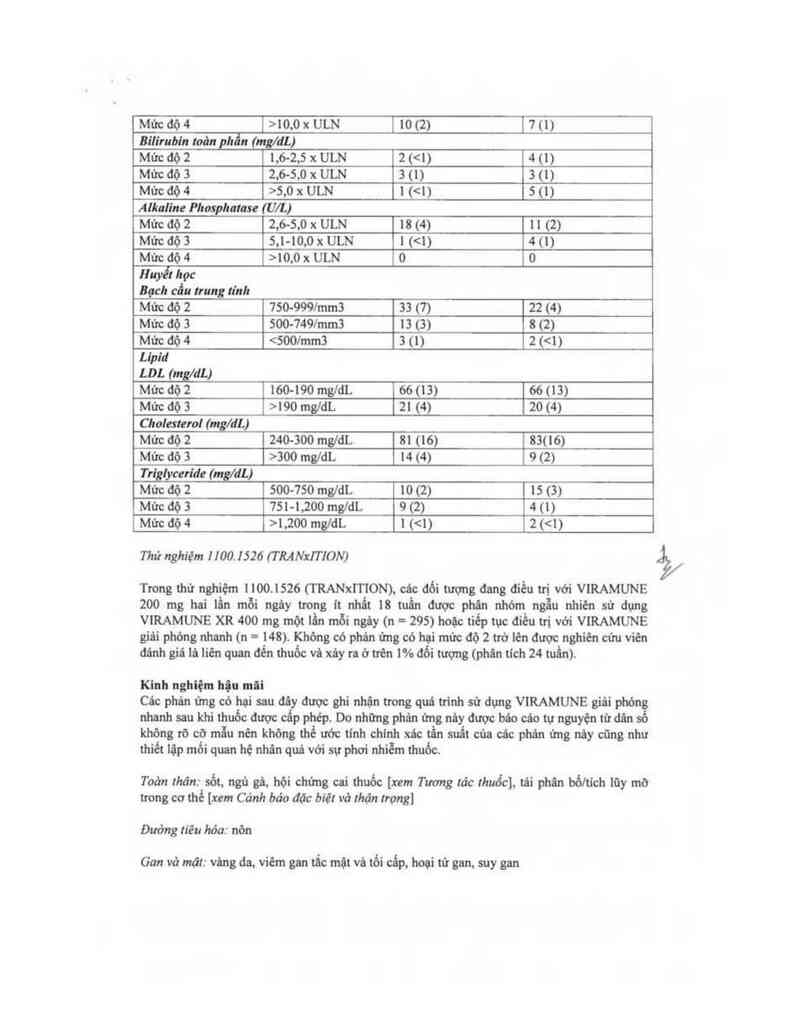
Thử nghiệm ] l00. I526 (T RAleT ION)
Trong thử nghiệm 1100.1526 (TRANxI'I'ION). cảc đối tượng đang điếu trị với VIRAMUNE
200 mg hai 1ấn mỗi ngảy trong ít nhất 18 tuần được phán nhóm ngẫu nhiên sử dụng
VIRAMUNE xa 400 mg một lẩn mỗi ngây (n = 295) hoặc tiếp tục điều trị với VIRAMUNE
giải phớng nhanh (n = 148). Không có phân ứng có hại mức độ 2 trớ Ièn được nghiến cứu viên
đánh giá lù Iiên quan đến thuốc vả xảy ra ớ min … đối tượng (phân tích 24 tuấn).
Kinh nghiệm hặu mii
Các phán ứng có hại sau đây được ghi nhặn trong quá trinh sữ dụng VIRAMUNE giải phóng
nhanh sau khi thuốc được cấp phép. Do những phản ửng nây được bớo các tự nguyện từ dân số
khỏng rõ cớ mẫu nên khỏng thể ước tính chinh xâc tẩn suất của các phân ứng nây cũng như
thiết lập mổi quan hệ nhân quả với sự phơi nhiễm thuốc.
Toản thản: sới, ngủ gả, hội chứng cai thuốc [xem Tuưng !ảc !huổc]. tái phân bổltich lũy mớ
trong cơ thể [xem Cảnh băo đặc biệt vù Lhặn Lrọng]
Đường liêu hóa: nỏn
Gan vã mải: vâng da, viêm gan tắc mật vả tối cấp. hoại tử gan, sưy gan
Huyết học: thiếu mảư. tâng bạch cầu ải toan, giảm bạch cầu trung tinh
Xét nghiệm: giảm phospho huyết thanh
Cơ xương: Đau khớp, hứy cơ vãn kèm phán ứng da vâlhoộc gan
Thấu kính: dị cảm
Du vả phần phụ: phản ửng đi ứng bao gồm phản ứng giống phản vệ. phù mạch, nồi bỏng nước.
viêm miệng gây loét vả mề đay đã được báo cảo. Ngoèi m, hội chứng quả mẫn vả phản ứng
quá mẫn đi kèm với phát ban vả cảc đấu hiệu toán thân như sổt, rộp da, tồn thưong miệng.
viêm kết mạc, phù mặt. đau Cơ hoặc khớp, khó chiu. mệt mòi hoặc bất thuờng gan đáng kể
[xem Cánh báo đãc biệt vả Ihận Lrọng] củng với một hoảc nhiều tác dụng phụ sau: viêm gan.
táng bạch cầu ải i…. giâm bạch cầu hạt. nổi hạch vả/hoặc rối loạn chức náng thận đã được
báo cảo.
Thông báo cho bác sĩ cđc tăc dụng phụ gặp phăi khi dùng II: uốc.
QuáJiềz
Chưa cớ thuốc giâi độc cho quá liễu nevirapine. Các truờng hợp quá Lièu VIRAMUNE giải
phỏng nhanh ở khoáng 1iểu từ 800 đển 1800 mg mỗi ngây, sử dụng trong 15 ngảy đã được báo
cảo. Bệnh nhân gặp phâi các biển cổ như phù, hồng ban nủt. mệt mòi, sổt. đau đầu, mất ngủ.
buồn nôn. thâm nhiễm phồi, ban ớớ. chóng mặt. nôn vả giảm cân. Tẩt cả các biển cố giâm nhẹ
sau khi ngùng VIRAMUNE giải phỏng nhanh.
mc diển: duv_n lý hgc
Cơ chế Lác dụng
Nevirapine lả một thuốc ức chế mcn sao chép ngược không nucleoside (NNRTI) của HIV-l.
Nevirapine gắn trực tiểp vảo mcn sao chép nguợc vả ức chế tảc dụng của poiymcrase phụ
thuộc RNA vả polymcrase DNA phụ thuộc DNA bằng cách phá vỡ vi tri xúc tác cùa men Tác
dụng của nevirapine không phâi do cạnh ưanh với khuôn mẫu (temp1ate) hoặc các nucleoside
triphosphate. Men sao chẻp ngược HIV-2 vả các polymerasc DNA eukaryotic (như DNA-
polymcrase u, 0. 1 hoặc 6 ở ngưới) không bị ửc chế bởi nevirapine.
Tác dụng kháng virus
Tác đụng kháng virus của ncvirapinc đã được xác đinh trong một loạt các dòng tế bảo bao gồm
các tế bèo đơn nhân ở máu ngoại vi. đại thực bảo nguồn gổc bạch cẩu đon nhân, vả tế bảo dạng
nguyên bảo lympho. Trong nhũng nghiên cửu gần đãy sử dụng tế bảo Lhặn phôi thai người mã
số 293. giá ưi EC50 (nồng độ ửc chế som cùa nevirapine lả 90 nM đổi với 2932 chùng HlV-l
phân lặp tự nhiên mã trong đó chủ yểu lá các chủng phân lặp trên lâm sâng từ nhỏm B tại Mỹ.
Trong thử nghiệm náy. giá trị EC50 phân vị thứ 99 lẻ 470 nM. Giả tri EC50 trung vị lả 63nM
(khoảng từ 14—302 nM. n=29) đối với các chủng phân lập lâm sâng cùa HIV-l từ iớp A. B. C.
D. F, G. H vả dạng lưu hảnh tái tổ hợp CRFOi_AE, CRFOZ_AG and CRF12_BF . Nevirapine
không có tác dụng kháng virus trong nuôi cấy Lẻ bâo đới với các phân 1ập HIV—I(n=3) vả mv-
2 từ nhóm 0 tải tẹo trong tế bảo đơn nhản máu cuống rốn. Nevirapine kết hợp với efavirenz
thế hiện tác đụng đối kháng mạnh với kháng HIV-1 trong nuôi cẳy tế bâo vả bổ sung tác đụng
đối kháng với thuốc ửc chế protease lả ritonavir, hoặc chất ức chế chung enfuvirtidc.
Nevimpine có tảc dụng hiệp đổng kháng HIV-1 khi phối hợp với thuốc ức cbế proteesc như
ạmprcnavir, atazanavir, indinavir, lopinavir, nelfinavir, saquinavir vả tipranavir; vả cảc thuốc
NRTI như abacavir, đidanosine, emtricitabine, 1amivudine, stavuđỉne, tenofovir vả zidovudine.
Tảc dụng kháng HIV—l cùa nevirapine bị đối kháng bời thuốc kháng viêm gan B (HBV)
adefovir, và thuốc kháng vỉếm gan C (HCV) ribavirin trong nuôi cấy tế bảo.
Để khảng
Trong nuôi cẩy tế bảo, đã xuất hiện các phân lập HIV giảm nhạy cảm với nevirapine (từ 100-
250 lần ). Phân tích kiếu gen cho thẩy sự đột biến trong gen HIV-l R'I` mã YI8IC vảfhoặc
V106A phụ thuộc vảo chùng virus và dòng tế bảo đã dùng. Thời gian xuất hiện sự đề kháng
nevirapine trong nuôi cấy tế bảo không bị thay đổi khi chọn nevirapine kết hợp với nhiều
NNRTI.
Sự thay đổi kiểu gen và kiến hỉnh trong cảc phân lập HIV-l từ những bệnh nhân trước đó chưa
điều trị HIV sử dụng nevirapine (n=24) hoặc ncvirapine + ZDV (n=l4) được theo dõi trong cảc
thử nghiệm pha IlII tứ ] đển 2 12 tuần. Sau một tuần đơn trị liệu với nevirapine, phân lập HIV-
] từ 3l3 bệnh nhân đã thấy giảm nhạy cảm đối với nevirapine trong nuôi cấy tế bảo. Một hoặc
nhiều đột biến gen RT tại axit amin vị trí K103N, V106A, V1081, YISIC, Y188C vả Gl9OA
được phát hiện trên các chùng HIV—l phân lập từ vải bệnh nhân ngay 2 tuần sau khi bắt đầu
điều ni. Tại thời điếm 8 tuần đơn ni liệu với VIRAMUNE, 100% bệnh nhân thử nghiệm
(n=24) có phân lập HIV giảm nhạy cảm với nevirapine trong nuôi cấy tế bảo › 100 lần so với
ban đầu, và có một hoặc nhiến đột biến gen RT khảng ncvirapinc. 19 bệnh nhân (80%) có phân
lập dột biến gen ớ vị ni Y181C không liên quan đển 1iểu dùng.
Phân tich kiến gen cùa các phân lập từ những bệnh nhân chưa được điều trị với khảng
retrovirus có tải xuất hiện virus (n=7l) dùng nevirapine 1 lần/ngảy (n=25) hoặc 2 lần/ngảy
(n=46) kểt hợp với 1amivudine vả stavudinc (nghiên cứu 2NN) trong 48 tuần cho thẳy phân 1ập
trên 8/25 bệnh nhân và 23/46 bệnh nhân, tương ứng, có một hoặc nhiếu gen đột biến liên quan
đến kháng thuốc NNRTI bao gổm: Y181C, KLOLE, Gl9OA/S, KlO3N, V106A/M, VIOSI,
Y] 88C/L, A9SG, F227L vả M230L.
Trong thử nghiệm 1100.1486, phân tich kiến gen đã được tiến hânh trên chùng phân lập ban
đầu và trong quá trinh điếu trị lần lượt từ 23 và 34 bệnh nhân có xét nghiệm virus thất bại lần
lượt trong nhóm điểu ni bầng VIRAMUNE XR vả VIRAMUNE giải phóng nhanh. Đột biến
khảng nevirapine xuất hiện trong các chùng phân lập trong khi điều trị trong số 78% (18123)
bệnh nhân nhóm điều trị với VIRAMUNE XR có xét nghiệm virus thẫt bại và trong số 88%
(30/34) bệnh nhân nhỏ… điểu trị với VIRAMUNE giải phóng nhanh. Đột biến khảng
nevirapine tại vị trí Yl8lC xuất hiện riêng lẻ hoặc cùng với các dột biến khảng nevirapine tại
vị trí khảo (KIOIE, 1(103N, V106A, V1081, Y188 C/F/H/L/N, GI9OA, P225H, F227L,
M2301.) đã được tìm thẳy trong các chủng phân lập từ 14 bệnh nhân thất bại điều trị với
VIRAMUNE XR và 25 bệnh nhân thất bại điều trị với VIRAMUNE giải phóng nhanh. Đột
biến acid amin mới tại vị trí Y1811 đã xuất hiện ở cảc chùng phân lập trong quá. trình điều trị từ
1 bệnh nhân nhóm điều trị với VIRAMUNE XR vả đột biến acid amin mới tại vị trí Y188N đã
xuất hiện ớ cảc chủng phân lập từ bệnh nhân khác nhóm điều ni với VIRAMUNE giải phóng
nhanh. Phân tich kiểu hình cho thấy đột biến tại vị trí Y188N vả Y1811 tương ứng dẫn tới giảm
nhạy câm với nevirapine 103 lần và 22 lần.
Dế kháng chéo
Đã thẩy sự xuất hiện nhanh chỏng của các chủng HIV đề kháng chẻo với cảc thuốc ửc chế men
sao chép ngược khỏng nucleoside (NNRTI) trong nuôi cấy tế bảo. Các chủng phân lập HIV—l
kháng nevirapine đề kháng chéo với các thuốc ưc chế men sao chẻp ngược dclavirđinc vá
cfavirenz.
Dữ liệu đề kháng chéo giữa NNRTI nevirapine vả các thuốc ức chế RT nhỏm nucleoside còn
rất hạn chế. Trên 4 bệnh nhân, các phân lập để khảng zov in vítro vẫn ihè hiện sự nhạy cám
với ncvirapine vả trên 6 bệnh nhân, cảc phân lặp đề khảng nevirapine vẫn nhạy cảm với ZDV
vả dd]. Để kháng chẻo giũa nevirapine vâ cảc thuốc ức chế protease HIV thường không xảy ra
do các đich enzyme 1ả khác nhau. Đột biến tại vị trí Y188N dẫn tới giảm nhạy câm với
dclavirdine vả efavircnz lần lượt 22 lẩn vả 7 lần nhưng không giảm nhạy câm với etrnvirine.
Tương tự đột biển tại vi tri Y1811 lâm giảm nhạy cảm với đeiavirdine vả cưavirinc 1ần iượt 3
lần và 8 1ẩn nhưng không lảm giảm nhạy cảm với cfavirenz. Tuy nhiên, các chủng kháng
nevirapine nhạy cảm với NRTI dd! vả ZDV. Tương tự các chủng kháng ZDV nhạy cám với
ncvirapinc trong nuôi cấy tế bảo.
Dm độ ng ỈIE
Người Ión
Hấp thu vả sinh khả digig
Dược đỏng học của liều đơn VIRAMUNE xa đã được nghiên cứu ưên 17 người tinh nguyện
khỏe mạnh. Nevirapine được hấp thu với t.… trung binh khoảng 24 giờ. C,… ưung binh vả
AUCna của nevirapine tương ửng lả 2060 nglmL vả 161.000 ng.giờlmL. Sinh khả dụng tương
đối của 400 mg VIRAMUNE XR so với 400 mg VIRAMUNE giâi phỏng nhanh khoảng 75%.
Duợc động hợc đa 1iểu cùa VIRAMUNE XR đã dược nghiên cứu trên 24 bệnh nhân nhiễm
HIV-1 chuyển từ điều ưi dải ngảy bằng VIRAMUNE viên giâi phỏng nhanh sang
VIRAMUNE XR. AUCớua vả C… ưung binh cùa ncvirapine sau 19 ngây uống lủc đói
VIRAMUNE XR lả 82.000 ng.giờJmL vả 2920 nglmL. AUCMỦ vả C....u cùa nevirapine khi
uống VIRAMUNE xa vâo lủc no lần lượt lả 96.700 ng.giờ/mL vá 3150 nglmL. Sinh khả dụng
tường đối của 400 mg VIRAMUNE XR so với 400 mg VIRAMUNE giải phóng nhanh trong
điểu kiện đỏi vả no tương ứng lá 80% vả 94%. Sự khác biệt về sinh khá đụng của ncvirapine
khi sử đụng VIRAMUNE vâo thời điểm đói hoặc no được cho lả khỏng có ý nghĩa lâm sảng.
VIRAMUNE XR có thể uống củng hoặc khỏng cùng thức ãn.
Eiấlthbấi
Nevirapine có ải lục cao với lipid vả không bị ion hóa ưong mỏi trường pH sinh lý. Thể tich
phân bố (Vdss) của nevirapine ở người trướng thânh, khóc mạnh sau khi dùng đướng tĩnh
mạch lả 1, 21 * 0.09 leg, cho thấy nevirapine phân bố rộng ưong cơ thể người. Nevirapine
vượt qua hâng rảo nhau thai thai chóng vá được tim thẩy ưong sữa người mẹ [xem Sử dụng
Lrên dân số đác biệt]. Khoảng 60% nevirapine gắn với protein huyết tương và nồng độ thuốc
trong huyết tương nằm trong khoảng 1 — 10 mcg/mL. Nổng độ ncvirapine trong dich não tủy
người (n=6) bằng 45% (15%)nồng độ thuốc trong huyết tương; tỷ lệ nảy gần bằng tỷ lệ thuốc
không gắn với protein huyết tương.
Chuỵến hóaỉThải tn“:
Cảc thử nghiệm In vivo tiển hảnh trên người vả thử nghiệm in vitro tiến hảnh tLến microsome
gan người cho thẩy nevirapine chuyến hóa mạnh qua cytochrom p450 (oxy hóa) thảnh cảc chất
chuyền hoá hydroxyl hỏa. Các nghiên cứu In vitro trên microsome gan nguời cho thấy chẩt
chuyền hóa oxy hóa của nevirapine chủ yếu qua ưung gian cytochrom P450 (CYP) từ nhóm
isozym CYP3A vả CYP286 mặc đủ các isozym khảc có thể đóng vai trò thứ yếu. Trong một
thử nghiệm về thải trứ cân bằng khổi lượng tiến hảnh ưên 8 người tinh nguyện nam khỏe
mạnh. đối tượng tham gia được sử dụng VIRAMUNE 200 mg hai lần mỗi ngảy cho đến trạng
thái ốn đinh, sau đó sử đụng một liểu đơn so mg ncvirapine đánh dắu c“_ khoảng 91,4 i
Lo.sơxớ lìểu đảnh dẩn phóng xạ được tim thấy, tỷ lệ tim thấy trong nước tiến (8.3 c 11,1%) cho
thấy đây là con đường thái trù chinh so với phân (10,1% 1 1.5%). Hơn 80% hoạt tính phóng xạ
trong nước tiền 111 đo liẻn hợp glucuronidc của câc chất chuyền hớn hyđroxyl hóa Con đường
chuyến hóa qua P450, 1ién hợp glucuroniđc vả thải trừ các chất chuyền hóa glucuronid hớn qua
thận cho Lhẩy con đường chuyển đạng sinh học và thải trừ chinh của nevirapine ở người. Chỉ
một phần nhỏ (đưới 5%) hoạt tinh phóng xạ được tim thấy trong nước tiều (đại điện cho đưới
3% tổng liếu) tạo ra bới hoạt chất gốc; vi thể, con đường thâi trứ qua thận đóng vai trò nhỏ
trong thải trừ hoạt chất gốc.
Nevirapine là chất gây cảm ứng của cảc enzym chuyển hóa cytochrome P450 3A vả 286 cùa
gan. Kết quả xét nghiệm crythromycin trong hơi thờ và chất chuyển hóa trong nước tiều cho
thấy ncvirapinc cám ứng khoảng CYP3A vả CYP2Bó. Cảm ứng tự động con đường chuyền
hóa qua trưng gian CYP3A vớ CYP286 đẫn đến độ thanh thải biếu kiến của ncvirapinc tăng
khoáng 1,5 - z iần khi điều ưi 1iên tục chuyển từ một liều đơn sang liều VIRAMUNE giải
phóng nhanh 200—400 mglngảy ưong 2-4 tuần. Câm ửng tự động cũng dẫn đến giảm thời gian
bán thải pha thải trừ của nevirapine trong huyết tương từ khoáng 45 giờ (liều đơn) xuống
khoảng 25-30 giờ sau khi dùng đa
1iều zoo-mo mglngảy.
Dân số đặc biệt
Suỵ thân
Trong một thử nghiệm về dược động học, cảc bệnh nhân có huyết thanh âm tinh với HIV-l bị
suy thặn nhẹ (CrCL 50—79 mUphủt; n=7), ưung bình (CLCL 30—49 mllphủt; n=6) hoặc nặng
(CrCL dưới 30 mUphủt; n=4) được sử dụng một liều đon 200 mg VIRAMUNE giải phóng
nhanh. Những bệnh nhân náy chưa cằn lọc thận. Ngoái ra, thử nghiệm bao gồm 6 bệnh nhân
suy thận cấn lọc thận. Dược động học cùa nevirapine ớ nhũng bệnh nhân suy thặn (nhẹ, trung
binh hoặc nặng) thay dồi không đáng kể. Tuy nhiên. AUC cùa nevirapine ở những bệnh nhân
cần lọc thận giâm 44% sau 1 tuần sử đụng thuốc. Chưa có bằng chứng về sự tích lũy chất
chuyển hóa hyđroxy của ncvirapine trong huyết tương bệnh nhân cần lọc thận. Một liểu bổ
sung 200 mg VIRAMUNE giái phóng nhanh được chi đinh sau mỗi đợt lọc máu. [xem Líểu
lượng vả cảch dùng]. VIRAMUNE XR chưa được nghiến cứu trên bệnh nhản rới Ioạn chức
nãng thận.
Suỵ gan
Trong một thử nghiệm ở trạng thái đừng so sánh 46 bệnh nhân bị xơ gan nhẹ (n=17; lan tòa
trên một số khoảng cữa. chỉ số Ishak 1.21, ưung binh (n=20; lan tòa trến hầu hết các khoảng
cừa có thế có vách xơ nổi cừa-cừn, cứa-trung tâm; chỉ số ishack 3—4) hoặc nặng ( n=9, vảch xơ
đáng kẻ có thể bị chai gan không mẩt bù tương ứng Child—Pugh A; Chỉ số lshak 5—6), dược
động học đa liếu cùa nevirapine vả 5 chắt chuyển hóa oxy hóa của nó không bị ânh hướng Tuy
nhiên, khoảng 15% bệnh nhân xơ gan có nồng độ đáy ncvirapinc trên 9000 mcg/mL (cao gấp 2
lần nồng độ đảy binh thường). Vì vậy, cản theo dỏi cẩn thận bệnh nhân suy gan đề phát hiện
bằng chứng độc tính do thuốc [xem Cảnh báo dặc biệt vò Lhản Lrọng].
Trong một thử nghiệm dược động học. bệnh nhân chai gnn âm tinh với HIV-l bị suy gan nhẹ
(Child—Pugh A; n=6) hoặc ưung binh (Child-Pugh B; n=4) sử dụng một liều đon 200 mg
VIRAMUNE giâi phóng nhanh, mủc tăng đảng kể AUC của ncvirapinc đã được ghi nhặn ờ
một bệnh nhân có Chiid-Pugh B vả cổ chướng cho thấy những bệnh nhân cớ chức nâng gan
xấu đi và cố chướng có thể có nguy co tich iũy nevirapine trong hệ tuần hoán. Do ncvirapine
kich ứng chẳt chuyến hóa của nó khi dùng đa iiều nén thừ nghiệm đơn liểu có thể không phản
ảnh ảnh hướng của suy gan iên dược động học đa 1iẻu.
Không sử dng nevirapine cho bệnh nhân suy gan ưung bình hoặc nặng (Child-Pugh phân loại
B hoặc C [xem Chổng chỉ định. Cánh báo đđc biệt và rhặn trọng}. VIRAMUNE XR chưa được
đảnh giá trén bệnh nhân suy gan.
Giới tính
Nữ giới có mẹ thanh ihới nevirapine thấp hơn 13,8% so với nam giới. Do cả khối lượng cơ thể
vả chỉ số khối cơ ihẻ (BMI) đều ảnh hướng đến độ thanh thải cùa ncvirapinc nẽn ảnh hướng
cùa giới tính không thể giải thích đờn thuần bắng kich thước cơ mè.
Bệnh nhân nữ có xu hướng có nồng độ đáy cao hơn (khoảng 20.30%) ở cả hai nhóm
VIRAMUNE giải phóng nhanh vù VIRAMUNE giái phóng chậm.
Qhùng tôc
Sự Liing nồng độ ncvirapinc trong huyết tương (dữ liệu gộp từ một số thử nghiệm lâm sảng) ở
bệnh nhân nhiễm HIV-l (27 người da đen, 24 người Mỹ gổc Tây ban nha, 189 người đa trắng)
không cho thấy khác biệt đáng kể trong nồng độ đảy của nevirapine ở trạng thái ốn đinh (C...-um
trung vị = 4.7 mcglml. ở người da đcn. 3,8 mcglml ở người Mỹ gốc Tây Ban Nha, 4.3 mcg/mL
ở người đa trắng) khi điều trị đâi ngảy với VIRAMUNE giải phỏng nhanh liều 400 mglngảy.
Tuy nhiên ảnh hướng của chủng tộc Iẽn được động học của ncvirapinc khỏng được đánh giá
riêng biệt.
Trong thử nghiệm 1100.1486, bệnh nhân da đcn (n=80 ngườilnhỏm) cho thắy nổng độ đây cao
hơn bệnh nhân da trắng (250-325 ngườilnhỏm) khoảng 30% ở cá hai nhóm VIRAMUNE giải
phóng nhanh vả VIRAMUNE xa sau 48 tuần điểu ưi với liễu 400 mglngảy.
Ẹênh nhân Lớn tuồi
Dược động học của ncvirapine ở những bệnh nhân người lớn nhiễm HIV-l dường như không
thay đối theo tuổi (phạm vi từ 18—68 tuồi); tuy nhìến, nevirapine chưa được đánh giá rộng rãi
ưến bệnh nhân từ 65 tuồi trở lên.
Nhìn chung, phơi nhiễm thuốc ở trẻ em tương tự như ghi nhận ở người lớn sử dụng
VIRAMUNE XR.
Cảc chẩt không hoạt tinh của VIRAMUNE viến giái phóng chặm đôi khi sẽ được bải tiết ưong
phân dưới dạng cảc chất mềm hydrat hóa.
Đóng gỏi
Chai 30 và 90 vién giâi phóng chậm.
Bâo guâg
Dưới 30°C.
Ẹnn đùgg
24 tháng.
Sản xuất bới
Boehringer Ingelheim Roxane Inc,
Columbus, OH 43228, USA Jvỳ
Thuốc bán theo đơn.
Đọc kỹ hướng dẫn sữ đụng trước khi dùng.
Hỏi ý kiến bác si nếu cần them thông tin.
Bâo quân nơi an toân, ngoái tầm với cũa trẻ.
,,22 Mar JroLg
chiM ,X Awi'fcank
11 “W
^ Boehringer
Liiil Ingelheim
Boehringer lngelheỉ … ' `ử'
i~:…zó cục TRUỞNG
" Ẩ fi 'lV If Ồ
Ji rz.f:.jrs n Ấ’cèii Ểwian »
(1 o
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng