









PARTICULARS TO APPEAR ON THE OUTER PACKAGING Z nlB W
CARDBOARD BOX
BỘ Y TẾ
CỤC QL'AN LÝ DƯỢC
ĐA PHÊ DUYỆT
n…:
.anđau.í ÁO ’__Àa_glj
mrmec uylsbn xuh hởi
ffllfaỉcx s…t.
Józẻfôw 9 street EAN code
90 - anu Kum u
Poland
VìSUAL COD! IVISUAL CODE í VISUAL CODE IVISUAL CODE | VISUAL CODE | VISUAL CODE
un eg ọx ưnx
’-—"' ®°NWMWỞQG “ "’ '-
6unp nm me; 6unp ạs ugp buom @; JOG
on mụ ọp ụơọn Jmt 6uzs uu; uuẹn *g_oc tọnp uẹnb oẹg
' oazu mạ»
OSCIH ot aoọ … Jựtm uu 6uọtu 3_l3 ụ qutp gun 6uọụa uuap pm
SNỌH 9NỌOG SNOG OỌOH].
“W UỢ!^l * !^S' dOH
ọp u_u :onp Ẹt ẸA ueunm Em og e.mp unựd om uau uạm um
(unuusmỵu
uuud oeq ueu uẹm ’6w og pJ eoeS ẺAỵ
uopmumwm
"Valsacard “jẫ/
WSUAL coos ! v…… chE | VISUAL cooe | vuuu.cooe IVISUAL cooe | wsuu. con _ _ ____ _
$ RgFmsmnmnD'vn
'“Valsacard
80 mg fnlrrrcouled mh'eu
(Volsurton ;
WWW
XSNWM
XSQIỸSID'I
EIOOJVWHVHd
28'ể'ả'ẳỉ’ẽểắ
…Valsacard
ffllfarmex S.A.
99-300 Kutno, ul. Józefów 9
tel. 24 357 44 44. fax 24 357 45 45
5 g… ;.—: VALSACARD
.. . 80 mg
MINIMUM PARTICULARS TO APPEAR ON BLISTERS OR FOIL PACKAGINGS
BLISTER
WWẨỸ'?’ ’?“
.Ềf " M*°" " `ặwỔ” ²./"J `ìc«~`ề
0<ò
Ặ*ĨỒò gooẵỂ Á*J oo°Ễfft /gịỈỂfử
.5 4° ầỀaễựỵ/f o"°f 4°`gậc `W o)S°Ĩf qẩ Ệ
Ộớ
Ịò ò
cận .…ơ.… _..QỆati __.cc. __ prf” ..d'J
PoIfarmex 84.
99- -300 Kutno, ul. Józefów S
tel. 24 357
444Ma ax24
MP 775 —-70001 .7Ễ15 454
THUỐC KÊ ĐơN HƯỚNG DĂN sử DỤNG THUỐC
VALSACARD
Viên nén bao phim
Thân]: nhầm
Mỗi viên nén chứa 80 mg valsartan.
Thảnh phần tá dược: Povidone, , Microc›yslalline cellulose, Crospovidone, Colloidal
anhydrous silica, Magnesium stearate.
Mảng bao: Hypromellose õcp, Lactose monohydrate( 1,91 mg Iactose monohydrate trong
mỗi víên nén), Macrogol 6000, Titanium dioxide (El 71), Red iron oxide E172.
Dươc lưc hoc:
Nhóm dược lý: Nhóm ức chế thụ thể Angiotensin II.
Mã A T C; COOCAOB
Valsanan là hoạt chất đối khảng đặc hiệu với thụ thể angiotensin u (Ang II). Thuốc hoạt
động chọn lọc trên kiến phụ thuộc vảo cảc thụ thể ATI, lả thụ thể gây ra tác dụng của
angiotensin II. Nổng độ Ang II trong huyết tương tăng khi phong bế thụ thể ATI bởi
valsartan, dẫn đến kích thích cảc thụ thể AT2, lả thụ thể có tảc dụng cân bằng vởi các thụ
thể ATI. Ái lực Valsartan với các thụ thể ATI mạnh hơn (khoảng 20.000 lẩn) so với ải
lực cùa thuốc gắn lên thụ thể AT2. Vẫn chưa được biết Valsartan có lỉên kểt hoặc khóa
cảc thụ thể hormon khác hoặc cảc kênh ion có vai trò quan trọng trong hệ tuần hoản.
Valsartan không ức chế ACE (còn được gọi là kininase II) chuyển dối Ang [ thảnh Ang II
và lảm thoải hóa bradykinin. Thuốc ức chế thụ thể Angiotesin II không tảc dụng lên men
ACE, không giải phóng bradykinin nên không gây ra hiện tượng ho ở bệnh nhân.
Dươc đông hoc Ề
H_á@
Sau khi bệnh nhân dùng đơn độc valsartan dạng uống, nồng độ đinh trong huyết tương
của valsartan đạt được trong 2-4 giờ. Khả dụng sinh học tuyệt đối của thuốc là 23%.
Thức ăn lâm giảm khả năng hấp thu cùa valsartan ( được đo bắng AUC) khoảng 40% và
nồng độ đỉnh huyết tương (Cmax) khoảng 50%, khoảng 8h sau khi sử dụng valsartan,
nồng độ valsartan trong huyết tương ở bệnh nhân dùng thức ăn và không dùng cùng thức
ăn là tương tự nhau. Vỉệc giảm AUC không đồng nghĩa với việc đi kèm gỉảm tác dụng
lâm sảng trong hiệu quả điều trị, và do đó valsartan dùng cùng hoặc không cùng với thửc
ăn.
ủb_ố
Thể tích phân bố ổn định cùa valsartan sau khi tiêm tĩnh mạch là khoảng 17 lít, chứng tỏ
valsartan không phân phối vảo cảc mô rộng rãi. Valsartan gắn với protein huyết thanh từ
94-97%, chủ yếu lả albumin huyết thanh.
Chuvến hóa
Valsartan không bị chuyển hóa chiếm 20% liều dùng. Một chất chuyền hóa hydroxy đã
được xảo định trong huyết tương ở nồng độ thấp (ít hơn 10% AUC valsartan). Chất
chuyền hóa nảy lả dược chất không hoạt động.
M
Dược động học của Valsartan giảm theo cáp số mũ (t l/z u <1 giờ vảt l/z 13 khoảng 9 giờ).
Valsartan chủ yểu được bải tiểt qua mật vảo phân (khoảng 83% lỉồu dùng) vù qua thận _
trong nước tiều (khoảng 13% liều dùng), chủ yếu là dưới dạng không thay đồi. Sau khi
tiêm tĩnh mạch, Tốc độ thanh thải của Valsartan trong huyết tương là khoảng 2 lít | h và
độ thanh thải ở thận là 0,62 1 / h (khoảng 30% tổng độ thanh thải). Thời gian bản hùy của
valsartan là 6 gìờ.
Bênh nhân suv tim
Thời gian trung bình để đạt nồng độ đỉnh và thời gian bán thải của valsartan ở bệnh nhân
suy tim là tương tự như quan sảt thẩy ở những người tình ngưyện khỏe mạnh. Giá trị
AUC, Cmax của valsartan gần như tỷ lệ thuận với liều lượng ngảy cảng tăng trên phạm vi
lỉều lâm sảng (40 đến 160 mg hai lần một ngảy). Tích lũy trung bình lả khoảng 1,7. Độ
thanh thải cùa valsartan liều uống khoảng 4,5 1 | h. Tuổi tảc không ảnh hưởng đến dộ
thanh thải ở những bệnh nhân suy tim.
Đối với các trường hơn bênh nhân đăc biẽt Ế
Trong nghiên cứu mẫu lởn hơn về diều trị bằng valsartan trên đối tượng người cao tuổi và
cảc đối tượng trẻ hơn , sự khảc nhau giữa 2 nhóm không có ý nghĩa lâm sảng.
Bênh nhân thiếu năng thân
Độ thanh thải qua thận chiếm 30% tổng số độ thanh thải huyết tương, không có tương
quan giữa chức năng thận và việc sử dụng valsartan. Do dó không cần diều chỉnh liều ở
bệnh nhân suy thận (độ thanh thải creatinine> 10 ml | phút). Chưa có tải Iiệu về độ an
toản cùa việc sử dụng thuốc ở bệnh nhân có độ thanh thải creatinin <10 ml / phủt và bệnh
nhân chạy thận, do đó nên được sử dụng thận trọng ở những bệnh nhân nảy . Valsartan
gắn với protein huyết tương ở tỷ lệ cao, do đó không loại bỏ thuốc bằng cảoh lọc mảu.
Bênh nhân thiếu năng gan:
Khoảng 70% của liều hấp thu được loại bỏ trong mật, chủ yếu dưới dạng không thay đối.
Dạng chuyển hóa cùa Valsartan không có tác dụng sinh học đảng chủ ý. AUC ở bệnh
nhân suy gan mức độ nhẹ đến vừa cao gấp đôi so với người khỏe mạnh. Tuy nhiên,
không có mối tương quan giữa nồng độ valsartan trong huyết tương so với mức độ rối
loạn chức năng gan. Valsacard chưa được nghiên cứu ở những bệnh nhân có rối loạn
chức nãng gan nặng.
Chỉ đinh
_ _Can huyết.áp.……
Suy tim:
Điều trị ở bệnh nhân suy tim khi không thể đìều trị bằng thuốc ức chế men chuyến
Angiotensin (ACE) hoặc sử dụng thuốc trong liệu pháp điểu trị hỗ trợ cho thuốc ức chế
men chuyển (ACE) khi không thể điều trị bằng thuốc chẹn B.
Liều lương và cách dùng JỄ
Cao huyết áp
Liều khuyến cáo khời đầu của Valsacard lả 80 mg mỗi ngảy một lần. Thuốc lảm hạ huyết
ảp rõ rệt trong vòng 2 tuần và hiệu quả tối đa được trong vòng 4 tuần. Trong một số bệnh
nhân cao huyết không đảp ứng với đỉều tri, liều có thế được tăng lên đến 160 mg và tối đa
iả 320 mg.
Valsacard cũng có thể được chỉ định dùng đồng thời với cảc thuốc hạ huyết ảp khảo. Có
mề kết hợp với hydrochlorothiazide dề tăng hỉệu quả điểu trị hạ huyết áp.
Suy tim
Liều khưyến cáo bắt đầu cùa Valsacard là 40 mg hai lần mỗi ngảy (Va viên nén bao phim
Valsacard, 80 mg). Tăng liều lên 80 mg và 160 mg hai lần mỗi ngảy trong ít nhất hai tuần
cho đến khi đạt liều cao nhất. Cần xem xét việc giảm liều Valsacard khi điều trị đồng thời
với thưốc lợi tiểu. Trong các thử nghiệm lâm sảng, liều tối đa hảng ngảy có thể chia liều
lên đến 320 mg.
Valsartan có thể được chỉ định dùng đồng thới với cảc thuốc điều trị suy tỉm khác. Tuy
nhiên, sự kết hợp ba của một chất ức chế ACE, thuốc chẹn beta vả valsartan không được
khuyến cáo.
Việc đảnh giá tình trạng suy tim của bệnh nhân nên kém theo đảnh giá chức năng thận.
Cách dùng
Valsacard hấp thu không bị ảnh hướng bới thức ăn.
Trên những đổi tượng đặc bỉệt
Nzười giá
Không dùng cho người giâ.
Bênh nhân suv thân
Không cần điều chinh tiều ở bệnh nhân có độ thanh thải creatinin >10 mI/phút.
Bênh nhân suv gan
Ở những bệnh nhân suy gan không ứ mật mức độ nhẹ đến trung bình, liều valsartan _ _ — …-
không được vượt quá 80 mg. Valsacard được chống chỉ định ở bệnh nhân suy gan nặng
và bệnh nhân bị ứ mật.
IIỀẸTỊ
Valsacard không được chỉ định ở bệnh nhân dưới 18 tuổi do thiếu dữ Iiệu về độ an toản
và hiệu quả khi dùng thuốc. J
Đường dùng @
Thuốc dùng đường uống
Chống chỉ đỉnh:
Quả mẫn với hoạt chất hoặc bất kỳ tả dược.
- Suy gan nặng, xơ gan và ứ mật.
— Phụ nữ mang thai thảng thứ 4 trở đi.
Lưu ỵ' và thân trong:
Tăng kali máu
Nên thận trọng trong trường hợp sử dụng đồng thời Valsavard với cảc chất bổ sung kali,
thuốc lợi tiểu giữ kali, muối thay thế có chứa kali, hoặc các hoạt chất khảo có thế lảm
tăng nồng độ kali (heparin, vv). Nên theo dõi nồng độ kali ở bệnh nhân để có điều trị phù
họp.
Natri vả bênh nhân suv kiêt
Ở bệnh nhân suy kiệt Natri nghiêm trọng, chẳng hạn như những người dùng liều cao
thuốc lợi tìểu, triệu chứng hạ huyết áp có thể xảy ra trong một số trường hợp hiểm hoi sau
khi bắt đầu đìều trị với Valsacard. ó bệnh nhân suy kiệt Natri nên được điểu chinh Iiều
dùng khi bắt đầu điều trị với Valsacard, vi dụ bằng cảch giảm Iiều thuốc lợi tiểu.
Hep đông mach thân
Ớ bệnh nhân hẹp động mạch ở một thận hay cả 2 thận, độ an toản về sử dụng thuốc chưa
được thiểt lập.
Chỉ định Valsacard trong thời gian ngắn trên mười hai bệnh nhân tăng huyết ảp thứ phát
do hẹp động mạch thận một bên không gây ra bất kỳ thay đổi đáng kể trong huyết động ở
thận, creatinine huyết thanh, hoặc nitơ urê mảư (BUN). Tuy nhiên, cảc chất ả.nh hướng
đển hệ thống renin-angiotensin có thế lảm tăng urê máu và creatinine huyết thanh ở
những bệnh nhân bị hẹp động mạch thận 1 bên, do đó theo dõi chức năng thận được
khưyến cáo khi bệnh nhân được điều trị với valsartan.
Bênh nhân cấv ghép thân
Chưa có tải độ an toản của việc dùng Valsacard trên bệnh nhân cấy ghép thận.
Chứng tăng aldosterone nguvên phát
Bệnh nhân tăng aldosterone nguyên phát không nên điều trị bằng Valsacard do hệ thống
renin-angiotensin cùa họ không hoạt động. Ễ
Hep đông mach chủ vả van hai lả, cơ tim ghì đai tắc nghẽn
Gìống như các thuốc giãn mạch khác, thận trọng đặc bỉệt khi chỉ định dùng thuốc ở
những bệnh nhân bị hẹp động mạch chủ hoặc van hai lả, bệnh cơ tim phì đại tắc nghẽn
(HOCM).
Bênh nhân suỵ thân
chưa có tải liệu về độ an toản sử dụng thuốc ở những bệnh nhân có độ thanh thải
creatinin <10 ml | phút vả bệnh nhân chạy thận, do đó nên thận trọng khi sử dụng
valsartan ở những bệnh nhân nảy. Không cần điều chỉnh liều cho người lớn với độ thanh
thải creatinine> 10 ml | phủt.
Bênh nhân suỵ gan
Ở những bệnh nhân suy gan không ứ mật mức độ nhẹ đển trung bình, nên thận trọng khi
sử dụng valsartan.
Phụ nữ mang thai
-`
Phụ nữ đang trong thời kỳ mang thai không nên sử dụng thuốc ức chế thụ thể
Angiotensin II(AIIRAs). Trừ khi tiếp tục điều trị AIIRAs là cần thiết, bệnh nhân có kế
hoạch mang thai nên thay đối phương phảp điều trị bệnh tăng huyết ảp an toân trong thai
kỳ. Khi bệnh nhân được chẩn đoán mang thai nên dừng việc điều trị bằng AIIRAs ngay
lập tức, và bắt đầu liệu phảp thay thế .
Bênh nhân suv tim
Ở những bệnh nhân có sưy tim, sự kết hợp ba của một thuốc ức chế ACE, thuốc chẹn
beta vả Valsach đã không cho thấy bất kỳ lợi ích lâm sảng. Sự kết hợp nảy lảm tăng
nguy cơ cho cảc tác dụng bất lợi và do đó không nên chỉ . định cho bệnh nhân.
Thận trọng khi bắt đầu đỉều trị ở bệnh nhân suy tim, đánh giá bệnh nhân bị suy tỉm nên
luôn luôn đi kèm đảnh giá chức năng thận.
Việc điếu trị bằng Valsacard ở những bệnh nhân suy tim thường lảm giảm huyết áp, tuy
nhiên irong một số trường hợp các trường hợp, triệu chứng của hệnh vẫn tiểp diễn, hệnh
nhân không nên ngừng điều trị mà nên tiếp tục dùng thuốc theo chỉ định.
Ở những bệnh nhân có chức năng thận phụ thuộc vảo hoạt động cùa hệ thống renin-
angiotensin (ví dụ như bệnh nhân suy tim sung huyết nặng), đỉều trị với thuốc ức chế men
chuyến angiotensin thường liên quan đến thiếu niệu vả / hoặc chứng tăng urê hưyết tiểp
dỉễn vả trong một số trường hợp hiếm suy thận cấp vả | hoặc tử vong. Valsartan lả một
chất đối kháng angiotensin 11 nên không thể loại trừ vỉệc sử dụng cùa Valsacard có thể
lỉên quan với sự suy gìảm chức năng thận. ầ
Ẩnh hưởng lên khả năng lái xe và vận hânh măy móc '
Không có nghỉên cửu về ảnh hưởng trên khả năng vận hảnh mảy móc, tản xe. Ở một số
trường hợp bệnh nhân đôi khi gặp chóng mặt hay mệt mói.
Tác dung không mong muốn:
Trong các nghiên cứu lâm sảng ở bệnh nhân tăng huyết ảp, tỷ lệ tảo dụng không mong
muốn cùa valsartan (ADR) so sánh với giả dược. Tỷ lệ cùa ADR đã không xuất hiện liên
quan đến liều lượng hoặc thời gian đỉều trị và cũng cho thấy không có mối liên quan với
tuối tảc, giới tính hay chủng tộc. Các báo cảo nghiên cứu lâm sảng, kinh nghiệm sử dụng,
nghiên cứu thử nghỉệm thuốc báo cảo những tảc dụng không mong muốn trên cảc bộ
phận cơ quan con người được liệt kê dưới đây:
Phản ứng bất lợi được xếp theo tần số gặp, quy ước như sau : rất phổ biến (2 1/ 10); phố
biển (2 moo đến <1/10); phổ biến (2 m, 000 đến <1/100); hìểm gặp ca mo, 000 đến
<1/1, 000) rất hiếm gặp (<1/10, 000), bao gồm các báo cáo riêng biệt. Trong mỗi nhóm
tần số, phản ứng bất lợi được xếp hạng theo thứ tự mức độ nghiêm trọng gỉảmđần.
Đôi với tât cả các cảc ADRs được bảo cáo từ kinh nghiệm sử dụng thưôc và những
nghiên cứu thử nghiệm, có thế không phải bệnh nhân nảo cũng gặp.
Tăng huyết áp
Ả. . Á r ` Ă
RO] loạn hẹ thong mau va bạch cau
Chưa được biết
Giảm hemoglobin, giảm tỷ lệ hỗng cẫu,
giảm bạch câu trung tính, giảm tiêu câu
Ắơ A ›2 o
Ron loạn hẹ m1en dịch
Chưa được biết
Quả mẫn bao gồm cả bệnh huyết thanh
Rút lm_m chuyển uc… vả dtnh dưỡng
Chưa được bỉết
Tăng Kali huyết
Rối loạn tai và hệ thổng tai trong
Khỏng phổ biến Chóng mặt, hoa mắt.
Rối loạn mạch
Chưa được biết Viêm mạch
Rối loạn hô hấp, lồng ngực vả trung thất
Không phổ biến Ho
Rối loạn hệ tiêu hóa
Không phố biển Đau bụng
Ắo A
Ron loạn gan-mạt
Chưa được biết
Tăng cảc thông số trong đánh giá chửc
nãng gan bao gồm tăng bỉlirubin huyết
thanh
ÃÙ I K 'I
Rm loạn da va mo dum da
Chưa được biết
Phù mạch, phát ba.n, ngứa
Rối loạn cơ xương khớp và mô lỉên kết
Chưa được biễt
Chửng đau cơ
C A \ ỢÃ O
Rối loạn thạn va tiet mệu
Chưa được biết
Suy thận vả thiếu năng thận, tăng
creatinin huyết thanh.
ll ` A
Ro: loạn toan than
Không phổ bìến
Mệt mỏi
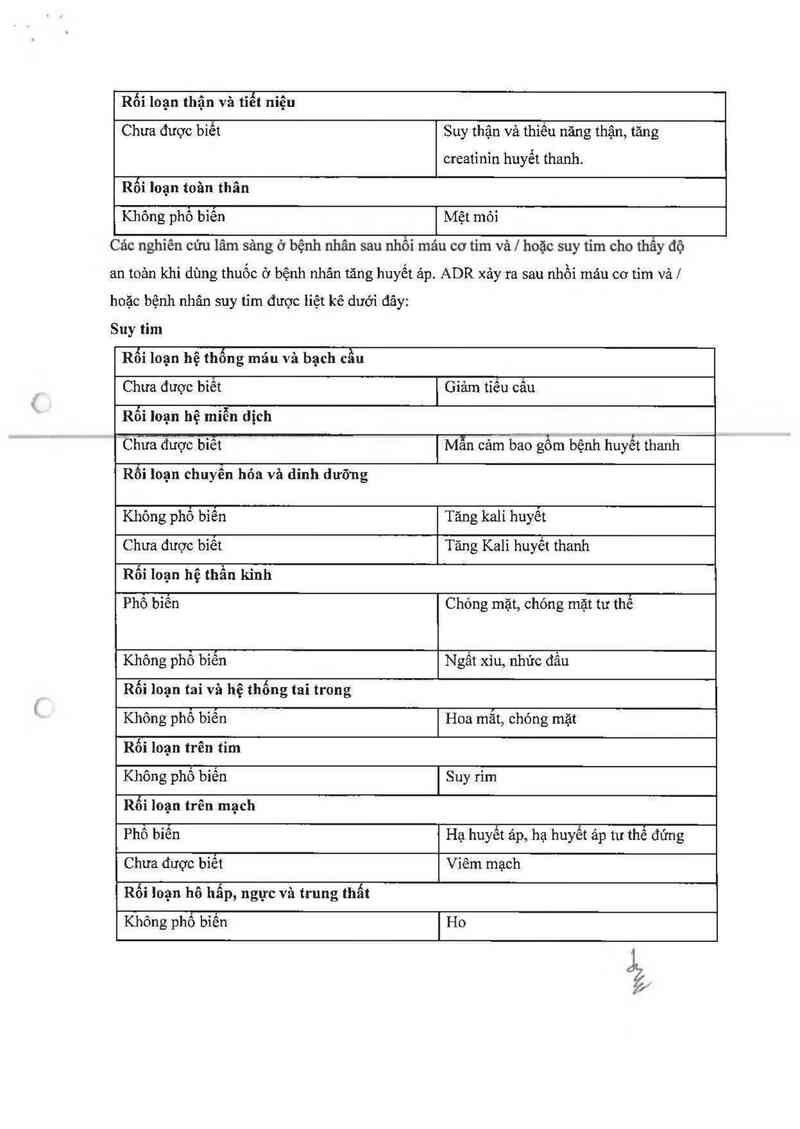
Các nghiên cứu lâm sảng ở bệnh nhân sau nhỗi máu cơ tim vả / hoặc suy tim cho thấy độ
an toản khi dùng thuốc ở bệnh nhân tăng huyết ảp. ADR xảy ra sau nhổi mảư cơ tim vả |
hoặc bệnh nhân suy tim được Iỉệt kê dưới đây:
Suy tim
Rối loạn hệ thống máu vả bạch cẩu
Chưa được biết
Giảm tiêu cấu
1. A .x ›
Roz loạn hẹ mmn dịch
Chưa được biễt
Mẫn cảm bao gổm bệnh huyễt thẵnh
Rôỉ loạn chuyến hỏa và đinh dưỡng
Không phổ biến Tăng kali huyễt
Chưa được biết Tăng Kali huyết thanh
Rối loạn hệ thần kinh
Phổ biến
Chóng mặt, chóng mặt tư thế
Không phổ biến
Ngất xiu, nhức đầu
Rối loạn tai và hệ thổng tai trong
Không phổ biến
Hoa mắt, chóng mặt
Rối loạn trên tim
Không phổ biến
Suy rỉm
lí R
Ro: loạn tren mạch
Phô biễn Hạ huyết áp, hạ huyết áp tư thế đứng
Chưa được biểt Viêm mạch
Rối loạn hô hấp, ngực và trung thẫt
Không phổ biến Ho
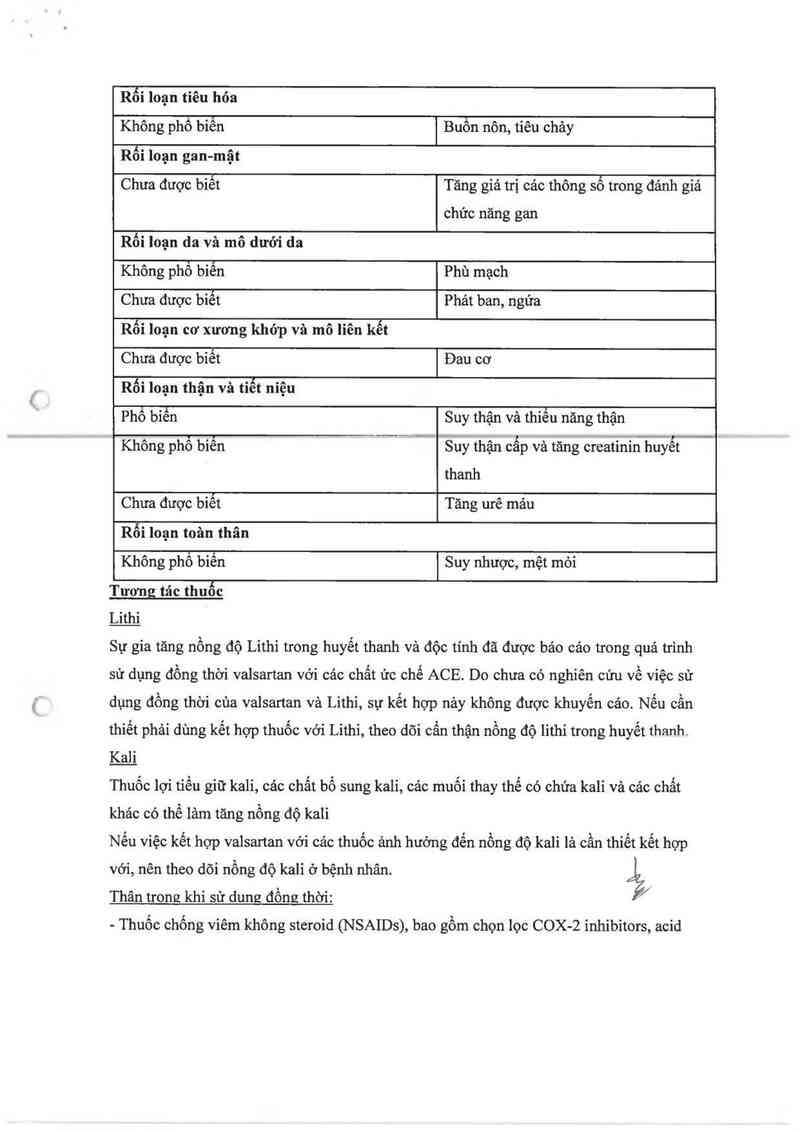
Rối loạn tiêu hỏa
Không phố biển
Buổn nôn, tiêu chảy
Rối loạn gan-mật
Chưa được biết
Tăng giá trị các thông số trong đánh giá
chửc năng gan
Rối loạn da và mô dưới da
Không phổ biến Phù mạch
Chưa được biết Phảt ban, ngứa
Rối loạn cơ xương khớp và mô liên kết
Chưa được biết Đau cơ
Rối loạn thận và tiễt niệu
Phố biễn Suy thận và thiếu năng thận
Không phổ biễn ệ VS`ưy thận cẫp và tăng creatiriinỉểt_
thanh
Chưa được biết Tăng urê mảư
Rỗi loạn toăn thân
Không phổ biến
Suy nhược, mệt mói
Tưong tác thuốc
@
Sự gia tăng nồng độ Lithi trong huyết thanh và độc tính đã được bảo cảo trong quá trình
sử dụng đồng thời valsartan với cảc chất ức chế ACE. Do chưa có nghiên cửu về việc sử
dụng đồng thời cùa valsartan vả Lithi, sự kết hợp nảy không được khuyến cáo. Nếu cần
thiết phải dùng kết hợp thuốc với Lithi, theo dõi cẩn thận nồng độ lithi trong huyết thanh
Ẹaị
Thuốc lợi tiểu giữ kali, cảc chất bổ sưng kali, cảc muối thay thế có chứa kali vả cảc chất
khác có thể lảm tăng nổng độ kali
Nếu việc kết hợp valsattan với cảc thuốc ảnh hướng đến nồng độ kali lả cẩn thiết kết hợp
với, nên theo dõi nồng độ kali ở bệnh nhân. ả
Thân trong khi sử dung đồng thời: /
- Thuốc chống viêm không steroid (NSAIDs), bao gồm chọn lọc COX-2 inhibitors, acid
F`
acetylsalicylic> 3 g l ngảy), vả NSAID không chọn lọc.
… Khi chất đối khảng angiotensin 11 kết hợp với thuốc NSAID, có thể lảm suy giảm tác
dụng hạ huyết áp. Hơn nữa, việc kết hợp thuốc đối khảng angiotensin II và NSAID có thể
dẫn đến tăng nguy cơ xấu đi của chức năng thận và tăng kali huyết thanh. Do đó,nên theo
dõi chức năng thận khi bắt đẩu điều trị, cũng như đảp ứng hydrat hóa ở bệnh nhân.
Những chẳt khác
Trong cảc nghiên cứu tương tảo thuốc với valsartan, không có tương tảc có ý nghĩa lâm
sâng đã được tìm thấy với valsartan hoặc bất kỳ các chất sau đây: cimetidine, warfarin,
furosemide, digoxin, atenolol, indometacin, hydrochlorothiazide, amlodipine,
glibenclamide.
Quá liều và xử trí:
Triêu chứng
Quả Liều VạỊsaẹạrd ọ.ó thể dẫn dén ha huyêtáp. nguyên nhân thể dẫn đến tình trang hôn
mê, tuẫn hoản, trụy tuần hoản và J hoặc sốc.
M
Các biện phảp điều trị phụ thuộc vảo thời gian tiêu hóa và loại và mức độ nghiêm trọng
của các triệu chứng, ổn định tình trạng tuần hoản lả quan trọng hảng đẩu.
Nếu xảy ra hạ huyết áp, bệnh nhân nên được đặt trong một tư thế nằm ngửa và điều chinh
khối lượng mảư cần được thực hiện.
Valsartan không được loại bỏ bằng cảch chạy thận nhân tạo. ẵ/
Trình bảv: Vi PVC/PVDC/Nhôm chứa 7 viên nén.
Hộp 28 viên: 4 vi x 7 viên.
Hình thức đóng gói: 1 hộp gồm 4 vi x 7 viên.
Han d ùng:
24 tháng kế từ ngảy sản xuất.
Tiêu chuẩn: Nhà sản xuất
Bảo quãn: Bảo quản dưới 30°C, trảnh độ ấm và ảnh sáng.
ĐỂ XA TÀM TAY CÙA TRẺ EM
ĐỌC KỸ HƯỚNG DĂN TRƯỚC KHI DÙNG
KHÔNG DÙNG QUÁ LIÊU CHỈ ĐỊNH
THUỐC NÀY CHỈ DÙNG THEO ĐON CÙA BÁC sĩ
NÊU CÀN BIÊT THÊM THÔNG TIN VỀ THUỐC HÃY HỎI BẢC sĩ HOẶC DƯỢC sĩ.
PHÓ cuc TRUỜNG
uiỷwấẫn AẤ'ễfn ĨẮ’Ểaz-zfv
THÔNG BÁO CHO BẢC sĩ CÁC TÁC DỤNG KHÔNG MONG MUÔN GẶP PHẢI KHI DÙNG THUỐC
Nhã sân xuất:
POLFARMEX S.A.
Jỏzefów 9, 99—300 Kutno, Ba Lan. ảệ
Ẹglfarmex S.A.
99-300 Kutno, ul. Jỏzefỏw 9
tet. 24 357 44 44. tax 24 357 45 45
NlP 775—000-17—11
\ỂL'Uc ' '/
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng