





















«GICi. t.Ezi^… l`r li'Jl"fJ lĩl'iặiJịịua
u'u`m nm'ơs tn uc
Mq. … n
hu)…le mu
nu un ợI II~…I c…ì ui ›
inịnug le | nmuuu vWãì; ocnnpes unwupnnn
W _ ' @
cumnơnonuuuhcmuvcmoxoòcưamut
uovnmwmuuauou_-
wmlwu a.ncwuumởủc
WINunnọ—ụonyuAniumwn
w'aưwmnpuwuo
- Uli’wszđunosznwnvouưumunwwlwn 10… w1Mlntwũmn
uw>wu
un
… - uu › … uoc Al JMWỐS...
Sporanox® IV
itraconazole (10 mg/ml)
iNT
iỄỄỂZJ'fflỄ 25 ml concentrate ot Sporanox LV. tor solution 10! infusion
đo concentrado de Sporanox LV. para solución destinada a la intusión
G o. 9 % Sodium Chlorlde in)cction
50 mi solution tot intusiun- intmenous use
de solución para Intusión uso lntmenoso
@ Extension lhe | Vía de extensión
E
ắ'Ểị
Janssen7
)
\\ r,’
\ ,
\
x \ .
c\ {, ,
|
uuunuus …… c .… uunuv
.nnp …;1
c 32° -
i.Ẹ_iầ ìmo. 000 và <… 000
Rất hiếm gặp lụglmL. Cảo điếm breakpoint có thế diễn dịch đã không được thiết lập cho nấm s_
Các nghỉến cứu in vilro cho thấy itraconazole ức chế sự phát triển cùa nhiếu loại vi nắm gây bệmi/cho
người ở nồng độ thông thường_ < ! ụg/mL. Cảc vỉ nắm nảy bao gổm; '
vỉ nâm ngoải da (các chúng T rzchophyton spp, Microsporum spp Epidermophyton jloccosum) nâm
mcn (cảc chùng Candida bao gổm C. albicans, Czyptococus neofiarmans, Malassezia Spp.,
Trichosporon spp., Geolrichum spp. ); Aspergillus spp. ; Histoplasma spp.; Paracoceidz'oides
brasiliensis; Sporothrix schenckii; Fonsecaea spp.; Cladosporz'um spp.; Blastomyces dermatỉtidis;
Coccidiodes immitis; Pseudallescheria boydii; Penicillium marnefflai; vả cảc vi nấm vả nấm mcn khảo.
Candida krusei, Candida glabrata vả Cand:da tropicalz's thường là cảc chủng Candida kém nhạy cảm
nhất, ở vải thử nghỉệm phân lập trong ống nghiệm cho thấy chủng đế khảng với itraconazole.
Cảc loại vi nấm chính không bị ức chế bới itraconazole lả Zygomycetes (Rhizopus spp Rhizomucor
spp.. Mucor spp. vả Abst'dia spp. ), F usarzum spp., Scedosport'um spp. vả Scopulariopsz's spp
Sự đế khảng azole có vẻ hình thảnh chậm vả thường là kết quả của nhiếu đột biến gen. Các cơ chế đã
được mô tả gổm sự biếu hiện quá mức cúa ERGI 1, vốn mã hóa mcn đích l4a-dcmcthylasc, cảc đột
biến điềm trong ERGII dẫn đến giảm ải iực với đích vả/hoặc sự biếu hiện quá mức của chất vận
chuyến lảm tăng bom ra ngoải. Đế khảng chéo giữa cảc azole đã được quan sảt thấy ở Candz'da spp. .,
mặc dù sự để khảng cùa ] thuốc trong nhóm không nhất thiết có nghĩa lá để khảng với cảc azole khác.
Chủng nấm Aspergillusfizmigatus đã được báo cáo có đề kháng với itraconazole.
Đặc tính dược động học
Dược động học cùa itraconazole đường tĩnh mạch được khảo sảt trên những người khóc mạnh vả cảc
bệnh nhân sau khi sử dụng đơn liều vả đa lỉều, vả trong những nhóm bệnh nhân đặc biệt sau khi sử
dụng đơn liếu.
Chế độ đa liếu bao gỗm truyền itraconazole 200 mg trong ] giờ ngảy hai lần vảo ngảy điều trị thứ 1 vả
2, sau đó truyền 200 mg trong | giờ ngảy một lần từ ngảy thứ 3 tới ngảy 7.
Mỗi liếu 200 mg itraconazole tĩnh mạch chứa 8 g hydroxypropyl-B-cyclodcxtrin đề lảm tăng tính hòa
tan của itraconazole. Những dữ liệu dược động học của mỗi thảnh phần sẽ được mô tả bến dưới. (Xem
Ilraconazole; xem Các nhóm bệnh nhân đặc biệt- Suy thặn, Hydroxypropyl- fi -Cyclodextrin.)
Itraconazole
Cảc lính chẩt dược động học chung
Nồng độ đính trong huyết tương cùa itraconazole đạt được tại thời điểm kết thúc 1 giờ truyền.
Itraconazole được chuyến hỏa mạnh ở gan thảnh nhỉếu chẳt chuyến hóa. Chẳt chuyến hóa chính là
hydroxy-itraconazole có hoạt tính kháng nắm in vilro tương đương itraconazole. Nổng độ chẩt chuyến
PJ_Spomnux w _ccos 285ep2010_v2 sn s
;.ủ
Í” 4
hóa nảy trong huyết tương gấp 2 lần itraconazole Mối quan hệ dược động học của itraconazole có đặc
trưng lá không tuyên tính vả, do đó có sự tích tụ trong huyết tương sau nhỉếu lẩn dùng lập lại. Trạng
thải nồng độ hằng định đạt được sau liều itraconazole IV thứ tư vả liếu thứ bảy đối với hydroxy-
itraconazole. Nồng độ đinh trung bình sau 4 lìếu itraconazole IV 200mg ở những người khỏe mạnh là
3021 ng/mL vởi itraconazole và 1450 ng/mL đối vởi hydroxy-ỉtraconazolc, trong khi giá trị nồng độ
tối thiếu trung bình lần lưọt lả 523 ng/ rnL và 959 ng/mL. Nồng độ thanh thải trung binh cúa toản bộ
itraconazole trong huyết tương sau khi dùng đường tĩnh mạch là 278 mL/phút. Thời gỉan bán hủy trung
binh của itraconazole là khoảng 35 giờ ở trạng thái hẳng định.
Phân bố \ _ ,
Hầu hết itraconazole trong huyết tương kết hợp với protein (99, 8%) vởi albumin lả thảnh phân găn kêt
chính (99, 6% cho chất chuyến hớa hydroxy) Nó cũng có ái tính mạnh với lipid. Chi có 0,2%
ỉtraconazolc 1ả tồn tại dưới dạng thưốc tự do trong huyết tương. Itraconazole được phân bố ở thể tích
biếu kiến lớn trong cơ thể (>700L), phân bố nhiều ở mô: nông độ ở mô phổi, thận, gan, xương, dạ dảy,
lách và cơ, cao gâp 2- 3 lần nộng độ tương ứng ở huyết tương, sự thâm nhập của thuốc vảo các tổ chức
sửng, dặc biệt lả da đến 4 iần cao hơn trong huyết tương. Tỉ lệ ở mỏ năo so với huyết tương vảo
khoảng ].
Chuyển hóa
Itraconazole được chuyển hóa mạnh ở gan thảnh nhiếu chất chuyến hóa. Cảo nghiến cúu in vitro cho
thẫy CYP 3A4 lả enzym chính có liên quan đển sự chuyến hóa của ìtraconazole. Chất chuyâ/hộzĩ
chính lả hydroxy-itraconazolc có hoạt tính kháng nấm in vitro tương đương itraconazole
T hải trừ , ,
Thải trù qua thận cùa itraconazole vả chât chuyền hóa hoạt tính hydroxy-itraconazoie chiêm ít hơn 1%
liếu tĩnh mạch Dựa trên liếu uống, sự thải trừ qua phân của dạng thuốc không đối trong khoảng từ 3%
tới 18% của iiếu dùng Itraconazoic được thải trù chủ yếu dưới dạng chẳt chuyến hóa không hoạt tính
trong nước tiều (35%) và trong phân (54%) trong vòng một tuần sau một liều uống.
Nhóm bệnh nhân đặc biệt
Suy gan
Không có nghiến cứu nảo được thực hiện với itraconazole IV ở những bệnh nhân suy gan. ltraconazolc
chủ yếu được chuyến hóa ở gan Đơn lỉều uống (viên nang 100 mg) đã được dùng ở 12 bệnh nhân xơ
gan vả 6 người khóc mạnh ở nhóm chứng; nồng độ đinh (Cmax), AUC và thời gian bản hủy
itraconazole được đo vả so sánh gỉũa các nhóm. Ớ nhóm bệnh nhân xơ gan, Cmax trung bình cùa
itraconazole giảm rõ rệt (giảm 47%). Thời gian bán thải trung binh kéo dải hơn nhóm không bị suy gan
(37 gíờ so với 16 giờ, tương ứng) Tổng nồng độ itraconazole, dựa vảo AUC 1ả tương đương nhau ở
nhóm xơ gan và nhóm khóe mạnh. Không có dữ iiệu về việc dùng itraconazole lâu dâi ở những bệnh
nhân xơ gan. (Xem phần Líều dùng vả cách dùng và phần Lưu ý và lhận Irọng đặc biệt khi sử dụng).
Suy thận
Một phần nhỏ (<1 %) của một Iiếu itraconazole đường tĩnh mạch được bải tiết không đối qua nước tiếu.
Sau khi dùng iiều đơn tĩnh mạch, thời gian bán hủy trung bỉnh cùa itraconazole ở những bệnh nhân suy
thận nhẹ (CrCL 50-79 mL/ phủt), trung bỉnh (CrCL 20-49 mL/ phủt) vả suy thặn nặng (CrCl <20
mL/min) thì tương tự như ở những người khóc mạnh. (ngưỡng trung bình 1ần lượt 42-49 gìò ở những
bệnh nhân suy thặn vả 48 giờ ở người khỏe mạnh.) Nồng độ phơi nhiễm chung của ìtraconazole, dựa
trên AUC, thì giảm ở những bệnh nhân suy thận trung bình khoảng 30% vả suy thận nặng khoảng 40%
so với nhũng người có chức nảng thận bình thường.
Chưa có dữ liệu ở những bệnh nhân suy thận điều trị lâu dải với itraconazole. Lọc thận thì không có
tác động trên thời gian bán hủy hay thải trừ itraconazole hoặc hydroxy-itraconazole. (Xem thêm phần
Liều dùng vả cách dùng, C hống chỉ định, vả Lưu ý và lhận trẹmg đặc biệt khi sử dụng).
P] Sportinox ] V _CCDS 28Sep2010_v2 9/ 1 S
H ydroxypropyl j›'-C ycIodexmn
Ở những bệnh nhân có chức năng thận bình thường, dữ [iệu dược động học cùa hydroxypropyl- B —
cyclodcxtrin, một thảnh phần cùa dạng bảo chế SPORANOXQĨJ đương tĩnh mạch, có thời gian bán hủy
ngắn 1 đến 2 giở, và chứng tớ không có sự tich lũy sau các liều liến tiếp hằng ngảy. Ở những người
khỏe mạnh vả ở những bệnh nhân có suy gỉảm chức năng thận từ nhẹ tới nặng, phần lớn của liều 8g
hydroxypropyl- B--cyciodcxtrin được thải trù trong nước tiếu Sau một liếu tĩnh mạch đơn itraconazole
200 mg, sự thanh thải của hydroxypropyl- B-cyclodextrin bị giảm ở những người suy thận kết quả là
nồng độ hydroxypropyl- [3-cyclơdextrin trong mảu sẽ cao hơn Ở những người có chức năng thận giảm
nhẹ, trung bình hay nặng, thì thời gian bán hùy của thuốc sẽ cao hon so với giá trị bình thường lần iượt
khoảng hai, bốn hay sảu lần. Ở những bệnh nhân nảy, việc truyền líên tục có thể dẫn đến tích tụ
hyđroxypropyl- -B-cyclodextrin cho tởi khi đạt tới tình trạng hằng định. Hydroxypropyl- B—cyclodcxtrin
bị thải bởi lọc thận.
Dữ lỉệu an toân tiền lâm sảng
Itraconazoìe
ltraconazole đã trải qua bộ thử nghiệm chuẩn về các nghiên cứu an toản tiền lâm sảng.
Những nghiến cửu dộc tính câp với itraconazole trên chuột nhắt, chuột cống, chuột lang vả chó cho
thắy giới hạn an toản rộng. Những nghiên cứu độc tính mạn đường uống trên chuột công vả trên Ê)'ó
cho thắy độc tính mạn ở nhiếu cơ quan hoặc mô đích như: vô thượng thận, gan vả hệ đại thực bâoi v,an
nhân cũng như các rối loạn chuyến hóa lipid thế hiện bằng những tế bảo xanthoma trong nhiếu cơ qiiưn
khác nhau _
ở liếu cao, khảo sảt mô học của vỏ thượng thận cho thấy sự phù nổ có thế hồi phục với sự phi đại cùa
lớp reticularis vả fascỉculata của vỏ thượng thận, thinh thoảng kèm với sự mỏng đi cùa lớp
glomerulosa. Sự thay đổi ở gan có thể hồi phục được thấy ở lỉễu cao. Sự thay đồi nhẹ được thấy trong
các tế bảo xoang tỉnh mạch và sự tạo khoang trong bảo tương cùa tế bảo gan, điếu nảy cho thắy rôi
loạn chức năng tế bảo, nhưng không có biếu hỉện vỉêm gan hay hoại tử tế bảo gan. Sự thay đồi mô học
cùa hệ thống thực bảo đơn nhân được đặc trưng chính bởi đại thục bảo với sự tăng những chất tương
tự protein trong nhỉếu mô như mô.
Không có dấu hiệu nảo cho thấy itraconazole có khả năng gây đột biến gen.
[traconazole không phải là một chẳt có khả năng gây ung thư trên chuột nhắt hay chuột cống. Tuy
nhiên trên chuột đực, có tần suất sarcom mô mêm cao hơn, có thế do tăng cảc phản ứng viêm mạn
khôngác tính của mô liên kết như là một hệ quả cùa mức tãng cholesterol vả cholesterol hóa trong mô
liên kêt.
Không có bằng chứng nảo cho thấy có ảnh hướng chính trên sự sinh sản khi điếu trị với itraconazole.
Itraconazolc được cho lả gây tăng có liến quan liếu trong độc tính trên mẹ, độc tính cho phôi thai, và
gây'dị tật thai trên chuột cống và chuột nhắt ở liếu cao. Trên chuột cống, dị tật thai bao gồm những
khiêm khuyêt hệ xương chính; trên chuột nhăt dị tật thai bao gổm thoảt vị não và phi đại lưỡi.
Mật độ khoáng trong xương thắp hơn đã được quan sát thắy ở những con chó chưa trướng thảnh sau
khi đùng itraconazole kéo dải.
Trong ba nghiến cứu độc tính trên chuột cống, itraconazole gây ra các khiếm khuyết xương Cảo khiếm
khuyết xương do nghiên cứu gây ra gổm giảm hoạt tính trên xương dẹt, lảm mỏng đi nhũng khoang
xương lớn vả tăng khả năng dễ gãy xương.
Hydroxypropyl-jỉ-cyclodexlrin (HP-fi-CD)
Nhũng nghiến cứu độc tính liếu đơn trên chuột nhắt, chuột cống và chó cho thấy giới hạn an toản rộng
sau khi tiếm HP- B-C D Trong những nghiến cứu độc tính bản cấp nảy, hầu hết cảc tác động đến được
điếu chỉnh về bản chất (những thay đổi mô học trong đường niệu, hoạt hóa của MP8) và cho thấy khả
năng hồi phục tốt
Sự thay đổi nhẹ ở gan xảy ra với liếu cao gấp 25 lần liếu HP B-CD khuyến nghị sử dụng trên ngưởi.
HP-[3- CD không gây vô sinh, không gây độc trực tiếp phôi thai và không gây dị dạng thai. Cấu trúc
Pl_Sporanox IV _CCDS 288ep2010_v2 1 Of'15
hóa học cùa HP-B-CD cũng không gậy nghi ngờ khả năng gây độc gen. Những xét nghiếm trênrcác tồn
thương của DNA, đột biên gen vả bât thường chromosomc in vitro và in vivo không bìêu 1ộ bât kì tác
động gây độc trên gen nảo cùa HP-B-CD.
TƯỚNG KY
SPORANOX® 1V chỉ được pha với 50 mL dưng môi tỉêm Natri Chlorid 0,9%, lả dung môi được cung
cấp kèm theo. `
Dung môi tiêm Natri Chlorid 0,9% thì tương thích với nhiễu loại thuốc, bao gôm SPORANOXỦ IV.
1traconazole có xu hướng kết túa khi SPORANOXƠD IV được hòa tan trong dung môi khảo ngoải 50
mL dung môi Natri Chlorìd 0,9% được cung cẳp.
THỜI HẠN SỬ DỤNG
. Óng tiếm SPORANOX® w:
Thời hạn sử dụng theo dạng đóng gói: 24 tháng.
Dung môi tiêm Natri Chlorid 0,9%: 36 tháng.
Dung dịch thuốc sau khi pha: 24 giờ
Ngảy hết hạn cùa bộ sản phấm lả ngảy hết hạn cùa thánh phần có ngảy hết hạn sớm nhất (tuối thọ
cúa bộ sản phẳm dưới 24 thảng).
1qu Ý ĐẶC BIỆT KHI BẢO QUÁN ,
Ong tiêm SPORANOX® IV: Không được bảo quản ở nhiệt độ trên 30°C. Giữ ông tiêm trorỞhộp Ị_
canon.
Dung dịch tỉêm Natri Chloride 0,9%: Không được bảo quản ở nhiệt độ trên 30°C. Không được đông
lạnh.
Dung dịch thưốc sau khi pha: tránh tiếp xúc trực tiếp với ánh sảng mặt trời. '
Theo quan điêm vi sinh học, thì thuôc sau khi pha nên được sư dụng ngay lập tức. Nêu không được sử
dụng ngay, thì thời gian bảo quản đê sử dụng và các đỉêu kiện bảo quản trước khi sử dụng là trách
nhiệm của người dùng vả thường không được `kéo dải quá 24 giờ ở nhiệt độ từ 2°C tới Ẹ“C, trừ khi cảc
thao tảc pha thuốc được thục hìện trong cảc điêu kiện vô trùng đã được thâm định vả kiêm soát.
Hưởng dẫn quy trinh sử dụng
Itraconazole có khuynh hưởng kết tủa khi 25 mL SPORANOX® ỈV đậm đặc được pha trong dung
môi khác 50 mL dung môi tiêm Natri Chloride 0,9%. Tổng lương đầv đủ 25 mL SPORANOX
w đậm đặc tử ống tiếm phải được pha vảo trong túi truyền chứa Natri Chiorid, lả tủi được thiết
kế chuyên biệt để dùng với dung dịch thuốc SPORANOX® w. Chỉ sử dụng cảc thảnh phần của
đơn vị đóng gói bán hảng (như túi truyền NaCl, dây nối với khóa 2 đầu vả bộ lọc trong ống 0,2
ụm, và ống tiêm Sporanox® IV). SPORANOX® IV không được truyền chung với bất kì loại thuốc
hay dung dịch nảo khác (xem Tương kị).
Trước khi bắt đầu quá trình pha, SPORANOX® 1v nguyên chẳt, chất hòa tan (Natri Chlorid) phải
được kíểm tra bằng mắt thường. Chỉ những dung dịch trong suốt không lẫn bất kỳ phần tử nảo
khác mới được sử dụng để pha.
Tống lượng SPORANOX® 1v đậm đặc phải được bom vảo túi NaCI trong một lần bơm chậm duy
nhất (lên đến 60 giây). Trong suốt quá trình pha, có thể xuất hiện mảu trắng sữa nhưng sẽ trở nên
trong suốt sau khi pha trộn nhẹ nhảng. Khi kíếm tra bằng mắt thường túi sau khi pha và trước khi
truyền, có thế quan sát thẳy tùa sản phẩm nội tại. Tủa nảy không ảnh hưởng chất lượng của sản
phấm. Dây nối chuyên biệt với bộ lọc 0,2 ụm phải được sử dụng để ngăn các tùa nảy đi vảo hệ
tuần hoản cùa người nhận.
P1_SporanoxiV _CCDS 283ep20/0_v2 ] 1/15
SPORANOX IV phải được dùng tuân theo cảc hưởng dẫn sau: chỉ khi được pha chính xác như trong
hướng dẫn sử dụng mới được dùng
Mở ổng tiêm
Bè ống tiêm như hình dưới đây:
—— con…u polnl \
4— biahnq Inwl
Mở Iúi Natri chlorid
Xé bao bên ngoải tại chỗ khía chữ V vả lấy tủi dịch truyền ra.
Pha dung dịch thuốc SPORANOX® I V và dịch pha tiêm Natri Chlorid 0, 9%
Mỗi thảnh phần phải đế ở nhiệt độ phòng.
Chi pha trong tủi truyền được cung cấp.
sư dụn kĩ thuật vô khuẩn và kim rủt thuốc có chiều dải phù hợp (không kèm trong bộ,k' ›, rút _
hết thuoc từ ống tiêm và sau đó đưa dung dịch thuốc SPORANOX® IV đậm đặc vảo tiị
truyền bằng cách đâm kim và bom vảo đâu đưa thuốc vảo. Bơm toản bộ thể tích (25 mL dung
dịch SPORANOX® w đậm đặc vảo túi trong một lần bơm chậm duy nhất (lên đến 60 giây).
Trong quá trinh pha có thể xuất hiện mảu trắng sữa. Đây là hiện tượng binh thường đối với sản
phẩm và sẽ biến mất sau khi toân bộ 2SmL SPORANOX® [V được hòa tan trong túi truyền
NaCl và sau khi trọn nhẹ nhảng. Rủt kim ra sau khi đã bơm SPORANOX® IV vảo trong túi.
Trộn nhẹ nhảng các thảnh phần trong tủi một khi dun dịch thuốc SPORANOX® IV đã được
bơm hết vảo tủi. Dung dịch truyền sẽ trở nên trong suot nhưng có thế quan sát thấy tủa nội tại
(được mô tả là có sợi đến giống như bông, mờ mờ đến có những hạt mảu trắng riêng biệt).
Những tủa nảy không ảnh hưởng chất lượng sản phẩm.
Dung dịch sau khi pha nên được sử dụng ngay lập tức và nên được bảo vệ tránh ánh sảng mặt
trời trực tiếp. Trong Iủc tiêm truyền, tiếp xúc với ánh sáng bình thuờng trong phòng thì chấp
nhận được. (Xem Thời hạn sử dụng và Lưu ý đặc biệt khi báo quản).
Thao tác tráng ống trước khi truyền:
Trước khi truyền, cathctcr phải được trảng để tránh vấn đề tương kỵ giữa lượng tổn đọng cùa thuốc
khác và itraconazole.
Lâm đầy dây nối được cung cấp trong bộ kit có bộ lọc 0,2 ụm bên trong bằng dung dịch NaCI
0,9% đã tiệt trùng và nối trực tiếp vảo catheter tĩnh mạch.
Trảng dây nối được cung cấp trong bộ kit vả cathetcr tĩnh mạch bằng dung dịch NaCI 0,9% đã tiệt
trùng
T iêm Iruyền
Dung dịch pha'được dự định đếtruyến đon Iiều. Không sử dụng dung dịch để truyền nếuđung
dịchcó mảu trăng sữa không biên mât sau khi trộn nhẹ nhảng hoặc chứa vật thế lạ hoặc nêu túi
truyẽn bị hỏng.
Tủi truyền phải chứa 25 mL SPORANOX® IV và 50 mL dung môi tiêm Natri Chlorid 0,9%.
PI_Sporanox IV _CCDS 285ep20/0 _v2 12l15
).
0 Chú ỷ: Một đường truyền với bầu đếm giọt không được cung cấp theo bộ kit. Đóng dụng cụ kỉếm
soát dòng chảy (như khỏa van) gắn trên đường truyền. Loại bỏ phẩn có thể bẻ gãy của đầu ra.
Dùng kĩ thuật vô khuẩn, đẩy kim của đường truyền vảo trong cổng ra của tủi truyền.
0 Mở chậm khóa van vả lảm đẩy một nửa bầu đếm giọt bằng cách bóp nhẹ.
Mở khóa van đến khi tất cả các khí bị đầy khỏi dây truyền.
Gắn dây truyền vảo cải khóa van hai đầu cùa dây nối.
Dịch truyền SPORANOX® bây gỉờ đã sẵn sảng đề truyền cho bệnh nhân.
Chinh tốc độ truyền là 1 mL/phút (khoảng 25 giọt/phủt) bằng cảch chinh van lưu lượng (van
xoay hoặc bơm truyền).
Truyền 60 mL dung dịch thuốc đã pha nảy cho bệnh nhân trong khoảng 1 giờ.
Ngưng khi đã truyền được 60 mL.
Lưu ý rằng 200 mg itraconazole đă được truyền cho bệnh nhân.
Tráng đường truyền theo cảc thao tác mô tả bên dưới.
Thao lác Irảng ống sau khi truyền:
0 Sau khi truyền, phải trảng ống để lảm sạch catheter. Điều nảy được thực hỉện nhằm tránh cảc
vấn đề tương kỵ thuốc giữa lượng itraconazole đọng ở cathetcr và những thuốc khảc mã có thế
được tmyên sau đó qua cùng một catheter.
o Trảng óng nối và catheter bằng 15— 20 mL dung dịch vô trùng natri chlorid 0, 9% ờ … óa ,
van 2 đầu, ngay trưởc bộ lọc 0 ,2ụm trong ống ửẨỷĩ/
o Tráng bằng dòng chảy liên tục từ 30 giây đến 15 phút.
0 Sau khi trảng, gỡ và bỏ tủi đựng dịch truyền, dây truyền vả dây nối.
o Không được khử trùng lại và dùng lại bộ dụng cụ truyền của SPORANOXỂ
Đế tránh kết tủa, những thuốc khác chi được truyền qua catheter sau khi đã tráng ống. `
Nêu đang dùng Ioại cathctcr nhiêu ông, không được tiêm các thuôo khảo trước khi truyẽn xong
SPORANOX® W và catheter đã được tráng xong.
l. Tủi dịch truyền natri chlorid
2. Òng tiêm SPORANOX® N
3. Dây truyền với bầu đểm giọt (không kèm theo bộ)
4&5 Dây nối với khóa van 2 đầu vả bộ lọc trong ống
Pl_Sporanox ] V _CCDS 285ep2010_v2 13… 5
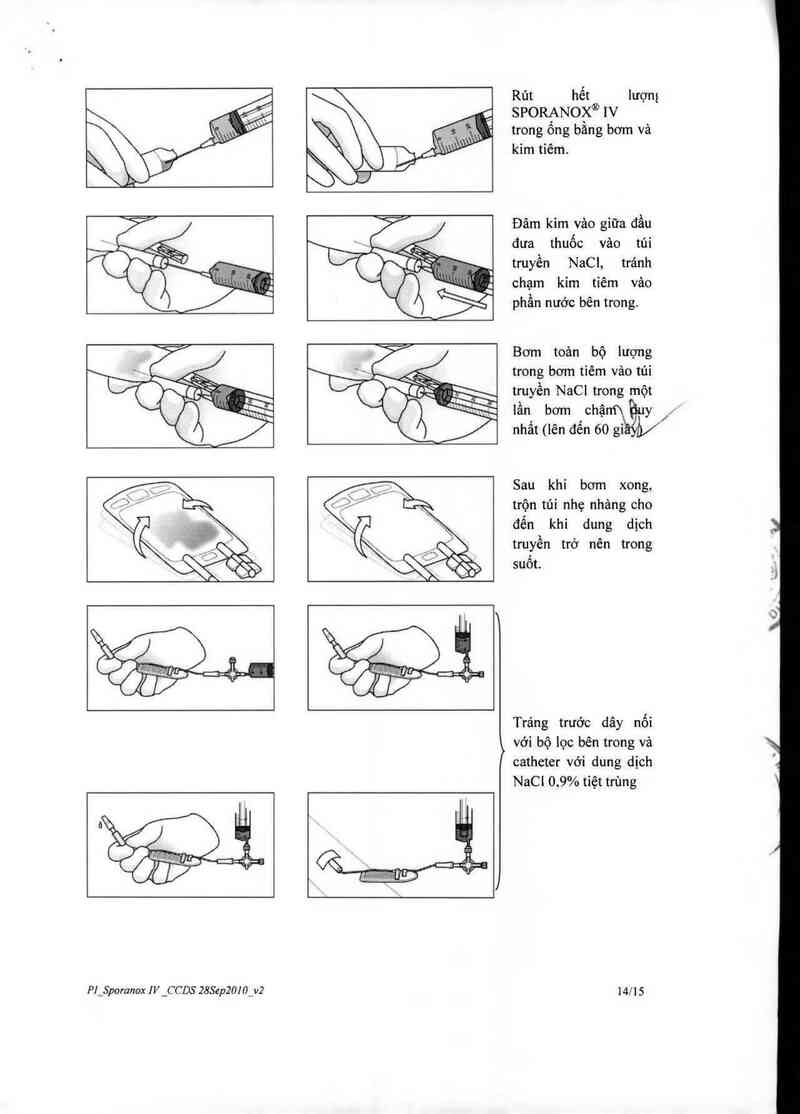
Rút hết htợm
SPORANOX® w
trong ống bằng bơm và
kim tiêm.
Đâm kim vảo giữa đầu
đưa thuốc vảo tủi
truyền NaCl, tránh
chạm kim tiêm vảo
phần nước bên trong.
Bơm toản bộ lượng
trong bơm tiêm vảo túi
truyền NaCl trong một
lần bơm chậnĩ\Ồu
nhất ( Ien đến 60 gihyby/
Sau khi bơm xong,
trộn túi nhẹ nhảng cho
đến khi dung dịch
truyền trở nên trong
suốt
Trảng trước dây nối
> với bộ lọc bên trong vả
catheter với dung dịch
NaCI 0.9% tiệt trùng
PI _Sporanox [ V _CCDS 28Sep2010_v2 14H 5
_ Loại bỏ phần có thể bẻ
/ —~ gãy ở đầu ra cùa tủi
truyền NaCl vả đâm kim
của dây truyền vảo.
Lâm dầy dây truyền vớ
dung dịch SPORANOX°
w đã pha và gắn với dâj
nối có bộ lọc bên trong
Điều chinh tốc độ truyềt
lmL/phút (khoảng 21
giọt/phủt)
Ngừng khi đã truyền
được 60mL sau khoảng
một giờ. Sau khi hoản tất
việc truyền, dây nối với
bộ lọc bên trR vả .,
cathctcr phải đượỀ Ing/’
với 15 - 20mL dung địch
NaCI 0,9% đã tiệt trùng.
Gỡ vả bỏ tủi đựng dịch
truyền, dây truyền vả dây
nối.
Di
Li
Đọc kỹ hướng dẫn sử dụng trước khi dùng.
Nếu cẩn thêm thông tin, xin hỏi ý kiến bác sĩ.
Thuốc nây chỉ dùng theo sự kê đơn của thẩy Ihuốc.
Giữ thuổc ngoải tồm tay trẻ em.
Sãn xuất và xuất xưởng ống thuốc SPORANOX® [V tại:
GlaxoSmithKline Manufacturing S.p.A.,
Strada Provincialc Asolana N.90 (loc. San Polo)- 43056 Torrilc (PR), Ý.
Sản xuất tủi dung môi pha truyền NaCl 0,9%:
Catalent France Limoges SAS,
rue de Dion Bouton — ZI Nord, 87000 Limoges, Pháp
Đóng gỏi thứ Cẩp và xuất xưởng bộ sản phẫm (bộ kit) tại:
Lusomedicamenta Sociedade Tecnica Farmaceutica, S.A.,
Estrada Consiglicri Pedroso, 69 -B, Queluz de Baixo, 2730—055 Barcarena, Bồ Đảo Nha.
Công ty đãng ký: JANSSEN-CILAG Ltd., Thái Lan
Mọi câu hỏi/Báo cáo tảc dụng ngoại ý/ Than phiền chẩt lượng sản phẫm xin liên hệ:
VPĐD Janssen-Ciiag Ltd., TP Hồ Chí Minh.
ĐT: +84 8 382148²8
E-mail: ìacvndrugsafetvỉaìits.inì.com
Pl_Sporanox I V _ C C DS 285ep2010_v2 l 5/ 15
TUQ. cục TRUỞNG
P.TRUỞNG PHÒNG
~JJL"
" iFẢẢKẸÌẮ \ Ộ\`uẺ `NkU “\
t 1…um mgmc
”il"' ~.`.iỄỉ LHỈ'ỌA
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng