





xMMXZCMQ
Scaled of 90% WL
’IIlEIXDEIdS
XL
BỘ Y TẾ
CLF QL'AAN LÝ DUớC
ĐAPHEDUYỀT
MờL/OJJA
Lãn đfiueễấủẢ/i/iệ
ẳtu ogg dSIì salnsde_) .IỊUỊpJaJ
1LLEIXDHdS
auỊogpam uonduosaid g
SPECXETIL
”[LLEIXDÊIcIS
THẢNH PH : cừng chứa -
Cefdinir USP ................................ 300 mg V’rChỔW
J cn! ĐỊNH, CHÓ_NG ỌHI ĐỊNH. LIEU DUNG,
i CACH DUNG VA_ CAC THÔNG TÌN KHAC:
Xem từ hướng dán sử dụng.
Báo quán ở nhiệt dộ dưới 30°C, nơi khô mát
tránh anh sáng vá tránh ảm
Tiêu chuán: usp_az
Đọc kỹ hưởng dán_sừ dụng truớc khi dùng
Không _dùng quá liêu chn đinh
Đê xa tâm tay ttè em 8
Hộp 01 vỉx 10 viên
901. DLH Park. S.V.Road,
Goregaon (West). Mumbai - 400 062. INDIA.
llWlil
906015|10100
'ILLHXDEIdS
DNNK/Importer-
nm mỆu
N hãn hộp .TẬIỞTHẦNH PHỔ l
Ẹ Prescnphon medicme
SPECXETIL
Cefdinir Capsules USP 300 mg
Manufactured by:
composmon:
Each c_apsule contains: Zl M LABO RATORl ES LTD
Cefdmưusp ., 3°° mg Plotnos B-21.22.M1.0.0Are8.
Store beiow 30°C in cool. div place. protected trom light Kalmeshwar. Nagpur — 441501 Maharashtra, INDIA
and rnoisture Manufacture for:
Mfg. Lic. No.: v:rchow w
MEALTNCARE PRIVAYE LIMITED
Baich No
› 901 .DLH Park. S v Road.
Exp Dale. ddimmlva Goregaon (West), Mumbai … 400 062 lNDIA
m_u mỆn
m THÀNH PHỐ '
iiõ chỉ mua
Nhãn vỉ ’
SPECXETIL
(Cet'dinỉr 300 mg)
THÀNH PHẢN
Mỗi viên nang có chứa:
Hoạt chất: Cefdinir USP ......... 300 mg
Tả dược: Natri lauryl sulphat, magnesi stearat, natri tinh bột glycollat, bột talc, nang E.H.G. cỡ số “1”
cÁc ĐẶC TÍNH DƯỢC LÝ:
Duoc lưc hoc:
Cũng như cảc cephalospon'n khảc, hoạt tính diệt khuấn cùa cefdinir do sự ức chế tồng hợp thảnh tế bảo. Cefdinir ốn định
với sự có mặt cùa cảc loại enzym B-lactamase.
Cefdinir cho thấy có hoạt tinh đối với với cảc Ioải vi khuẩn sau:
Vi khuẩn Gram dương hiếu khi:
— Staphylọcoccus aureus (bao gổm các loảỉ vi khuấn sinh ra 6— —lactamase)
GHI C HU Cefdinỉr vô hoạt đôi với staphylococci đề kháng với methicillin.
~ Srreptococcus pneumoniae (chi có loải vi khuắn nhạy cảm với penicillin)
— Sireptococcus pyogenes
Vi khuấn Gram âm hiếu khí
- Haemophilus induen. ae (bao gồm các loải vi khuấn sính ra B—lactamase)
- Haemophilus parainjiuenzae (bao gổm các Ioải vi khuấn sinh ra B—lactamase)
- Moraxella catarrhalis (bao gồm các loải vi khuấn sinh ra 13-lactamase)
Cefdinir thế hiện nồng độ ức chế tối thiểu in vitro (Mle) ở 1 ụg/mL hay thấp hớn đối với các loải vỉ khuấn (> 90%) sau
đây; tuy nhiên độ an toản & hiệu quả cua cefdinir trong việc đỉều trị các nhiễm trùng lâm sảng do cảc vi khuấn nảy chưa
được thỉểt lặp trong cảc nghiên cửu lâm sảng đủ & kiềm soát tốt
Vi khuẩn Gram dương hiêu khí
StaphylocOccus epidermidis (chi với loải vi khuẩn nhạy cảm với methicillin), Streptococcus agalactiae. srrepiococci
nhóm Virìdans
GHI CHÚ: Cefdinir bất hoạt với Enterococcus & giống Slaphylococcus đề kháng vởi mcthicillin
Vi khuấn Gram âm hiếu khí
Citrobacter diversus. Escheríchia coli. Klebsiella pneumoniae. Proleus mìrabilis
GHI CHÚ: Cefdinir bất hoạt với giống Pseudomonas vả Enterobacter
Dược động học:
HấD thu
Sinh kha dung đường uống
Nổng độ cefdinir tối đa trong huyết tương đạt đuợc vảo 2—4 giờ sau khi dùng uống thuốc dưới dạng viên nang hay hỗn
dịch. Nồng độ cefdinir huyết tưong tăng theo liều, nhưng sự tảng nảy it hơn với Iiểu từ 300 mg (7 mg/kg) đến 600 mg (14
mglkg). Nếu người trướng thảnh khờe mạnh dùng thuốc dưới dạng hỗn dịch, sinh khả dụng của cefdinir là 120% so với
viên nang. Sinh khả dụng ước tinh cùa viên nang cefdinir là 21% với liều viên nang 300 mg, & 16% với vìên nang 600
mg Sinh khả dụng tuyệt đối uớc tinh cùa hỗn dịch cefdinir là 25%. Dạng hỗn dịch uống cefdinir 250 mg/S mL tương
đương sinh học với 125 mg/S mL ở người trường thảnh khóe mạnh trong điều kiện uống nhanh.
Anh hưởng cu`a thửc ăn
Cmax & AUC cùa cefdinir dạng viên nang giảm theo thứ tự 16% & 10%, khi dùng với bữa an giản mớ. Ở người trường
thảnh khi dùng dạng hỗn dịch uỏng 250 mgl5 m. với bữa ăn giảm chất béo, Cmax & AUC của cefdinir giám theo thứ tự
44% & 33%. Độ lớn của sự giảm nảy dường như không khác biệt về lâm sảng Vì vậy, có thể uống cefdinir có hoặc
khõng kèm thức ãn.
Viên nang cetdim'r
Nổng độ cefdinir huyết tương & cảc giá trị thông số dược động học sau khi uống Iiểu đơn aoo- & 600-mg cefdinir ở người
truớng thảnh trong bảng sau:
Cảo giá trị thông số dược động học cefdinir huyết tuơng trung binh (tSD) sau khi UJ viên nang ở người trướng thảnh
Líều Cmax tmax AUC
(ụg/mL) (giờ) (ụg-giờ/mLì
300 mg 1,60 (0,55) 2,9 (0,89) 7,05 (2,17)
600 mg 2,87 (1,01) 3,0 (0,66) 11,1 (3,87)
Cefdinir không tích lũy trong huyết tương khi uống 1 hay 2 Iầnlngảy ở những đối tượng có chức năng thận binh thường
P__hân bố:
Thể tích phân bố trung binh (Va) của ccfdinir ở người trướng thảnh là 0, 35 leg (i 0,29); ở đối tượng nhi (tuồi 6 thảng-IZ
tuổi), cefdinir V,, là 0,67 leg (i 0,38). Cefdinir gắn vảo protein huyết tương 60% đển 70% ở cả người trướng thảnh & đối
tượng nhi; sự găn kểt là độc lập với nông độ.
Mô da rỏg Ở người trướng thảnh nồng độ cefdinir tối đa là 0,65 (0 33-1 1) & 1,1 (0,49-1,9)pg1mL đuợc thẳy là 4 đến 5
giờ sau khi uống viên nang theo thứ tự liếu 300- & 600-mg Các giá trị Cmax & ẨUC trung bình theo thứ tự là 48% (x 13)
& 91% (t 18) của các giá trị huyết thanh tương ứng
Mỏ amiđan Ó nguời trướng thảnh đang phẫu thuật cắt amiđan chọn lọc, nổng độ cefdinir ở mỏ amiđan trung binh tương
ứng với 4 giờ sau khi uông liều đơn 300- & 600- -mg lả 0,25 (0, 22- 0 ,46) & 0,36 (0,22-0 80) 11ng Nồng độ mô amidan
trung binh 1ả24% (i 8) nông độ huyết tương tương ửng
Mỏ xoang 0 người trưởng thảnh đang phẫu thuật xoang xương sảng & xoang hảm trên chọn lọc, nồng độ cefdinir mô
xoang trung bình tương ứng 4 giờ sau khi uỏng liều đơn 300 & 600 mg lả < 0,12 ( < 0,12-0,46) & 0 ,21 ( < 0, 12- 2 ,O) ụglg.
Nổng độ mô xoang trung bình lả 16% (_:i: 20) nông độ huyết thanh tương ứng
Mỏ nhỏ:" Ó nguời trường thảnh đang trải qua phép soi phế quản chần đoản, nồng độ cefdinir nỉẻm mạc phế quản trung
binh tương ứng4 giờ sau liều đớn 300- & 600-mg1ả0 78 ( < 0, 06- 133) & 1 14( < 0, 06- 1,92) ụgmL, & 1ả 31%(t18)
nồng độ huyết thanh tương ứng Nồng độ nội mô trung binh tương ứng là 0 29 (< 0, 3-4 ,73) & 0,49 (< 0, 3- 0 ,59) ụg/mL, &
là 35% (3: 83) nổng độ huyểt thanh tương ứng
Tai giữa. Trong SỐ 14 bệnh nhi bị viêm tai gìữa di vi khuắn cẳp tinh, nồng độ cefdinir trong chắt dịch tai giữa tương ứng
3 giờ sau khi uỏng liều đơn 7- & 14— —mgỉkg lả 0 ,21 ( < 0 ,09-0 ,94) & 0,72 (0,14—1,42) ụglmL Nổng độ trong chẩt dịch tai
giữa trung bình lả 15% (t 15) nồng độ huyết thanh tương ửng.
@ Chưa có sẵn thông tin về độ xâm nhập cúa cefdinir vảo dịch não tùy
Chuvền hỏa & bải tiết
Cefdinir không đuợc chuyến hóa đáng kể Hoạt tinh chủ yểu do thuốc gốc. Cefdinir thải trừ chủ yểu qua thận với thời gian
bản hủy trung binh trong huyết tương (IV,) là 1,7 (1: 0 ,6) giờ IỚ đối tượng khỏe mạnh với chức nảng thận binh thường, độ
thanh thải thặn lãi 2 ,0 (i 1 ,0) mLf'phủt/kg, & độ thanh thái đường uỏng là 11,6 (+. 6,0) & 15,5 (3: 5 4) mL/phủt/kg với Iiều
theo thứ tự 300 mg & 600 mg. Phần tram liếu trung binh không đối trong nước tiếu sau liều 300- & 600-mg theo thứ tự lả
18, 4% (zi: 6 4)&11,6%(t 4 6) Độ thanh thải cefdinir giảm ở bệnh nhân rối loạn chức nảng thận
Do sự bải tiết qua thận lả đuờng thải chiếm uu thế nên iiều lượng nẽn được điểu chính ở cải: bệnh nhân với chúc nảng thặn
suy đang kế hay những đồi tượng đang lọc mảu
Dân số đảo biêt ỂỆ7I
- Bệnh nhân suy thận
Dược động học cùa ccfđìnir được nghiên cứu ờ 21 người trưởng thảnh với chủc náng thậnỉhẵy đối Sự giảm ti lệ thải
cefdinir độ thanh thải đuờng uống (CLiF ), & độ thanh thải thận thì tương ửng với sự giảm độ thanh thải creatinine (CLƠ)
Kết quả lả, nồng độ cefdinir huyết thanh cao hơn & kéo dải hơn ở những đối tượng suy thận hơn so với nhung đồi tượng
không suy thận. Ô cảc đối tượng có CLcr giữa 30 & 60 mLiphủt, Cmax & ti,, giảm khoáng 2 lần & AUC giám khoảng 3
lần Ờ cảc đối tượng với CLC, < 30 mLi,phút Cmax giảm khoáng.. 7 1ần, t,, giám khoáng 5 lần, & AUC giảm khoáng 6 lần.
Khuyến cảo chinh liều ờ cảc bệnh nhân suy thận đảng kế (độ thanh thái creatinine < 30 mL/phùt)
- Lọc mảu
Dược động học cua cefdinir được nghiên cứu ở 8 nguời trường thảnh đang lọc mảu Lọc mảu (thời lượng 4 giờ) thải 63%
cefdinir ra khới cơ thể & thời gian bán hủy t, giảm rõ rệt tư 16 (t 3,5) đến 3,2 (zi: 1,2) giờ Việc chinh ]íều được khuyến
cáo ở dân số bệnh nhân nảy.
- Bệnh gan
Vi cefdinir thái chú yểu qua đường thặn & chuyến hóa không đảng kề nên các nghiên cứu ờ các bệnh nhân suy gan không
được thực hiện. Khỏng cẩn chinh Iiều ở dân số bệnh nhãn nảy
- Bệnh nhăn lớn tuổi
Tảc động cùa tuối tác trẻn duợc động học cùa cefdinir sau 1 Iiều đơn 300 mg được đảnh giả ở 32 đối tưọng 19 đến 9]
tuồi. Sự phơi nhíễm toản thân với cefdinir giảm đảng kế ở cảc đối tuợng lớn tuối (N= 16), Cmax đến 44% & AUC đến
86% Sự táng nảy do sự giám độ thanh thải cefdinir Thể tích phân bố cũng giảm rõ rệt, vì vậy không có sự thay đối đảng
kế ở thời gian bản hùy t,, (người lớn tuối: 2, 2 t 0 6 giờ so với người trẻ tuôi: 1, 8 i- 0, 4 giờ). Vì độ thanh thải cùa ccfdinir
cho thắy chủ yếu liên quan đển sự thay đổi chức nãng thặn hơn là tuối tảc, bệnh nhân 1ớn tuồi không yêu cầu đìều chinh
Iiếu nêu họ không bị suy thặn đáng kể (độ thanh thải creatinine < 30 mL/phút).
- Giới tính & Chùng tộc
Kẻt quả cúa 1 phãn tich gộp của cảc dược động học lâm sảng [N = 217) cho thắy không có sự ảnh hướng đáng kể cùa giới
tính hay tuối tảc trên dược động học cùa ccfdinir.
CHỈ ĐỊNH
Nhằm giảm sự phát triền cùa vi khuẩn khảng thuốc và duy tri hiệu quả cùa cefdinir vả cảc thuốc khảng khuấn khác,
cefdinir chỉ nên được dùng để điểu trị hay ngăn ngừa cảc nhiễm trùng mã đã được chửng minh hay nghi ngờ gây ra do vi
khuắn nhạy cảm Viên nang cefdinir được chỉ định trong điều trị bệnh nhân nhiễm trùng mức độ từ nhẹ đến trung binh do
các loảì vi khuẩn nhạy cảm trong cảc bệnh đuợc liệt kê dưới đây:
Nzười miqng thảnh & thanh thiếu niên
- Viêm phôi mắc phái do cộng đồng
Gây ra bới Haemophilus injluenzae (bao gồm nòi vi khuẩn sinh ra B-lactamase), Haemophilus parainfiuenzae (bao gồm
nòi vi khuẩn sinh ra B—lactamase), Slrepiococcus pneumoniae (chi vởi nòi vi khuẩn nhạy cảm với penicillin), & vả
Moraxella catarrhalís (bao gổm nòi vi khuẩn sinh ra [3 iactamasc)
- Viẽm phồi mản tinh tang nậng cẳp tính
IIVI
Do Haemophilus infiuen: ae gây ra (bao gồm nòi vi khuấn sinh ra 13 -lactamasc), Haemophilus parm'nfiuenzae (bao gồm nòi
vi khuắn sinh ra [3- lactamase), Szrepmcoccus pneumoniae (chi với nòi vi khuần nhạy cảm với penicillin), and Morarella
catarrhaiis (bao gôm nòi vi khuẩn sinh ra B- lactamase).
— Viêm xoang hảm trên cẳp tinh
Do Haemophilus infiuenzae gây ra ( bao gổm nòi vi khuẩn sính ra B-lactamase), Slreplococcus pneumoniae (chi vởi nới vi
khuẩn nhạy cảm với pcnicillin), and .Moraxella catarrhali's (bao gồm nòi vi khuần sinh ra B-Iactamase).
- Viêm họngz’Viẽm amidan
Do Srreptococcus sinh mù gây ra.
Các tinh trạng nhiễm trùng đa không phức tạp và nhiễm trùng cẩu trúc da do Sfaphyt'ococcus aureus gây ra (bao gồm nòi
vi khuẩn sinh ra B—lactamasc) vả Streplococcus pyogenes.
Bênh nhân nhi
- Viêm tai giữa cấp tinh do vi khuẩn
Do Haemophiluổ infiuen:ae gãy ra (bao gổm nòi vi khuẩn sinh raB- lactamase), Srreptococcus pneumoniae (chi với nòi vỉ
khuấn nhạy cám với pemcdlm ), and Morarella catarrhaiis (bao gõm nòi vi khuấn sinh raB lactamase).
- Viêm họng,;Viêm amidan
Do Sireptococcus sinh mù gảy ra
Các tinh trạng nhiễm trùng da không phủc tạp và nhỉễm trùng cấu trúc đa
Do Staphylococcus aureus gảy ra (bao gôm nòi vi khuẩn sinh ra [3-1 actamase) vả Streptococcus pyogenes
UÊULUỢNGVÀCÁCHSỬDỤNG
Liều khuyến cáo & thời gian điều trị đối với nhiễm trùng ớ người 1ón & thanh thiểu niên được mô tả trong sơ để dưới
đây; tồng liều hảng ngảy cho tất cả cảc tinh trạng nhiễm trùng lả 600 mg. Liềul lần mỗi ngảy trong suốt 10 ngảy cũng
hiệu quả như lìều 2 lằn mỗi ngảy Liều ] lấn môi ngảy chưa được nghiên cứu trên viêm phối hay nhiễm trùng da; vì vậy,
nên dùng viên nang cefdinir 2 lần mỗi ngảy đổi với các tinh trạng nhiễm trùng nảy, Có thế uỏng viên nang cefdinir không
phụ thuộc vảo bữa án.
Người rrướng thảnh & thanh thiếu niên 72 13 Iuồi)
Loại nhiệm ir_ùng Liều lượng Thời gian
Viêm phôi mão phải do cộng đông 300 mg mới 12h 10 ngảy
Đọ1 cắp tính vỉêm phế quản mản tính ịẵẵ Ệẳ Tnôỗii 122Jihhoặc ĨOđẳịảlyo ngảy
Viêm xoang hảm trên cắp tinh ịẵẵ ỆỄ Ẹẵẫ ẩẫE hoặc ẫẵ Zẳẳỉ ÍỰ /
Viêm họnngiêm amidan ẫẵẵ Ệẳ ỆỄỈ ẳỉhhh°ặc io ảẵà'ịgày ư
M …
Bénh nhản suy Jhản
Đối với người trường thảnh có độ thanh thái creatinine < 30 mLzmin, Iiều cefdinir nên lả 300 mg l lấn mỗi ngảy.
Bệnh nhi có độ thanh thải creatinin <30 mbmin/l, 73 … ,nên dùng liếu 7 mg/kg (tối đa 300 mg) 1 lẳn mõi ngảy
Bénh nhân lọc máu
Phương phảp lọc máu sẽ thải trừ cefdinir khói cơ thể Ở cảc bệnh nhân duy trì chế độ lọc mảu mãn tính ,liếu điều trị khớỉ
đầu được khuyến các lá 300— —mg hay 7 mg/kg mỗi ngảy Ở phần cuối cùa mỗi giai doạn iọc mảu nên dùng 300 mg (hay 7
mg/kg). Cảc liều tiểp theo (300 mg hay 7 mgfkg) được dùng mõi ngảy tiểp theo
Đường dùng lhưồc: đường uống
CHỐNG CHỈ ĐỊNH:
Cefdinír chống chỉ định ở cảc bệnh nhân có cơ địa dị ứng vời nhóm kháng sinh cephalosporin hay mẫn cảm với bất kỳ
thảnh phần nảo của thuốc
TÁC DỤNG PHỤ
Tác dung ohu THÔNG THƯỜNG
- Tiêu cháy, nhức đầu, buồn nôn
Chú v nếu có bẩt cứ tác dung ghu NGHIÊM TRONG nảỵ xảv ra khi dùng ccfdinir
Phản ứng dị ứng nghiêm trọng (mẫn đớ; phát ban; ngứa; khó thớ; nạng ngực; phù miệng, mặt, môi hay lưỡi); phăn có máu;
thay đồi lượng nước tiêu; nước tiều sẫm mảu; sốt, lạnh run, hay đau họng; da đó, sưng, phồng hay lột da; động kinh; tiêu
cháy nặng hay ỏi mưa; đau dạ dảy nặng hay vọp bé; chảy mảu hay bẩm tím bẩt thường; kich thich âm đạo hay tỉểt dịch;
vảng da hay mắt
Cảc nehiên cứu iâm sảng- Viên nang cefdinir ( Noươi lớn hav thanh thiểu niên)
Trong cảc nghiên cứu lâm sảng, 5093 người lớn & thanh thiểu niên (3841 người Mỹ & 1252 không phái người Mỹ) được
điều tri với liều viên nang cefdinir khuyến cáo (600 mg ngảy) Hẳu hết cảc tác dụng phụ ngoại ý đểu nhẹ & tự giới hạn
Khớng có tư vong hay tản tật vĩnh viên do cefdinir 147 trong Số 5093 (3%) bệnh nhán khỏng tiẽp tục dùng thuốc do tảc
dụng phụ ngoại ý được các nhả chuyên gia cho rằng có khả nảng & chẳc chắn liên quan dến điều trị vởỉ cefdinir Việc
ngừng thuốc nảy chú yểu lả do rôỉ loạn đường tiêu hóa, thưởng là tiêu chảy hay buồn nôn 19 trong số of 5093 (0 ,4%)
bệnh nhân ngừng thuốc do mẫn đỏ được nghĩ là liên quan đến việc dùng cefdinir
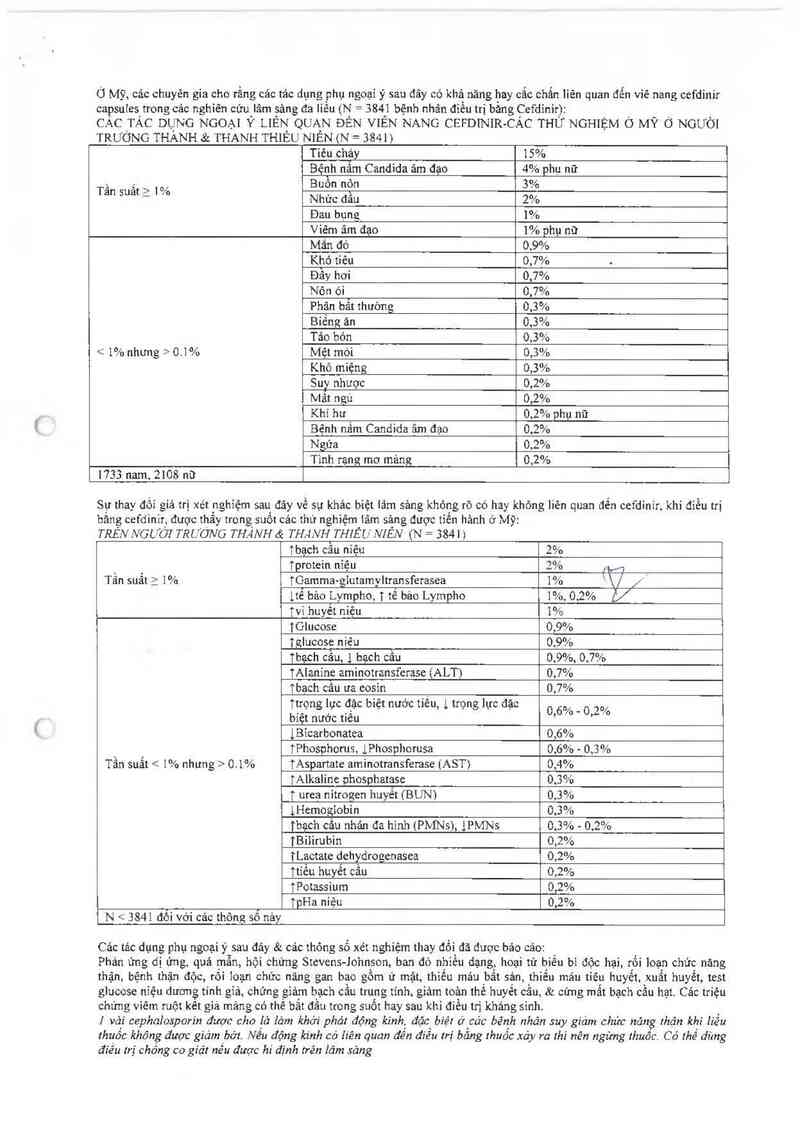
Ở Mỹ, cảc chuyên gia cho rằng các tảo dụng phụ ngoại ý sau đây có khả nảng hay cẳc chẳn liên quan đến vỉẽ nang cefdinir
capsuies rrong các nghiên cứu lâm sảng đa liều (N= 3841 bệnh nhân điểu trị bằng Cefdỉnỉr):
CÁC TẢC DỤNG NGOAI Ý LIỂN QUAN ĐỂN VIÊN NANG CEFDINIR- CẢC THỬ NGHIỆM Ở MỸ Ở NGƯỜI
TRUÓNG THÀNH & THANH THIỂU NIÊN (N= 3841)
Tiêu chảy 15%
Bệnh ã… Candỉda âm đạo 4% phụ nữ
` ` 0
Đau bụng 1%
Viêm âm đạo 1% phụ nữ
Mản đó 0,9%
Khó tiêu 0,7%
Đây hơi 0,7%
Nôn ÓỈ O,7°fo
Phân bât thường 0,3%
Biếng án 0,3%
Táo bón 0,3%
< 1% nhưng > 0.1 % Mệt mòi 0,3%
Khô miệng 0,3%
Suy nhược 0,2%
Mẫt ngư o,:m
Khi hư 0.2% phụ nữ
Bệnh nắm Candỉda âm đạo 0.2%
Ngứa 0,2%
Tình rạng mơ mảng 0,2%
1733 nam, 2108 nữ
Sự thay đồi giá trị xét hghỉệm sau_ đây về sự khảc biệt lâm sảng không rõ có hay khỏng liên quan đến cefdinir, khi điều trị
băng cefdinir, được thãy trong_suôt cảc thừ nghìệmị1âm sặng được tỉên hảnh ở Mỹ:
TRE:V NGƯO'Ỉ TRƯONG THANH & THANH THIELJ'NÍEN (N = 3841)
Tbạch cẳu niệu 2%
Tproteỉn nỉệư 2% ,M
Tần suất 2 1% TGamma-glutamyltransferasea 1% \\] /
Ltễ bảo Lympho, )” tê bảo Lympho 1%, 0,2% V
Tvi huyết niệu 1%
TGlưcose 0,9%
ĩglucose niệu 0.9%
Tbạch câu, ) bạch câu 0,9%, 0,7%
TAlanine aminotransferase (ALT) 0,7%
Tbạch câu ưa eosin 0,7%
Ttrọng lực đặc biệt nước tiều, L trọng lực đặc
.. . ., °/ -02°/
biẹtnươc ueu 0’6 o ’ “
J,Bĩcarbonatea 0,6%
TPhosphorus, )Phosphorusa 0,6% — 0,3%
Tần suẳt < 1% nhưng > 0.1% TAspartate aminotransferase [AST) 0,4%
1'Alkaline phosnhatasc 0.3%
T urea nitrogen huyết (BUN) 0,3%
LHemoglobin 0.3%
Tbạch cấu nhân đa hình (PMNs), lPMNs 0,3% - 0,2%
TBilirubin 0,2%
ĩLactate dehydrogenasea 0,2%
Ttiếu huyết cẩu 0,2%
TPotassium 0,2%
TpHa niệu 0,2%
N < 3841 đối với các thông số nảy
Cảc tảo dụng phụ ngoại ý sau đây & cảc thỏng số xét nghiệm thay đổi đã được bảo cảo:
Phản ứng dị ứng quả mân, hội chửng Stevens-Johnson, ban đỏ nhìểu dạng, hoại từ biến bỉ độc hại, rối loạn chức nảng
thận, bệnh thận độc, rôi loạn chửc năng gan bao gõm ứ mặt, thiếu máu bắt sản, thiếu mảu tiêu huyết xuất huyết, tcst
glucose nỉệu dương tính giả, chứng giảm bạch cầu trung tính giảm toản thế huyết cần, & cứng mất bạch cầu hạt. Các tríệu
chứng viêm rưột kêt giả mảng có thể bắt đầu trong sưôt hay sau khi điểu trị khảng sinh.
] vải cephaiosporin được cho Ia` Iờm khời phải động kinh đặc bi_êr ở cảc bênh nhân suy giám chửc nãng rhận khi Iiếu
!huốc không được giảm bớt Nếu động kinh có Iíên quan đến điểu Irị bằng thuốc xáy ra lhi nên ngừng thuôo Có rhế dùng
đíếu trị chống co giặt nếu được hi dịnh !rẻn lâm sảng
Thông bảo vói Bác sĩ các tác dụng phụ gập phải khi sử dụng rizuốc.
LƯU Ý KHI SỬ DỤNG
Cảnh báo: _ _
Trước khi bắt đằu điếu trị với cefdinir, nên tìm hiêu cân thặn nhằm quyết định Iiệu các bệnh nhân đã có phán ứng quả
nhạy cảm trước đó với cefdinir các cephalosporin khác, penicillins, hay các thuốc khảo. Nén thận trỌng nểu ccfdinir được
điểu trị cho bệnh nhân nhạy cảm với penicillin vi có ghi nhận rõ rảng sự quá nhạy cảm chéo giữa các khâng sinh nhỏm B—
Lactam & có thể xảy ra ở đến 10% bệnh nhân có tiền sử dị ứng penicillin. Nếu có phản ưng dị ứng với cefdinir xảy ra thì
nên ngừng thuốc. Phản ứng quả nhạy cảm trầm trọng cấp tinh có thể đòi hòi phái điều trị với epinephrin & các phương
phảp đánh giá khấn cấp, bao gôm oxygen, truyền dung dịch tĩnh mạch truyền tĩnh mạch kháng histamin, corticosteroid,
cảc amin tâng ảp, & quản lý đường thớ, như đã chỉ định trên lâm sảng
Tình trạng tiêu chảy iiên quan đến C Ioslridium difflcile đã được báo cảo với việc sư dụng gần như tất cả cảc thuốc khảng
vi khuân, bao gôm cả ccfdínir, & có thể phân loại độ nghiêm trọng tử tiêu cháy nhẹ đến viêm ruột kết gây rư vong Việc
điểu trị vởi các thuốc khảng vi khuẩn sẽ iảm biến đổi quân thế vi khuẩn bỉnh thường cùa ruột kểt dẫn đến sự tăng trướng
quá múc của C. difflcile
C dịfflciie san sinh các độc tố A & 8, góp phần vảo vỉệc phảt triền tinh trạng tiêu chảy iiên quan đến Clostrz'dium
diffl`cile Việc tảng cảc chất độc gây ra bởi cảc loải vi khuẩn C df'jjĩcile gây ra tinh trạng bệnh tật & tử vong gia tảng, vì
những tinh trạng nhiễm trùng nảy có thế khó chũa đối với cảc điều trị kháng khuẩn & có thể dẫn tới cắt ruột kểt. Tình
trạng tiêu chảy liên quan đến Closzridium d fi` c:lẹ phải được xem xét ở tẳt cả cảc bệnh nhản đang bị tiêu chay do sư dụng
khảng sinh. Xem xét tiến sư y khoa cấn thận lá. cân thiết vi tinh trạng tiêu chảy liên quan đến C!ostridium dịfflcile đă được
bảo cáo lả xảy ra suốt 2 tháng sau khi dùng các thuốc kháng khuấn
Nếu tinh trạng tiêu chảy Iiẽn quan đển Cỉostridium difflcile (CDAD) bị nghi ngờ hay khâng định, việc đang đùng kháng
sinh mà không phải để diệt C dfflicile có thể không được tiêp tục. cung câp chẩt dinh dưỡng & điện giải cân thiết, bổ sung
protein, đỉểu ttị khảng sinh dối với C dfflciỉe, & đảnh giá giải phẫu nên được bắt đầu như được chỉ định trên iâm sảng.
Thận trọng
- Vìệc kẽ toa ccfdinir trong tinh trạng thiếu bằng chứng về viêm do vi khuẳn hay chỉ định dự phòng không chắc mang lại
lọi ich cho bệnh nhân & lảm tãng nguy cơ phảt triên vi khuần kháng thuốc
- Do với các khảng sinh phố rộng khảc vỉệc điếu trị kéo dải có thẻ dẫn đển tình trạng bùng phả) & táng rrướng quá mức
cùa các sinh vật đề kháng nên vỉệc gỉảm sảt bệnh nhân cãn thận lả cấn thỉểt Nếu tinh trạng nhiễm trùng nghiêm trọng xáy
ra trong quả trinh đỉều trị thì nên ảp dụng đỉếu trị thay thể thích hợp.
Cefdínir, như cảc khảng sinh phố rộng khảo, nên được kê toa ] cảch thận trọng ở cảc bệnh nhân có tiển sư viêm ruột kết.
Ở các bệnh nhân suy thận (creatinine clearance < 30 lephủt), nên giảm tống liều hẳng ngảy cùa cefdinir _
Khá nãng sinh ung !hư. khá nãng sinh dột biên suy giảm chức năng sinh sán (“Ý
Khả nảng gây ung thư cùa ccfdinir chưa được đánh giá. Không thẳy tảo dụng gây ung thư trong phép phả ch đột biên
đảo ngược vi khuần hay phép phân tích đột biến điếm Khỏng thấy tảc động gây vô nhìễm sãc thể … vitro trồng phép phân
tích quang sai cấu trúc nhiễm sâc thế hay' … vivo trong phép phân tich vi nhân ở tùy xương chuột. Ó chuột, khả nảng sinh
sản không bị ánh hưởng bới cefdinir ớ liều uống lẽn đến) 1000 mg/kgfngảy (gắp 70 lần ỉiều ớ người dựa trẻn mg/kg; ngảy,
gấp 11 lần dựa trên mg/mẵv’day).
Sử dụng ơ trẻ nhí:
Độ an toản & hiệu quả ở trẻ sơ sinh & nhũ nhi dưới 6 thảng tuốì chưa được thảnh lập Việc sử đụng cefdinir trong điếu Irị
viêm xoang. hảm trẻn ở bệnh nhân nhi (tuối tù 6 tháng đến 12 tuổi) được ửng hộ bời bằng chứng từ cảc nghìên cứu kiềm
soát đủ & tốt ở người trướng thảnh & thanh thiếu niên, sinh lý bệnh viêm xoang cẳp tương tự ở người iởn & trẻ nhi, & dữ
liệu dược động học so sánh ớ dân số bệnh nhi
Sử dung ở người lớn mói:
Hỉệu quả có thế so sảnh được ớ bệnh nhân lởn tuồi & người trướng thảnh trẻ tuồỉ. Trong khi ccfđinir được dung nạp tổ) ớ
lất cả cảc nhỏm tuối, thì trong cảc nghiên củư lâm sảng, ở bệnh nhân lớn tuối xuất hỉện tỉ lệ thấp hơn tác dụng phụ ngoại ỷ,
bao gổm tiêu chảy, hơn người trưởng thảnh trẻ tuối. Việc điếu chinh lỉểư ở bệnh nhân lớn tuốỉ iả không cằn thìết nểu chủc
năng thặn không suy giảm đảng kế.
TƯỚNG TÁC THUỐC
Thuốc kháng acid (chứa nhôm hay magnesi)
Việc dùng kèm 300-mg viên nang cefdinir vởi zo mL hỗn dịch chửa nhôm hay magnesi lảm giảm nồng độ tối đa (Cmax)
& diện tích dưới đường cong (AUC) cùa sự hấp thu khoảng 40%. Thởi gian đạt Cmax kéo dải khoảng 1 giờ. Không có ảnh
hưởng đảng kể trên dược động học cùa cefdinir nếu dùng thuốc khảng acid 2 giờ trước hay sau khi uống cefdinir. Nếu cẳn
dùng thuốc kháng acid suốt thòi gian điều trị với ccfdinir, thì nên uống cefdinir ít nhất 2 gỉờ trước khi hay sau khi dùng
thuốc kháng acid
Probenecid: Cũng như các khảng sinh B-lactam khác, probenecid ức chế sự bải tiết cefdinir qua thận, dẫn đến tảng gắp
đôi AUC, tăng 54% nồng độ cefdinir đinh trong huyểt thanh & sự kéo dải thời gian bán thải tự, rõ rảng đến 50%
Chẩt bổ sung sẳt & các thức ãn gỉảu chẫt sắt
Vỉệc dùng đồng thới cefdinir với ! thưốc điều trị bổ sung sắt chứa 60 sẳt nguyên tố (như FeSO,J hay cảc vitamin bổ sung
10 mg sãt nguyên tố sẽ lảm gìảm sự hấp thu Iẳn lượt 80% và 31% Nếu cấn bổ sung sắt suốt quá trinh điếu trị với cefdinir,
thì nên đùng cefdinir tối thiều 2 giờ trước hay sau khi dùng sắt
Ánh hướng cùa thức ản giản chất sẳt (chủ yếu là cảc ngũ cốc ản sáng giảm chất sẳt) lên sự hẳp thu ccfdinir chưa được
nghiên cứu
Đã có báo cảo về đi tiêu phân hơi đỏ của bệnh nhân dùng cefdinir Trong nhiều trường hợp, bệnh nhân cũng đang dùng
cảc chế phầm chứa sắt. Mảu hơi đó là do sự hình thảnh 1 phức hợp không hắp thu giữa cefdinir hay các sản phẩm giáng
phân cùa nó vả sắt trong ống tiêu hóa
SỬ DỤNG Ở PHỤ NỮ có THAI VÀ CHO CON BÉ“
Có thai. phân loại B
Cefdinir không sinh quải thai trên chuột ở liều uống lên đến 1000 mg/kg/ngảy (gấp 70 lần 1iểu ở người dựa trên
mglkg/ngảy, gâp 11 lần dựa trên mg/mZIngảy) hay trên thò ở iiều uống lên đến 10 mg/kg/ngảy (gấp 0 7 1ần liểu ở người
dưa trên mg/kglngảy; gấp 0,23 iần dựa trén mglmzfngảy). Độc tính trên mẹ (giảm tảng cân) được quan sảt thấy ở thò ớ 1iểu
dung nạp tôi đa đên 10 mglkglngảy mã không có tảc dụng phụ ngoại y' trên con cái. Tình trạng giảm cân năng xảy ra ở bảo
thai chuột ở 1iểu_ > 100 mg/kglngảy, & ở chuột con ở liều_ > 32 mg/kg/ngảy Không quan sát thây ảnh hưởng trên thông số
sinh sản ở mẹ hay sự sống còn cùa con, sự phát triền, hảnh vi, hay chức năng sinh sản.
Vì vậy, tuy nhiên. chưa có đủ các nghiên cứu trên phụ nữ có thai. Vì :ca'c nghiên cứu trên khả năng sinh sản của động
vật không luôn !uõn dự đoán về đáp ứng của người nên thuốc nảy chỉ được dùng suốt thai kỳ nếu thật sự cần thiết.
Phụ nữ đang cho con bú: Không phát hiện cefdinir trong sữa mẹ ở liếu đơn 600 mg.
TẢC ĐỌNG LÊN KHẢ NĂNG LÁ1 XE VÀ VẶN HÀNH MÁY MÓC:
Chưa có bảo cảo
QUÁ LIÊU
Thông tin về việc quá liều trên người chưa có sẵn. Trong cảc nghiên cứu về độc tinh trên chuột cấp, 1 liều đơn dạng uống
SóOO-mg/kg không gây tảc dụng phụ ngoại ý. Cảc dầu hiệu & các triệu chứng độc tinh do quá liều với các khảng sinh [3-
lactam khác bao gôm buổn nôn, nôn ói suy thượng vị, tiêu chảy, & co giật. Lọc máu thải trừ cefdinir khói cơ thể Điều có
thế có ích trong trường hợp phản ứng độc nghiêm trọng do quá liều, đặc biệt nếu chức năng thận bị tổn thương.
BẢO QUẢN: Báo quản dưới 300 C, nơi khô mảt, trảnh ám vả ánh sảng.
HAN DÙNG: 24 tháng kế từ ngảy sản xuất. ,.
TRÌNH BÀY.
- Hộp ] vi x 10 vìén
TIÊU CHUẨN: USP 32
KHUYẾN CẢO:
Địcy kỹ hướng dẫn sử dụng trước khi dùng.
- N u cân thêm thông tin, xỉn hòi ý kỉến bảc sĩ
- Bâo quãn thuốc trảnh xa tầm tay trẻ em.
- Thuốc nầy chỉ dùng theo sự kế đơn cũa thầy thuốc
SÀN XUẤT bỏ1':
Zim Laboratories Ltd. .
Plot nos. B—21,22, M.LD.C Area, Kalmeshwar, Nagpur — 441501 Maharashtra, India (An Độ)
PHÓ cục TRUỞNG , ,
ỉ;»
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng