










0
ta
II
mod
imWĐMWWQHỤdDGỤHM
to um Iuo hu tud him…ơ 1
'…Jtl '…Wđ ua WM m … ou
hu mqu 1111! q:ud n…u 'Adlmamuoqo ;: mo
'me1 Mua mnod M.t 'l. un Mil mot: ve to tumm I 11
'u Aldù «» Ap… uu nnl mun amum nu: Mummmauo uch
umod mon uuud n… m nu mon 09 m a umd em: I MW
:summwul tuw :oGemo pusn
vevaDrug Deltvery.Sưáems Inc..
,-, « :tư—> ;t-; . ›
C 6
U. .
u Ul
Q 0
1'hy`plbh
Each52om'patoh umtalncS4.ãm otgơ…n
h … cưyhto-vhylacetate mlymer adhesive
Transdermat Drug Dolivery System
1 patch
5.²5
[133.41
7.368?
16'2981
UGVC'OI
~ ' ~ BỘ Y TẾ
CỤC QUẢN LÝ DƯỢC
ĐÃ PHÊ DUYỆT
Lân đâu:AỄJ…DĨi…/…AỆ
[131.21
Pantone: . Pautone 1757C I Black
I Pantone msc I hntonetnzc
IPM No.: 2009th-017-2
Product Name: Sancuso Cth box
Market:
Dimensions:
Revision: 3
@
Date: 16 Nơv 2012
/PRESCRIPTION ONLY MEDICINE R
KEEP OUT OF REACH ot= CHILDREN X
ẽ
Sancusơ~ g
Ễiệ.3mgoigrẹrgsetrgnr S ] ForExtemaluseOnty ỂỂ`ẫ-c
ransoerma rug ewery ystem :
3.1 mg124 hours 1 Patch ² ỂỄ
7 day patch
g Each 52 cm' patch oontains 34.3 mg ot granisetron.
Ễ For Transdermal Use Only.
ễ Read patient intormation betore use. Do not cut patch.
Store below 30°C. Keep pouoh ìn outer carton.
Mtd. by: Aveva Drug Delivety Systems Inc..
3250 Commerce Parkway,
Miramar. Fiorida 33025, USA mmunuũưm
ã'
Mld tư: PmStmkan hc, Bodminstor. NJo7921. ,,ẵ
lmpmtod by Invtda Australia Pty Ud. Ghatsaond NSW 2067. g
Importh by lnv'nta Thaimd Ltd. Bangkok. Thailand. ẵ tã Ễ
lmpnrtod by Inwd: Fuiliuines hc. Ế
Cautiom Foed, Dmgs. Devices and Cosmehcs An 1 f _
\ prutúbtts dispens'mg wuthnut ptesniutíun. m mam 1_1mtntna
INVfDA
)
Pantone; l Pantone 2757c I Btack
I Pantone 2925C . Pantone 032C
IPM No.: 2009INV-018-2
Product Name: Sancuso CPx1 foil
Market:
Dimensions:
Revision: 1
Date: 14 Nov 2012
~Sancuso (Granisetron Transdermal Patch) 1
THÔNG TIN KÊ TOA ĐẨY ĐỦ
Sancuso (Miếng dán đế thấm qua da Granisetron)
MO TA
Sancuso ohứa granisetron, đó là 1 ohất chống buồn nôn và chống nôn. Về mặt hoá học, đây lả l—
methyl-N-[( 1 R,3 r,5S)-9-methyl—9-azabicyclo[3.3. ] ]non-3-yl]-l H—indazole-3—carboxamide với trọng
lượng phân tử 3124 Công thức dựa trên thực nghiệm của nó là CtgHchttO, trong khi đó cấu trúc
hoá học của nó là :
cn3
CH
1 x ,
\ N
N
/
NH
O
Granisctron
Granisetron là 1 chất rắn mảu trắng đến trắng ngả không tan được trong nước. Sancuso là 1 miếng
dản mòng, mờ, loại có chứa chất nên thấm được qua, miêng dán nảy hình chữ nhật có góc tròn, gôm
có 1 lớp đệm phía sau, lớp chất nến có thuốc và 1 lớp lót chất phóng thích.
Danh sách tá dược
Backing laỵer
Polyester (Hostaphan MN] 5 DMF )
Ink components: Titanium dioxide (E171), Polyamide resin, Polyethylenc wax Z
Matrix laver
Acryiate-vinylacetate copolymer (Duro-Tak 387—2287)
Release liner
Siliconised polyester
DẠNG BÀO CHẾ
Miếng dản đế thấm qua da.
DANG TRÌNH BÀY
Sancuso (Miếng dán thấm Iqua da Granisetron) được trình bảy dưới dạng 1 miếng 52 cm2 chứa
34 ,3mg granisetron Mỗi miêng được in ở một mặt với hảng chữ “Granisetron 3,1 mg/24giờ” Mỗi
miêng Sancuso được đóng gói trong 1 bao nhỏ riêng biệt bằng plastic được lót lá thiếc vả được dản
kín.
Sancuso được đóng trong gói có 1 miếng.
DẠNG LIÊU DÙNG VÀ HÀM LƯỢNG
3,1 mg granisetron trong 24 giờ cho tới 7 ngảy.
> 1- AN Pi….h'ti`fặt`
11.11 iiittN *
Sancuso (Granisetron Transdermal Patch) 2
CHỈ ĐỊNH VÀ SỬ DỤNG
Sancuso (Miếng dán Granisetron) được chỉ định đề phòng ngừa buồn nôn vả nôn ở bệnh nhân đang
được điếu trị với phảc đồ hóa trị liệu có khả năng gây nôn ở mức độ trung bình vả /hoặc mức độ cao
trong thời gian tới 5 ngảy liên tục.
LIỆU VÀ CÁCH DÙNG
Miêng dán da nên được dán lên vùng da sạch, khôỳ, lảnh lặn ở vùng mặt ngoải cánh tay. Sancuso
không nên dản lên vùng da đò, bị kích thích hay bị tôn thương.
Mỗi miêng dán được đóng gói trong 1 cải bao nhỏ và nên dản trực tiêp lên da sau khi bao nhỏ được
mở ra.
Không được cắt miếng dản nảy thảnh nhiều miếng nhò.
Người lớn
Dản ] miếng lên vùng mặt ngoải oánh tay trong một thời gian tối thiếu là 24 giờ trước đợt hóa trị
liệu Miếng dản nảy có thể dùng tối đa là 48 giờ trước khi bắt đầu đợt hóa trị liệu khi cần. Bóc miếng
dản sau 1 thời gian tối thiều là 24 giờ từ khi hoản tất đợt hóa trị liệu. Miếng dán nảy Có thế để tới 7
ngảy tùy thuộc vảo thời gian của phác đồ hóa trị liệu.
CHỐNG CHỈ ĐỊNH
Sancuso bị chống ohỉ định dùng cho bệnh nhân đã biết oó quá mẫn với granisetron hoặc bắt kỳ thảnh
phẩn nảo oùa miêng dản. jỹ/
THẬN TRỌNG VÀ PHÒNG NGỪA
Tiêu hỏa
Sử dụng granisetron ở bệnh nhân có thề lảm che khuất tiến triền của iiệt ruột vả| hoặc tỉnh trạng
căng trướng dạ dảy gây ra do bệnh lý.
Phản ửng da
Trong cảc thử nghiệm lâm sảng với Sancuso, những phản ứng ở vùng dản thuốc được ghi nhận
thường ở mức độ nhẹ và không dẫn đến việc phải ngưng dùng thuốc.
Nếu phản ứng ở mức độ nặng, hay phản ứng da toản thể xảy ra (chẳng hạn như ban dị ứng, bao gồm
hồng ban, ban dát, ban sân hoặc ngứa), phải gỡ bỏ miếng thuốc dán.
Tiếp xúc với ánh sáng
Granisetron có thế bị ảnh hưởng bời ánh sảng tự nhiên trực tiếp hay ảnh sảng nhân tạo. Bệnh nhân
phải được dặn nên che phủ những vị trí dán thuốc, chắng hạn cho bằng quân ảo, nếu có nguy co tiếp
xúc với ánh sáng trong suôt thời gian dùng thuốc và oho tới 10 ngảy sau khi gỡ bỏ miếng thuốc dản
vì phản ứng da có khả năng xảy ra (xem phần 13. 2).
Ẩnh hưởng lên khả năng lái xe và vận hảnh máy mỏc
Không có dữ liệu nảo về ảnh hướng của granisetron dùng qua da lên khả năng lải xe và sử dụng
mảy móc. Như lả một biện pháp phòng ngừa, nên khuyên bệnh nhân không lái xe và sử dụng máy
móc nêu họ có cảm giảc chóng mặt, buôn ngủ hay nhin mờ.
WR*Q. I
-Sancuso (Granisetron Transdennal Patch) 3
SỬ DỤNG ở NHỮNG NGƯỜI ĐẶC BIỆT
Có thai
Phân loại B về nguy cơ cho thai
Nghiên cứu về sinh sản với granisetron hydrochloride được thực hiện ở chuột mang thai với liều lên
tới 9 mg/kg/ngảy (54 mg/m2 /ngảy, khoảng 20 lần nhiều hơn liều khuyên dùng ở người khi dùng
miếng thuốc dán Sancuso, dựa trên diện tích bề mặt cơ thế) và liếu uỏng lến tới 125 mg/kg/ngảy
(750 mg/mZ/ngảy, khoảng 326 lần nhiến hơn liều Sancuso khuyên dùng ở nguời dựa trên diện tích bề
mặt oơ thể). Nghiên cứu về sinh sản được thực hiện ở chuột mang thai với liếu tiêm tĩnh mạoh lên tới
3mg/hg/ngảy (36mg/m2 /ngảy, khoảng 16 lần nhiều hơn liều dùnzg Sancuso ở người dựa trên diện
tích bề mặt cơ thế) và liếu uỏng lên tới 32mg/kg/ngảy (384mg/m2 /ngảy, khoảng 167 lần nhiến hơn
liếu dùng Sancuso ở người dựa trên diện tích bề mặt cơ thề). Những nghiên cứu nảy không đưa ra
bất kỳ chứng cớ nảo vê giảm khả năng sinh sản hoặc có hại cho thai do dùng granisetron Tuy nhiên,
không oó các nghiên cửu đẩy đủ và được kiếm soát tốt ở phụ nữ mang thai. Vì nghiên cứu về sinh
sản ở súc vật không luôn luôn dự đoản cho cảc đáp ứng ở người, Sancuso không nên dùng trong thai
kỳ chỉ khi thật sự cân thiết
Phụ nữ đang trong thời kỳ cho con bú
Không rõ là granisetron có được tiết vảo sữa mẹ hay không. Vì có nhiến thuốc được tiết vảo sữa mẹ,
nên thận trọng khi dùng Sancuso cho phụ nữ đang trong thời kỳ oho con bú.
Dùng ở trẻ em 1
An toản và hiệu quả cùa Sancuso ở bệnh nhi dưới 18 tuối chưa được xảo lập.
Dùng ở người giả
Cảo thử nghiệm iâm sảng của Sancuso không bao gồm số lượng đầy đủ cảc bệnh nhân có tuối lớn
hơn 65 hoặc hơn để xảo định xem họ đảp ứng có khảo với bệnh nhân trẻ tuối hay không. Kinh
nghiêm lâm sảng khảo được bảo cảo không ghi nhận sự khảo biệt trong đảp ứng giữa bệnh nhân g_iả
và bệnh nhân trẻ. Nói chung, lựa chọn điều trị thận trọng cho 1 bệnh nhân giả là cân thận vì có tân
suất cao hơn oủa giảm chức năng gan, thận, hoặc tim, vả vì có mắc bệnh khảo đồng thời hoặc có điều
trị bằng thuốc khác.
Bệnh nhân suy thận hoặc suy gan
Mặc dù không có nghiên cứu nảo được thực hiện để thăm dò về dược động học của Sancuso ở bệnh
nhân có suy thận hoặc suy gan, thông tin về dược động học đã có cho granisetron dạng tiêm tĩnh
mạoh (xem phần DƯỌC LÝ LÂM SÀNG: Dược động học 12.3).
TƯỢNG TÁC THUỐC
Granisetron không` gây ra hoặc ức ohế hệ thống men cytochrome P- 450 in vỉt›o Không có nghiên
oứu rõ rảng nảo vê sự tương tảo thuốc - thuốc để tìm hiếu sự tương tảo về dược động học và dược
lực học với cảc thuốc khảc. Tuy nhiên, ở người, tiêm granisetron hydrochloride được dùng an toản
với thuốc nhóm benzodiazepines, thuốc an thần và thuốc chống loét thường được kê toa chung với
điếu trị chống nôn Tiêm granisetron hydrochloride cũng tỏ ra không tương tảo với cảc phảc đồ điếu
trị bệnh ung thư có tính gây nôn. Đồng ý với những dữ liệu nảy, không có tương tảo thuốc nảo có
liên quan vế lâm sảng được ghi nhận trong các thử nghiệm lâm sảng với Sancuso.
—Sanouso (Granisetron Transdermal Patch) 4
Vì granisetron được chuyến hóa bởi cảc men ohuyển hóa thuốc ở gan oytochrome P-450 (CYPIAI
vả CYP3A4), oảo ohất khời dẫn hoặc chất ức chế các men nảy có thể thay đối độ thanh lọc và do
vậy, thay đôi thời gian bản hủy cúa granisetron. Ngoài ra, hoạt tính oùa cytochrome P- 450 tiếu nhóm
3A4 (liên quan đến chuyển hóa oủa một sô thuốc giảm đau gây nghiện chính) không bị thay đối bởi
granisetron hydrochloride in vitro. Trong thực nghiệm in vitro cảc nghiên cứu ở tiếu thế người,
ketoconazole ức chế sự oxy hóa vòng của granisetron hydrochloride. Tuy nhiến, ý nghĩa lâm sảng
oùa sự tương tảo thuốc vê dược động học in vivo với ketoconazole vẫn chưa được biết. Trong 1
nghiên cứu vê dược động học ở người, sự khời dẫn men ở gan với Phenobarbital có kết quả lả tăng
25% độ thanh lọc toản bộ huyết tương của granisetron hydrochloride tiêm tĩnh mạch Ý nghĩa lâm
sảng cùa sự thay đổi nảy vẫn chưa được biết.
PHẢN ỦNG KHÔNG MONG MUÔN
Kinh nghiệm từ các thử nghiệm lâm sâng
Tính an toản của Sancuso đã được đánh giả ở 404 bệnh nhân đang được hóa trị liệu vả tham dự vảo
2 nghiên cứu` mù đôi, có dùng chất so sảnh với thời gian sử dụng miếng thuốc dán tới 7 ngảy Nhóm
chứng bao gồm 406 bệnh nhân nhận liều uống hằng ngảy lả 2mg granisetron, từ 1 tới 15 ngảy.
Phản ứng không mong muốn được cảc nhà nghiên cứu xem là có liên quan đến thuốc xảy ra ở 8, 7%
(35/404) bệnh nhân dùng Sancuso vả 7,1% (29/406) bệnh nhân uống granisetron Phản ứng không
mong muốn thường gặp nhất là tảo bón xảy ra ở 5,4% bệnh nhân cùa nhóm Sancuso và 3,0% bệnh
nhân của nhóm uỏng granisetron.
Bảng 1 liệt kê cảc phản ứng không mong muốn xuất hiện trong lúc điều trị xảy ra ở ít nhất 3% bệnh
nhân điều trị với Sancuso hay granisetron uống.
Bảng 1: Tần suất cảc phản ứng không mong muốn trong các nghíên cứu mù đôi có đối chứng
với hoạt chẩt tương đương ở bệnh nhân ung thư đang nhận hóa trị liệu (các biến cố > 3%ở
nhóm nây hay nhỏm kia)
Miếng dán Granisetron ffl
Hệ thống cơ thể Sancuso uống
Triệu chứng thường có N=404 N=406
( %) ( %)
Các triệu chứng tiêu hóa
Táo bón 5,4 | 3,0
Cảo triệu chứng thẫn kinh
Nhức đầu 0,7 ) 3,o
Chất đối kháng thụ thể 5-HTg, như granisctron, có thế liên quan đến rối loạn nhịp hoặc bất thường
trên ECG. Có 3 ECG được thực hiện ở 588 bệnh nhân ngẫu nhiên ở nghiên cứu Pha" Jĩ vảo lúc
trước điếu trị, vảo ngảy thứ nhẩt oủa dợt hóa trị liệu, và 5 đến 7 ngảy sau khi bắt đầu đợt hóa trị
liệu Kéo dải QTcF lớn hơn 450 milli- -giây dược thấy ở tổng số 11 (1, 9%) bệnh nhân sau khi dùng
granisetron, trong đó 8 (2, 7%) bệnh nhân uống granisetron và 3 (1,1%) bệnh nhân dản thuốc.
Không có sự xuất hiện mới của kéo dải QTcF lớn hơn 480 mi1i- g-iây được phát hiện ở bất kỳ bệnh
nhân nảo trong nghiên cứu nảy Không có rôi loạn nhịp được phảt hiện trong nghiên oứu nảy.
Sancuso (Granisetron Transderma1 Patch) 5
Kinh nghiệm về Granisetron
Vì nghiên cứu nảy được tiến hảnh trong điều kiện rất khảo nhau, tỉ lệ cảc phản ứng không mong
muôn trong oảo thử nghiệm lâm sảng oùa ] thuốc không thế được so sảnh một oách trực tiếp với tỉ lệ
nảy trong các thử nghiệm lâm sảng cùa 1 thuốc khảo và có thế không phản ảnh được tỉ lệ nảy quan
sát được trong thực tế.
Cảo biến cố không mong muốn đã được bảo cảo trong thử nghiệm lâm sảng với cảo dạng trình bảy
khảo của granisetron bao gồm :
Tiêu hóa: đau bụng, tiêu ohảy, tảo bón, tăng men AST vả ALT, buồn nôn vả nôn
Tim mạch. ~ tăng huyết ap, hạ huyết ảp, đau thắt ngực, rung nhĩ vả ngất hiếm khi được ghi nhận.
Thần kinh trung ương: ohóng mặt, mất ngủ, nhức đầu, lo au, buồn ngủ và suy nhược.
Tăng mẫn cảm: hiếm có phản ứng tăng mẫn cảm, thỉnh thoảng ở mức độ nặng (chẳng hạn như phản
ứng phản vệ, khó thở, hạ huyết ảp, nôi mề đay) được ghi nhận
Khác: sốt, cảc biến cố thường kèm với hóa trị liệu cũng được ghi nhận: giảm bạch cầu, giảm cảm
giảc ngon miệng, thiếu mảu, hói đầu, giảm tiếu cầu.
Thông ơbáo cho bác sĩ các tác dụng phụ không mong muốn gặp phải trong khi dùng thuốc.
QUÁ LIÊU
Không có thuốc đối khảng đặc hiệu cho trường hợp quả liếu granisetron. Trong trường hợp quá liều,
cân phải điếu trị triệu chứng
Quả liều tới 38,5 mg granisctron hydrochloride, như là 1 liều duy nhất tiêm tĩnh mạch, đã được báo
cảo không có triệu chứng hoặc chỉ oó nhức đầu nhẹ.
Trong cảc thử nghiệm sâng không có trường hợp quá liều nảo với Sancuso được bảo oảo. g
DƯỢC LÝ LÂM SÀNG
Cơ chế tảo dụng
Granisetron là 1 chất đối khảng thụ thể ohọn lọc 5 -hydroxytryptaminq (S-HT3) với ải tính ít hoặc
không có ái tính với oác thụ thể serotonin khảc, bao gôm 5- HT;, 5- HT…, 5- HTtBJC, 5- HT2 , với thụ
thể alpha… aiphaỵ, hoặc beta-adrencrgio; với thụ thể dopamine-Dzl hoặc với histamine-H 1,
benzodiazepine; picrotoxin hoặc thụ thể opioid.
Thụ thế serotonin cùa loại S-HT3 được định vị ở ngoại biên trên đầu tận oùng oùa dây thần kinh 10
vả ở trung tâm của vùng lẫy cò thụ thể hóa học cùa vùng postrema. Trong lúc hóa trị liệu có gây
nôn, tế bảo enterochromafftn ở niêm mạc phóng thích serotonin, chất nảy sẽ kích thích thụ thể 5-
HT; Điếu nảy lảm khởi phảt xung động thần kinh hướng tâm qua dây phế vị, do đó gây nôn. Nghiên
cứu trên sủc vật cho thấy răng, khi gắn kết với thụ thể 5- HT;, granisetron phong bế sự kích thích của
serotonin và tiếp theo lá ức chế nôn sau khi có những kich thích gây nôn như oiplastin. Ớ mô hình
súc vật chồn sương, 1 lần tiêm granisetron phòng ngừa được nôn do dùng liều cao ciplastin hoặc lảm
ngừng nôn trong vòng 5 tới 30 giây.
Dược lực học
Trong cảc nghiên cửu ở người, granisetron thấm qua da không gây tảo dụng có ý nghĩa lâm sảng trên
huyết ảp, nhịp tim hoặc ECG Không có chứng cớ nảo vế tảo dụng trên nông độ trong huyết tương
của prolactin hoặc aldosterone được tim thấy trong cảo nghiên cứu về sử dụng granisetron.
Sancuso (Granisetron Transdermal Patch) 6
Hiệu quả cùa thời gian di chuyến từ miệng —manh trảng sau khi dán miếng Sancuso chưa được
nghiên cứu. Tiêm granisetron hydrochloride tỏ ra không có tảo dụng trên thời gian di chuyên từ
miệng— manh trảng ở người khóe mạnh với 1 liếu tiêm tĩnh mạch là 50 mcg/kg hoặc 200 mcg/kg.
Uống 1iếu duy nhất hoặc nhiếu liếu granisetron hydrochloride lảm ohậm sự di chuyến qua đại trảng ở
người khỏe mạnh.
Dược động học
Hâp thu . `
Granisetron thâm qua da nguyên vẹn đê vảo tuân hòan băng quá trình khuếch tản thụ động.
Sau khi dản ] mìếng Sancuso vả để trong 7 ngảy ở 24 người khỏe mạnh, có sự thay đối rất khảo
nhau ở từng người sử dụng về sự tiếp xúc thuốc trong cơ thể được quan sảt Nồng độ tối đa đạt tới ở
khoảng 48 giờ (thay đối từ 24- 168 giờ) sau khi dản miếng Sancuso. Cmm trung binh lả 5, 0 ng/mL
(CV:I70%) vả AUC…ggtư trung binh là 527 ng—giờ/mL (CV : 173 %).
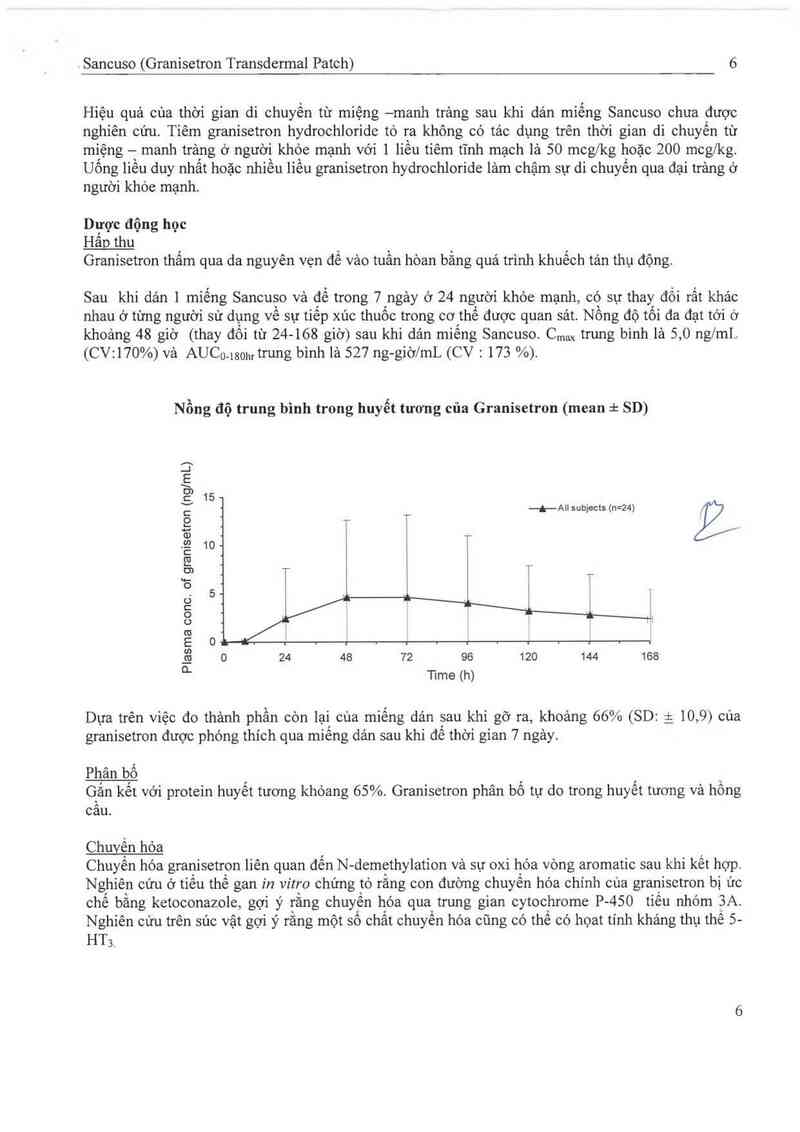
Nồng độ trung bình trong huyết tương của Granisetron (mean =t SD)
15
+Aii subjects (n=24) Z
0 24 48 72 96 120 144 168
Time (h)
Plasma conc. of granisetron (ng/mL)
Dựa trên việc đo thảnh phần còn lại của miếng dản sau khi gỡ ra, khoảng 66% (SD: Ê 10,9) cùa
granisetron được phóng thích qua miêng dản sau khi đế thời gian 7 ngảy.
P_hân bố
Gắn kết với protein huyết tương khỏang 65%. Granisetron phân bố tự do trong huyết tương và hồng
cầu.
Chuỵến hòa
Chuyến hóa granisetron liên quan đến N- demethylation và sự oxi hóa vòng aromatic sau khi kết hợp
Nghiên cứu ở tiêu thế gan ín vitro chứng tỏ răng con đường chuyến hóa chính oủa granisetron bị ức
chế bằng ketoconazole, gợi ý rằng chuyến hóa qua trung gian cytochrome P- 450 tiêu nhóm 3A
Nghiên cứu trên súc vật gợi ý răng một sô chất chuyến hóa cũng oó thể có họat tính khảng thụ thể 5-
HTs.
Sancuso (Granisetron Transdermal Patch) 7
Thải tiêt
Thanh lọc chủ yếu qua ohuyển hóa ở gan. Dựa trên 1 nghiên cứu với thuốc dạng tiêm tĩnh mạch,
khoảng 12% cùa liếu dùng được thải tiết dưới dạng không đổi trong nước tiếu của người khóc mạnh
trong 48 giờ. Phần còn lại oủa liều dùng được thải tiết dưới dạng chất chuyến hóa, 49% trong nước
tiếu, và 34% trong phân.
Phân nhòm đối tương sử dung
Giới
Không có chứng oở đề cho rằng phụ nữ oó nồng độ granisetron cao hơn nam giởi sau khi dán miếng
Sancuso. Tuy nhiên, không có sự khác biệt có ý nghĩa vê hiệu quả lâm sảng quan sảt được giữa 2
giới.
Nhi khoa
Không có nghiên cứu nảo được thực hiện để tỉm hiếu về dược động học của thuốc ở trẻ em.
Người giả, vả người có suv gan hoăc suv thân
Mặc dù không có nghiên oứu nảo được thực hiện đề tìm hiếu về dược động học oủa Sancuso ở người
giả, vả ở những bệnh nhân có suy thận hoặc suy gan, những thông tin về dược động học sau đây đã
có oho granisetron tiêm tĩnh mạoh.
Ở người giả, và bệnh nhân suy thận hoặc suy gan, dược động học của granisetron được xác định sau
khi tiêm tĩnh mach 1 liêu 40 mog/kg granisetron hydrochloride
Người già Z
Ở người giá tình nguyện (tuổi trung bình 71) cảc thông số về dược động học sau khi tiêm tĩnh mạoh
] liếu 40 mog/ kg granisetron hydrochloride, độ thanh lọc thấp hơn vả thời gian bản hùy dải hơn
quan sảt được so với người tình nguyện trẻ hơn khóe mạnh.
Bệnh nhăn suy thận \
Độ thanh` lọc toản phân cùa granisetron không bị ảnh hưởng ở bệnh nhân có suy thận nặng được
dùng ] liêu tiêm tĩnh mạch 40 mcg/kg granisetron hydrochloride.
Bệnh nhăn suy gan
Ở bệnh nhân suy gan do có liến quan đến ung thư gan, độ thanh lọc toản bộ trong huyết tương sau
khi tiêm tĩnh mạch ] lỉều 40 mcg/kg granisetron hydrochloride bị giảm một nứa so với bệnh nhân
không suy gan. Do oó sự thay đổi rộng trong oảo thông số về dược động học và sự dung nạp tốt với
liều khuyến cảo kế trên, việc điếu chinh liếu ở bệnh nhân suy chức năng gan lá không cần thiết.
ĐỘC TÍNH KHÔNG có TÍNH LÂM SÀNG
Khả năng gây ung thư, gây đột biến gen và giảm khả nãng sinh sản
Trong 1 nghiên cứu 24 thảng vẻ khá năng2 sinh ung thư, chuột được oho uống granisetron 1, 5 hoặc
50 mglkg/ngảy (6, 30 hoặc 300 mg/m2 /ngảy) Liều 50 mg/kg/ngảy được giảm đến còn 25
mg/kg/ngảy (150 mg/m2 lngảy²) trong suốt tuần 59 do có tính độc. Đối vởi ] người cân nặng 50 kg có
chiều cao trung bình (1, 46 m2 diện tích bề mặt cơ thế), những liều cho trên tư2ợng trưng gâp khoảng
2, 6, 13 và 65 lần 1iều khuyên dùng trên lâm sảng (3,1 mg/ngảy, 2, 3 mg/m 2/ ngảy, cung câp qua
Sancuso (Granisetron Transđermal Patch) 8
miếng dản Sancuso, dựa trên diện tích bề mặt cơ thế). Có sự tăng lên có ý nghĩa thống kê về tằn suất
của carcỉnzoma tế bảo gan vả adeoma của tế bảo gan ở chuột đực được điếu trị với liếu 5 mg/kg/ngảy
(30 mg/m2 /ngảy, gấp khoảng 13 lần liếu Sancuso khuyên dùng ở người, dựa trên điện tích bề mặt cơ
thế) và hơn nữa, vả ở chuột cải điếu trị vói liều 25 mg/kg/ngảy (150 mg/m2 /ngảy, gẳp khoảng 65 lần
liếu Sancuso khuyên dùng ở người, dựa trên diện tzích bề mặt cơ thế). Không có tãng sô khối u ương
gan quan sát được ở liếu ] mg/kg/ngảy (6 mg/m2 /ngảy, gấp khoảng 2 ,6 lằn liếu Sancuso khuyên
dùng ở người, dựa trên diện tích bề mặt cơ thế) ở chuột đực vả liếu 5mg/kglngảy (30 mgỉm'lngảy,
gâp khoảng 13 lần liều Sancuso khuyên dùng ở người, dựa trên điện tích bề mặt cơ thể) 0 chuột cải
Trong ] ngzhiên cứu 12 thảng vế độc tính cùa thuốc uống, điếu trị bằng granisetron 100mg/ng ngảy
(600 mgấm2 lngảy, gắp khoảng 261 lần liểu Sancuso khuyến dùng ở người, dựa trên diện tích bề mặt
oợ thế) đã gây ra adenoma tế bảo gan ở chuột đực và chuột cải trong lúc đó không có những khối u
như thế được tim thẳy trong nhóm ohuột đối chứng. Một nghiên cứu 24 tháng vẻ khả năng sinh ung
thư của granisetron đã không cho thấy một sự tăng lến có ý nghĩa thống kê về tần suất khối u, nhưng
nghiên cứu nảy không được xảo dịnh.
Vì việc phát hiện khối u xảy ra trong những nghiên cứu ở chuột, chi nên ghi toa Sancuso với liếu vả
cho những chỉ định đã được khuyên cảo (xem CHI ĐỊNH VA SƯ DỤNG, vả LIEU VA CACH
DUNG). .fv
Granisetron không có khả năng gây đột biến trong thứ nghiệm Ames in vitro vả trong xét nghiệmể/
để biết trước sự đột biến ở tế bảo lymphoma chuột, và trong thử nghiệm ở nhân sinh sản cùa chuột in
vivo và xét nghiệm UDS ở tế bảo gan chuột in vilro vả ex vivo. Tuy nhiên, granisetron lảm tăng đảng
kể về UDS trong tế bảo HeLa in vitro vả tãng đảng kế tần suất oủa tế bảo có tinh trạng đa bội nong 1
thử nghiệm in vier về sự lệch hướng nhiễm sảc thế ớ tế bảo lympho người.
Granisetron với liếu tiếm dưới da lến tới 6mg/kg/ngảy (36mg/m2 /ngảy, gắp khoáng 16 lần liếu
Sancuso khuyên dùng ở người, dựa trên diện tich bề mặt cơ thế) vả liếu uống lên tới 100
mg/kg/ngảy (600 rng/m2 .lngảy, gấp khoảng 261 lần liếu Sancuso khuyến dùng ở người, dựa trên
diện tích bề mặt cơ thế) được tim thắy không có tác dụng lến khả năng sinh sản cùa chuột đực và
chuôt cái.
Tính độc với ánh sảng
Khi được thư nghiệm về khả nảng độc với ánh sảng in vitro ở dòng tế bảo buồng trứng cùa chuột
hamstcr Trung quôc (CHO), ở liếu 200 vả 300 mcg/ml, granisetron lảm tăng tỉ lệ phần trăm cùa tế
bảo có lệch hướng nhiễm săc thế sau khi được chiếu ảnh sảng
Granisetron không gây độc với ảnh sảng khi được thử nghiệm ín vitro ở dòng nguyên bảo sợi cưa
chuột. Khi được thử nghiệm in vivo ở ohuột lang, miếng dản Sancuso không tỏ ra có bất kỳ sự kich
thích nảo với ảnh sảng hoặc tăng nhạy cảm với ảnh sảng. Không có nghiến cứu nản về tính độc với
ảnh sảng được thực hìện ở người.
THỬ NGHIỆM LÂM SÀNG
Hiệu quả của Sancuso trong phòng ngửa buồn nôn vả nôn gây ra do hóa trị liệu ( CINV) được đảnh
giá trong 1 nghiên cứu Pha 3 ngẫu nhiên, ghẻp nhóm song song, mù đôi, mù giả tiến hảnh ở Hoa Kỳ
và ngoải Hoa Kỳ. Nghiên cứu nảy so sảnh hiệu quả, khả năng đung nạp và độ an toản cùa Sancuso
- Sancuso (Granisetron Transdermal Patch) 9
với hiệu quả, khả năng dung nạp và độ an toản của iiếu 2mg granisetron uống hảng ngảy trong
phòng ngừa buồn nôn vả nôn ở 641 bệnh nhân đang nhận hóa trị Iiệu nhiến ngảy.
Đối tượng nghiên cứu được chọn ngẫu nhiên vảo thử nghiệm gồm có 48% nam và 52% nữ tuổi từ 16
đến 86 đang nhận hóa trị liệu nhiều ngảy oó khả năng gây nôn ở mức trung bình (ME) hoặc mức cao
(HE). 78% bệnh nhân là người da trắng, 12 % người châu Ả, 10% người Tây Ban Nha hoặc Bồ Đảo
Nha vả 0% người da đen.
Miếng dán granisetron được dản từ 24 giờ đến 48 giờ trước khi liều đầu tiên oủa đợt hóa trị liệu, vả
được giữ nguyên tại chỗ trong 7 ngảy Granisetron uống được cho hảng ngảy trong suốt thời giạn
của đợt hóa trị liệu, 1 giờ trước môi liếu hóa trị liệu. Hiệu quả được đảnh giá từ lủc dùng liều lần
đầu tiên cho đến 24 giờ sau khi bắt đầu dùng Iiều hóa trị của ngảy cuối cùng
Tiếu chí đánh giá chính cùa thử nghiệm là tỉ lệ bệnh nhân đạt được tình trạng không bị nôn vảlhoặc
ợ, cũng không có buồn nôn và không dùng thuốc giải cứu từ lần dùng thuốc đầu tiên cho đến 24 giờ
sau khi bắt đầu dùng liếu cùa ngảy ouõi cùng oùa đợt hóa trị liệu Sử dụng định nghĩa nảy, hiệu quả
của Sancuso được thiết lập là 60,2 % bệnh nhân dùng Sancuso dản ở oảnh tay và 64, 8 % bệnh nhân
uống granisetron (độ khảo biệt -4, 89%; khoảng tin cậy- -,12 91% đến + 3,13%).
Một đánh giá việc dản miếng có hoạt chất hoặc miếng dản có giả dược ở 621 bệnh nhân cho thấy
rằng ít hơn 1% các miếng dán bị tróc ra trong giai đoạn 7 ngảy đề miếng thuốc dán tại ohỗ
HẠN DÙNG
3 năm kế từ ngảy sản xuất. Z
BÁO QUẢN VÀ XỬ LÝ
Giữ ở nhiệt độ dưới 30°C.
Nên đê Sancuso trong bao bì nguyên cùa nó. Đê trảnh xa trẻ em.
THÔNG TIN CHỈ DẨN CHO BẸNH NHÂN
Tỉêu hỏa
Vì việc dùng granisetron có thề lảm che khuất tiến triến cùa liệt ruột vả/hoặc tình trạng cãng trướng
dạ dảy gây ra do bệnh lý, bệnh nhân nên được hướng dẫn để bảo cho bảo sĩ biết nếu họ bị đau bụng
hay sưng bụng.
Phản ửng da
Bệnh nhân nên được hướng dẫn để bóc bó miếng thuốc dản nếu họ bị phản ứng da nghiêm trọng,
hoặc phản ứng da toản thân (chắng hạn như ban dị ứng, gồm hồng ban, ban dảt, ban sấn hoặc ngứa).
Khi bóc bỏ miếng thuốc dán, bệnh nhân nên gỡ bỏ nó một cảch nhẹ nhảng.
Tiếp xúc với ảnh sảng mặt trời
Granisetron có thế bị giảm chất iượng bởi ảnh sáng mặt trời trực tiếp hoặc tiếp xúc đèn cực tím.
Ngoài ra, 1 nghiến cứu in vitro dùng tế bảo buồng trứng chuột hamster cho rằng granisetron có khả
năng gây độc khi tiếp xúc với ảnh sảng (xem phần 12. 2)
. Sancuso (Granisetron Transdermal Patch) 10
Phải dặn bệnh nhân che phủ vị trí đặt miếng thuốc dản, chắng hạn bằng quần ảo, nều có nguy cơ
tiếp xúc với ảnh sáng mặt trời hoặc đèn cực tím trong suốt thời gian dùng miệng thuốc dản và cho
tới 10 ngảy sau khi bóc bỏ miếng thuốc dản
SẢN XUẤT BỞI
Avova Drug Delivery Systems Inc.,
Miramar
FL 33025 @
USA
Thuốc chỉ được kê toa.
Đoc kỹ hướng dẫn sử dụng trước khi dùng.
N u cân thêm thông tin xin hỏi ý kiên bảo sỹ.
NGÀY KIỂM LẠI BẢN THÔNG TIN NÀY
19 thảng 03 năm 2012
PHÓ CỤC TRUỞNG
Jạu,tễn nth %…
10
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng