












SJĐ/ỢE’]
easweg
uetdeMol
: sưu 'dxa \
: wo '…
: '°N …
2 620 óó 9
llllllÌliỈÌ °“ ²t
M
10 Tablets
Carton contains 1 strip with 10 tnblets.
Tolvaptan
Samsca
iablets
15 mg
Bt
MUST INITIATE IN HOSPITAL
DISPENSE THE ENCLOSED
MEDICATION GUIDE T0 EẦCH PA'HENT
Tolvaptan
Samsca
15 mg
tablets
am…
\\\\\\\\
FORIIULATDN:
Each Iablet ccntalns 15 mg ot tclvaptan.
Please see package mserl ior indications and
dosage Iniormahon.
CAUTION: Foods, Dmgs. Devnces and Cosmetics
Act prohttillS dispensing wnhoui prescriptton,
Slore at temperature not exceedmg 30'C.
Reg. No. :
……umu ln _
Ú'shko Korea Otsuka Pharmaceutical (o, Ltd.
...…dmủunuưdtụnt …
11. iqikpngdm Jq«t Withmup. Mum
t'ụnngudo, Km
, /ỉ
////////
5 ²²²8
c ²“O
g=. ~ợom
ễ* =11ẵ.—o›
ẵ` m’Z—<
U t~
ếĨ- c ~.Ễ
fi= ~io
l~
\r
Ê?
Ỉ'Ề'PẶẶA . .
…vm m …Tnu im
LAI. Ld.
Bu Đa
…… &mmu
.
……»sn. W…ifnq , (
% ả ²
Wu…. iiq …… mg '
ut u.
EID› En.
bu… &Ưunũwlu
i
;
th thị WMM t
ua u:. :
Em Em
k" _ "“ịw ` 'iì
s
'ổầ
l9.' «" ,
Việt: Samsca tablets 15 mg
v ồ .
egĩ'lổẫlẵán _Ầơn
%ỎẠ _TyeO R'SAMSCA tablets 15 mg
\ _ (Mỗi vỉên nén có chửa 15 mg tolvaptan)
Hộp 10 viên (1 ví x 10 viên)
Chỉ định, chống chỉ định` liều dùng, cảch dùng và cảc thông
tin khác: đề nghị xem trong tờ HDSD kẻm theo, Số lô SX,
NSX, HD xem “Batch/Lot no.“, “Mfg.Date”, “ExpDate”
trên bao bì. Bảo quản nơi khô, nhiệt độ dưới 30°C.
Đế xa tầm lay zre' em
Đọc @ huờng dẫn sử dụng Irước khi dùng
Sản xuất bời: Korea Otsuka Pharmacautìcaì Co., Ltd.
(Hản Quốc)
sẽ dãng ký: DNNK:
Hướng dẫn sử dụng
' g dẫn sử dụng trưởc kfzi dùng
f thông tin xin hói ý kiên Bác sỹ
Rx SAMSCA tablets 15 mg
(tolvaptan)
MÔ TẨ:
Thảnh phần:
Mỗi viên nén SAMSCA tablets 15 mg có chứa 15 mg tolvaptan vả cảc tả dược sau: lactose
monohydrate, tỉnh bột ngô, microcrystalline cellulose, hydroxypropyl cellulose, low-substìuted
hydroxypropyl cellulose, FD&C Blue No.2 Aluminum lake, Magnesium stearate.
Mô tả:
SAMSCA tablets lSmg là viên nén mảu xanh da trời, hình tròn, một mặt có vạch khắc cùng với
chữ “SAMSCA” và **15”.
DANG BÀO CHẾ: viên nén
ouv CÁCH ĐÓNG GÓI: Hộp 1 ví x 10 viên
CHỈ ĐINH:
Giảm Natri mảu:
.ị/
SAMSCA được chỉ định để điếu trị giảm Natri mảu có tăng thể tích và bình thể tích có ý nghĩa
lâm sảng (Natri huyết thanh < 125 mEq/L hoặc giảm Natri máu ít rõ rảng mà có triệu chứng và
không đáp ứng vởì việc đìểu chỉnh hạn chế dịch), bao gồm cảc bệnh nhân suy tim, và Hội chứng
tiết hóc môn chống bải niệu không thích hợp (SIADH).
Gìới hạn quan trọng:
Bệnh nhân cần can thiệp để tăng Natri huyết thanh khẳn cấp để phòng ngừa hoặc để điều trị các
triệu chứng trầm trọng vẻ thần kinh không nên được điều trị với SAMSCA.
Chưa xảc minh được việc tảng Natri huyết thanh vởi SAMSCA có đưa lại một lợi ích về triệu
chứng cho bệnh nhân hay không .
LIÊU DÙNG VÀ CÁCH DÙNG:
1. Liều thường dùng ở người lón:
Giảm Natri máu:
Bệnh nhân nên ở trong bệnh viện để bắt đầu hoặc bắt đầu lại việc điều trị để đánh giá đáp ứng điều
trị và do sự đỉều chinh quá nhanh chóng của việc giảm Natri mảu có thể gây ra việc hủy myelin
thẩm thấu dẫn đển chứng loạn ngôn, câm, khó nuốt, ngủ lịm, thay đổi tình cảm, liệt từ chi co cứng,
cơn động kinh, hôn mê và tử vong.
Liều khởi đầu thường dùng của SAMSCA là 15 mg dùng ngảy một lần không lỉên quan đến bữa
ãn. Tăng liếu lên 30 mg ngảy một lần, sau ít nhất 24 giờ, tởi tối đa 60 mg ngảy một lần, khi cần để
đạt được nồng độ Natri huyết thanh mong muốn. Trong thời gian bắt đẩu và chỉnh lỉều, thường
xuyên kiếm tra sự thay đổi cùa cảc chất điện giải trong huyết thanh và thể tích huyết thanh. Tránh
hạn chế dịch trong 24 gỉờ điều trị đầu tiên. Nên khuyên bệnh nhân đang dùng SAMSCA có thế
tìếp tục uống chất lỏng khi khảt.
Không sử dụng SAMSCA quả 30 ngảy để giảm thiều nguy cơ tốn thương gan.
Page ! oflS
R.v
2. Ngùng thuốc:
Tiếp sau việc ngừng dùng SAMSCA, nên khuyên bệnh nhân tiếp tục hạn chế dịch vả nên kiếm tra
tinh trạng thay đối Natri huyết thanh và thể tích huyết thanh.
3. Dùng cùng VÔ“! chẩt ức chế CYP 3A, tác nhân gây cảm ứng CYP 3A và chẫt ức chế P-
gP²
Chẩt ức chế CYP 3A-
Tolvaptan được chuyển hóa bởi CYP 3A, và việc dùng cùng vởì chất ức chế mạnh CYP 3A gây
tăng nông độ (gấp 5) Tảc dụng cùa chất ức chế trung bình C YP 3A trên tolvaptan chưa được đánh
giá. Tránh dùng SAMSCA cùng với chắt ức chế trung bỉnh CYP 3A.
Tác nhân gây cảm ửng CYP 3Az
Dùng SAMSCA cùng vởỉ tảc nhân có khả năng gây cảm ứng CYP 3A (ví dụ rìfampicin) lảm gỉảm
nông độ tolvaptan huyết thanh còn khoảng 85%. Do vậy, tác dụng lâm sảng mong muốn cùa
SAMSCA có thế không thấy được 0 lìếu khuyến cảo. Do vậy nên kiếm tra đảp ứng của bệnh nhân
vả điếu chỉnh liếu.
Chẩt ửc chế P gp:
Tolvaptan là chất được chuyến hóa bời P- -gp. Dùng SAMSCA cùng vởi chất ức chế P- -gp (ví dụ
cyclosporin) có thế cần phải giảm liều SAMSCA.
CHỐNG CHỈ ĐINH:
Không sử dụng SAMSCA trong những trường hợp sau: J
1. Cần tăng khẩn cẩp Natri huyểt thanh:
SAMSCA chua được nghiên cứu để dùng khi cần tăng khẩn cắp Natri huyết thanh.
2 Bệnh nhân không có khả nãng có cãm giác khát hoặc có đáp ứng thỉch hợp với khát
Những bệnh nhân không thể tự động đìếu chinh cân bằng chất lòng có tăng đảng kế ngưy cơ phải
gánh chịu sự điếu chỉnh quá nhanh chóng của Natri huyết thanh, tãng Natri mảu và giảm thể tích
máu.
3. Giảm Natri máu giảm thể tỉch máu:
Các nguy cơ đi kèm với tình trạng xâu đi của chứng giảm thê tích mảu, bao gôm cảc biến chứng
như giảm huyêt ảp và suy thận, lả nhiêu hơn so vởi lợi ích đưa lại.
4. Dùng đồng thời với các chẩt ức chế CYP SA mạnh:
Ketoconazol 200 mg dùng cùng với tolvaptan tăng nồng độ tolvaptan lên 5 lần. Liều cao hơn được
dự kìến sẽ lảm tăng nông độ tolvaptan hơn. Không có đầy đủ kinh nghíệm để xâc định việc điều
chính liếu lượng lả cân thìết để cho phép sử dụng an toả…n tolvaptan với chất ức chế CYP 3A mạnh
như clarithromycin, ketoconazol, ỉtraconazol, rỉtonavỉr, indinavỉr, nelfinavir, saquinavir,
nefazodon, vả telithromycin.
5. Bệnh nhân bí tiểu:
Dự kiến không có lợi ích lâm sảng nảo ở những bệnh nhân không thể đi tiều.
A A : <Ắ -: I K ' o Ả ' . Ă \ -› w : u ẵ Á
6. Bẹnh nhan co tịen sư qua man vơi bat cư thanh phan nao cua thuốc hoạc VO'I dan xuat
của benzachin.
7. Bệnh nhân có tãng Natri mảu
CẨNH BÁO VÀ THÁN TRONG:
Page 2 of 15
CẨNH BÁO: KHỞI ĐẢU VÀ TÁI-ỊKHỞI ĐÀU sử DỤNG THUỐC ở BỆNH VIỆN
VÀ THEO DÓI MỨC NATRI HUYET THANH
SAMSCA nên được bắt đầu và tái bắt đầu sử dụng trên bệnh nhân chỉ khi ở trong
bệnh viện nm' có thể theo dõi được chặt chẽ mức Natri huyết thanh
Sự điều chỉnh quá nhanh chóng chứng hạ Natri mảu (ví dụ > 12 mEq/L/24 giờ) có thể gây ra
sự hùy myelin thấm thấu dẫn đến chứng loạn ngôn, câm, nuốt khó, ngủ lịm, thay đổi tình
cảm, [iệt tứ chi co cứng, co giật, hôn mê vả tử vong. Ở những bệnh nhân nhạy cảm bao gồm
cả những người có suy dinh dưỡng nặng, nghiện rượu, bệnh gan tỉến triến, thì tốc độ điều
chỉnh chậm hơn mức Natri máu có thế được khuyên dùng.
1. Sự điều chỉnh quá nhanh chóng Natri huyết thanh có thể gây ra các di chứng thần
kinh nghiêm trọng (xem mục CANH BÁO)
Hội chứng hủy myelin thẩm thấu là một nguy cơ liên quan đến sự điều chỉnh quá nhanh chóng cùa
hạ Natri mảu (ví dụ > 12 mEq/L/24 giờ). Sự hủy myelin thẩm thấu dẫn đến chứng loạn ngộn, câm,
nuốt khó, ngủ lịm, thay đổi tình cảm, liệt tứ chi co cứng, co giật, hôn mê hoặc tử vong Ở những
bệnh nhân nhạy cảm, bao gồm cả những người có suy dinh dưỡng nặng, nghiện rượu, bệnh gan
tiến triến, thì tốc độ sứa chữa chậm hơn mức Natri mảu có thế được khuyến dùng. Trong các thử
nghiệm lâm sảng có kiếm soát trong đó tolvaptan được cho dùng liếu chuẩn độ bắt đầu từ 15 mg
một lần mỗi ngảy, 7% số bệnh nhân được điều trị bằng tolvaptan có mức Natri huyết thanh < 130
mEq/L đã có sự gia tăng Natri huyết thanh lớn hơn 8 mEq/L trong khoảng 8 giờ và 2% có sự gia
tăng lớn hơn 12 mEq/L trong 24 giờ. Khoảng 1% số bệnh nhân được điếu trị bằng giá dược có
mức Natri huyết thanh < 130 mEq/L đã có sự gia tăng lớn hơn 8 mEq/L trong 8 giờ vả không có
bệnh nhân nảo có sự gia tăng lớn hơn 12 mEq/L/24 giờ. Hội chứng hủy myelin thẩm thấu đã được
báo cảo lá có liên quan đến việc điều trị với SAMSCA. Bệnh nhân điều trị vởi Samsca cần được
theo dõi để đánh giá nồng độ Natri huyết thanh và tình trạng thần kinh, đặc biệt là trong thời gian
bắt đầu và sau khi chỉnh liều. Bệnh nhân mắc SIADH hoặc có nồng độ Natri huyết thanh ban đầu
rất thấp có thế có nguy cơ lởn hơn trong khi điều chỉnh Natri huyết thanh quá nhanh chóng. Ở
nhũng bệnh nhân dùng SAMSCA nêu có thấy sự phát triến quá nhanh chóng gia tăng Natri huyết
thanh, phải ngừng dùng hoặc giản đoạn đỉều trị với SAMSCA và cân nhắc việc dùng dịch nhược
trương. Hạn chế dùng dịch trong 24 giờ đầu tiên điếu trị vởi SAMSCA có thể lảm tăng khả năng
điều chỉnh quá nhanh chóng cùa Natri huyết thanh, và nói chung nên trảnh.
Theo dõi chặt nồng độ Na+ huyết thanh trong quá trình điều trị. (' /
2. Tổn thương gan:
SAMSCA có thể gây tốn thương gan nghiêm trọng và có khả năng gây tử vong. Trong một nghiên
cứu mở có đối chứng giả dược dùng tolvaptan lâu dải ở những bệnh nhân bị bệnh thận đa nang
NST trội (ADPKD), đã quan sảt thấy cảc trường hợp tổn thương gan nghiêm trọng được cho là do
tolvaptan. Sự gia tăng của ALT lớn hơn ba lần giới hạn trên cùa mức bình thường có liên quan với
tolvaptan (42/958 hoặc 4,4%) so với giả dược (5/484 hoặc 1,0%). Trường hợp tổn thương gan
nghiêm trọng thường đuợc quan sát bắt đầu 3 thảng sau khi bắt đầu sử dụng tolvaptan mặc dù sự
gia tăng cùa ALT đã xảy ra trưởc 3 thảng.
Bệnh nhân có cảc triệu chứng có thể chỉ ra tổn thương gan, bao gồm mệt mói, chán ăn, khó chịu ở
bụng trên bên phải, nước tiếu sâm mảu hoặc vảng da nên ngừng điêu trị với SAMSCA.
Hạn chế sử dụng với SAMSCA quả 30 ngảy để tránh tổn thương gan. Trảnh sử dụng ở bệnh nhân
đang mắc bệnh gan tiềm ẩn, bao gôm cả xơ gan, bởi vì khả năng phục hồi sau tôn thương gan có
thế bị suy giảm.
3. Mất nước và Giảm thể tích máu:
Page 3 of15
`f \.h ~
Điều trị với SAMSCA đem lại sự thải trữ nước mà không mất chất điện gìải, mã được bù đắp
từng phần binh thường bằng lượng nước uống vảo. Sự mất nước và giảm lưu lượng máu có thể
xảy ra.. đặc biệt lá ở những bệnh nhân có khả năng bị giảm thể tích dịch đang dùng thuốc lợi tiều
hoặc những bệnh nhân bị hạn chế dùng dịch. Trong cảc thử nghiệm nhiếu liếu, có so sảnh với giả
dược trên 607 bệnh nhân có giảm Natri mảu được điều trị với tolvaptan, tỷ lệ mất nước lá 3,3%
cho tolvaptan vả 1,5% cho bệnh nhân được điếu trị bằng giá dược. Ở những bệnh nhân dùng
SAMSCA mã có phảt triến cảc biểu hiện y khoa đảng kế hoặc triệu chứng của giảm lưu lượng
máu, cần tạm ngừng hoặc ngừng dùng SAMSCA và tiến hảnh chăm sóc hỗ trợ cùng với việc kiếm
soát cẩn thận cảc dẩn hiệu sông còn, cân bằng dịch và điện giải. Hạn chế dịch trong khi điều trị
với SAMSCA có thế lảm tảng nguy cơ mất nước và giảm lưu lượng mảu. Bệnh nhân đang dùng
SAMSCA nên tiếp tục uống chất lòng để giải khảt.
4. Dùng cùng với dung dịch muối ưu trương:
Không khuyến cảo việc sử dụng đồng thời với dung dịch muối ưu trương.
5. Tăng Kali máu hoặc cảc thuốc gây tăng Kali huyết thanh:
Việc điều trị với tolvaptan có liên quan với một sự giảm cấp tính thể tích dịch ngoại bảo mà nó có
thể dẫn đến tăng Ka1i huyết thanh. Nồng độ Kali trong huyết thanh nên được theo dõi sau khi bắt
đẩu điếu trị bằng tolvaptan ở những bệnh nhân có mức Kali huyết thanh > 5 mEq/L cũng như
những bệnh nhân đang dùng thuốc được biết lả gây tăng nồng độ Kali trong huyết thanh.
SỬ DUNG ở NHỮNG ĐÓI TƯỜNG ĐÁC BIÊT:
Không cần điều chỉnh liếu theo tuổi, giới tính, chủng tộc, hoặc chức năng tim. 1_
1 /
1. Phụ nữ mang thai:
Phân loại thuốc cho phụ nữ mang thai: C.
Chưa có cảc nghiên cứu đầy dù và được kiếm soát tốt việc sử dụng SAMSCA ở phụ nữ mang thai.
Ở cảc nghiên cứu trên động vật, đã xảy ra hở vòm miệng, ngắn chi, mắt nhò, dị tật xương, giảm
trọng lượng thai nhi, chậm hóa xương cùa thai nhi, và thai lưu SAMSCA chỉ nên được sử dụng
trong thời kỳ mang thai chỉ khi khả năng lợi ich lả nhiều hơn nguy cơ tiềm tảng đối với thai nhi.
Trong cảc nghiên cứu phát triến phôi thai, chuột cống và thỏ mang thai được cho uống tolvaptan
uỏng trong quá trình sỉnh cơ quan. Chuột cống được cho uống tolvaptan với liếu gâp 2-162 lẩn
liếu tối đa khuyến cảo cho người (MRHD) (trên cơ sở diện tích bề mặt cơ thể). Giảm trọng lượng
thai và chậm hóa xương của thai xảy ra gâp 162 iần so với MRHD. Cảc dấu hiệu cùa độc tính ở
chuột cống và thỏ mẹ (giảm sự tãngỊ cân cơ thế và sự tiêu thụ thực phẩm) xảy ra gâp 16 vả 162 lần
so với MRHD. Khi thò mang thai uống tolvaptan gấp 32 đến 324 lần MRHD (trên cơ sở diện tích
bề mặt cơ thế), có giảm sự tăng cân cơ thể mẹ vả sự tiêu thụ thục phẩm ở tất cả cảc liếu, và tăng
sẩy thai ở liều trung bình và cao (khoảng 97 vả 324 lằn cảc MRHD). Tại liếu gắp 324 lằn MRHD,
có tăng tỷ lệ cứa thai lưu, mắt nhỏ, mi măt mờ, hở hảm ếch, ngắn chi và dị tật xương.
2. Chuyển dạ và sinh con:
Tảo dụng của SAMSCA đối với thời kỳ chuyến dạ và sinh con ở người chưa được biết rõ.
3. Phụ nữ cho con bủ:
Chưa biết liệu SAMSCA có bải tiết vảo sữa mẹ hay không. Tolvaptan được bải tiết vảo sữa của
những con chuột cho con bú. Vì có nhiếu loại thuốc được bải tỉêt vảo sữa mẹ và vì những tiếm
tảng của các phản ứng bất lợi nghiêm trọng ở trẻ nhỏ đang bú sữa mẹ từ SAMSCA, cần quyết định
ngừng cho con bú hoặc ngừng dùng SAMSCA, có xem xét đến tầm quan trọng cùa SAMSCA với
người mẹ.
Page 4 of 15
V
4. Sử dụng ở trẻ em:
Chưa xảc định được an toản và hiệu quả cùa SAMSCA ở bệnh nhân trẻ cm.
5. Sử dụng ở người cao tuổi:
Trong tống số cảc bệnh nhân có giảm Natri mảu được điếu trị với SAMSCA trong cảc nghiên cứu
lâm sậng, 42% là 65 tuối trở lên, trong khi 19% lá 75 tuồi vả nhiến hơn. Không thẫy có sự khảo
biệt tống thế về an toản và hiệu quả giữa cảc bệnh nhân nảy và bệnh nhân trẻ hơn, vả cảc kinh
nghiệm lâm sảng khảc được báo cảo đã không xác định được sự khảc biệt trong đảp ửng giữa cảc
bệnh nhân cao tuổi và trẻ hơn, nhưng độ nhạy cảm lớn hơn của một số bệnh nhân lớn tuổi không
thể được loại trừ. Việc lớn tuổi không có ảnh hưởng đến nổng độ trong huyết thanh của tolvaptan.
6. Sử dụng ơ bệnh nhân suy gan:
Suy gan vừa và nặng không ảnh hưởng tới việc sử dụng tolvaptan đến mức độ liên quan tới iâm
sảng Trảnh sử dụng tolvaptan ở những bệnh nhân đang mão bệnh gan tiềm ấn
7. Sử dụng ở bệnh nhân suy thặn:
Không cần điều chinh liều theo chức nãng thận. Không có dữ liệu nghiên cứu lâm sảng ờ nhưng
bệnh nhân có độ thanh thải creatinine < 10 mL/phủt vả vì tảc động của thuốc đển nông độ Natri
huyết thanh dường như lá không có ở mức độ suy thận rất thấp nên không khuyến cảo dùng thuốc
nảy cho bệnh nhân có độ thanh thải creatinin < 10 mL/phút. Không có hiệu quả ở những bệnh
nhân vô niệu.
8. Sử dụng ở những bệnh nhân suy tim sung huyết
Nồng độtolvạptan khi sử dụng ở bệnh nhân suy tim sung huyết không bị tăng về mặt lâm sảng.
Không cân điêu chinh liêu.
Trong một nghiên cứư dược `lý lâm sảng, AUC cùa tolvaptan ở những bệnh nhân bị phù tim (suy
tim sung huyết) cao gâp 3,4 lân ở những người khỏe mạnh.
TƯơNG TÁC THUỐC:
1. Tác động của cảc thuốc đến Tolvaptan ổ ./
Ketoconazol và các chẫt ức chế CYP 3A mạnh
SAMSCA được chuyển hoá chủ yếu bới CYP 3A. Ketoconazol là một chắt ức chế mạnh CYP 3A
và cũng ức chế P- -.gp Dùng đồng thời SAMSCA vả ketoconazol 200mg hảng ngảy lảm tăng gấp 5
lằn tiếp xúc với toIvaptan Dùng đồng thời SAMSCA và 400 mg ketoconazol hảng ngảy hoặc với
cảc chất ức chế CYP 3A mạnh khác (như clarithromycin, itraconazol, telithromycin, saquinavir,
nelfinavh, ritonavir vả nefazodon) ở mức liếu cao nhất ghi trên nhăn được dự đoản sẽ lảm tăng
hơn nữa tiếp xức tolvaptan. Do vậy, không nên dùng đồng thời SAMSCA với các chất ức chế
CYP 3A mạnh.
Cảc chất ức chế CYP 3A trung bình
Tảo động của các chất ức chế CYP 3A trung bình (như erythromycin, fluconazol, aprepitant,
diltiazem vả verapamil) đến tiếp xúc khi dùng kết hợp với tolvaptan chưa được đảnh giá. Tảng
đảng kể tiếp xức với tolvaptan khi dùng kết hợp SAMSCA với cảc chất ức chế CYP 3A trung
bình. Do vặy, nên trảnh dùng kết hợp SAMSCA với các chất ức chế CYP 3A trung bình.
Nưóc' ep bưởi
Dùng kết hợp SAMSCA và nước ép bưới lảm tăng gấp 1,8 lần tiếp xúc với tolvaptan.
Chẩt ửc chế P-gp
Page 5 of 15
\VJ .
Cần giảm liếm SAMSCA ở những bệnh nhân điếu trị kết hợp với các chất ức chế P-gp như
cyclosporin dựa vảo đáp ứng lâm sảng.
Rifampicin vả cảc chẫt cảm ửng CYP 3A khảc
Rifampicin là một chất cảm úng CYP 3A và P- -gp. Dùng kết hợp rifampicin vả SAMSCA lảm
giảm bớt tiếp xúc tolvaptan 85% Do đó, hiệu quả lâm sảng được mong đợi của SAMSCA khi có
mặt rifampicin và các chất thùc đẩy khác (như rifabutin, rifapentin, barbiturates, phenytoin,
carbamachin và St. John’s Wort) có thế không đạt được ờ mức liều SAMSCA thường dùng. Có
thế phải tăng liếu cùa SAMSCA.
Lovastatin, Digoxin, Furosemid, vả Hydrochlorothiazid
Dùng kết hợp lovastatiu, digoxin, furosemid, vả hydrochlorothiazid với SAMSCA không có tác
động thích đảng về phương diện lâm sảng đến việc sử dụng tolvaptan.
2. Tác động của Tolvaptan đến các thuốc khảc
Digoxin
Digoxin là chất nến P-gp. Dùng kết hợp SAMSCA với digoxin lảm tăng AUC cùa digoxin lến
20% và Cmax của digoxin lên 30%.
Warfarin, Amiodaron, Furosemid, vã Hydrochlorothiazid
Dùng đồng thời tolvaptan với warfarin, furoscmid, hydrochlorothiazỉd, hoặc amiodaron (hoặc chẳt
chụyến hoá có hoạt tính của nó, desethylamiodaron) không lảm thay đôi dược động học của các
chât nảy tởí mức độ lâm sảng đáng kê. \
Lovastatin Ĩ/
SAMSCA là một chất ức chế yếu CYP 3A. Dùng kết hợp [ovastatỉn vả SAMSCA lảrh tăng nồng
độ lovastatỉn vả chật chuyên hoá có hoạt tính lovastatin-B hydroxyacid tương ứng 1,4 vả 1,3 lần.
Không có sự thay đôi tương ứng vê phương diện lâm sảng.
Tương tác dược lực học
Tolvaptan tạo ra tỷ 1ệ lớn hơn giữa lượng thế tich nước tiễu 24 giờllượng bải xuất nước tiếu so vớ
liều furosemid hoặc hydrochlorothỉazid. Dùng kết hợp tolvaptan với furosemid hoặc
hydrochlorothỉazid tạo ra tỷ lệ giữa thể tích nước tiếu 24 giờ/lượng bải xuất nước tiến là tương tự
với tỷ lệ sau khi dùng một minh tolvaptan.
Mặc dù các nghiên cứu tựơng tảc cụ thể chưa được thực hiện, trong cảc nghiên cứu lâm sảng
tolvaptan được sử dụng đồng thời với cảc chất chẹn beta, cảc chất chẹn thụ thể angiotensin, các
chẳt ức chế men chuyến angiotensin vả cảc chất lợi tiếu giữ Kali Cảo tác dụng không mong muốn
tăng Kali huyết cao gâp khoảng 1-2% khi dùng đồng thời tolvaptan với các chất chẹn thụ thể
angiotensin, các chắt ức chế mcn chuyến angiotensin vả cảc chẩt lợi tiếu giữ Kali so với khi dùng
với giả dược. Nên giảm sảt mức Kali huyết trong khi điếu trị thuốc kết hợp.
Gìống như một chất đối kháng thụ thể V2, tolvaptan có thể gây cản trở hoạt động chủ vận của
desmopressin (dDAVP) Ở nam giới bị bệnh Von Wiliebrand (VW) nhẹ, truyền tĩnh mạch dDAVP
2 giờ sau khi uỏng tolvaptan không lảm tăng yếu tố kháng nguyên VW hoặc yêu tố hoạt động VIII.
Không khuyến cáo dùng SAMSCA với chất chủ vận V2.
TÁC DUNG KHÔNG MONG MUỐN:
Page 6 of 15
Ả. "
1. Kinh nghiệm các thử nghiệm lâm sâng
Hạ Natri mảu
Do cảc thử nghiệm lâm sảng được thực hiện trong cảc điều kiện rất khảo nhau, tỷ lệ các tảc dụng
không mong muôn được ghi nhận trong cảc thử nghiệm lâm sảng cùa thuốc không thể so sánh trực
tiếp với tỷ lệ trong cảc thử nghiệm lâm sảng của thuốc khảc và có thế không phản ảnh tỷ lệ ghi
nhặn trong thực tế. Thông tin biếu hiện có hại từ cảc thử nghiệm lâm sảng có được, do vậy, cung
cấp cơ sở để nhận biết các biền hiện có hại xuất hiện có liên quan đến sử dụng thuốc và tỷ lệ ước
tinh.
Trong các thử nghiệm đa liều, có đối chứng với giả dược, 607 bệnh nhân giảm Natri mảu (Natri
huyết thanh < lBSmEq/L) được điều trị bằng SAMSCA. Tuổi trung bình của cảc bệnh nhân nảy là
khoảng 62,70% sô bệnh nhân là nam giới và 82% lá người da trắng. 189 bệnh nhân được điều trị
tolvaptan có Natri huyết thanh < 130 mEq/L, và 52 bệnh nhân có Natri huyết thanh < 125 mEq/L.
Giảm Natri máu được cho là do bị xơ gan ở 17% bệnh nhân, suy tim ở 68% bệnh nhân vả Hội
chứng tiết hóc môn chống bảỉ niệu không thích hợp (SlADH)/khác ở 16% bệnh nhân. Trong số
những bệnh nhân nảy, 223 người được điều trị với liều chuẩn khuyến cáo (15 mg chỉnh liều đến
60 mg khi cần thiết để tăng Natri huyết thanh).
Có hơn 4000 bệnh nhân được điều trị bằng các liếu uống tolvaptan trong các thử nghiệm lâm sảng
mờ hoặc có đối chứng với giả dược. Khoảng 650 trong sô những bệnh nhân nảy bị giảm Natri
mảu; khoảng 219 trong số những bệnh nhân bị giảm Natri mảu nảy được điều trị bằng tolvaptan
trong 6 thảng hoặc hơn.
Cảc tác dụng không mong muốn phổ biến nhất (tỷ lệ › 5% nhiều hơn giá dược) được thấy trong 2
thử nghiệm 30 ngảy, mù đôi, có đối chứng với giả dược ở bệnh nhân giảm Natri máu trong đó
tolvaptan được sử dụng ở cảc liều được điều chinh (15 mg đến 60 mg một lần mỗi ngảy) lả khảt |
nước, khô miệng, suy nhược, táo bón, đái rẳt hoặc đa niệu và tăng đường huyết. Trong cảc thử
nghiệm nảy,l 10% (23/223) trong số bệnh nhân được điếu trị bầng tolvaptan phải ngừng điều trị do
biếu hiện có hại, so sảnh với 12% (26/220) bệnh nhân dùng giả dược; không có tác dụng khôngfi/
mong muốn nảo lảm gián đoạn thử nghiệm xảy ra ở tỷ lệ > 1% trong số cảc bệnh nhân điều trị Ễ/
toivaptan `
Bảng 1 liệt kê cảc tảc dụng không mong muốn được báo cảo ở các bệnh nhân giảm Natri mảu
được điều trị với tolvaptan (Natri huyết thanh < 135 mquL) và ở một tỷ lệ nhiều hơn ít nhất 2%
các bệnh nhân dùng giả dược trong 2 thứ nghỉệm 30 ngảy, mù đôi, có đối chứng với giả dược.
Trong các thử nghiệm Inảy, 223 bệnh nhân đã dùng tolvaptan (_liều khời đẩu 15mg, chinh lên liếu
30 và 60mg khi cằn để tăng Natri mảu). Cảo biếu hiện có hại dẫn đến tử vong chiếm 6% ở các
bệnh nhân điều trị tolvaptan và 6% ở các bệnh nhân dùng giả dược trong các thử nghiệm nảy.
Bảng 1. Các tác dụng không mong muốn (nhiều hơn 2% so với giả dược) ở các bệnh nhân bị
giãm Natri máu được điều trị tolvaptan trong các thử nghiệm mù đôi, có đối chửng với giả
dược
Hệ cơ quan Tolvaptan Giả dược
Thuật ngữ ưa dùng MedDRA 15 mg/ngây-60 mg/ngây
(N = 223) (N = 220)
n 1% ) n (%)
Rối Ioạn đường tiêu hóa
Khô miệng 28 (13) 9 (4)
Chứng táo bón 16 (7) 4 (2)
Các rối loạn thông thường và các tác dụng không mong muốn xảy ra khi
uống thuốc
Khát“ | 35 (16) ] 11 <5)
Page 7 of IS
Suy nhược 19 (9) 9 (4)
Sốt 9 (4) 2 (1)
Rối loạn dinh dưỡng vã chuyến hoá
Tăng đường huyêtD 14 (6) 2 m
Chản ăn° 8 (4) 2 (1)
Rổi loạn tiết niỆu và thận
Chứng đải răt hoặc chứng đải nhiếu | 25 (11) | 7 (3)
Cảo biếu hiện sau được gộp vảo cảc ADR ở Bảng 1:
“ chửng khảt nhiều; b đải thảo đường; ° ăn không ngon miệng; d tăng lượng nước tiều, buồn tiều, tiếu đêm
Trong một phân nhóm các bệnh nhân bị giảm Natri mảu (N= —,475 Natri huyết thanh < 135 mEq/L)
được nhận vảo trong một thử nghiệm mù đôi, có đối chứng với giả dược (thời gian díếu trị trung
binh khoảng 9 thảng) trong sô các bệnh nhân mà tình trạng suy tim xấu hon, các tác dụng không
mong muôn sau xuất hiện ở các bệnh nhân được đíếu trị tolvaptan ở tỷ lệ nhiều hơn it nhất 2% so
với giả dược: tử vong (tolvaptan 42%, giá dược 38%), buổn nôn (tolvaptan 21%, giá dược 16%),
khảt (toivaptan 12%, giá dược 2%), khô miệng (tolvaptan 7%, giá dược 2%) vả chứng đái nhiều
hoặc đải rắt (tolvaptan 4%, giá dược 1%).
Xuất huyết đường tiêu hóa ở bệnh nhân xơ gan:
Ớ nhữngbệnh nhân bị xơ gan được điều trị bằng tolvaptan trong cảc thử nghiệm hạ Natri máu,
xuảt huyết tiêu hóa đã được bảo cáo trên 6 trong sỏ 63 (10%) bệnh nhân được điêu trị tolvaptan và
1 trong sô 57 (2%) bệnh nhân dùng gíả dược.
Cảc tảc dụng không mong muốn sau xuất hiện ở < 2% trên số bệnh nhân bị giảm Natri mảu được
điếu trị bằng SAMSCA vả ở tỷ lệ lớn hơn giá dược trong cảc nghỉên cứu mù đôi có đối chửng giả
dược (N= —607 tolvaptan, N=51 8 gỉả dược) hoặc ở < 2% trên sô bệnh nhân trong thứ nghỉệm không
có đối chứng cùa cảc bệnh nhân bị hạ Natri mảu (N=l ] 1) vả không được đề cập trong nhản thuốc.
Rối loạn hệ bạch huyết và mảu: đông mảu nội mạch lan tỏa
Rối Ioạn tím: huyết khối trong tim, rung thất '
Xét nghiệm: kéo dải thời gỉan prothrombin 2
Rối loạn đường riêu hóa: viêm đại trảng do thiếu máu
Rồi loạn dinh dưỡng và chuyến hoá: nhiễm toan xeton do đái thảo đường
Rối loạn cơ xuong và mô Iiên kểt; globin cơ niệu kịch phát
Hệ thần kinh: tai biến mạch mảu não
Rồi loạn thận tiết niệu: xuất huyết niệu đạo
Rối loạn ruyến vú vả hệ sinh sản (ởphụ nữ) : xuất huyết âm đạo
Rối loạn trung ihẩt, ngực, hệ hô hấp: tắc mạch phổi, suy hô hấp
Rồi Ioạn mạch: chứng huyết khối tĩnh mạch sâu
2. Kinh nghiệm sau khi đưa thuốc ra thị trường
Cảo tảo dụng không mong muốn sau đã được ghi nhận trong quá trình SAMSCA được lưu hảnh sử
dụng Do các tảc dụng không mong muốn được báo cáo tự nguyện từ một nhóm dân số không bỉết
sô lượng chỉnh xác nên không biết được tần suất hoặc xác định được mối liên quan với việc sử
dụng thuốc.
Thần kinh: Hội chứng hủy myeiin thấm thấu
Xét nghiệm: Tăng Natri máu
Page 8 of 15
.,.
I\
Loại bỏ iượng nước tự do thừa trong cơ thể lảm tảng độ thấm thấu huyết thanh và nồng độ Natri
mảu. Tất cả các bệnh nhân được đỉều trị bằng tolvaptan, đặc biệt lả những bệnh nhân có mửc Natri
máu trở về binh thường, nên tiếp tục được theo dõi để đảm bảo lượng Natri máu vẫn ở trong giới
hạn bình thường. Nếu thấy Natri máu cao, nên giảm liếu hoặc tạm ngừng sử dụng tolvaptan, kết
hợp với dùng nước hoặc truyền. Trong cảc nghiên cứu lâm sảng ở cảc bệnh nhân bị gỉảrn Natri
máu, tăng Natri mã… đã được bảo cảo như là một tảo dụng không mong muốn ờ 0,7% sô bệnh
nhân dùng to1vaptan so với 0,6% số bệnh nhân dùng giả dược; phân tích cảc số liệu trong phòng
thí nghiệm chỉ ra răng tỷ lệ bị tãng Natri máu là 1,7% ở cảc bệnh nhân dùng tolvaptan so với 0 8%
ở cảc bệnh nhân dùng giả dược.
Thỏng báo cho bác sỹ bẩ! kỳ tác dụng không mong muốn nản xảy ra khi dùng thuốc.
DƯỚC ĐÔNG HOC:
Dược động học của tolvaptan sau khi dùng cảc liếu đơn lên đến 480 mg và các đa liếu lên đến 300
mg ] lẩn/ngảy đã được khảo sát trên người khỏe mạnh. Dìện tích dưới đường cong (AUC) tãng tỷ
lệ thuận với liều dùng. Tuy nhiên, sau khi sử dụng liếu > 60mg, Cmax tăng ít hơn so với tỷ lệ tảng
cùa liếu dùng. Cảo đặc tính dược động học cùa tolvaptan có định, với trạng thái tỷ lệ ón định của
đối hình S- (- ) đến R-(+) ở khoảng 3 Sinh khả dụng tuyệt đối của tolvaptan khoảng 56%. Ít nhất
40% lỉếu được hấp thu lả toivaptan hoặc chất chuyển hoá Nồng độ đinh của tolvaptan ở khoảng
giữa 2 và 4 giờ sau uống thuốc Thức ăn không ảnh hướng đến sinh khả dụng cùa tolvaptan Số
liệu in vilro chi ra rằng tolvaptan là chất nên và chắt ức chế cùa P- -gp. Tolvaptan gắn kết nhiến với
protein huyết tương (99%) và phân bố trong thể tích biến kiến 3 leg. Nhìn chung, toivaptan được
bải tiết hoản toản bới đường không qua thận vả chủ yếu được chuyến hoá bởi CYP 3A. Sau liếu
uống, độ thanh thải khoảng 4 mL/phút/kg và thời gỉan bán thải pha cuội khoảng 12 giờ. Hệ số tích
lũy cùa tolvaptan với chế độ liếu ngảy một lần là 1,3 vả nồng độ đảy s 16% của nổng độ đình, gợi
ý thời gian bán thải thấp hơn 12 giờ. Có sự thay đối giữa cảc chủ thể về nổng độ đỉnh và trung
bình cùa tolvaptan với hệ số phần trăm cùa sự thay đối trong khoảng 30 đến 60%.
Ở cảc bệnh nhân bị giảm Natri máu độ thanh thải cùa toivaptan gỉảm còn khoảng 2 mL/phút/kg.
Suy gan trung binh hoặc nặng hoặc suy tim sung huyết lảm giảm độ thanh thải và tăng thể tich
phân bố của tolvaptan, nhưng không thay đối tương ứng liên quan dẳu hiệu lâm sảng Phơi nhiễm
hoặc phản ửng với tolvaptan ở các đối tượng có độ thanh thải creatinin trong khoảng từ 79 đến 10
mL/phứt và các bệnh nhân chức nảng thận binh thường không khảc nhau.
Trong một nghiến cứu ở các bệnh nhân có độ thanh thải creatinine trong khoảng 10— 124 mL/phủt
dùng một lỉếu đơn tolvaptan 60 mg, AUC vả Cmax cùa tolvaptan huyết tương thẩp hơn một nứa ở
những bệnh nhân bị suy thận nặng có liến quan đối chứng Đinh Natri mảu đạt 5 — 6 mquL,
không phụ thuộc vảo chức năng thận, nhưng tảc dụng khới đầu vả bổ sung của tolvaptan đến mủc
Natri máu sẽ chậm hơn ở những bệnh nhân bị suy thận nặng.
Dươc LƯC HOC ỳ’
1. Cơ chế tác dụng
Tolvaptan là chất đối kháng thụ thể V; vasoprcssin chợn lọc với ải lực vói thụ thể V2 gấp 1, 8 lần
so vởi vasoprcssin arginine tự nhiên Ái lực tolvaptan vởỉ thụ thế V; lớn hơn gấp 29 lần so với thụ
thể Vịa. Khi nông thuốc với liều từ 15 đến 60 mg tolvaptan gây đối khảng tảc dụng cùa
vasopressin vả lảm tảng bải tỉết nước tiếu dẫn đến tăng độ thanh thải nước tự đo (aquaresis), gỉảm
nông độ thầm thấu nước tiếu, vả lảm tăng nồng độ Natri huyết thanh Bải xuất Natri vả Kali qua
nước tiểu vả nổng độ Kalỉ huyết thanh không thay đối đảng kể Các chẳt chuyến hoá của tolvaptan
không hoặc có tác dụng đối khảng yếu với thụ thể Vg ở ngươi so Vởỉ toivaptan.
Nồng độ của AVP tự nhiên trong hưyết thanh có thế tãng (trung bình 29 pglmL) khi dùng
tolvaptan.
l’agc 9 of 15
2. Dược lực học
Ở các đối tượng khỏe mạnh khi uống 1iếư đơn SAMSCA 60 mg, tác dụng lợi tiếu và tăng Natri
xuất hiện trong vòng 2- 4 giờ sau uỏng thuốc. Đỉnh tảc dụng tăng khoảng 6 mEq Natri huyết thanh
và tăng khoảng 9 mL/phút tỷ lệ bải xuất nước tiếu đạt được trong vòng 4 đến 8 giờ sau uống
thuốc; do đó, tảo dụng dược lý chậm sau so vởi nồng độ tolvaptan trong huyết thanh. Khoảng 60%
đinh tảc dụng trên Natri huyết thanh được duy tri liên tục 24 giờ sau khi uỏng thuốc, nhưng tỷ lệ
bải xuất nước tiếu ở thời điếm nảy thì không được nâng lên nữa. Cảc Iiếu cao hơn 60 mg tolvaptan
không lảm tăng tác dụng lợi tìểu hay Natri huyết thanh hơn nữa. Tác dụng của tolvaptan trong các
khoáng Iiều khuyến cảo là từ 15 đến 60 mg dùng ngảy một lần để hạn chế tác dụng lợi tiểu và kết
quả lảm tãng nồng độ Natri.
Trong nghìên cứu đa liếu, có đối chứng với giả dược vả hoạt chất, song song, mù đôi (tolvaptan vả
giả được) vẽ tảo dụng của tolvaptan lên khoảng QTc, 172 người khỏe mạnh dùng ngân nhiên
tolvaptan 30 mg, tolvaptan 300mg, giả dược hoặc moxifioxacin 400 mg ngảy ] lẳn. Ớ hai liều 30
mg vả 300 mg, không có tảc dụng đảng kế của tolvaptan đểu khoảng QTc ờ ngảy ] vả ngảy 5. Ở
liều 300 mg, đỉnh tolvaptan huyết thanh cao hơn gấp khoảng 4 lần đinh ở liều 30 mg
Moxifioxacin tăng khoảng Q' I` o 12 ms vảo lủc 2 giờ sau khi uỏng thuốc ngảy ] vả 17 ms vảo lúc 1
giờ sau khi uống thuốc ngảy 5, cho thấy rằng nghiên cứu đã được thiết kế vả kiếm soát hợp lý để
phát hỉện ra tác dụng cùa tolvaptan lên khoảng QT
ĐÒC TỈNH PHI LÂM SÀNG:
Ung thư, đột biến gen, giảm khả năng sinh sản
Cho uống tolvaptan trọng hai nảm với chuột cống đực vả chuột cống cải với liều lên đến 1000
mg/kg/ngảy (gấp 162 lẩn liều tổi đa khuyến cáo dùng cho người [MRHD] dựa trên cơ sở diện tich
bề mặt cơ thế), vả chuột nhắt đực ở liếu lẽn đến 60 mg/kg/ngảy (gấp 5 lần MRHD) và chuột nhắt
cải ớ lìều lến đến 100 mg/kg/ngảy (8 lần MRHD) không lảm tăng tỷ lệ mắc cảc khối u.
Tolvaptan cho kết quả âm tinh khi xẻt nghỉệm độc tính gen trong hệ thống xét nghiệm in vilro
(định iượng đột biên vi khuân vả xét nghiệm bât thường nhièm sảc thế trong cảc tế bảo nguyên
bảo sợi ớ phỏi chuột đông Trung Quôc) và in vívo (định lượng vì nhân chuột công)
Trong một nghiên cứu về khả nãng sinh sản trong đó những con chuột cống đực và cái được cho
uỏng tolvaptan vởi liếu 100,300 hoặc 1000 mg/kg/ngảy, mức liều cao nhất có liến quan với việc
giảm đảng kế thế vảng và mô cắy so với mẫu chứng.
Độc tính về sinh sản và phá! !riến.’ ì/
Ở chuột cống mang thai, việc cho uống tolvaptan với liếu 10, 100 và 1000 mgfkg/ngả trong thời
gian hình thảnh các cơ quan bảo thai có liến quan vởi giảm tăng trọng lượng cơ thể chuột mẹ và
giảm tiếu thụ thực phẳm ở mức liếu ]00 và 1000 mg/kg/ngảy, vả giảm trọng lượng của thai nhi và
chậm hóa xương của bảo thai ở mức liếu 1000 mg/kg/ngảy (gấp 162 lằn MRHD dựa trên cơ sở
diện tich bề mặt cơ thế) Việc cho uống tolvaptan với iiếư 100,300 và 1000 mglkg/ngảy ở thỏ
mang thai trong thời gian hình thảnh cảc cơ quan có liên quan với giảm tăng trọng lượng cơ thể
cùa thò mẹ và giảm tiêu thụ thực phẩm ơ tất cả cảc liều, và gây sẩy thai ở liều trung binh và liếu
cao Ở mửc liếu 1000 mg/kg/ngảy (gắp 324 lần MRHD), đã quan sảt thấy có tăng tỷ lệ thai lưu,
mắt nhò, mí mắt mở, hớ hảm ếch, ngăn chi, dị tật xương Chưa có nghiên cứu đầy đủ và được
kiếm soát tốt cùa SAMSCA ở phụ nữ mang thai. SAMSCA nên được sử dụng trong thai kỳ nểư
lợi ích đưa lại lả cao hơn nguy cơ cho thai nhi.
NGHIÊN CỨU LÂM SÀNG:
Hạ natri máu:
Trong hai nghíên cứu đa trung tâm, có đối chứng với gỉả dược, mù đôi (SALT- -1 vả SALT- -2), tổng
cộng 424 bệnh nhân bị giảm Natri mảu có tăng thể tích vả binh thể tích (Natri huyết thanh < 135
Page 10 of 15
mEq/L) do nhiều nguyên nhân cơ bản (suy tim, xơ gan, hội chứng tiết hóc môn chống bải niệu
không thỉch hợp [SIADH] vả cảc bệnh khác) được điếu trị trong 30 ngảy với tolvaptan hoặc giả
dược sau đó theo đõi thêm 7 ngảy sau khi dừng thuốc. Bệnh nhân có triệu chứng, bệnh nhân có
thế phải bổ sung muối trong quá trình điếu trị, bệnh nhân hạ Natri mảu cấp tinh và thoảng qua liên
quan đến chấn thương đầu hoặc bệnh nhân sau mổ và bệnh nhân hạ Natri máu cơ bản do quá khát,
suy thượng thận không kiếm soát hoặc suy giảp không kiếm soát đã được loại trừ. Bệnh nhân
được chọn ngẫu nhiên để uống hoặc gỉả dược (N= 220) hoặc tolvaptan (N= 223) o liều uống khời
đầu 15 mg môi ngảy một lần. Nồng độ Natri huyết thanh trung bình lúc bắt đầu vảo nghiên cứu lả
129 mEq/L Hạn chế dịch lá có thế trảnh được nêu có thế trong 24 gỉờ đầu tiên điếu trị để trảnh sự
điếu chỉnh quá nhanh chóng của Natri huyết thanh, vả trong 24 giờ đầu tiên điếu trị 87% bệnh
nhân không có hạn chế dịch. Sau đó, bệnh nhân có thể tiếp tục hoặc khởi đầu hạn chế dịch (được
xảc định là lượng dịch uống hảng ngảy_ < 1 ,0 lít/ngảy) như đã nêu ra về mặt iâm sảng.
Liều tolvaptan có thế được tăng lến mỗi 24 giờ đến 30 mg mỗi ngảy một lần, sau đó đến 60 mg
mỗi ngáy một lần, cho đến khi một trong hai hoặc liếu tối đa 60 mg hoặc Natri máu bình thường
(Natri huyết thanh > 135 mEq/L) đã đạt được. Nồng độ Natri huyết thanh đã được xảo định 8 giờ
sau khi bắt đầu uống thuốc và hảng ngảy cho đến 72 giờ, trong thời gian đó chuẩn độ đã được
hoản thảnh Việc điếu trị được duy trì trong 30 ngảy và đánh giá Natri huyết thanh vảo các ngảy
11, 18, 25 và 30. Vảo ngảy kết thúc nghiên cứu, tất cả các bệnh nhân trước đó điều trị hạ Natri
mảu đã được đánh giá lại sau 7 ngảy. Tiêu chí chính cho những nghiên cửu nảy là mức AUC trung
binh hảng ngảy cho sự thay đổi Natri huyết thanh từ đường cơ sở đến ngảy thứ 4 và từ đường cơ
sở đến ngảy thứ 30 ở bệnh nhân có Natri huyết thanh dưới 135 mEq/L So với giả dược, tolvaptan
gây ra một sự gia tăng lớn hợn về mặt thống kê mức Natri huyết thanh (p < 0 ,0001) trong cả hai
giai đoạn trong cả hai nghiên cứu (xem bảng 2). Đối vởi nhũng bệnh nhân có Natri huyết thanh
<130 mEq’L hoặc < 125 mEq/L, tảc dụng tại ngảyl thứ 4 và ngảy thứ 30 vẫn có ý nghĩa (xem Bảng
2) Tác dụng nảy cũng dã được nhỉn thấy trên tắt cả các nhóm bệnh (ví dụ như CHF, xơ gan,
SIADH / khảc).
Bảng 2. Tác dụng điếu trị vởỉ tolvaptan 15 mglngây đển 60 mglngây
Tolvaptan , .i
15 mg/ngảy— Giả dược Tac dụng dự kien
60 mglngây (95 /0 CD
Bệnh nhân có mức Natri huyết thanh < 135 mEqu (quần thể ITT)
Thay đối huyết thanh trung
bình hảng ngảy [Nai] AUC cơ
sở đên ngảy 4 (mEq/L) 4’02ỂỄ—8) OỄỗẫ›® 3,7<(ỄỀ-ỗlỏỉ)
Trung bình (SD) ’ ² P ,
N
Thay đôi huyết thanh trung
bmlịẵlẳẳẳ ẳgỆy [Na ] AUC cơ 6,2 (4’0) 1,8 (3a7) 4,6 (3,9—5,2)
gay 30 (mEq/L) 213 203 < 0 0001
Trung bỉnh (SD) P ,
N
… , i A . 14% 25%
o *
/o bẹnh nhan can hạn che dịch 30/215 51/206 p < 0,01
. Phân nhóm có mức Natri huyết thanh < 130 mquL
Thay đôi huyêt thanh trung
bình hảng ngảy [Nai] AUC cơ
" ả ` 458 330 0,7 2,5 ’ ”- ’
sơ đen ngay 4 (mquL) 1ẵ0 ) 1ỗ5 ) 4 2<(30Ễ1050Ệ)
Trung bình (SD) P i
N
Page Ilof15
"\..-
Thay đối huyết thanh trung
\ i u +
bmh.haflg “gẳly [Na ] AUC °° 7,914,1i 2,614,21 5,5 (4,4-6,5)
sơ đen ngay 30 (mEq/L) 110 105 < 0 0001
, p ,
Trung binh (SD)
N
, , _ o 36°/
% bệnh nhân cân hạn che dịch* 2ẫ/91/ỉ’0 3811ỗ6 p < 0,01
Phân nhóm có mửc Natri huyết thanh < 125 mE IL
Thay đôi huyết thanh trung
\ . : +
bmh Ề“’“ẵ "gẫy [Na ] AUC °“ 5,7 (3,8) 1,0 (1,8) 5,3 (3,8-6,9)
sơ đen ngay 4 (mEq/L) 26 30 p < 0 0001
Trung bình (SD) ’
, N
Thay đôi huyêt thanh trung
bmh,harẵg "gỂy [Nai AUC CƠ 10,0 (4,8) 4,1 (4,5) 5,7 (3,1-8,3)
sơ đen ngay 30 (mEq/L) 26 30 p<00001
Trung binh (SD) ’
N
, › . 35% 50%
0 ^ ^ " " * =
/o bẹnh nhan can hạn che dịch 9/26 15130 p 0,14
*Hạn chế dịch được xảc định lả < 1L/ngảy vảo bẫt cứ lủc nảo trong thời gian điếu trị
Ở những bệnh nhân hạ Natri máu (được xảc định là <135 mEq/L), nồng độ Natri huyết thanh tăng
lên đến một mửc độ lớn hơn đảng kế 0 những bệnh nhân được điếu trị tolvaptan so với bệnh nhân
dùng gíả dược díễu trị cảng sớm 8 giờ sau liều đầu tiên, và sự thay đối đã được duy trì trong 30
ngảy Tỷ lệ bệnh nhân cân hạn chế chất lỏng (được xác định lả < 1 L/ngảy vảo bất cứ lúc nảo
trong thời gian điếu trị) cũng it hơn đáng kể (p < 0 ,01) ở nhóm uống tolvaptan (30/215,14'V0) so
với nhóm dùng giả dược (51/206, 25%).
Hình 1 cho thấy sự thay đổi so với ban đầu mức Natri huyết thanh ờ nhũng bệnh nhân có Natri
huyết thanh < 135 mEq/L. Trong thời gian 7 ngảy kế từ ngảy ngừng uống tolvaptan, nồng độ Natri
huyết thanh 6; những bệnh nhân được uỏng tolvaptan giảm xuông mức tương tự như những bệnh
nhân dùng giả dược.
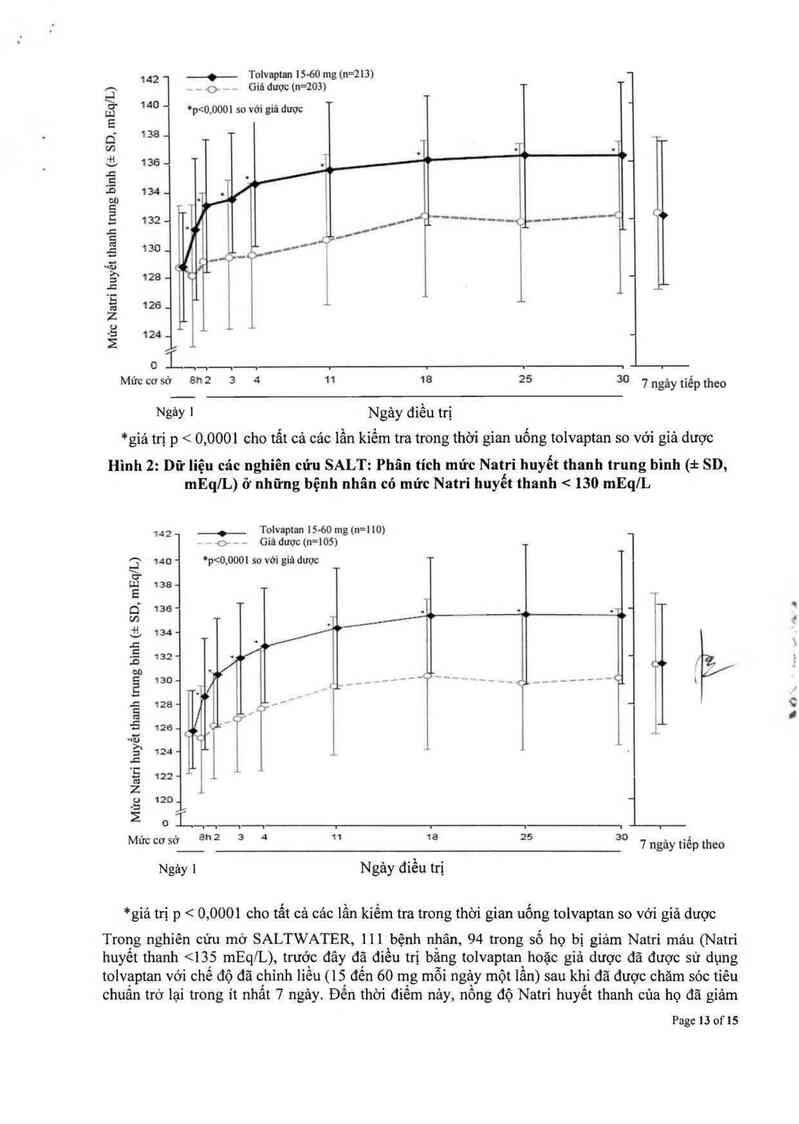
Hình 1: Dữ liệu các nghiến cứu SALT: Phân tích mú'c Natri huyết thanh trung bình (i SD,
mquL) ở những bệnh nhân có mức Natri huyết thanh < 135 mquL
Page 12 of15
142 q _.— Tợlvaptan 15-60 mg (n=213) T
ị , © , Glá duợc (n=203)
@; “° - °p<0.0001 so vởi giá dược “
E ae
" 1 -
9: .1 .'
3 136 … -
5
.E
» 134 -
DD
Ẹ _, 1
Ê 132 - ————————— ,. ________ . -
Ế 1
-5 130 -
«ồ
g~ 128 … —
£
ã 126 - '
2
U
—b 124 - -
ẵ ,
Mức cơ sở Bh ² 3 4 11 18 ²5 30 7 ngảy tiếp theo
Ngầy l Ngảy điêu trị
*giả trị p < 0, 0001 cho tất cả cảc lần kiếm tra trong thời gian uống tolvaptan so với giả dược
Hình 2: Dữ Iiệu cảc nghiên cứu SALT: Phân tích mức Natri huyết thanh trung binh (:1: SD,
mquL) ở những bệnh nhân có mức Natri huyết thanh < 130 mquL
142 + Tợlvaptan 15—60 mg (n=1 10) _
<> _ _ Glá dược (n=105)
ị un ~ °p<0,0001 so với giả dược
ơ
m 138 ~
E
Q“ 136 - .
m 4
ịL 134 -
€
3 132 "
Ế) 130 1
- … <
Ê ,
.: 128 - \
ả !
ẵ 126 …
…$ (
Ề 124 —
.:
'E
F; 122 -
Z
0 120 - -
—b 4:
2 0 I I I I I I I I
. ~ 8112 3 4 11 18 25 o .;
Mưc cơ sơ 7 ngảy t1ep theo
Ngảy ] Ngảy điêu trị
*giá trị p < 0,0001 cho tất cả cảc lần kiểm tra trong thời gian uống toIvaptan so với giả dược
Trong nghiên cứu mở SALTWATER, 111 bệnh nhân, 94 trong số họ bị giảm Natri mảu (Natri
huyết thanh <135 mEq/L), trước đây đặt điếu trị bằng tolvaptan hoặc giả dược đã được sử dụng
tolvaptan với chế độ đã chỉnh liều (15 đến 60 mg môi ngảy một lần) sau khi đã được chăm sóc tiêu
chuẩn trở lại trong ít nhất 7 ngảy. Đến thời điểm nảy, nông độ Natri huyết thanh cùa họ đã giảm
Page 13 oflS
xuống mức ở trong khoảng giữa mức ban đầu của họ vả mức sau khi dùng giả dược. Khi bắt đầu
điều trị, nổng độ Natri huyết thanh trung bình tăng lên mức giống như mức đã quan sảt thấy tmớc
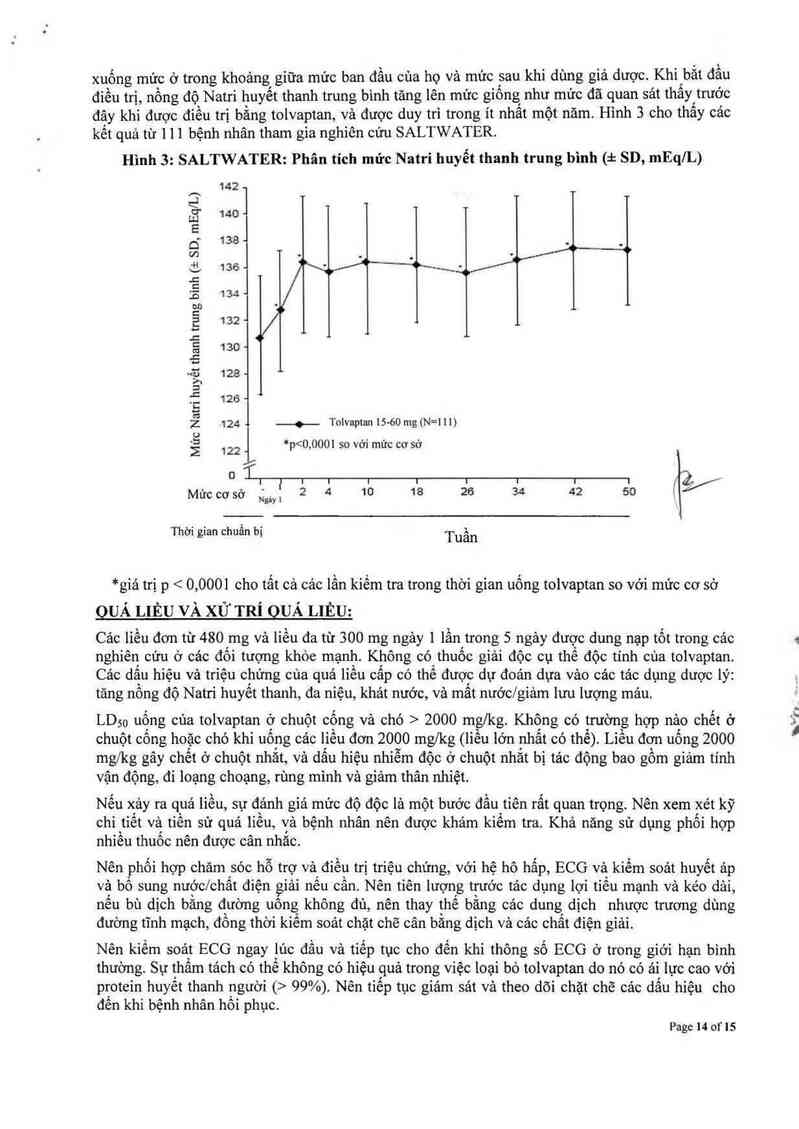
đậy khi được điếu trị bằng tolvaptan, và được duy trì trong it nhất một năm. Hình 3 cho thấy cảc
kết quả từ 1 l 1 bệnh nhân tham gia nghiến cứu SALTWATER.
Hình 3: SALTWATER: Phân tích mửc Natri huyết thanh trung bình (ả: SD, mEq/L)
1421
140 -
138 -
Mức Natri huyết thanh trung binh (i SD, mEq/L)
ủi
N
.124 . + Tolvaptan 15›60 mg (N=] ] l)
, . , .
122 _ p<0.0001 so VỚI mưc cơ sơ
,»
0 T | ) 1 I I I | I | —| /
Mức cơ sở Nà 1 4 10 18 26 34 42 50
8 y
. . A . À
Thờ1 gian chuan bị Tuan
*giả trị p < 0,000] cho tất cả các lần kiểm tra trong thời gian uống tolvaptan so với mức cơ sở
OUÁ LIÊU VÀ xử TRÍ QUÁ LIÊU:
Cảc liều đơn từ 480 mg vả Iiều đa từ 300 mg ngảy 1 lần Itrong 5 ngảy được dung nạp tốt trong cảc
nghiên cứu ở cảc đối tượng khỏe mạnh. Không có thuốc giải độc cụ thể độc tính của tolvaptan.
Các dấu hiệu vả triệu chứng của quá liều cấp có thế được dự đoản dựa vâo cảc tác dụng dược lý:
tăng nồng độ Natri huyêt thanh đa niệu, khảt nước, và mât nước/giảm lưu lượng mảu
LDso uống của tolvaptan ớ chuột cống vả chó > 2000 mglkg. Không có trường hợp nảo chết ở
chuột công hoặc chó khi uống các liều đơn 2000 mg/kg (liếu lớn nhất có thế). Liều đơn uống 2000
mglkg gây chết ở chuột nhắt, vả dấu hiện nhiễm độc ở chuột nhắt bị tảc động bao gồm giảm tính
vận động, đi loạng choạng, rùng mình và giảm thân nhiệt
Nếu xảy ra quá liếu, sự đảnh giá mức độ độc là một bước đầu tiên rất quan trọng Nên xem xét kỹ
chi tiết vả tiến sử quá liều, và bệnh nhân nên được khảm kiếm tra. Khả năng sử dụng phối hợp
nhiến thuốc nên được cân nhắc.
Nên phối hợp chăm sóc hỗ trợ và điếu trị triệu chứng, với hệ hô hấp, ECG vả kiếm soát huyết áp
vả bổ sung nước/chất điện giải nếu cần. Nên tiên lượng trước tảc dụng lợi tiếu mạnh và kéo dải,
nếu bù dịch bằng đường uỏng không đù, nên thay thế bằng cảc dung dịch nhược trương dùng
đuờng tĩnh mạch, đồng thời kiếm soát chặt chẽ cân bằng dịch vả cảc chất điện giải.
Nên kìềm soát ECG ngay lủc đầu và tiếp tục cho đến khi thông số ECG ở trong giới hạn bình
thường. Sự thẩm tảch có thế không có hiệu quả trong việc loại bỏ tolvaptan do nó có ải lực cao với
prptein huyết thanh người (> 99%). Nên tiếp tục gỉảm sát và theo dõi chặt chẽ các dấu hiệu cho
đên khi bệnh nhân hôi phục.
Page 14 of 15
""Ifl
MÔ TÁ:
Tolvaptan có tên hóa học là (i)-4'-[(7-chioro—Z,3,4,5-tetrahydro-S-hydroxy-lH-l-benzazepin-l-yl)
carbonyl]—o-tolu-m—toluidide.
Công thức phân tứ: CzestClNzO;
Trọng lượng phân tứ: 448,94.
Công thức cấu tạo: /
HO
CI °
ĐIỀU KIẺN BẢO OUẢN: Bảo quản nơi khô, nhiệt độ không quá 30°C.
HAN DÙNG: 36 tháng kế từ ngảy sản xuất.
NHÀ SẢN XUẤT: Korea Otsuka Pharmaceutical Co., Ltd.
27, Jeyakgongdan 3-gi1, Hyangnam-eup, Hwaseong-si, Gyeonggi-do, Hản Quốc.
TUQ. cục TRUỞNG
P.TRUỜNGPHÒNG
«Ấỷưyẫn JỐJỹ Jfíẫng
Page 15 of 15
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng