











LABEL
Artwork of secondary packaging
\\\)
ằ\Ì\ \ Ồx\ \ \\ \ \ồ\_.\\ \
a'\_\
xxxx xx- xx ,\\x_\
\\ `-.\
\\ \, xxxx-xx—xx \
\\\\\\\
1…104 lwủnlxsu lmuưmxsmos
ỔRibomustin“
Pwdor for eonuntnh
for solution for infucion
Remơ bledtxưởm bởi
Jenmn … NV.
T…… 30. Bouu. B—2340,
Beb'unBl
Xuất xử: Bồ
CT'ĐKi Janlun-Cúeg Ltd., nm Lm
DMK
`
Janssen J
Ốỹểé (éỏ' w .ctD)
ị2nĩm)
ví… PHQNG
ĐẠI DI`ẸN
BO Y TẾ
CL'C Ql'.-\N Li" D…C
ĐẨPH
ẸDtYẸT
áu -ẵp~é…ẻỉa
R, R:
CRibomustin" ORlbomustm
muh W Bond:musdn Nydmchlodd
25 mg 25 mg
em… … aooc. m… Bột pha dỊch cọ… m 66
“* "'° pha dung dịch tllm truyỒn
Chỉ ơưm. mu om. m ui ưnh mạch
thvùdctfửugtinkhác'Xltì Lodtưa25mu…n
xemtrongtùhườngcủưủ hydroditond.tươnum
dung … m. 22,7 mg bondơnusun
SO kh hom 1 !
muôcsAumeoaow aằựềMWmưủsgm
oe anu TAY TRẺ EM m“ MM
_ SĐK1VN - xxxxx - xx
oọc KỸ HƯỞNG DAN sư
oụuo mươc x… nùuo Hộọt nọ
\
Janssen J
m
ORibomustin'
WM…
25 mg
sm bobw 30°C. P…
hun Im.
lndleltnm. mm
…… other
nhưmotm: Mu b …
…
PRESWTDN WLY
KEEP OUT OF mu
OFCHILDREN
READ THE LEAFLET
CAREFULLY BEFORE USE
0 …t-Oiln2015
SP_Ribomustin_25mg_DE_v2
LABEL
Artwork of primary packaging
fflibomustin'2s mg
Icndmultmc nymumona I Imdmumn mmcmoud ]BnSSEUĩ
lột phe dịch đ_hn đận d phi dung Ịeh tihl tuyến ỉnh mgeh
Lo chủ 25 mg bendamullm hydrochlorid tương 6ch 22 7 mg mamusm
Mlnuhetumd bylSln mất bởi Oncotec Phlnne Piodukbon GmbH, GennlnyĐúc
Retused by!th xuởng bởi Jinsscn Phannnuutu NV. quuano'
@ Jun…«Colng 2015
661354
PP_Ribomuslin__25mg DE v2
RIBOMUSTINTM
Thuốc nây chỉ dgmg theo đơn của bác sỹ.
Đ c ' hướng dân sử dụng trước khi dùng.
Neu can thêm thông tin xin hỏiỷ kiến bác sỹ.
THÀNH PHẦN _
Bendamustin hydrochlorid dạng bột vi tinh thể, mảu trắng đê hoản nguyên và pha loãng
thảnh dung dịch truyền tĩnh mạch.
Lọ chứa 25 mg bendamustin hydrochlorid, tương đương 22,7 mg bendamustin.
Lọ chứa 100 mg bendamustin hydrochlorid, tương đương 90.8 mg bendamustin.
] ml dịch đậm đặc chứa 2,5 mg bendamustin hydrochlorid khi được hoản nguyên theo
Hướng dẫn sử dụng và xử lý.
Tá dược: Mannitol
CHỈ ĐỊNH
Bệnh bạch cẩu lympho mạn: Điểu trị bước một cho bệnh bạch cấu lympho mạn (giai
đoạn B hoặc C theo Binet) ở bệnh nhân không thich hợp hóa từ phôi hợp với fludarabin.
U lympho không Hodgkin: U lympho không Hodgkin thể diễn tiến chậm ở bệnh nhân
bệnh tiên triên sau điều trị với rituximab hoặc hóa trị phối hợp với rituximab.
Đa u tủy: Điếu trị bước một cho đa u tủy (phân loại Durie-Salmon giai đoạn II có tiến
triến hay giai đoạn 111) phối hợp với prednison ở bệnh nhân trên 65 tuối mà không thích
hợp ghép tế bảo gốc tự thân và bệnh nhân có bệnh lý thằn kinh trên lâm sảng vảo thời
điểm chấn đoản mã không thể sử dụng điếu trị có bortezomỉb hay thalidomid.
LIÊU DÙNG VÀ CÁCH DÙNG
Dùng tiêm truyền tĩnh mạch trong 30—60 phút.
Bệnh bạch cẩu lympho mạn: bendamustin hydrochlorid 100 mglm² diện tích bề mặt cơ
thể, vảo ngảy 1 và ngảy 2 cùa cảc chu kỳ, mỗi chu kỳ 4 tuẫn, tối đa 6 chu kỳ.
U lympho không Hodgkin: bendamustin hydrochlorid 120 mglm² diện tích bề mặt cơ
thể vảo ngảy 1 và ngảy 2 cùa cảc chu kỳ, mỗi chu kỳ 3 tuần, trong ít nhất 6 đến 8 chu kỳ
(tối đa 8 chu kỳ).
Đa u tủy: bendamustin hydrochlorid 120-150 mg/m² diện tích bề mặt cơ thế, vảo ngảy 1
và ngảy 2, phối hợp với prednison 60 mg/m² diện tích bề mặt cơ thể tiêm tĩnh mạch hay
uống từ ngảy ] đến ngảy 4 cùa cảc chu kỳ, mỗi chu kỳ 4 tuần trong ít nhất 3 chu kỳ.
Nên trì hoãn hay ngừng điếu trị nếu số lượng bạch cầu giảm 3.000 lụL vả/ hoặc số lượng
tiểu cầu giảm < 75. OOO/ụL. Có thể tiếp tục điều trị sau khi số lượng bạch cầu tăng >
4. OOO/ụL vả sô lượng tiều câu tăng > 100. OOO/ụL.
Số lượng bạch cấu và tiếu cầu thấp nhất đo được sau 14- 20 ngảy, phục hồi sau 3- 5 tuần.
Khuyến cảo nên theo dõi chặt chẽ công thức mảu trong khoảng thời gian nghỉ không đỉếu
trị (xem Cảnh báo vả thận trọng).
Pl_Ribomustin_DE_lPl Dec 2014_v1 11’12
ASEN
. ì"
Trong trường hợp độc tính không thuộc hưyết học, việc giảm liều phải dựa trên mức độ
độc tính xâu nhất theo Tiếu chuẩn độc tính thường gặp (CTC) của chu kỳ trước. Khuyến
cáo giảm 50% liếu dùng trong trường hợp độc tinh mức độ 3 theo CTC. Khuyến cảo
ngừng điếu trị trong trường hợp độc tính mức độ 4 theo CTC.
Nếu cẩn điếu chinh liếu cho một bệnh nhãn thì liều đã giảm được tính tiêng cho bệnh
nhân đó phải được dùng vảo ngảy 1 và ngảy 2 của chu kỳ điếu trị tương ứng.
Xem hướng dẫn chuẩn bị và sử dụng thuốc trong mục Hướng dẫn sử dụng và xử lý.
Suy gan
Dụa trên dữ liệu dược động học, không cần điếu chinh liếu 6 bệnh nhân suy gan nhẹ
(bỉlirubin huyết thanh < 1 ,2 mg/dL). Khuyến cáo giám 30% liều dùng ở bệnh nhân suy
gan trung bình (bìlirubin huyết thanh 1,2- 3 mg/dL).
Khộng có sẵn dữ liệu ở bệnh nhân suy gan nặng (bilirubin huyết thanh > 3 mgde) (xem
Chống chỉ định).
Suy thận ` ` `
Dựa trên dữ liệu dược động học, không cân điêu chinh liêu ở bệnh nhân có độ thanh thải
creatinin > 10 mL/phút. Kinh nghiệm ở bệnh nhân suy thận nặng còn hạn chế.
Bệnh nhân nhi
Tinh an toản và hiệu quả của bendamustin trên bệnh nhân nhi chưa được xác lập do dữ
liệu còn hạn chê. -
Bệnh nhân `cao tuổi , ` \ ` _
Không có băng chứng cho thây cân điêu chỉnh liếu ở bệnh nhân cao tuôi (xem Đặc tính
dược động học).
CHỐNG CHỈ ĐỊNH
Quá mẫn với hoạt chất hoặc với bất kỳ tả dược nảo (xem Tả dược)
Đang cho con bú
Suy gan nặng (bilirubin huyết thanh > 3 mg/dL)
Vảng da
Suy tùy xương nặng và thay đối số lượng tế bảo máu nghiêm trọng (bạch cầu giảm <
3.000 /ụL vả] hoặc tiểu cầu giảm < 75.000/ụL)
Trải qua đại phẫu dưới 30 ngảy trước khi bắt đầu điếu trị
Nhiễm trùng, đặc biệt đi kèm giám bạch cằu
Đang chùng ngừa bệnh sốt vảng
CẨNH BÁO VÀ THẬN TRỌNG
Suy tủy
Bệnh nhân được diếư trị với bendamustìn hydrochlorid có thế bị suy tùy (suy tủy xương).
Khi có biển cố suy tủy do điều trị, nên theo dõi bạch cầu, tiếu câu, hemoglobin và bạch
cầu trung tính và đánh giá lại trước khi bắt đầu chu kỳ điếu trị tiếp theo. Trước khi bắt
đầu chu kỳ điếu trị tiếp theo khuyến cảo cần đạt được các thông số sau đây: số lượng
bạch cẳu > 4. 000/ụL và số lượng tiến cầu > 100. 000/ ụL
Suy tủy do điếu trị có thế cân điếu chinh liếu vả/hoặc trì hoãn liếu. Không nên dùng
ribomustin khi bị suy tùy nặng hoặc thay đối số lượng tế bảo máu nghiêm trọng. Xem
phần Liều dùng và cảch dùng.
Nhiễm trùng
Đã có bảo cáo về nhiễm trùng, bao gồm viêm phối và nhiễm khuẩn huyết. Trong vải
trường hợp hiếm gặp, nhiễm trùng liên quan với tình trạng cần phải nhập viện, sôc nhiễm
Pl_Ribomustin_DE_lPl Dec 2014_v1 21" 1 2
A \\
l/ . h"A
trùng và tử vong. Bệnh nhân suy túy sau điếu trị với bendamustin hydrochlorid thi dễ bị
nhiễm trùng. Bệnh nhân bị suy tủy sau điếu trị vởi Ribomustin được khuyên liên hệ với
thầy thuốc nêu có nhũng triệu chứng hay dấu hiện nhiễm trùng, bao gôm sốt hay triệu
chứng của đường hô hấp.
Phản ứng trên da
Một sô phản ứng trên da dã dược bảo cảo Cảc biến cố nảy bao gổm phảt ban phản ứng
độc trên da và phảt ban da dạng bóng nước. Một vải biến có xảy ra khi dùng bendamustin
kết hợp với các tảc nhân chống ung thư khác, do đó chưa rõ mối liên hệ chính xác. Khi
xuất hiện phản ứng trên da. nêu tiêp tục điếu trị thì cảc phản ứng nảy có thể tiến triến và
nặng lên; vì thế cân theo dõi chặt chẽ cảc bệnh nhân có phản ưng da. Nếu phản ứng da
nghiêm trọng hoặc tiến triền, nên tạm dừng hay ngừng điếu trị Ribomustin. Đối với
những phản ứng trên đa nghiêm trọng mà nghi ngờ có liến quan với bendamustin
hydrochlorid thì nên ngừng điếu tn'. Đã có bảo cảo vê cảc trường hợp bị hội chứng
Stevens-Johnson vả hoại từ biểu bì nhiễm độc (TEN) khi dùng bendamustin đông thời
với allopurinol và các thuốc khác dược biết gây nên hội chứng nảy.
Bệnh nhân có các rổi Iogn tim `
Nên theo dõi chặt chế nông độ kali trong mảu trong thời gian điêu trị với bendamustin
hydrochlorid và nên bỏ sung kali khi K+ <3,5 mEq/L và phải đo diện tâm đô.
Buồn_nõn, nôn
Có thế dùng thuôo chông nôn đê điêu trị cảc triệu chứng buôn nôn vả nôn.
Hội chửng ly giải khổỉ u
Đã có báo cáo về hội chứng ly giải khối u liên quan đến điếu trị với Ribomustin ở những
bệnh nhân tham gia cảc thử nghiệm lâm sảng. Hội chứng nảy có khuynh hướng xảy ra
trong vòng 48 giờ của liếu Ribomustin đầu tiên vả nêu không can thiệp có thể dẫn đến
suy thận câp vả tử vong. Các biện phảp dự phòng bao gôm tình trạng dịch đầy đủ, theo
dõi chặt chế sinh hóa mảu, đặc biệt lả nông độ kali vả acid uric. Có thế cân nhắc sử dụng
allopurinol trong 1 dến 2 tuần đầu tiên điếu m với Ribomustin nhưng không nhất thiết là
một diều tri tìêu chuẩn.
Sốc phản vệ
Các phản ứng trong khi truyền đối với bendamustin hydrochlorid thường xảy ra ở cảc thử
nghiệm lâm sảng. Nhin chung cảc triệu chứng thường nhẹ, bao gôm sốt, ớn lạnh, ngứa và
nôi ban. Trong một số hiếm trường hợp đã gặp phản ứng phản vệ hay sốc phản vệ nặng.
Phải hỏi bệnh nhân về cảc triệu chứng gợi ý phản ứng do truyền sau cho kỳ điếu trị đầu
tiên. Phải cân nhắc sử dụng các biện pháp phòng ngừa cảc phản ứng nặng, bao gổm sử
dụng khảng histamin, hạ sốt và corticosteroid ở những chu kỳ tiếp theo trên những bệnh
nhân có xảy ra phản ứng tiêm truyền trước đó
Những bệnh nhân bị phản ứng kiến dị ứng độ 3 hoặc xấu hơn là những trường hợp điển
hình không được sử dụng lại thuốc.
Ngừa thai
Bendamustin hydrochlorid lả chất gây đột biến và quái thai.
Phụ nữ không nên có thai trong thời gian điếu trị. Bệnh nhân nam không nến có con trong
lúc điếu trị và đến 6 thảng sau điếu trị. Cảc bệnh nhân nảy nên được tư vấn về việc bảo
quản tinh trùng trước khi điều trị với Ribomustin bời vì có khả năng bị vô sinh không hồi
phục.
T hoá! mạch
P!_Ribomusrin_DE_lPl Dec 2014 v! 3/12
,\ `ó \\
II '/1".
'l
Nến ngừng ngay lập tức nếu truyền thuốc ra ngoải mạch. Nến lấy kim ra sau khi đã hủt ra
một it. Sau đó nên chườm lạnh vùng mô bị tôn thương và đề cao cảnh tay. Chưa thấy lợi
ích rõ rảng với những điếu trị hỗ trợ như sử dụng corticosteroid.
Bệnh ác tính khăc
Đã có bảo cáo về cảc khối u thứ phát, bao gồm hội chửng rối loạn sinh tủy, các rối loạn
tăng sinh tủy, bệnh bạch cầu cấp dòng tùy vả carcinôm phế quản Chưa xác định được
mối liên quan với điểu trị bendamustin.
T at hoạt động viêm gan B
Đã có bảo cáo về tái hoạt động viêm gan B bao gồm kết cục tử vong và có thể xuất hiện
viếm gan do tái hoạt vi rút viêm gan B. Nến áp dụng các biện phảp thích hợp xác định
bệnh nhăn nhiễm viêm gan B trước khi điếu trị với Ribomustin, nên theo dõi thường
xuyên chức nãng gan và các chi dắu (markers) viêm gan B, nên sử dụng thuốc thích hợp
vả/hoặc biện pháp phòng ngừa đế ngản ngừa tải hoạt vi rút viếm gan B.
TƯỚNG TÁC VỚI CÁC THUỐC KHÁC VÀ CÁC LOẠI TƯO’NG TÁC KHÁC
Không có nghiên cứu tương tác thuốc in-vivo.
Khi kết hợp Ribomustin với cảc thuốc gây ức chế tùy, có thế có khả năng ảnh hướng trên
tủy xương do Ribomustin vả/hoặc các thuốc sử dụng đồng thời. Bất kỳ đỉếu trị nảo lảm
giảm thể trạng của bệnh nhân hay suy giảm chức năng tùy xương cũng có thế gia tăng
độc tính của Ribomustin.
Kết hợp Ribomustin với cyclosporin hay tacrolimus có thể dẫn đến ức chế miễn dịch quá
mức với nguy cơ lảm tăng sinh dòng lympho.
Kìm hãm phân bảo có thể lâm giảm sự tạo thảnh kháng thể sau chúng ngùa vi rút sống
giảm độc lực và lảm tãng nguy cơ nhiễm trùng có thể dẫn đến kết cục tử vong. Nguy cơ
nảy tăng_lến ở những đối tượng đã bị ức chế miễn dịch bới bệnh lý nến của họ.
Sự chuyên hóa bendamustin liến quan đến enzym có cùng chức năng cytochrom P450
(CYP) 1A2 (xem Đặc tỉnh dược động học). Vì thế, có khả năng xảy ra tương tảo với cảc
chất ức chế CYP1A2 (như t1uvoxamin, ciprofioxacin, acyclovir, cimetidin)
PHỤ NỮ có THAI, CHO CON BÚ VÀ KHẢ NĂNG SINH SẢN
Phụ nữ có thai
Không đủ dữ kiện về việc sử dụng Ribomustin ơ phụ nữ có thai. Trên các nghiến cứu tiến
lâm sảng, bendamustin lả chất gây độc phôi /thai, sinh quải thai và gây độc gen (xem
Thông tin tíền lâm sảng). Phụ nữ có khả nãng mang thai phải dùng cảc biện phảp tránh
thai hiệu quả trước, trong và một tháng sau khi điếu trị với Ribomustin.
Trong thời gian mang thai, không nên sư dụng Ribomustin trừ khí lợi ich vượt trội nguy
cơ. Người mẹ nên được biết vê nguy cơ đối với thai Nếu điếu trị vởi Ribomustin lả hoản
toản cân thiết trong lủc dang mang thai hay nếu có thai trong khi đang điếu trị, bệnh nhân
nên được biết vế ngưy cơ cho đứa trẻ chưa sinh ra và nên được theo dõi cấn thận. Nến
xem xét khả nãng tư vắn về di truyền.
Phụ nữ cho con bú
Chưa rõ bendamustin có đi qua sữa mẹ hay không, vì thể chống chỉ định Ribomustin khi
đang cho con bú (xem Chống chỉ định). Phải ngùng cho con bú trong quả trinh đìếu trị
vởi Ribomustin.
Khả nãng sinh sản
PI_Rỉbomustin_DE_/Pl Dec 2014_v1 41’1 2
|| I.mvì.xápu
—…*1
Nam giới được điếu trị với bendamustin nên được khuyên không có con trong khi điếu trị
và 6 thảng sau khi kết thúc điếu trị. Nên tư vẳn bảo quản tinh trùng trước điếu trị bới vi
có thể xảy ra vô sinh không phục hồi khi điếu trị với Ribomustin.
ẢNH HƯỞNG TRÊN KHẢ NĂNG LÁI XE VÀ VẶN HÀNH MÁY MÓC
Chưa tiến hảnh các nghiến cứu về ảnh hưởng của thuốc trên khả năng lái xe và vận hảnh
máy móc. Tuy nhiên, mất điếu hờa vận động, bệnh lý thằn kinh ngoại vi và ngủ gả đă
được báo cảo khi điếu trị với Ribomustin (xem Tác dụng không mong muốn). Nên hướng
dẫn bệnh nhân trảnh những công việc mang tính nguy hiếm như lải xe và vận hảnh mảy
móc nếu họ có những triệu chứng nếu trên.
TÁC DỤNG KỊ-IÔNG MONG MU_óN
Cảc phản ứng bât lợi thường gặp nhât khi sử dụng bendamustin hydrochlorid là phản ứng
bất lợi vê huyết học (giảm bạch cầu, giảm tiếu cẩu), độc tính trên da (phản ứng dị ứng),
triệu chứng toản thân (sốt), triệu chứng đường tiêu hóa (buồn nôn, nôn).
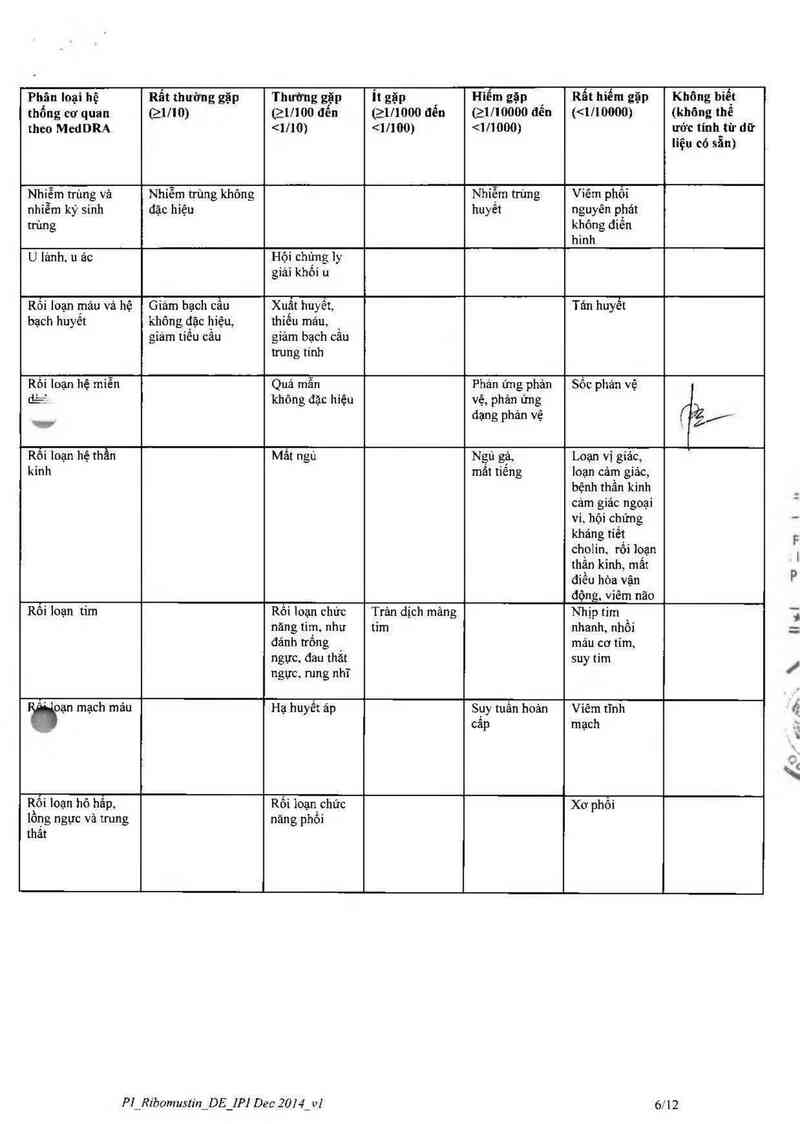
Bâng dưới đây cung câp dữ liệu thu được từ cảc thử nghiệm lâm sảng với bendamustin
hydrochlorid.
Pl_Ribomuszin_DE_ỉPl Dec 2014_v1 5112
—4->7 \in…
|
`
`
Phân loại hệ Rẩt thường gặp Thường gặp it gặp Hỉễm gặp Rất hiếm gặp Không biết
thống cơ quan (21l10) czmoo đến (21/1000 đến emoooo đển (<1710000) (không thế
theo MedeA <…m <1/100) <111000) ước tính từ dữ
liệu có sẵn)
Nhiễm trùng vả Nhiễm trùng không Nhiễm trùng Viêm phôi
nhiễm ký sinh đặc hiệu huyết nguyên phảt
trùng không điển
hình
U lảnh, u ảc Hội chùng ly
giải khối u
Rỏi loạn mẽ… và hệ Giảm bạch câu Xuất huyết, Tán huyết
bạch huyết không đặc hiệu, thiếu máu,
giám tiếu cầu giảm bạch cầu
trung tinh
Rối loạn hệ miễn Quá mẫn Phản ứng phản Sốc phán vệ
Ẻ khỏng đặc hiệu vệ, phản ứng
_ dạng phan vẹ C ẳ/
Rôi loạn hệ thẩn Mắt ngủ Ngủ gạ, Loạn vị giác,
kinh mât tiẽng loạn cảm giảc,
bệnh thần kinh
cám giác ngoại
vi, hội chứng
kháng tiết
cholin, rối loạn
thân kinh, mắt
điếu hòa vận
động, viếm não
Rối loạn tim Rối loạn chưc Trản dịch mảng Nhịp tim
nảng tim. như tim nhanh, nhôi
đánh trông J máu cơ tím,
ngực, đau thãt suy tim
ngực. rung nhĩ
Wạn mạch mảu Hạ huyết áp Sụy tuần hoản Viêm tĩnh
_ _ câp mạch
Rối loạn hô hâp, Rối ioạn chức Xơ phôi
lổng ngực và trung
thât
nảng phối
Pl_Ribom ustin_DE_lPl Dec 2014_ v]
112
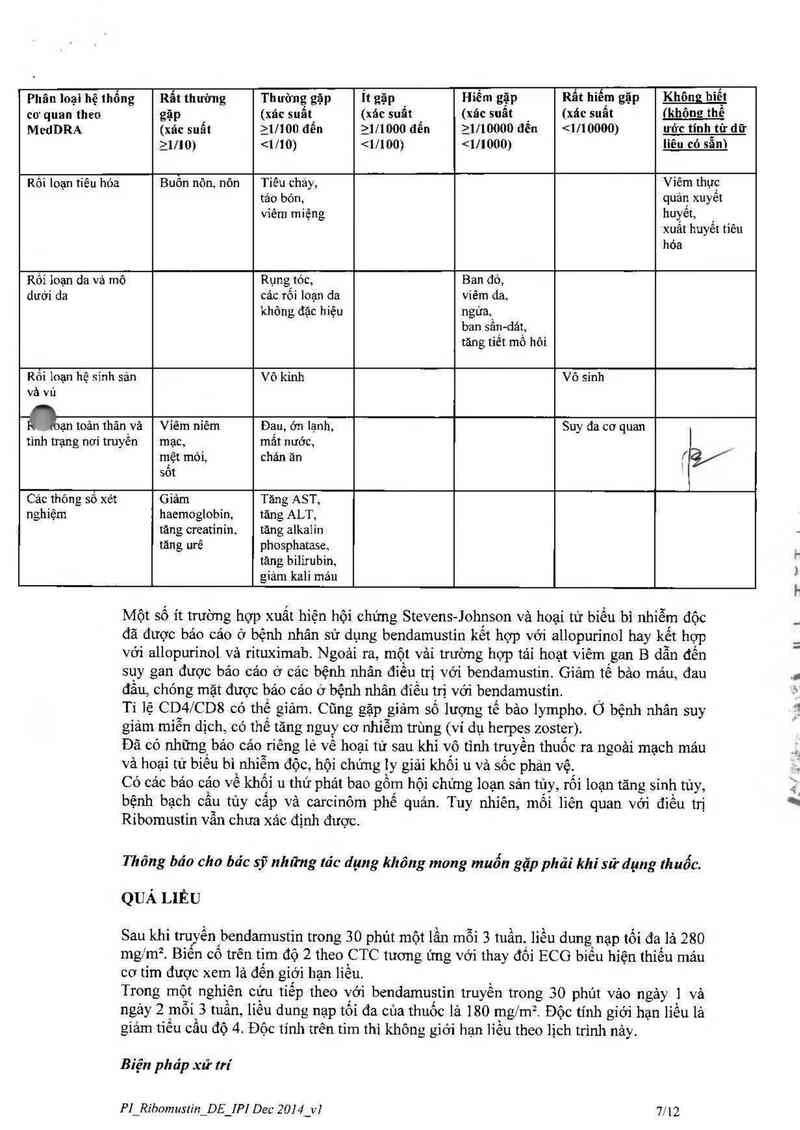
Phân loại hệ thổng Rat thường Thường gặp Ít gặp _ Hiếm gặp Rất hiếm gặp ủfflLềj
cơ quan theo gặp (xác suãt (xác suât ’ (xác suât _ (xác suât (k_họ_tg_th_e
MedDRA (xác suất 21l100 đến >1/1000 đên 21l10000 đên <1/10000) ước tínhgtứ dữ
21110) <1/10) <1/100) <111000) _l_Ỉ_Ễ_IJ_ỆS_ỄỊIJ
Rối Ioạn tiêu hóa Buôn nỏn, nôn Tiếu chảy, Viếm thực
táo bón, quan xuyet
viêm miệng huyêt, _
xuảt huyết tiếu
hỏa
Rôi ioạn da và mô Rụngtóc, Ban đỏ,
dưới da các rôi loạn da viêm da,
không đặc hiệu ngừa,
ban sân-dát,
tãng tiết mô hỏi
Rối loạn hệ sinh sản ve kinh Vô sinh
và vú
ủạn toản thân vả Viêm niêm Đạn, ớn lạnh, Suy đa cơ quan
tình trạng nơi truyền mạc, mât nước,
mệt mòi, chán ản f V
sôt
Cảo thỏng sô xét Giảm Tăng AST,
nghiệm haemoglobin, tăng ALT,
tăng creatinin, tăng alkalin
tăng ưrế phosphatase,
tăng bilirubin,
giảm kali mảu
Một số ít trường hợp xuất hiện hội chứng Stevens—Johnson vả hoại tử biếu bì nhiễm độc
đã được bảo cáo ở bệnh nhân sử dụng bendamustin kết hợp với allopurinol hay kết hợp
với allopun'nol vả rituximab. Ngoài ra, một vải trường hợp tái hoạt viêm gan B dẫn đến
suy gan được báo cảo ở các bệnh nhân điếu trị với bendamustin Giảm tế bảo mảu, đau
đẳu, chon g mặt được bảo cảo ở bệnh nhân điếu trị với bendamustin.
Tỉ lệ CD4/CD8 có thế giảm. Cũng gập giảm số lượng tế bảo lympho. Ở bệnh nhân suy
giảm miễn dịch, có thể tăng nguy cơ nhiễm trùng (ví dụ herpes zoster).
Đã có những báo cảo riêng lẻ vế hoại từ sau khi vô tình truyền thuốc ra ngoải mạch mảu
vả hoại từ biến bì nhiễm độc, hội chủng ly giải khối u và sôc phản vệ.
Có các bảo cáo về khối u thứ phảt bao gôm hội chứng loạn sản tủy, rối loạn tăng sinh tủy,
bệnh bạch cầu tủy cấp và ca…rcinôm phế quản. Tuy nhiên, môi liên quan với điếu trị
Ribomustin vẫn chưa xác định được.
Thông báo cho bác sỹ những ta'c dụng không mong muốn gặp phải khi sử dụng lhuốc.
QUÁ LIỀU
Sau khi tru fền bendamustin trong 30 phút một lần mỗi 3 tuần. liếu dung nạp tối đa lả 280
mglm² Biên cố trên tim độ 2 theo CTC tương ứng với thay đối ECG biếu hiện thiếu mảu
cơ tim được xem lả đến gíới hạn liếu.
Trong một nghiến cứu tiếp theo với bendamustin truyền trong 30 phút vảo ngảy 1 vả
ngảy 2 mỗi 3 tuần, lỉếu dung nạp tối đa cùa thuốc lá 180 mglm². Độc tính giới hạn liếu lả
giảm tiều cầu độ 4. Độc tinh trên tim thì không giới hạn liếu theo lịch trinh nảy.
Biện pháp xử trí
PI_Ribomustin_DE_lPl Dec 2014_v1 7112
Không có chất đối khảng đặc hiệu. Có thể thực hìện ghép tùy xương và truyền các chế
phẳm mảu (tiều cầu, hồng cầu lắng) hoặc sử dụng các yêu tố tăng trưởng tạo huyết như lá
những biện pháp xử trí hiệu quả để kỉếm soát tác dụng phụ vế huyết học. Bendamustin
hydrochlorid vả cảc chẳt chuyến hỏa bị thẩm tách vởi mức độ nhỏ
ĐẶC TÍNH DƯỢC LỰC HỌC
Nhóm dược lý điếu trị: thuốc chống ung thư, nhóm alkyl, mã ATC: LOIAAO9
Bendamustin lá thuốc nhóm alkyl chống khối u với hơạt tính độc đảo ở chỗ có chửa vòng
benzimidazol giống purin Tảc động chống ung thư vả gây độc tế bảo cùa bendamustin
chủ yếu dựa trên sự găn kết chéo của các sợi DNA đơn và kẻp bằng sự alkyl hóa Kết quả
là chửc năng nhân đôi của DNA, tồng hợp vả sừa chữa DNA bị hỏng Bendamustin có
hoạt tính chống lại cả hai loại tế bảo: tế bảo đang phân chia vả tế bảo khỏng hơạt động.
Cơ chế hoạt động chính xảo cùa bendamustín vẫn còn chưa rõ
Tảc dụng chống khối u của bendamustin hydrochlorid được chửng minh trong một số
nghiên cứu ỉn vitro trên nhìếu dòng tế bảo khối u khác nhau 0 người (ung thư vú, ung thư
phối tế bảo nhỏ và không tế bảo nhỏ, carcinôm buồng trứng và các bệnh bạch câu khác
nhau) và in-vivo trên nhỉếu kiểu khối bị thực nghiệm khảc nhau có nguồn gốc từ chuột
nhắt, chuột cống và người (ung thư hắc tố, ung thư vú, ung thư mô mếm, u lympho, bệnh
bạch cầu và ung thư phối tế bảo nhỏ).
Bendamustin hydrochlorid cho thấy hoạt tính trên những dòng tế bâo khối u ở người khác
vởi những thuốc nhóm alkyl khảc. Hoạt chất của thuốc cho thấy không có hay có rất ít để
khảng chéo với các dòng tế bảo khối u ở người với cảc cơ chế để khảng khác nhau ít nhắt
một phần do sự tương tảo với DNA tương đổi bến vững. Hơn nữa, các nghiên cứu lâm
sảng cho thấy không có sự kháng chéo hoản toản cùa bendamustin với anthracyclin, các
thuốc nhóm alkyl hay rituximab. Tuy nhiên, số bệnh nhân được đánh giá còn ít.
Bệnh bạch cầu lympho mạn (Chroníc Lymphocytic Leukemía - CLL)
Chi định dùng cho CLL được hỗ trợ bởi một nghiên cứu nhãn mớ, đơn lẻ so sánh
bẹndamustin vả chlorambucil Một nghỉên cứu đa trung tâm, ngẫu nhiên, tìến cứu bao
gổm 319 bệnh nhân CLL chưa điếu trị trước đó, giai đoạn B hay C theo Bỉnet vả có chỉ
định điếu trị. Điều trị bước một với bendamustin hydrochlorid 100 mg/m² truyền tĩnh
mạch vảo ngảy ] vả ngảy 2 (BEN) được so sánh với chlorambucil 0,8 mg/kg vảo ngảy ]
vả ngảy 15 (CLB) trong 6 chu kỳ cho cả hai nhóm Bệnh nhân dùng allopurinol với mục
đích phòng ngừa hội chứng ly giải khối u.
Bệnh nhân đuợc điếu trị BEN có trung vị sống còn không trỉến tríến bệnh dải hơn một
cách có ý nghĩa so với điếu trị CLB (21,5 tháng so với 8, 3 thảng, p < 0,000] trong theo
dõi gần nhất) Sống còn toản bộ không khác biệt có ý nghĩa thống kê (trung vị không đạt
được). Trung vị thời gian đáp ứng là 19 tháng với BEN so với 6 thảng với CLB (p <
0 ,.0001) Đánh giá tính an toản trên cả hai nhóm điếu trị khỏng thẳy bất kỳ phản ửng bắt
lợi nảo xét về bản chắt vả vế tần suất. 34% bệnh nhân vởí BEN được giảm liếu. Ngừng
điều trị vởỉ BEN ở 3, 9% bệnh nhân do phản ứng dị ứng
U lympho khõng Hodgkin diễn tỉến chậm (Indolent Non-Hodgkỉn ’s Lymphoma-
iNHL)
Chỉ định cho u lympho không Hodgkin diễn tiến chậm (iNHL) dựa trên hai thử nghiệm
pha II không có đôi chưng.
Trong một nghiên cứu mâu chốt, tiền cứu đa trung tâm, nhãn mờ, trên 100 bệnh nhản
iNHL tế bảo B khảng trị với rituximab đơn trị hoặc phối họp đã được đơn trị liệu với
BEN. Bệnh nhân đã nhận trung vị 3 đợt hóa trị hay thuốc sinh học trưởc đó. Trung vị số
đợt điếu trị có rítuximab trước đó là 2 Bệnh nhân không đáp ứng hay tiển tríên bệnh
trong vòng 6 thảng sau điếu trị rituximab. Liều cùa BEN lả 120 mg/m² truyền tĩnh mạch
vảo ngảy ] Vả ngảy 2 trong tối thiếu 6 chu kỳ. Thời gian đìều trị phụ thuộc vảo đáp ứng
(kế hoạch lả 6 chu kỳ). Tỉ lệ đảp ứng toản bộ lả 75% bao gồm 17% đảp ửng hoản toản
PI_Ribomustin_DE_lPl Dec 2014_v1 8sz 2
pl""'ff ] ~—…
\
\\
(đảp ứng hoản toản vả dảp ửng hoản toản không xảc định) và 58% đáp ứng một phận,
được đảnh giả bởi một úy ban xem xét độc lập. Trung vị thời gian đảp ứng là 40 tuân.
Nhìn chung BEN được dung nạp tốt khi sử dụng theo liếu và lịch trình nảy.
Chỉ định nảy còn được hỗ trợ hơn nữa bởi một nghiên cứu mở, đa trung tâm, tiến cứu
khảc trên 77 bệnh nhân. Dân số bệnh nhân đa dạng hơn bao gồm: U lympho không
Hodgkin (NHL — non- -Hodgkin Lymphoma) tế bảo B diễn tiến chậm hoặc bị biến đổi
kháng rituximab đơn trị hay phối hợp. Bệnh nhân không đáp ứng hay tiến triến bệnh
trong vòng 6 thảng hay có phản ứng không thuận lợi với điều trị rituximab trước đó.
Bệnh nhân đã nhận trung vị 3 đợt điều trị trước đó bằng hóa trị hay bằng sinh học Trung
vị số đợt điều trị trước dó có rituximab là 2. Tỉ lệ đảp ứng toản bộ là 76% với trung vị
thời gian đảp ứng lả 5 tháng (29 tuần [khoảng tin cậy 95%: 22,1; 43,1]).
Bendamustin kết hợp với rituximab (BR) được nghiên cứu trong một thử nghiệm có tựa
đề “Một nghiên cứu đa trung tâm pha Il dế khảo sát tính an toản vả tảc dụng của SDX-
105 (Bendamustin) khi kểt hợp với Rituximab ở bệnh nhân NHL thế diễn tiến chậm hay
tế bảo mantle tái phát”. Bệnh nhân dùng một liếu rituximab 375 mg/m2 vảo thời điếm 7
ngảy trưởc khi bắt đầu chu kỳ 28 ngảy đẩu tiên của bendamustin vả rituximab Tiếp theo,
dùng rituximab liếu đơn 375 2mg/m vảo ngảy đầu tiên cùa ] chu kỳ, sau đó dùng
bendamustin với liếu 90 mg/m2 /ngảy vảo ngảy thứ hai và thứ ba của chu kỳ. Kế hoạch
điếu trị là 4 chu kỳ 28 ngảy. Có 67 bệnh nhân tham gia vảo thử nghiệm và 66 trường hợp
nhận ít nhất một liếu bendamustin vả rituximab (BR) Kết quả nghiên cứu nảy cho thấy
diều trị phối hợp bendamustin vả rituximab hiệu quả ở bệnh nhân NHL thế diễn tiến
chậm hay NHL tế bảo mantle tái phát vởi tỉ lệ đảp ứng toản bộ 92% và đáp ửng hoản toản
41%. Đảp ứng đạt được bền vững với trung vị thời gian đáp ứng là 91 tuần vả trung vị
sống còn không tiến triến bệnh 100 tuần. Một tỉ lệ cao đảp ứng bến vững được quan sát
thấy ở cả hai nhóm bệnh nhân: nhóm được điều trị trước đó với rituximab và nhóm kháng
trị alkyl gần đây nhất.
Đa u tủy
Một nghiên cứu mở, ngẫu nhiên, đa trung tâm, tiến cứu gổm 131 bệnh nhân đa u tùy tiến
xa (giai đoạn II tỉến triên hay giai đoạn 111 theo phân loại Durie— —.Salmon) Điếu trị bước
một với bendamustin hydrochlorid phối hợp với prednison (BP) duợc so sảnh với điếu trị
bằng melphalan vả prednison (MP). Đối tượng đưa vảo thử nghiệm không đủ tiêu chuẩn
đếghép tủy cũng không có bệnh lý đặc biệt đi kèm. Liều bendamustin hydrochlorid ISO
mg/m² truyền tĩnh mạch vảo ngảy ] vả ngảy 2 hoặc melphalan 15 mglm² tiêm tĩnh mạch
vảo ngảy 1, và đếu được phối hợp với prednison Thời gian đỉếu trị phụ thuộc vảo đảp
ứng điếu trị; trung bình 6, 8 chu kỳ ở nhóm BP và 8 7 chu kỳ ở nhóm MP.
Bệnh nhân được điếu trị vởi BP có trung vị sống còn không tiến triến dải hơn so với MP
(15 thảng [khoảng tin cậy 95% 12-21] so với 12 thảng [khoảng tin cậy 95% 10-14]
(p= —0 ,.0566) Trung vị thới gian thất bại điếu trị là 14 tháng ơ nhóm BP và 9 thảng ơ nhóm
MP. Thời gian lui bệnh là 18 tháng ở nhóm BP và 12 thảng ở nhóm MP. Sự khác biệt về
sống còn toản bộ thi không có ý nghĩa thống kê (35 tháng ở nhóm BP so với 33 tháng ở
nhóm MP). Tính dung nạp ở cả hai nhóm điêu trị phù hợp với dữ liệu về tính an toản đã
được biết của các thuốc điều trị tương ứng vởi sự giảm liều thuốc nhiều hơn đảng kế ở
nhóm BP.
ĐẶC TỈNH DƯỢC ĐỘNG HỌC
Phân bố
Sau khi truyền tĩnh mạch 30 phủt, thể tich phân bố ở trung tâm là 19,3 L. Trong điều kiện
ốn định sau khi tiêm tĩnh mạch nhanh thể tích phân bố iả 15, 8- 20, 5 L.
Trên 95% hoạt chất được gắn kết với cảc protein huyết tương (chủ yểu lả albumin).
PI_Ribomuslin_DE_lPl Dec 2014_v1 9a“ ] 2
Chuyển hóa
Đường thải trừ chính của bendamustin lả thùy phân thảnh monohydroxy- vả dihydroxy-
bendamustin Sự tạo thảnh N-desmcthyl—bendamustin vả gamma-hydroxy-benđamustin
qua chuyển hóa ở gan nhờ' tsoenzym cytochrom P450 (CYP) 1A2 Đương chuyến hóa
chính khảo của bendamustin nhờ găn kết với glutathion
In- -vitro, bendamustỉn không ức chế CYP 1A2, CYP 2C9/10, CYP 2D6, CYP 2El vả
CYP 3A4.
Thải trừ
Độ thanh thải toản bộ trung bình sau truyền tĩnh mạch 30 phủt vói líếu 120 mg/rn2 diện
tích bề mặt cơ thể cho ]2 đối tượng thử nghiệm là 639,4 mL/phút Khoảng 20% liếu sử
dụng tìm thấy trong nước tiếu 24 giờ. Lượng bải tiết trong nước tiếu theo thứ tự là
monohydroxy-benđamustin > bendamustin > dihydroxy-benđamustin > chất chuyến hóa
oxy hóa > N-desmethyl bendamustin. Trong mật, các sản phâm chuyên hóa chỉnh có tính
phân cục bị thải trừ.
Say gan
Ở các bệnh nhân có 30- 70% gan bị phá hủy do khối u vả suy gan nhẹ (bilirubin huyết
thanh < 1,2 mg/dL), đặc tính dược động học không thay đối. Không có sự khảo bỉệt có ý
nghĩa giữa bệnh nhân nảy với bệnh nhân có chức năng gan và thận bình thường về Cmax,
t…, AUC, th, thế tỉch phân bố và độ thanh thải. AUC và độ thanh thải toản bộ trên cơ
thể cùa bendamustin ti lệ nghịch với bilirubin huyết thanh.
Suy thận
Ở các bệnh nhân có độ thanh thái creatinin > 10 mL/phút, kể cả cảc bệnh nhân phải lọc
mảu, không có sự khảo biệt có ý nghĩa so với bệnh nhân có chức năng gan và thận bình
thướng xét về c…, t…, AUC, W, thể tích phân bố vả thanh thải.
Bệnh nhãn cao tuổi
Bệnh nhân đên 84 tuôi cũng được bao gồm trong cảc nghiên cứu dược động học. Tuổi
cao không ảnh hướng đên dược động học cùa bendamustin.
THÔNG TIN TIỀN LÂM SÀNG
Các phản ứng bất lợi không quan sát thắy trên cảc nghiên cứu lâm sảng, nhưng đã gặp ở
động vật với mức phơi nhiễm tương tự như mức phơi nhiễm trên lâm sảng và có khả
năng liến quan đến việc sử dụng trên lâm sảng như sau:
Cảo nghiến oứu mõ học ở chở cho thấy xung huyết đại thể nhin thấy được ở niêm mạc và
xuất huyết đưòng tiêu hóa. Nghiên cứu vi thể qua kính hiến vi cho thấy những thay đối
rộng của mô bạch huyết thế hiện sự ức chế míễn dịch vả các thay đổi cùa ông thận và tinh
hoản, cũng như oảo thay đối hoại tứ, teo nhỏ cùa biếu mô tiến liệt tuyến
Các nghiên cứu ở động vật cho thấy bendamustin lả tảo nhân gây độc thai và quái thai.
Bendamustin gây ra sự khác thường của nhiễm sắc thế và là tác nhân gây đột biến gen in-
vívo cũng như ín—vivo. Trong nghỉên cứu dải hạn ở ohuột cái, bendamustin lả tảo nhân
sinh ung thư.
TÍNH TƯỚNG KY
Thuốc nảv không nên trộn với cảc thuốc khảo ngoại trừ những thuốc được đề cập trong
phần Hướng dẫn sử dụng vả xử lý.
HẠN DÙNG
PI_Ribomustỉn_DE_lPl Dec 2014_v1 10:"12
iạK
\
up
`.
\\n\
J.?y x…»l
36 thảng từ ngảy sản xuất.
Không dùng thuốc đã quá hạn sử dụng ghi trên nhãn.
Bột đông khô nên được hoản nguyên ngay sau khi mở lọ thuốc.
Thuộc hoản nguyên cân được pha loãng ngay với dung dịch NaCl 0,9%.
Dung dịch truyền tĩnh mạch
Sau khi hoản nguyên và pha loãng, thuốc ổn định về hóa học và vật lý trong 3 ,5 giờ ở
25°C/ 60%RH vả trong 2 ngảy ở 2°C đến 8°C trong túi bằng polyethylen.
Từ quan điếm về vi sỉnh học, dung dịch nảy nên được sử dụng ngay tức thì Nếu không
được sử dụng ngay, người dùng chịu trảch nhiệm về thời gian và điếu kiện bảo quản
trước khi sử dụng.
ĐIỀU KIỆN BẢO QUẢN
Giữ thuốc trong hộp đế trảnh ánh sảng.
Bảo quản ở nhiệt độ dưới 30°C .
Để bảo quản thuốc đã hoản nguyên hay pha loãng, xem Hạn dùng.
Đế xa tầm tay trẻ em.
QUY CÁCH ĐÓNG GÓI
Bendamustin được đóng gói trong lọ thủy tinh 26 mL hoặc 60 mL mảu nâu loại I vởi nút
lọ bằng cao su và một năp lọ bằng nhôm, dễ mở.
Lọ 26 mL chứa 25 mg bendamustỉn hydrochlorid
Lọ 60 mL chứa 100 mg bendamustin hydrochlorid.
Hộp 1 lọ.
HƯỚNG DÃN SỬ DỤNG VÀ XỬ LÝ
Khi thao tảo Ribomustin, nến trảnh hít vảo hay tiế xúc với da vả niêm mạc (mang găng
tay và quần ảo bảo hộ!) Phần cơ thể bị nhiễm thuôo nên được rửa cẩn thận bằng nước và
xả phòng, nên rứa mắt vởi nước muối sinh lý. Khuyến cảo nếu có thể nên pha chế trên
những bản lảm việc an toản đặc biệt không thấm nước, nền hấp thu hoản toản. Phụ nữ có
thai tránh không thao tảo xử lý các chất kìm hãm tế bảo
Bột pha dung dịch đậm đặc để pha dung dịch truyền tĩnh mạch phải dược hoản nguyên
với nước pha tiêm, pha loãng với dung dịch pha tiêm NaCl 9 mg/mL (0,9%), sau đó sử
dụng bằng cảch truyền tĩnh mạch. Nên sử dụng kỹ thuật vô trùng.
1. Hoản nguyên thuốc
Hoản nguyên mỗi lọ Ribomustin chứa 25 mg bendamustin hydrochlorid trong 10 mL
nước pha tiêm vả lắc.
Hoản nguyên mỗi lọ Ribomustin chứa 100 mg bendamustin hydrochlorid trong 40 mL
nước pha tiêm vả lẳc.
Mỗi mL dung dịch dã hoản nguyên chứa 2,5 mg bendamustin hydrochlorid và là dung
dịch không mảu, trong suốt.
2. Pha Ioãng
Ngay khi thu được dung dịch trong suốt (thường sau 5- 10 phút) pha loãng ngay toản bộ
liếu khuyến cảo cùa Ribomustin với dung dịch NaCI 0,9% để được thế tich cuối cùng
khoảng 500 mL.
Ribomustin phải được pha loãng với dung dịch NaCl 0,9% và không được phép pha với
bất kỳ dung dịch tiêm truyền nảo khảo.
PI_Ribomustỉn_DE_/PI Dec 20l4_v1 ] i 1 1 2
\\“ì
3. Cách dùng ' `
Dung địch pha chế được trưyên tĩnh mạch trong 30-60 phút.
Lọ thuôo chỉ sử dụng một lân duy nhât.
HỰỚNG DÃhỊ HỦY THUỐC
Bât cứ chế phâm không sử dụng hoặc thừa nên được hủy bỏ theo những qui định của
nước sở tại.
Sản xuất tại: Oncotec Pharma Produktion GmbH
Am Pharmapark, Dessau, Roblau, 06861, Đức
Dản nhãn, đóng gói thứ cấp và xuất xưởng lô thảnh phấm tại:
Janssen Pharmaoeutica NV
Tumhoutseweg 30, Beerse, B-2340, Bỉ
Công ty đăng ký: JANSSEN-CILAG Ltd., Thải Lan
Mọi câu hỏi/Bảo cảo tác dụng ngoại ỷ] Than phiến chẩt lượng sản phẩm xin liên bệ:
VPĐD Janssen-Cilag Ltd., TP Hồ Chí Minh.
ĐT: +84 8 38214828
E-mail: iacvndruesafetyífflitsini.com
Phiên bản: IP] Dec 2014, số 2
PI_Ribomutịn_DE_lPl Dec 2014_v1
Ngảy sứa đôi: 8/5/2015
TUQ. CỤC TRUỘNG
P.TRUỞNG PHONG
/ịỷuắyẫn Jẳty Jf'ẫìng
PI_Ribomustin_DE_lPl Dec 2014_v1 12/12
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng