









1…«1106ĩ
iu
/ ẫ Ý/ớJ
LABELLING
ARTWORK OF SECONDARY PACKAGING OF REMINYL PR 16MG:
|
Bộ Y TẾ
cục QUẦN LÝ DƯỢC
A
DUYỆT
~
ĐA PHE
_
sảẵ . ……ẵ ẵằ
S ẵỄEE . ›: ẫỄ :3…ẵ. sư
25. . ẫfi 8ẫ . sẵị … ẵẵ
ễ…ầ u.›. ẵ ỉẵẫs. 2. SỄỄỂ
uỀ u .oẵỀ uảEỄ. … Ễ
8% S. % ….Ễ &. .ễ. ẵẵ
86.9: 3 8 …ẫễE. …n 3m
Ềc ẵỀEỄ ẵm
2 .… ẫJỀEÊuSw
Êm...
.22 …nẵẵzbễfflíỉn S.oeỄỉúEonì.xmz.xmoễm
Ển 0 «S :(.Sứ 010
Ổ .0mẵỏ :!0 dn
ỂEỔ cắm 5! ỂỀn Gỗ Ễ x220
› .25 850 .ĩĩoã … aưỗ 8:
ãỄa›ẳcỂẵdũỉtfỉboỗuẵ.ểẫ ỉ
.oỄỏ ,ẵ .on ễẫ ,›z Ễm :ỈnỈq
.sãẵẵẫẵsễỉEầnaỉ Eỉ?ễx
ã.ễuẵ› Ễa
52 .«5, ẵ u!9ễ ỗồ
ẫnũă›Ễ«ỉEỉ›ũẻ ` CÙmmCÙ—
› …...Ễx '
ẳẩ ã Eaỉ Ẻề e. DỄ:
ẵễ Ềe Ề
Eun 5… uẵ E. Ễsẵ a›cẵzu 9a5 .88. 68 .cễEu
ỦSỀSẾẾỂ?EỄÌ .ẵaot
ẫẽiẳẻẵổ…ẵẵ ỤẺ b` .Ề.EẺQk a
l.ỄSzẳãuuầéicuoosqfiẳẵẵnim
oẫoĩ: ẫfiẵùaẫoễzoxoẵ
u…onasuẩoẹãfoẵơâa
..Ê :lnin
Ễ ă«ẳ u! uEẺ Ể. Ểẩuũ
ềễ ẵỀỄ
:… «E. ›5. :E !… wo
oễẵ..ẵoỉẵeềẵẳ.
8. ! u..ễ!mF..
apszhs oraln
Reminyl16 mg 280m1caplulal
16
PR… 968 82… E: 8
Ễuễu B 53… B …8 aẵx
:…Qẳ .ẵ ỉ ẵễõ …… v…ạ
SỄỄcEẵ ..….B 8…
ẩẵềẽ
ễỂ ầẳ`ẵẵềẫẵẵễ
nm ỄỂ ẵ…Ể
{
E:……mz \v
Y
W
Y
g
M
……
…
u…
…
o
yI_PR 16rng_v3
SP_Remin
LABELLING
ARTWORK OF PRIMARY PACKAGING OF REMINYL PR IGMG
P
inEM1NYL° Pmtofaed Retaase Caian 16 mg
( galamamine (as nyửobromide
mmn ! ị
REMINYL' Pmlomcd Relem 0mb 161m
gatantamne (u hyủobrom de)
` Janssen [
RĐAINVL' Pmlonpd FU le 16
' galamamine (as hyỄỂbỦe) m
pnssen7
Januun P…I ulN. Lsnmnenn SG om 54 250
BI ldm mmm, mit wma: hutừnuôc wù nnau W:
đi 1! JIIIM Phumnuulnl NV. Tum… 30,
n…u sm. BI Đemnmg mge genw cbvltlúiảp.
ut… nơiơmvi :_ult mong 10 man» uolm w JANSEN
CJLM !. PA. -Y
sư_…u_Pa tm_va
RffllNYL’ W Release 11: 16
galamamine (as hydmbcrễnpỀe) mg
iMSEFI ! \
REMINYL' Pmlnngod Reieue Clpwle16 mg(
galantam'na (as hyứobrofntde)
mnsscn [
' gaimtamine (as hydrobromớe) m,
ị |BnM’ÌT
'— …1m 1 ……Jvm (
\ /
Foil side
`
PP_Reminyl_PR 16 mg_v3
su…umumn dcnamiiocgmpmmmemu () †. -
'
s:
\
z
»
d" .
@"
Dim
8… -C)
Dom
( __»…— … ĩ
Luu
Mon <-
Lun
Tablet side
REMINYL®
THÀNH PHÀN sò LƯỢNG VÀ CHẤT LƯỢNG
tương đượng với 8 mg (hoặc 16 mg) galantamin.
DẠNG BÀO CHẾ
Viên nang gỉải phóng kéo dâi dùng đường uổng
- Viên nang 8 mg galantamin có mảu trăng mờ, vỏ gelatin cứng cỡ số 4 có in chữ “G 8”, chứa các hạt
mảu trắng đểu trăng nhạt.
- Viên nang 16 mg galantamin có mảu hổng mờ, vò gelatin cứng cỡ số 2 có in chữ “616”, chứa các
hạt mảu trắng đến trắng nhạt
ĐẶC TỈNH LÂM SÀNG
Chỉ định điều trị
REMINYL được chỉ định điều trị sa sủt trí tuệ do bệnh Alzheimer mức độ nhẹ đến vừa.
Liều dùng và cách sử dụng /
Người lởn
Nên uông viến nang REMINYL giải phóng kéo dải ngảy một lần vảo buổi sáng, tốt nhất là trong bữa
ãn. Liều khởi đầu khuyến cảo là 8 mg/ngảy. _
Bệnh nhân đang được điều trị với REMINYL giải phóng tức thì (viến nén hoặc hỗn dịch) có thế
chuyến sang dùng viên nang REMINYL giải phóng kéo dải bằng cách uống liếu cuôỉ cùng cùa
REMINYL giâi phóng tức thì vảo buổi tối và bắt đầu với liệu trình ngảy một lần với viên nang
REMINYL giải phóng kẻo dải vâo sảng kế tiếp. Khi chuyến từ REMINYL giải phóng tửc thì sang
viên nang REMỊNYL gíải phóng kéo dải thì tổng liều uông hảng ngảy nên như nhau.
Phải đảm bảo uống đủ nước trong quá trình điều trị.
Liều duy trì:
- Liều duy trì khởi đầu là 16 mg xl lẩn/ngây và bệnh nhân nên được duy trì vởi liều 16 mg/ngảy
trong ít nhất 4 tuần.
- Gia tăng đến liếu duy trì tối đa 24 mg x ] lần/ngây cần phải được cân nhắc sau khi đã có những
đảnh giá đúng đắn về lợi ích lâm sảng và độ dung nạp.
- Không có hiệu' ưng dội ngược sau khi ngưng điểu trị đột ngột (Ví dụ: chuẩn bị phẫu thuật)
T rẻ em
Không nên sử dụng REMINYL cho trẻ em. Chưa có dữ liệu về việc sử dụng REMINYL cho bệnh nhi.
qu gan và suy thận
Nông độ galantamin trong huyết tương có thể gia tăng ở những bệnh nhân bị suy chức năng gan hoặc
thận mức độ trung bình tởi nặng.
Ở những bệnh nhân bị suy chức năng gan mức độ trung binh, dựa vảo mô hình dược động học, nên
khới đầu với liền 8 mg cảch ngảy trong ít nhất 1 tuân, tốt nhất vảo buổi sáng. Sau đó, bệnh nhân nên
tiểp tục với 8 mg ngảy một lần trong ít nhất 4 tuần. Ở những bệnh nhân nảy, tổng liều mỗi ngảy không
nên vượt quá 16 mg.
Không nên sử dụng REMINYL cho những bệnh nhân bị suy chức nãng gan nặng.
Không cần chinh liều đối với những bệnh nhân có độ thanh thải Creatinin lớn hơn 9 mL/phủt.
Không nên sử dụng REMINYL cho những bệnh nhân suy thận nặng (độ thanh thải Creatinin dưới 9
mL/phủt) bởi vì chưa có đầy đủ dữ liệu.
PI_Reminyl_ PR 16mg_CCDS 20May2011_v3 1111
Điều trị đồng thời
Cần xem xét việc giảm liếu ở những bệnh nhân được điều trị bằng những thuốc ức chế CYP2D6 hoặc
CYP3A4 mạnh (xem phần Tương tác với những thuốc khác vả các dạng tương tác).
Chổng chỉ định
Không được sử dụng REMINYL cho những bệnh nhân đã được biết quá mẫn với galantamin
hydrobromid hoặc bất cứ tá dược nảo cùa thuốc.
Chú ý và thận trọng
REMINYL được chỉ định điểu trị sa sút trí tuệ do bệnh Alzheimer mức độ nhẹ đến vùa… Lợi ích
của REMINYL ở bệnh nhân sa sút trí tuệ cảc thể khảc hoặc cảc thể cùa suy giảm trí nhớ khác
chưa được chứng minh.
- Bệnh nhân bị bệnh Alzheimer bị sụt cân. Việc điếu trị cảc bệnh nhân nảy bắng những thuốc ức chế
men cholinestcrase, kể cả galantamin, đến có liên quan đến tình trạng sụt cân. Do đó cẩn phải theo
dõi thể trọng bệnh nhân trong quả ttinh điều trị.
- Cũng như những thuốc kích thích hệ cholinergic khảo, REMINYL cần thận trọng khi sử dụng
trong những trường hợp sau:
0 Tim mạch: Do tác dụng dược lý, các thuốc kích thích hệ cholinergic có thế có những tác động
của tăng trương lực thần kinh đối giao cảm lên nhịp tim (Ví dụ: Nhịp tim chậm), Điều nảy có
thể đặc biệt quan trọng đối với những bệnh nhân bị “Hội chứng suy nút xoang hoặc có cảc
dạng rối loạn dẫn truyền trên thất hoặc ở những người đang đồng thời sử dụng thuốc lảm giảm
nhịp tỉm đảng kế như digoxin và các thuốc ức chế thụ thể 13. Trong các nghiên cứu lâm sảng,
việc sử dụng REMINYL lá có liên quan tới ngất và hiếm khi có tinh ữạng nhịp tỉm rất chậm.
0 Tiêu hóa: Đối với những bệnh nhân có nguy cơ khởi phát bệnh lý loét đường tiêu hóa (V i dụ
như những bệnh nhân có tiến sứ bị loét hoặc cảc yếu tố thuận lợi để gây loét) bao gồm những
bệnh nhân đang sử dụng đồng thời các thuốc chống viêm non-steroidc (NSAIDS), thì cân phải
theo dõi chặt chẽ để tìm cảc triệu chứng. Tuy nhiên, cảc nghiên cứu lâm sâng cho thấy
REMINYL không lảm tăng tần suất loét và xuất huyết tiêu hóa (so với giả dược). Không nên
sử dụng REMINYL cho nhũng bệnh nhân có bệnh lý gây tắc nghẽn đường tiêu hóa hoặc
những bệnh nhân đang hối phục sau phẫu thuật đường tìêu hóa.
0 Thẩn kinh: Mặc dù cảc thuốc kích thích hệ cholinergic có khả nãng gây cảc cơn co giật, cơn co
giật cũng có thế là một biến hiện cùa bệnh Alzheỉmer.
0 Bệnh phối: Do những tác động kích thích hệ cholinergic, nên cảc thuốc nhóm nảy cần được sử
dụng thận trọng ở nhũng bệnh nhân có tiền sư hen phe quản nặng hoặc bệnh phổi tắc nghẽn.
o Tiết niệu-sinh dục: Không nên sử dụng REMINYL cho những bệnh nhân bị tắc nghẽn đường
bải niệu hoặc đang hổi phục sau phẫu thuật bảng quang.
An toản trên bệnh nhân bị suy giảm nhận thủc mức độ nhẹ (MCI)
REMINYL không được chỉ định cho những cá thể bị suy giảm nhận thức mức độ nhẹ (MCI), ví dụ
như, những người đã được chứng minh là sự suy giảm tn' nhớ biệt lập nặng hơn tuối và kiến thức của
họ, nhưng không thỏa mãn cảc tiêu chí của bệnh Alzheimer
Các đối tượng nghiên cứu thế MC] trong 2 nghiên cứu có kiếm chứng không thỏa mãn hai tiêu chí về
hiệu quả đầu tiến. Mặc dù tỷ lệ tử vong ở 2 nghiên cứu thấp, các trường hợp tử vong khảc đã được ghi
nhận đằu tiên ở các đối tượng ngân nhiên dùng gala.ntamin hơn placebo, nhung tỷ lệ các tảo dụng
ngoại ỷ nghiêm trọng là giông nhau giữa 2 nhóm điểu trị. Tử vong do rất nhiều nguyên nhân không dự
đoán được ở nhóm dân sô giả. Khi đưa thêm vảo dữ liệu thu được từ một nhóm bệnh nhân lớn hơn là
những người đã ngưng sử dụng trước khi kết thúc thời gian mù đôi, không thẩy bằng chứng về việc
tảng nguy cơ tử vong ở những đối tượng được điều trị với REMINYL trong thời gian nảy. Cảo đối
tượng ở nhóm giả dược ngưng việc điểu trị trước khi chết nhiều hơn ở nhóm galantamin có thế là
nguyên nhân dẫn đến sự khác biệt về tỷ lệ tử vong cùa cảc gbi nhận ban đầu.
Pl_Reminyi_ PR 16mg_CCDS 20May2011_v3 2/11
Cảo kết quả của nghiên cứu MCI rất khảc biệt trên các đối tượng quan sảt trong cảc nghiến cứu của
bệnh Alzheimer. Trong cảc nghiên cứu tổng hợp về bệnh Alzheimer (N=4614), tỷ lệ tử vong ở nhóm
giả dược có số lượng cao hơn ở nhóm REMINYL.
Tương tác với cảc thuốc khác và câc dạng tương tác khác
Các tương tác dược lực học
Do cơ chế tác dụng, không nên sử dụng đồng thời galantamin với cảc thuốc kích thích hệ cholinergic
khảc. Galantamin đối khảng với tảc dụng của cảc thuốc kháng cholinergic. Thông thường ở các thuốc
kích thích hệ cholinergic, tương tác dược lực học có thể xảy ra với các thuốc lảm giảm đáng kể nhịp
tim (Ví dụ Digoxin và các thuốc ức chế thụ thể 13). Galantamin, như một thuốc kích thích hệ
cholinergic, có thế tảo động mạnh lên sự dãn cơ kiều succinylcholine trong khi gây mê.
Các tương tác dược động học
Galantamin chuyến hóa qua nhiều con đường và được thải qua thận.
Bằng những nghiên cứu trong phòng thí nghiệm đã xảo định được 2 enzyme chủ yểu tham gia vảo quá
trình chuyền hóa cùa REMINYL lả CYP2D6 vả CYP3A4.
Sự hấp thu của galantamin không bị giảm khi sự bải tìết acid dịch vị bị ức chế.
Các thuốc khác ảnh hưởng lên chuyền hóa của galantamin.
Những thuốc ức chế mạnh men CYP2D6 vả CYP3A4 có thế lảm gia tăng phần diện tích dưới đường
cong (AUC) của galantamìn.
Nhiêu nghiên cứu về dược động đa liếu cho thấy khi được uống cùng với ketoconazol vả paroxetin thì
phần diện tich dưới đường cong cùa galantamin gia tăng theo thứ tự là 30% và 40%. Còn khi được
uỏng cùng với Erythromycin-loại thuoc ưc chê men CYP3A4 khảc— thì AUC của galantamin chỉ tăng
khoảng 10%. Phân tích trên nhóm dân số bị bệnh Alzheimer cho thấy rằng độ thanh thải cùa
galantamin giảm khoảng 25- 33% khi nó được uống chung với amitriptylin, fluoxetin, fiuvoxamin,
paroxetin vả quinidin, được biết là những thuốc ức chế men CYP2D6.
Vì vậy, trong giai đoạn khới đầu điều trị với các thuốc ức chế mạnh men CYP2D6 vả CYP3A4, bệnh
nhân có thể có cảc tảo dụng phụ cholinergic, nổi bật là buồn nôn vả nôn. Trong nhũng trường hợp như
vậy, cẩn dựa vảo khả năng dung nạp mả xem xét đến việc giảm 1iếu duy trì cùa galantamin. (Xem
Liều dùng và cách sử dụng).
Memantin, một đối khảng thụ thể N-methyl-D-aspartate (NMDA), ở liều 10 mg/ngảy trong 2 ngảy,
tiếp theo sau đó là liểu 10 mg, ngảy 2 lần trong 12 ngảy không thấy có tảo động trên dược động học
của galantamin 16 mg/ngảy tại giai đoạn ỏn định. /
Anh hưởng của Galantamin lên chuyền hóa của các thuốc khác \
Liều điều trị cùa galantamin (l2mg x 2 lằn/ngảy) không ảnh hưởng lên dược động học của digoxin vả
warfarin. Galantamin không ảnh hưởng đến tảo dụng kéo dải thời gian prọthrombin cùa warfan'n.
Cảc nghiên cứu trong phòng thí nghiệm cho thắy tiềm năng gây ức chế của galantamin đối với cảc
dạng chủ yếu của men cytochrome P450 ở người là rất thấp.
PHỤ NỮ có THAI, CHO CON BỦ
Phụ nữ có thai
Những nghiên cứu về sinh sản được tiến hảnh ở chuột mang thai với liều lên đến 16 mg/kg (gấp
khoản 25 lần liếu điều trị ở người) và ở thỏ mang thai với Iiếu lên đển 40 mglkg (gấp khoảng 63 lần
liều đieu trị ở người) đã không cho thấy bất kỳ bằng chứng nảo về tỉềm năng gây quái thai. Có ghi
nhận được sự gia tăng không có ý nghĩa thống kê về tần suât gây bất thường ở cảc xương nhỏ vói liều
16 mg/kg ơ chuột.
Chưa có nghiên cứu sử dụng REMINYL ở phụ nữ mang thai. REMINYL nên được sử dụng trong khi
mang thai chỉ khi nảo lợi ích mà nó mang lại cho bả mẹ quan trọng hơn nguy cơ đối với bảo thai.
Pi_Remnnyi_ PR 16mg_CCDS 20May2011_v3 3/11
Cho con bú
REMINYL hiện chưa được biết là có bâi tiết qua sữa mẹ hay không vả chưa có nghiến cứu nảo ở phụ
nữ đang cho con bú. Vì vậy, những phụ nữ đang uống REMINYL không nên cho con bú
Tác động trên khả năng lái xe vận hảnh mảy móc
Bệnh Alzheimer có thể gây giảm đần khả nãng lải xe và vận hảnh mảy móc Hơn nữa, giống như cảc
thuốc kích thích hệ cholinergic khảc, REMINYL có thể gây choáng váng và ngủ gả, tím là ảnh hưởng
đến khả năng 1ái xe và vận hảnh mảy móc, đặc biệt trong tuần khới đầu điếu trị đầu tiên.
Tác dụng ngoại ỷ
Dữ liệu nghiên cứu lâm sảng
Dữ liêu mù đôi — Phản ứng neoai 1? báo cáo ở tần suất (
Tính an toản của REMINYL được đánh giá trên 4457 bệnh nhân sa sút trí tuệ thế Alzheimer từ nhẹ
đến trung bình nặng, những người đã tham gia trong 7 nghiên cứu mù đôi, kiêm chứng giả dược.
Phản ửng ngoại ý bảo cáo ở tần suất 21% khi điều 111 vởi REMINYL - được trình bảy ở Bảng 1.
Bảng 1. Phản ứng ngoại ỷ bảo cảo ớ tẩn suất 21% khi điếu trị với REMINYL- ở
7 nghiên cứu mù đôi, đối chứng giả dược
REMINYL Giả được
Hệ thốnglcơ quan (n=2932) (n=1525)
Tác dụng ngoại ỷ % %
Rối loạn chuyến hóa và dinh dưỡng
Giảm thèm ăn 5,2 1,4
Biếng ăn 3,8 1,0
Rối ioạn tâm thần
Trâm cảm 4,2 2,9
Rối loạn hệ thần kinh trung ương
Choản váng / 8,9 4,6
Đau đẵi 1 / 7,6 5,4
Run ( 2,0 0,8
Ngât 1,8 0,7
Hôn mê 1,7 0,7
Buổn ngủ 1,7 0,8
Rối loạn tim mạch
Chậm nhip 1,2 0,3
Pi_Rern1nyl_ PR 16mg_CGDS 20May2011_v3 4111
Bảng 1. Phản' ưng ngoại ỷ bảo cáo ở tần suất >1% khi điều trị vởi REMINYL- ở
7 nghiên cứu mù đôi, đối chứng giả dược
REMINYL Giã dược
Hệ thốnglcơ quan (n=2932) (n=1525)
Tảo dụng ngoại ỷ % %
Rối loạn tiêu hóa
Buồn nôn 25,0 7,6
01 12,8 3,1
Tiếu chảy 9,0 6,3
Đau bụng 2,4 0,9
Đau vùng bụng trên 2,0 1,4
Khó tiêu 1,8 1,3
Khó chịu ở dạ dảy 1,6 0,6
Khó chịu vùng bụng 1,0 0,4
Rối loạn mô dưới da & vùng da
Tăng tiết mồ hôi 1,2 0,7
Rối loạn mô liên kết và cơ xương
Co thẳt cơ 1,5 oịg
Rối loạn chung và tình trạng cơ thể
Mệt mỏi ( 430 ỉẳ
Suy nhược ). /""2,3 ,
Không khóe Ẩ~ý/ 1,4 0,7
Các chỉ số khác \.
Giảm cân 5,1 1,4
Trong một nghiên cứu lâm sảng mù đôi, ngẫu nhiên có kiếm chứng, tính an toản của REMINYL dạng
viên nang giải phóng kéo dải, ngảy một lần có tần suất tương tự như REMINYL dạng viên nén
Buồn nôn vả ói là hai tảo dụng ngoại ỷ thường gặp nhất thường xảy ra trong thời gian điếu chỉnh liều,
kéo dải khoảng hơn 1 tuần trong hầu hết cảc trường hợp và đa sô bệnh nhân chỉ có một cơn. Kê toa
cảc thuốc chống nôn và đảm bảo uống đủ nước sẽ cải thiện tình hinh.
Phản ứng ngoai v— Dữ liêu nhãn mớ báo cáo với tần suất _21 %
Tính an toản cùa REMINYL được đánh giá trên 1454 bệnh nhân sa sủt trí tnệ thể Alzhcimer từ nhẹ
đển trung binh nặng, những người đã tham gia trong 5 nghiên cứu mở. Thông tin trinh bảy trong phần
nảy được lấy từ dữ liệu tổng hợp
Phản ímg ngoại ý bảo cảo ở tẩn suất >1% khi điếu trị với REMINYL- không được ttĩnh bảy 0 Bảng 1
bao gôm té ngã, với tần suất 6, 5% trong 5 nghiên cứu mớ
Dữ liêu mù đôi. nhãn mớ — Phản ứng neoai 13 báo cáo ở tấn suát <1%
Phản ứng ngoại ý bổ sung được bảo cảo ớ tẩn suất <1% % khi điếu trị vói REMINYL trong các dữ
liệu mù đôi, nhăn mở được trình bảy ở Bảng 2.
Pijfeminyl_ PR tômg,_CCDS 20May2011_v3 5111
Bâng 2. Phản ứng ngoại ý báo cáo ở tần suất <1% khi điểu trị với REMINYL ở các
nghiên cứu mù đôi hoặc nhãn mớ
Rối loạn chuyển hóa và dinh dưỡng
Mất nước
Rối loạn hệ thần kỉnh trung ương
Bất thường vị giảc, ngủ nhiều, dị cảm
Rối loạn ở mắt
Đốm thị giác
Rối loạn tim
Block nhĩ thất mức độ một, hồi hộp, chậm nhịp xoang, ngoại tâm thu trên thất
Rối loạn mạch
Đỏ bừng, hạ ảp
Rối loạn tiêu hỏa
Nôn khan
Rối loạn mô liên kết và cơ xương
Yếu cơ
(3 Bảng 3, các tảc dụng ngoại ý được trình bảy theo phân loại tần suất dựa trên tần suất trong các
nghiên cứu lâm sảng.
Bảng 3. Cảc tác dụng ngoại ý được xác định trong thời gian đưa(ra thị
trường và kinh nghiệm điếu trị với REMINYL theo tân suât ước
tính dựa trên các nghiên cứu iâm sảng
Rối loạn hệ miễn dịch
Không thường gặp — Quá mẫn
Rối loạn tãm thần
Thường gặp— Áo giảc
Không thường gặp— Áo thị, Áo thanh
Rối loạn tai nghe và mê(đạo
Không thường gặp — U tai
Rối loạn tim mạch ,
Thường gặp — Cao huyêt ảp
Rối loạn hệ gan - mật
Hiêm gặp — Viêm gan
Các chỉ số khác
Không thường gặp - Tăng men gan
T hông báo cho bác sĩ những tác dụng không mong muốn gặp phải khi dùng thuốc.
Quá liều
Triệu chứng
Các dấu hiệu và triệu chứng của quá liền của galantamin có thể xảy ra tương tự như sự quá liếu của
cảc thuốc kích thích cholinergic khảc. Những tác dụng nảy thường ảnh hưởng lên hệ thần kinh trung
ương, hệ phó giao cảm và đảm nối thần kinh cơ. Ngoài triệu chứng yểu cơ và nmg cơ cục bộ, một so
hay tất cả những biếu hiện của cơn cholinergic có thể khởi phát: nôn ói dữ dội, co thắt Iong tiêu hóa,
tảng tiết nước bọt, chảy nước mắt, tiêu tiện, đại tiện, toát mồ hôi, nhịp tim chậm, hạ huyết’ ap, ngã qụy
và co giật. Tăng yêu cơ cùng với tăng tiết khí quản và co thắt phế quản có thể dẫn tới nguy hiếm tính
mạng do ngạt thờ.
Có các bảo cáo sau khi đưa thuốc ra thị trường cùa Torsade de Pointes, kéo dải khoảng QT, nhịp tim
chậm, nhịp nhanh thất và mất ý thức ngắn có liên quan đến việc quá liều galantamin do vô ỷ. Trong
Pl_Reminyi_ PR 1õmg_CCDS 20May2011_v3 6111
một trường hợp đã biết được liếu, 8 viên nén hảm lượng 4 mg (tông 32 mg) đã được uỏng vảo bụng
trong một ngảy.
Hai trường hợp nữa do vô tinh uống 32 mg (buồn nôn, nôn, khô miệng; buồn nôn, nôn, đau ngực vùng
dưới xương ức) và một trường hợp uống 40 mg (nôn) dẫn đến phải nằm viện để quan sảt vê sự hồi
phục. Một bệnh nhân, người đã được kê đơn 24 mg/ngảy và có tiền sử bị ảo gìảc trên 2 năm, đã uống
nhầm 24 mg ngảy 2 lần trong 34 ngảy vả ảo giác tiến triển cần phải nhập viện. Một bệnh nhân khảc,
người đã được kê đơn 16 mg/ngảy hỗn dịch uông, đã vô tình uống 160 mg (40 mL) đả vã mồ hôi, nôn,
vả gân như ngẩt một giờ sau đó, cần phải nhập viện điếu nị. Cảo triệu chứng của bệnh nhân nảy đã
được giải quyết trong vòng 24 giờ.
Điều trị
Cảc biện pháp hỗ trợ thông thường nên được sử dụng trong mọi trường hợp quá liều. Đối vởi những
ca nặng, thuốc khảng cholinergic như atropine được sử dụng như antidote cho các thuốc kỉch thích hệ
cholinergic. Liều khởi đầu nên là 0, 5- l mg tỉêm tĩnh mạch, cảc liếu kế tiểp dựa vảo “đáp ứng lâm sảng.
Nên liên lạc với trung tâm kiếm soát độc chất để có được những thông tin mới nhất vê cảch xử trí quả
liếu bới vì những chiến lược quản lý quá liều đang phảt triển liên tục.
TÍNH CHẤT DƯỢC LÝ
Dược lực học
Nhóm được lý trị liệu: Thuốc chống sa sút trí tuệ, ATC code: N06DA04 (
Galantamin, một alkaloiđ bậc 3,1ả một thuốc ức chế cạnh tranh, chọn lọc và có thế đảo ngược đối với
acetylcholinesterase. Ngoài ra, galantamin lảm gia tăng tảc động nội tại cùa acetylcholin lên receptor
nicotin, có lẽ thông qua việc găn kết vảo một vị trí allosteric của receptor. Kết quả là có thể đạt được
một sự gia tăng hoạt tính của hệ cholinergic liên quan tới việc cải thiện chức năng nhận thức ở những
bệnh nhân sa sút trí tuệ loại Alzheimer.
Các n hiên cứu lâm săng
Cảo liêu dùng của REMINYL cho hiệu quả kiếm soát bệnh trong các thử nghiệm lâm sảng lả 16, 24
và 32 mg/ngảy. Trong cảc liếu nảy, liều 16 và 24 mg/ngây được tin rằng có tỉ sô giữa hiệu quả/nguy
cơ tốt nhất và được coi như lá cảc liều khuyến nghị sử dụng. Hỉệu quả của galantamin đă được nghiên
cứu bằng cảch sử dụng 4 cảch đảnh giá kết quả đặc trưng lâ: ADAS- C-og (Đảnh giả nhận thức dựa trên
hoạt động), CIBIC- Plus (Lượng giả toản bộ bởi cảc bác sĩ độc lập dựa trên phòng vân lâm sảng với
người bệnh và người săn sóc), đảnh giá các hoạt động cùa cuộc sông hảng ngảy và bản đảnh giá tâm
thần kinh, NPI (Thang đo lường các rôi loạn hảnh vi).
Trong cảc nghiên cứu lâm sảng, hoạt động của cảc bệnh nhân điếu trị bằng galantatnin đảnh giả bằng
ADAS— —Cog (Xem hinh) vả CIBIC-plus tôt hơn một cảch ón định và có ý nghĩa thống kê so với các
bệnh nhân dùng giả dược. Cảc bệnh nhân được điều trị trong 6 tháng bầng galantamin có điểm
ADAS- C-og cải thiện một cảch đáng kể so với điếm ban đằu của họ. So với cảc bệnh nhân không được
điếu trị, nhóm điều trị galantamin đạt được một lợi ích đáng kế và duy trì chức năng nhận thức. Điều
trị bằng galantamin cũng đã giữ được cảc hoạt động của cuộc sống hảng ngảy như ăn mặc, vệ sinh,
chuẩn bị bữa ăn. Những điếu nảy được lượng giá bằng Đánh giá Sự Bất lực trong Sa sủi trí tuệ (DAD)
vả Họp tác Nghiên cứu Bệnh Alzheimer (ADCS) Bán đánh giá ADL, lượng iả liên quan tởi người
săn sóc. Cảc liều 16 và 24 mg galantamin mỗi ngảy duy trì điếm NPI trong su t giai đoạn 11 ên cứu
trong khi điếm của bệnh nhân dùng giả dược giảm một cách rõ rệt, như là hậu quả của sự xuat hiện rối
loạn hảnh vi.
PI_Reminyl_ PR 16mg_CCDS 20May2011_v3 7111
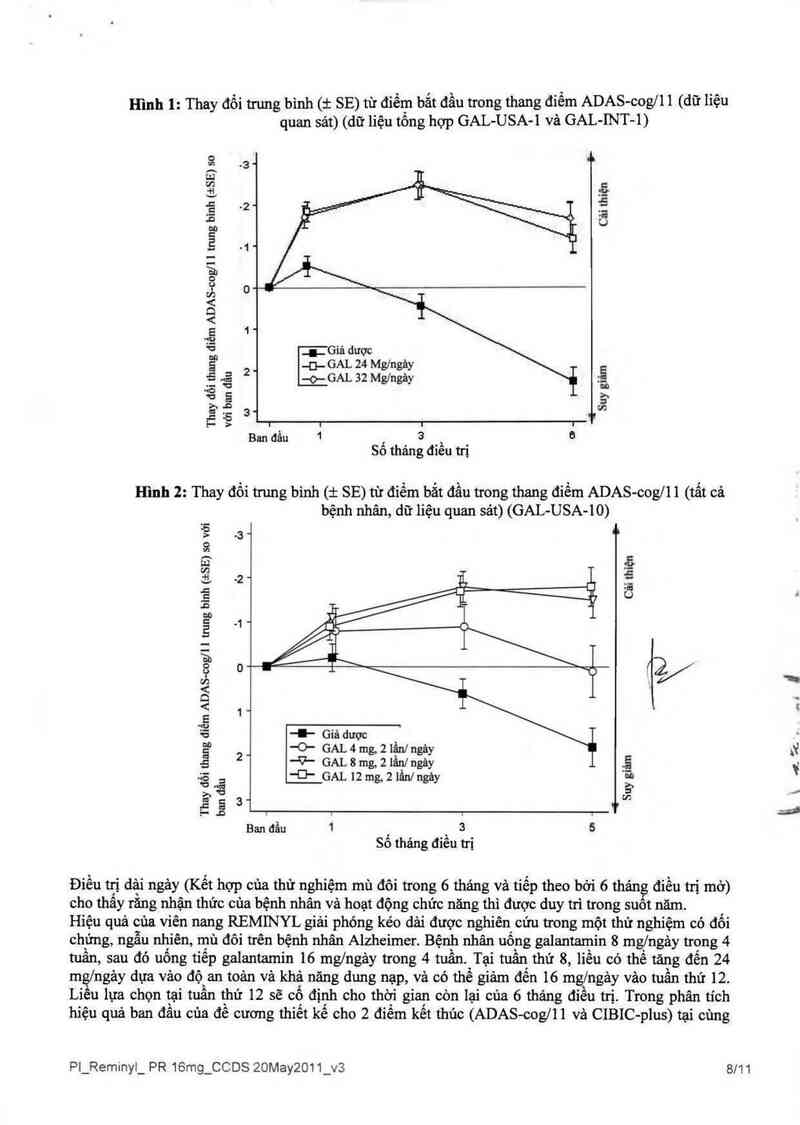
Hình 1: Thay đổi trung bình (1 SE) từ điếm bắt đầu trong thang điếm ADAS-cog/ll (dữ liệu
quan sảt) (dữ liệu tổng hợp GAL-USA-l vả GAL- INT-l)
8 .3 4 đi
[3
ẵ .~ĩ~›
Ễ ² ị
~° u
E:“
Ê —1 —
ả
3
ra 0 '
<
Q
<
E 1 1
za
g ĩGiả dược
ã 2 _ -Q-GAL 24 Mglngảy ẵ
Ế ẻ Lo-GAL 32 Mglngảy ~a
“8 g ?
>. Đ Ví
Ế zẻ 31 1 I I | "
Ban đầu 1 , 3 _ Ồ
Sô thảng điêu trị
Hình 2: Thay đổi trung binh (1 SE) từ điếm bắt đằu trong thang điếm ADAS-cog/ll (tất cả
bệnh nhân, dữ liệu quan sảt) (GAL-USA-IO)
Ễ .3- 11
8
ẩ .ẽ
03 2- Ể
Ể o
.0
DD
ễ "“
ã› i
° 0 J. 2
ả
s 1` _
e + Giádươc ẩn]
°“ _ -O- GAL4mg,ZI ngây
Ế ² —V- GAL8mg,2lầnlngảy _ẵ
Ễ…ă ~_D-_GAtizmg,ziâmngiiy ẵ
2“ 3- …
sẽ . , . , Y
Banđấu 1 3 5
số thảng điều trị
Điếu trị dâi ngảy (Kết hợp cùa thử nghiệm mù đôi trong 6 tháng và tiếp theo bỏi 6 thản điếu trị mở)
cho thấy rằng nhận thức của bệnh nhân và hoạt động chức năng thì dược duy trì trong suot năm.
Hiệu quả của viên nang REMINYL giải phóng kéo dải được nghiên cứu trong một thử nghiệm có đối
chứng, ngẫu nhiên, mù đôi trên bệnh nhân Alzheimer. Bệnh nhân nông galantamin 8 mg/ngảy trong 4
tuần, sau đó uống tiếp galantamin 16 mg/ngảy trong 4 tuần. Tại tuần thứ 8, iiều có thể tăng đến 24
mg/ngây dựa vảo độ an toản và khả năng dung nạp, và có thế giảm đến 16 mg/ngảy vảo tuần thứ 12.
Liên lựa chọn tại tuần thứ 12 sẽ cố định cho thời gian còn lại của 6 thảng điếu trị. Trong phân tích
hiệu quả ban đầu của đề cương thiết kế cho 2 điếm kết thủc (ADAS—cogl 11 vả CIBIC-plus) tại cùng
Pi_Rerninyl_ PR 16mg_CCDS 20May2011_v3 8111
thảng 6, REMINYL giải phóng kéo dải cho thấy cải thiện có ý nghĩa hơn giá dược chi trên ADAS-
cog/ 11 Thếm vảo đó, REMINYL giải phóng kéo dải cải thiện có ý nghĩa thống kế các hoạt động sống
hảng ngây (ADCS- ADL) tốt hơn giá dươc, một tiêu chuẩn quan trọng thứ 2 để đảnh giá hiệu quả. Cảo
kết quả về hiệu quả là tương tự nhau ở viên nang REMINYL giải phóng kéo dải và viên nén
REMINYL, một thuốc được coi như hoạt chẳt kiểm chứng trong nghiên cứu nây.
Đặc tính dược động học
Galantamin lả thuôo có thanh thải thấp (thanh thải huyết tương vảo khoảng 300 mL/phút) với thể tích
phân bố trung bình (V d,, trung bình 175 L). Thải cùa galantamin theo hảm số mũ bậc 2, vởi thòi gian
bán thải tận cùng `khoảng 7- 8 giờ.
Sau khi uống ] liều duy nhất 8mg galantamin, sự hấp thu xảy ra nhanh chóng với nồng độ đỉnh huyết
tương lả 43+13 ng/mL, đạt được sau 1 ,2 giờ và diện tích dưới đường cong trung bình (AUC) lả
427+102 ng. giờ/mL. Khả dụng sinh học tuyệt đối cùa galantamín đường uống lả 88, 5%. Uống
galantamin chung với thức ăn sẽ lảm giảm tốc độ hắp thu (Cmax giảm khoảng 25%), nhưng khỏng ảnh
hưởng đến mức độ nó được hấp thu (AUC).
Sau khi uống lỉều lặp lại 12 mg galantamín 2 lầnlngảy, trung bình cùa nồng độ đảy— đinh dao động
giữa 30 và 90 ng/mL Dược động học cùa galantamin thì tuyến tính trong khoảng liều từ 4- 16 mg x 2
lầnlngảy
7 ngảy sau khi uống ] liếu duy nhất 4mg 3H- -galantamin, 90 97% hoạt tính phóng xạ được tìm thẳy
trong nước tiếu và 2, 2-6, 3% trong phân. Sau khi tiêm tĩnh mạch hoặc uống, 18- 22% liếu dùng được
bâi tiết qua nước tiếu dưới dạng galantamin không đổi trong vòng 24 giờ, với thanh thải qua thận
khoảng 65 mL/phủt, tương đương với 20—25% tông lượng thanh thải huyết tương.
Cảc con đường chuyến hóa chính lả: N-oxy hóa, N-demethyl hóa, 0- demethyl hóa, glucoronid hóa và
epime hóa. O-demethyl thì quan trọng hơn nhiều ở những người chuyển hóa mạnh của CYP2D6. Mức
độ bảì tìết của tông hoạt tính phóng xạ trong nước tiểu và phân không khác biệt giữa những người
chuyến hóa mạnh và những nguời chuyển hóa kém. Các nghiến cứu in vitro đã xác định răng
cytochrome P450 2D6 vả 3A4 là những ISO enzyme cytochrome P450 chính tham gia vảo sự chuyến
hóa galantamin.
Trong huyết tương của những người chuyến hóa mạnh và kém, dạng galantamin không đối vả cảc
glucoronid của nó đại diện cho phẫn lởn hoạt tính phóng xạ cùa mẫu Trong huyết tương của nhưng
ngưởì chuyến hỏa mạnh, glucoronid cùa O- -desmethyl- galantamin thì cũng quan trọng.
Không có chẳt chuyến hóa có hoạt tính nảo của galantamin (nor galantamin, O- -dcsmethyl-galantamin
vả O— —desrnethyl-norgalantamffl) được phảt hiện dưới dạng không kết hợp trong huyết tương của
những người chuyến hóa mạnh và chuyền hóa kẻm sau 1 liễu duy nhất. Norgalantamin có thể được
phảt hiện trong huyết tương ở những bệnh nhân sau khi sử dụng nhiều lẩn, nhưng không vượt quá
10% nồng độ galantarnin
Dữ liệu từ cảc thử nghiệm lâm sảng trên bệnh nhân cho rằng nồng độ galantamin trong huyết tương ở
những bệnh nhân Alzheimer cao hơn 30-40% so với người trẻ khoẻ mạnh
Dược động học cùa galantamin ở những người suy chức năng gan nhẹ (thang điếm Child- -Pugh 5- -6)
thì tương tự như ở người khoẻ mạnh. Ở những bệnh nhân bị suy chức năng gan tnmg binh (thang
điềm Child-Pugh 7-9), diện tích dưới đường cong và thời gian bán thải cùa galantamin tăng khoảng
30% (xem Liều dùng và cách sử dụng).
Sự phân bố cùa galantamin được nghiến cứu trên những người trẻ có chức năng thận khảo nhau. Thải
trừ của galantamin giảm cùng với sự gỉảm thanh thải creatinin. Nồng độ galantamin trong huyết tương
gia tảng 38% ở những người suy chức năng thận trung bình (thanh thải creatin= 52- 104 mL/phút) vả
tảng 67% ở những người suy thận nặng (thanh thải creatinin = 9- 51 mL/phủt) so với những người
khoẻ mạnh cùng độ tuồi và cân nặng (thanh thải creatinin 2 121 mL/phút). Phân tích vả mô phỏng
dược động học trên dân số thống kê cho thấy rằng không cần díều chỉnh liếu ở những bệnh nhân
Alzhermer có suy thận miền lả thanh thải creatinin tối thiều lả 9 mL/phủt (xem Liều dùng vả cách sử
dụng) bởi vì thanh thải của galantamin thấp ở những bệnh nhân Alzheimer
2,z/
Pl_Remảnyl_ PP 1õmg_CCDS 20May2011_v3 g…
Gắn kết protein huyết tương: Gắn kết protein huyết tươn của galantamin thấp: 17, 7i0, 8%. Trong
mảu toản phẩn, galantamin chủ yếu được phân phối ở hong cẩu (52, 7%), dịch huyết tương (39%)
trong khi phần galantamin gắn kết với protein huyết tương chi có 8, 4%. Tỷ lệ về nông độ của
galantamin trong máu toản phần so vởì huyết tương lả ], 17.
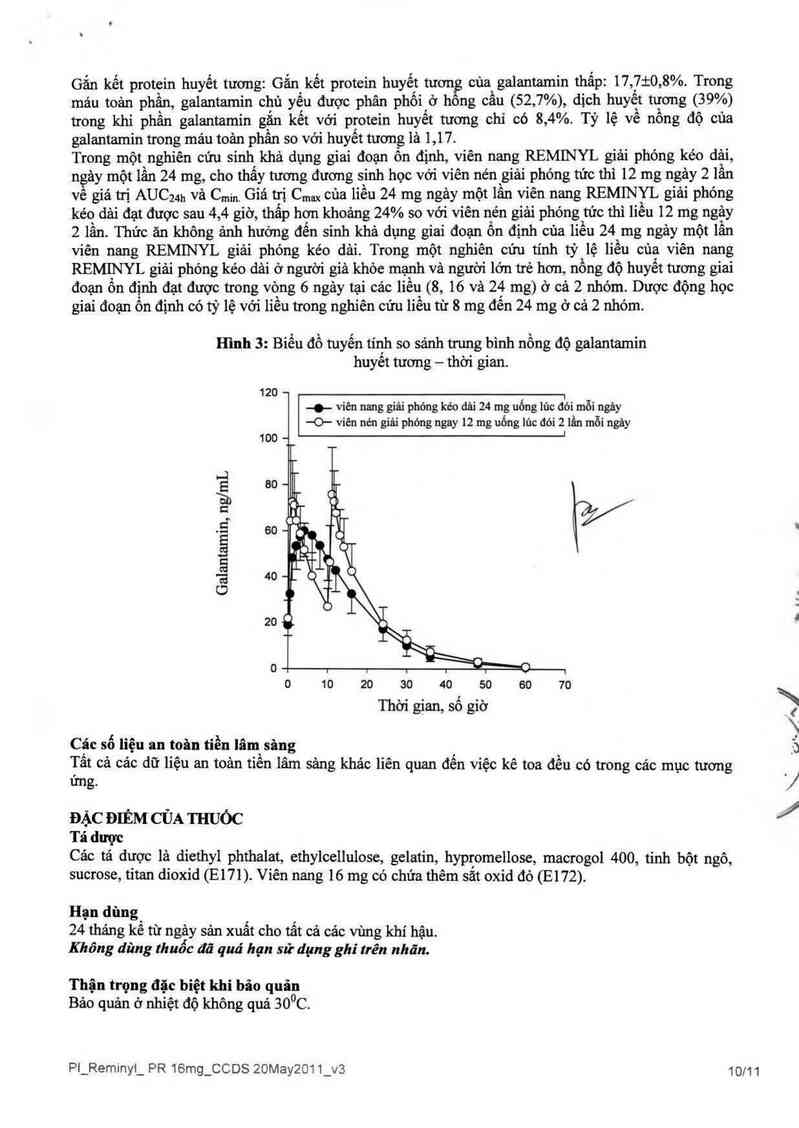
Trong một nghiến cứu sỉnh khả. dụng giai đoạn ôn định, viên nang REMINYL giải phóng kéo dải,
ngảy một lần 24 mg, cho thấy tương đương sinh học với viên nẻn giải phỏng tức thì 12 mg ngảy 2 lần
vé giá trị AUC… vả Cmm Giá trị Cmax của liều 24 mg ngảy một lần viên nang REMINYL giải phóng
kẻo dải đạt được sau 4, 4 giờ, thấp hơn khoảng 24% so với vỉên nén giải phóng tức thì liếu 12 mg ngảy
2 lần. Thức ản không ảnh hưởng đến sinh khả dụng giai đoạn on định cùa liều 24 mg ngảy một lần
viên nang REMINYL giải phóng kéo dải. Trong một nghiên cứu tính tỷ lệ liền của viên nang
REMINYL giải phóng kéo dải ở người giả khỏe mạnh và người lớn trẻ hơn, nổng độ huyết tương giai
đoạn ỏn định đạt được trong vòng 6 ngảy tại các liều (8,16 và 24 mg) ở cả 2 nhóm. Dược động học
giai đoạn ỏn định có tỷ lệ với liếu trong nghiến cứu liếu từ 8 mg đến 24 mg ở cả 2 nhóm.
Hình 3: Biến đồ tuyến tính so sánh trung bình nồng độ galantamin
huyêt tuơng — thời gian.
120
' `l
+ viến nang giải phóng kéo dâi 24 mg uỏng lúc đói mỗi ngảy
-O- viến nẻn giải phóng ngay 12 mg uống lủc đói 2 lẩn mỗi ngảy
|
Galantamin, ng/mL
oto 2030… so so vo
Thờigịan,sôgiờ
Các số liệu an toân tiền lâm sâng
Tất cả cảc dữ liệu an toản tiền lâm sảng khảo liên quan đến việc kế toa đều có trong các mục tương
ứng.
ĐẶC ĐIỂM CỦA THUỐC
Tá duợc
Các tá dược lả diethyl phthalat, ethylcellulose, gelatin, hypromellose, macrogol 400, tinh bột ngô,
sucrose, titan dioxid (E171). Viên nang 16 mg có chứa thêm sắt oxid đỏ (E172)
Hạn dùng
24 tháng kế từ ngảy sản xuất cho tất cả các vùng khí hậu.
Không dùng thuốc đã qua' hạn sử dụng ghi trên nhãn.
Thận trọng đặc biệt khi bảo quản
Bảo quản ở nhiệt độ không quá 30°C.
Pl_Reminyl_ PR 16mg_CCDS 20May2011_v3 10/11
\ \ 'uh/«Í
Bỉm chất và số lượng bao bì
Viên nang gỉải phóng kéo dải: được đóng gói~trong vi PVC—PE-PVDCInhÔm chửa 7 viến 8 mg, 16
mg. Cảc vì được đóng trong hộp giây carton. Môi hộp chứa 4 vỉ.
Đọc kỹ hướng dẫn sử dụng trước khi dùng.
Nếu cẩn thêm thông tin, xin hỏi ý kiến bảc sĩ.
Thuốc nảy chỉ dùng theo đơn của bác sỹ.
Giữ ngoảỉ tẩm tay trẻ em.
NHÀ MÁY SẢN XUẨ_T
Sán xuất bản thănh phảm các hạt thuốc giái phóng kéo dải tại:
Janssen Pharmaceutica NV, Lammerdrìes 55, Olen, B- 2250, Bi.
Kiếm nghiệm. xuất xưởng các hạt thuốc giái phóng kéo dãi tại:
Janssen Pharmaceutica NV, Turnhoutseweg 30, Beerse, B-2340, Bỉ.
Đóng nang. đóng gói sơ cấp, thứ cấp, kiếm nghiệm và xuất xưởng thảnh phấm tại:
JANSSEN CILAG S.P.A., Via C. Janssen (loc. Borgo S. Michele) - 04100 Latina, Ý
Công ty đãng kỷ: JANSSEN-CILAG Ltd., Thải Lan
Mọi câu hỏi/Báo cáo tác dụng ngoại ý/ Than phiền chẩt lượng sản phẫm xin liến uẹ:
VPĐD Janssen-Cilag Ltd., TP Hồ Chí Minh.
ĐT: +84 8 382148²8
E—mail: iacvndrugsafefflâitsjnicom
Phiên bản: CCDS 20May201 ].
PI_Reminyl†PR Iómg_CCDS 20May2011_v3
Ngăy sửa đói: 10/09/2015.
"JỊ\N`
TLỉQ. C_ỤC TR ưởxo
1"ÀRLUNG PHỒNG
", x-kaJz ›Ífllỉ/ ›Wrìng
Pl_Reminyl_ PR 16mg_CCDS 20May2011_v3 11l11
+ "Lưu ý những sản phẩm đăng trên website thuộc loại thực phẩm chức năng: những sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh"
+ Dùng thuốc theo chỉ định của Bác sĩ
+ Đọc kỹ hướng dẫn sử dụng trước khi dùng